-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Chirurgická léčba pokročilého kolorektálního karcinomu
Surgical treatment of advanced colorectal cancer
Colorectal cancer is one of the most common malignant diseases in developed countries, its incidence is increasing. In the Czech Republic is incidence very high and it is, excluding all skin cancers, on the first place in all cancers. Advanced colorectal cancer, unfortunately, affects a considerable proportion of our population. Emerging opportunities of multimodality treatment significantly improve the prognosis of these patients. The only chance for long term survival is radical surgical resection. For locally advanced tumors is multiorgan resection indicated. In the case of metastatic disease, both liver and lungs, we must always consider the possibility of resection of these metastases. In case of synchronous metastases we can performe simultaneous resection or staged resection. Liver first approach is prefered recently. In the case of metastatic peritoneal dissemination we must consider cytoreductive surgery and HIPEC, although the resectability of such involvement is low.
When deciding on multiple organ resection, pelvic exenteration, resection of liver or lung metastases, cytoreductive surgery or HIPEC we consider overall assessment findings, all available tests and overall condition of the patient in a multidisciplinary team (MDT). All patients with advanced colorectal cancer should be discussed in these teams, even though it seems to be primarily inoperable.Keywords:
advanced colorectal cancer – resection of metastases – cytoreductive surgery and HIPEC
Autoři: M. Levý; V. Visokai; L. Lipská; K. Veškrňa; J. Šimša
Působiště autorů: Přednosta: doc. MUDr. Jaromír Šimša, Ph. D. ; Chirurgická klinika 1. LF UK a Thomayerovy nemocnice Praha
Vyšlo v časopise: Prakt. Lék. 2017; 97(1): 9-16
Kategorie: Přehledy
Souhrn
Kolorektální karcinom je jedním z nejčastějších maligních onemocnění ve vyspělých státech, jeho incidence narůstá. Ze všech nádorových onemocnění zaujímá v České republice po nádorech kůže první místo. Pokročilý kolorektální karcinom bohužel postihuje značnou část naší populace. Rozvíjející se možnosti multimodální léčby významně zlepšují prognózu postižených nemocných. Vzhledem k tomu, že jedinou nadějí na dlouhodobé přežívání nemocných pokročilým kolorektálním karcinomem je radikální chirurgické odstranění nádoru, zaujímá chirurgie své neoddiskutovatelné místo v jeho léčbě. U lokálně pokročilých nádorů je z chirurgického hlediska indikována multiorgánová resekce. V případě metastatického postižení jater a plic musíme vždy zvažovat možnosti resekce, a to jak simultánně v případě synchronní metastáz, tak i ve dvou dobách, kdy stále více je primárně upřednostňována resekce jater jako první krok. V případě metastatického postižení peritonea musíme zvážit možnost peritonektomie a HIPEC, byť resekabilita takovéhoto postižení bývá nízká.
Při rozhodování o multiorgánové resekci, pánevní exenteraci, resekci jaterních či plicních metastáz, peritonektomii či HIPEC musíme vycházet z celkového posouzení nálezu, všech dostupných vyšetření a také celkového stavu pacienta v multioborovém týmu. Zde by měli být konzultováni všichni pacienti s pokročilým KRK, byť se primárně zdá být onemocnění již neovlivnitelné.Klíčová slova:
pokročilý kolorektální karcinom – resekce metastáz – peritonektomie a HIPECPOKROČILÝ KOLOREKTÁLNÍ KARCINOM
Kolorektální karcinom (KRK) je jedním z nejčastějších maligních onemocnění ve vyspělých státech jeho incidence narůstá. Ze všech nádorových onemocnění zaujímá po nádorech kůže v ČR první místo (obr. 1).
Obr. 1. Incidence nádorů v České republice (2009–2013) (zdroj NOR, ÚZIS ČR) 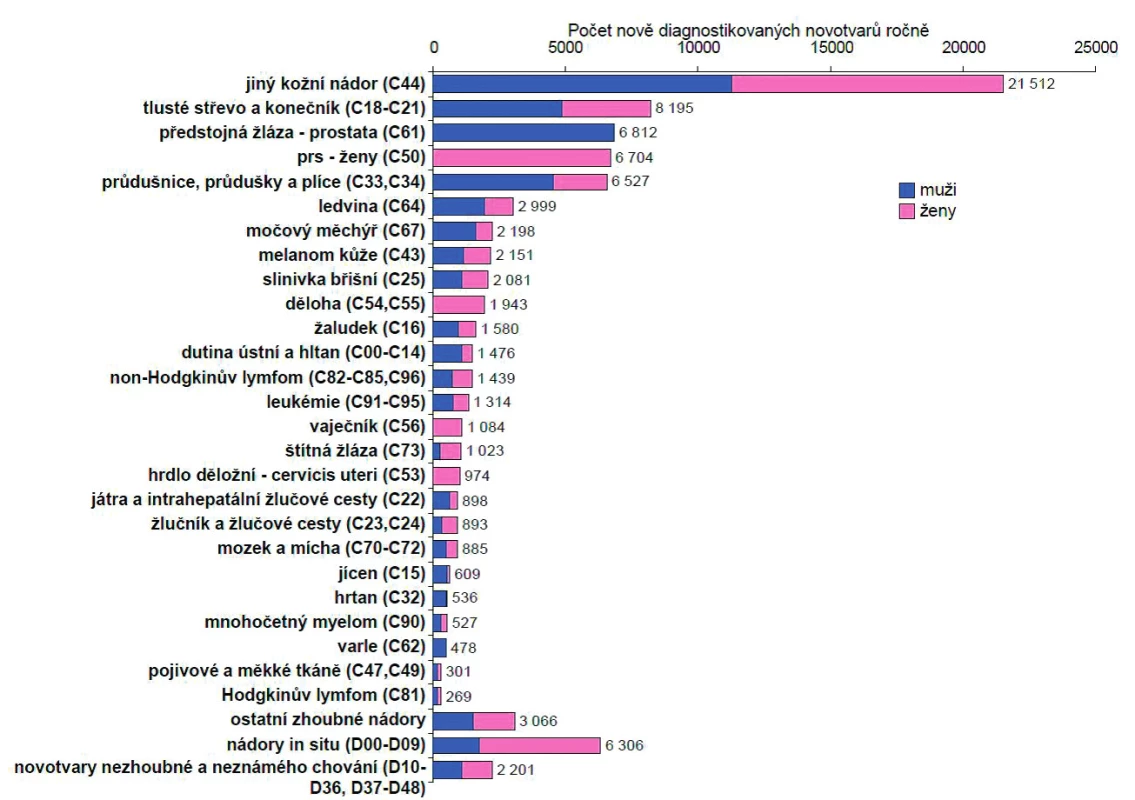
Česká republika se, pokud jde o incidenci KRK, umisťuje na předních místech na světě. Podle dat GLOBOCAN z roku 2012 se mužská část naší populace umisťuje na 4. místě na světě (3. v Evropě), u žen je incidence ve světovém srovnání na počátku druhé desítky (5) (obr. 2).
Obr. 2. Světové srovnání incidence a mortality u KRK (muži, ženy) (GLOBOCAN 2012) 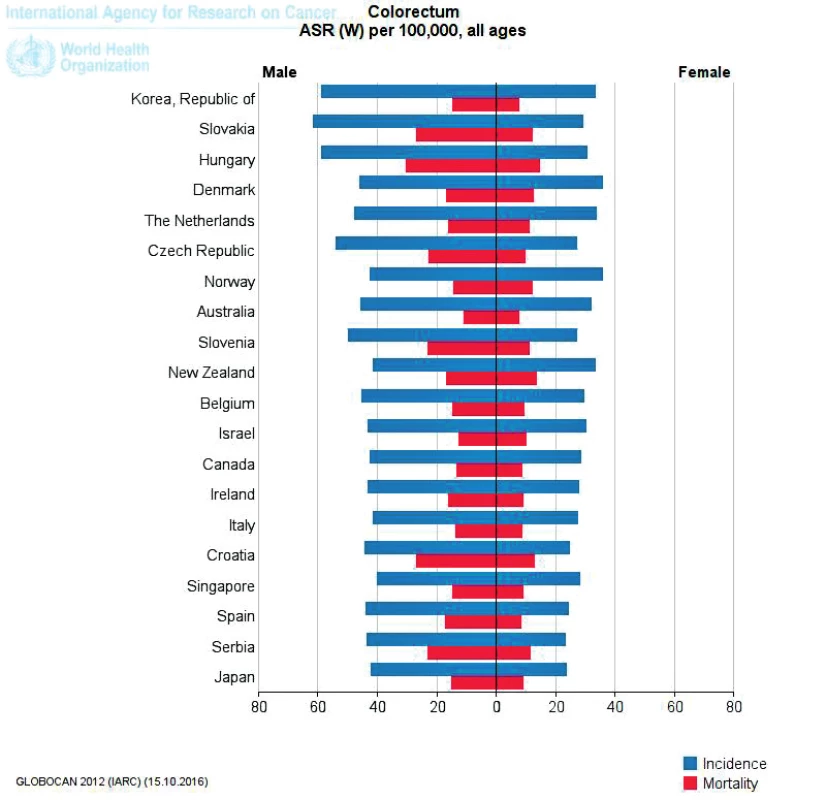
Ročně je v České republice nově diagnostikováno kolem 8000 pacientů s tímto karcinomem a téměř 4000 pacientů na něj zemře. Hrubá incidence nádorů tračníku je 45/100 000 obyvatel, mortalita 21/100 000, incidence nádorů rektosigmoidea 8/100 000, mortalita 4/100 000, u nádorů konečníku je incidence 22/100 000 a mortalita 11/100 000 obyvatel. Celkem je tedy incidence KRK 75/100 000 obyvatel a mortalita 36/100 000 obyvatel za rok (2014) (4).
Pokročilost nádorového onemocnění stanovujeme podle stagingových systémů, v našem případě prakticky vždy podle systému TNM (Union for International Cancer Control – UICC). Hodnotíme T – „velikost“ nádoru – u KRK hloubku invaze střevní stěnou, N – nádorové postižení uzlin a M – přítomnost vzdálených ložisek – metastáz. Jako pokročilý KRK lze označit nádory jednak T4 – přesahující na jiný orgán, N pozitivní a M pozitivní. Dle TNM klasifikace tedy stadia IIC a výše.
V České republice dle dat Institutu biostatistiky a analýz je zastoupení pokročilejších stadií u nádorů volného tračníku celkem 42 % (stadia III a IV), u rektosigmoideálního přechodu 43 % a u rekta 44 %. Přitom ze všech hlášených KRK není známé stadium u 9 %, kde se spíše jedná o pokročilejší stadia. Dá se říci, že pokročilý KRK postihuje cca jednu polovinu pacientů s tímto onemocněním. Prognóza je zde významně horší než u pacientů s méně pokročilým onemocněním. Nicméně za použití multimodální léčby lze dnes i pacienty ve stadiu IV vyléčit a například pětileté přežití u radikálně operovaných metastatických stadií (nejenom játra) dosahuje v specializovaných centrech až k 50 %.
POKROČILÝ KRK – POKROČILÝ NÁDOR – MULTIORGÁNOVÉ RESEKCE
Asi u 10–15 % nemocných s kolorektálním karcinomem je prorůstání nádoru do přilehlých nitrobřišních orgánů či struktur, ale bez prokazatelných vzdálených metastáz. Tato „lokálně pokročilá“ varianta kolorektálního karcinomu je charakterizována agresivním lokálním růstem a invazí či adhezí k přilehlým strukturám, ale s nízkou schopností k tvorbě vzdálených metastáz. Přes velikost nádoru, penetraci stěnou střevní i postižení sousedních orgánů lze docílit potenciálně kurabilní resekce, zejména vzhledem k překvapivě častému negativnímu nálezu v uzlinách. Histologicky jsou to nádory dobře diferencované, spíše s ohraničeným než infiltrativním růstem, převážně bez angioinvaze, bez postižení lymfatik. V případě pokročilého nádoru v malé pánvi je indikována en bloc pelvická exenterace, pětileté přežití po radikální R0 resekci dosahuje až 52 % a jsou srovnatelné s výsledky dosahovanými u pacientů, kde tumor neinvaduje okolní orgány. Pokud však není provedena en bloc resekce, ale transekce nádorem, je pětileté přežití je pouze kolem 15 %, lokální recidiva dosahuje až 100 % a další adjuvantní léčba je neúspěšná. V literatuře je udávaná morbidita v 11,5 %, mortalita 3,6 % a je srovnatelná s klasickými resekčními výkony (11).
Asi 60 % lokálně pokročilých (ale potenciálně kurabilních) karcinomů postihuje esovitou kličku a rektum, druhou nejčastější lokalizací je cékum a pravý tračník. Vnitřní rodidla tvoří asi polovinu současně odstraněných orgánů, asi ve 35 % to jsou močový měchýř, tenké střevo, stěna břišní, z dalších orgánů ledviny, ureter, slezina, žaludek, duodenum, pankreas a játra (obr. 3, 4).
Obr. 3. Nádor příčného tračníku prorůstající do bránice, žaludku, kaudy pankreatu, současně další nádor na tračníku – provedena multiorgánová resekce 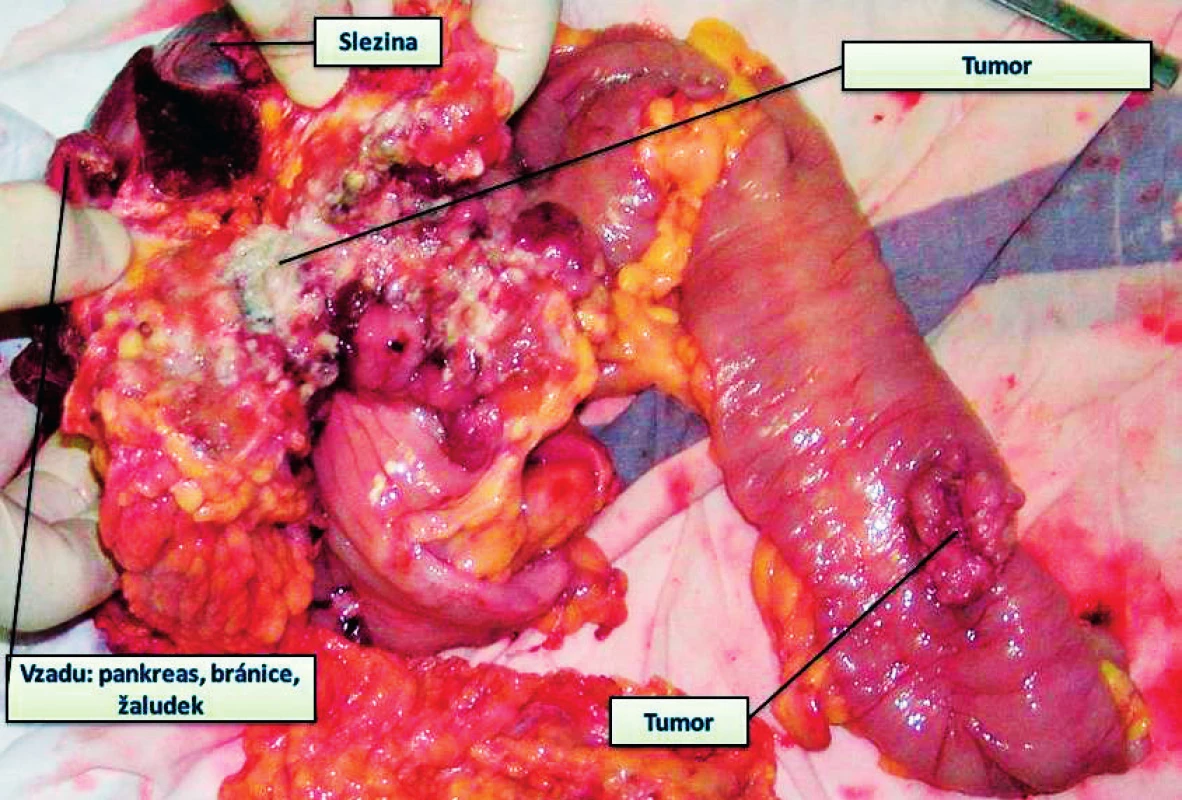
Obr. 4. Stav po resekci výše zobrazeného karcinomu – multiorgánová resekce 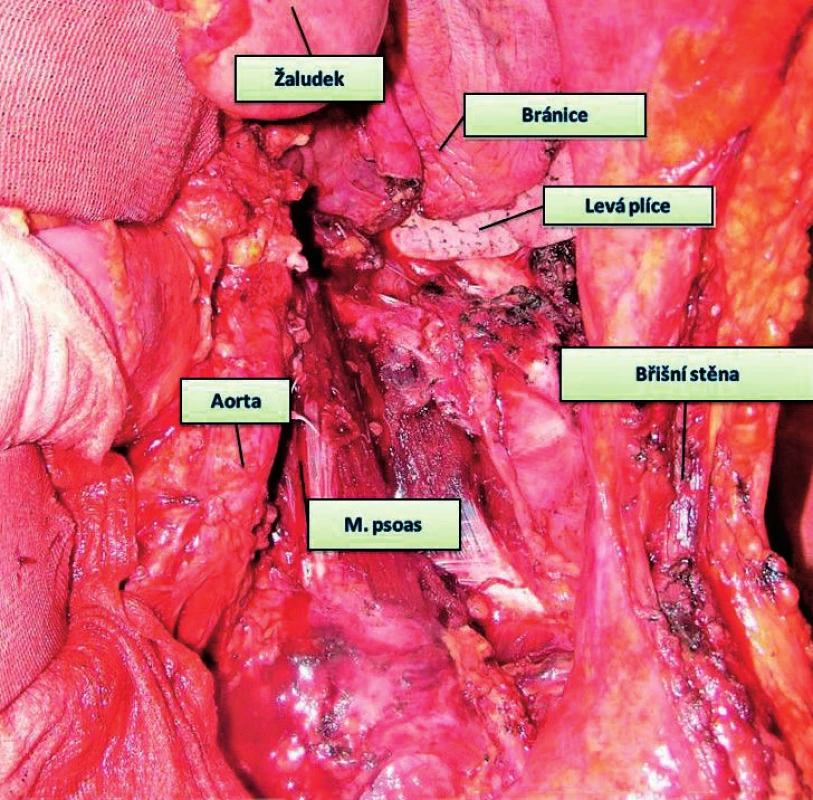
Karcinom rekta často prorůstá do pelvických orgánů, prostaty, močového měchýře, vnitřních rodidel, tenkých kliček i do jiných úseků tračníku, zejména v ileocekální oblasti. Dosažení radikality však vyžaduje extenzivní, multiorgánové a rozšířené hemikolektomie až subtotální kolektomie současně s en bloc resekcí dalších orgánů (žaludek, tenké střevo, bránice, pankreas, játra, ledviny, gynekologické orgány atd.). U nádorů rekta jsou nutné až pelvické exenterace nezřídka s resekcí skeletu pánve, nejčastěji části křížové kosti. En bloc multiviscerální resekce je ideální chirurgickou metodou k řešení těchto lokálně pokročilých, infiltrujících nebo adherujících kolorektálních tumorů. Pro řadu nemocných s rozsáhlými nádory je jedinou nadějí na dlouhodobé přežívání. Na druhou stranu se však jedná o velmi extenzivní operační výkony zatížené vysokým rizikem perioperačních krevních ztrát, vysokou pooperační morbiditou (30−45 %) i mortalitou (5−10 %). Indikace k těmto často extrémním a rizikovým operacím proto musí být velmi precizní. V dnešní době by navíc vždy měla vycházet z rozhodnutí mezioborového indikačního týmu pracoviště, které má s uvedenou problematikou zkušenosti a je schopné řešit často se vyskytující pooperační komplikace (obr. 5).
Obr. 5. Stav po pelvické exenteraci pro pokročilý nádor rekta 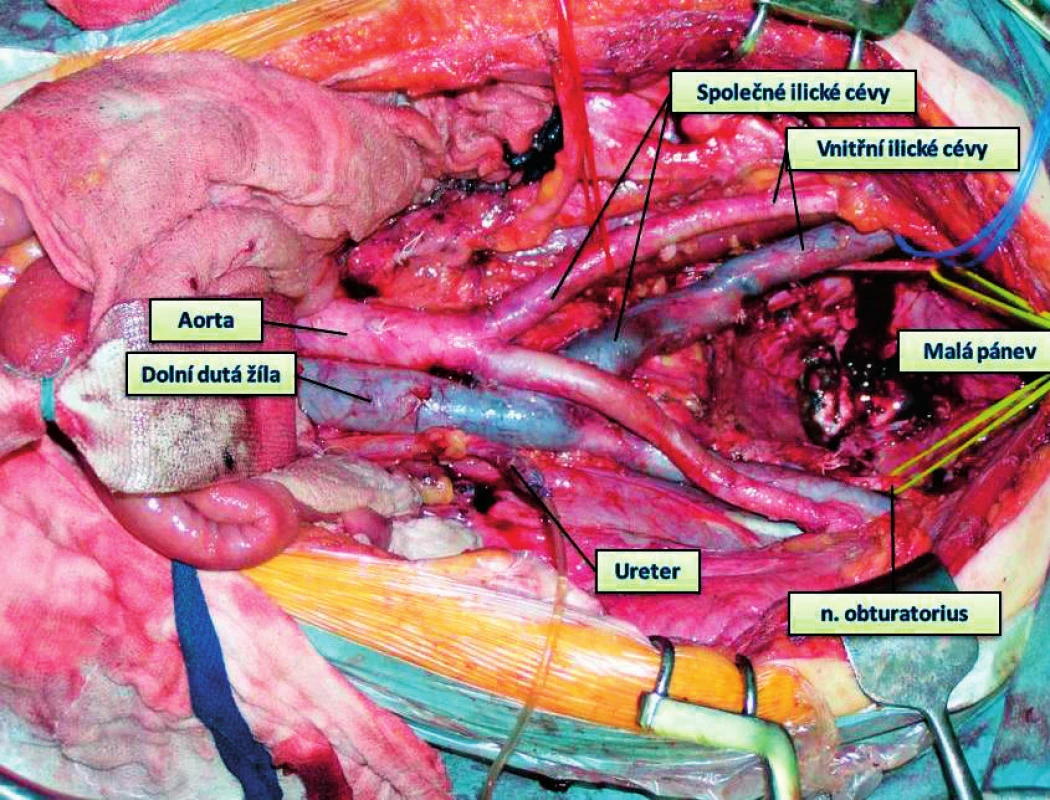
Velký důraz je kladen na preciznost předoperačního stagingu, jehož cílem je minimalizovat výskyt situace, kdy pokročilost nádoru je zřejmá až při operaci a kdy operující kolorektální chirurg není jednak připraven a také často nemá dostatečné zkušenosti k provedení multiorgánové resekce zahrnující pankreas, játra, močový trakt v požadovaném rozsahu. Taková situace by neměla být řešena tak, že se operující snaží jednotlivé orgány separovat, aby provedl operaci menšího rozsahu, tím však poruší linii tumoru a operace již není R0. Nebo prohlásí nález za inoperabilní, aniž by nemocného předal na pracoviště, které je schopné multiviscerální resekci provést. Obojí znamená pro nemocného minimální šanci na dlouhodobé přežití. Proto je nezbytné se vyhnout jakýmkoliv pokusům o oddělení adherujících okolních orgánů od primárního tumoru.
Další skupina nemocných potenciálně indikovaných k multiorgánovým resekcím jsou nemocní s lokální recidivou po operacích kolorektálního karcinomu, kdy u části nemocných lze provést radikální R0 extenzivní reoperaci.
Dosažení radikality R0 resekce je nejdůležitějším terapeutickým faktorem ovlivňujícím další přežití nemocného. Pelvická exenterace přes signifikantní morbiditu a mortalitu je často jediným řešením jak en bloc odstraněním pelvických orgánů docílit radikality operace u pokročilých, nebo recidivních karcinomů rekta. Za zásadní považujeme dodržení en bloc resekce bez pokusů o separaci orgánů od tumoru, nebo odeslání nemocného na pracoviště schopné extenzivní pelvické resekce provádět (10). Pro optimální péči o nemocné je nutná úzká spolupráce chirurgů, urologů, gynekologů, anesteziologů a onkologů. Tento „základní tým“ se však samozřejmě neobejde bez specialistů řady dalších odborností, zejména z oblasti gastroenterologie, radiologie a patologie.
Pokročilý nádor – závěr
Závěrem je nutné říci, že jedinou nadějí na dlouhodobé přežívání nemocných s místně pokročilým karcinomem rekta je radikální chirurgické odstranění nádoru. Nejčastěji jde o nádory rekta, jak primární, tak recidivující. Také pro některé další nádory malé pánve urologického a gynekologického původu, zejména pak perzistující nebo recidivující po primární radioterapii, může být pánevní exenterace kurativní léčebnou variantou. Při rozhodování o multiorgánové resekci nebo pánevní exenteraci je velmi důležitým aspektem také kvalita života nemocného. Ponechaný pokročilý nádor malé pánve, často provázený nekontrolovatelným odchodem stolice i moči, bolestmi a zápachem, je pro pacienta a jeho nejbližší okolí tristní situací s velmi nízkou kvalitou života. Pečlivé stanovení rozsahu nádoru, celkového stavu nemocného a jeho schopnosti podstoupit rozsáhlý výkon je před těmito operacemi zásadní. Zhodnocení všech výše uvedených faktorů a stanovení léčebného postupu má dnes vždy vycházet z rozhodnutí mezioborového indikačního týmu. Při hodnocení nemocného je nezbytné pečlivě zvážit všechny faktory, které mohou po operaci negativně ovlivnit život pacienta. K tomu patří i zhodnocení mentálního stavu pacienta se zaměřením na určení stupně jeho závislosti na okolí, (ne)schopnosti se o sebe postarat, nebo schopnost snášet eventuální poruchy mobility po kompozitních resekcích. Rovněž ztráta sexuálních funkcí jako důsledek operace (pelvické exenterace) musí být srozumitelně zdůrazněna a vysvětlena nemocnému i jeho partnerovi (partnerce). Všechny sociální aspekty musí být opakovaně projednány s nemocným i jeho rodinou a pečlivě vyhodnoceny při rozhodování o indikaci k multiorgánové resekci.
POKROČILÝ KRK – POZITIVNÍ UZLINY
Pokročilost onemocnění ve smyslu přítomnosti nádorových buněk v lymfatických uzlinách lze před a v době průběhu operace pouze předpokládat, potvrdí jej až histopatologické vyšetření preparátu. Případná pozitivita uzlin nemodifikuje vlastní chirurgický výkon – standardní lymfadenektomie je součástí každého radikálního chirurgického zákroku, nicméně významně ovlivňuje prognózu nemocných a ovlivňuje i adjuvantní terapii. Obecně lze říci, že pacient s pozitivním nádorovým postižením lymfatických uzlin by měl v pooperačním období dostat adjuvantní chemoterapii, pokud uzliny postiženy nejsou, záleží na rozsahu nádoru ve smyslu T a M (obr. 6, 7).
Obr. 6. Ilustrační obrázek – zvětšené lymfatické uzliny v závěsu tenkého střeva 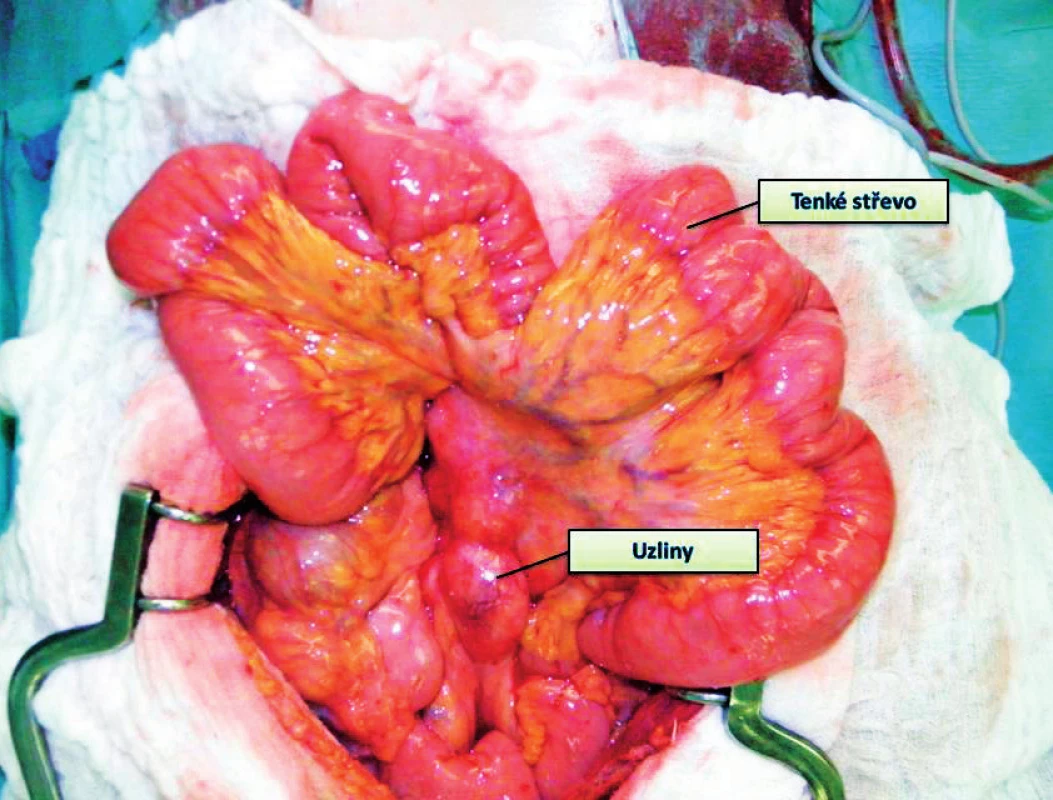
Obr. 7. Stav po lymfadenektomii kolem horní mezenterické žíly při pravostranné hemikolektomii 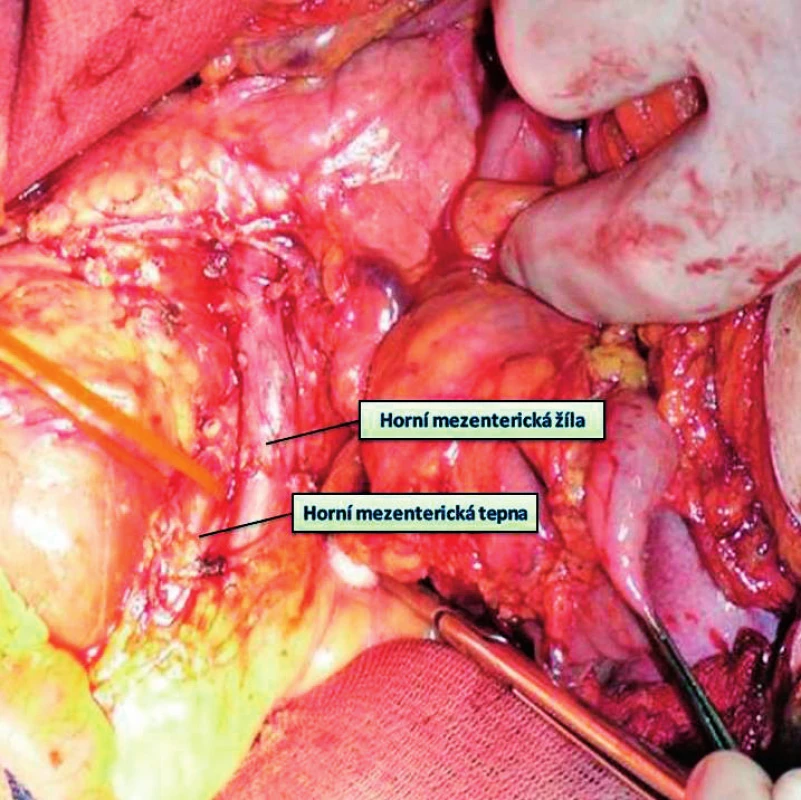
POKROČILÝ KOLOREKTÁLNÍ KARCINOM – METASTÁZY
Jaterní metastázy
V době stanovení diagnózy kolorektálního karcinomu se nachází 15–25 % pacientů již ve IV. metastatickém stadiu. Většina těchto metastáz je lokalizována v játrech, nazýváme je metastázami synchronními. Dlouhodobá prognóza těchto nemocných je dobrá pouze, jsou-li takovéto metastázy chirurgicky odstraněny. V době diagnózy je ale pouze 20 % těchto metastáz primárně operabilních. V posledních dekádách došlo díky rozvoji technických možností v kombinaci s výrazným zlepšením účinnosti chemoterapie ke zlepšení přežívání pacientů. Při multimodální léčbě je v dnešní době po resekcích jaterních metastáz dosahováno ve velkých centrech pětiletého přežití až 50 %. Léčba je komplexní, zahrnuje léčbu chirurgickou, chemoterapii a u nádorů rekta v určitých případech i radioterapii. Klíčovým faktorem je ale stále dosažení kompletní resekce jaterních metastáz (8). V posledních 20 letech dochází k posunu v případech rozsáhlejšího postižení jaterního parenchymu, a to jak z hlediska resekability, tak z hlediska bezpečnosti pro pacienta (6). Pooperační mortalita se dnes pohybuje pod 1–4 % a i u rozsáhlých jaterních resekcí nepřevyšuje počet jaterních selhání 5 %.
Česká republika patří v incidenci kolorektálního karcinomu a tím pádem i v incidenci jaterních metastáz na přední místa ve světě. Ročně se objevuje nově zhruba 7000 pacientů s diagnostikovanými jaterními metastázami. Z výsledků dotazníkových akcí provedených v roce 2000 a následně v roce 2008 plyne, že pouze zlomku těchto nemocných se v České republice dostane náležité chirurgické péče a že nepříznivý trend v poskytování léčby se v průběhu posledního desetiletí nezměnil (9).
Management synchronních jaterních metastáz
Od osmdesátých let 20. století se vedou diskuze o tom, jak načasovat resekci jater u synchronních metastáz, zda operovat současně s primárním tumorem na střevě (tzv. simultánní resekce) či odloženě. V současnosti se nově vede diskuze i o pořadí případné dvoufázové operace (7).
Primární operace střeva
Tradiční chirurgický přístup u pacientů se synchronními jaterními metastázami zahrnuje dvoufázový postup – nejprve resekce primárního tumoru, následuje chemoterapie a nakonec odloženě s odstupem 3 týdnů až 6 měsíců resekce jater. K argumentům podporujícím tento postup patří:
- možnost rozvoje náhlé příhody břišní v souvislosti s ponechaným tumorem – obstrukce, krvácení, perforace – která si vyžádá urgentní chirurgické řešení s vyšší morbiditou a mortalitou
- interval mezi primární resekcí tumoru a resekcí jater umožní detekci primárně okultních metastáz (v játrech či i jinde), což umožní buď řešení tohoto postižení během resekce jater, nebo při generalizaci onemocnění ušetří část pacientů zbytečné operace spojené s její morbiditou a mortalitou
Nevýhodou tohoto postupu je možnost progrese onemocnění před resekcí jater, nejčastěji u těch pacientů, kteří měli pooperační komplikace a vzhledem k nim neabsolvovali adjuvantní terapii dle plánu.
Simultánní resekce
Zastánci odložených výkonů argumentují zvýšeným rizikem komplikací anastomotických při splanchnické kongesci při a po resekci jater a také zvýšeným rizikem jaterního selhání při možných septických komplikacích střevního výkonu. Zastánci jednodobých výkonů argumentují výsledky studií, které neprokazují horší krátkodobé ani dlouhodobé výsledky a současně pacient podstupuje pouze jeden operační výkon. Dále odstranění všech metastatických ložisek během jednoho výkonu je prevencí progrese onemocnění, která může být podpořena pooperačním stavem imunosuprese. V neposlední řadě simultánní resekce zabraňuje možnosti progrese onemocnění při odkládání či přerušování chemoterapie mezi resekcí střeva a jaterních metastáz.
Na druhou stranu nesmíme zapomenout na ty pacienty, kteří jsou plánováni k dvoudobému výkonu a kteří tento výkon již nepodstoupí. Pak mohou být výsledky skupiny synchronních metastáz operovaných ve dvou dobách uměle lepší. Z ekonomického pohledu simultánní operace zkracují délku hospitalizace a snižují náklady na léčbu.
Liver first přístup
K historicky tradičnímu přístupu k synchronním jaterním metastázám se v posledních letech staví postup obrácený – primární resekce jater při ponechání resekce primárního tumoru do druhé doby.
K argumentům pro tento typ přístupu patří:
- rozvíjející se chemoterapie se stále vyšší účinností bránící dalšímu rozvoji onemocnění v játrech
- předoperační podávání chemoterapie na bázi oxaliplatiny a irinotekanu působí příznivě na primární tumor (udávané procento odpovědi nad 70 %)
- pooperační mortalita u pacientů po resekci primárního tumoru za přítomnosti jaterních metastáz je vyšší než u resekce tumoru bez přítomnosti metastáz
- možnost rozvoje NPB při ponechaném tumoru je udávána jen mezi 7–20 %
- narůstající možnosti řešit komplikace primárního tumoru nechirurgickými metodami (stent, endoskopie)
- možné anastomotické komplikace po resekci oddalují či ruší adjuvantní terapii
- metastázy v játrech jsou pro přežití pacienta zásadnější než primární tumor
Dosud dostupná literatura ukazuje u vybraných pacientů na dobrou proveditelnost tohoto výkonu, nízkou perioperační mortalitu a morbiditu a dobré onkologické výsledky. Pětileté přežití se u těchto pacientů pohybuje mezi 31–89 %. Celkové počty pacientů ve zmiňovaných studiích nedosahují však zatím tak vysokých počtů (celkem 121 pacientů v reprodukovatelných souborech), abychom mohli dělat zásadní závěry o přednostech či nevýhodách tohoto postupu.
Indikační rozvaha
Pro stanovení léčebné strategie jsou zásadní:
- celkový biologický stav pacienta a staging nádorového onemocnění
- funkční zdatnost jater
Pacient před operací kolorektálního karcinomu (ať už s metastázami, nebo bez nich) by měl být diskutován v multioborovém indikačním týmu. Podle symptomatologie primárního tumoru dělíme pacienty do skupin:
- symptomatický tumor
- asymptomatický tumor
Pokud jsou již před operací zjištěny metastázy v játrech, můžeme pacienty rozdělit do několika skupin dle resekability. Je nutné si ovšem uvědomit, že resekabilita metastáz je subjektivním pojmem, rozhodují zkušenosti chirurga a vybavení a možnosti pracoviště. Dále při současných multimodálních možnostech léčby i primárně neresekabilní metastázy se mohou stát metastázami resekabilními:
- resekabilní jaterní metastázy, ty je možné ještě dále dělit na primárně dobře resekabilní a primárně hraničně resekabilní
- potenciálně resekabilní metastázy
- primárně neresekabilní jaterní metastázy
Symptomatický tumor
Pokud je zvažován k indikaci pacient se symptomatickým tumorem na tračníku většinou se volí primárně operační řešení. V případě synchronních jaterních metastáz, které jsou dobře resekabilní, zvažujeme simultánní resekci. V případě primárně hraničně resekabilních metastáz je nejčastěji voleným postupem primární resekce střeva následovaná adjuvantní léčbou a případnou resekcí jater ve druhé době. Ke zvážení je i primární vyvedení derivační stomie, následně podání neoadjuvantní chemoterapie a po restagingu opět indikace k simultánní resekci. Tento postup umožňuje časnější podání chemoterapie, zvláště pokud stomii provádíme laparoskopicky.
U symptomatického tumoru rekta je situace složitější. Obvykle není doporučován simultánní velký výkon na střevě (resekce rekta) a resekce jater pro větší procento septických komplikací při resekcích rekta. Postupujeme pak obvykle tak, že se primárně konstruuje stomie, která umožní brzké zavedení chemoterapie, následuje restaging a indikace k resekci rekta. Výkon na játrech, pokud nejde o velmi lehce odstranitelné metastázy, se odkládá do druhé doby.
Při potenciálně resekabilních metastázách jater je indikována konverzní multimodální léčba zahrnující metody, jako jsou portální embolizace, radiofrekvenční ablace, transarteriální chemoembolizace v kombinaci se systémovou léčbou. U pacientů se symptomatickým tumorem musíme vyřešit překážku vyvedením stomie. Po restagingu bude indikován další postup.
Kombinace primárně neresekabilních jaterních metastáz a symptomatického tumoru vyžaduje paliativní léčbu v kombinaci buď s vyvedením stomie, zavedení stentu, nebo jednoduché resekce tračníku.
Asymptomatický tumor
Pokud se primární tumor neprojevuje, do možností léčby stále více vstupuje neoadjuvantní terapie, která může zasáhnout nejenom metastázy, ale i primární tumor. Můžeme tak uvažovat o odložení chirurgického řešení po kůře chemoterapie s následným restagingem. Odklad primárního operačního řešení má však i své nevýhody – od rizika progrese nemoci do inoperabilního stadia přes možnost poškození jaterního parenchymu chemoterapií po možnost takové odpovědi na chemoterapii, že se některé jaterní metastázy „ztratí“. Jak prokázaly některé studie, tyto „missing“ metastázy mizí však většinou jen radiologicky. Radiologicky „neviditelné“ metastázy jsou při operaci patrné v 25–45 % a u pacientů, kde došlo ke kompletní patologické odpovědi, je dlouhodobé bezpříznakové období 20–50 % toho, kterého dosahujeme u pacientů léčených resekcí + chemoterapií.
U pacientů s asymptomatickým tumorem přichází též v úvahu novější přístup k řešení synchronních jaterních metastáz, a to „liver first“ řešení. Toto řešení je obzvlášť vhodné u pacientů, u kterých je riziko progrese onemocnění v játrech v době, kdy by pacient byl v rekonvalescenci po resekci tlustého střeva.
Management metachronních jaterních metastáz
V případě metachronní jaterních metastáz (objevují se po resekci primárního nádoru) je postup jednoduší. Ke zvážení jsou dva možné přístupy, oba kombinují léčbu chirurgickou a onkologickou. Opět dělíme metastázy na:
- resekabilní jaterní metastázy, je možné ještě dále dělit na primárně dobře resekabilní a primárně hraničně resekabilní
- potenciálně resekabilní metastázy
- primárně neresekabilní jaterní metastázy
Obecně by každý pacient měl být léčen onkologicky a po dosažení resekability by měly být metastázy resekovány. Diskuze je tak v multidisciplinárních týmech vedena především u pacientů s primárně resekabilními metastázami, kdy by podání chemoterapie před resekcí nemělo vést k plné radiologické odpovědi (mizející metastázy). Proto je individuálně volen buď primárně resekční výkon, nebo tři série chemoterapie s restagingem (CT kontrolou) a resekcí časně. U potenciálně a primárně neresekabilních metastáz probíhá kůra chemoterapie s pravidelným restagingem do chvíle, kdy lze označit metastázy za resekabilní, nebo dále s paliativním záměrem (obr. 8).
Obr. 8. Stav po metastasektomii jater – 2krát neanatomická resekce 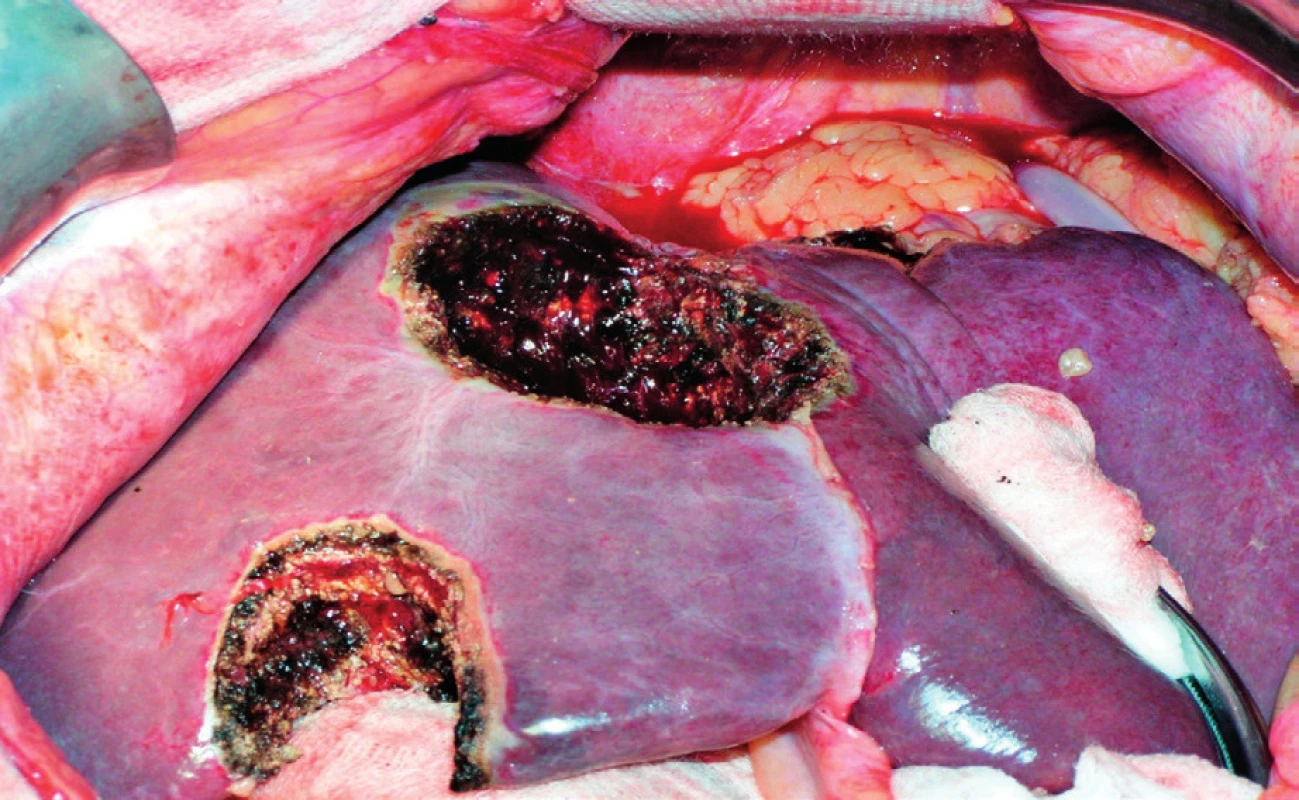
Pokročilý KRK – jaterní metastázy – závěr
Každý pacient musí být hodnocen a plánována jeho terapie individuálně. U synchronních metastáz a symptomatických tumorů zvažujeme obvykle standardní posloupnost výkonů – resekce střeva a následně jater, v případě nekomplikovaných resekcí se kloníme k simultánní resekci, jinak výkon ve dvou dobách s adjuvantní chemoterapií mezi výkony. V případě asymptomatického tumoru se stále více kloníme k primárně onkologické, medikamentózní terapii a následně pokračujeme chirurgickým výkonem. Zde opět v případě jednoduchých resekcí volíme simultánní operaci, v případě komplikovaných výkonů hodnotíme všechny faktory onemocnění a zvažujeme pořadí dvoudobých výkonů. Obecně bychom měli v první době řešit to postižení, které pacienta více ohrožuje. U metachronních jaterních metastáz volíme většinou kombinaci primárně onkologické terapie a sekundárního chirurgického zákroku. Zásadní je však pro všechny postupy úzká spolupráce chirurga, onkologa, radiologa a dalších specialistů v rámci multidisciplinárních týmů.
Management plicních metastáz
Plicní metastázy kolorektálního karcinomu jsou přítomny cca u 2 % pacientů. I zde rozvíjející se medikamentózní onkologická léčba i chirurgické techniky umožnily u k operaci indikovaných pacientů dosahovat pětiletého přežití až v 50 %. Je-li odstraněn primární kolorektální tumor, ložiska v plicích jsou resekovatelná a nejsou přítomna jiná extrahepatická ložiska nádoru, je indikována resekce plic. K významným prognostickým faktorům při resekcích plicních metastáz KRK patří synchronní nebo metachronní charakter metastáz, délka mezi operací primárního tumoru a vznikem metastáz (disease free interval – DFI), kompletnost odstranění plicních metastáz (R status), postižení hrudních mízních uzlin tumorem, hladina CEA před metastazektomií a 1 měsíc po ní, solitární versus mnohočetné plicní metastatické postižení, indukční předoperační chemoterapie, histologický typ a diferenciace tumoru, stejně jako cévní invaze v histopatologickém vyšetření. Důkladné předoperační zhodnocení pacienta zahrnuje kromě onkologického posouzení přínosu operace i respirační funkční testy. Pokud – především z interních důvodů – není pacient schopen resekčního výkonu, přistupuje v úvahu zvážení radiofrekvenční ablace. Podmínky k radiofrekvenční ablací jsou: kontrolovatelnost primárního tumoru (resekabilita + chemoterapie), limitovaný počet metastáz do 3, maximální velikost tumoru 5 cm, nemožnost radikálního chirurgického zákroku a lokalizace tumoru/ů v zevních 2/3 plíce (ne blízko k mediastinu).
Volba chirurgického přístupu, zda miniinvazivně – torakoskopicky, či klasicky z torakotomie závisí na počtu a lokalizaci ložisek. Pokud jde o typy výkonů, metodou volby jsou atypické resekce plic kombinované se systematickou lymfadenektomií mediastinálních lymfatických uzlin. Centrálně uložené nádory vyžadují lobektomii či bilobektomii. Pneumonektomie se provádí pouze ve výjimečných případech pouze, kde nejde provést výkon menší. Stejně jakou u metastáz jaterních bychom měli volit výkon maximálně zachovávající zdravý plicní parenchym tak, aby v budoucnu bylo možné provádět další případné resekce.
Stejně jako u ostatních lokalizací sekundarit KRK došlo v posledním desetiletí k posunu směrem k aktivnímu přístupu jak onkologickému, tak chirurgickému a multimodální přístup je základem úspěšné strategie i v léčbě plicních metastáz KRK (3).
Management peritoneálních metastáz
Peritoneum je po játrech druhým nejčastějším orgánem, kde se vytvářejí metastázy KRK. Zhruba 4–7 % pacientů s KRK má již v době diagnózy vlastního nádoru přítomny peritoneální metastázy. U cca 20–25 % pacientů s KRK je peritoneum jediným místem diseminakce KRK, přesto je prognóza těchto pacientů špatná s mediánem přežití 6–9 měsíců od diagnózy. Takovéto postižení je stále ještě obecně považováno za terminální stadium onemocnění, kde je chirurgická léčba zvažována pouze jako paliativní část léčby (kolostomie apod.) a pacientům je doporučována paliativní chemoterapie.
Symptomy peritoneálního rozsevu KRK nejsou specifické, zahrnují břišní dyskomfort, nevolnost, občas bolesti břicha spojené s ascitem a eventuálně střevní obstrukcí. Pokud je přítomen ascites, pak jeho punkce a cytologické vyšetření může vést ke stanovení diagnózy. Standardní zobrazovací techniky v době diagnostiky primárního nádoru (CT, MR, PET, UZ) odhalují peritoneální diseminaci cca u 40 % pacientů s těmito metastázami, u 8 % pacientů je karcinóza náhodným nálezem při operaci. V případě pochybností o přítomnosti peritoneální diseminace nádoru může být přínosná diagnostická laparoskopie. Vyšší riziko vzniku peritoneálních metastáz je u primárních mucinózních karcinomů, karcinomů T4, u pacientů s pozitivními lymfatickými uzlinami a neradikálně operovaných. Pokud jde o peritoneální relaps onemocnění po kurativní resekci je medián vzniku peritoneálních metastáz 14–16 měsíců.
Léčba peritoneálních metastáz
Historicky byla peritoneální diseminace považována za terminální stadium onemocnění a pacienti byli indikováni k paliativní chemoterapii. Klasická chemoterapie (5-fluorouracil + leukovorin) nepřinášela ve srovnání s jinými místy diseminace dobré výsledky. V dnešní době nové chemoterapeutické režimy využívající oxaliplatinu, irinotecan, bevacizumab, cetuximab nebo panitumumab zlepšují významně přežívání pacientů i s peritoneálním rozsevem KRK. Otevírá se zde tak také prostor pro multimodální léčbu těchto metastáz. Intraperitoneální podávání chemoterapie je zkoumáno cca od poloviny 20. století a na zvířecích modelech je prokázáno, že její užití po resekci primárního nádoru snižuje významně riziko následného peritoneálního rozsevu. V klinických studiích tento adjuvantní efekt intraperitoneální chemoterapie jednoznačně prokázán není. Intraperitoneální chemoterapie je užívána buď jako časná pooperační laváž dutiny břišní – EPIC (early postoperative intraperitoneal chemotherapy) – a to prostřednictvím ponechaných portů po dobu několika dní po výkonu a lze ji v průběhu několika měsíců opakovat, nebo jako kombinaci cytereduktivní chirurgie (peritonektomie) a hypertermní perioperační chemoterapie HIPEC (hyperthermic intraperitoneal chemotherapy). V tomto případě se zdá být výsledek mnohem slibnější a na velkých souborech pacientů především v USA a Německu jsou demonstrovány výsledky této léčby, které jsou srovnatelné s výsledky multimodální léčby jaterních či plicních metastáz (u KRK a peritoneální diseminací pětileté přežití kolem 40 %) (2). V minulosti byla v České republice tato metoda dostupná velmi omezeně (NNB – prof. Antoš), nicméně v posledních 2 letech dochází k jejímu rozvoji i na jiných pracovištích (Všeobecná fakultní nemocnice v Praze, Thomayerova nemocnice v Praze, Fakultní nemocnice v Olomouci) a stoupá i počet indikovaných pacientů (1). Samozřejmě, peritonektomie a HIPEC je výkonem náročným (doba operace 8–10 hodin) spojeným s významnou morbiditou a každý pacient musí být indikován na základě rozhodnutí multioborového týmu (obr. 9, 10, 11).
Obr. 9. Peritoneální metastázy KRK na levé bránici 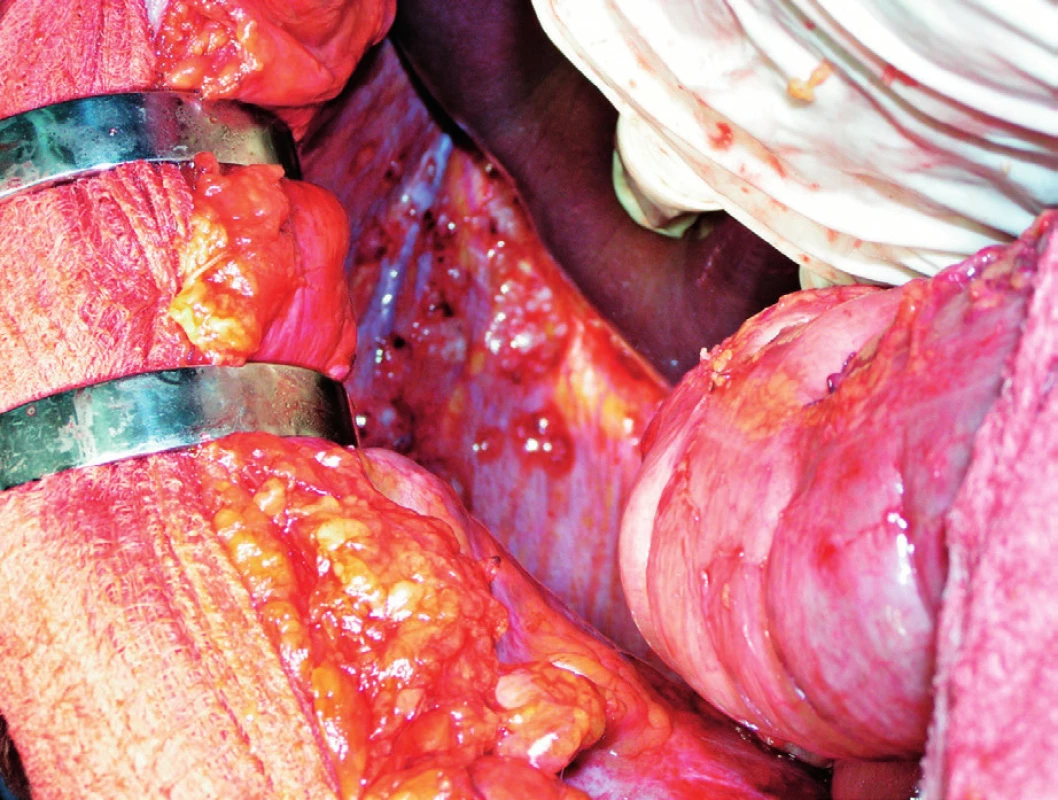
Obr. 10. Resekát parietálního peritonea – peritonektomie 
Obr. 11. Uzavřený lavážní systém HIPEC 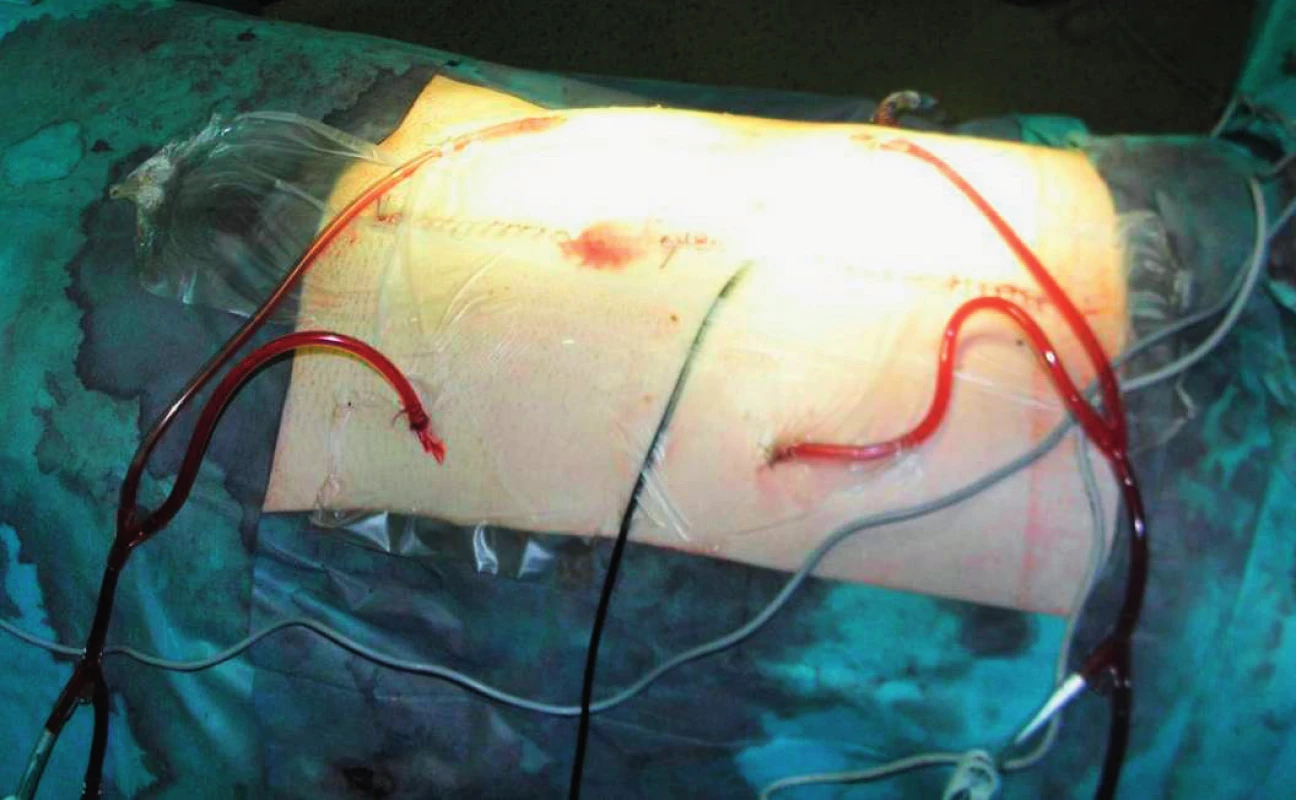
ZÁVĚR
Pokročilý kolorektální karcinom bohužel postihuje značnou část naší populace. Rozvíjející se možnosti multimodální léčby významně zlepšují prognózu takto postižených nemocných. Vzhledem k tomu, že jedinou nadějí na dlouhodobé přežívání nemocných pokročilým kolorektálním karcinomem je radikální chirurgické odstranění nádoru, zaujímá chirurgie své neoddiskutovatelné místo v jeho léčbě. Při rozhodování o multiorgánové resekci, pánevní exenteraci, resekci jaterních metastáz, plicních metastáz, peritonektomii či HIPEC musíme vycházet z celkového posouzení nálezu, všech dostupných vyšetření a také celkového stavu pacienta v multioborovém týmu. Zde by měli být konzultováni všichni pacienti s pokročilým KRK, byť se primárně zdá být onemocnění již neovlivnitelné.
Střet zájmů: žádný.
ADRESA PRO KORESPONDENCI:
MUDr. Miroslav Levý, Ph.D., MBA
Chirurgická klinika 1. LF UK a Thomayerovy nemocnice, Praha
Vídeňská 800, 140 59 Praha 4
e-mail: miroslav.levy@ftn.cz
Zdroje
1. Antoš F, Vítek P, Marx J, a kol. Cytoreduktivní chirurgie a hypertermická intraperitoneální peroperační chemoterapie (CRS + HIPEC) – patří už nyní do léčebných standardů? Klin Onkol 2016; 29(Suppl 2): 2S49.
2. Aoyagi T, Terracina KP, Raza A, et al. Current treatment options for colon cancer peritoneal carcinomatosis. World J Gastroenterol 2014; 20(35): 12493–12500.
3. Čapov I, Doležel J, Vlček P, a kol. Opakované plicní resekce v chirurgii plicních metastáz. Rozhl Chir 2013; 12 : 694–698.
4. Dušek L, Mužík J, Kubásek M, a kol. Epidemiologie zhoubných nádorů v České republice [online]. Masarykova univerzita [2005] [cit. 2016-11-04]. Dostupný z: http://www.svod.cz. Verze 7.0 [2007].
5. Ferlay J, Soerjomataram I, Ervik M, et al. GLOBOCAN 2012 v1.0, Cancer Incidence and Mortality Worldwide: IARC CancerBase No. 11 [Internet]. Lyon, France: International Agency for Research on Cancer 2013. Available from: http://globocan.iarc.fr
6. Kala Z, Kysela P. Chirurgická resekční léčba jaterních metastáz kolorektálního karcinomu. Medicína po promoci 2012; 13(5–6): 53–59.
7. Levý M, Mráček M, Jirsová A, a kol. Možnosti léčby synchronních jaterních metastáz kolorektálního karcinomu. Lékařské listy 4/2014; 15–17.
8. Mráček M, Strnad R. Chirurgická léčba jaterních metastáz kolorektálního karcinomu. Postgraduální medicína 2015; 17(2): 130–137.
9. Ryska M, Pantoflíček J, Dušek L. Léčba jaterních metastáz kolorektálního původu v České republice: současný celostátní survey. Rozhl Chir 2010; 89 : 100–108.
10. Šimša J, Visokai V, Lipská L, Levý M. Pánevní exenterace v léčbě pokročilých nádorů malé pánve. Rozhl Chir 2014; 93(1): 34–37.
11. Visokai V, Lipska L, Bergmann P, et al. Multiorgan resections for advanced colorectal cancer. Anticancer Res 2006; 26(4B): 3183–3186.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek Intoxikace paracetamolemČlánek Recenze
Článek vyšel v časopisePraktický lékař
Nejčtenější tento týden
2017 Číslo 1- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Magnosolv a jeho využití v neurologii
-
Všechny články tohoto čísla
- Motivace pacienta k léčbě a preventivním opatřením
- Povinnosti ošetřujícího lékaře při posuzování zdravotního stavu pro účely invalidity, sociálních dávek a zaměstnanosti
- Rizikové faktory pádu u hospitalizovaných pacientov
- Syndrom mnohočetné chemické přecitlivělosti
- Přístup pacientů k prevenci z pohledu všeobecných praktických lékařů
- Může být krátkodobý pobyt v hospici přínosný?
- Intoxikace paracetamolem
- Promeškaná včasná léčba Alzheimerovy nemoci u geriatrické pacientky
- Vzpomínka na endokrinologa MUDr. Pavla Langera
- Vzpomínkový večer na MUDr. Josefa Kamínka
- Recenze
- Chirurgická léčba pokročilého kolorektálního karcinomu
- Praktický lékař
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Intoxikace paracetamolem
- Rizikové faktory pádu u hospitalizovaných pacientov
- Syndrom mnohočetné chemické přecitlivělosti
- Povinnosti ošetřujícího lékaře při posuzování zdravotního stavu pro účely invalidity, sociálních dávek a zaměstnanosti
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



