-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Ambulantní flebektomie u trombofilních pacientů
Ambulatory phlebectomy in patients with a factor V Leiden mutation
The occurrence of sterile inflammation of both superficial and deep venous system and of embolism was evaluated in two groups of patients, which underwent an ambulatory phlebectomy of the saphenous complex. Histological examination was focused on the saphenous vein in thrombophilic patients.
In the first group (n=593), only half of the patients took sick leave. In this group, we observed a sterile inflammatory reaction in the inguinal area in 35 patients. These patients had no sickness leave, thus they were not able to follow an adequate treatment regimen.
In second group of patients (n=565), that all took sick leave, no complication occurred. As laboratory assessment of thrombophilia is not routinely performed and there is no difference in clinical symptoms of chronic venous insufficiency with or without thrombophilia, it is necessary to respect a two-week phase of healing accompanied with changes of blood acute protein levels. Thus, two weeks of sick leave following major saphenous complex resection is recommended. An ambulatory phlebectomy is a safe method even in thrombophilia, without risk of pulmonary embolism. There is no need of heparinization. Patients suffering from thrombophilia have more serious signs of vessel wall damage in comparison with others.Key words:
ambulatory phlebectomy, thrombophilia.
Autoři: M. A. Horáková 1; V. Křížková 2; J. Kočová 2; E. Horáková 1
Působiště autorů: Flebologická soukromá ordinace, Praha Vedoucí: Dr. med. MUDr. Magdalena Anna Horáková 1; Lékařská fakulta UK, Plzeň Ústav histologie a embryologie Vedoucí: doc. MUDr. Jitka Kočová, CSc. 2
Vyšlo v časopise: Prakt. Lék. 2009; 89(10): 545-551
Kategorie: Přehledy
Souhrn
U dvou skupin pacientů, u kterých byla provedena ambulantní flebektomie safénového komplexu, jsme hodnotili výskyt sterilní zánětlivé reakce povrchového a hlubokého žilního řečiště a výskyt embolie. Histologické vyšetření jsme zaměřili na vyšetření safén u trombofilních pacientů.
V první skupině (n=593) byla pracovní neschopnost vystavena pouze u poloviny pacientů. V této skupině jsme u 35 pacientů zaznamenali výskyt sterilní zánětlivé reakce v oblasti třísla. Jednalo se o pacienty bez pracovní neschopnosti, kteří v zaměstnání nemohli dodržovat správnou rekonvalescenci.
Ve druhé skupině pacientů (n=565), kde všem byla vystavena neschopnost, jsme neměli žádnou komplikaci. Jelikož se vyšetření trombofilního stavu rutinně nedělá a klinicky se trombofilie od obrazu chronické žilní insuficience bez trombofilie neliší, je třeba respektovat 14 dní trvající fázi hojení se změnami proteinů akutní fáze v krvi. Z toho vyplývá doporučení, aby po flebektomii kmenových safén pracovní neschopnost trvala dva týdny. Ambulantní flebektomie je u trombofilie metoda bezpečná, bez rizika embolie. Pacienty není třeba heparinizovat. Trombofilní pacienti mají ve srovnání s ostatními výraznější poškození cévní stěny.Klíčová slova:
ambulantní flebektomie, trombofilie.Úvod
Trombofilie se označuje jako hyperkoagulační stav. Lze tak obecně nazvat stav, kdy je v cévním systému – arteriálním, žilním nebo v mikrocirkulaci – zvýšena dispozice k tvorbě trombů, ke které však ještě nedošlo (1). Bobek s Čepelákem ji chápali jako „celkové onemocnění, které je zapříčiněné změněnou reaktivitou organismu s porušenými regulativními mechanismy v procesu srážení krve“(2). Tato hypotéza byla později plně potvrzena.
Deficit inhibitoru koagulace antitrombinu spojený s trombofilií byl popsán v r. 1965 a poté následoval objev i dalších přirozených inhibitorů koagulace – proteinu C (J. Stefano v r. 1976) a proteinu S (R. DiScipio v r. 1977) (1). Za příčinu rezistence vůči aktivovanému proteinu C je označena tzv. Leidenská mutace FV (R. Bertina a spol. v r. 1994) (1).
Cíl práce
V naší práci jsme se zaměřili na ambulantní flebektomii u dvou skupin pacientů a její průběh a hodnotili jsme průběh flebektomie u pacientů s trombofilií.
- Sledovali jsme výskyt sterilní zánětlivé reakce povrchového a hlubokého žilního systému a výskyt embolie.
- Histologicky jsme vyhodnotili vybraných 6 pacientů s trombofilií (3 pacienti s Leidenskou mutací, 2 pacienti s Leidenskou mutací s kombinací MTHFR mutací a jeden pacient se samotnou mutací MTHFR).
Metodika
A.
Retrospektivně byl vyhodnocen pooperační průběh pacientů po provedené ambulantní flebektomii kmenových safén. Byl proveden náhodný výběr dvou skupin pacientů:
1) První skupinu tvořili pacienti (n=593), u kterých byla provedena ambulantní flebektomie velké safény (vena saphena magna=VSM). Výkon byl prováděn u všech pacientů v místní anestézii. Byla provedena extrakce velké safény podle Dortu (3) s ligaturou v úrovni hiatus saphenus (HS). Je to místo, kde VSM přestupuje fascia muscularis a dostává se do intrafasciálního prostoru mezi fascia muscularis a superficialis. Tuto ligaturu v oblasti HS nazývá Dortu jako suprafasciální krosektomii (3). Klasická krosektomie je vždy subfasciální. (Obr. 1). Její obrovskou nevýhodou je, že provádí nikoli extrakci, ale pouze podvaz přídatných safén, které jsou nejčastějším zdrojem recidiv (Obr. 2). Krosektomie suprafasciální, kterou prezentují manželé Dortu v r. 1982 (Obr. 3) v rámci ambulantní flebektomie, zůstává trvale nad fascia muscularis, ale na rozdíl od klasické Mullerovy ambulantní flebektomie (4) přestupuje fascia superficialis.
Obr. 1. Zbylé ponechané větvení VSM a přidatných safén po klasické chirurgii 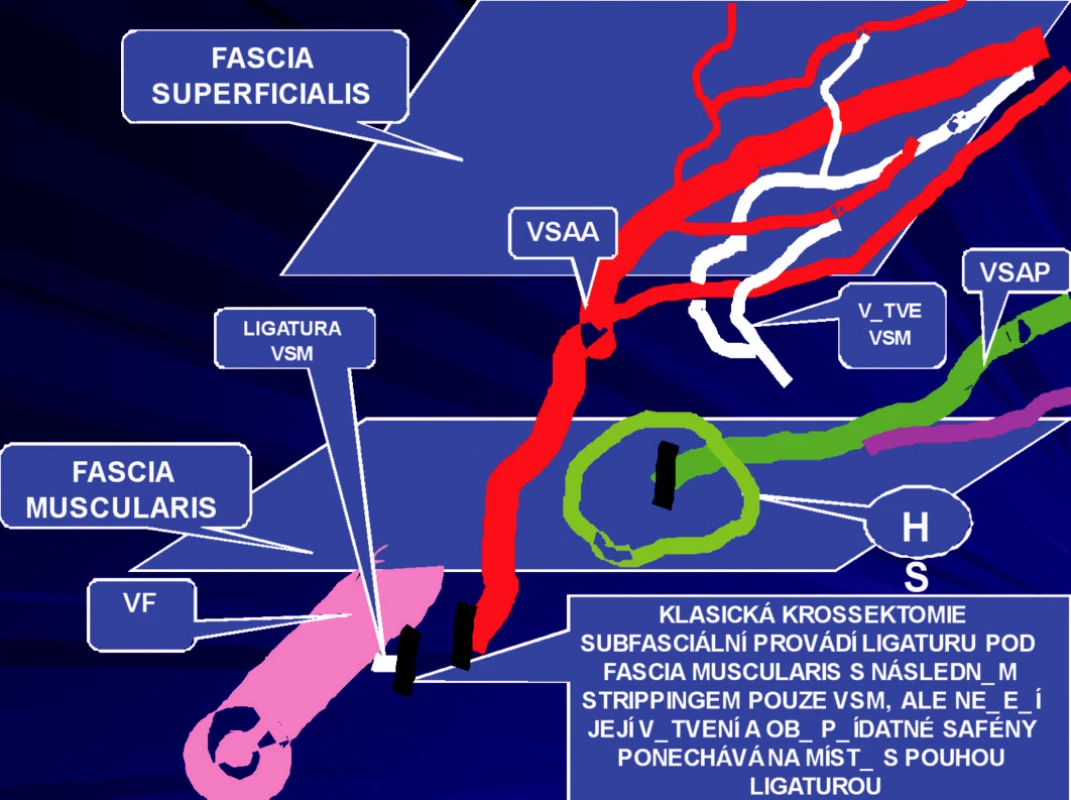
Obr. 2. Stav po klasickém strippingu po pěti letech; recidiva z ponechaných a pouze ligaturovaných přidatných safén VSAP i VSAA 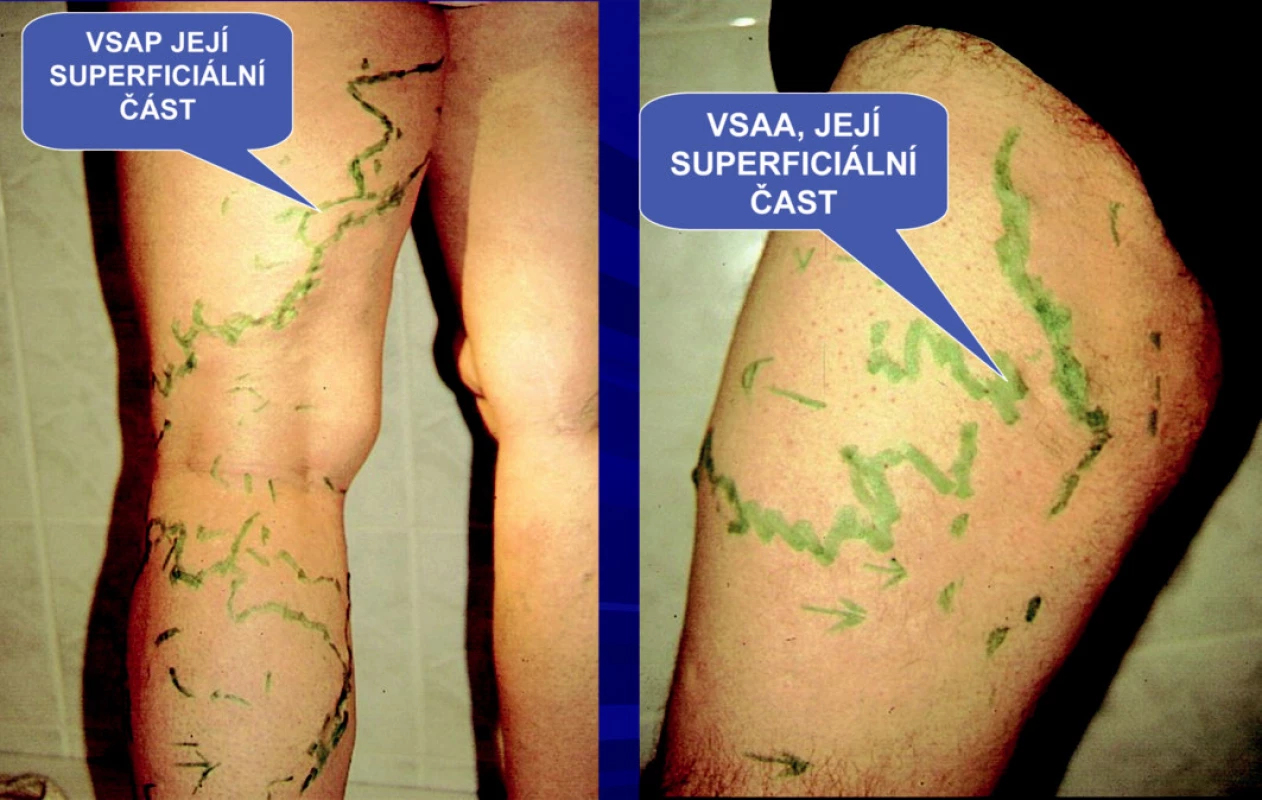
Technika Dortu se podle literatury dá použít přibližně v 37 % případů, kdy safénový komplex má klasické uspořádání (5).
Pod pojmem safénový komplex rozumíme komplex tří safén:
- VSM, tzv. velká saféna,
- vena saphena accesoria anterior (VSAA), tzv. přední přídatná saféna, a
- vena saphena accesoria posterior (VSAP), tzv. zadní přídatná saféna, z níž pak odstupuje vena Giaccomini, která tvoří spojnici mezi VSM a malou safénou.
Safénový komplex může mít klasické uspořádání, tzv. klasický safénový komplex, kdy přídatné safény odstupují od kmenové safény nad fascia muscularis. Odstupují z velké safény teprve až v oblasti HS nebo ještě distálněji (Obr. 3). Tento klasický safénový komplex se však vyskytuje u menšiny pacientů. Ve většině případů v oblasti HS odstupuje pouze jedna z přídatných safén. Z toho vyplývá, že tato technika podle Dortu má omezení v indikaci.
Obr. 3. Typ klasického uspořádání safénového komplexu, kdy VSAA i VSAP odstupují z VSM nad Fascia muscularis v oblasti HS – tvoří 37 % případů 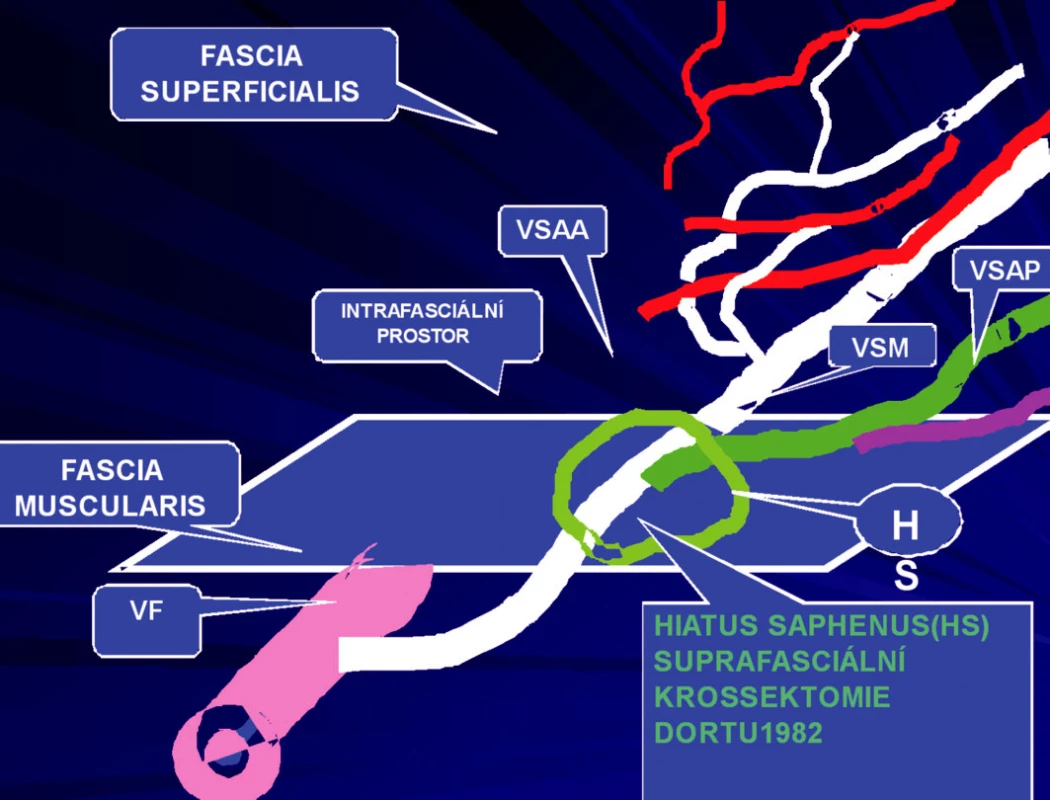
V této skupině u poloviny byla vystavena PN, u další poloviny nikoliv. Chodící režim však byl podmínkou u všech pacientů.
2) Druhou skupinu tvořili pacienti (n=565), u kterých byla provedena ambulantní flebektomie podle našeho nového postupu, který provádíme od r. 2000. Touto novou technikou můžeme odstranit obě přídatné safény VSAA i VSAP v rámci jednoho výkonu bez ohledu na jejich variabilní uspořádání. Mohli bychom ji chápat jako suprafasciální krosektomii vena saphena accesoria anterior a suprafasciální krosektomii vena saphena accesoria posterior. VSM se odstraňuje technikou podle Dortu se suprafasciální krosektomií v oblasti HS.
Naší novou technikou odstraňujeme celý safénový komplex (Obr. 4) bez omezení v indikaci.
Obr. 4. Odstranění celého safénového komplexu (Horáková); VHS odstupuje od VSM, pouze VSAP, VSAA má svůj samostatných průběh 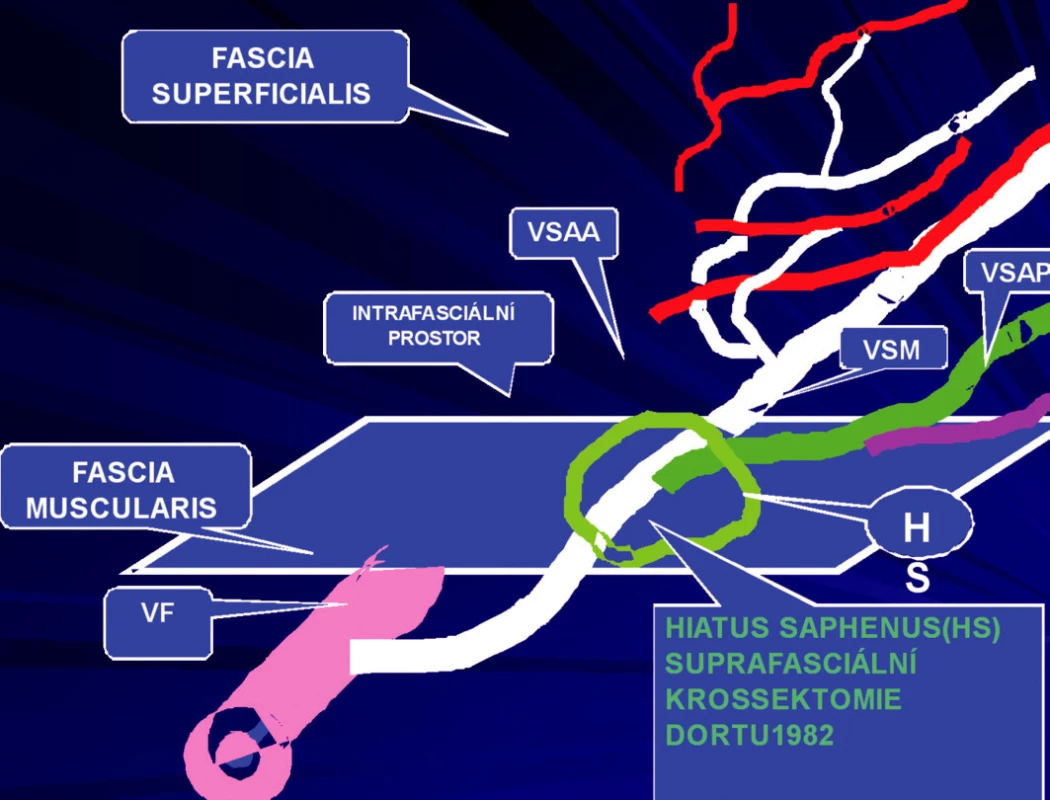
Vedle klasického safénového komplexu stojí zjednodušeně ještě další dva typy:
a) Safénový komplex typ I – kdy pod fascia muscularis z VSM odstupuje VSAA, která potom dále proráží již samostatně fascia muscularis a má svůj samostatný průběh.
Vlastní velká saféna proráží fascia muscularis v oblasti HS, kde se dostává mezi fascia muscularis a superficialis a zde z ní ve většině případů odstupuje VSAP (Obr. 5, 6). VSAA stojí samostatně a ligatura se provádí samostatně mimo HS, ale přibližně v úrovni HS (Obr. 7). U klasických chirurgických zákroků bývá nejčastějším zdrojem recidiv, jelikož má svou velikou variabilitu a ve většině případů není klinicky manifestní.
Obr. 5. Safénový komplex typ I – VSM a z nich odstupující VSAA pod fascia muscularis, VSAP odstupuje až v HS, VSAA má nad fascia muscularis samostatný průběh mimo HS 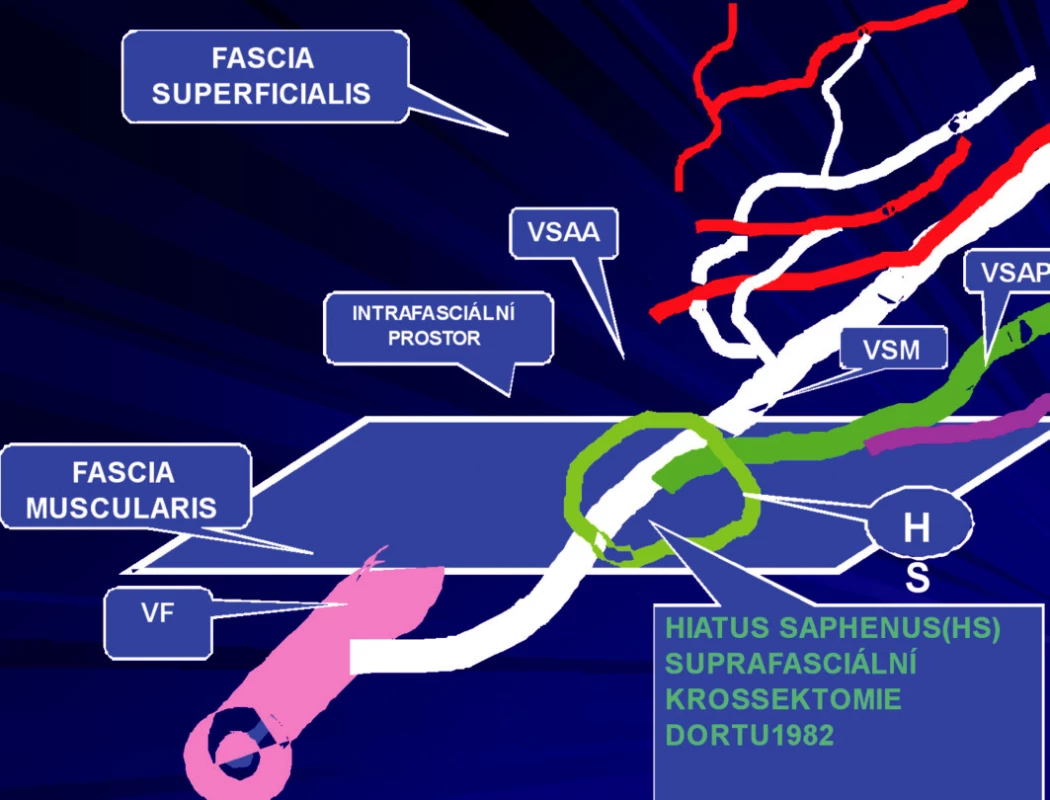
Obr. 6. Ambulantní flebektomie. Safénový komplex typ I – z VSM odstupuje v HS VSAP 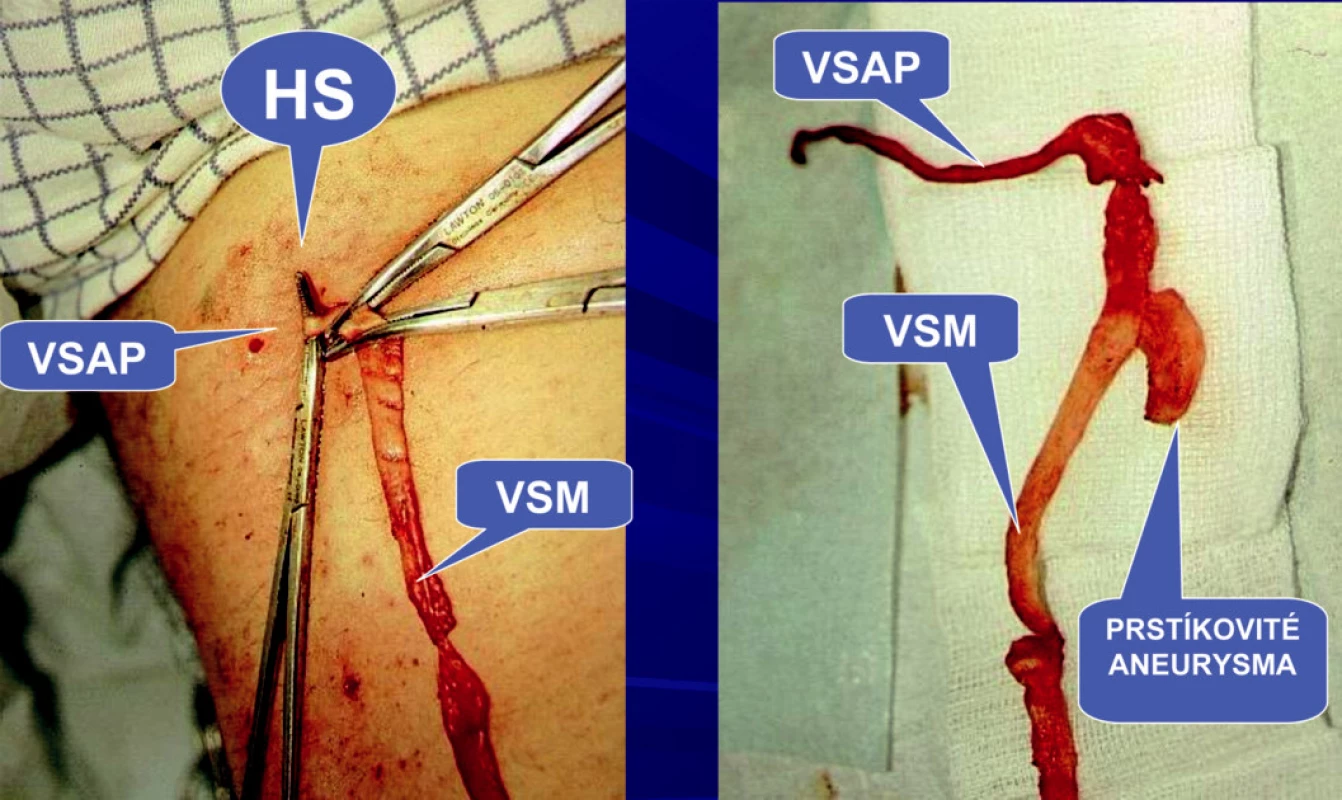
Obr. 7. Safénový komplex typ I – intrafasciální flebektomie VSAA, která je uložena mimo HS, ligatura intrafasciální části VSAA v oblasti horní třetiny stehna v úrovni HS a její intrafasciální a superficiální část po extrakci 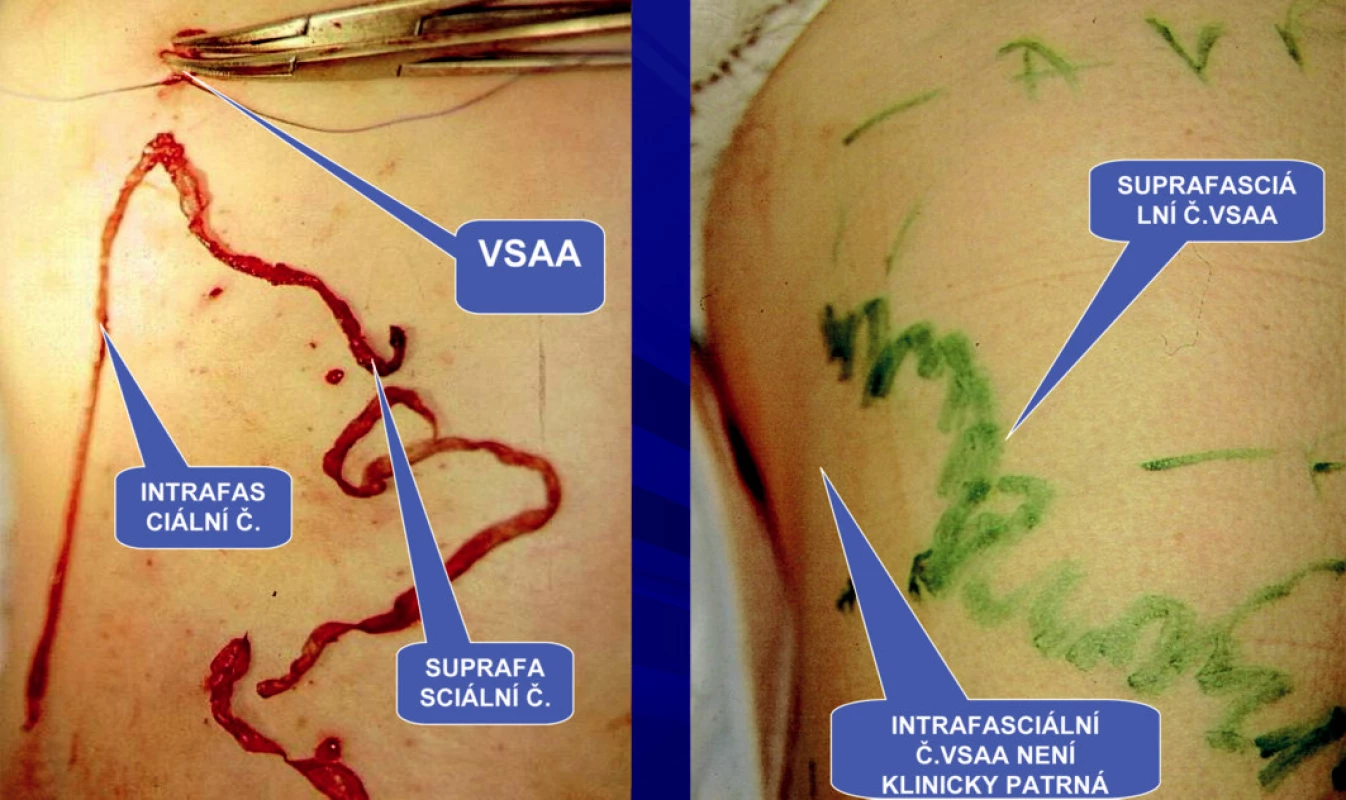
b) Safénový komplex typ II – kdy pod fascia muscularis z VSM odstupuje VSAP, která pak má dále již svůj samostatný průběh. V oblasti HS odstupuje od velké safény VSAA, nebo je její odstup z VSM ještě trochu více distálněji (Obr. 8, 9).
Obr. 8. Safénový komplex typu II – pod fascia muscularis odstupuje z VSM VSAP, nad fascia muscularis má již svůj samostatný průběh, VSAA odstupuje z VSM až nad fascia muscularis v oblasti HS 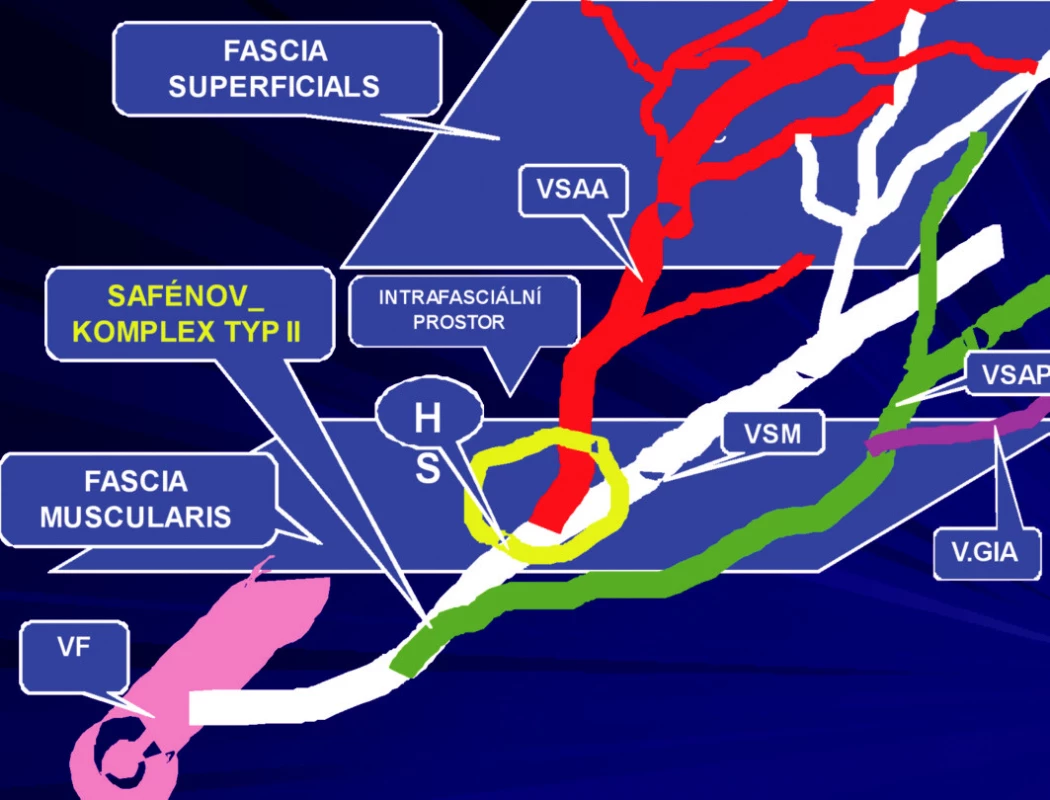
Obr. 9. Safénový komplex typ II. Intrafasciální flebektomie celého safénového komplexu – VSM a z ní odstupující VSAA v oblasti HS probíhá mimo HS, nad fascia musularis má svůj samostatný průběh 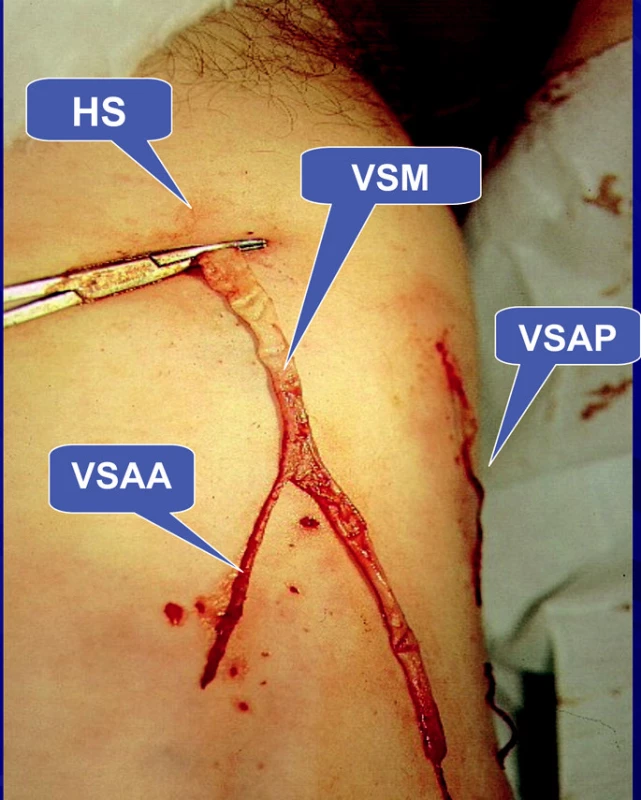
Přídatné safény ve většině případů nelze určit hmatem. Zde se uplatňuje postup, který se nám plně osvědčil. Nejprve musíme zjistit duplexním sonografem u stojícího pacienta přesnou polohu superficiálních větví těchto safén. Toto vyšetření je časově velmi náročné, jelikož superficiální větve přídatných safén se naplňují pozvolna, takže nejsou na první pohled ultrazvukem vždy patrné. Intrafasciální část přídatných safén získáme pak tahem přes superficiální větvění těchto safén. Ligaturu provádíme v úrovni HS s následnou extrakcí safén (Obr. 10). Po ligatuře dochází k atrofii zbylého úseku safén pod fascia muscularis (Obr. 11).
Obr. 10. Extrakce celého safémového komplexu VSAA probíhá mimo HS. Z VSM odstupuje v HS pouze VSAP. Klinicky manifestní suprafasciální část přidatných safén VSAA a VSAP u téhož pacienta. Vlastní VSM nemá na stehně klinickou manifastaci, její průběh je intrafasciální. 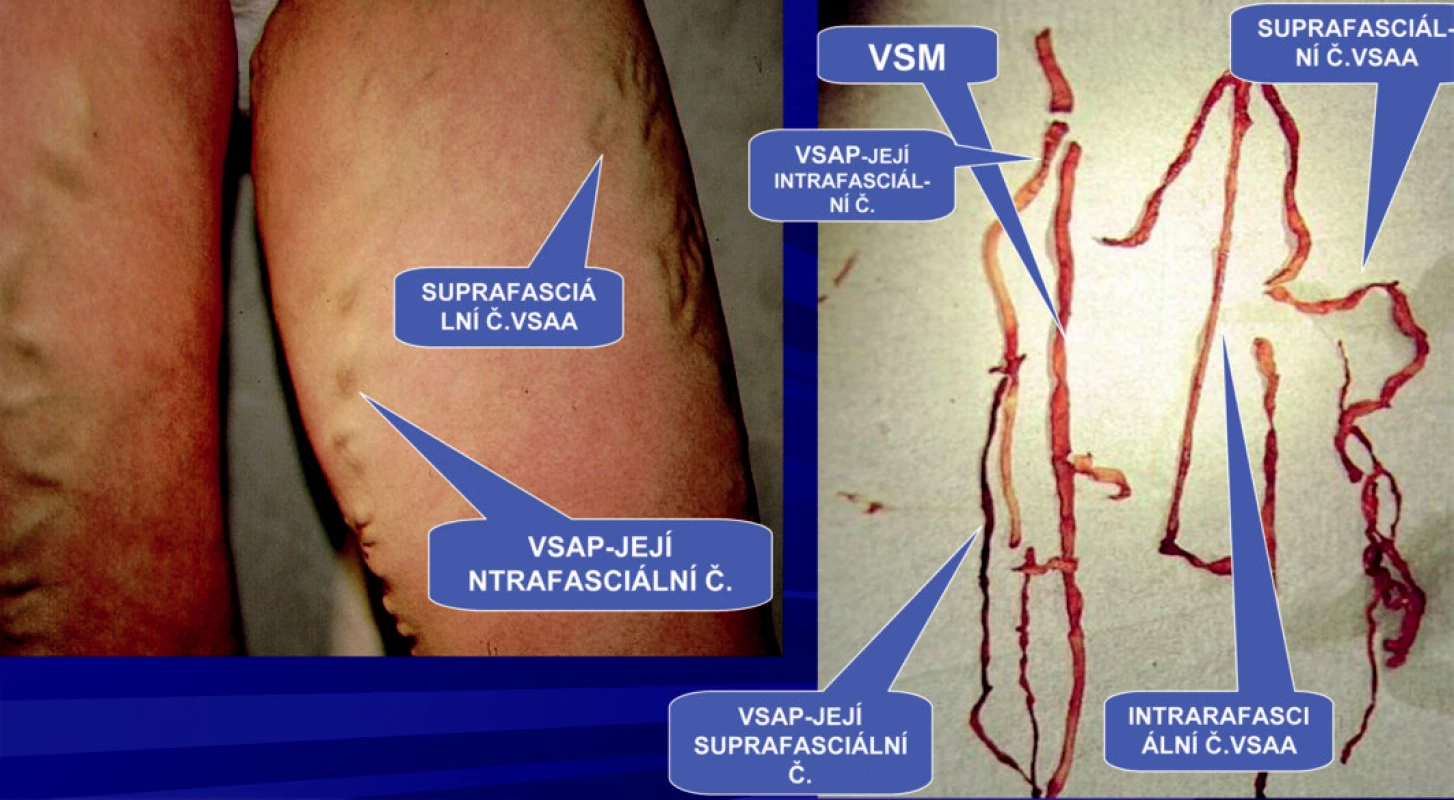
Obr. 11. Stav před a po AF na LK. Safénový komplex typ I – na sonografu pod fascia muscularis odstupuje z VSM VSAA, která je dominantní a může být lehce zaměněna se samotným kmenem, který je menší. Na stehně nejsou intrafsciální úseky safén klinicky manifestní. Po provedené AF dojde k atrofii sunfasciálních úseků safén. 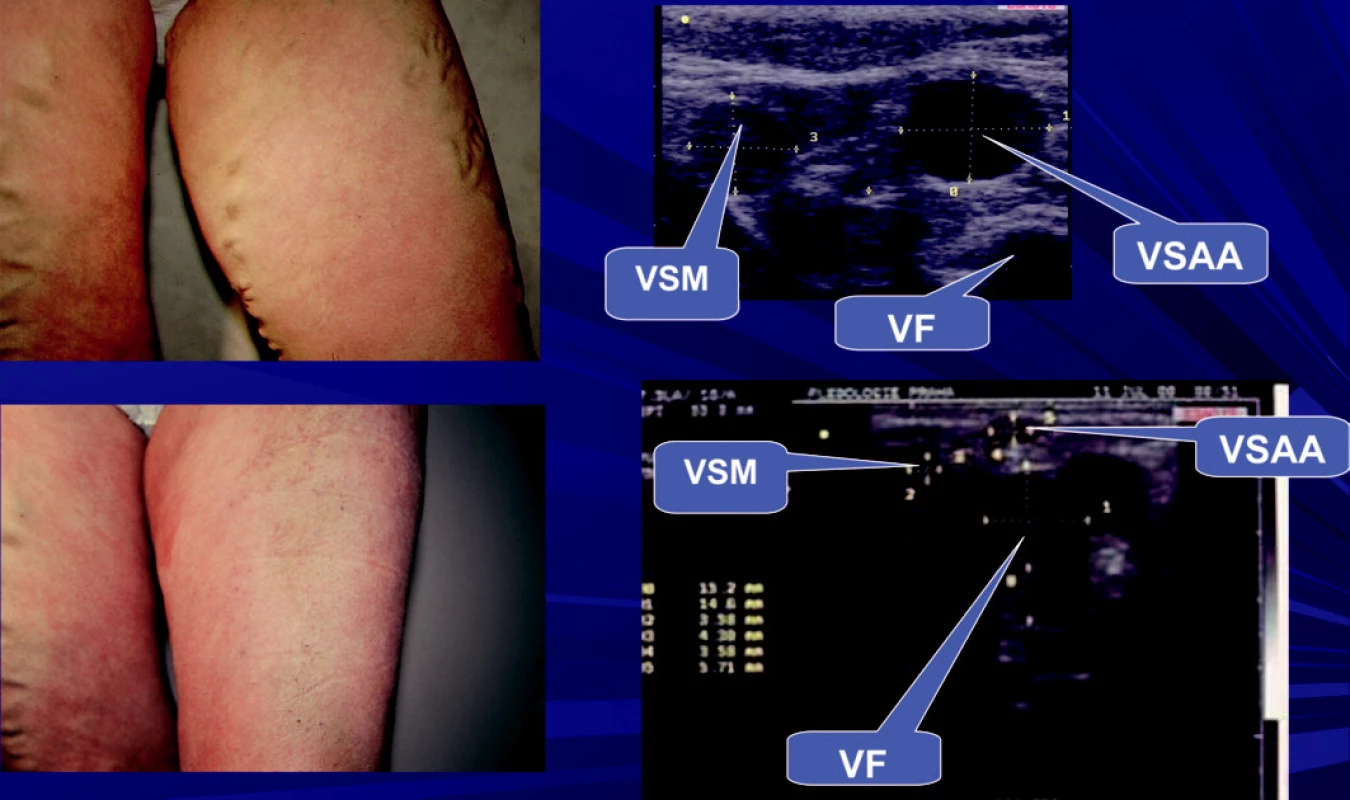
Pracovní neschopnost byla v této skupině vystavena u všech pacientů.
B.
K histologickému vyšetření jsme užívali příčných řezů (orientovaných kolmo na průběh žíly). Pro orientační hodnocení jsme užívali klasické barvení typu hematoxylin-eosin (HE), ale více se nám osvědčilo barvení modifikovaným trichromem (M-TRI) dle Kočové, zejména s ohledem na kvantifikaci jednotlivých komponent žilní stěny (11).
Při něm odlišíme
- kolagen – zbarvený zeleně,
- buňky hladké svaloviny a erytrocyty – barví se červeně,
- jádra buněk a elastická vlákna – jsou zbarvena černě (Obr. 12).
Obr. 12. VSM M-TRI dle Kočové, zvětšení 40 x 10, s fragmentací elastických vláken a degenerativními (metabolickými) typy buněk hladké svaloviny. 
Výsledky
Dvě sledované skupiny pacientů se odlišovaly ve výskytu sterilní zánětlivé reakce se zarudnutím pokožky v oblasti hiatus saphenus po ligatuře VSM. Komplikace typu hluboké trombózy a plicní embolizace se nevyskytly ani u jednoho pacienta v obou sledovaných skupinách.
V první skupině (n=593) jsme pozorovali u 35 pacientů (6 %) atypickou reakci po provedeném výkonu. U všech nemocných šlo o výraznou sterilní zánětlivou reakci v místě ligatury insuficientní velké safény v oblasti hiatus saphenus. Zánět byl provázen zarudnutím pokožky v oblasti hiatus saphenus a v oblasti třísla. Duplexní monografie prokázala nestlačitelnost zbylého úseku velké safény až po terminální chlopeň, která již byla volně stlačitelná.
V této skupině bylo možno pouze u dvou pacientek provést dodatečně vyšetření Leidenské mutace. U jedné z nich šlo o zcela náhodný nález. Druhou pacientku jsme ještě před plánovaným výkonem poslali na vyšetření trombofilního stavu, jelikož výkon v r. 1996 byl sám velmi náročný pro velkou fragilitu varixů, a pacientka měla velmi bouřlivou reakci se zarudnutím a velkou bolestivostí v oblasti hiatus saphenus. Vyšetření potvrdilo Leidenskou mutaci v kombinaci s mutací MTHFR.
Když jsme vyhodnocovali těchto 35 pacientů zpětně, šlo ve 33 případech o pacienty, kteří odmítli pracovní neschopnost a šli následný den do práce.
Druhou skupinu pacientů tvořil soubor získaný náhodným výběrem pacientů (n=565), u nichž šlo o zákroky rozsahem větší a náročnější ve srovnání s první skupinou. Všichni pacienti měli pracovní neschopnost nebo dovolenou po dobu dvou týdnů. V této skupině se nevyskytla ani jedna ze tří komplikací.
U poloviny operovaných se objevila bolestivost v místě ligatury velké safény, ale zarudnutí a zánět okolní tkáně zde nebyly pozorovány ani u jednoho pacienta, ve srovnání s první skupinou.
V této skupině mělo 10 pacientů již potvrzenou trombofilii (z toho šlo ve 4 případech o Leidenskou mutaci, ve 4 případech o kombinaci mutace MTHFR a Leidenské mutace a ve 2 případech o čistou MTHFR mutaci). V této skupině jsme pouze u 3 pacientů s Leidenskou mutací zaznamenali opakované povrchní flebitidy v anamnéze, současně byla prokázána i mutace MTHFR, u dalších dvou pacientek se v anamnéze vyskytly opakované potraty. U dalších 5 pacientů byla přítomná trombofilie zcela inaparentní. Pouze u dvou pacientů byla provedena heparinizace nízkomolekulárním heparinem (Fraxiparine inj. s.c.).
Histologický nález
U trombofilních osob jsme pozorovali změny od endotelu intimy až po vasa vasorum adventitie. Endotelové buňky byly různé velikosti, od plochých po kubické až nízce cylindrické, některé silně vakualizované až s tzv. balónovitým vyklenutím buněčné membrány do lumina s nasedáním adhezivních molekul a krevních elementů, připomínající dysplastické změny endotelu v tepnách u aterosklerózy. Pod endotelem je výrazné zmnožení hladkých svalových buněk, které jsou nápadně světlé, tj. s degenerací myofibril (Obr. 12).
Tyto změny hladkých svalových buněk pozorujeme i v tunica media a v tunica adventitia, pokud tam jsou longitudinální svalové svazky. Dokonce i ve vasa vasorum adventicie vidíme v arteriolách místy degenerované světlé formy leomyocytů (Obr. 13). Dále byl nápadný zmnožený počet vasa vasorum a buněčných infiltrátů (Obr. 14). Je to typický nález svědčící pro zánětlivé a reparativní procesy.
Obr. 13. Tunica adventitia, M-TRI dle Kočové, zvětšení 40 x 10, s fragmentací elastických vláken a degenerovanými (metabolickými) typy buněk hladké svaloviny, které jsou obsaženy přímo ve stěně viditelné vasa vasorum. 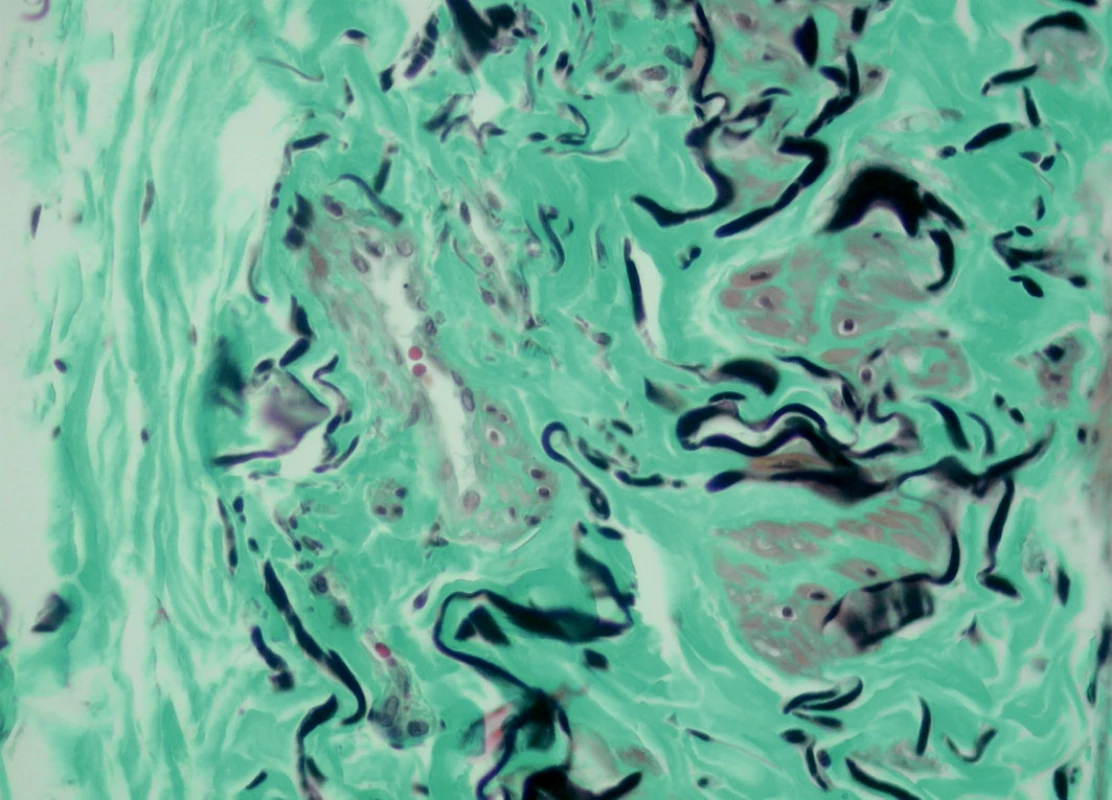
Obr. 14. M-TRI dle Kočové, zvětšení 20 x 10. Tunicaintima a přechod tunica media s dilatovanými erytrocyty vyplněnými a početnými vasa vasorum v okolí s buněčnými infiltráty a s fragmentovanými elestickými vlákny. 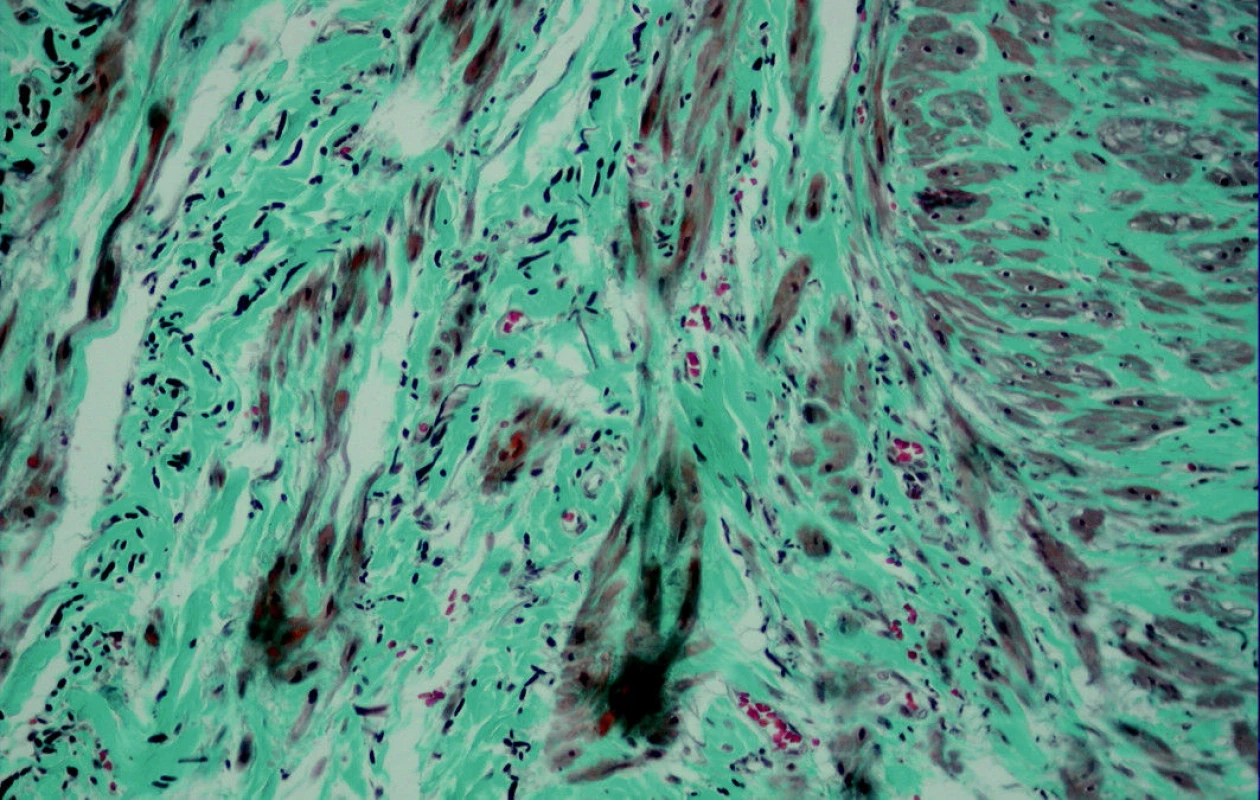
Lze tedy shrnout, že histologicky jsou změny ve stěně u osob s trombofilií podobné, ale výrazněji vyjádřeny než u varixů osob bez trombofilie.
Diskuse
V etiopatogenezi trombofilie zaujímá vedle hereditárních vlivů důležité postavení zánět, a to nejen jako její příčina, ale i následek. To, že trombotizace je provázena zánětlivou reakcí, bylo známo již antickým lékařům. John Hunter (1728–1793) označuje trombus tvořený v zanícených cévách jako inflammatory crust. Virchow (1821–1902) potvrzuje vztah zánětu k žilní a arteriální trombóze (1).
V klinické praxi se však s hyperkoagulací, která je vyvolána zvýšenou produkcí koagulačních faktorů a inhibitorů fibrinolýzy, setkáváme nejčastěji při zánětlivé reakci. Zánětlivá reakce, která vede k trombotizaci, může být infekčního nebo neinfekčního původu.
Infekční zánětlivá reakce, kterou vyvolají viry nebo bakterie, je fylogeneticky velmi starým obranným mechanismem imunitního systému, který má po vytvoření fibrinového valu okolo ložiska lokalizovat infekci a zabránit její diseminaci.
K neinfekční zánětlivé reakci, tzv. sterilní zánětlivé reakci, dochází po traumatu nebo operačních zákrocích. Je potřebná k zahájení následného reparativního procesu – hojení rány (1).
Poranění živé tkáně vyvolávají v lidském organismu adaptační odezvu, nazývanou také reakcí akutní fáze, která směřuje k minimalizaci škod jimi vyvolaných a k hojení rány.
Zvýšení hladiny proteinů akutní fáze, jejichž koncentrace v séru narůstá, patří:
- C-reaktivní protein,
- sérový anuloid A a P složka sérového amyloidu,
- dále pak proteiny komplementového systému,
- koagulační proteiny FVII, FVIII, fibrinogenu a inhibitoru fibrinolýzy PAI1,
- a další.
Jejich zvyšování hladiny probíhá obecně až do 10. či 12. dne po operačních zákrocích, a tím se zvyšuje sklon k trombogenezi (1). Tato skutečnost je opomíjena a je nutno na ni pamatovat u všech operačních zákroků.
Výskyt trombofilií v populaci se obecně odhaduje na 30 % (6), z toho postižení FV-Leiden mutace se pohybuje podle literatury od 5–15 % (1, 7, 8, 9). Někteří autoři poukazují i na velké regionální rozdíly (7, 8). Výskyt FV-Leidenské mutace stoupá u pacientů postižených trombózou, kde je již výskyt mutace u 20–40 % postižených (10). Přesné procentuální zastoupení Leidenské mutace u pacientů s klinicky manifestními varixy nemáme, jelikož se vyšetření zatím obecně rutinně nedělá. Je však třeba mít na paměti, že existuje celá řada různých kombinací FV Leidenské mutace s dalšími typy trombofilií, jako mutací MTHFR. Ve více případech jsme pozorovali, že klinický průběh byl u těchto pacientů obecně težší. Klinicky však Leidenskou mutaci nelze od obrazu běžné chronické žilní insuficience rozlišit (Obr. 15).
Obr. 15. Klinicky není možné trombofilii rozeznat od vzhledu pacientů, kteří nemají trombofilii, Jsou možné různé klinické obrazy s varikozitami, ale i bez nich. Na obrázku je stav před a po provedené AF celého safénového komplexu, kdy dojde k výraznému zlepšení klinického stavu. 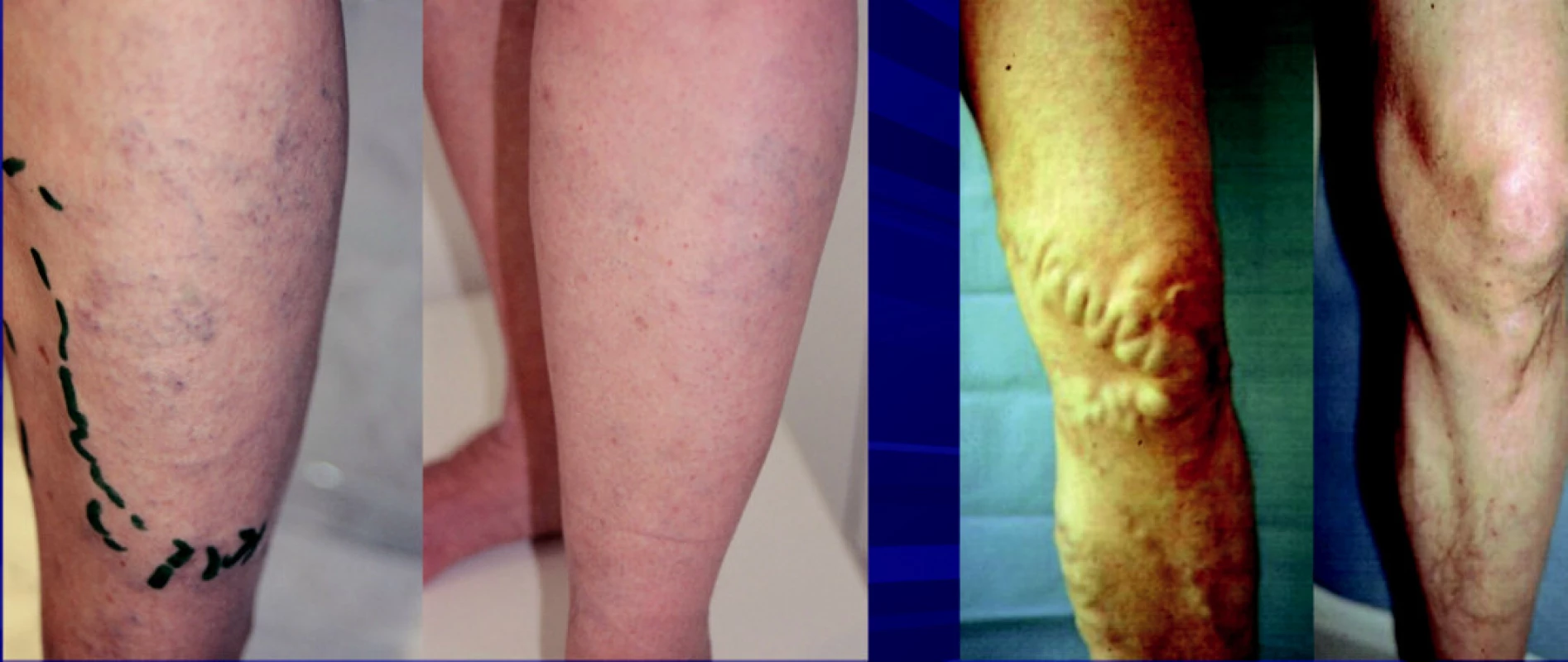
Naše nová varianta ambulantní flebektomie, kdy provádíme suprafasciální krosektomii VSM současně se suprafasciální krosektomií VSAA i VSAP, je technika bezpečná i u pacientů postižených trombofilíí. Je to výkon náročnější časově, kdy potřebujeme 4 hodiny pracovat na stehně a přibližně 3 hodiny práce v oblasti na lýtku. Tento nový postup výrazně snížil recidivy.
Obrovskou výhodou u takto náročné flebektomie je, že se provádí v lokální anestezii. Při lokální anestezii není vyřazen tonus svalstva, ale ani tonus fascií, což už je velká přednost této anestezie. Pacient má vlastně po celou dobu výkonu zachovanou hybnost končetiny, se kterou také během výkonu provádí cviky, aby nedošlo k přeležení končetiny. Tím, že u tohoto typu anestezie se nevyřadí svalstvo a facie ze své funkce, už samo o sobě představuje antitrombotický účinek pro končetinu. Dále má pacient okamžitý chodící režim po výkonu. Z ambulance ten den po výkonu odchází a ještě ten večer přibližně 1,5 hodiny nachodí. Skutečně ani u jednoho pacienta jsme nezaznamenali případ embolie nebo trombózy v důsledku provedeného výkonu.
Přestože pacienti s trombofiliemi mají větší sklon k trombogenezi, můžeme na základě našich výsledků shrnout, že ambulantní flebektomie je metoda pro pacienty s trombofilií bezpečná. O bezpečnosti výkonu ambulantní flebektomie referuje i Muller (4) po 40-ti leté zkušenosti. Muller sice neprováděl intrafasciální flebektomii velké safény, ale prováděl intrafasciální flebektomii malé safény a jeho poznatky jsou velmi cenné.
Na základě retrospektivního rozboru pooperačních průběhů u našich pacientů je třeba zdůraznit, že pacientů s trombofilií může dojít při nedodržení chodícího režimu po provedeném zákroku k neúměrné reakci, která pacienta zdravotně sice neohrožuje, ale která může pacienta dost vylekat a následkem toho se může pacient i neadekvátně chovat. Bolestivost, kterou si pacient přivodí je naprosto zbytečná, jak jsme dokázali na druhém souboru pacientů. Této neadekvátní bolestivé reakci se lze snadno vyhnout, když pacient správně dodrží 14-ti denní chodící režim a respektuje průběh hojení končetiny (tzv. akutní proteinovou fázi hojení, spojenou se zvýšení hladiny proteinů akutní fáze v krvi, která trvá 12 dní).
Dále jsme zachytili určité odlišnosti u pacientů s Leidenskou mutací ve srovnání s ostatními varikózními pacienty. Superficiální varixy u Leidenské mutace, jakož i u některých mutací MTHFR vykazovaly
- velkou křehkost, a
- byla zde velká citlivost výkonu.
I když je histologické hodnocení žilní stěny vždy velmi obtížné, jak vzhledem k postmortálnímu kontrakčnímu fenomenu, tak k individuálním změnám cév, můžeme říci, že změny cév trombofilních pacientů jsou výraznější. Tím si vysvětlujeme i větší křehkost varixů trombofilních pacientů a větší citlivost výkonu v místní anestezii.
Pro varikózní žíly jsou dále typická asymetrická ztluštění a ztenčení jednotlivých segmentů žilní stěny, a to i na jediném řezu. Sami jsme již v našich předchozích studiích zachytili zcela odlišný charakter mezi velkou a malou safénou (13), kde kromě rozdílu stěny obou safén jsme nalezli ve stěně střídání úseků varikózních změn s úseky ještě zcela zachovalé normální žilní stěny.
V další studii, kde jsme se zabývali aneuryzmaty ve varikózně změněné stěně, jsme nalezli úseky zcela ztluštělé žilní stěny, která velmi prudce přecházela do úseku zcela tenké stěny tvořené pouze endotelem a mezibuněčnou hmotou bez svaloviny(14).
Většina autorů předpokládá, že zeslabení žilní stěny je výsledkem změny struktury žilní stěny, jak v souhrnu referuje např. Golledge (15). Sansilvestri-Morel (16) uvádí, že buńky hladké svaloviny varikózní žíly produkují více kolagenu typu I než III. Křížková-Prokopová (17) pozoruje změnu poměru jednotlivých komponent žilní stěny ve shodě s literaturou, přibývá kolagenu a ubývá počet elastických vláken, ta jsou dezorganizována a fragmentována. Častým nálezem bývají i zmnožená a dilatovaná vasa vasorum. Jak popisuje Badier (18) právě změny ve fenotypu buněk hladké svaloviny, změna metabolismu extracelulární matrix a neo-angiogeneze jsou hlavní mechanismy přispívající k varikózní remodelizaci žilní stěny.
Metabolické (degenerativní) formy buněk hladké svaliny (SMC) jsou typickým nálezem, většinou ojediněle v tunica intima, dle stupně postižení – někde i ve shlucích zasahují až do tunica media. Tyto formy se liší od kontraktilních forem SMC jak redukcí počtu kontraktilních filament, tak i ztrátou barvitelnosti cytoplasmy – typicky perinukleárně.
Jak popisuje Wali (19), ve varikózně změné VSM buňky hladké svaloviny mění strukturu, podléhají degenerativním změnám, jsou vakualizované se známkami fagocytické aktivity a oddělené zvětšeným množstvím extracelulárních kolagenních vláken. O dvou typech různých SMC svědčí i rozdílná intenzita zbarvení v případě imunohistochemické detekce hladkosvalového aktinu zjištěná v práci Porta (20).
Mutace MTHFR je podceňovaná. V našem souboru měli její nositelé horší klinický průběh i výskyt phlebitis superficialis právě kombinace mutací (FV-Leiden + MTHFR).
Je třeba pacienty upozornit na tuto skutečnost, že i zánět žilní stěny může proběhnout klinicky zcela inaparentně. Histologicky jsme zachytili větší zmnožení vasa vasorum i buněčných infiltrátů u trombofilních pacientů! Tento zánět se může teprve až za určitých náročnějších situacích stát manifestní. Sami jsme u našich potvrzených mutací zachytili klinicky manifestní phlebitis superficialis u dvou pacientek po jízdě automobilem trvající déle než 3 hodiny a u jednoho muže po cestování letadlem trvajícím rovněž přes 3 hodiny letu.
Na základě našich výsledků bychom doporučovali u pacientů s varixy heparinizaci nízkomolekulárními hepariny
- při letech a cestování obecně déle než 3 hodiny,
- dále při úrazech a sádrových fixacích a imobilizaci pacienta
- při zákrocích v jiné než lokální anestezii.
Závěr
Ambulantní flebektomie s kompletní extrakcí celého safénového komplexu je metoda bezpečná bez rizika embolie, trombózy nebo jiné vážné komplikace pro pacienta. Musí se však dodržet správné podmínky výkonu:
- PN po dobu 14 dní, jelikož doporučujeme respektovat 12 dní trvající reakci akutní fáze provázenou zvýšením proteinů akutní fáze v krvi.
- Intenzivní chodící režim po dobu dvou týdnů
Leidenskou mutaci nelze klinicky rozeznat. Tím, že se vyšetření nedělají rutinně, často nevíme zda-li před sebou mutaci máme, nebo ne. Pomoci může anamnéza – je nutno se ptát
- na proběhlou phlebitis superficialis,
- na opakované samovolné potraty, nebo
- na porody mrtvého plodu.
Zkratky
- AF: ambulantní flebektomie
- HE: hematoxylin-eosin
- HS: hiatus saphenus
- MTHFR: metylentetrahydrofolátová reduktáza
- M-TRI: modifikovaný trichrom
- SMC: degenerativní metabolická forma myocytu
- VF: vena femoralis
- VSM: vena saphena magna
- VSAA: vena saphena accesoria anterior
- VSAP: vena saphena accesoria posterior
- VSP: vena saphena parva
Poděkování
Mé srdečné poděkování patří pracovnímu týmu Ústavu histologie a embryologie Lékařské fakulty Univerzity Karlovy v Plzni, díky němuž celá práce mohla vzniknout.
Dr. med. MUDr. Magdalena Anna Horáková
Flebologie
Holečkova 70
150 00 Praha 5
Zdroje
1. Kvasnička, J. Trombofilie a trombotické stavy v klinické praxi. Praha: Grada Publishing, 2003.
2. Bobek, K., Čepelák, V. Tromboembolická nemoc žilního původu. Praha: Státní zdravotnické nakladatelství, 1959, s. 148.
3. Dortu, J. La crossectomie sus-fasciale: au cours de la phlébectomie ambulatoire du complexe saphénien interne à la cuisse. Phlébologie 1993, 46(1), p. 123-137.
4. Muller, R. Mise au point sur la phlébectomie ambulatoire selon Muller. Phlébologie 1996, 49(30), p. 335-344.
5. Lang, J., Wachsmuth, W. Bein und Statik. Berlin-Heidelberg-New York: Springer-Verlag, 1972; p. 109.
6. Potron, G., Trzeciak, M.C. Compte rendu de la réunion sur l’hémostase. Phlébologie 2005, 58(4), p. 373-383.
7. Hamel-Desnos, C., Ouvry, P., Nesnos, P. et al. Sclérothérapie et thrombophilie: Démarche pour un consensus dans la sclérothérapie chez les thrombophiles. Phlébologie 2003, 56(2), p. 165-169.
8. Vojáček, J., Malý, M. Arteriální a žilní trombóza v klinické praxi. Praha: Grada Publishing, 2004.
9. Azoulay, J.P., Franchitti, D.S., Vin, F. Accidents trombo-emboliques au décours de la sclérothérapie. Thrombophlie et sclérothérapie. Phlébologie 2000, 53(4), p. 442-467.
10. Hanss, M. Thrombophilie: Indications du bilan d’hémostase en 2004 et perspectives d’avenir. Phlébologie, 2004, 57(4), p. 403-407.
11. Kočova, J. Overall staining of connective tissue and the muscular layer of vessels. Folia Morphologica 1970, 3, p. 293-295.
13. Horáková, M.A., Kočová, J., Prokopová, V., Horáková, E. Étude comparative chez l´adulte de l´évolution des petite et grande saphènes à travers l´observation et l´analyse de la varicose de ces deux types de veines. Phlébologie 2000, 2, p. 147-153.
14. Horáková, M.A., Kočová, J., Křížková, V., Horáková, E. Histologie, structure de la paroi et évolution de l’anévrysme veineux de la grande veine saphène par rapport à celui de la petite saphène. Phlébologie 2002, 55(2), p. 139-147.
15. Golledghe, J., Quigley, F.G. Pathogenesis of varicose veine. Eur. J. Vasc. Endovasc. Surg. 2003, 25, p. 319-324.
16. Sansilvestri-Morel, P., Rupin, A., Badier-Commander, C. et al. Imbalance in the synthesis of collagen type I and collagen type III in smooth muscle cells derived from human varicose veins. J. Vasc. Res. 2001, 38, p. 560-568.
17. Prokopová-Křížková, V., Kočová, J., Horáková, M., Třeška, V. Struktura stěny normální a varikózní vény dolní končetiny. Praktická flebologie, 1998, 1, s. 34-36.
18. Badier-Commander, C., Couvelard, A., Henin, D. et al. Smooth muscle cell modulation and cytokine overproduction in varicose veins. An in situ study. J. Pathol. 2001, 193, p. 398-407.
19. Wali, M.A., Eid, R.A. Smooth muscle changes in varicose veins: an ultrastructural study. J. Smooth Muscle. Res. 2001, 37, p. 123-135.
20. Porto, L.C., Ferreira, M.A.P., Costa, A.M.A., da Silveira, P.R.M. Immunolabeling of type IV collagen, lamini and varicose saphenous veine. Angiology 1998, 49, p. 391-398.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek Jmenování nových profesorůČlánek Velký mezonČlánek NÁZORČlánek NÁZORČlánek Co píše o alkoholu LancetČlánek Jubilea
Článek vyšel v časopisePraktický lékař
Nejčtenější tento týden
2009 Číslo 10- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Magnosolv a jeho využití v neurologii
-
Všechny články tohoto čísla
- Posuzování zdravotního stavu a pracovní schopnosti u onkologicky nemocných
- Ambulantní flebektomie u trombofilních pacientů
- Dříve vyslovená přání (advance directives) v USA
- Patofyziologie, symptomatologie a diagnostika hyperaktivního močového měchýře
- Jmenování nových profesorů
- Vrozené poruchy sexuálního vývoje (DSD) a jejich následky
- Skupinová kognitivně behaviorální terapie obezity v primární prevenci metabolického syndromu
- Terapeutická role ambroxolu v léčebném ovlivňování mukociliární clearance u „bronchitického fenotypu“ CHOPN
- Léčba rekombinantním humánním erytropoetinem
- Zpráva WHO o úmrtích při dopravních nehodách
- Akreditace ordinací všeobecných praktických lékařů v České republice
- Mikrometastáza v sentinelové uzlině – nutnost disekce axilárních uzlin?
- Neobvyklý případ závislosti na více psychoaktivních látkách
- Občanský průkaz při poskytování zdravotní péče
- Miniportréty slavných českých lékařů
- Velký mezon
- Enzym ozdobený Nobelovou cenou
- Ceny Josefa Hlávky za rok 2008
- NÁZOR
- NÁZOR
- Co píše o alkoholu Lancet
- Jubilea
- Praktický lékař
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Občanský průkaz při poskytování zdravotní péče
- Léčba rekombinantním humánním erytropoetinem
- Vrozené poruchy sexuálního vývoje (DSD) a jejich následky
- Akreditace ordinací všeobecných praktických lékařů v České republice
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



