-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Neuroendokrinní nádor prsu – metastáza či primární karcinom prsu? Kazuistika
Neuroendocrine tumor of the breast - metastasis or primary breast carcinoma? Case report
A 74-year-old women with a history of neuroendocrine tumor in the terminal ileum presented on screening mammography with an irregular hypoechogenic mass in the upper outer quadrant of the left breast. A core biopsy showed a neuroendocrine tumor, interpreted as a probable metastasis from the intestinal primary. Other masses were found in the right lobe of the liver. Resection of the masses in the breast and liver was performed at the same time. Morphological and immunohistochemical findings (positive neuroendocrine markers, estrogene receptors and negative cytokeratine 7, mammaglobin, GCDFP-15, cytokeratine 20 and progesterone receptors) were consistent with a diagnosis of a metastatic well-differentiated neuroendocrine tumor, despite some estrogen receptor positivity. Issues of primary and metastatic breast neuroendocrine tumors are discussed in detail.
Keywords:
neuroendocrine tumor – breast carcinoma – metastasis
Autoři: Markéta Petrová
Působiště autorů: Oddělení patologické anatomie, Oblastní nemocnice Náchod a. s.
Vyšlo v časopise: Čes.-slov. Patol., 51, 2015, No. 3, p. 128-131
Kategorie: Původní práce
Souhrn
Prezentujeme případ 74-leté ženy s neuroendokrinním nádorem terminálního ilea, u které bylo na screeningové mamografii nalezeno nepravidelné hypoechogenní ložisko v horním zevním kvadrantu levého prsu. V punkční biopsii z ložiska zastižen obraz neuroendokrinního nádoru a bylo vysloveno podezření na jeho metastatický původ z tenkého střeva. Další ložiska byla přítomna v pravém laloku jater. Pacientce byla následně provedena resekce ložiska v prsu a ložisek v játrech. Morfologický a imunohistochemický obraz (pozitivita neuroendokrinních markerů, estrogenových receptorů a negativní průkaz cytokeratinu 7, mammaglobinu, GCDFP-15, cytokeratinu 20 a progesteronových receptorů) v resekátech odpovídal dobře diferencovanému neuroendokrinnímu tumoru, i přes pozitivitu estrogenových receptorů velmi pravděpodobně metastatického původu z tenkého střeva. V předkládaném článku diskutujeme problematiku primárních a metastatických neuroendokrinních nádorů prsu.
Klíčová slova:
neuroendokrinní nádor – karcinom prsu – metastáza
Neuroendokrinní nádory (NETy) představují heterogenní skupinu poměrně vzácných nádorů, které se od běžných epitelových nádorů liší histogenetickým původem, mikroskopickým obrazem i biologickým chováním. Histogeneticky mají tyto nádory blízký vztah k rozptýleným endokrinním buňkám difúzního neuroendokrinního systému, nebo podle dnešních představ spíše k prekurzorům těchto buněk. Často jsou spojeny s hromaděním a uvolňováním biologicky aktivních látek jako je serotonin, somatostatin, gastrin a další. NETy postihují především střední úsek trávicího traktu a bronchopulmonální systém. V prsu patří k raritním nádorům. V této lokalitě tvoří méně jak 0,1 % všech nádorů prsu (1). Jsou reprezentovány neuroendokrinními nádory primárními (tj. dobře diferencované neuroendokrinní tumory, neuroendokrinní karcinomy, nádory s neuroendokrinní diferenciací) a metastatickými. Bez znalosti klinických dat a v málo reprezentativním vzorku není diagnostika těchto lezí snadná. Na metastatický původ NETy z gastrointestinálního traktu by nás měla upozornit nepřítomnost intraduktální složky nádoru, absence mikrokalcifikací a imunohistochemická pozitivita neuroendokrinních markerů při negativitě markerů specifických pro mléčnou žlázu. V prsu se však mnohem častěji setkáme s metastázami jiných nádorů, především s maligním melanomem a karcinomy jakékoliv lokalizace (hlavně plic, ledvin a vnitřního genitálu) (2), u děvčat pak s rhabdomyosarkomem (3).
MATERIÁL A METODIKA
K histologickému vyšetření jsme obdrželi proužky tkáně z jehlové biopsie mléčné žlázy fixované v 10% formalínu. Materiál byl zpracován klasickou parafinovou technikou a preparát byl obarven hematoxylinem eozinem. Následně bylo provedeno imunohistochemické vyšetření, při kterém byly použity tyto protilátky: chromogranin (klon 5H7, 1 : 600, Novocastra), synaptofyzin (klon SY38, 1 : 10, Dako), cytokeratinový kokteil (klon AE1/AE3, 1 : 100, Dako), cytokeratin 7 (CK7) (klon OV-TL12/30, 1 : 100, Dako), cytokeratin 20 (CK20) (klon Ks20.8, 1 : 25, Dako), mammaglobin (klon 304-1A5, 1 : 200, Dako), gross cystic disease fluid protein 15 (GCDFP-15) (klon EP1582Y, cca 1 : 28, Ventana), estrogenový receptor (ER) (klon SP1, 1 : 1000, Ventana), progesteronový receptor (PR) (klon 1E2, 1 : 1000, Ventana ) a Ki-67 (klon 30-9, 1 : 500, Ventana), caudal type homeobox 2 (CDX2) (klon DAK-CDX2, 1 : 50, Dako).
POPIS PŘÍPADU
U 74-leté ženy byla v roce 2010 provedena pravostranná hemikolektomie pro NET terminálního ilea. Histologicky se jednalo o dobře diferencovaný neuroendokrinní tumor maximálního rozměru 25 mm s metastázami ve 4 z 6 vyšetřených lymfatických uzlin (obr. 1). S odstupem 2 let bylo na screeningové mamografii nalezeno nepravidelné hypoechogenní ložisko průměru 5 mm v horním zevním kvadrantu levého prsu. V punkční biopsii ložiska mléčné žlázy byl mikroskopicky zastižen invazivně rostoucí solidně alveolárně uspořádaný maligní nádor tvořený buňkami s drobnými uniformními jádry, jemně zrnitým chromatinem a středním množstvím eozinofilní cytoplazmy (obr. 2A), mitózy nebyly patrny. Vzhledem k anamnéze pacientky bylo vysloveno podezření na metastatický původ z tenkého střeva a nález byl konzultován na pracovišti vyššího typu, kde bylo provedeno imunohistochemické vyšetření. Nádorové buňky exprimovaly chromogranin, synaptofyzin a cytokeratinový koktejl (AE1/AE3). Negativní byl průkaz CK7, CK20, GCDFP-15, mammaglobinu a progesteronových receptorů (obr. 2B-F). Proliferační aktivita stanovená markerem Ki-67 byla nízká (do 1 %). Ve dvou třetinách buněk byla přítomna slabá až středně silná exprese estrogenových receptorů (obr. 2D). Nález byl i přes pozitivitu estrogenových receptorů uzavřen jako dobře diferencovaný neuroendokrinní tumor (NET-G1), velmi pravděpodobně metastazující z tenkého střeva s nutnou klinickou korelací.
Obr. 1. Dobře diferencovaný neuroendokrinní tumor terminálního ilea, barvení HE (zvětšení 40x). 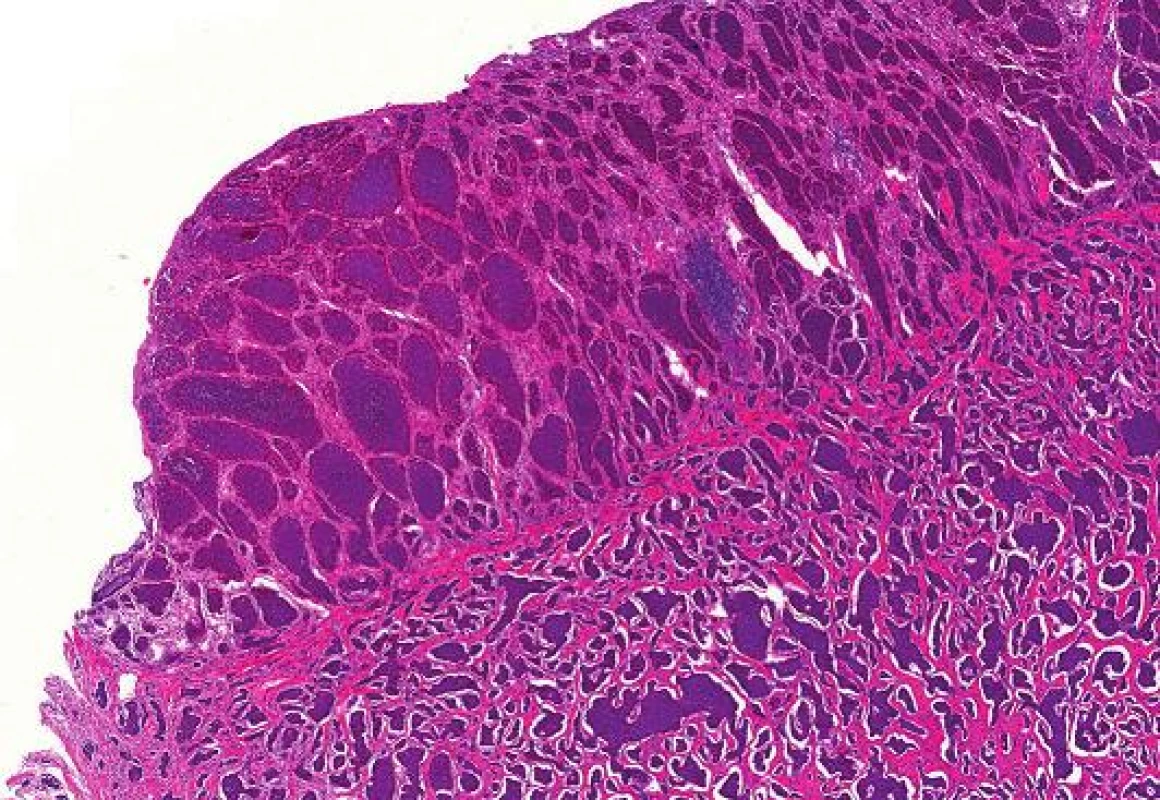
Obr. 2. Jehlová biopsie mléčné žlázy. A: barvení HE (zvětšení 200x), B: imunohistochemický průkaz chromograninu (zvětšení 100x), C: imunohistochemický průkaz AE1/AE3 (zvětšení 100x), D: imunohistochemický průkaz ER, slabá až středně silná pozitivita v nádoru, pozitivní vnitřní kontrola v lalůčcích mléčné žlázy (zvětšení 100x), E: imunohistochemický průkaz mammaglobinu, negativní exprese v nádoru, pozitivní vnitřní kontrola v lalůčcích mléčné žlázy (zvětšení 100x), F: imunohistochemický průkaz GCDFP-15, negativní exprese v nádoru, pozitivní vnitřní kontrola v lalůčcích mléčné žlázy (zvětšení 100x). 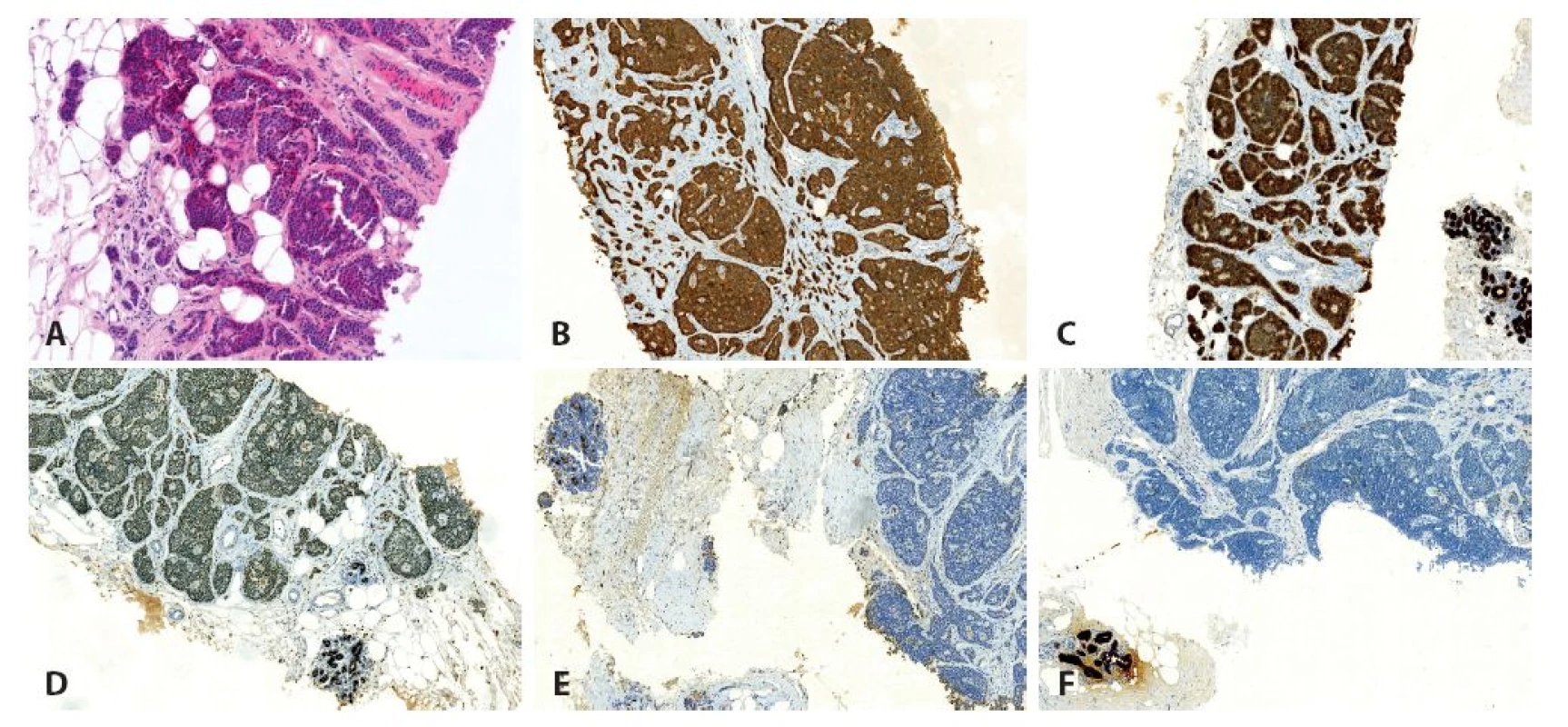
Pacientka podstoupila v jedné době extirpaci ložiska v prsu se sentinelovými uzlinami a resekci suspektních ložisek velikosti 16 mm a 3 mm v játrech. Morfologický obraz nádoru v extirpátu z prsu byl shodný s punkční biopsií. Celkem byly vyšetřeny 4 lymfatické uzliny, které byly zpracovány jako sentinelové. Nádorové struktury v nich prokázány nebyly. V játrech šlo o metastázy NET-G1 obdobného vzhledu jako v ložisku z levého prsu.
DISKUZE
Neuroendokrinní nádory jsou tumory pomalu rostoucí, často se klinicky projevují až generalizací s metastatickým postižením lymfatických uzlin, jater, plic a kostí. K neobvyklým lokalizacím metastáz neuroendokrinních nádorů patří prs, dále měkké tkáně orbity a srdce (4). V prsu se imunohistochemickou analýzou prokáže neuroendokrinní (NE) diferenciace ve více než 30 % invazivních karcinomů prsu, především v mucinózním karcinomu a solidním papilárním karcinomu. Jde většinou o ojedinělou expresi NE markerů v izolovaných buňkách či skupinkách buněk (5). Za primární neuroendokrinní karcinom prsu (PNEC) je považován nádor exprimující NE markery ve více jak 50 % nádorových buněk (6). V poslední WHO klasifikaci nádorů prsu z roku 2012 najdeme nádory neuroendokrinního vzhledu v podskupině málo častých nádorů invazivního karcinomu. Jsou dále členěny na: dobře diferencované neuroendokrinní tumory (neuroendocrine tumors well-differentiated), neuroendokrinní karcinomy (neuroendocrine carcinomas, poorly differentiated/small cell carcinomas) a nádory s neuroendokrinní diferenciací (carcinomas with neuroendocrine differentiation). Pro odlišení primárního a metastatického NETu jsou zásadní relevantní klinická data a imunohistochemické vyšetření.
PNEC je v literatuře popisováno kolem 30 případů (7). Klinicky se neodlišují od ostatních karcinomů prsu. 45 % nádorů je dobře diferencovaných, 40 % středně a 15 % špatně diferencovaných (8). Sapino a kol. popisuje pět morfologických typů - solidní, alveolární, malobuněčný, solidní-papilární a celulární-mucinózní (9). Diagnostická je exprese NE markerů ve více jak 50 % nádorových buněk a přítomnost in situ složky nádoru. Imunohistochemicky obvykle bývá pozitivita CK7, mammaglobinu, GCDFP-15, estrogenových a progesteronových receptorů (10), onkoprotein HER-2 je obvykle negativní (11). Na samotnou imunohistochemii však nelze spoléhat, vždy je nutná klinická korelace. Pozitivita vyšetřovaných markerů s nižší diferenciací nádoru klesá. Exprese GCDFP-15 byla přítomna v 6 z 9 případů PNEC a exprese mammaglobinu ve 4 z 9 případů PNEC (12).
NETy metastazující z gastrointestinálního traktu morfologicky věrně napodobují primární zdroj, tvoří solidně-alveolární, rozetovité či trabekulární formace. Imunohistochemicky je průkaz mammaglobinu a GCDFP-15 vždy negativní. Ojediněle je v literatuře popisována pozitivita ER a PR (12,13). Crona se spolupracovníky uvádí v retrospektivní studii pozitivitu ER v 1/13 případů NET tenkého střeva (13). U NETů metastazujících z plic se s pozitivitou ER a PR setkáme daleko častěji, pozitivita ER je udávána až ve 41/71 (57 %) případů a exprese PR u 22/71 (30 %) případů (14). NET terminálního ilea u naší pacientky exprimoval ER slabě a středně silně ve 2/3 buněk, tedy stejně jako metastatické ložisko v prsu (obr. 3). Z dalších imunohistochemických markerů, který by nás mohl navést na původ NETu z GITu je CDX2. CDX2 je markerem intestinální diferenciace (normální i nádorové střevní tkáně), známá je vysoká míra exprese u kolorektálních karcinomů. Aberantní exprese CDX2 je však Popisována i u adenokarcinomů močového měchýře, prostaty, cervixu, mucinózního karcinomu ovaria a dalších. Lin a kol. popisuje ve studii 60 NETů GITů (primárních i metastatických) pozitivitu CDX2 ve 100 % NETů apendixu, v 86 % NETů tenkého střeva, v 75 % NETů tlustého střeva, v 18 % NETů rekta, v žádném NETu žaludku nebyla Exprese CDX2 zastižena (15). U PNEC prsu doposud nejsou údaje o expresi CDX2 známy, vzhledem k absenci exprese CDX2 u adenokarcinomů prsu (16) se však předpokládá jejich negativita.Vyšetření CDX2 v našem případu ukázalo difúzní silnou pozitivitu jak v nádoru střeva tak v ložisku v prsu. Demonstrovaný případ neuroendokrinního nádoru v prsu je tedy díky klinicko-patologické korelaci ukázkou vzácné metastázy NETu střeva. Tabulka č. 1 shrnuje hlavní vyšetřované markery našeho případu ve srovnání s PNEC. Kontrolní octreoscany provedené po resekci prsu byly bez patologické kumulace somatostatinových receptorů. V současné době (poslední kontrola v září 2014) je pacientka bez dalšího klinicky zjevného metastatického postižení.
Obr. 3. Imunohistochemický průkaz ER v NETu terminálního ilea, slabá až středně silná pozitivita (zvětšení 200x). 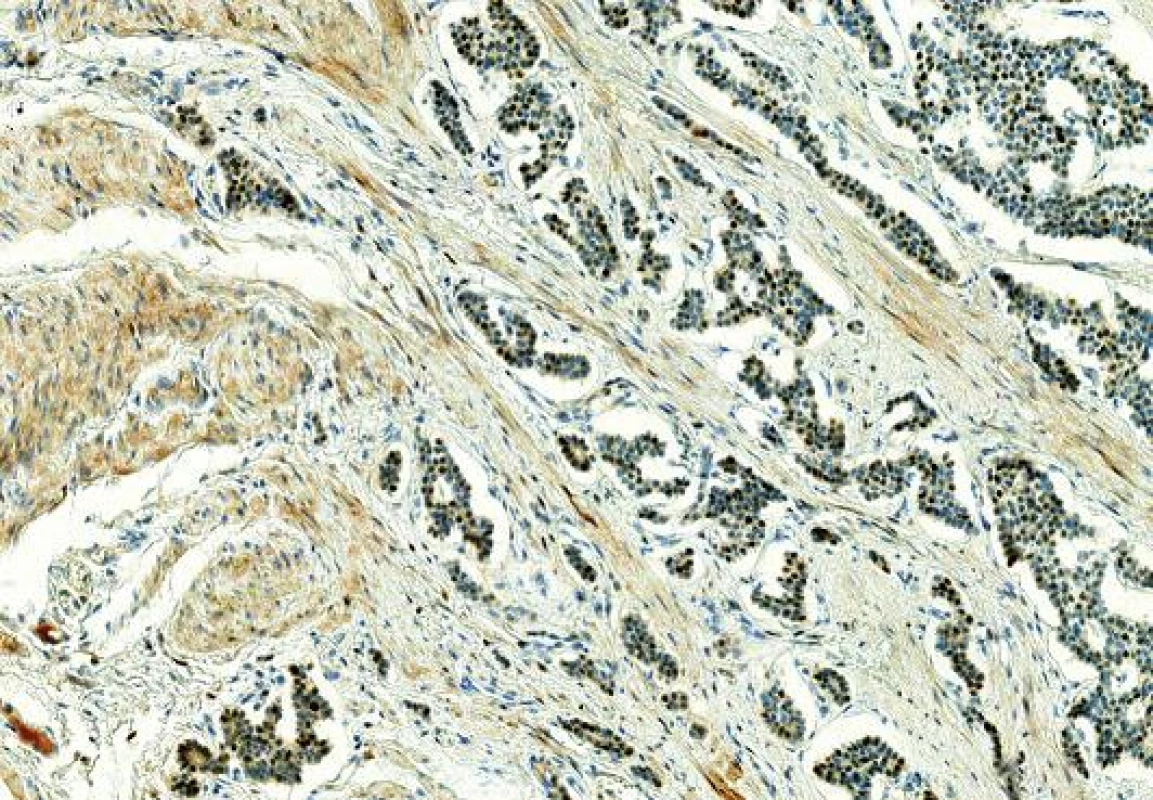
Tab. 1. Souhrn vyšetřovaných markerů u NET GIT v porovnání s PNEC. 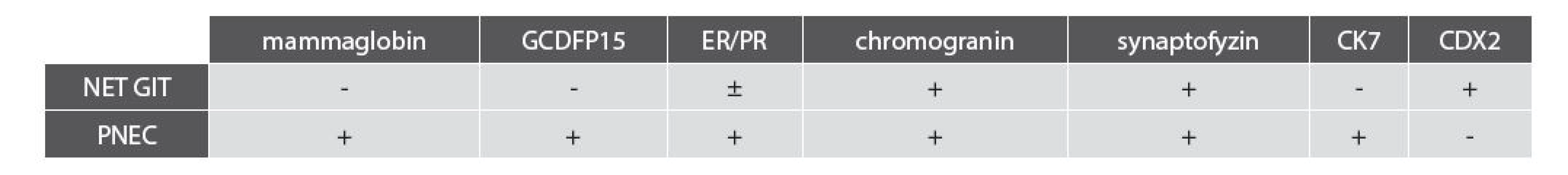
NET GIT, neuroendokrinní nádor gastrointestinálního traktu; PNEC, primární neuroendokrinní karcinom prsu; GCDFP15, gross cystic disease fluid protein 15; ER/PR, estrogenové a progesteronové receptory; CK7, cytokeratin 7; CDX2, caudal type homeobox 2. PODĚKOVÁNÍ
MUDr. E. Hovorkové za konzultační vyšetření. MUDr. T. Rozkošovi za laskavé zhotovení fotodokumentace a poskytnutí metodiky imunohistochemického vyšetření.
PROHLÁŠENÍ
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Adresa pro korespondenci:
MUDr. Markéta Petrová
Oddělení patologické anatomie
Purkyňova 446, Náchod 547 69
tel.: +420 491 601 251
e-mail: petrova.marketa@nemocnicenachod.cz
Zdroje
1. Ogawa H, Nishio A, Satake H, et al. Neuroendocrine tumor in the breast. Radiat Med 2008; 26(1): 28–32.
2. Kinkor Z, Mečiarová I. Metastázy epitelových neuroendokrinních tumorů do prsu – omyl není nutný. Breast Cancer News 2013; 3(2): 4-7.
3. Vizcaino I, Torregrosa A, Higueras V, et al. Metastasis to the breast from extramammary malignancies: a report of four cases and a review of literature. Eur Radiol 2001; 11(9): 1659-1665.
4. Srirajaskanthan R, Desai K, Jayaratnam A, Carras E, Toumpanakis C, Meyer T, Caplin M. Uncommon sites for metastasis of neuroendocrine tumor in adults. J Clin Oncol 2009; 27(15S): e15683.
5. Lakhani SR, Ellis IO, Schnitt SJ, et al. WHO Classification of Tumours of the Breast (4th ed.).Lyon: IARC; 2012 : 62-63.
6. Hanby AM, Brannan R. Neuroendocrine Tumours of the Breast. In: Khan A. Surgical Pathology of Endocrine and Neuroendocrine Tumours. New York, NY: Humana Press; 2009 : 165-172.
7. Akhtar K, Zaheer S, Ahmad SS, Hassan MJ. Primary neuroendocrine carcinoma of the breast. Indian J Pathol Microbiol 2009; 52(1): 71–73.
8. Tavassoli FA, Devilee P. WHO Pathology and Genetics of Tumours of the Breast and Female Genital Organs. Lyon: IARC; 2003 : 32-34.
9. Sapino A, Righi L, Cassoni P, Papotti M, Pietribiasi F, Bussolati G. Expression of the neuroendocrine phenotype in carcinomas of the breast. Semin Diagn Pathol 2000; 17(2): 127–37.
10. Fritzsche FR, Thomas A, Winzer KJ, et al. Co-expression and prognostic value of gross cystic disease fluid protein 15 and mammaglobin in primary breast cancer. Histol Histopathol 2007; 22(11): 1221-1230.
11. Ghanem S, Kabaj H, Naciri S, Glaoui M, Ismaili N, Benjaafar N, Errihani H. Primary neuroendocrine carcinoma of the breast: A rare and distinct entity. J Canc Res Exp Oncol 2011; 3(5): 50-54.
12. Richter-Ehrenstein CH, Arndt J, Buchendahl ACH, et al. Solid neuroendocrine carcinoma of the breast. Metastases or primary tumors? Breast Canc Res Treat 2010; 124(2): 413-417.
13. Crona J, Granberg D, Norlen O, Wärnberg F, Stålberg P, Hellman P, Björklund P. Metastases from Neuroendocrine Tumors to the Breast Are More Common than Previously Thought. A Diagnostic Pitfall? World J Surg 2013; 37(7): 1701-6.
14. Sica G, Wagner PL, Altorki N et al. Immunohistochemical expression of estrogen and progesterone receptors in primary pulmonary neuroendocrine tumors. Arch Pathol Lab Med 2008; 132(12): 1889–1895.
15. Lin X, Saad RS, Luckasevic TM, Silverman JF, Liu Y. Diagnostic value of CDX-2 and TTF-1 expressions in separating metastatic neuroendocrine neoplasms of unknown origin. Appl Immunohistochem Mol Morphol 2007; 15(4): 407-414.
16. O’Connell FP, Wang HH, Odze RD. Utility of immunohistochemistry in distinguishing primary adenocarcinomas from metastatic breast carcinomas in the gastrointestinal tract. Arch Pathol Lab Med 2005; 129(3): 338-347.
Štítky
Patologie Soudní lékařství Toxikologie
Článek Jaká je Vaše diagnóza?
Článek vyšel v časopiseČesko-slovenská patologie

2015 Číslo 3-
Všechny články tohoto čísla
- Transplantační patologie - I. díl
- Aby mohl patolog morfologii interpretovat, musí nejdříve tkáni rozumět
- MONITOR aneb nemělo by vám uniknout, že
- Úvod do problematiky transplantační patologie
- Specializační kurz v patologii
- Transplantace ledviny z pohledu nefrologa
- MONITOR aneb nemělo by vám uniknout, že
- Tubulo-intersticiální rejekce štěpů ledviny
- Humorální rejekce a aktualizace Banffské klasifikace 2013
- MONITOR aneb nemělo by vám uniknout, že
- Infekce po transplantaci ledviny
- “Shadow cell” diferenciácia v endometrioidných karcinómoch tela maternice. Jej častý výskyt a pozitivita na beta-katenín
- Jaká je Vaše diagnóza?
- Neuroendokrinní nádor prsu – metastáza či primární karcinom prsu? Kazuistika
- MONITOR aneb nemělo by vám uniknout, že
- Jaká je Vaše diagnóza? Odpověď
- Melanocytární matrikom - kazuistika
- Adenom pylorických žlázek: histologické, imunohistochemické a molekulárně genetické zhodnocení 23 nádorů
- MONITOR aneb nemělo by vám uniknout, že
- Česko-slovenská patologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Adenom pylorických žlázek: histologické, imunohistochemické a molekulárně genetické zhodnocení 23 nádorů
- Infekce po transplantaci ledviny
- Úvod do problematiky transplantační patologie
- Neuroendokrinní nádor prsu – metastáza či primární karcinom prsu? Kazuistika
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



