-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Granulomatózní hepatitida jako vzácná terapeutická komplikace
Granulomatous hepatitis as a rare therapeutic complication
Intravesical BCG application is an established and relatively simple treatment for superficial carcinomas of the urinary bladder. It is usually well tolerated and has only mild side effects. We report a case of a 76-year-old immunocompetent man in whom this treatment led to a rare complication characterized by granulomatous hepatitis and pneumonitis. Elastography of the liver was used during diagnosis.
Key words:
granulomatous hepatitis – elastography – BCG – urinary bladder cancer
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Submitted:
9. 3. 2016Accepted:
7. 4. 2016
Autoři: K. Dvořák 1; V. Šmíd 1; R. Jakša 2
Působiště autorů: IV. interní klinika – klinika gastroenterologie a hepatologie 1. LF UK a VFN v Praze 1; Ústav patologie, 1. LF UK a VFN v Praze 2
Vyšlo v časopise: Gastroent Hepatol 2016; 70(2): 141-144
Kategorie: Hepatologie: kazuistika
doi: https://doi.org/10.14735/amgh2016141Souhrn
Intravezikální aplikace BCG vakcíny je zavedená, relativně jednoduchá a bezpečná terapeutická metoda užívaná v léčbě povrchových karcinomů močového měchýře. Obvykle bývá dobře tolerována, nežádoucí účinky bývají mírné. Prezentujeme případ 76letého imunokompetentního pacienta, u kterého vedla tato léčba k vzácné komplikaci ve formě granulomatozní hepatitidy a pneumonitidy. V diagnostice tohoto stavu byla použita také elastografie jater.
Klíčová slova:
granulomatózní hepatitida – elastografie – BCG – tumor močového měchýřeÚvod
Bacillus Calmette-Guérin (BCG) je živá atenuovaná forma Mycobacterium bovis, která se užívá k vakcinaci proti tuberkulóze. Imunoterapie pomocí intravezikální aplikace BCG je relativně jednoduchá a efektivní metoda, která se užívá při léčbě povrchového karcinomu močového měchýře. Virulence atenuovaného BCG je u imunokompetentních pacientů velmi nízká, a tato terapie je tak obvykle dobře tolerována [1]. Bývají udávány pouze mírné symptomy, jako jsou subfebrilie, únava a dysurie. Nežádoucí účinky se vyskytují u 3–5 % pacientů a obvykle představují infekční komplikace (bakteriální cystitida, granulomatózní prostatitida, epididymitida, orchitida). Vzdálené manifestace BCG diseminace, jako jsou vaskulární či oční komplikace, jsou méně časté [2], a diseminace BCG infekce manifestující se jako granulomatózní pneumonitida nebo hepatitida jsou raritní [3].
Prezentujeme případ 76letého imunokompetentního pacienta s anamnézou karcinomu močového měchýře a granulomatózní hepatitidou a pneumonitidou jako komplikací intravezikální BCG imunoterapie.
Popis případu
V létě 2015 byl na naší klinice vyšetřován 76letý pacient s metabolickým syndromem (diabetik 2. typu, hypertonik, hyperlipoproteinemie na terapii statiny), po kurativní resekci karcinomu žlučníku v roce 2010, po transuretrální resekci tumoru močového měchýře v roce 2013. V prosinci 2014 byla zjištěna jeho recidiva – tři papilární tumory v močovém měchýři, které byly odstraněny transuretrálně – a následně bylo rozhodnuto o imunoterapii instilací BCG do močového měchýře.
Pět dnů po deváté intravezikální aplikaci BCG vakcíny se objevily febrilie, polakisurie a strangurie a pacient byl vyšetřen a následně přijat na Urologickou kliniku 1. LF UK a VFN v Praze pro suspektní uroinfekci. Nasazená antibiotická léčba (ciprofloxacin + gentamicin) byla bez efektu, vedla naopak k progresi renální insuficience. Pacient byl vyšetřen pneumologem (pro febrilie související s aplikací BCG), nefrologem (pro zhoršování renálních parametrů) a hepatologem (pro elevaci jaterních testů). Kvůli hypokalemii a progresi renálních parametrů byl pak k další léčbě přeložen na intermediální lůžko IV. interní kliniky 1. LF UK a VFN v Praze.
Provedená vyšetření
Při fyzikálním vyšetření byl kromě jizvy po subkostálním řezu v pravém podžebří konstatován normální nález. Laboratorní vyšetření odhalila lehkou hyponatremii (Na 132 mmol/l) a hypochloremii (Cl 94 mmol/l), mírnou elevaci renálních parametrů (urea 10,8 mmol/l, kreatinin 116 μmol/l), smíšenou jaterní lézi (celkový bilirubin 19,7 μmol/l, konjugovaný bilirubin 11,6 μmol/l, ALT 2,54 μkat/l, AST 3,11 μkat/ l, GGT 8,89 μkat/l, ALP 4,41 μkat/l), dále CRP 69,3 mg/l a prokalcitonin 0,65 μg/l. V krevním obraze byla patrná mírná normochromní normocytární anémie (hemoglobin 120 g/l, MCV 89,5 fl, MCH 28,9 pg) – anémie chronických chorob, která byla u pacienta přítomna i v minulosti, a dále mírná trombocytopenie (trombocyty 138 × 109/l).
Játra i žlučovody vykazovaly normální sonografický obraz, žlučník nebyl patrný (stav po cholecystektomii). Skiagram hrudníku bez pozoruhodností. Pro podezření na akutní cholangitidu (febrilie, cholestáza) bylo provedeno MRCP, které vyloučilo choledocholitiázu či jinou obstrukci žlučových cest. Dále byly vyloučeny virové hepatitidy, negativní byly i autoprotilátky (ANA, SMA, AMA, LKM).
Pacient byl od přijetí do nemocnice léčen antibiotiky (ciprofloxacin + gentamicin, cefotaxim, amikacin, linezolid), přesto přetrvávaly febrilie kolem 38 °C. Kromě horeček byl však bez výraznějších subjektivních potíží. Vzhledem k předchorobí s léčbou pomocí BCG, febriliím a nálezu smíšené jaterní léze byla vyslovena suspekce na granulomatózní hepatitidu jako možnou komplikaci této terapie.
Byla tedy provedena jaterní biopsie a histologický nález v játrech tuto diagnózu potvrdil (obraz granulomatózní hepatitidy s cholestázou) (obr. 1 a 2). Dále jsme vyšetření doplnili o výpočetní tomografii s vysokým rozlišením (HRCT – high resolution CT) vyšetření plic (obr. 3), kde byl patrný takřka typický obraz mikronodulárního tuberkulózního procesu. Tuberkulinový test byl negativní (Mantoux II 0 mm), QuantiFERON Gold pozitivní. Pacient byl následně přeložen na pneumologickou kliniku.
Obr. 1. Jaterní biopsie – punkční váleček jaterního parenchymu délky 6 mm se zánětlivou, převážně lymfocytární infiltrací, s neutrofilními granulocyty a „interface“ aktivitou. Jaterní parenchym je lobulárně uspořádaný s četnými hepatocyty s balonovitou degenerací, místy zřetelně zformovanými cholestatickými rozetami. Často nacházíme nekazeifikující epiteloidní granulomy (šipky) infiltrované lymfocyty a některé i s obrovskými buňkami Langhansova typu. Fig. 1. Liver biopsy – liver biopsy specimen, length 6 mm, with inflammatory infiltration, consisting almost entirely of lymphocytes, with neutrophils and interface hepatitis. Liver tissue with lobular arrangement with numerous ballooning hepatocytes and markedly formed cholestatic liver cell rosettes. There are frequently found non-caseating epithelioid granulomas (marked with arrows) infiltrated with lymphocytes and some with Langhans giant cells. 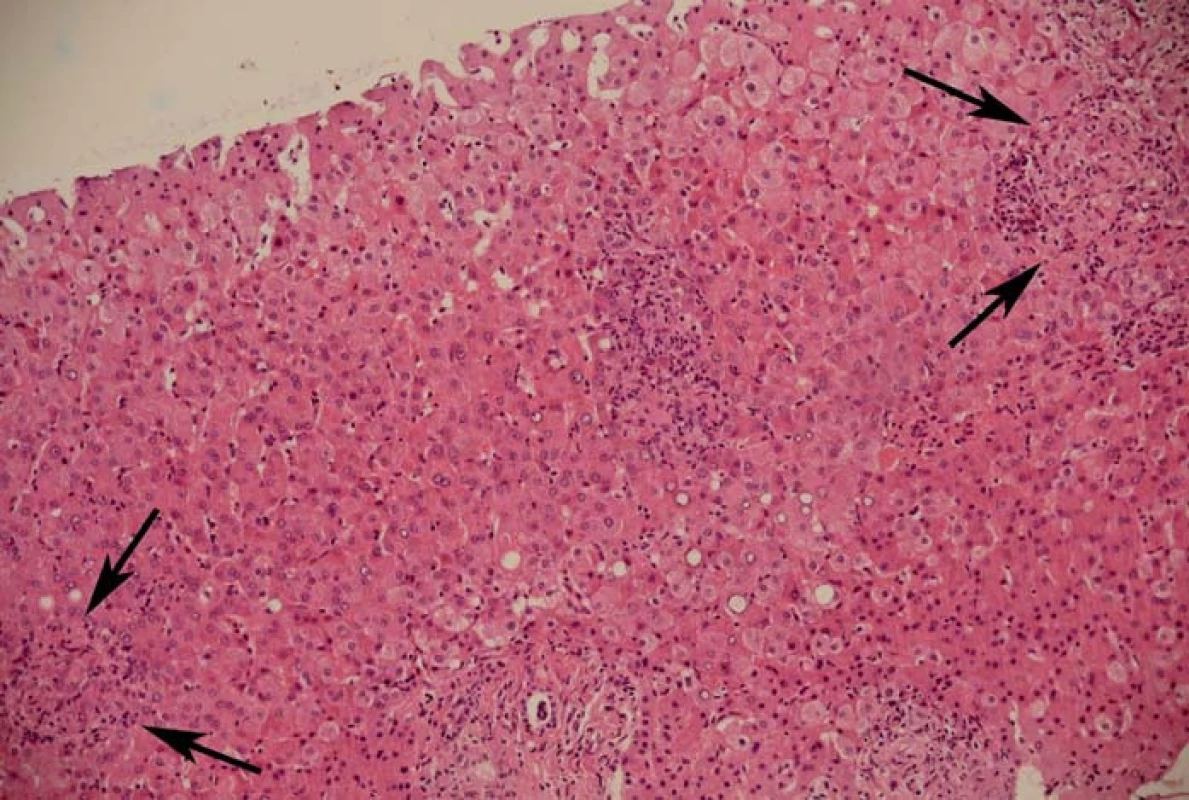
Obr. 2. Detail jednoho z četných nekazeifikujících epiteloidních granulomů infiltrovaných lymfocyty (šipky), některé i s obrovskými buňkami Langhansova typu. Fig. 2. Detail of one of numerous non-caseating epithelioid granulomas with lymphocyte infiltration (marked with arrows), some of them with Langhans giant cells. 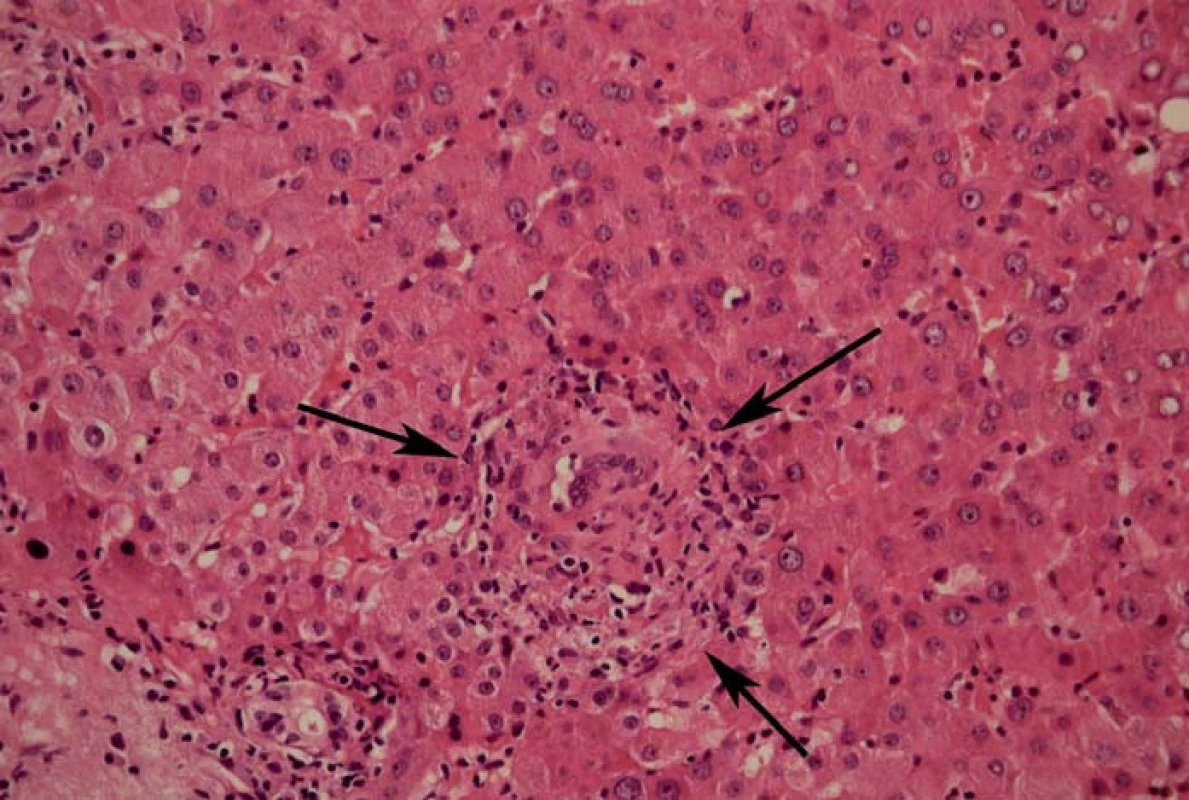
Obr. 3. HRCT plic s nálezem mikronodulárního procesu typického pro tuberkulózní postižení. Fig. 3. HRCT scan of lungs with micronodular process typical of tuberculosis. 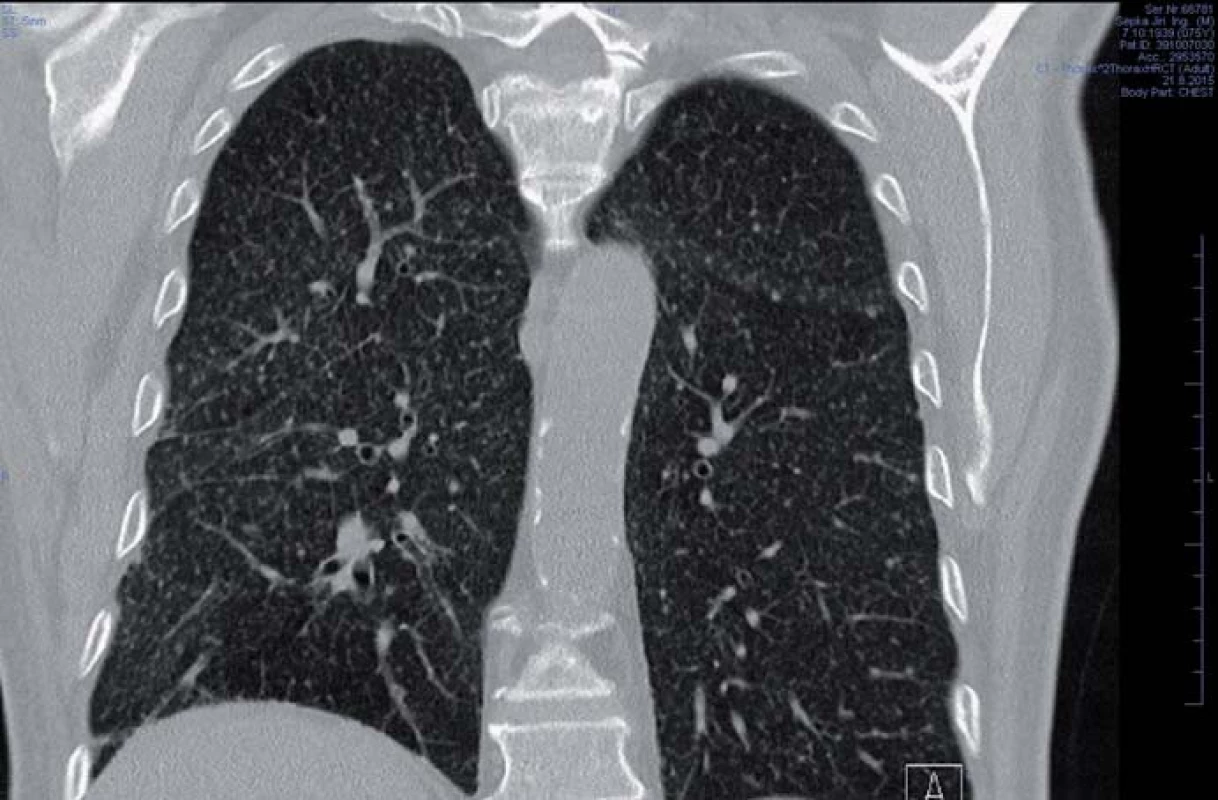
Zde byl již i na skiagramu hrudníku nález drobnoložiskového procesu s maximem v pravé plíci. Opakovaně bylo odebráno sputum na bakteriologii. Provedena bronchoskopie (atrofická sliznice, jinak normální endobronchiální nález) a bronchoalveolární laváž (BAL). Provedenými vyšetřeními (kultivace sputa na bakteriologii, BAL, cytologické vyšetření, vyšetření metodou polymerázové řetězové reakce (PCR)) nebyla zjištěna tuberkulózní infekce.
Léčba a následné sledování
Po přijetí na pneumologickou kliniku byla zahájena antituberkulózní léčba trojkombinací isoniazid + rifampicin + ethambutol, pacient byl od druhého dne podávání antituberkulotik afebrilní a febrilie se již znovu neobjevily. Stav byl uzavřen jako pneumonie s hypersenzitivní reakcí a granulomatózní hepatitidou po BCG instilacích do močového měchýře. Koncem hospitalizace se objevily průjmy, nasazen perorálně metronidazol (500 mg tbl 3× denně 14 dnů). Kultivace stolice ani stanovení klostridiového antigenu a toxinu nebylo provedeno a pacient byl propuštěn po čtyřech týdnech hospitalizace domů.
Za necelé tři týdny byl pacient opět přijat na naši kliniku pro průjmy, které se postupně horšily, a výrazný váhový úbytek (celkem 20 kg za tři měsíce). Krev ve stolici nepozoroval, teploty neměl. Na základě pozitivity antigenu a A a B toxinů Clostridium difficile byla diagnostikována postantibiotická klostridiová kolitida (CRP 42 mg/l, albumin 27,2 g/l, leukocyty 5,48 × 109/l, jaterní testy již byly v normě). Sonograficky patrné mírné zesílení stěny tlustého střeva v pravém hypogastriu, elastografické vyšetření jater již s normálními hodnotami (ARFI 1,19 m/s vs. 2,36 m/s v době jaterní biopsie).
Po standardní léčbě perorálním vankomycinem (250 mg 4× denně dva týdny) se stav postupně zlepšil a došlo k vymizení klostridiového antigenu a toxinů ve stolici. Při nutriční podpoře perorálním sippingem pacient po 14 dnech hospitalizace přibral na váze 4 kg. Po půl roce od propuštění má pacient zpátky svou původní hmotnost a je nadále sledován v nutriční ambulanci.
Dále je pacient v dispenzarizaci pneumologa, kontrolní HRCT plic po třech měsících bylo se stacionárním nálezem mikronodulárního plicního procesu.
Diskuze
Granulomatózní hepatitida asociovaná s BCG instilací do močového měchýře je vzácná komplikace. Je popisována u méně než 1 % pacientů podstupujících tuto terapii. V největším dosud publikovaném retrospektivním souboru 2 602 pacientů mělo pouze 18 z nich (0,7 %) granulomatózní hepatitidu, pneumonitidu nebo obojí [3], ačkoli frekvence rozvoje asymptomatické granulomatózní hepatitidy může být vyšší. Patogeneze tohoto stavu není zcela jasná, pravděpodobně souvisí s hypersenzitivní reakcí (IV. typu) na BCG, mykobakterie nebývají až na výjimky [4] u těchto pacientů prokazovány [5]. Ani u našeho pacienta nebyla infekce mykobakterií prokázána. Otázkou je, jak byl průkaz mykobakterií ovlivněn předchozím užíváním antibiotik (amikacin, fluorochinolony, linezolid), která vykazují rovněž určitý antituberkulotický efekt.
Laboratorní obraz elevace jaterních testů byl shodný s ostatními publikovanými případy. Zahrnoval mírnou elevaci bilirubinu, transamináz (zejména GGT) a ALP. V diagnostice granulomatózní hepatitidy má zatím nezastupitelné místo jaterní biopsie. Zajímavým faktem je patologicky vysoká hodnota při elastografickém vyšetření jater (při jinak normálním sonografickém nálezu na játrech) a její následná normalizace po odeznění potíží. Falešně vyšší elastografické hodnoty jsou známy při akutních vzplanutích virových hepatitid (zejména virové hepatitidy B nebo autoimunitní hepatitidy) a jediné měření tuhosti jaterní tkáně při akutní elevaci transamináz nad trojnásobek normy je bráno jako nespolehlivé ve vztahu k hodnocení pokročilosti jaterní fibrózy [6]. Údaj o vývoji elastografických parametrů jater u granulomatózní hepatitidy jsme v literatuře nenalezli. Je otázkou do budoucna, zda by nebylo možné se při jasné klinické situaci jaterní biopsii vyhnout.
Léčba komplikací spojených s intravezikální aplikací BCG závisí na jejich závažnosti. Mírné komplikace jako subfebrilie, dysurické potíže nebo únava obvykle rychle vymizí a nevyžadují žádná zvláštní terapeutická opatření. V případě trvající horečky, nočních potů a známek závažnějšího systémového postižení má být zahájena antituberkulózní terapie. Mycobacterium bovis je obvykle rezistentní na pyrazinamid, a tak má režim obvykle obsahovat isoniazid, rifampicin, ethambutol a event. fluorochinolon. Obvyklá doba léčby bývá šest měsíců. V případě předpokládané hypersenzitivity byl popsán příznivý efekt kortikosteroidů [7], jejich rychlé vysazení však může vést k rekurenci symptomů a opětovné tvorbě granulomů [8].
K zamyšlení je podávaná antibiotická terapie. V našem případě byl pacient původně přijat pro suspektní uroinfekci, na kterou byla nasazena dvojkombinace antibiotik (ciprofloxacin a gentamicin). Otázkou je, zda musela být antibiotická léčba opakovaně eskalována při negativních kultivačních nálezech, relativně nevysokých zánětlivých parametrech CRP 67–75 mg/l, prokalcitonin 0,65 μg/l) a uspokojivém klinickém stavu pacienta. Tato léčba mohla oddálit až znemožnit průkaz mykobakterií. Její efekt na stav pacienta je při zpětném hodnocení také spíše sporný. Efekt antituberkulotik bývá udáván v horizontu několika týdnů [9,10], v případě našeho pacienta to bylo po prvním dnu. To spolu s faktem, že se nepodařilo nijak prokázat mykobakterie, vedlo k závěru, že se nejednalo o diseminaci mykobakterií, ale o hypersenzitivní reakci. Antibiotická terapie měla v případě našeho pacienta rovněž významné nežádoucí účinky zahrnující progresi renální insuficience na počátku léčby a klostridiovou kolitidu na jejím konci.
Závěr
Granulomatózní hepatitida je vzácnou komplikací léčby povrchových tumorů močového měchýře pomocí intravezikální aplikace BCG vakcíny. Projevuje se zejména febriliemi a elevací jaterních testů charakteru smíšené jaterní léze. Patofyziologie tohoto stavu není zcela jasná, ve většině případů hraje nejvýznamnější roli hypersenzitivní reakce imunitního systému. Léčba závisí na klinickém stavu pacienta, v případě alterace celkového stavu pacienta je nutné podávání kombinace antituberkulotik. Diagnóza je histologická, role elastografického vyšetření jater by měla být zhodnocena v budoucnu.
Podpořeno grantem AZV 15-28745A.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 9. 3. 2016
Přijato: 7. 4. 2016
MU Dr. Karel Dvořák, Ph.D.
IV. interní klinika – klinika gastroenterologie a hepatologie
1. LF UK a VFN v Praze
U Nemocnice 2
128 08 Praha 2
k2dvorak@gmail.com
Zdroje
1. Lamm DL. Complications of bacillus Calmette-Guerin immunotherapy. Urol Clin North Am 1992; 19(3): 565–572.
2. Koga H, Kuroda M, Kudo S et al. Adverse drug reactions of intravesical bacillus Calmette-Guerin instillation and risk factors of the development of adverse drug reactions in superficial cancer and carcinoma in situ of the bladder. Int J Urol 2005; 12(2): 145–151.
3. Lamm DL, van der Meijden PM, Morales A et al. Incidence and treatment of complications of bacillus Calmette-Guerin intravesical therapy in superficial bladder cancer. J Urol 1992; 147(3): 596–600.
4. Rival G, Garot D, Mercier E et al. Acute respiratory failure and septic shock induced by Mycobacterium bovis. A rare side effect of intravesical BCG therapy. Presse Med 2006; 35(6 Pt 1): 980–982.
5. Liu J, Tran V, Leung AS et al. BCG vaccines: their mechanisms of attenuation and impact on safety and protective efficacy. Hum Vaccin 2009; 5(2): 70–78.
6. Chang PE, Goh GB, Ngu JH et al. Clinical applications, limitations and future role of transient elastography in the management of liver disease. World J Gastrointest Pharmacol Ther 2016; 7(1): 91–106. doi: 10.4292/wjgpt.v7.i1.91.
7. Wittes R, Klotz L, Kosecka U. Severe bacillus Calmette-Guerin cystitis responds to systemic steroids when antituberculous drugs and local steroids fail. J Urol 1999; 161(5): 1568–1569.
8. Elkabani M, Greene JN, Vincent AL et al. Disseminated Mycobacterium bovis after intravesicular bacillus Calmette-Guerin treatments for bladder cancer. Cancer Control 2000; 7(5): 476–481.
9. Delimpoura V, Samitas K, Vamvakaris I et al. Concurrent granulomatous hepatitis, pneumonitis and sepsis as a complication of intravesical BCG immunotherapy. BMJ Case Rep 2013; 2013: pii: bcr2013200624. doi: 10.1136/bcr-2013-200624.
10. Gonzalez OY, Musher DM, Brar I et al. Spectrum of bacille Calmette-Guerin (BCG) infection after intravesical BCG immunotherapy. Clin Infect Dis 2003; 36(2): 140–148.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek HepatologieČlánek Histologický test
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2016 Číslo 2- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
-
Všechny články tohoto čísla
- Hepatologie
- Histologický test
- Chronicky zvýšená aktivita pečeňových enzýmov
- Metody neinvazivního stanovení pokročilosti jaterní fibrózy
- Krvácení z varixů – pohled na terapii po Bavenu VI
- Infekcie pri cirhóze pečene – naše skúsenosti
- SOUTĚŽ O DVĚ NEJLEPŠÍ PŮVODNÍ PRÁCE 2016
- Makro-AST jako příčina izolované chronicky zvýšené aktivity AST – popis dvou případů
- Granulomatózní hepatitida jako vzácná terapeutická komplikace
- Závažné život ohrozujúce parazitárne ochorenie pečene komplikované disemináciou do pľúc
- Sartanová enteropatie – kazuistika a přehled literatury
- Úloha vápnika a vitamínu D při prevencii kolorektálneho karcinómu
- Dopis redakci časopisu Gastroenterologie a hepatologie
- 11th Congress of ECCO, Amsterdam, The Netherlands
-
XX. hradecké gastroenterologické a hepatologické dny
a X. mezinárodní endoskopický workshop - Výběr z mezinárodních časopisů
-
Správná odpověď na kvíz
Ganglioneurom tlustého střeva - Kreditovaný autodidaktický test: hepatologie
- Eziclen® – spolehlivý prostředek k očištění střeva před koloskopickým vyšetřením
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Eziclen® – spolehlivý prostředek k očištění střeva před koloskopickým vyšetřením
- Chronicky zvýšená aktivita pečeňových enzýmov
- Metody neinvazivního stanovení pokročilosti jaterní fibrózy
- Makro-AST jako příčina izolované chronicky zvýšené aktivity AST – popis dvou případů
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



