-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaVýsledky prospektívneho sledovania slizničných zmien v tenkom čreve kapsulovou enteroskopiou u pacientov s Crohnovou chorobou liečených biologickou liečbou
Results of prospective evaluation of mucosal changes in the small bowel by capsule enteroscopy in patients with Crohn’s disease treated with infliximab and adalimumab
Introduction:
Until recently, the focus of treatment of patients with Crohn’s disease (CD) was on improvement of the signs and symptoms of the disease without aiming at mucosal healing (MH). However, in recent years MH has proven to be an important therapeutical goal in patients with CD. Interest was raised recently by findings showing that biological agents not only rapidly improve the symptoms but also induce healing of ileocolonic lesions. As a consequence, current clinical trials regard MH as an important therapeutical goal and it has also been implemented in clinical practice to a greater extent. Aim:The aim of the proposed study is to evaluate mucosal lesions in the small intestine by capsule endoscopy (CE) in patients with CD before the administration of infliximab (IFX) and adalimumab (ADA) and following one-year maintenance treatment with these agents. The secondary endpoint is to evaluate the tolerance of CE by the patient, the possible side effects of this procedure and also the diagnostic efficacy of this procedure in patients with CD. Material and methods: Following approval from the Ethics Committee and after signing the Informed Consent, the group of consequently included 50 patients with CD, not previously treated with IFX (n = 25) or ADA (n = 25), but suitable for biological treatment with respect to the indication criteria, were monitored. After patients with CD were included in the study, CE using the M2A capsule was performed in each patient before the first dose of biological treatment was administered. Results were seen as conclusive if the following signs of CD localized in the small intestine were observed: erythema, edema, villus abrasion, aphtous lesions, ulcerations, scars, openings of fistula, possible strictures, bleeding. Results were seen as inconclusive if the findings were not typical for active CD: isolated aphtous lesions and ulcerations (fewer than 3) and normal. Examination was regarded as complete if the capsule reached cecum. Tolerance of CE from the patient’s side and side effects were also evaluated. The efficacy of the examination was assessed in each patient (conclusive findings, inconclusive findings or normal findings) before and after treatment with IFX and ADA. Results: From the group of prospectively enrolled patients with CD (n = 50) we had to exclude 4 patients due to IFX infusion reactions and 4 patients due to reactivation of CD (2 treated with IFX and 2 with ADA). 42 patients (19 treated with IFX and 23 with ADA) concluded the prospective evaluation by means of 1-year treatment with biological agents and repeated CE examination. In the group of ADA treated patients (n = 23) after one year we observed a change from conclusive to normal in 2 patients. We observed in 1 patient a deterioration of the findings from inconclusive to conclusive and in 1 patient from inconclusive to normal. In all the other patients the findings remained without change (in 9 conclusive, in 9 normal and in 1 inconclusive). In the group of IFX treated patients (n = 19) after one year we observed changes from conclusive to normal in 2 patients. In all the other patients the findings remained without change (in 6 conclusive, in 8 normal and in 3 inconclusive). The CE examination was well tolerated, without serious side effects, in all patients. In 7 patients the capsule did not reach cecum. Conclusion: Despite the fact that we did not observe statistically significant effect of ADA or IFX treatment on small bowel MH, we observed in our group of CD patients improvement by means of a drop in the Crohn’s Disease Activity Index (CDAI) during 1-year maintenance biological treatment. CE could therefore in the future be helpful in selecting the right patient with mucosal lesions in terms of achieving the best clinical results for the biological treatment. The validity of this approach is necessarily to be determined in prospective studies with CD patients, where MH has to be established as the main treatment goal. Further studies are also needed to create a standardized endoscopic scoring system for MH, which has to be proven in prospective clinical studies evaluating long-term development of CD. Until then it is not clear what our approach to MH in clinical practice should be.Key words:
Crohn’s disease – mucosal healing – capsule endoscopy – infliximab – adalimumab
Autoři: L. Kužela; M. Oltman; J. Šutka; B. Zacharová; P. Paulen; B. Repákova; V. Syč-Milý; M. Rajská
Působiště autorů: Gastroentero-Hepatologické centrum THALION
Vyšlo v časopise: Gastroent Hepatol 2010; 64(2): 22-30
Kategorie: IBD
Souhrn
Úvod:
Donedávna bola liečba pacientov s Crohnovou chorobou (CD) zameraná na zlepšenie príznakov a symptómov ochorenia, bez zamerania sa na slizničné hojenie (SH). SH sa však ukázalo v priebehu posledných rokov ako dôležitý liečebný cieľ u pacientov s CD. Záujem vzrástol aj vďaka nedávnym výsledkom ukazujúcim, že biologická liečba dokáže nielen rýchlo zlepšiť symptómy, ale aj indukovať hojenie ileokolonických lézií. Pre uvedené je SH v súčasnosti považované v klinických štúdiách za dôležitý cieľ liečby a je aj vo zvýšenej miere používané v klinickej praxi. Ciele práce: Cieľom štúdie bolo vyšetriť slizničné lézie na tenkom čreve kapsulovou enteroskopiou (KE) u pacientov s CD pred podaním infliximabu (IFX) alebo adalimumabu (ADA) a následne po jednoročnej udržiavacej biologickej liečbe. Druhým cieľom bolo zistiť toleranciu KE u pacientov, jej možné nežiadúce účinky a taktiež zistiť diagnostickú výťažnosť tohto vyšetrenia u pacientov s CD. Materiály a metódy: Po schválení etickou komisiou a podpísaní informovaného súhlasu sme prospektívne do štúdie zaradili a sledovali 50 pacientov s CD, ktorí neboli v minulosti liečení ako IFX (n = 25), tak ADA (n = 25), ale spľňali indikačné kritériá na biologickú liečbu. Po tom ako pacienti s CD boli zaradení do štúdie, realizovali sme u každého vyšetrenie KE (M2A kapsulou) pred podaním prvej dávky biologickej liečby a po ročnej liečbe. Nález sme hodnotili ako diagnostický v prípade, že sme našli zmeny svedčiace pre CD lokalizovanú v tenkom čreve: erytém, edém, strata črevných klkov, aftoidné lézie, ulcerácie, jazvy, ústie fistule, možná striktúra, krvácanie. Nález bol hodnotený ako podozrivý, ak zmeny neboli typické pre aktívnu CD: ojedinelé afty a ulcerácie (v počte menej ako tri) alebo normálny nález. Vyšetrenie sme považovali za úplné, ak kapsula dosiahla cékum (slepé črevo). Okrem nálezu sme sledovali aj toleranciu vyšetrenia KE zo strany pacienta a nežiadúce účinky vyšetrenia. Výsledky: Zo skupiny prospektívne zaradených pacientov (n = 50) sme museli vyradiť zo sledovania štyroch pacientov pre IFX infúzne reakcie a štyroch pacientov pre reaktiváciu CD (2 liečení IFX a 2 ADA). 42 pacientov (19 liečených IFX a 23 ADA) ukončilo prospektívne sledovanie spočívajúce v jednoročnom podávaní biologickej liečby a opakovanom vyšetrení KE. V skupine pacientov liečených ADA (n = 23) došlo pri porovnaní výsledkov KE pred biologickou udržiavacou liečbou a po nej u dvoch pacientov k vymiznutiu diagnostického nálezu a zmene na negatívny. U jedného pacienta sme zaznamenali zhoršenie nálezu v zmysle zmeny z podozrivého na diagnostický. Jeden pacient s podozrivým nálezom mal po ročnej liečbe negatívny nález. U ostatných pacientov nález ostal bez zmeny (u 9 diagnostický, u 9 negatívny a u 1 podozrivý). V skupine pacientov liečených IFX (n = 19) došlo pri porovnaní výsledkov KE pred biologickou udržiavacou liečbou a po nej u dvoch pacientov k vymiznutiu diagnostického nálezu a k zmene na negatívny. U ostatných pacientov nález ostal bez zmeny (u 6 diagnostický, u 8 negatívny a u 3 podozrivý). Vyšetrenie KE bolo u všetkých pacientov dobre tolerované, bez nežiadúcich účinkov. U siedmych pacientov kapsula nedosiahla k cékum. Záver: Napriek skutočnosti, že sme nezaznamenali štatisticky významný účinok udržiavacej ADA alebo IFX liečby na SH v tenkom čreve, zaznamenali sme v skupine pacientov s CD zlepšenie v zmysle pokles indexu aktivity (CDAI) počas 1-ročného podávania udržiavacej biologickej liečby. KE preto môže v budúcnosti byť skôr nápomocná pri selekcii pacientov so slizničnými léziami, v zmysle dosiahnutia čo najlepších klinických výsledkov biologickej liečby. Validitu tohto prístupu je potrebné určiť v prospektívnych štúdiách s CD pacientmi, kde SH by malo byť stanovené ako kľúčový cieľ. Ďalšie štúdie sú potrebné aj na vytvorenie štandardizovaného endoskopického skórovacieho systému pre SH, ktorý by sa overil v prospektívnych klinických štúdiách sledujúcich dlhodobý vývoj CD. Dovtedy nie je úplne jasné, ako by malo byť SH používané v klinickej praxi.Kľúčové slová:
Crohnova choroba – slizničné hojenie – kapsulová endoskopia – infliximab – adalimumabÚvod
Crohnova choroba (CD) je charakterizovaná transmurálnym, často granulomatóznym Th 1 zápalovým procesom, ktorý môže postihnúť ktorúkoľvek časť gastrointestinálneho traktu (GIT-u), často však postihuje tenké črevo (TČ), hrubé črevo alebo oboje. CD je ochorenie, ktoré sa môže prezentovať rozlične u rôznych pacientov, a veľa “naoko” podobných pacientov môže mať nielen kompletne odlišný priebeh ochorenia, ale aj odpoveď na liečbu [1]. Vzhľadom na svoj priebeh je CD charakterizovaná prítomnosťou rozsiahlych oblastí ulcerácií v GIT-e. Tieto ulcerácie môžu byť pôvodcom fistúl, translokácií mikróbov a môžu viesť k toxickému megakolon, perforácii a krvácaniu [2]. Tieto komplikácie sú hlavnou indikáciou pre resekciu postihnutej časti čreva. Chirurgické riešenie však nezastaví progresiu ochorenia. Pre uvedené sa v poslednej dobe presadzuje, aby efektívna liečba CD bola komplexná a mala za cieľ ako kompletné vyhojenie ulcerácii v čreve, tak klinickú remisiu [3].
Na základe výsledkov štúdií z minulosti sa ukazovalo, že TČ môže byť postihnuté zápalovými zmenami v 30 % [4]. Výsledky týchto štúdií boli založené najmä na rádiologických vyšetreniach, keďže TČ bolo po mnohé roky považované za orgán “nedosiahnuteľný” dostupnými vyšetrovacími modalitami a tradičnými endoskopickými technikami bolo ťažko možné vyšetriť celé črevo. V roku 2000 Idan et al ako prví opísali kapsulovú enteroskopiu (KE) a jej prvé klinické použitie u pacientov s krvácaním do TČ [5]. Následne sa ukázalo, že KE dokáže odhaliť aj rôzne lézie v TČ charakteristické pre postihnutie CD, ako napríklad erytém, aftózne lézie alebo ulcerácie, poprípade fistuly. KE môže byť nápomocná aj u pacientov s diagnostikovanou CD s cieľom vyšetriť skryté krvácanie do GIT-u, dokáže určiť rozsah ochorenia alebo odpoveď na protizápalovú liečbu [6]. Voderholzer et al ukázali pomocou KE, že k postihnutiu TČ dochádza o mnoho častejšie ako bolo pôvodne uvažované. Našli postihnutie TČ až u 60 % pacientov s diagnostikovanou CD [7].
Počas dekád bolo cieľom tradičnej liečby dosiahnuť indukciu, udržať remisiu, ako aj kontrolovať symptómy navodené ochorením. Postupom času na základe výsledkov početných štúdií sa ciele manažmentu postupne vyvíjali, a preto v súčasnosti by mal klinik pri vyberaní špecifickej terapie pacientovi s CD vziať do úvahy viac činiteľov zahŕňajúc pacientov vek, komorbiditu, predchádzajúcu liečbu, závažnosť ochorenia, lokalizáciu, spojitosť s extraintetinálnymi manifestáciami a komplikácie spojené s ochorením. Toto všetko sa stalo možným až po zavedení biologickej liečby [8]. Niektorí autori preto udávajú, že nastal čas zmeniť ciele liečby CD nasledovne: indukovať a udržať remisiu bez užívania kortikosteroidov; kompletne vyhojiť sliznicu tenkého a hrubého čreva; zabrániť komplikáciám ochorenia a chirurgickým zákrokom; zabrániť vzniku karcinómu a zabrániť mortalite [3].
Výsledky štúdií z posledných rokov ukazujú, že slizničné hojenie (SH) by mohol byť najlepší ukazovateľ klinickej odpovede a zároveň aj prevenciou komplikácií CD. I keď nie vždy nutne liečime pacienta, ktorý sa má dobre na biologickej liečbe s cieľom dosiahnuť aj SH, štúdie (ako aj naša) môžu napomôcť v objasnení potreby endoskopického vyšetrenia u pacientov, ktorí sú symptomatickí na biologickej liečbe s cieľom optimalizovať dávkovanie alebo zmeniť terapiu za iný biologický agens [9–10].
Pre uvedené sme na našom pracovisku realizovali štúdiu za účelom prospektívnym spôsobom hodnotiť slizničné zmeny na TČ pred podaním infliximabu (IFX) alebo adalimumabu (ADA) a následne po absolvovaní ročnej biologickej liečby, pomocou KE. Prvotným cieľom štúdie bolo zistiť účinnosť ročného podávania IFX alebo ADA v ovplyvnení, respektíve vyhojení lézii na TČ. Druhým cieľom bolo zistiť toleranciu KE u pacientov s CD, jej možné nežiadúce účinky a taktiež diagnostickú výťažnosť tohto vyšetrenia. Predkladaná klinická štúdia je pre vyššie uvedené jedna z mála [10–11], ktorá si dala za cieľ odpovedať na otázku, aká je skutočná účinnosť IFX alebo ADA so zameraním na hojenie lézií v TČ, ktoré sa v súčasnosti ukazujú ako rozhodujúce v prognóze pacientov s CD.
Metódy
Pacienti
Po súhlase vydanom etickou komisiou a po podpísaní písomného informovaného súhlasu sme sledovali skupinu „po sebe“ prospektívne zaradených pacientov CD, neliečených IFX alebo ADA, ktorí boli indikovaní na bio-logickú liečbu na základe v súčasnosti odporúčaných indikácií:
- muž alebo žena vo veku 18 až 65 rokov
- ťažká, aktívna CD (index aktivity – Crohn´s Disease Activity Index (CDAI) viac ako 220, C reaktívny proteín viac ako 15 mg/ml).
Exklúzne kritériá boli: fistulujúca forma CD, pacienti s tuberkulózou alebo inými ťažkými infekciami, ako sú sepsa, abscesy a oportúnne infekcie ako herpes zoster, cytomegalovírusová infekcia, pozitivita vyšetrenia anti-HIV, anamnéza malígneho ochorenia v dobe 5 rokov pred zahájením podania biologickej liečby, pacienti so stredne ťažkým alebo ťažkým zlyhaním srdca (NYHA trieda III/IV), pacienti s anamnézou precitlivelosti na IFX a iné myšie bielkoviny alebo na niektorú z pomocných látok, pacienti s anamnézou precitlivelosti na ADA, gravidita, dojčenie, dysfágia, užívanie nesteroidových antiflogistík (ktoré samé o sebe môžu navodiť slizničné lézie na TČ, podobné ako pri CD) a prítomnosť pacemakera.
Ženy v plodnom veku museli počas užívania IFX alebo ADA používať primeranú antikoncepciu (abstinencia, perorálna antikoncepcia, IUT, sterilizácia), aby zabránili počatiu a v jej užívaní museli pokračovať najmenej 6 mesiacov po poslednom podaní IFX alebo ADA.
U každého zaradeného pacienta sme zaznamenali pohlavie, vek, CDAI pred ročnou biologickou liečbou a po nej, fajčenie, užívanie kortikosteroidov, chirurgické zákroky pred biologickou liečbou a počas nej, nežiadúce účinky biologickej liečby, prítomnosť extraintestinálnych manifestácií pred liečbou a po nej, nález z vyšetrenia KE pred ročnou biologickou liečbou a po nej, nežiadúce účinky vyšetrenia KE.
Design štúdie
Po zaradení pacienta do štúdie (v rámci inklúznych kritérií) sme pred prvým podaním biologickej liečby (intravenózne podaný IFX alebo subkutánne aplikovaný ADA) každému pacientovi s CD realizovali KE vyšetrením PillCam SBTM kapsulou. Záznam po každom vyšetrení bol vyhodnotený a elektronicky uchovaný. Následne sme začali s podávaním IFX formou intravenóznej infúzie po dobu 2 hod, v dávke 5 mg/kg, v schéme 0., 2. a 6. týždeň s následným podávaním každých 8 týždňov celkovo po dobu 12 mesiacov. Podávanie IFX sa uskutočnilo na základe platného odporučenia dávkovania a spôsobu podávania. Podávanie ADA sme realizovali taktiež podľa podávania z SPC. Úvodný dávkovací režim ADA u pacientov s ťažkou CD bol 80 mg v týždni 0, nasledovaný 40 mg v týždni 2. V prípade, že bola potrebná rýchlejšia odpoveď na liečbu (závažná aktivita ochorenia hodnotená podľa indexu aktivity CDAI), použili sme na začiatku liečby režim 160 mg v týždni 0 a 80 mg v týždni 2. Následné pokračovacie dávky po úvodnej liečbe boli u každého pacienta 40 mg každý druhý týždeň podané subkutánnou injekciou celkovo po dobu 12 mesiacov. Počas liečby IFX a ADA pacienti naďalej užívali ostatnú medikáciu na CD (imunosupresíva...). V priebehu liečby boli pacienti s CD sledovaní na základe odporúčaných postupov, ďalej sme pri každej návšteve pacienta zvážili a v prípade potreby zároveň aj zaznamenali zmenu v podávaní kortikosteroidov so zameraním na ich úplné vysadenie. Nález z vyšetrenia KE sme hodnotili ako diagnostický (obr. 1) – v prípade, že nález svedčal pre CD lokalizovanú v tenkom čreve: erytém, edém, strata črevných klkov, aftoidné lézie, ulcerácie, jazvy, ústie fistule, možná striktúra, krvácanie. Podozrivý (obr. 2) – v prípade, že nález nebol úplne typický pre aktívnu CD: ojedinelé afty a ulcerácie (v počte menej ako tri) alebo normálny nález (obr. 3). Vyšetrenie sme považovali za úplné, ak kapsula dosiahla cékum (slepé črevo). Okrem nálezu sme sledovali aj toleranciu vyšetrenia KE zo strany pacienta a možné nežiadúce účinky vyšetrenia.
Obr. 1. Diagnostický nález z vyšetrenia kapsulovou enteroskopiou. Fig. 1. Conclusive finding using capsule enteroscopy. 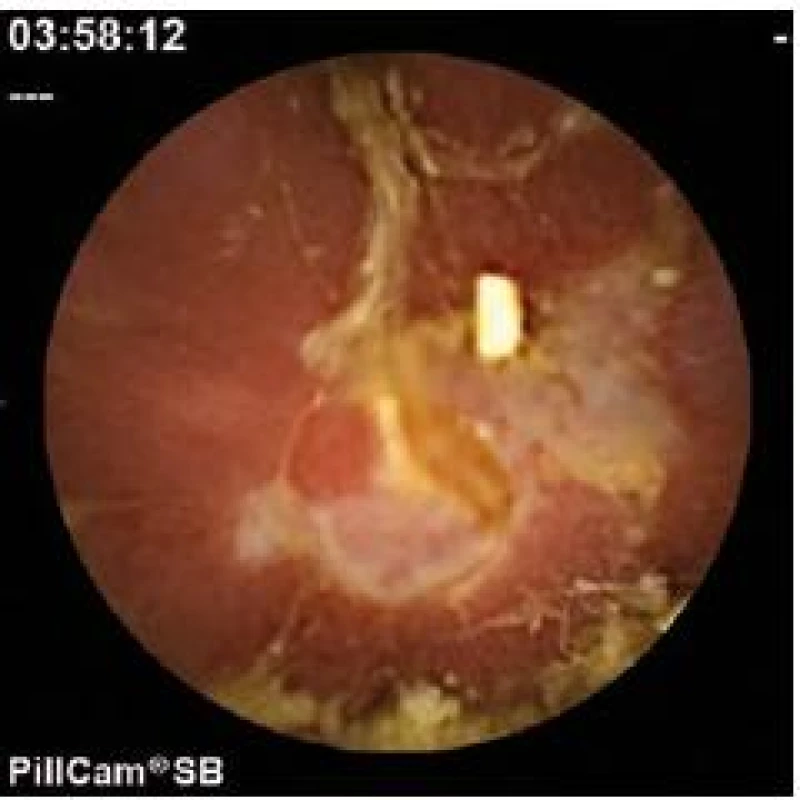
Obr. 2. Podozrivý nález z vyšetrenia kapsulovou enteroskopiou. Fig. 2. Inconclusive finding using capsule enteroscopy. 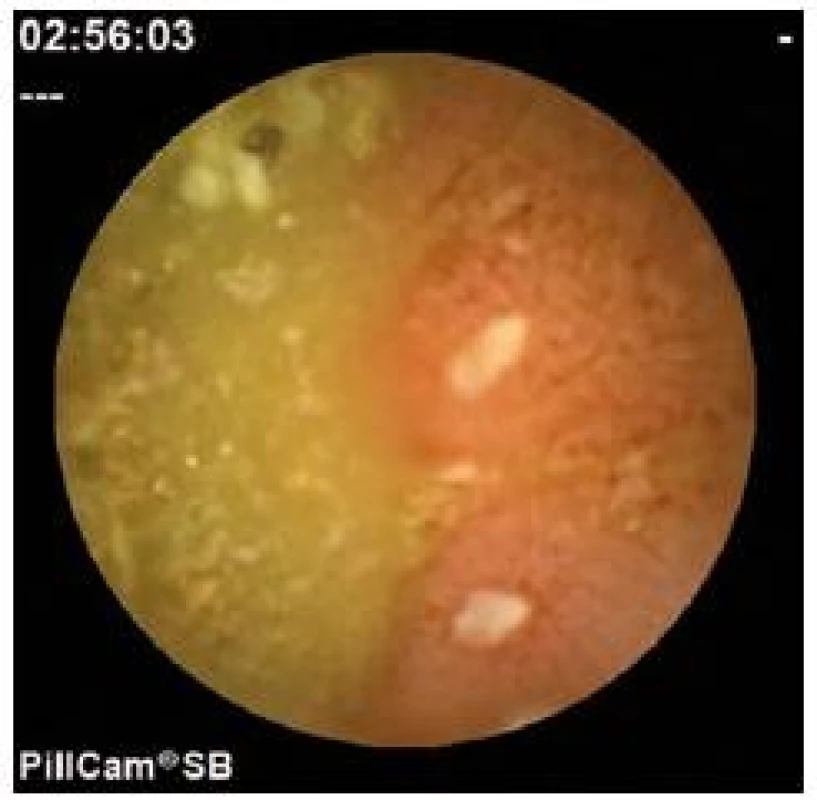
Obr. 3. Normálny nález z vyšetrenia kapsulovou enteroskopiou. Fig. 3. Normal finding using capsule enteroscopy. 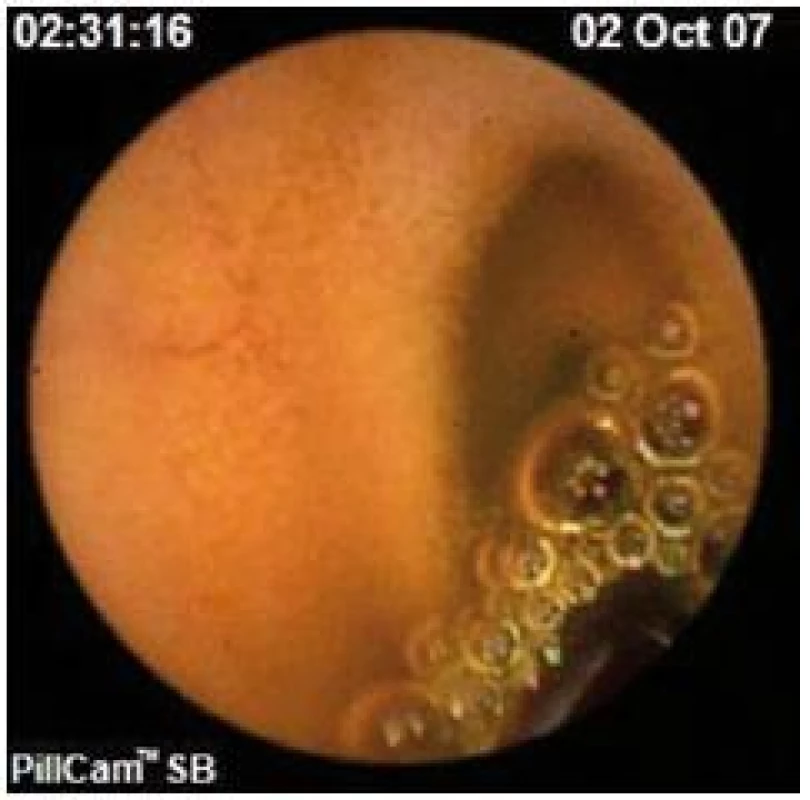
Štatistická analýza
- Na porovnanie nálezov KE pred bio-logickou terapiou a jeden rok po liečbe sme použili neparametrický párový Wilcoxonov test.
- Pri porovnaní skupín v sledovaných kvalitatívnych znakoch sme použili chí kvadrát test v kontingenčných tabuľkách a pre porovnanie veku 2-výberový 2-stranný Studentov t-test.
- Na porovnanie počtu extraintestinálnych manifestácií CD sme použili McNemarov test.
Všetky testy sme robili na hladine významnosti α = 0,05. Použili sme štatistický softvér SPSS 16.0.
Výsledky
Pacienti
Do štúdie sme prospektívne zaradili 50 pacientov s CD. 25 pacientov bolo liečených IFX (tab. 1) a 25 pacientov liečených ADA (tab. 2).
Tab. 1a. Charakteristika pacientov na terapii infliximabom. Tab. 1a. Characteristics of patients treated with infliximab. 
Tab. 1b. Charakteristika pacientov na terapii infliximabom. Tab. 1b. Characteristics of patients treated with infliximab. 
Tab. 2a. Charakteristika pacientov na terapii adalimumabom. Tab. 2a. Characteristics of patients treated with adalimumab. 
Tab. 2b. Charakteristika pacientov na terapii adalimumabom. Tab. 2b. Characteristics of patients treated with adalimumab. 
Celkovo sme plánovali do projektu zaradiť 60 pacientov. Vyššie uvedený počet (n = 50) sme zvolili vzhľadom na to, že nie všetci pacienti, ktorých sme plánovali do projektu zaradiť, spľňali inklúzne kritériá, a to i napriek tomu, že Gastroentero-Hepatologické centrum THALION je jedno zo siedmych aplikačných a indikačných centier biologickej liečby na Slovensku a má dostatok pacientov s CD. Vyššie uvedené inklúzne kritériá nám preto nedovolili zaradiť všetkých pacientov sledovaných v našom centre. Pre nežiadúce účinky podávania IFX sme museli vyradiť zo sledovania štyroch pacientov (išlo o alergické reakcie, ktoré ustúpili po podaní kortikoidov). Nežiadúce účinky liečby ADA vedúce k ukončeniu liečby sme v nami sledovanom súbore pacientov nezaznamenali. Pre relaps ochorenia sme zo sledovania vyradili dvoch pacientov na terapii IFX a dvoch pacientov na terapii ADA (celkovo n = 4).
To značí, že ročné podávanie biologickej liečby a dve vyšetrenia kapsulovou endoskopiou (pred biologickou liečbou a po nej) celkovo ukončilo 42 pacientov (z celkového počtu zaradených 50 pacientov). Pri porovnaní skupín sa neukázal štatisticky významný rozdiel ani v jednom sledovanom znaku. Skupiny sa nelíšili štatisticky významne vo veku ani v pomere žien a mužov. Na porovnanie skupín v sledovaných kvalitatívnych znakoch sme použili chí kvadrát test v kontingenčných tabuľkách a pre porovnanie veku 2-výberový 2-stranný Studentov t-test. V skupinách liečenej ADA aj IFX sme zaznamenali štatisticky významne viac operácií pred terapiou ako počas terapie. Nežiaduce účinky sa vyskytli iba u štyroch pacientov v skupine liečenej IFX, ale ani v tomto znaku sa skupiny nelíšili štatisticky významne. Po ročnej liečbe liekom ADA aj IFX došlo k štatisticky významnému zníženiu počtu pacientov s extraintestinálnymi manifestáciami (p = 0,031, p = 0,016).
Vyšetrenie KE
U všetkých zaradených pacientov (n = 50) prebehlo vstupné vyšetrenie KE bez komplikácií, nežiadúce účinky sme nepozorovali u žiadneho pacienta. U pacientov, ktorý ukončili sledovanie (n = 42) a realizovali sme u nich aj druhé vyšetrenie KE po ročnej biologickej liečbe, sme nezaznamenali nežiadúce účinky vyšetrenia. Pacienti neudávali dyskomfort ani počas vyšetrení KE, ani po ňom. U siedmych pacientov nebolo vyšetrenie hodnotené ako úplné – to značí, že kapsula u nich nedosiahla cékum, a tým pádom nebolo vyšetrené celé TČ.
V nami sledovanom súbore pacientov liečených ročným podávaním ADA (n = 23) sme zaznamenali nasledovné zmeny pri porovnaní vyšetrenia KE pred liečbou a po něj. V skupine pacientov s diagnostickým nálezom sme zmenu na TČ po liečbe nezaznamenali u deviatich pacientov, u dvoch sa nález zmenil na negatívny. V skupine pacientov s podozrivým nálezom sa u jedného pacienta nález zmenil na diagnostický, u jedného ostal podozrivý a u jedného sa zmenil na negatívny. V skupine pacientov s negatívnym nálezom sme u všetkých deviatich sledovaných nezaznamenali zmenu, to značí nález ostal negatívny.
V nami sledovanom súbore pacientov liečených jeden rok IFX (n = 19) sme pozorovali nasledovné zmeny pri porovnaní vyšetrenia KE pred liečbou a po něj. V skupine pacientov s diagnostickým nálezom sme zmenu na TČ po liečbe nezaznamenali u šiestich pacientov, u dvoch sa nález zmenil na negatívny. V skupine pacientov s podozrivým nálezom sme zmenu nezaznamenali ani u jedného z troch pacientov. Takisto v skupine pacientov s negatívnym nálezom sme u všetkých ôsmich sledovaných nezaznamenali zmenu, to značí nález ostal v tejto skupine negatívny.
Nález podľa CE pred terapiou a jeden rok po terapii sa nelíšil štatisticky významne ani v jednej skupine. V skupine liečenej ADA došlo celkovo u troch pacientov k zlepšeniu a u jedného pacienta k zhoršeniu stavu a v skupine liečenej IFX došlo u dvoch pacientov k zlepšeniu stavu.
Diskusia
CD je chronické zápalové ochorenie GITu, ktoré pravdepodobne vzniká následkom stimulácie dysfunkčnej imunitnej odpovede u geneticky predisponovaných jednotlivcov [2]. CD nie je spojená s perforujúcimi komplikáciami alebo fibrostenózou hneď od začiatku ochorenia. U väčšiny pacientov ochorenie začína iba s prítomnosťou čisto zápalových lézií. Pokračujúcou zápalovou aktivitou alebo relapsmi stúpa aj počet komplikácií a môže dôjsť k vzniku striktúr alebo fistúl [1]. Pre uvedené viacerí autori navrhujú „agresívnejší” prístup k CD v rámci manažmentu už od samého začiatku ochorenia, s cieľom zlepšiť jeho prognózu [3]. Biologická liečba v terapii pacien-tov s CD doslova znamenala revolúciu v prístupe k pacientom, v manažmente ochorenia dosiahla udržanie remisie a je bez potreby podávania kortikosteroidov, dokázala významne zabrániť komplikáciám ochorenia, hospitalizáciám, potrebe chirurgického riešenia a mortalite, ako aj dosiahla významné zlepšenie kvality života pacientov [8]. V ére biologickej terapie možno po prvý krát v rámci plánovaných cieľov liečby hovoriť už aj o modifikácií prirodzeného priebehu ochorenia. Hlboké a dlhotrvajúce hojenie zápalových lézií sú pravdepodobným predpokladom dosiahnutia takéhoto cieľa [3]. Dáta týkajúce sa vzťahu medzi závažnosťou slizničných lézií a vývinom CD sú v súčasnosti nedostačujúce. CD je chronicky intermitentne aktívne ochorenie, a i keď SH v súčasnosti na základe doterajších dát vyzerá ako dôležitý znak účinnosti liečby v akútnom štádiu, úloha SH v progresii ochorenia ešte nebola dostatočne vedecky zdokumentovaná. Dopad hojaceho efektu liečby na výsledok samotnej CD bol doteraz preskúmaný najmä u IFX. Systematická osemtýždňová liečba IFX dokázala indukovať kompletné SH u skoro polovice liečených pacientov. Pacienti, u ktorých došlo ku krátko a dlhodobému SH mali väčšiu redukciu v počte hospitalizácií, chirurgických zákrokov a dní strávených na jednotke intenzívnej starostlivosti v porovnaní s pacientmi, u ktorých došlo iba k parciálnemu hojeniu, alebo k hojeniu vôbec nedošlo. [12]. Pre uvedené sa predpokladá, že SH môže byť najlepší ukazovateľ pre určenie klinickej odpovede a zároveň aj v prevencii komplikácií CD [10]. Používanie SH ako prediktívneho činiteľa pre priebeh ochorenia, potrebu podávania kortikosteroidov a potrebu chirurgického riešenia posilňujú aj výsledky štúdie Froslieho et al. Nedostatočné SH na druhej strane však môže predstavovať indikáciu na intenzifikované režimové stratégie s cieľom zabrániť závažný priebeh a komplikácie ochorenia [13]. Lichtenstein et al taktiež ukázali, že pacienti so SH mali menšiu potrebu hospitalizácie a chirurgických zákrokov po liečbe IFX. Táto štúdia predpokladala úlohu SH v monitorovaní účinnosti liečby u pacientov počas sledovania [14]. Schnitzler et al ukázali vo svojej štúdii, že SH indukované dlhodobou udržiavacou liečbou IFX je spojené so zlepšenou prognózou ochorenia, hlavne v podobe menšej potreby väčších brušných chirurgických zákrokov [10]. Rutgeerts et al ukázali početnú (nie štatisticky významnú) redukciu hospitalizácií pre CD u pacientov so SH [15].
Výsledky našej štúdie ukázali, že pri porovnaní skupín liečených IFX a ADA sa neprejevil štatisticky významný rozdiel ani v jednom sledovanom znaku. Skupiny sa nelíšili štatisticky významne vo veku ani v pomere žien a mužov. Naše výsledky ukázali, že napriek klinickému úspechu liečby (subjektívne zlepšenie pacientov liečených biologickou terapiou), poklesu indexu aktivity (u všetkých 42 pacientov, ktorí ukončili sledovanie, bol CDAI nižší ako 150), nedošlo k signifikantnému zlepšeniu endoskopického nálezu na TČ pri vyšetrení KE. Nález podľa CE pred terapiou a jeden rok po terapii sa nelíšil štatisticky významne ani v jednej skupine. V skupine liečenej ADA došlo u troch pacientov k zlepšeniu a u jedného pacienta k zhoršeniu stavu a v skupine liečenej IFX došlo u dvoch pacientov k zlepšeniu stavu. Nežiaduce účinky sa vyskytli iba u štyroch pacientov v skupine liečenej IFX, ale ani v tomto znaku sa skupiny nelíšili štatisticky významne. Po ročnej liečbe liekom ADA aj IFX došlo k štatisticky významnému zníženiu počtu pacientov s extraintestinálnymi manifestáciami.
V rámci diskusie je potrebné vyzdvihnúť skutočnosť, že do štúdie boli zaradení pacienti aj s negatívnym nálezom pri KE na TČ, nakoľko biologická liečba je na Slovensku indikovaná, nie na základe endoskopického nálezu na TČ, ale na základe aktivity ochorenia. Indikácia biologickej liečby je teda tažká, aktívna CD (CDAI viac ako 220 alebo CRP viac ako 15 mg/ml). Znamená to, že na Slovensku liečbu dostanú pacienti s ohľadom na aktivitu ochorenia a nie pre endoskopický nález na TČ. Vzhľadom na design našej štúdie sme preto zaradili po splnení indikačných kritérií všetkých pacientov, u ktorých bola príslušnou zdravotnou poisťovňou schválená biologická liečba a na zaradenie do štúdie nemal vplyv nález pri vyšetrení KE pred podaním liečby, keďže cieľom bolo hodnotiť zmeny na sliznici TČ pred podaním biologickej liečby a po nej. U všetkých pacientov, ktorí mali negatívny nález pri vyšetrení KE, sme realizovali kolonoskopické vyšetrenie. To potvrdilo nález Crohn-kolitídy, čiže z tohoto pohľadu nemožno vyšetrenie KE hodnotiť ako málo senzitívne pre diagnózu CD. Taktiež treba podoktnúť, že pri selektovaní pacienta na vyšetrenie KE je vhodné myslieť aj na nerozpoznané stenózy na TČ a z tohoto pohľadu vylúčiť prípadné uviaznutie kapsule ešte pred indikovaním vyšetrenia KE.
Výsledky našej štúdie ukázali, že biologická liečba sa napriek svojej vysokej cene ukazuje ako efektívna v zmysle vynaložených finančných prostriedkov, samozrejme za predpokladu, že je indikovaná iba u tých pacientov, ktorý z nej budú čo najviac a dlhodobo profitovať. Optimálna indikácia biologickej liečby umožní minimalizovať nadbytočné alebo aj predčasné podanie týchto liekov, a tým pádom aj docieli zníženie možných nepriaznivých medicínskych, ako aj ekonomických dopadov liečby. Ďalším prirodzeným záverom štúdie je podpora skutočnosti, že regionálne odporúčania týkajúce sa biologickej liečby pacientov s CD by mali byť realizované príslušnými odborníkmi, ktorý sa pri ich vypracovaní budú opierať nielen o analýzy a výsledky veľkých medzinárodných štúdií, ale aj o vlastné klinické skúsenosti a mali by v rámci takýchto odporúčaní zahrnúť i ekonomické možnosti lokálneho zdravotníctva.
Endoskopické určenie aktivity CD je medzinárodne používané a akceptované ako dôležitá objektívna modalita v manažmente CD počas posledných dekád. Naše výsledky môžu taktiež prispieť k znalosti významu SH u CD tým, že sme sledovali vzťah SH v prospektívnej štúdií na základe vopred určených diagnostických kritérií.
Záver
Záverom možno konštatovať, že napriek dostupným dátam stále existuje aj v súčasnosti potreba realizácie štúdií, ktoré ukážu, či remisia spojená s kompletným SH TČ pri terapii IFX alebo ADA má tendenciu k prevencii progresie ochorenia, či dokáže zabrániť hospitalizáciám, chirurgickým zákrokom alebo pobytom na jednotke intenzívnej starostlivosti. Tieto dáta môžu zároveň aj ukázať, či kompletné SH dokáže oddialiť relaps CD po ukončení biologickej liečby. Veľkou terapeutickou dilemou v tejto dobe ostáva naďalej pacient bez SH, ktorý je v remisii a neužíva kortikosteroidy. Možno v takomto prípade zvážiť zintenzívnenie medikamentóznej liečby so zreteľom na zvýšenú možnosť nežiadúcich účinkov, zvýšenú cenu liečby, ale bez jasných dát indikujúcich ozajstný benefit v zmysle zastavenie progresie ochorenia. Nedostatočné SH môže na druhej strane predsa len predstavovať indikáciu k intenzifikačným režimovým stratégiám s cieľom zabrániť závažnejšiemu priebehu a komplikáciám ochorenia. Do budúcna sú preto potrebné ďalšie štúdie zamerané na objasnenie vzťahu medzi SH a redukciou komplikácií CD s cieľom pomôcť jasnejšie určiť náš finálny terapeutický cieľ.
Výskumná úloha bola podporená grantovým projektom APVV-0239-06.
Zoznam skratiek uvedených v texte:
- ADA – adalimumab
- CD – Crohnova choroba
- GIT – gastrointestinálny trakt
- IFX – infliximab
- KE – kapsulová endoskopia
- SH – slizničné hojenie
- TČ – tenké črevo
Zoznam skratiek uvedených v tabuľkach:
- m – muž
- ž – žena
- PSC – primárna sklerotizujúca cholangitída
- EIM – extraintestinálne manifestácie
doc. MUDr. Ladislav Kužela, CSc.
Gastroentero-Hepatologické centrum THALION
Mýtna 5, 811 07 Bratislava, SK
kuzela@thalion.sk
Zdroje
1. Cosnes J, Cattan S, Blain A et al. Long-term evolution of disease behavior of Crohn’s disease. Inflamm Bowel Dis 2002; 8(4): 244–250.
2. Shanahan F. Host-flora interactions in inflammatory bowel disease. Inflamm Bowel Dis 2004; 10 (Suppl 1): S16–S24.
3. Rutgeerts P, Vermeire S, Van Assche G. Mucosal healing in inflammatory bowel disease: impossible ideal or therapeutic target? Gut 2007; 56(4): 453–455.
4. Steinhardt HJ, Loeschke K, Kasper H et al. European Cooperative Crohn’s Disease Study (ECCDS): clinical features and natural history. Digestion 1985; 31(2–3): 97–108.
5. Iddan G, Meron G, Glukhovsky A et al. Wireless capsule endoscopy. Nature 2000; 405(6785): 417.
6. Saruta M, Papadakis KA. Capsule endoscopy in the evaluation and management of inflammatory bowel disease: a future perspective. Expert Rev Mol Diagn 2009; 9(1): 31–36.
7. Voderholzer WA, Beinhoelzl J, Rogalla P et al. Small bowel involvement in Crohn’s disease: a prospective comparison of wireless capsule endoscopy and computed tomography enteroclysis. Gut 2005; 54(3): 369–373.
8. Lichtenstein GR, Abreu MT, Cohen R et al. American Gastroenterological Association Institute medical position statement on corticosteroids, immunomodulators, and infliximab in inflammatory bowel disease. Gastroenterology 2006; 130 : 935–939.
9. Rutgeerts P, D’Haens GR, Van Assche GA et al. Adalimumab induces and maintains mucosal healing in patients with moderate to severe ileocolonic Crohn’s disease—first results of the EXTEND Trial. Gastroenterology 2009; 136 (Suppl 1): A116.
10. Schnitzler F, Fidder H, Ferrante M et al. Mucosal healing predicts long-term outcome of maintenance therapy with infliximab in Crohn’s disease. Inflamm Bowel Dis 2009; 15(9): 1295–1301.
11. Efthymiou A, Viazis N, Mantzaris G et al. Does clinical response correlate with mucosal healing in patients with Crohn’s disease of the small bowel? A prospective, case-series study using wireless capsule endoscopy. Inflamm Bowel Dis 2008; 14(11): 1542–1547.
12. Rutgeerts P, Feagan BG, Lichtenstein GR et al. Comparison of scheduled and episodic treatment strategies of infliximab in Crohn‘s disease. Gastroenterology 2004; 126(2): 402–413.
13. Frøslie KF, Jahnsen J, Moum BA et al. Mucosal healing in inflammatory bowel disease: results from a norwegian population-based cohort. Gastroenterology 2007; 133(2): 412–422.
14. Lichtenstein GR, Yan S, Bala M et al. Infliximab maintenance treatment reduces hospitalizations, surgeries, and procedures in fistulising Crohn’s disease. Gastroenterology 2005; 128(4): 862–869.
15.Rutgeerts P, Diamond RH, Bala M et al. Scheduled maintenance treatment with infliximab is superior to episodic treatment for the healing of mucosal ulceration associated with Crohn’s disease. Gastrointest Endosc 2006; 63(3): 433–442.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2010 Číslo 2- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Cinitaprid – v Česku nová účinná látka nejen pro léčbu dysmotilitní dyspepsie
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
-
Všechny články tohoto čísla
- Diagnostika a liečba pacientov s Peutz-Jeghersovým syndrómom
- Výsledky prospektívneho sledovania slizničných zmien v tenkom čreve kapsulovou enteroskopiou u pacientov s Crohnovou chorobou liečených biologickou liečbou
- 5. ECCO kongres, Kongresové centrum v Praze, 25.–27. 2. 2010
- Hepatologický dodatek ke článku: Doporučení pro vakcinaci a profylaxi infekčních chorob u nemocných s Crohnovou chorobou a ulcerózní kolitidou léčených imunosupresivy a biologickou léčbou (Česká a slovenská gastroenterologie a hepatologie 2010; 64(1): 40–
- Redukce příjmu kuchyňské soli ve stravě – účinný a levný prostředek ke zlepšení zdraví a prodloužení věku
-
Ctirad John. Zrcadlo mých lásek aneb vzpomínky.
Vyvolal a sestavil František Houdek. Praha: Galén 2009. 334 stran. - Za docentem MUDr. Jaroslavem Šetkou, CSc. (20. 8. 1925–10. 11. 2009)
- Za prof. MUDr. Zdeňkem Mařatkou, DrSc.(27. 6. 1914–24. 3. 2010)
- Zřízení nové sekce IBD v našem časopise
- Ohlédnutí za IV. kongresem ČGS
- Standardy – jak dále? (Projekt Mzd ČR)
- Mycobacterium avium subsp. paratuberculosis, etiologický faktor u Crohnovy choroby?
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Diagnostika a liečba pacientov s Peutz-Jeghersovým syndrómom
- Mycobacterium avium subsp. paratuberculosis, etiologický faktor u Crohnovy choroby?
- Za docentem MUDr. Jaroslavem Šetkou, CSc. (20. 8. 1925–10. 11. 2009)
- Výsledky prospektívneho sledovania slizničných zmien v tenkom čreve kapsulovou enteroskopiou u pacientov s Crohnovou chorobou liečených biologickou liečbou
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



