-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaRekombinantní aktivovaný faktor VII (rFVIIa) v léčbě závažného poporodního krvácení
Data z registru UniSeven v České republice
Recombinant activated factor VII in the treatment of life threatening post‑partum haemorrhage; registry UniSeven in the Czech Republic
Objective:
To analyze the data related to the treatment of 80 Czech patients with life threatening post-partum haemorrhage recorded in the clinical registry UniSeven during years 2004-2009.Design:
Retrospective, observational, multicentre study.Settings:
ICU and Obstetrics departments of University and Regional hospitals in Czech Republic.Material and methods:
UniSeven is an international academic project of Masaryk University in Brno, Czech Republic, focused on recording of clinical data related to „off-label“ use of rFVIIa (Novo Seven) in life threatening bleeding. Data of 80 case reports of post partum haemorrhage from the registry was analysed from the clinical (efficacy and safety) as well as laboratory aspects.Results:
In 97.5% of our patients the treatment with rFVIIa was able to control the bleeding. In 53 women (66.3%) only one dose of rFVIIa was sufficient to control the bleeding. The rest of the patient received two or more rFVIIa doses. First dose of rFVIIa given to patients who needed more than one dose was significantly lower (96.6 μg/kg) compared to patient succesfully treated with one dose only (110.6 μg/kg; p = 0.048). The mortality rate in our cohort of patients was 2.5%. We have not recorded any thrombembolic event as and adverse event related to the rFVIIa treatment. In 74.3% of patients where rFVIIa was administered before considering the hysterectomy, it was able to avoid hysterectomy what we consider to be a significant improvement of the patients‘ quality of life.Conclusions:
Our data were also considered during the work up of national guidelines for the treatment of life threatening post-partum haemorrhage in the Czech Republic.Key words:
post-partum haemorrhage, hysterectomy, rFVIIa, clinical registry.
Autoři: D. Seidlová 1; J. Blatný 2; M. Penka 2; P. Ovesná 4; P. Brabec 4; P. Ševčík 1; P. Ventruba 5; V. Černý 3
Působiště autorů: Klinika anesteziologie, resuscitace a intenzivní medicíny a Anesteziologicko-resuscitační oddělení FN, LF MU Brno 1; Oddělení klinické hematologie FN, LF MU, Brno 2; Klinika anesteziologie, resuscitace a intenzivní medicíny FN, Hradec Králové 3; Institut biostatistiky a analýz Lékařské a Přírodovědecké fakulty MU, Brno 4; Gynekologicko-porodnická klinika FN, LF MU, Brno 5
Vyšlo v časopise: Ceska Gynekol 2010; 75(4): 297-305
Souhrn
Cíl studie:
Hodnocení efektu léčby poporodního krvácení s pomocí rFVIIa u 80 pacientek zaznamenaných v klinickém registru UniSeven letech 2004-2009.Typ studie:
Retrospektivní, observační, multicentrická.Typ pracoviště:
JIP, ARO a gynekologická pracoviště nemocnic II. a III. typu v ČR.Materiál a metody:
Registr UniSeven je mezinárodní akademický projekt Masarykovy univerzity v Brně, zaměřený na záznam klinických a laboratorních údajů souvisejících s podáním rFVIIa (Novo Seven) v „nehemofilických“ indikacích. Data spojená s léčbou peripartálního krvácení u 80 žen byla analyzována z pohledu klinického (efektivita a bezpečnost) a laboratorního.Výsledky:
U 97,5 % žen s život ohrožujícím krvácením v našem souboru bylo dosaženo s pomocí podání rFVIIa kontroly krvácení. Byla nalezena statistická závislost mezi nutností opakování podání rFVIIa a velikostí první dávky. U 53 žen (66,3 %) stačila k zástavě krvácení pouze jediná dávka rFVIIa. U ostatních pacientek bylo třeba podat 2 a více dávek léku. První dávka rFVIIa byla u pacientek, které vyžadovaly druhé a další podání, signifikantně nižší (96,6 μg/kg) oproti případům, kde stačilo jen jedno podání léku (110,6 μg/kg; p = 0,048). Mortalita spojená s život ohrožujícím poporodním krvácením byla v našem souboru 2,5 %. U žádné z pacientek nebyla zaznamenána trombemoblická komplikace hodnocená jako nežádoucí účinek léčby rFVIIa. U 74,3 % pacientek, kterým byl rFVIIa podán před zvažovanou hysterektomií, se podařilo díky této léčbě hysterektomii zabránit, a tak zachovat fertilitu.Závěr:
I na základě zde prezentovaných dat byl vypracován doporučený postup pro léčbu život ohrožujícího krvácení v České republice.Klíčová slova:
poporodní krvácení, hysterektomie, rFVIIa, klinický registr.ÚVOD
Ve vyspělých zemích je poporodní krvácení (PPH) hlavní příčinou mateřské mortality. Jeho incidence se pohybuje mezi 0,1–0,2 % [1, 2, 3].V České republice zemře z tohoto důvodu každoročně 5-10 žen [3, 4, 5], desetkrát více je jich pak krvácením ohroženo na životě a mnohdy trpí i doživotními následky. Nejčastější příčinou PPH je děložní atonie [4, 6, 7, 8, 9, 10].
Vývoj rFVIIa se datuje od osmdesátých let minulého století a registrace preparátu pro léčbu pacientů s hemofilií a inhibitorem (protilátkami proti exogenně podávanému faktoru VIII/faktoru IX) proběhla v EU v roce 1996 [11, 12, 13]. Hemostatický efekt rFVIIa spočívá ve zvýšení resp. obnovení tvorby trombinu, především na povrchu aktivovaných destiček. Toto množství trombinu pak zajistí další aktivaci destiček, zvýšení adheze a agregace destiček, aktivaci dostupných koagulačních faktorů a následně tvorbu dostatečně pevné fibrinové zátky. Restituce tvorby trombinu pomocí léčebně podaných dávek rFVIIa rovněž vede k aktivaci TAFI (trombinem aktivovaný inhibitor fibrinolýzy) a FXIII (faktor XIII), a tím brání nadměrné fibrinolýze [13, 14, 15, 16], rFVIIa tedy zvyšuje resp. obnovuje tvorbu klíčového enzymu koagulační kaskády - trombinu a normalizuje tak proces krevního srážení. Tím, že působí pouze lokálně v místě poranění cévy (exprese tkáňového faktoru v subendoteliálních vrstvách cévní stěny a aktivace destiček v místě poranění), nedochází k systémové aktivaci koagulace [17].
Léčba rFVIIa (NovoSeven) je indikována a jeho podání je podle registrace přípravku určeno k léčbě krvácivých příhod [18] a pro prevenci krvácení při operacích nebo invazivních procedurách u následujících skupin pacientů: pacienti s vrozenou hemofilií s inhibitory proti koagulačním faktorům VIII nebo IX > 5 BU (Bethesda unit), pacienti s vrozenou hemofilií, u kterých se očekává vysoká anamnestická odpověď na faktor VIII nebo IX, pacienti se získanou hemofilií, pacienti s vrozeným nedostakem faktoru VII, pacienti s Glanzmannovou trombastenií s protilátkami proti GP IIb-IIIa a/nebo HLA.
Od roku 1999 [19] je rFVIIa opakovaně použit i u pacientů bez primární poruchy koagulace (tedy v „off-label“ indikacích) v různých oborech. Stejně tak proběhlo několik různě zaměřených klinických studií. K dalším nejčastějším indikacím podání patřilo život ohrožující krvácení u válečných, ale i mírových traumat [19-25]. V oblasti gynekologie a porodnictví byly publikovány jednotlivé kazuistiky, soubory kazuistik i souhrnné review týkající se podání rFVIIa [5, 26-32], v některých zemích byly vydány i doporučené postupy léčby PPH zahrnující podání rFVIIa [4, 10, 43] a objevily se práce vycházející z dat klinických registrů v severní Evropě [6] a v Itálii [7].
Od roku 2004 probíhá sběr dat týkající se podání rFVIIa v nehemofilických indikacích v rámci mezinárodního registu UniSeven. Tento klinický registr shromažďuje případy z České republiky, Slovenska, Slovinska, Polska a Maďarska. Jde o vědecký akademický projekt Institutu biostatistiky a analýz Masarykovy univerzity a je podporován neomezeným edukačním grantem společnosti NovoNordisk Česká republika. Poskytovatel grantu nemá možnost zasahovat do sběru ani zpracování dat, ani jinak ovlivňovat vstupy či výstupy registru.
Z tohoto registru byly vybrány kazuistiky pacientů z České republiky, jichž je do současnosti celkem 558, a z nich dále bylo analyzováno 489 pacientů starších 15 let.
Analýza dat registru měla hodnotit úspěšnost léčby život ohrožujícího PPH sledováním mortality spojené s tímto stavem a kromě toho potvrdit či vyvrátit hypotézu, že časné podání rFVIIa před zvažovaným provedením hysterektomie může vést k jejímu odvrácení, a tím k zachování fertility ženy.
SOUBOR PACIENTŮ A METODIKA
Byla provedena retrospektivní analýza dat z registru UniSeven zahrnující případy léčby život ohrožujícího krvácení (ŽOK) za pomoci rFVIIa u pacientů bez primární poruchy koagulace. Byla definována skupina pacientů, provedena validace jednotlivých případů a dalšímu hodnocení byli podrobeni pacienti starší 15 let. V registru bylo po validaci nalezeno 80 pacientek s PPH. U toho souboru jsme hodnotili demografické údaje, způsob léčby krvácení s důrazem na provedení či neprovedení hysterektomie, vybrané laboratorní parametry a jejich trend, množství podaných transfuzních přípravků, krevních derivátů a náhradních roztoků, odhadovanou krevní ztrátu, mortalitu, morbiditu, počet dávek a dávkování rFVIIa a případné nežádoucí účinky léčby. Hodnocena byla rovněž doba umělé plicní ventilace (UPV) a doba pobytu na jednotce intenzivní péče (JIP). Bylo provedeno srovnávací hodnocení mezi skupinou pacientek s podáním rFVIIa před zvažovaným provedením hysterektomie a pacientek, kterým byl rFVIIa podán až během nebo po hysterektomii. Léčba byla hodnocena jako efektivní, pokud pacientka přežila, jako sekundární efekt léčby bylo hodnoceno zachování dělohy.
UniSeven registr je vytvořen a je spravován Institutem biostatistiky a analýz Masarykovy univerzity (www.iba.muni.cz, www.uniseven.cz). Parametrická struktura projektu byla navržena na základě znalostí o mechanismu účinku rFVIIa a řady publikací o použití tohoto přípravku při kontrole kritického krvácení [23, 24, 25].Databázový systém byl založen na modifikované verzi systému TrialDB. On-line komunikace mezi klientem a serverem probíhá pomocí zabezpečeného protokolu HTTPS (Hypertext Transfer Protocol Secure), který využívá šifrování pomocí SSL (Secure Socket Layer) [33, 34, 35].
Základní popis souboru pacientů a léčby ŽOK je proveden pomocí frekvenčních tabulek a popisných statistik: průměru, mediánu, minima, maxima a 5% a 95% kvantilů pozorovaných hodnot. Pro testování rozdílu hodnot mezi sledovanými skupinami pacientů jsou použity standardní neparametrické metody, v případě spojitých proměnných je použit Mannův-Whitneyho test, v případě hodnocení vztahu kategoriálních proměnných pak je použit odpovídající test pro kontingenční tabulky (Fisherův exaktní test pro dvě kategorie binárního charakteru ano/ne a Pearsonův χ2 test pro hodnocení vztahu dvou proměnných s více než dvěma kategoriemi). Pro stanovení statistické významnosti je použita hladina α = 0,05.
VÝSLEDKY
1. Demografické údaje a příčiny ŽOK
V registru UniSeven bylo po validaci nalezeno celkem 558 případů léčby ŽOK pomocí rFVIIa z různých příčin a indikací. Pacientů starších 15 let bylo 489 (295 mužů a 194 žen); u 80 žen byla důvodem podání rFVIIa léčba peripartálního krvácení; 78 (97,5 %) pacientek s PPH přežilo, 26 (32,5 %) zůstala zachována děloha.
Pokud jde o příčinu ŽOK v celé populaci zkoumaných subjektů, největší část zaujímali traumatizovaní (39,9 %). PPH se však podílelo 16,4 %! Ačkoli se v literatuře uvádí, že nejčastější příčinou ŽOK je trauma [36, 37, 38], po rozčlenění na muže a ženy, bylo jasně patrno, že v ženské populaci pacientů zadaných do databáze registru Uniseven bylo nejčastější příčinou ŽOK právě poporodní krvácení (viz tab. 1, 2 a graf 1, 2).
Tab. 1. Pacienti v UniSeven registru starší 15 let; rozložení dle pohlaví 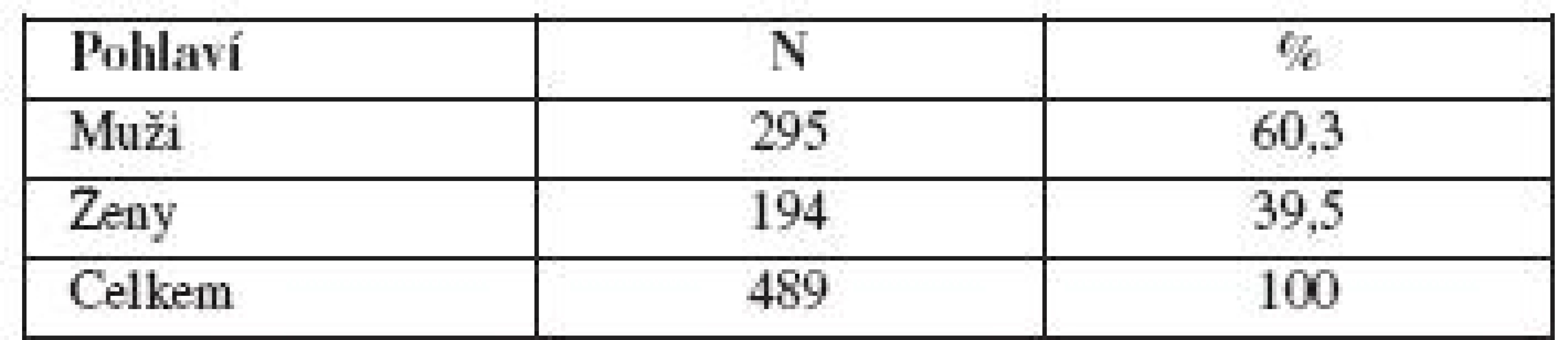
Tab. 2. Pacienti v UniSeven registru starší 15 let; rozložení podle důvodu podání rFVIIa 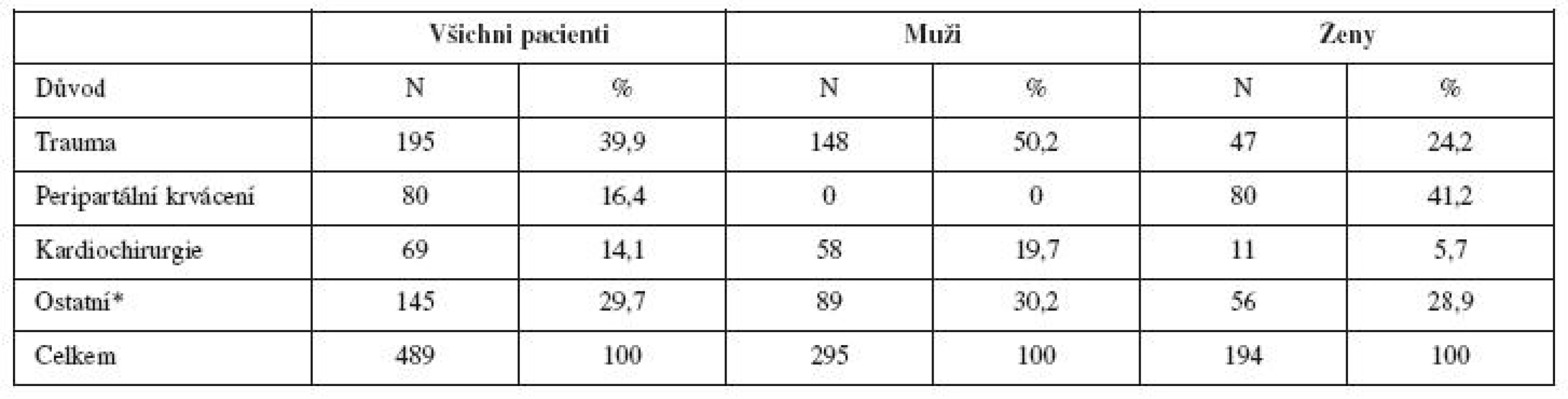
* intrakraniální krvácení, netraumatologická chirurgie, onkologie, ortopedie Graf 1. Pacienti v UniSeven registru starší 15 let, důvod podání rFVIIa 
Graf 2. Pacienti v UniSeven registru starší 15 let, důvod podání s ohledem na pohlaví 
2. Dávkování rFVII u PPH, laboratorní a klinické parametry
U všech pacientek s PPH probíhala standardní léčba ŽOK podle mezinárodních [39]i národních [40] doporučenízahrnující substituci erytrocytů podáním EBR (erytrocyty bez buffy coatu resuspendované) s cílem dosažení hladiny hemoglobinu (Hb) nad 60g/l, doplnění koagulačních faktorů formou dostatečného množství FFP (čerstvě zmrazená plazma) 10–20 ml/kg/dávku; max 40 ml/kg/den, náhradu trombocytů (Plt) s cílem dosažení hladiny min. nad 50x109/l, ideálně nad 100x109/l a naprosto zásadníroli pro úpravu koagulace pak měla substituce fibrinogenu (Fbg) v dávce 2-4g k dosažení jeho dostatečné hladiny (minimálně nad 1g/l).
Vlastní léčba PPH pak vycházela z příčiny vzniku krvácení a zahrnovala jak terapii děložní atonie, tak specializované gynekologicko-chirurgické postupy a v některých případech i intervenčně radiologické postupy [4, 5, 8, 43].
Pokud tato léčba nevedla k zástavě krvácení, bylo zvažováno provedení hysterektomie. V některých případech byl již před tímto krokem podán rekombinantní faktor VIIa.
Celková průměrná dávka rFVIIa použitá k léčbě PPH byla 10,3mg. Průměrně bylo k zástavě krvácení třeba podat 1,4 dávky a průměrná první dávka byla 106,1 μg/kg. Jedna dávka byla dostatečná u 66,3 % žen, dvě dávky obdrželo 26,3 % pacientek (tab. 3, 4).
Tab. 3. Pacientky s PPH léčené rFVIIa; dávkování (*chybějí údaje u 2 pacientek) 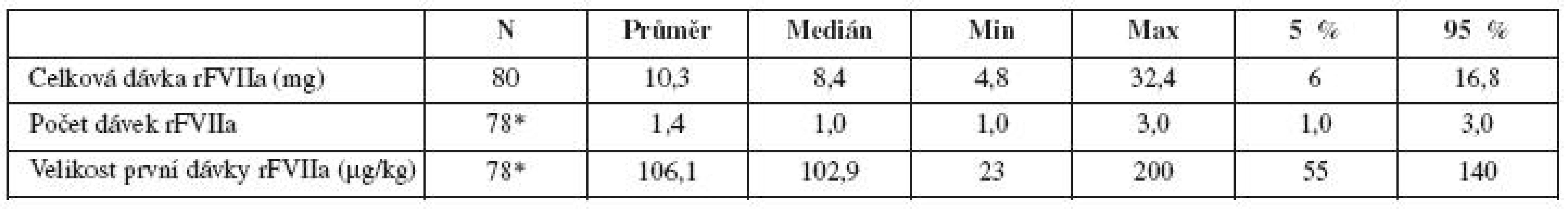
Tab. 4. Pacientky s PPH léčené rFVIIa; počet dávek 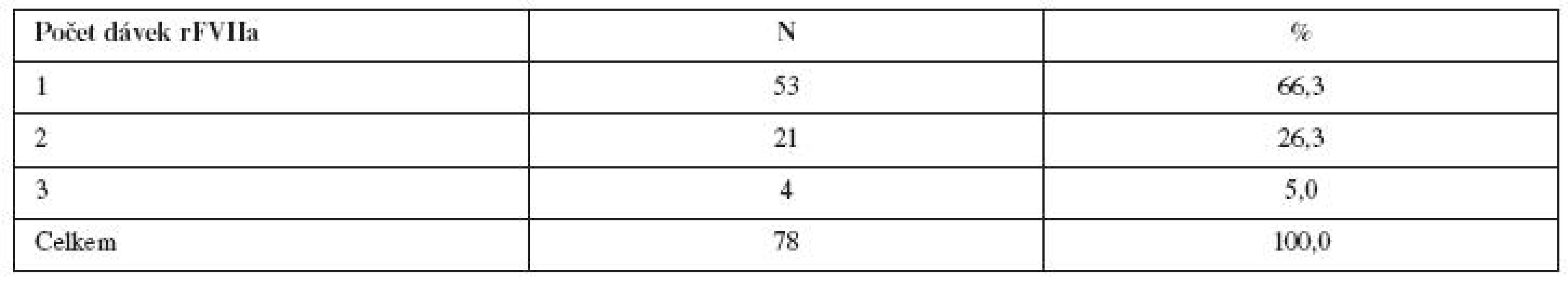
Byla shledána statisticky významná závislost (p = 0,048) velikosti první dávky rFVIIa na nutnosti opakovaného podání rFVIIa (tab. 5). První dávka rFVIIa byla u pacientek, které vyžadovaly druhé a další podání, signifikantně nižší (96,6 μg/kg) oproti případům, kde stačilo jen jedno podání léku (110,6 μg/kg).
Tab. 5. Pacientky s PPH léčené rFVIIa; porovnání velikosti první dávky rFVIIa v Ķg/kg vzhledem k celkovému počtu dávek 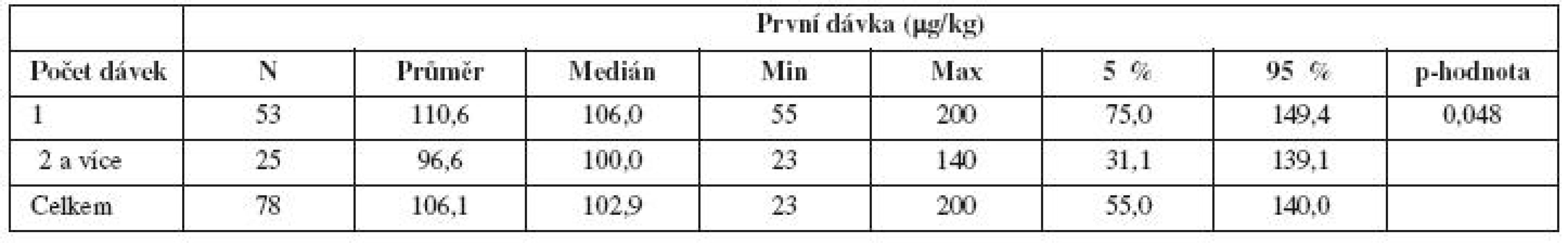
Po podání rFVIIa došlo ke statisticky významnému zlepšení všech sledovaných laboratorních parametrů - hodnoty Hb (hemoglobin), Htc (hematokrit), Plt (trombocyty), INR (mezinárodní normalizovaný poměr), aPTT (aktivovaný parciální tromboplastinový čas), Fbg (fibrinogen) a rovněž ke zmenšení velikosti krevní ztráty (tab. 6).
Tab. 6. Pacientky s PPH léčené rFVIIa; laboratorní a klinické parametry před podáním a po podání rFVIIa a jejich porovnání 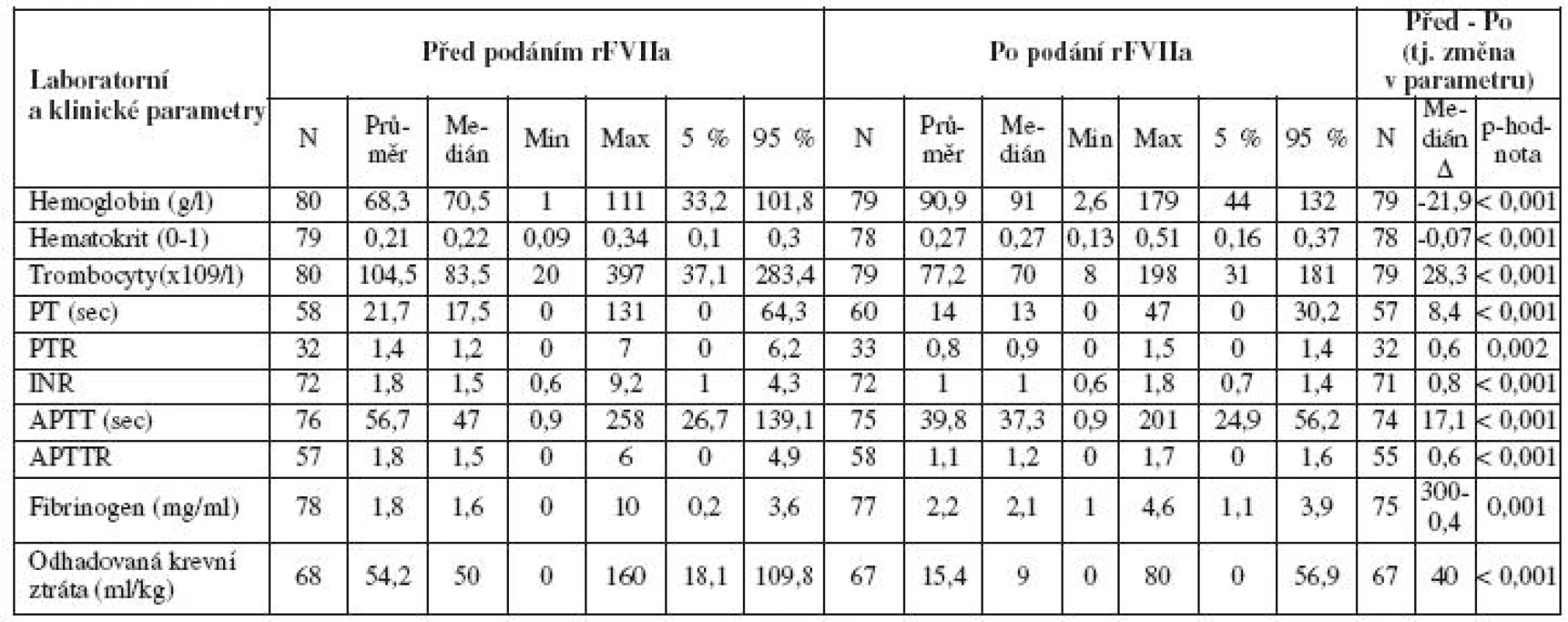
Stejně tak došlo ke statisticky významnému snížení množství podávaných EBR, FFP a fibrinogenu a náhradních roztoků při srovnání časových intervalů 24 hodin před podáním a 24 h po podání rFVIIa (tab. 7).
Tab. 7. Pacientky s PPH léčené rFVIIa; porovnání množství aplikovaných transfuzních přípravků, krevních derivátů a náhradních roztoků 24 hodin před podáním a 24 h po podání rFVIIa (* srovnání není možné vzhledem k více než polovině záznamů s nulovou spotřebou) 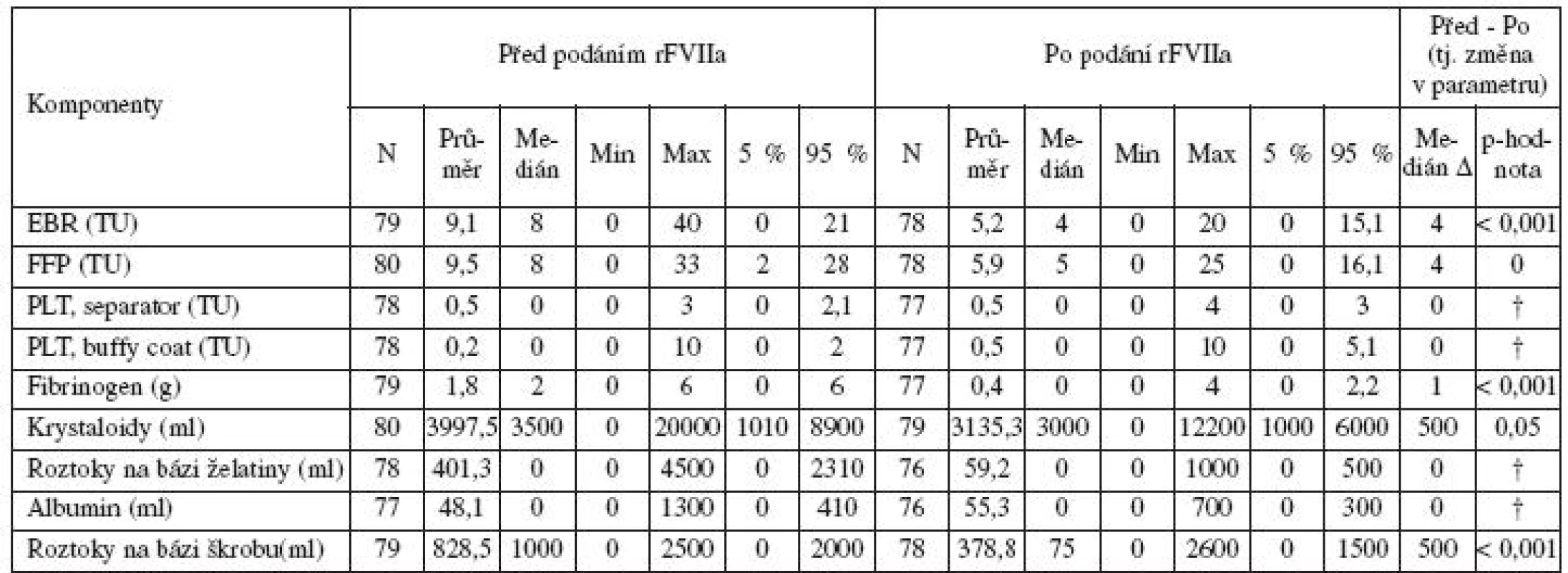
3. Nežádoucí účinky léčby a mortalita pacientů
U žádné z pacientek v souboru s PPH nebyla zaznamenána trombemolická komplikace, která by byla hodnocena jako související s léčbou rFVIIa. V celém UniSeven registru (558 pacientů) se vyskytly tři trombembolické komplikace (0,53 %).
V souboru 80 pacientek s PPH zemřely v důsledku krvácení 2 pacientky, což představovalo 2,5% mortalitu (graf 3).
Graf 3. Mortalita pacientů vzhledem k důvodu podání rFVIIa 
4. Hodnocení vedlejšího efektu léčby rFVIIa, odvrácení hysterektomie
Akutní abdominální hysterektomie byla provedena u 51 (63,8 %) z 80 pacientek. U 26 (32,5 %) z 80 rodiček došlo po podání rFVIIa k zástavě krvácení a hysterektomii nebylo nutno provést. U tří pacientek (3,75 %) záznam o operačním výkonu chybí (tab. 8).
Tab. 8. Provedení/neprovedení hysterektomie u pacientek s PPH léčených rFVIIa 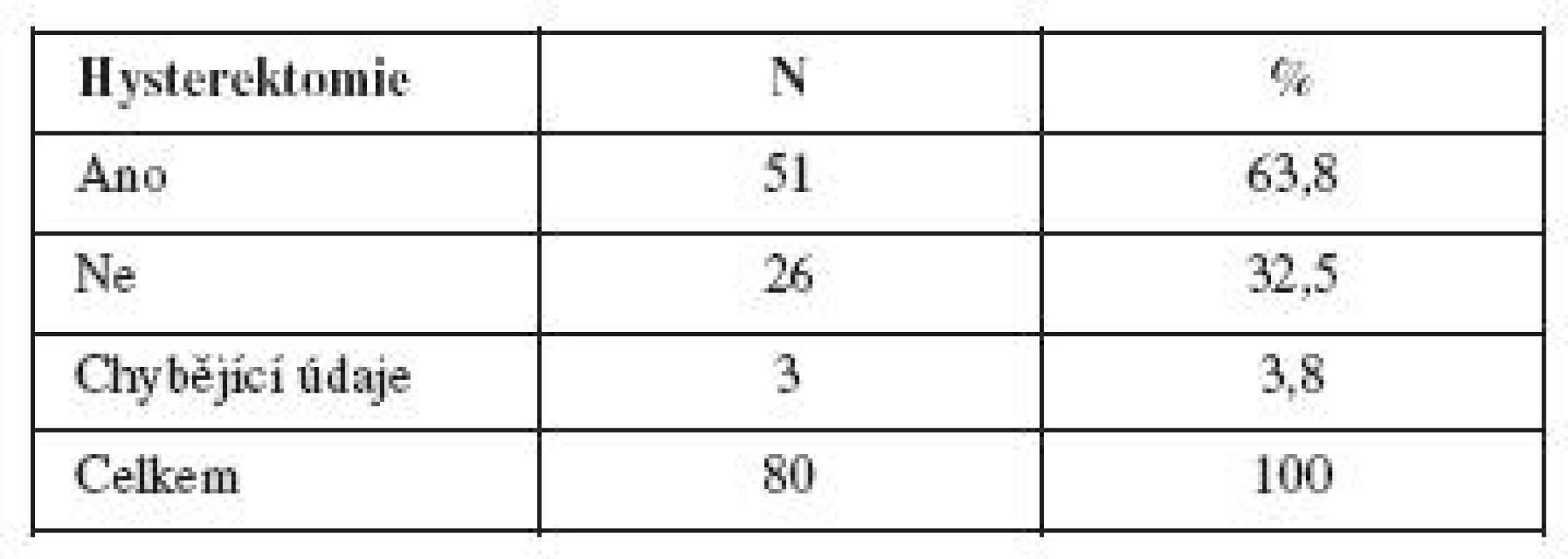
Tabulka 9 pak ukazuje skladbu pacientek, kterým byla provedena hysterektomie: devíti z nich (17,6 %) byl aplikován rFVIIa před jejím provedením, 23 (45,1 %) v průběhu hysterektomie a 18 (35,3 %) až po hysterektomii. U jedné pacientky není čas podání rFVIIa vzhledem k hysterektomii uveden.
Tab. 9. Doba podání rFVIIa u pacientek s PPH v souvislosti s provedením hysterektomie 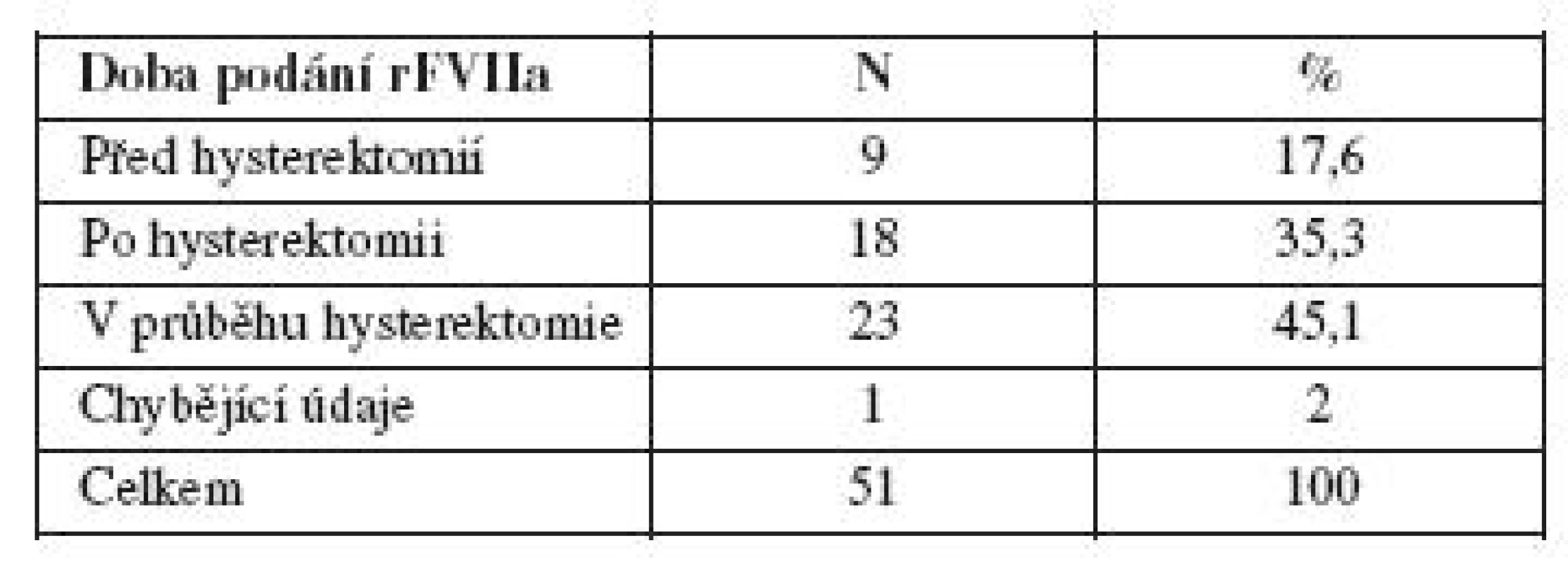
K následující analýze byla použita data 77 pacientek s PPH, u kterých bylo známo, zda byla, nebo nebyla provedena hysterektomie (tab. 10, 11). Pacientky jsme rozdělili do dvou skupin:
Tab. 10. Doba podání rFVIIa a provedení/neprovedení hysterektomie 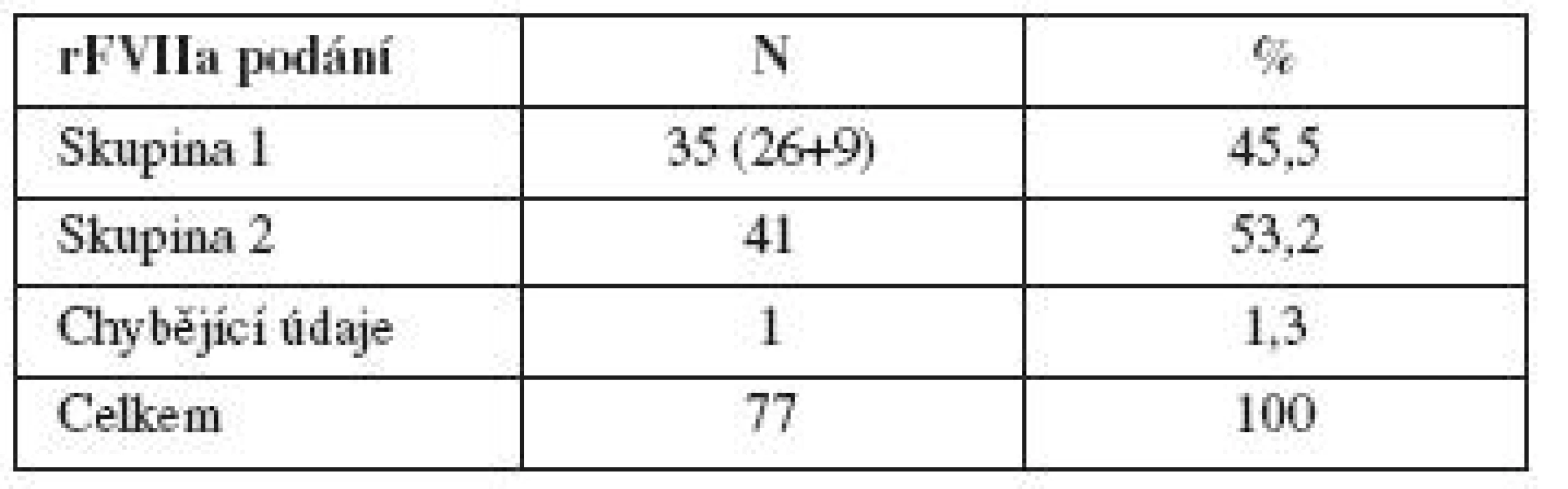
Tab. 11. Porovnání počtu podaných dávek rFVIIa u pacientek s PPH léčených rFVIIa v souvislosti s provedením/neprovedením hysterektomi 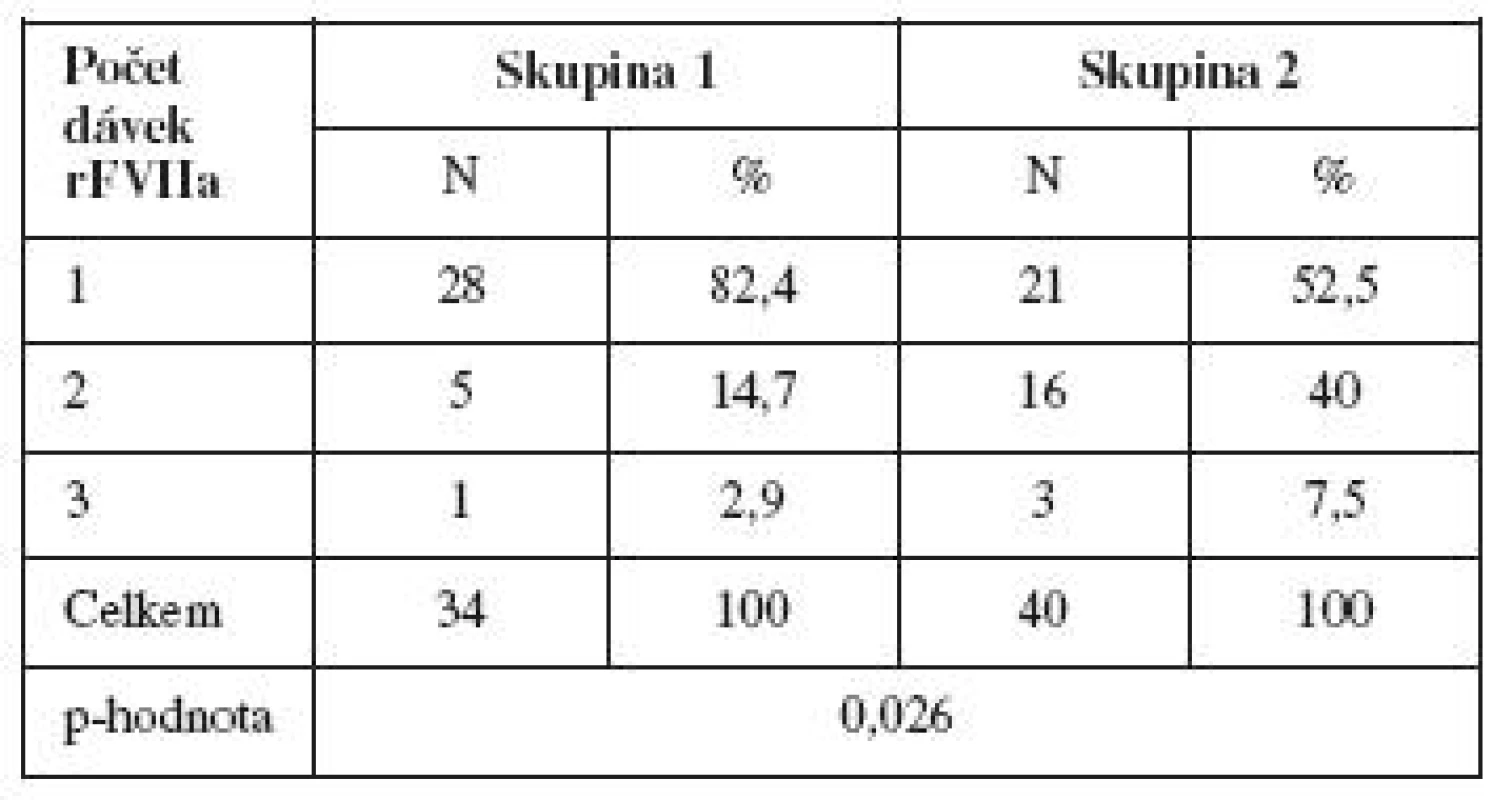
Skupina 1: rFVIIa byl podán před zvažovaným operačním výkonem. Poté buď došlo k zástavě krvácení a hysterektomie nebyla nutná, nebo zástavy krvácení dosaženo nebylo a hysterektomie byla provedena z vitální indikace.
Skupina 2: pacientky, které první dávku rFVIIa dostaly až v průběhu nebo po provedení hysterektomie.
Ve skupině 2 bylo 41 (53,2 %) pacientek, které dostaly první dávku rFVIIa až během nebo po hysterektomii. Skupina 1 zahrnovala 35 (45,5 %) pacientek. Pouze devíti z nich (25,7 % z 35) bylo nutno hysterektomii provést i přes léčbu rFVIIa! Lze tedy říci, že u 74,3 % našich pacientek, kterým byl pro ŽOK podán rFVIIa před zvažovanou hysterektomií, se přispěním této léčby podařilo hysterektomii zabránit!
Nenalezli jsme statisticky signifikantní rozdíl ve velikosti první dávky ani celkového množství podané dávky rFVIIa mezi skupinou 1 a skupinou 2. Naproti tomu počet dávek mezi oběma skupinami byl rozdílný (p = 0,026, viz tab. 11). Pacientkám skupiny 1 bylo podáno méně dávek ve srovnání s pacientkami skupiny 2.
Velmi signifikantní byl dále rozdíl v délce UPV (umělé plicní ventilace) i pobytu na JIP (jednotce intenzivní péče) mezi pacientkami skupiny 1 a skupiny 2 (tab. 12).
Tab. 12. Porovnání doby pobytu na JIP a doby UPV u pacientek s PPH léčených rFVIIa v souvislosti s provedením/neprovedením hysterektomie 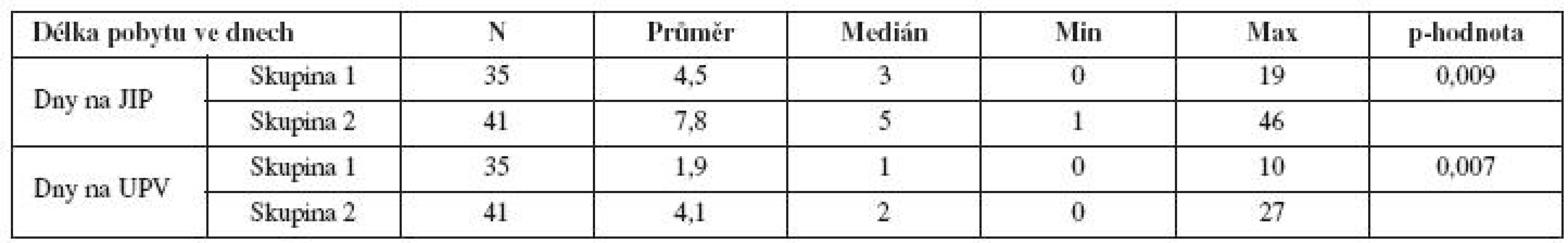
DISKUSE
Naše práce hodnotí v literatuře ojedinělý [6, 7] soubor pacientek: 80 případů léčených rFVIIa pro PPH. Léčba rFVIIa je v naší práci hodnocena jednak v souvislosti se záchranou života pacientky, a dále hodnotí, zda byla ženě zachována děloha, a tedy i šance na budoucí otěhotnění.
Analýza našeho souboru pacientek léčených rFVIIa se zabývá nejen laboratorními parametry, nežádoucími účinky preparátu či mortalitou pacientek, ale popisuje i způsob léčby rFVIIa a jeho dávkování s ohledem na případnou nutnost opakování podání. Naší hlavní snahou bylo na základě vlastních dat nalézt nejvhodnější režim léčby PPH. Poté na těchto podkladech dosáhnout konsenzu klinických oborů a vytvořit doporučený léčebný postup s cílem nejen záchrany života rodičky, ale i zachování dělohy s ohledem na budoucí reprodukční schopnost ženy postižené závažným poporodním krvácením.
Obdobně, jako např. v pracích Alfirevic, Barillari [6, 7] a dalších, i v našich výsledcích v některých případech ani chirurgická intervence včetně hysterektomie nevedla k zástavě krvácení. Teprve po podání rFVIIa došlo k úpravě stavu pacientky a zástavě krvácení. O to významnější je konstatování faktu, že u 26z 35 našich pacientek, kterým byl rFVIIa podán ještě před rozhodnutím o provedení hysterektomie, došlo k zástavě krvácení a hysterektomii nebylo nutno provést. Lze tedy spekulovat, že kdyby byl tento přístup zvolen i u pacientek, kterým byla hysterektomie provedena před podáním rFVIIa, byl by počet pacientek se zachovanou dělohou ještě vyšší.
V rámci registru zaměřeného na podávání rFVIIa v nehemofilických indikacích v České republice jsme identifikovali skupinu, která má z použití rFVIIa nejvyšší benefit, měříme-li tento přínos mortalitou spojenou se život ohrožujícím krvácením. Z 558 pacientů dostupných v registru ke dni analýzy měla jednoznačně nejnižší mortalitu (2,5 %) právě skupina pacientek s peripartálním krvácením. Průměr mortality u ostatních pacientů zadaných v registru byl 38 %. Jsme si vědomi toho, že nelze přímo srovnávat mortalitu rozdílných stavů vedoucích k ŽOK, přesto se domníváme, že uvedená informace má klinický a snad i etický význam, neboť porod by neměl být stavem, který vede k ohrožení života.
V literatuře se uvádí, že nejčastější příčinou vzniku ŽOK je trauma [36, 37, 38], a to až v padesáti procentech. V souboru pacientů zadaných v registru UniSeven a léčených pro ŽOK s pomocí rFVIIa bylo trauma nejčastější příčinou krvácení pouze u mužů. U žen bylo nejčastější příčinou právě PPH. Vzhledem k tomu, že selekce pacientů zadávaných do registru nebyla nijak ovlivňována, nepředpokládáme tedy ani zkreslení výsledků v této oblasti a domníváme se, že se jedná o reprezentativní vzorek české populace trpící život ohrožujícím krvácením.
U pacientek s PPH byla nalezena statistická závislost mezi nutností opakování podání rFVIIa a velikostí první dávky. Tam, kde byla dostačující již první (a tedy jediná) dávka, bylo pacientkám aplikováno průměru 110,6 μg/kg. Pacientkám léčeným dvěma a více podáními rFVIIa byla podána signifikantně nižší první dávka: průměrně 96,6 μg/kg (p = 0,048). Lze tedy spekulovat, že při podání vyšší iniciální dávky je efekt léčby rFVIIa lepší, a přitom se sníží celková spotřeba rFVIIa. To koresponduje s publikovanými pracemi, kde byl rFVIIa užit pro léčbu hemofilie s inhibitorem [15].
U pacientek s PPH došlo po aplikaci rFVIIa k úpravě sledovaných laboratorních parametrů, snížení velikosti krevních ztrát, množství podaných transfuzí, krevních derivátů a náhradních roztoků. V parametrech úpravy hladiny hemoglobinu, hematokritu, APTTR (aktivovaný parciální tromboplastinový test - poměr) a PTR (protrombinový test - poměr) dosáhly rozdíly hladiny statistické významnosti. Zlepšené laboratorní parametry korelovaly s klinickým stavem, což je podle našeho soudu nepřímým důkazem o efektivitě poskytnuté hemostatické léčby.
Ve skupině pacientek s PPH nebyly nalezeny žádné trombembolické příhody, které by byly hodnoceny jako vzniklé v souvislosti s léčbou rFVIIa. V souboru ostatních kazuistik ŽOK zadaných v registru se vyskytly tři trombembolické komplikace (0,53 %). Toto číslo nekoresponduje s pracemi Hsia a Hardyho, které hodnotily 17 proběhnuvších studií týkajících se podání rFVIIa v nehemofilických indikacích [41, 42]. Avšak ani jedna z těchto studií se netýkala PPH, a naopak v souboru pacientek s PPH Alfirevic a Barillari [6, 7] byly trobembolické komplikace výjimečné.
Jedním z důležitých aspektů naší práce bylo zjistit, zda léčba pomocí rFVIIa umožní zachování dělohy. Na základě výše uvedených dat konstatujeme, že v našem souboru vedla komplexní léčba PPH včetně včasného podání rFVIIa k záchraně života i dělohy u 74,3 % pacientek s ŽOK, u nichž by bez této léčby musela být s vysokou pravděpodobností hysterektomie provedena a u kterých nelze vyloučit, že by byly i po tomto výkonu nadále v ohrožení života.
Více než polovina z celkového počtu pacientek – 41 (53,2 %) – dostala první dávku rFVIIa až během nebo po hysterektomii. Domníváme se, že alespoň u části těchto nemocných by bylo zřejmě možno hyterektomii rovněž zabránit, kdyby byl rFVIIa podán zavčas, tedy před operačním výkonem.
Čím později byl lék podán, tím vyšší byla jeho spotřeba, a to i přes to, že se hysterektomii již nepodařilo zabránit. I tento fakt jednoznačně vede k úvaze, že pokud má být rFVIIa podán, pak co nejdříve a nejlépe před zvažovanou operací.
Provedli jsme rovněž porovnání skupiny žen s podáním rFVIIa před zvažovanou hysterektomií se skupinou žen s podáním první dávky rFVIIa až během nebo po provedení hysterektomie. Obě skupiny vykázaly stejnou úpravu laboratorních parametrů, stejný pokles ve spotřebě podaných transfuzních přípravků i krevních derivátů. Avšak skupina, které byl rFVIIa podán před zvažovanou operací a hysterektomii poté nebylo nutno provést, měla signifikantně kratší dobu pobytu na JIP a dobu UPV. Tento fakt má jasné vysvětlení v delší době hojení i rekonvalescence u žen po hysterektomii. Skupina, které byl rFVIIa podán před zvažovanou operací, obdržela rovněž méně transfuzí EBR a FFP. Pacientky, kterým byla touto léčbou zachráněna děloha, dostaly navíc signifikantně nejnižší celkovou dávku rFVIIa. Časné podání podle našeho názoru tedy vedlo nejen k záchraně dělohy, ale pravděpodobně i k nižšímu počtu transfuzí a nižším celkovým nákladům na léčbu. Pochopitelně pro přesné zhodnocení ekonomických ukazatelů by bylo nutno provést farmakoekonomický rozbor, který však nebyl cílem této práce.
I na základě výše uvedených dat byla v roce 2008 v ČR vydána doporučení týkající se léčby PPH. Podání rFVIIa je zde zvažováno jako možnost zástavy krvácení před případným provedením hysterektomie [43].
Jako další výstup naší práce potvrzující oprávněnost včasného podání rFVIIa vidíme možnost získání časové rezervy. Léčbou rFVIIa lze zřejmě docílit (alespoň dočasné) úpravy koagulačních parametrů s následnou stabilizací stavu pacientky a možností jejího transportu do nemocnice vyššího typu a/nebo do příjezdu specialisty a provedení superspecializovaných výkonů. Toto tvrzení však není podloženo konkrétními analýzami našich pacientů. Vychází spíše z empirického pozorování autorů a uživatelů registru UniSeven.
V naší práci jsme se nezabývali příčinou PPH, neboť další členění relativně malého souboru pacientek by snížilo výpovědní hodnotu. Tento fakt nepovažujeme za zásadní omezení a věříme, že neovlivnil námi postulované závěry a úvahy.
S ohledem na to, že nemáme přístup k vlastním ani literárním údajům o srovnatelném souboru pacientek léčených v ČR bez použití rFVIIa v době po roce 2004, nemohli jsme provést srovnání s takovou skupinou. V případě, že bychom volili historickou kontrolu z doby před rokem 2004, se lze domnívat, že by byl patrný rozdíl ve standardní léčbě krvácení, a tudíž bychom se vystavili riziku chybných srovnání a závěrů.
ZÁVĚR
Za 5 let od roku 2004 do roku 2009 byl rFVIIa podán a zdokumentován v registru UniSeven v České republice u 80 žen z indikace PPH (což v České republice při asi 100 tisících porodech za rok představuje jedno podání na 6 tisíc porodů). Celkem bylo v této době v „off-label“ indikaci podání rFVIIa léčeno pro ŽOK a v registru Uniseven zaznamenáno 558 pacientů.
U 78 (97,5 %) z 80 žen léčených rFVIIa pro PPH bylo dosaženo kontroly krvácení. Pouze 2 pacientky (2,5 %) na následky PPH zemřely.
Vzhledem k tomu, že u žádné z pacientek nebyla zaznamenána trombembolická komplikace hodnocená jako související s léčbou rFVIIa, se podání tohoto preparátu v indikaci PPH v našem souboru jeví jako bezpečné.
U 35 pacientek byl preparát podán před zvažovaným provedením hysterektomie. Z nich u 26 (74,3 %) bylo dosaženo kontroly krvácení a nebylo nutno provést hysterektomii.
Časné podání rFVIIa může pravděpodobně být významným faktorem v redukci počtu hysterektomií u peripartálního krvácení. Tam, kde selhaly konvenční postupy, může léčba rFVIIa vést k zástavě krvácení, záchraně dělohy, a tím k zachování fertility ženy.
Vzhledem k závažnosti problematiky PPH a s ohledem na výše prezentovaná data byla v České republice v roce 2008 na základě konsenzu oborů anesteziologie a intenzivní medicíny, gynekologie a hematologie vydána závazná klinická doporučení: Diagnostika a léčba akutního peripartálního život ohrožujícího krvácení – doporučený postup (Česká gynekologie 2008; 73, 6 : 377-379].
V tomto materiálu je kladen velký důraz na snahu o zachování fertility ženy za využití dříve méně obvyklých gynekologických, cévně-chirurgických a intervenčně radiologických technik [3] a v léčbě je doporučeno zvážit i podání rFVIIa.
I na základě aktualizovaných doporučení pro léčbu traumat v evropském kontextu [44] a dva roky od vydání klinických doporučení léčby PPH v ČR [43] se jeví jako nevyhnutelné provést jejich revizi. Tento článek by měl být zároveň výzvou, abychom se znovu pokusili vrátit se ke sporným bodům, které se týkají především podání antitrombinu, hladiny fibrinogenu doporučené pro jeho substituci a k otázce aplikace heparinů z pohledu společností, které stály u vzniku doporučení a minimálně na půdě odborného časopisu vyvolat diskusi.
Zároveň budeme v rámci Jihomoravského kraje iniciovat projekt, který si klade za cíl vznik registru všech případů závažného PPH s možností jeho následného rozšíření na celou ČR.
Práce byla podpořena neomezeným edukačním grantem společnosti NovoNordisk Česká republika, s.r.o. spojeným s podporou registru UniSeven. Nositelem grantu je Institut biostatistiky a analýz Masarykovy univerzity v Brně.
Publikace byla primárně publikována v časopise Anesteziologie a intenzivní medicína 2010, 21, č. 5. Vzhledem k aktuálnosti tématu uveřejňujeme práci se svolením redakce. Redakční rada AIM netrvá na dodržení jinak požadovaného časového odstupu publikace obou článků.
Práce má dva hlavní autory: D. Seidlová a J. Blatný, kteří se na ní podíleli stejnou měrou.
MUDr. Dagmar Seidlová
Fakultní nemocnice Brno, PRM
Anesteziologicko-resuscitační oddělení
Obilní trh 11
602 00 Brno 2
e-mail: dagmarseidl@email.cz
Zdroje
1. Zhang, W., Alexander, S., Bouvier-Colle MacFarlane, A., MOMS-B Group. Incidence of severe pre-eclampsia, postpartum haemorrhage and sepsisas a surrogete marker of severe maternal morbidity in a European population-based study: the MOMS-B survey. BJOG 2005, 112, p. 89-96.
2. Khan, KS., Wojdyla, D., Say, L., et al. WHO analysis of maternal death; a systematic review. Lancet 2006, 367, p. 1066-1074.
3. Rodička a novorozenec 2008, 2007. Praha: Ústav zdravotnických informací a statistiky ČR.
4. Feyereisl, J. Závažné postpartální hemoragie a doporučený postup k léčbě. Čes Gynek 2008, 73, 6, p. 375-376.
5. Binder T. Šokové stavy v porodnictví. In Moderní porodnictví. Praha: Grada 2008, s. 303-304.
6. Alfirevic, Z., Elbourne, D., Pavord, S., et al. Use of recombinant activated factor VII in primary postpartum hemorrhagie. The northern european registry 2000-2004. Obst Gynecol 2007, 110, p. 1270-1278.
7. Barillari, G., Frigo, M., Casarotto, M., et al. Use of recombinant activated factor VII in severe post-partum haemorrhage: Data from Italian Registry A multicentic observational retrospective study. Trombosis Res 2009, 6, p. 41-47.
8. Roztočil, A. Nepravidelnosti III. doby porodní. In Moderní porodnictví. Praha: Grada 2008, s. 298-301, 307-309.
9. Franchini, M., et al. A critical review on the use of recombinant factor VIIa in life-threatening obstetric postpartum hemorrhage. Semin Thromb Hemost 2008, 34, p. 104–112.
10. Duffy, MR. Guidelines for use of recombinant factor VIIa in life-threatening post-partum haemorrhage. Inter J Obstet Anest 2007, 16, p. 299-300.
11. Hedner, U., et al. Successful use of recombinant factor VIIa in patient with severe haemophilia A during synovectomy. Lancet 1988, 2, p. 1193.
12. Ingerslev, J., Freidman, D., Gastineau, D., et al. Major surgery in haemophilic patients with inhibitors using recombinant factor VIIa. Haemostasis 1996, 26(Suppl. 1), p. 118–123.
13. Monroe, DM., Hoffman, M., Olivier, JA., Roberts, HR. Platelet activity of high-dose factor VIIa is independent of tissue factor. Br J Haematol 1997, 99, p. 642–647.
14. Hedner, U. Mechanism of action, development and clinical experience of recombinant FVIIa. J Biotechnol 2006, 124, p. 747–757.
15. Kjalke, M., et al. High-dose factor VIIa increases initial thrombin generation and mediates faster platelet activation in thrombocytopenia-like conditions in a cell-based model system. Br J Haematol 2001, 114, p. 114–120.
16. Galán, AM., Tonda, R., Pino, M., et al. Increased local procoagulant action: a mechanism contributing to the favorable hemostatic effect of recombinant FVIIa in PLT disorders. Transfusion 2006. 43, p. 885–891.
17. Salaj, P., Brabec, P,. Penka, M., et al. Effect of rFVIIa dose and time to treatment on patients with haemophilia and inhibitors: Analysis of HemoRec registry data from the Czech Republic, Haemophilia 2009, 15, p. 725-729.
18. Blatny, J., Kohlerova, S., Zapletal, O., et al. Prophylaxis with recombinant factor VIIa for the management of bleeding episodes during immune tolerance treatment in a boy with severe haemophilia A and inhibitors. Haemophilia 2008 Sep;14(5), p. 1140-1142.
19. Kenet, G., Walden, R., Eldad, A., Martinowitz, U. Treatment of traumatic bleeding with recombinant factor VIIa. Lancet 1999, 354(9193), p. 1879.
20. Martinowitz, U., Kenet, G., Lubetski, A., et al. Possible role of recombinant activated factor VII (rFVIIa) in the control of hemorrhage associated with massive trauma. Can J Anaesth 2002, 49, p. 15–20.
21. Bowman, LJ., et al. Use of recombinant activated factor VII concentrate to control postoperative hemorrhagie in complex cardiovascular surgery. Ann Thorac Surg 2008, 85, p. 1669–1677.
22. Mayer, SA., Brun, NC., Begtrup, K., et al. Recombinant activated factor VII intracerebral hemorrhage trial investigators: recombinant activated factor VII for acute intracerebral hemorrhage. N Engl J Med 2005, 352, p. 777–785.
23. Johansson, PI., Eriksen, K., Nielsen, SL., et al. Recombinant FVIIa decreases perioperative blood transfusion requirement in burn patients undergoing excision and skin grafting—results of a single centre pilot study. Burns 2007, 33, p. 435–440.
24. Lodge, JP., Jonas, S., Jones, RM., et al. Efficacy and safety of repeated perioperative doses of recombinant factor VIIa in liver transplantation. Liver Transpl 2005, 11, p. 973–979.
25. Dutton, RP., et al. Factor VIIa for correction of traumatic coagulopathy. J Trauma 2004, 57, 4, p. 709-719.
26. Ahonen, J., Jokela, R. Recombinant factor VIIa for life-threatening post-partum haemorrhage. Br J Anaesth 2005, 94, p. 592–595.
27. Hosain, N., et al. Use of recombinant activated factor VII for massive postpartum hemorrhage. Acta Obstet Gynecol 2007, 86, p. 1200-1206.
28. Segal, S., et al. The use of recombinant factor VIIa in severe postpartum hemorrhage. Acta Obstet Gynecol Scand 2004, 83, p. 771–772.
29. Haynes, J., Laffan, M., Platt, F. Use of recombinant activated factor VII in massive obstetric haemorrhage. Int J Obstet Anesth 2007, 16, p. 40–49.
30. Sobieszczyk, S., Breborowiciz, GH., Platicanov, V., et al. Recombinant factor VIIa in the management of postpartum bleeds; an audit of clinical use. Acta Obstet Gynecol 2006, 85, p. 1239-1247.
31. Holub, Z., Feyereisl, J., Kabelik, L., Rittstein, T. Successful treatment of severe post-partum bleeding after caesarean section using recombinant activated factor VII. Čes Gynek 2005, 70, p. 144–148.
32. Mannová, J., Petrenko, M., Seidlová, D., a kol. Aktivovaný rekombinantní faktor VII u závažného poporodního krvácení: kazuistiky. Prakt Gyn 2007, 14, 4, s. 171–176.
33. Nadkarni, PM., Brandt, C., Frawley, S., et al. Managing attribute—value clinical trials data using the ACT/DB client-server database system. J Am Med Inform Assoc 1998, 5(2), p. 139-151.
34. Nadkarni, PM., Brandt, CM., Marenco, L. WebEAV: automatic metadata-driven generation of web interfaces to entity-attribute-value databases. J Am Med Inform Assoc 2000, 7(4), p. 343-356.
35. Nadkarni, PM., Marenco, L. Easing the transition between attribute-value databases and conventional databases for scientific data. Proc AMIA Symp 2001, p. 483-487.
36. Mayo, A., Martinowitz, U., Kluger, Y. Coagulopathy in the critically injured patient. Yearbook of Intensive Care and Emergency Medicine 2006, p. 232-243.
37. Chiara, O., Cimbanassi, S., Vesconi, S. Critical bleeding in blunt trauma patiens Yearbook of Intensive Care and Emergency Medicine 2006, p. 244-254.
38. Rossaint, R., Spahn, DR. Trauma: Bleeding, Coagulopathy and Blood Component Transfusion Yearbook of Intensive Care and Emergency Medicine 2006, p. 255-264.
39. Vincent, JL., Rossaint, RB., Ozier, YZDD., Spahn, DR. Recommendations on the use of recombinant activated factor VII as an adjunctive treatment for massive bleeding - a European perspective. Critical care 2006, 4, 10, p. 120.
40. Blatný, J., Cvachovec, K., Černý, V., a kol. Zásady podpory koagulace u život ohrožujícího a neztišitelného krvácení – konsensuální stanovisko. Anest Intenzivní Med 2006, 6.
41. Hsia, CC., Chin-Yee, IH., McAlister, VC. Use of recombinant activated factor VII in patients without hemophilia. A meta-analysis of randomized control trials. Ann Surg 2008, 248, p. 61-68.
42. Hardy, JF., Belisle, S., Van der Linden, P. Efficasy and safety of recombinant activated factor VII to control bleeding in nonhemophiliac patients: A rewiev of 17 randomized controlled trials. Ann Thoracic Surg 2008, 86, p.1038-1048.
43. Binder, T., Cvachovec, K., Černý, V., a kol. Diagnostika a léčba akutního peripartálního život ohrožujícího krvácení – doporučený postup. Čes Gynek 2008, 73, 6, s. 377-379.
44. Rossaint, R., Bouillon, B., Cerny, V., et al. Management of bleeding following major trauma: an updated European guideline. Critical Care 2010 14, p. R52.
Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicína
Článek vyšel v časopiseČeská gynekologie
Nejčtenější tento týden
2010 Číslo 4- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Isoprinosin je bezpečný a účinný v léčbě pacientů s akutní respirační virovou infekcí
-
Všechny články tohoto čísla
- Česká perinatologie 2010: Quo vadis?
- Etika neonatální intenzivní péče
- Dystokie ramének plodu při vaginálním porodu
- Perinatální paréza brachiálního plexu
- Sutura ruptury perinea 3. a 4.stupně
- Závažné porodnické poranění a anální inkontinence
-
Rekombinantní aktivovaný faktor VII (rFVIIa) v léčbě závažného poporodního krvácení
Data z registru UniSeven v České republice -
Trombotická trombocytopenická purpura v těhotenství
Kazuistika - Ruptury dělohy v těhotenství – kazuistiky
- Analýza fragmentů volné fetální DNA v plazmě těhotných žen v průběhu těhotenství
- DNA analýza AZF oblasti Y chromozómu u Slovákov s poruchou plodnosti
- Doporučení k provádění prevence RhD aloimunizace u RhD negativních žen
- Aloimunizace těhotných žen non-RhD erytrocytárními antigeny: přehledový článek
- Lokální protilátky proti spermiím a celkové hladiny imunoglobulinů v ovulačním cervikálním hlenu
- Hodnocení kostní minerální denzity ultrazvukem patní kosti a duální rentgenovou absorpciometrií předloktí v klinické praxi
- Komplikace radikálních onkogynekologických operací
- Proces reprodukčního stárnutí ženy – jeho příčiny a možnosti ovlivnění v praxi
- Postřehy z Turnhoutu – Belgie (3.–8. 5. 2010)
- Postřehy z ENTOG exchange Genk, Belgie(3.–8. 5. 2010)
- Univ. prof. MUDr. Ján Štencl, CSc., člen ČGPS ČLS J. E. Purkyňu h. c. – sedemdesiatročný
- K významnému životnímu jubileu prof. MUDr. Z. Štembery, DrSc.
- XXII. evropský kongres perinatální medicínyGranada, Španělsko
- Zápis ze 42. konferenceSekce gynekologie dětí a dospívajících ČGPS ČLS JEP
- Reakce na Zápis z konference Sekce gynekologie dětí a dospívajících ČGPS ČLS JEP
- Prof. MUDr. David Cibula, CSc. a Doškolování lékařů LEVRET s.r.o. připravili ve spolupráci se společností Bayer s.r.o. MALÉ DOŠKOLOVACÍ DNY podzim 2010
- Akce IPVZ
- Abstrakta kongresu ČGPS SSG 3.–6. 6. 2010 v Karlových Varech
- Česká gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Dystokie ramének plodu při vaginálním porodu
- Sutura ruptury perinea 3. a 4.stupně
- Perinatální paréza brachiálního plexu
- Komplikace radikálních onkogynekologických operací
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



