-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Orgánové transplantace od dárců se selháním oběhu
Autoři: Wojciech G. Polak
Působiště autorů: Oddělení hepatopankreatobiliární a transplantační chirurgie, Klinika chirurgie, Erasmus MC, Univerzitní lékařské centrum Rotterdam, Nizozemsko
Vyšlo v časopise: Čas. Lék. čes. 2017; 156: 370-373
Kategorie: Přehledové články
Souhrn
Nedostatek orgánů vede k častějším transplantacím od dárců po selhání oběhu. Tento přehled popisuje současnou praxi využití dárců po selhání oběhu (DCD – donor after circulatory death), klasifikaci DCD a odběr orgánů od těchto dárců. Jsou diskutovány výsledky a prezentovány nové strategie DCD.
Navzdory faktu, že DCD reprezentují dárce s rozšířenými kritérii, přísný výběr orgánů a nové technologie, jako jsou přístrojové nebo normotermní perfuze, umožňují lepší využití DCD a dosažení podobných výsledků jako u dárců po smrti mozku (DBD – donor after brain death).Klíčová slova:
orgánová transplantace, darování orgánů, smrt ze selhání oběhu, přístrojová perfuze, outcomeÚVOD
Již mnoho let jsou transplantace léčbou konečných stadií orgánového selhání (1). Většina transplantovaných orgánů pochází od zemřelých dárců, i když v některých zemích je šířeji používán přenos jater či ledvin od žijících dárců (2).
Mechanismus smrti rozděluje zemřelé dárce na dárce po smrti mozku (DBD), u nichž je prokázána mozková smrt, a na dárce po selhání oběhu (DCD), dříve označované za dárce bez bijícího srdce nebo dárce po kardiální smrti. V počátcích orgánových transplantací pocházely všechny přenášené orgány od DCD, protože neurologická kritéria smrti (tzv. Harvardská kritéria smrti mozku) byla popsána a přijata až v roce 1967 (3). Od té doby pochází většina orgánů pro transplantace od DBD a mnoho zemí má legislativu definující smrt mozku a upravující transplantace od DBD.
Vývoj chirurgických technik a anesteziologických postupů stejně jako pokrok imunosupresivní léčby vedl k nárůstu počtu transplantací. Současně se hlavním omezením orgánových transplantací stal nedostatek DBD, zvláště v zemích s omezenými možnostmi přenosu ze žijícího dárce. Proto je rostoucí pozornost v mnoha zemích věnována dárcovství po oběhovém selhání.
Cílem této práce je shrnout současný stav dárcovství po selhání oběhu a výsledky orgánových transplantací od DCD.
KLASIFIKACE DCD A DIAGNÓZA SMRTI DCD
Kategorie DCD
Rostoucí zájem o DCD i potřeba standardizace dárcovství od DCD vedla v roce 1995 ke konání prvního Mezinárodního shromáždění o dárcích bez bijícího srdce v nizozemském Maastrichtu, kde byla stanovena kritéria pro potvrzení smrti DCD a 4 kategorie DCD (4). Bylo navrženo několik úprav těchto tzv. Maastrichtských kritérií DCD; v současnosti byla publikována nejnovější modifikovaná klasifikace DCD (tab. 1) (5–8).
První dvě kategorie (I a II) se nazývají nekontrolovaní dárci DCD, protože v obou kategoriích bývá doba teplé ischemie obvykle dlouhá v důsledku samovolné zástavy oběhu. V kategorii I se záchranáři ani nepokusili o resuscitaci („při příjezdu mrtev“), takže hlavním omezením pro tyto zemřelé z hlediska možnosti být dárcem je trvání teplé ischemie, která nemá být delší než 45 minut (8). Kategorie II zahrnuje nemocné po neúspěšné kardiopulmonální resuscitaci. V obou kategoriích byly přidány podkategorie: IA a IIA, pokud k zástavě oběhu došlo mimo zdravotnické zařízení (out-of-hospital), a IB a IIB, pokud nastala v nemocnici.
Kategorie III a IV se označují jako kontrolovaní dárci DCD. V kategorii III je úmrtí z cirkulační příčiny očekáváno po plánovaném ukončení život udržující kardiorespirační podpory (WLST – withdrawal of life-sustaining treatment). Multidisciplinární tým přijme v souhlasu s rodinou rozhodnutí o WLST, pokud je další léčba marná. Dárci kategorie IV mají diagnózu smrti mozku (DBD), avšak k neočekávané zástavě cirkulace došlo před odebráním orgánů. V některých evropských zemích, kde je možno provést eutanazii (Belgie, Lucembursko, Nizozemsko), se používá i kategorie V, zahrnující dárce se zástavou oběhu za lékařské asistence (9).
V současnosti v zemích jako Belgie, Nizozemsko, Spojené království a USA převažuje kategorie III DCD, zatímco ve Francii a Španělsku je častější kategorie II DCD (10).
Diagnóza smrti u DCD
U DCD je smrt diagnostikována na základě kardiopulmonálních kritérií (11). Po zástavě oběhu buď po WLST v kategorii III DCD, nebo po ukončení resuscitace v kategoriích I a II DCD nastává chvíle, kdy není poskytována žádná léčba – tzv. no touch období. Teprve po něm může být konstatována smrt a zahájen odběr. Důležité je, že období no touch nenastává u IV. typu DCD, kde již byla smrt mozku konstatována.
Původní doporučení prvního Mezinárodního shromáždění o dárcích bez bijícího srdce předpokládalo, že no touch období bude trvat 10 minut, ale po zveřejnění doporučení amerického Institute of Medicine v roce 1998 bylo zkráceno na 5 minut (4, 12). Ovšem v závislosti na legislativě se v jednotlivých státech trvání no touch období pohybuje mezi 2 a 20 minutami (tab. 2) (4).
ODBĚR ORGÁNŮ OD DCD
Odběr orgánů od DCD se liší od situace u DBD zvláště tím, že zástava oběhu nastává před zahájením perfuze studeným konzervačním roztokem. Rozdíly existují také mezi neřízenými (typy I a II) a řízenými (typy III–V) DCD kvůli odlišné logistice odběru (obr. 1) (13–15).
Obr. 1. Rozdíly v logistice mezi kontrolovanými (kategorie III–V) a nekontrolovanými (kategorie I–II) DCD 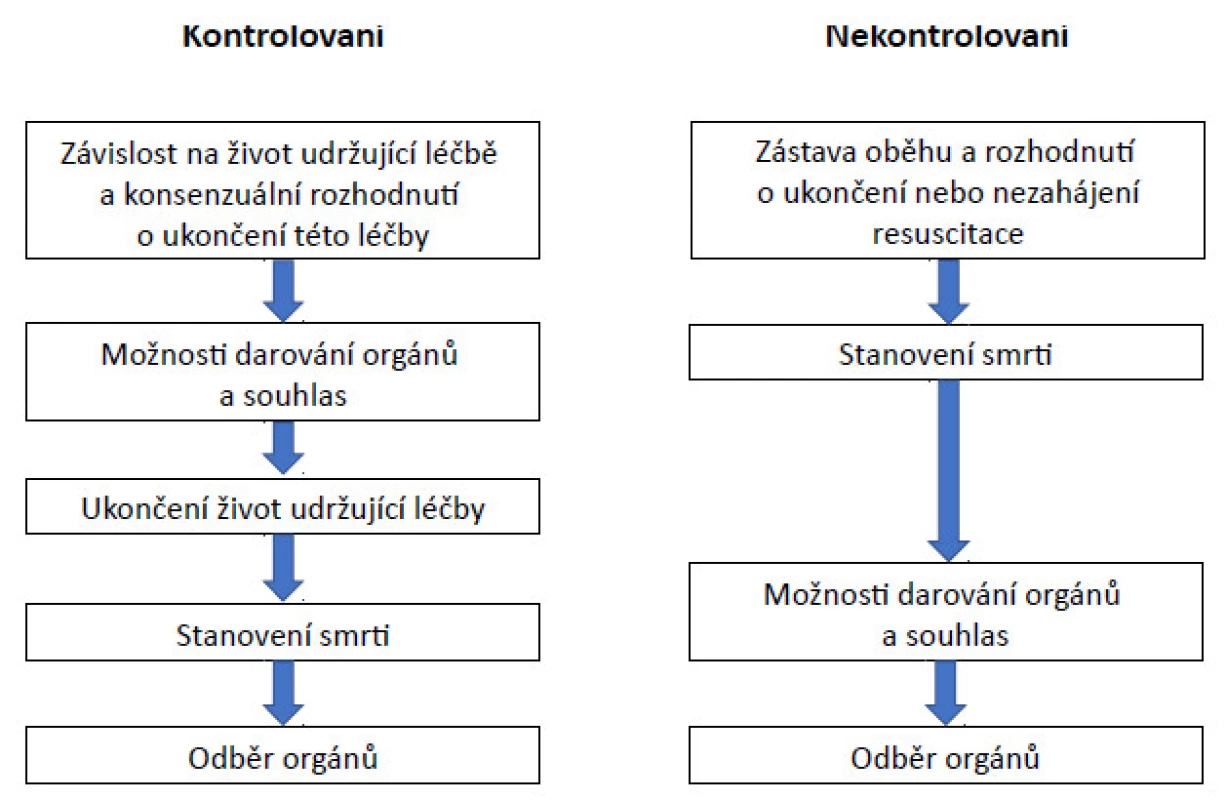
Hlavním cílem první fáze odběru orgánů je omezení období teplé ischemie nebo doby bez cirkulace krve u DCD, k čemuž u DBD nedochází. K tomu lze použít dva způsoby odběru:
1. studenou perfuzí cestou stehenní tepny po kanylaci katetru s trojitým lumen a dvěma balónky a s kanylací stehenní žíly k odvodu krve;
2. superrychlou technikou (torakolaparotomie) s přímou kanylací aorty pro studenou perfuzi a žilní vykrvácení a s přiložením aortální svorky nad bránicí (16–18).Studená perfuze je v některých centrech nahrazována normotermní regionální perfuzí (NRP) u neřízených a v současnosti i u řízených DCD (19, 20).
ORGÁNOVĚ SPECIFICKÝ VÝBĚR DCD
Orgány od DCD trpí nevyhnutelnou dobou teplé ischemie mezi zástavou oběhu a studenou perfuzí. To může způsobit poškození teplou ischemií vedoucí k časté primární afunkci (PNF – primary non-function) a opožděné funkci štěpu (DGF – delayed graft function), stejně tak k orgánově specifickým komplikacím, např. neanastomotickým biliárním strikturám při transplantaci jater. To je také důvod, proč jsou DCD považováni za dárce s rozšířenými kritérii a orgánově specifická omezení jsou častější než u DBD (21). Proto je třeba bez ohledu na typ orgánu vyvinout úsilí k minimalizaci jak teplé, tak studené ischemie v průběhu odběru a přenosu orgánů od DCD (22–25).
Ledviny
Věk DCD představuje nezávislý rizikový faktor PNF, DGF a ročního přežití štěpu; ledviny od dárců starších 60 let mají téměř dvojnásobné riziko selhání štěpu ve srovnání s ledvinami od DCD mladších 40 let. Ledvina od staršího DCD má být použita s omezením, zvláště při dalším rizikovém faktoru, jako je BMI > 45, diabetes, hypertenze nebo cévní mozková příhoda jako příčina smrti (23). Takové ledviny také nemají být transplantovány mladým příjemcům (23, 26). Trvání teplé ischemie (WIT – warm ischemia time) má být u DCD ledvin omezena na 20–30 minut; ledviny s WIT > 40 minut mají významně častěji PNF (23, 27).
Pankreas
Podle současných doporučení se má k transplantacím vaskularizovaného pankreatu přistupovat kriticky a jen v případech, kdy nejsou přítomné jiné rizikové faktory (24, 28). Transplantace pankreatu od obézních dárců (BMI > 30) je kontraindikovaná, ale ostrůvky od obézních dárců použity být mohou. První WIT má být nejvýše 30 minut pro vaskularizovaný pankreas a 60 minut pro přenos Langerhansových ostrůvků (24, 28).
Játra
Doporučení pro transplantaci jater od DCD byla navržena na 6. mezinárodním setkání o DCD v Paříži (8). Standardní játra od řízeného DCD splňují tyto požadavky: věk dárce ≤ 50 let, BMI ≤ 30, pobyt na jednotce intenzivní péče < 5 dnů, transaminázy nepřesahující 4násobek normální hodnoty nebo klesající, čas odběru orgánů < 30 minut, první WIT ≤ 30 minut, jaterní steatóza < 10 % a cílová doba studené ischemie (CIT – cold ischemia time) < 8 hodin (29, 30). Štěpy od DCD nesplňující tato kritéria jsou považovány za štěpy s rozšířenými kritérii a mohou být užity omezeně s ohledem na přínos pro příjemce.
V případě neřízených DCD je kontraindikací transplantace jater: doba bez cirkulace > 15 minut, doba mezi zástavou cirkulace a zahájením perfuze > 150 minut, neúspěšná implementace NRP, stoupající koncentrace transamináz během NRP (nad 4násobek normálních hodnot), špatný makroskopický vzhled jater a chudá vaskularizace žlučovodu (31).
Plíce
Pro transplantaci plic od DCD jsou kladeny stejné požadavky jako na dárce s rozšířenými kritérii: věk dárce < 65 let, kouření < 20 balení ročně, rtg hrudníku bez patologie, mechanická ventilace ≤ 4 dny, krevní převod < 5 transfuzních jednotek erytrocytů a parciální tlak kyslíku > 40 kPa (22). Navíc čas mezi WLST a zástavou oběhu nemá přesahovat 90 minut a první období teplé ischemie má být kratší než 60 minut. Pro transplantaci plic od neřízených DCD existují specifické požadavky (22, 32).
VÝSLEDKY
Transplantace ledvin
Transplantace ledvin od DCD je spojena s významně vyšší incidencí PNF a DGF ve srovnání s DBD (1–22 % a 28–88 % vs. 1–10 % a 13–35 %) (33–36). Ačkoli většina prací ukazuje, že vyšší výskyt DGF po transplantaci ledvin – na rozdíl od transplantace ledviny od DBD – neovlivňuje přežití štěpu, aktuální studie výsledků párovaných ledvin od DCD ukázala, že celková ztráta štěpů během 3 let byla významně vyšší u ledvin s DGF ve srovnání s ledvinami s bezprostředním nástupem funkce (14 vs. 4 %, poměr rizik 4,31) (33–37).
Na druhé straně podle databáze Spojeného království 5 - a 10leté přežití štěpu u příjemců ledvin od DCD dosahuje 86 a 75 %, u ledvin od DBD se hodnoty prakticky neliší (85 a 74 %) (střední doba sledování 7,5 roku) (38). Adjustované hodnoty 5letého přežití se mezi ledvinami od DCD a DBD nelišily. Rozdíly také neexistují mezi výsledky transplantace ledvin od DCD kategorie II a III (35).
Transplantace pankreatu
Dva aktuální systematické přehledy s metaanalýzou ukázaly srovnatelná přežití nemocných a pankreatických štěpů od DCD a DBD (39, 40). Roční přežití se nelišilo mezi simultánní transplantací pankreatu a ledviny a transplantací samotného pankreatu ani v případě DCD, ani DBD (87,2 % vs. 86,5 % a 76,6 % vs. 74,9 %). Podobně nebyly zjištěny žádné rozdíly mezi 3letým a 10letým přežitím pankreatického štěpu u DCD a DBD. Nicméně výskyt trombózy byl významně vyšší u DCD štěpů (9,2 %) než u štěpů od DBD (5,2 %). Hodnoty glykovaného hemoglobinu se po 1 roce od transplantace u DCD a DBD nelišily (54,3 mmol/mol vs. 56,3 mmol/mol).
Transplantace jater
V zemích s vysokým zastoupením DCD představují transplantace jater od DCD 1–21 % všech jaterních transplantací od zemřelých dárců (25). DCD je sám o sobě rizikovým faktorem pro přežití jaterního štěpu a byl zařazeno do indexu dárcovského rizika jak v USA, tak v Evropě (41, 42). Aktuální práce z regionu Eurotransplantu uvádějí riziko selhání štěpu od DCD o 70 % větší než u jater od DBD (43).
Vyšší riziko selhání štěpu od DCD je z větší části způsobeno vysokou pravděpodobností vývoje biliárních komplikací, zejména neanastomotických striktur (NAS, také označované jako ischemická cholangiopatie nebo biliární poškození ischemického typu) (44). V metaanalýze kolísal výskyt neanastomotických striktur od 3 do 39 % a zůstává hlavní příčinou retransplantace od DCD (45–47). Ovšem incidence NAS klesá po zavedení přísného výběru dárců s ohledem na první WIT, délku agonální fáze stejně jako zavedení perfuzních technik typu NRP nebo přístrojové perfuze.
Přestože většina studií uvádí, že přežití nemocných je kratší (ale ne významně) nebo stejné v případě DCD ve srovnání s DBD a pohybuje se v rozmezí 74–92 % u DCD kategorie III, analýza The Scientific Registry of Transplant Recipients ukazuje, že 1leté a 3leté dožití dosahovalo 82 a 71 % pro DCD ve srovnání s 86 a 77 % příjemců štěpů od DBD (44, 46, 47, 49, 50).
Přežití štěpů od DCD je většinou kratší než od DBD a kolísá mezi 69 a 86 % v jednom roce a 63 a 78 % po 3 letech, což bylo potvrzeno i současnou metaanalýzou, podle níž bylo 1leté a 3leté přežití štěpů od DCD méně časté než štěpů od DBD (45). Na druhou stranu dnešní pečlivý výběr dárců zlepšuje krátkodobé i dlouhodobé výsledky transplantací jater od DCD (51, 52).
Výsledky transplantací jater od neřízených DCD mohou být srovnatelné s výsledky od řízených DCD, pokud je proveden důsledný výběr dárců (31).
Transplantace plic
Podobně jako v případě jiných orgánů byly první pokusy s transplantací plic od DCD vyvolány nedostatkem orgánů od DBD (53, 54). První krátkodobé výsledky byly povzbuzující, takže v zemích, kde se provádí DCD odběry, jsou dnes transplantace plic od DCD z kategorie III široce akceptovány (55, 56).
Aktuální systematický přehled a metaanalýza ukázaly, že mezi DCD a DBD nejsou významné rozdíly v ročním přežití po transplantaci plic (68–94 % pro DCD) (57). Nebyly také prokázány rozdíly mezi DCD a DBD v primární dysfunkci štěpu (4–6 % pro DCD, 6–11 % pro DBD), incidenci akutní buněčné rejekce (6–63 % pro DCD, 3–46 % pro DBD), komplikacích týkajících se dýchacích cest ani ve výskytu syndromu obliterující bronchiolitidy.
Za povšimnutí stojí, že ve 4 ze 6 metaanalýz zahrnujících údaje o 3 - a 5leté mortalitě vyšly lépe transplantace od DCD, pro které tyto hodnoty dosahovaly 74–90 % a 71–90 %, zatímco v případě DBD 73–83 % a 61–84 %. Údaje z registru DCD Mezinárodní společnosti pro transplantace srdce a plic (ISHLT) svědčí pro podobné výsledky bez významných rozdílů mezi DCD a DBD (89 a 61 % vs. 88 a 61 %) (58).
Transplantace srdce
První transplantace lidského srdce v roce 1967 byla provedena od DCD, ale po zavedení DBD byly transplantace od dárců po zástavě oběhu většinou opuštěny (59). V důsledku vysoké úmrtnosti dětí na čekací listině byl koncept transplantací srdce od DCD úspěšně zaveden v Denveru v roce 2008 (60). To také bylo jedním z důvodů změny terminologie od „dárce s nebijícím srdcem“ a později „darování po kardiální smrti“ na současný termín „darování po selhání oběhu“, neboť samotné srdce mrtvé není.
V současnosti se setkáváme s dvěma přístupy k darování srdce od DCD: přímý odběr s následnou perfuzí ex situ nebo rychlá normotermní perfuze následovaná ex situ perfuzí (61, 62). První výsledky transplantací srdce od DCD jsou slibné, s ročním přežíváním od 75 do 100 % (62).
NOVÉ STRATEGIE TÝKAJÍCÍ SE DCD
Ex situ přístrojová perfuze
Dvě kontrolované randomizované studie, srovnávající statické skladování a hypotermní přístrojovou perfuzi (HMP) ledvin od DCD neprokázaly rozdíl v ročním přežívání nemocných a štěpů, ale většina studií či metaanalýz ukazuje nižší incidenci DGF perfundovaných ledvin od DCD oproti ledvinám od DCD uchovávaným v chladu (63–65). V mnoha centrech se HPM ledvin od DCD stala součástí běžné klinické praxe pro lepší krátkodobé výsledky, ačkoli střednědobé a dlouhodobé účinky přístrojové perfuze jsou podle čerstvých metaanalýz méně jasné (66).
Ex vivo normotermní přístrojová perfuze (NMP) používá okysličenou krev o teplotě 37 °C, čímž napodobuje prostředí in vivo umožňující resuscitaci dárcovských orgánů, klinické posouzení a biochemické vyšetření funkce orgánu.
Hosgood a Nicholson publikovali první transplantaci ledviny za použití NMP v roce 2011 a o 2 roky později výsledky své první klinické studie srovnávající NPM s chladným skladováním ledvin od dárců s rozšířenými kritérii, ve které doložili významně nižší výskyt DGF v NMP ledvinách (67–68).
Guarrera et al. publikovali povzbuzující výsledky hypotermní přístrojové perfuze u jaterních štěpů od dárců s rozšířenými kritérii (69). Jiná pracovní skupina z Curychu použila hypotermní okysličenou perfuzi (HOPE) u jater od DCD s vynikajícími výsledky (70). Mezinárodní případová analýza jaterních transplantátů od DCD hodnotící biliární komplikace včetně NAS, ročního přežití štěpu a menšího jaterního poškození ukázala lepší výsledky pro HOPE než pro statické uchování v chladu (71). Předběžné výsledky použití NMP u jaterních štěpů s rozšířenými kritérii vč. DCD jsou velmi slibné a potvrzují, že tato technika je proveditelná a dobře snášená (72). První klinická studie NMP při transplantacích jater včetně 4 štěpů od DCD doložila 100% půlroční přežití s 15% časnou dysfunkcí allogenního štěpu (73). Jiná práce ukázala skvělé výsledky použití NMP při transplantaci jater od DCD, která byla jinými centry odmítnuta (74).
Podobně jako u ledvin a jater hraje ex situ perfuze plic důležitou úlohu při transplantaci od DCD, zvláště při posuzování nejistých štěpů (75).
Normotermní regionální perfuze (NRP)
Johnson et al. popsali v roce 1997 použití extrakorporální membránové oxygenace (ECMO) při dárcovství orgánů (76). NRP umožňuje obnovu oběhu okysličenou krví dárce in situ a byla dále rozvinuta ve Španělsku pro neřízené DCD (19). Výsledky transplantací ledvin, jater a plic za použití NRP jsou v kategorii II DCD srovnatelné s výsledky od řízených DCD (77).
NRP byla také zavedena do DCD kategorie III, protože dovoluje dynamické posouzení funkce orgánu ještě před transplantací, a může tedy pomoci lepšímu výběru orgánů vhodných pro transplantaci (20, 78, 79). Aktuálně bylo publikováno rovněž použití NRP v kombinaci s HMP u transplantací jater od DCD (80).
U transplantací srdce od DCD představuje přístrojová perfuze jedinou reálnou možnost pro řádné funkční zhodnocení dárcovského srdce (61, 81).
ZÁVĚR
Dárci po selhání oběhu jsou cenným zdrojem orgánů pro transplantace. Ačkoli DCD patří k dárcům s rozšířenými kritérii, důkladný výběr orgánů získaných od DCD podle současných doporučení pomáhá dosáhnout podobných výsledků jako v případě DBD. Nové technologie jako MP či NRP umožňují lepší výběr orgánů a lepší uchování, což vede k dalšímu zvýšení míry odběru orgánů od DCD.
přeložil MUDr. Petr Sucharda, CSc.
Seznam použitých zkratek:
CIT trvání studené ischemie
DBD dárce po smrti mozku
DCD dárce po selhání oběhu
DGF opožděná funkce štěpu
HMP hypotermní přístrojová perfuze
HOPE hypotermní okysličená perfuze
MP přístrojová perfuze
NAS neanastomotická striktura žlučových cest
NMP normotermní přístrojová perfuze
NRP normotermní regionální perfuze
PNF primární afunkce
WIT trvání teplé ischemie
WLST ukončení život udržující kardiorespirační podpory
Adresa pro korespondenci:
Dr. Wojciech Polak MD, PhD, FEBS
P. O. Box 2040
3000 CA Rotterdam
the Netherlands
e-mail: w.polak@erasmusmc.nl
Zdroje
Literatura je uvedena u anglického originálu článku.
Štítky
Adiktologie Alergologie a imunologie Anesteziologie a resuscitace Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská dermatologie Dětská gastroenterologie Dětská gynekologie Dětská chirurgie Dětská kardiologie Dětská nefrologie Dětská neurologie Dětská onkologie Dětská otorinolaryngologie Dětská pneumologie Dětská psychiatrie Dětská radiologie Dětská revmatologie Dětská urologie Diabetologie Endokrinologie Farmacie Farmakologie Fyzioterapie Gastroenterologie a hepatologie Genetika Geriatrie a gerontologie Gynekologie a porodnictví Hematologie a transfuzní lékařství Hygiena a epidemiologie Hyperbarická medicína Chirurgie cévní Chirurgie hrudní Chirurgie plastická Chirurgie všeobecná Infekční lékařství Intenzivní medicína Kardiochirurgie Kardiologie Logopedie Mikrobiologie Nefrologie Neonatologie Neurochirurgie Neurologie Nukleární medicína Nutriční terapeut Obezitologie Oftalmologie Onkologie Ortodoncie Ortopedie Otorinolaryngologie Patologie Pediatrie Pneumologie a ftizeologie Popáleninová medicína Posudkové lékařství Praktické lékařství pro děti a dorost Protetika Psychologie Radiodiagnostika Radioterapie Rehabilitační a fyzikální medicína Reprodukční medicína Revmatologie Sestra Sexuologie Soudní lékařství Stomatologie Tělovýchovné lékařství Toxikologie Traumatologie Urgentní medicína Urologie Laboratoř Domácí péče Foniatrie Algeziologie Zdravotnictví Dentální hygienistka Student medicíny
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
- Psilocybin je v Česku od 1. ledna 2026 schválený. Co to znamená v praxi?
- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
-
Všechny články tohoto čísla
- Úvodem
- Editorial
- Transplantace tenkého střeva v České republice
- Indikace k transplantaci jater – kdy odeslat nemocného
- Klady a rizika duální transplantace ledvin
- Orgánové transplantace od dárců se selháním oběhu
- Psychologické hodnocení účastníků studie transplantace dělohy
- Psychologická problematika pacientů přeživších mimonemocniční srdeční zástavu
- Makrodiagnostické trendy současné soudnělékařské praxe v České republice
- Metodický pokyn Ministerstva zdravotnictví ČR o duchovní péči
-
Mezinárodní kongres Global Biobank Week 2017
K harmonii v biobankách - John Vane (1927–2004)
- 65 let brigádního generála v. v. doc. MUDr. Leo Kleina, CSc.
- Vzpomínka na prof. MUDr. Jaromíra Koláře, DrSc.
- 100 let od narození profesora Adolfa Žáčka
- Zemřel profesor Ivo Hána
- PŘEDNÁŠKOVÉ VEČERY SPOLKU ČESKÝCH LÉKAŘŮ V PRAZE (LEDEN – ÚNOR 2018)
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Indikace k transplantaci jater – kdy odeslat nemocného
- Transplantace tenkého střeva v České republice
- Orgánové transplantace od dárců se selháním oběhu
- Psychologická problematika pacientů přeživších mimonemocniční srdeční zástavu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



