-
Medical journals
- Career
Diferenciální diagnostika trombocytopenie u kriticky nemocných pacientů
Authors: J. Gumulec 1; R. Kula 2; O. Šimetka 3; L. Pleva 4; J. Ullrychová 5
Authors‘ workplace: Ústav klinické hematologie FN Ostrava, přednosta prim. MUDr. Jaromír Gumulec 1; Anesteziologicko‑resuscitační klinika FN Ostrava, přednosta prim. MUDr. Jan Jahoda 2; Porodnicko‑gynekologická klinika FN Ostrava, přednosta prim. MUDr. Ondřej Šimetka 3; Traumatologické centrum FN Ostrava, přednosta prim. doc. MUDr. Leopold Pleva, CSc. 4; Oddělení laboratoří a transfuzní služby Nemocnice Děčín, o. z., přednostka prim. MUDr. Jana Ullrychová 5
Published in: Vnitř Lék 2010; 56(Supplementum 1): 14-26
Category: 16th Parizek's Days, Ostrava-Poruba, March 25th –26th 2010
Overview
U mnohých kriticky nemocných pacientů se rozvinou poruchy hemostázy počínaje izolovanou trombocytopenií a komplexními defekty typu diseminované intravaskulární koagulace konče. Nově vzniklá trombocytopenie a multiorgánové selhání předikuje špatný výsledek. Pokles destiček u kriticky nemocného člověka má mnoho různých příčin a každá z nich může vyžadovat specifický typ léčebné a podpůrné péče. V posledních letech se mění pohled na patogenezi a klinický přístup k řešení mnohých poruch hemostázy kriticky nemocných pacientů. Nové poznatky pomáhají určit optimální diagnostickou a diferenciálně diagnostickou strategii.
Klíčová slova:
trombocytopenie – šok – sepse – diseminovaná intravaskulární koagulace – polékové trombocytopenie – imunitní trombocytopenie – jednotka intenzivní péčeÚvod
Trombocytopenie nebo pokles počtu krevních destiček během hospitalizace kriticky nemocných pacientů představuje:
- riziko delšího pobytu na jednotce intenzivní péče (JIP),
- prolongovanou závislost na umělé plicní ventilaci,
- vyšší incidenci hemoragických komplikací,
- větší závislost na transfuzích a
- vyšší mortalitu během hospitalizace [1–7].
Incidence případů s poklesem počtu krevních destiček pod 150 × 109/l se pohybuje mezi 41 a 46 %, pod 100 × 109/l mezi 20 a 25 % a pod 50 × 109/l ve 2–17 % [1–3,6,8,9]. U chirurgických a traumatologických pacientů je etiologie a dynamika poklesu počtu krevních destiček jiná a častěji klesne počet trombocytů pod hodnotu 100 × 109/l (až ve 35–41 % případů) [1,8].
Počet destiček typicky klesá během prvních 3–4 dnů hospitalizace na JIP [4,7], přičemž změny počtu destiček v čase mají větší význam pro další prognózu pacienta než tíže trombocytopenie [2,7,10]. Horší prognózu mají pacienti:
- u kterých se nadir počtu destiček objevil 4. den a později,
- u kterých se pokles počtu destiček začal upravovat nejdříve 6. den hospitalizace a
- u kterých byl pokles více než 30–50 % vstupní hodnoty (často bez trombocytopenie) [2,3,7,11].
Hloubka trombocytopenie pochopitelně ovlivňuje riziko hemoragických komplikací. U kriticky nemocných pacientů s počtem destiček pod 100 × 109/l je riziko krvácení 10krát vyšší než u pacientů s počtem destiček mezi 100 a 150 × 109/l [2]. Při dalším poklesu riziko krvácení narůstá, zvlášť významně u pacientů s počtem destiček pod 50 × 109/l [2,3,9,12]. Počet destiček pod 10 × 109/l je vzhledem k riziku spontánního krvácení důvodem pro profylaktickou transfuzi koncentrátu destiček [13–19]. Přítomnost přídatných rizikových faktorů, jako je sepse (zvláště u pacientů s těžkou sepsí léčených aktivovaným proteinem C a počtem destiček pod 30 × 109/l), trauma (pacient s poklesem počtu destiček pod 50 × 109/l), jiné poruchy hemostázy (např. diseminovaná intravaskulární koagulace), hyperleukocytóza (zvláště v době indukční terapie akutní promyelocytární leukemie nutno udržovat počet destiček v rozmezí 30–50 × 109/l), rychlý pokles počtu destiček, invazivní zákrok, zavedená antitrombotická léčba apod. může být důvodem k profylaktické transfuzi trombocytů i při vyšším počtu destiček [12,15–18,20,21].
Z uvedeného vyplývá, že interpretace poklesu počtu krevních destiček nemá být omezována jen s ohledem na riziko krvácivých komplikací a že pro odhad prognózy pacienta je třeba posuzovat dynamiku změn počtu destiček, i když není v trombocytopenických hodnotách [7].
Pokles destiček u kriticky nemocného člověka má mnoho různých příčin, které se velmi často kombinují. V tab. 1 jsou seřazeny podle etiopatogeneze. Každá z nich může vyžadovat specifický typ léčebné a podpůrné péče. Nejvýznamnější příčiny trombocytopenie u kriticky nemocných a četnost jejich výskytu jsou uvedeny v tab. 2. Přehledný článek shrnuje základní pravidla diagnostiky a diferenciální diagnostiky nejčastějších nebo z prognostického hlediska nejvýznamnějších typů trombocytopenie pacientů hospitalizovaných na JIP.
Table 1. Nejčastější trombocytopenie na JIP podle mechanizmu vzniku [38,41]. ![Nejčastější trombocytopenie na JIP podle mechanizmu vzniku [38,41].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/4b8531160c65f06a7f36590cc03b50e9.jpg)
*HELLP syndrom – Hemolysis, Elevated Liver enzymes, Low Platelets syndrome Table 2. Nejvýznamnější příčiny trombocytopenie u kriticky nemocných. 
Časná koagulopatie po traumatu
Koagulopatie u traumatu je multifaktoriální a klíčovými iniciátory jsou:
- poškození tkání,
- šok,
- hemodiluce,
- hypotermie,
- acidóza a
- systémová zánětlivá reakce (22).
Šok je primární hnací kolo časných potraumatických poruch hemostázy. Tíže tkáňové hypoperfuze přímo úměrně prohlubuje vzniklou koagulopatii [23,24]. Přes pravidelně vznikající prodloužení protrombinového testu (PT) a aktivovaného parciálního tromboplastinového času (APTT) časně po traumatu, ještě před hemodilucí, nedochází k významnému poklesu počtu destiček [23,25,26]. Trombocytopenie se po traumatu objevuje teprve vlivem hemodiluce a konzumpce [27–29]. Hemodiluce je navozena přesunem tekutiny z buněk a intersticia do plazmy a dále potencovaná objemovou resuscitací krystaloidy, koloidy a transfuzí erytrocytárních přípravků, resp. plazmy bez současného/dostatečného převodu destiček [27,28,30]. Není li tomu komplexní péčí zabráněno, poruchu hemostázy u pacienta s potraumatickou koagulopatií a trombocytopenií dále prohlubuje těžká hypotermie a acidóza [31,32] a později systémová zánětlivá odpověď organizmu na trauma [22].
Podle Hesse et al je koagulopatie vznikající velmi časně po těžkém traumatu výsledkem vystupňované aktivity iniciační fáze plazmatické koagulace. Trauma způsobí mnohočetné poškození endotelu s časnou aktivací faktorů X, II, V a VIII. Hypoperfuze tkání navozená hemoragickým šokem brání odstraňovaní nahromaděného trombinu (F IIa) a vede ke zvýšení jeho vazby na trombomodulin. Takto vzniklý komplex trombin trombomodulin aktivuje protein C, který působí antikoagulačně (inaktivuje faktory Va a VIIIa) a profibrinolyticky (tlumí inhibitor aktivátoru plazminogenu 1). Laboratorně se tato koagulopatie projevuje zřetelným a velmi časně vzniklým prodloužením PT a APTT s nepatrnými změnami počtu destiček a koncentrace fibrinogenu. V této fázi reakce organizmu na trauma nejde o diseminovanou intravaskulární koagulaci (DIC) [22,23]. DIC se v akutní podobě po traumatu objevuje, když mozková tkáň, tuk, plodová voda nebo jiný silný tromboplastin vstoupí do cirkulace. V subakutní podobě se rozvíjí jako následek poškození endotelu s aktivací koagulace, se vznikem trombotického poškození mikrocirkulace a s akcelerací konzumpce [29]. Tyto skutečnosti je třeba respektovat při volbě optimální léčebné strategie.
Sepse
U sepse dochází pravidelně k aktivaci koagulačních faktorů a destiček. Zatímco v iniciální fázi sepse bylo popsáno izolované snížení aktivity F XII, u těžké sepse a především u septického šoku klesá aktivita většiny koagulačních faktorů (manifestovaná prodloužením PT a APTT) a rozvíjí se i trombocytopenie [1,34]. Příčinou poklesu počtu destiček u sepse je:
- zvýšená konzumpce při rozvinuté diseminované intravaskulární koagulaci,
- hemodiluce jako následek tekutinové resuscitace v případě septického šoku,
- snížená produkce v kostní dřeni s častým podílem hemofagocytózy,
- destrukce destiček protilátkovým mechanizmem,
- poléková trombocytopenie, případně
- vystupňovaná sekvestrace destiček ve slezině (u pacientů s portální hypertenzí nebo splenomegalií), resp.
- pseudotrombocytopenie (viz níže) [1,35–41].
Diagnostická kritéria syndromu systémové zánětlivé odpovědi, sepse, těžké sepse, septického šoku a syndromu multiorgánové dysfunkce [42]
Syndrom systémové zánětlivé odpovědi (SIRS)
SIRS je soubor příznaků univerzální reakce organizmu na inzulty infekčního i neinfekčního charakteru. Za SIRS je považován stav, který se projevuje nejméně 2 následujícími příznaky:
- teplotou nad 38 °C nebo pod 36 °C,
- srdeční frekvencí nad 90/min,
- dechovou frekvencí nad 20/min nebo PaCO2 nad 32 mm Hg a
- počtem leukocytů nad 12 × 109/l nebo pod 4 × 109/l nebo více než 10 % nezralých neutrofilů.
Sepse
Sepse je systémová zánětlivá odpověď v důsledku potvrzeného infekčního procesu, tzn. nejméně 2 kritéria SIRS + přítomnost infekce (známky infekce jsou přítomnost mikroorganizmu v normálně sterilní tkáni).
Těžká sepse
Těžká sepse je sepse spojená s orgánovou dysfunkcí, hypoperfuzí tkání nebo hypotenzí.
Septický šok
Septický šok je případ těžké sepse s hypotenzí, která nereaguje na adekvátní tekutinovou resuscitaci a u níž jsou přítomny známky hypoperfuze (oligurie, laktátová acidóza, alterace mentálního stavu). Při léčbě vazopresory nemusí být aktuálně hypotenze, ale při přítomnosti známek hypoperfuze je i takový stav považován za septický šok.
Syndrom multiorgánové dysfunkce (MODS)
MODS je stav s poruchou funkce orgánu u kriticky nemocného pacienta, kdy porucha funkce je takového rozsahu, že homeostáza nemůže být zajištěna bez zevní intervence.
Diseminovaná intravaskulární koagulace
DIC je klinicko patologický syndrom komplikující řadu onemocnění (tab. 3) [33,43]. Jde o systémovou intravaskulární aktivaci koagulace, která může vést ke vzniku fibrinových sraženin v mikrocirkulaci různých orgánů. Poruchy mikrocirkulace způsobí ischemii postižených tkání vedoucí k multiorgánovému selhání a konzumpce destiček a koagulačních faktorů v mnohočetných mikrotrombech k hypokoagulaci manifestované krvácením.
Table 3. Onemocnění a stavy spouštějící DIC [33,43]. ![Onemocnění a stavy spouštějící DIC [33,43].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/0131424eb208a7fbb8e5840a82c94d34.jpg)
Klinický obraz
DIC se chová jako trombohemoragický syndrom s dynamicky se měnícím obrazem. Klasická, akutní DIC vzniklá např. v porodnictví má prudký průběh a projevuje se primárně krvácením (64–75 %), chronická DIC provázející často chronická nádorová onemocnění mívá převážně trombotické komplikace (7–23 %) [44,45].
Laboratorní obraz
Pro laboratorní diagnostiku DIC je vzhledem k dynamické a heterogenní povaze tohoto syndromu nezbytné u onemocnění a stavů s potenciálem rozvoje DIC indikovat opakované vyšetřování celého souboru testů (krevní obraz, PT, APTT, fibrinogen, D-dimery) [43]. Současné monitorování aktivity antitrombinu a proteinu C má prognostický význam [46–49]. Nejčastější odchylkou je pokles počtu destiček [44,45, 50–52].
Počet destiček
Trombocytopenie a/nebo jasný trend k poklesu počtu destiček je senzitivní, ale nespecifický projev DIC [52]. Trombinem indukovaná agregace destiček je hlavní příčinou jejich spotřeby v mnohočetných mikrotrombech, a proto lze podle hloubky poklesu počtu destiček usuzovat na intenzitu generace trombinu, tj. na dynamiku DIC [4,53,54]. V praxi to znamená, že pokračující pokles počtu destiček, byť v referenčním rozmezí, může být indikátorem aktivní generace trombinu – aktivní DIC, resp. že stabilizace počtu destiček upozorňuje na zastavení novotvorby trombinu – zastavení spotřeby destiček [43].
Skórovací systémy
Pro diagnostiku rozvinuté DIC se doporučuje používat skórovací systémy mezinárodní společnosti pro trombózu a hemostázu (ISTH) [43,55,56] nebo japonského ministerstva pro zdravotnictví a prosperitu (JMHW) [52] (tab. 4). Skórovací systémy nejsou dostatečně senzitivní pro doposud nerozvinutou DIC, přitom právě časná identifikace nerozvinuté DIC může zlepšit výsledky péče o kriticky nemocné. ISTH proto navrhuje v těchto případech používat skórovací systém pro nerozvinutou DIC s vědomím skutečnosti, že validace tohoto přístupu není zatím ukončena (tab. 5) [49,55]. Skórovací systém Japonské společnosti pro akutní medicínu (JAAM) se zdá být citlivější než systém ISTH [57–61].
Table 4. Skórovací systémy pro diagnostiku rozvinuté DIC [52,55]. ![Skórovací systémy pro diagnostiku rozvinuté DIC [52,55].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/d64e266234f56a9240f3988e6f542af4.jpg)
Table 5. Skórovací systém pro diagnostiku nerozvinuté DIC [49,55]. ![Skórovací systém pro diagnostiku nerozvinuté DIC [49,55].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/1c50a1f8be26c020aba157109b64547e.jpg)
Pseudotrombocytopenie
Pseudotrombocytopenie je falešně nízký počet krevních destiček stanovený in vitro, který neodpovídá skutečnému počtu destiček cirkulujících v krvi. Příčinou je shlukování destiček v odběrové zkumavce kvůli:
- protilátkám závislým na ethylenediaminetetraoctové kyselině (EDTA, častěji u pacientů s těžkou sepsí, autoimunitním nebo jaterním onemocněním) [35] nebo,
- nedostatečné antikoagulaci [41].
Hematologické analyzátory nemusí takto vzniklé shluky destiček rozpoznat, u některých vzorků zařazují jednotlivé shluky mezi červené krvinky nebo leukocyty a vydávají výsledek s falešně nízkým počtem trombocytů. Moderní analyzátory na přítomnost shluků destiček upozorňují [35,62,63]. V klinické praxi lze na pseudotrombocytopenii usuzovat v situacích, kdy klinický obraz neodpovídá výsledku vyšetření počtu destiček. Snadno lze shluky destiček prokázat prohlédnutím nátěru periferní krve v mikroskopu. Přesný počet destiček lze zpravidla určit vyšetřením nového vzorku krve odebraným do zkumavky s alternativním protisrážlivým roztokem – heparinem nebo citrátem (díky většímu objemu citrátu než EDTA dojde k naředění počtu destiček, a proto je nutné naměřený počet destiček vynásobit indexem 1,1) [64].
Poléková trombocytopenie
Přestože jsou léky častou příčinou akutní, imunitně podmíněné trombocytopenie dospělých pacientů, poléková etiologie nebývá v době diagnózy často správně rozpoznána. Na JIP bývá poléková trombocytopenie přehlédnuta, protože se zpravidla vyvíjí až 1–2 týdny po zahájení farmakoterapie, protože nemá specifické klinické projevy a protože u kriticky nemocných je mnoho dalších důvodů pro rozvoj trombocytopenie [65–67]. Správná diagnóza je při tom velmi užitečná, protože problém může být vyřešen jednoduchým ukončením podávání léku a recidivě může být zabráněno vyvarováním se opakovaného podávání léčiva [41,67].
Většina případů polékové trombocytopenie je zapříčiněna na léku závislými protilátkami, které těsně korespondují se strukturou léku a za jeho přítomnosti se pevně svou F(ab) doménou vážou na glykoproteiny destičkové membrány [65,66]. Typicky se polékové trombocytopenie objevují 1–2 týdny po zahájení léčby novým lékem nebo náhle po jednotlivé dávce léku, který byl v minulosti podáván intermitentně. Těžká trombocytopenie se může objevit bezprostředně po prvním podání antitrombotik blokujících vazbu fibrinogenu na destičkový glykoproteinový komplex IIb/IIIa (GP IIb/IIIa), jako jsou abciximab, tirofiban a eptifibatid. Počet destiček se začne upravovat obvykle 1–2 dny po přerušení léčby a typicky se znormalizuje během týdne [67]. Seznam léků s rizikem rozvoje trombocytopenie obvykle používaných na JIP je uveden v tab. 6 [41] a neustále aktualizovaná databáze léků s potenciálem rozvoje polékové trombocytopenie je k dispozici na www.ouhsc.edu/platelets [67].
Table 6. Necytostatická léčiva s rizikem rozvoje trombocytopenie používaná rutinně na JIP [41]. ![Necytostatická léčiva s rizikem rozvoje trombocytopenie používaná rutinně na JIP [41].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/860b17cbde3e5d33c87e94bcd0e72fa5.jpg)
Heparinem indukovaná trombocytopenie (HIT)
HIT je klinicko patologický syndrom, který se obvykle projevuje:
- jinak nevysvětleným poklesem počtu destiček o více než 50 % (vzhledem k hodnotě před podáním heparinu, přitom nadir počtu destiček nemusí být pod hodnotou 150 × 109/l) během 2. týdne léčby heparinem,
- převážně žilní, ale i tepennou trombózou,
- kožní lézí v místě s.c. aplikace heparinů nebo
- akutní anafylaktoidní reakcí (horečka, svědění, tachykardie, hypertenze, dušnost, srdeční zástava apod.) po i.v. bolusu heparinu [68,69].
Jde o protilátkami navozený nežádoucí účinek heparinu. Nejvýznamnějším antigenem je na destičkách lokalizovaný komplex destičkového faktoru 4 (PF4) s heparinem. Výsledkem je nekontrolovaná aktivace a agregace destiček s intravaskulárním uvolňováním prokoagulačních mikropartikulí, které akcelerují generaci trombinu. Trombocytopenie tedy není navozena imunitně podmíněnou fagocytózou retikuloendotelem, ale intravaskulární konzumpcí. Hloubka trombocytopenie koreluje s rizikem trombotických komplikací [70].
Laboratorní testování spočívá:
- v detekci protilátek vážících komplex PF4/heparin a
- v průkazu na heparinu závislé aktivace destiček sérem pacienta.
Klasické aktivační testy jsou serotonin release assay (SRA) a heparinem indukovaná aktivace destiček (HIPA) používající proprané trombocyty. Citlivost těchto testů je stejně jako citlivost polyspecificých imunologických testů (IgG/A/M) a IgG specifických enzymo imunoesejí (EIA) vysoká až 99 %, a proto mohou být tyto testy používány k vyloučení HIT (vysoká negativní prediktivní hodnota). Poměr senzitivita/specificita je nejvyšší u funkčních testů (specificita funkčních testů používajících proprané destičky je 95–99 %, polyspecifických IgG/A/M jen 50–75 % a IgG EIA 55–90 %) [71].
Pro diagnózu je nutné stanovení pravděpodobnosti HIT podle klinických projevů (4T skóre) [72] a průkaz protilátek aktivujících destičky (funkční HIT testy) nebo silnou pozitivitu imunologických testů [73].
Diagnostický algoritmus:
- Stanovení pravděpodobnosti HIT s pomocí 4T skóre (tab. 7). Pacient s nízkou pravděpodobností (skóre ≤ 3) nevyžaduje další testování a léčba heparinem může pokračovat.
- Je-li EIA negativní, HIT je velmi nepravděpodobná a léčba heparinem může pokračovat. Pozitivní výsledek screeningu EIA upozorňuje na přítomnost anti-PF4/heparin protilátek. Je-li IgG EIA slabě pozitivní (OD < 1,0), protilátky pravděpodobně nemohou aktivovat destičky. Není li reaktivita protilátek in vitro inhibována heparinem, HIT je velmi nepravděpodobná a léčba heparinem může pokračovat.
- IgG EIA s OD > 1,0 upozorňuje na zvýšené riziko aktivace destiček protilátkami. V případě pozitivity funkčních testů s použitím séra pacienta s takovým výsledem IgG EIA je pravděpodobnost HIT velmi vysoká. Negativní funkční test pravděpodobnost HIT snižuje a léčba heparinem může pokračovat.
- Přehodnocení klinického stavu má podpořit konečnou konfirmaci HIT nebo vyloučení diagnózy [70].
Table 7. Stanovení pravděpodobnosti HIT – 4T skóre [72]. ![Stanovení pravděpodobnosti HIT – 4T skóre [72].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/4608b07b0d2a271b2c94178039b91ce2.jpg)
†Greifswald, Německo (GW): rozvoj ve dnech 5.– 14. (spíše než 5.– 10.); pokles destiček během 1. dne (při podání heparinu v posledních 100 dnech). ‡GW: vznik po 14 dnech. §Kožní nekróza v místě aplikace heparinu. #Progrese představuje objektivně dokumentovaný nárůst velikosti trombu (obvykle prodloužení hluboké trombózy podle ultrazvuku); rekurence představuje nově vzniklý tromboembolus v původně postižené oblasti (obvykle nový defekt perfuze u pacienta s předchozí plicní embolizací). **dle GW suspektní, neověřená trombóza není v diagnostických kritériích obsažena. ††Označení existence jiné příčiny trombocytopenie jako možné nebo jisté je na rozhodnutí ošetřujícího lékaře.
Profylaxe nebo léčba nízkomolekulárními hepariny může, s poněkud menší frekvencí, také vést k rozvoji HIT [74] a nově byla popsána trombocytopenie s trombózou i po léčbě fondaparinuxem [75] a eptifibatidem [76].
Imunitní trombocytopenie
Dalším mechanizmem, který pravděpodobně může u kriticky nemocných, zvláště septických pacientů, vést k trombocytopenii, je vliv destičkových protilátek (PAIgG) [1,77–79]. Problémem PAIgG je ale nedostatečná specificita, protože zvýšený titr těchto protilátek byl prokázán jak u imunitních, tak u neimunitních trombocytopenií [80,81]. Pro zvýšení specificity testování destičkových autoprotilátek při diagnostice imunitní trombocytopenie je vhodné doplnit/nahradit screeningové vyšetření destičkových protilátek PAIgG provedením specifických testů na autoprotilátky zaměřené proti epitopům lokalizovaným na destičkových glykoproteinech IIb/IIIa, Ib/IX, případně Ia/IIa [82]. Průkaz specifických destičkových protilátek je u pacientů se sekundární imunitní trombocytopenií častý (až 83 %, signifikantně častější než u idiopatické imunitní trombocytopenie, kde se objevuje jen ve 48 %) [82] a stanovení specifických protilátek u kriticky nemocných s nevyjasněnou trombocytopenií může přispět ke zpřesnění péče [83].
Trombotické mikroangiopatie
Trombotické mikroangiopatie (TMA) je skupina onemocnění definovaných poškozením endotelu s intravaskulární agregací destiček a poruchou mikrocirkulace s častým rozvojem multiorgánového selhání [84-86]. Patří sem trombotická trombocytopenická purpura (TTP), hemolyticko uremický syndrom (HUS), preeklampsie a HELLP syndrom (Haemolysis Elevated Liver enzymes, Low Platelets) [87]. Obraz trombotické mikroangiopatie mívá i katastrofický antifosfolipidový syndrom.
Trombotická trombocytopenická purpura (TTP)
TTP je vzácný syndrom, který je ale třeba velmi rychle rozpoznat a léčit, protože odklad adekvátní terapie (výměnných plazmaferéz) představuje pro pacienty významné zhoršení prognózy [88]. Pro diagnózu TTP stačí náhlý vznik těžké trombocytopenie a mikroangiopatické hemolytické anémie (hemolytická anémie se zvýšením počtu schistocytů nad 4 % a negativním přímým antiglobulinovým testem). V typických případech se objevují fluktující neurologické projevy (od bolestí hlavy přes křeče, přechodné poruchy vědomí až po koma), poruchy funkce ledvin a horečka. Klasifikace TTP je v tab. 8 [87,89]. Příčinou je porucha štěpení velkých multimerů von Willebrandova faktoru vedoucí k hyperagregaci destiček s tvorbou mikrotrombů poškozujících mikrocirkulaci predominantně mozku a ledvin. V rámci laboratorní diagnostiky lze vystačit s provedením:
- krevního obrazu (trombocytopenie, anémie, zvýšené retikulocyty a schistocyty),
- základní koagulační testy, antitrombin a D-dimery (diferenciální diagnostika konzumpční koagulopatie),
- základní biochemie (ionty, urea, kreatinin, „jaterní“ testy, laktátdehydrogenáza, celkový a konjugovaný bilirubin, haptoglobin, moč chemickya mikroskopicky) a
- přímý antiglobulinový testy (k vyloučení imunitní hemolýzy).
Table 8. Klasifikace trombotické trombocytopenické purpury [87]. ![Klasifikace trombotické trombocytopenické purpury [87].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/28668d6cc4d2d778c1399dc5b6501c15.jpg)
Zásadní je, aby diagnóza byla provedena co nejdříve a aby byla léčba výměnnými plazmaferézami nastartována již během prvních 24 hod od vzniku potíží [87,88,90].
Hemolyticko-uremický syndrom (HUS)
HUS je definován mikroangiopatickou hemolytickou anémií, trombocytopenií a renálním selháním [91]. Kromě toho mohou onemocnění provázet enterokolitida (často onemocnění uvádí), neurologické komplikace, hepatopatie, pankreatopatie nebo kardiální projevy [87]. Klasifikace hemolyticko-uremického syndromu je uvedena v tab. 9 [87]. V případě epidemické formy dochází k poškození endotelu verotoxinem (tzv. Shiga toxinem) produkovaným zpravidla Escherichia coli 0157:H7, v případě sporadické formy je u takřka 50 % případů příčinou deficit komplementového faktoru H [87,90]. Schéma diferenciální diagnostiky TMA je v tab. 10 [87].
Table 9. Klasifikace hemolyticko-uremického syndromu [87]. ![Klasifikace hemolyticko-uremického syndromu [87].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/67202aa7d7723f7e24424f676520b384.jpg)
Table 10. Diferenciální diagnostika trombotických mikroangiopatií [87]. ![Diferenciální diagnostika trombotických mikroangiopatií [87].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/0f73e3173933f4d42a6a34838cda6353.jpg)
Preeklampsie
Preeklampsie je definovaná jako hypertenze, proteinurie, často provázená orgánovou dysfunkcí, vzniklá po 20. týdnu gravidity. Zpravidla se objevuje u nulipar nebo multipar s novým partnerem [92]. Krevní tlak nad 160/110 mm Hg a/nebo proteinurie nad 5 g/den jsou projevy těžké preeklampsie [93]. Preeklampsie komplikuje 2–5 % všech těhotenství [94], je příčinou trombocytopenie u 16 % všech trombocytopenických gravidit [95], resp. trombocytopenie se vyskytuje u 50 % těhotných žen s preeklampsií [96]. Etiologie není zcela vyjasněná, hlavním patofyziologickým jevem je insuficientní trofoblastická invaze mateřských spirálních arterií, což způsobuje poruchy prokrvení fetoplacentární jednotky. To vede k sekreci faktorů do mateřské cirkulace, které způsobují aktivaci endotelových buněk a alteraci vaskulární reaktivity. Generalizovaná aktivace endotelu vede k aktivaci destiček a později i koagulační kaskády v rámci rozvíjející se DIC. Velmi pravděpodobná je rovněž účast genetických dispozic a trombofilie [96].
HELLP syndrom
HELLP syndrom se objevuje asi u 10 % žen s těžkou preeklampsií [87], obvykle ve 3. trimestru u multipar starších 25 let [96]. Diagnostická kritéria zahrnují:
- mikroangiopatickou hemolytickou anémii (v některých případech může chybět, tzv. ELLP syndrom),
- elevaci aktivity aspartátaminotransferázy (AST) nebo alaninaminotransferázy (ALT) nad 70 IU/l (1,17 µkat/l) a
- trombocytopenii pod 100 × 109/l [97].
V některých případech může hypertenze a proteinurie chybět [98], ve 21 % případů se objevuje DIC [99] a bývá velmi často spojen s intrauterinní růstovou retardací. Mezi nejčastější klinické projevy kromě přetrvávající bolesti v epigastriu a pravém podžebří patří nauzea, nevolnost, malátnost, neklid a otoky. Od trombotické trombocytopenické purpury a hemolyticko-uremického syndromu může HELLP syndrom pomoci odlišit nepřítomnost významných neurologických projevů a těžkého selhání ledvin. Schéma diferenciální diagnostiky trombotických mikroangiopatií specifických pro těhotenství je uvedeno v tab. 11 [92].
Table 11. Klinické projevy CAPS v době plné manifestace. 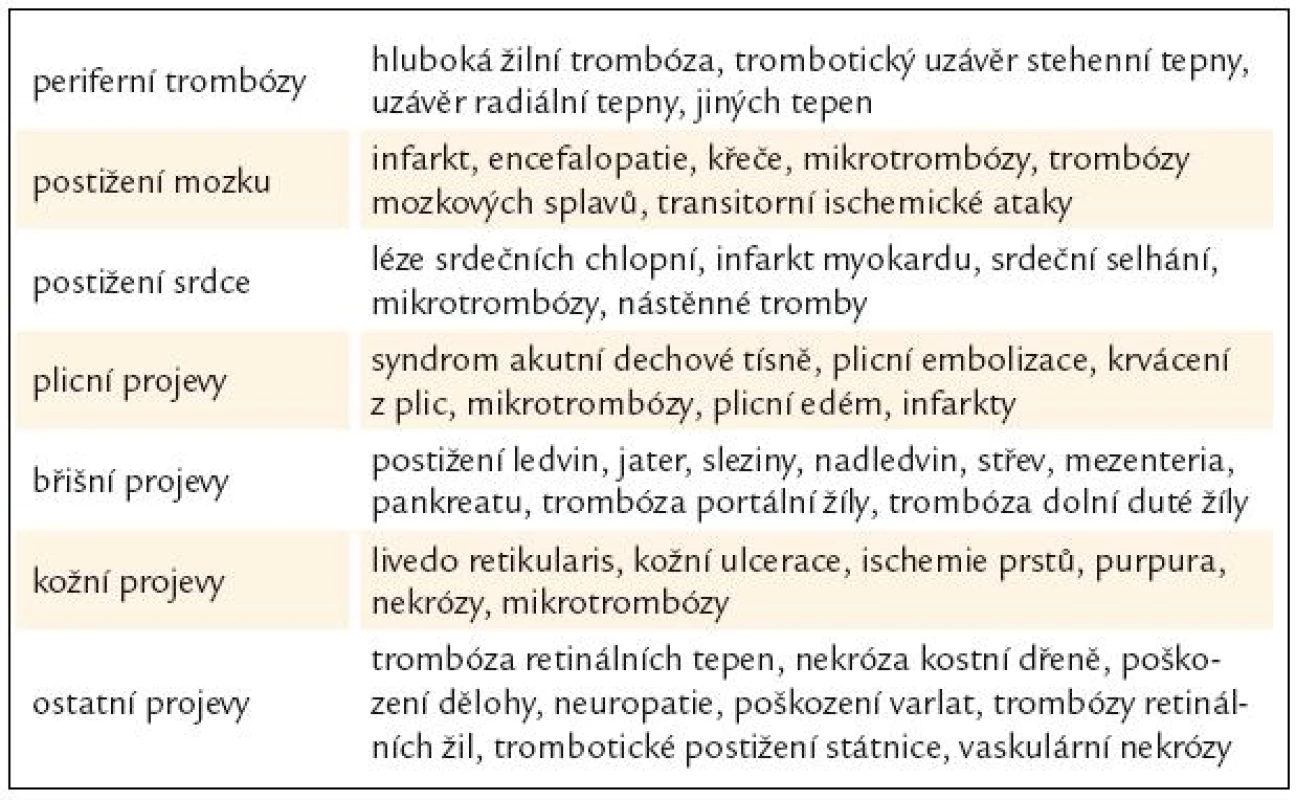
Antifosfolipidový syndrom
Antifosfolipidový syndrom je definován přetrvávající přítomností antifosfolipidových protilátek u pacientů s rekurentními žilními nebo tepennými tromboembolickými příhodami a těhotenskými komplikacemi. Trombocytopenie pod 100–150 × 109/l se objevuje u asi 20 % pacientů s APS a u 40 % případů APS provázejícího SLE [100–102], zpravidla bývá mírná v rozmezí 100–150 × 109/l [100–101], jen v menšině případů pod 50 × 109/l [100]. Trombocytopenie u těchto pacientů může být podmíněna imunitním mechanizmem jako u pacientů s ITP, současně však se nabízí, že současný výskyt trombocytopenie a trombózy u pacientů s APS je dán interakcí antifosfolipidových protilátek a destiček v podmínkách, které vedou k agregaci destiček a k trombóze [103].
Katastrofický antifosfolipidový syndrom (CAPS)
CAPS je život ohrožující stav charakterizovaný:
- mnohočetnými trombotickými cévními uzávěry postihujícími zpravidla drobné cévy s rozvojem MODS,
- velmi prudkým průběhem (zpravidla během jednoho týdne) a
- současným průkazem antifosfolipidových protilátek [104,105]. Patogeneze CAPS není zcela vyjasněná, mortalita je vysoká (kolem 50 %), může však být včasnou a účinnou léčbou (antikoagulace, kortikoidy, výměnná plazmaferéza, i.v. imunoglobuliny) snížena na 20 % [106]. Klinické projevy evidované CAPS registrem jsou uvedeny v tab. 11 [105], diagnostická kritéria v tab. 12 [104,105].
Table 12. Diagnostická kritéria CAPS [104–105]. ![Diagnostická kritéria CAPS [104–105].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/e0fd9e17d2930dcfc2a80f6ce5428299.jpg)
Na CAPS je třeba myslet u všech prudce se rozvíjejících kritických stavů s nevyjasněným prodloužením APTT, které může být navozeno přítomností antifosfolipidových protilátek. Včasné rozpoznání a zahájení léčby jednoznačně zlepšuje prognózu pacientů [106].
Diferenciální diagnostika trombocytopenie kriticky nemocných pacientů
Rychlou orientaci lze provést již na počátku hospitalizace. Předně je třeba u pacientů s laboratorním nálezem sníženého počtu destiček vyloučit pseudotrombocytopenii a poté zhodnotit všechny dostupné laboratorní výsledky s cílem definovat, kdy skutečná trombocytopenie vznikla. Jiná je etiologie trombocytopenie vzniklé před hospitalizací, jiná během ní (schéma 1). U kriticky nemocných pacientů je nutné mít na paměti, že prognosticky významný je i pokles destiček o 30–50 %, přičemž výsledná hodnota počtu destiček nemusí být v trombocytopenických hodnotách [2,3,7,11].
U kriticky nemocného pacienta je nutné opakované klinické a laboratorní monitorování (z hematologického hlediska krevního obrazu a koagulačních testů) s cílem včas identifikovat nejvýznamnější příčiny a typy trombocytopenie (schéma 2). Těsná spolupráce intenzivisty s hematologem může být nepochybně velmi užitečná.
Schéma 2. Diferenciální diagnostika trombocytopenie kriticky nemocných pacientů. 
Závěr
Pokles počtu krevních destiček je velmi častý nález u kriticky nemocných pacientů s mnohočetnými příčinami a prokázaným prognostickým významem i v situacích, kdy se absolutní počty destiček nepohybují v trombocytopenických hodnotách. Dobré výsledky péče jsou možné, jen je-li diagnosticky a terapeuticky postupováno komplexně a v některých klinických situacích dostatečně razantně.
prim. MUDr. Jaromír Gumulec
www.fnspo.cz
e-mail: jaromir.gumulec@fnspo.cz
Doručeno do redakce: 14. 4. 2010
Sources
1. Stephan F, Hollande J, Richard O et al. Thrombocytopenia in a surgical ICU. Chest 1999; 115 : 1363–1370.
2. Vanderschueren S, De Weerdt A, Malbrain M et al. Thrombocytopenia and prognosis in intensive care. Crit Care Med 2000; 28 : 1871–1876.
3. Strauss R, Wehler M, Mehler K et al. Thrombocytopenia in patients in the medical intensive care unit: bleeding prevalence, transfusion requirements, and outcome. Crit Care Med 2002; 30 : 1765–1771.
4. Akca S, Haji-Michael P, de Mendonca A et al. Time course of platelet counts in critically ill patients. Crit Care Med 2002; 30 : 753–756.
5. Shalansky SJ, Verma AK, Levine M et al. Risk markers for thrombocytopenia in critically ill patients: a prospective analysis. Pharmacotherapy 2002; 22 : 803–813.
6. Crowther MA, Cook DJ, Meade MO et al. Thrombocytopenia in medical-surgical critically ill patients: prevalence, incidence, and risk factors. J Crit Care 2005; 20 : 348–353.
7. Moreau D, Timsit JF, Vesin A et al. Platelet count decline: an early prognostic marker in critically ill patients with prolonged ICU stays. Chest 2007; 131 : 1735–1741.
8. Hanes SD, Quarles DA, Boucher BA. Incidence and risk factors of thrombocytopenia in critically ill trauma patients. Ann Pharmacother 1997; 31 : 285–289.
9. Mercer KW, Gail Macik B, Williams ME. Hematologic disorders in critically ill patients. Semin Respir Crit Care Med 2006; 27 : 286–296.
10. Kinasewitz GT, Yan SB, Basson B et al. Universal changes in biomarkers of coagulation and inflammation occur in patients with severe sepsis, regardless of causative micro-organism. Crit Care 2004; 8: R82–R90.
11. Nijsten MW, ten Duis HJ, Zijlstra JG et al. Blunted rise in platelet count in critically ill patients is associated with worse outcome. Crit Care Med 2000; 28 : 3843–3846.
12. Spahn DR, Cerny V, Coats TJ et al. Management of bleeding following major trauma: a European guideline. Crit Care 2007; 11: R17.
13. Rebulla P, Finazzi G, Marangoni F et al. The threshold for prophylactic platelet transfusions in adults with acute myeloid leukemia. Gruppo Italiano Malattie Ematologiche Maligne dell’Adulto. N Engl J Med 1997; 337 : 1870–1875.
14. Wandt H, Frank M, Ehninger G et al. Safety and cost effectiveness of a 10 × 109/L trigger for prophylactic platelet transfusions compared with the traditional 20 × 109/L trigger: a prospective comparative trial in 105 patients with acute myeloid leukemia. Blood 1998; 91 : 3601–3606.
15. Schiffer CA, Anderson KC, Bennett CL et al. Platelet transfusion for patients with cancer: clinical practice guidelines of the American Society of Clinical Oncology. J Clin Oncol 2001; 19 : 1519–1538.
16. Stanworth SJ, Hyde C, Brunskill S et al. Platelet transfusion prophylaxis for patients with haematological malignancies: where to now? Br J Haematol 2005; 131 : 588–595.
17. Slichter SJ. Evidence-based platelet transfusion guidelines. Hematology Am Soc Hematol Educ Program 2007 : 172–178.
18. Tosetto A, Balduini CL, Cattaneo M et al. Management of bleeding and of invasive procedures in patients with platelet disorders and/or thrombocytopenia: Guidelines of the Italian Society for Haemostasis and Thrombosis (SISET). Thromb Res 2009; 124: e13–e18.
19. Cosmi B, Alatri A, Cattaneo M et al. Assessment of the risk of bleeding in patients undergoing surgery or invasive procedures: Guidelines of the Italian Society for Haemostasis and Thrombosis (SISET). Thromb Res 2009; 124: e6–e12.
20. Bernard GR, Vincent JL, Laterre PF et al. Efficacy and safety of recombinant human activated protein C for severe sepsis. N Engl J Med 2001; 344 : 699–709.
21. Bernard GR. Drotrecogin a (activated) (recombinant human activated protein C) for the treatment of severe sepsis. Crit Care Med 2003; 31 (1 Suppl): S85–S93.
22. Hess JR, Brohi K, Dutton RP et al. The coagulopathy of trauma: a review of mechanisms. J Trauma 2008; 65 : 748–754.
23. Brohi K, Cohen MJ, Ganter MT et al. Acute traumatic coagulopathy: initiated by hypoperfusion: modulated through the protein C pathway? Ann Surg 2007; 245 : 812–818.
24. Niles SE, McLaughlin DF, Perkins JG et al. Increased mortality associated with the early coagulopathy of trauma in combat casualties. J Trauma 2008; 64 : 1459–1463; discussion 1463–1465.
25. Brohi K, Singh J, Heron M et al. Acute traumatic coagulopathy. J Trauma 2003; 54 : 1127–1130.
26. MacLeod JB, Lynn M, McKenney MG et al. Early coagulopathy predicts mortality in trauma. J Trauma 2003; 55 : 39–44.
27. Ho AMKM, Dion PW. Are we giving enough coagulation factors during major trauma resuscitation? Am J Surg 2005; 190 : 479–484.
28. Brummel-Ziedins K, Whelihan MF, Ziedins EG et al. The resuscitative fluid you choose may potentiate bleeding. J Trauma 2006; 61 : 1350–1358.
29. Hess JR, Lawson JH. The coagulopathy of trauma versus disseminated intravascular coagulation. J Trauma 2006; 60: (6 Suppl): S12–S19.
30. Malone DL, Hess JR, Fingerhut A. Massive transfusion practices around the globe and a suggestion for a common massive transfusion protocol. J Trauma 2006; 60 (6 Suppl): S91–S96.
31. Meng ZH, Wolberg AS, Monroe DM 3rd et al. The effect of temperature and pH on the activity of factor VIIa: implications for the efficacy of high-dose factor VIIa in hypothermic and acidotic patients. J Trauma 2003; 55 : 886–891.
32. Wolberg AS, Meng ZH, Monroe DM 3rd et al. A systematic evaluation of the effect of temperature on coagulation enzyme activity and platelet function. J Trauma 2004; 56 : 1221–1228.
33. Levi M. Disseminated intravascular coagulation. Crit Care Med 2007; 35 : 2191–2195.
34. Mavrommatis AC, Theodoridis T, Orfanidou A et al. Coagulation system and platelets are fully activated in uncomplicated sepsis. Crit Care Med 2000; 28 : 451–457.
35. Berkman N, Michaeli Y, Or R et al. EDTA-dependent pseudothrombocytopenia: a clinical study of 18 patients and a review of the literature. Am J Hematol 1991; 36 : 195–201.
36. Francois B, Trimoreau F, Vignon P et al. Thrombocytopenia in the sepsis syndrome: role of hemophagocytosis and macrophage colony-stimulating factor. Am J Med 1997; 103 : 114–120.
37. Stephan F, Thioliere B, Verdy E et al. Role of hemophagocytic histiocytosis in the etiology of thrombocytopenia in patients with sepsis syndrome or septic shock. Clin Infect Dis 1997; 25 : 1159–1164.
38. Drews RE. Critical issues in hematology: anemia, thrombocytopenia, coagulopathy, and blood product transfusions in critically ill patients. Clin Chest Med 2003; 24 : 607–622.
39. Zeerleder S, Voves C, Wuillemin WA. Comment on hemostatic markers and the sepsis-related organ failure assessment score in patients with disseminated intravascular coagulation in an intensive care unit by Okabayashi et al. Am J Hematol 2005; 79 : 344.
40. Levi M, Opal SM. Coagulation abnormalities in critically ill patients. Crit Care 2006; 10 : 222.
41. Rice TW, Wheeler AP. Coagulopathy in critically ill patients: part 1: platelet disorders. Chest 2009; 136 : 1622–1630.
42. Bone RC, Balk RA, Cerra FB et al. Definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis. The ACCP/SCCM Consensus Conference Committee. American College of Chest Physicians/Society of Critical Care Medicine. Chest 1992; 101 : 1644–1655.
43. Levi M, Toh CH, Thachil J et al. Guidelines for the diagnosis and management of disseminated intravascular coagulation. British Committee for Standards in Haematology. Br J Haematol 2009; 145 : 24–33.
44. Al-Mondhiry H. Disseminated intravascular coagulation: experience in a major cancer center. Thromb Diath Haemorrh 1975; 34 : 181–193.
45. Siegal T, Seligsohn U, Aghai E et al. Clinical and laboratory aspects of disseminated intravascular coagulation (DIC): a study of 118 cases. Thromb Haemost 1978; 39 : 122–134.
46. Fourrier F, Chopin C, Goudemand J et al. Septic shock, multiple organ failure, and disseminated intravascular coagulation. Compared patterns of antithrombin III, protein C, and protein S deficiencies. Chest 1992; 101 : 816–823.
47. Mesters RM, Mannucci PM, Coppola R et al. Factor VIIa and antithrombin III activity during severe sepsis and septic shock in neutropenic patients. Blood 1996; 88 : 881–886.
48. Faust SN, Levin M, Harrison OB et al. Dysfunction of endothelial protein C activation in severe meningococcal sepsis. N Engl J Med 2001; 345 : 408–416.
49. Egi M, Morimatsu H, Wiedermann CJ et al. Non-overt disseminated intravascular coagulation scoring for critically ill patients: the impact of antithrombin levels. Thromb Haemost 2009; 101 : 696–705.
50. Spero JA, Lewis JH, Hasiba U. Disseminated intravascular coagulation. Findings in 346 patients. Thromb Haemost 1980; 43 : 28–33.
51. Wilde J, Kitchen S, Kinsey S et al. Plasma D-dimer levels and their relationship to serum fibrinogen/fibrin degradation products in hypercoagulable states. Br J Haematol 1989; 71 : 65–70.
52. Wada H, Gabazza EC, Asakura H et al. Comparison of diagnostic criteria for disseminated intravascular coagulation (DIC): diagnostic criteria of the International Society of Thrombosis and Hemostasis and of the Japanese Ministry of Health and Welfare for overt DIC. Am J Hematol 2003; 74 : 17–22.
53. Neame PB, Kelton JG, Walker IR et al. Thrombocytopenia in septicemia: the role of disseminated intravascular coagulation. Blood 1980; 56 : 88–92.
54. Ten CH. Trombocytopenia: one of the markers of disseminated intravascular coagulation. Pathophysiol Haemost Thromb 2003; 33 : 413–416.
55. Taylor Jr. FB, Toh CH, Hoots WK et al. Towards definition, clinical and laboratory criteria, and a scoring system for disseminated intravascular coagulation. Thromb Haemost 2001; 86 : 1327–1330.
56. Toh CH, Hoots WK. The scoring system of the Scientific and Standardisation Committee on Disseminated Intravascular Coagulation of the International Society on Thrombosis and Haemostasis: a 5-year overview. J Thromb Haemost 2007; 5 : 604–606.
57. Gando S, Wada H, Asakura H et al. Evaluation of new Japanese diagnostic criteria for disseminated intravascular coagulation in critically ill patients. Clin Appl Thromb Hemost 2005; 11 : 71–76.
58. Gando S, Iba T, Eguchi Y et al. A multicenter, prospective validation of disseminated intravascular coagulation diagnostic criteria for critically ill patients: comparing current criteria. Crit Care Med 2006; 34 : 625–631.
59. Gando S, Saitoh D, Ogura H et al. Natural history of disseminated intravascular coagulation diagnosed based on the newly established diagnostic criteria for critically ill patients: results of a multicenter, prospective survey. Crit Care Med 2008; 36 : 145–150.
60. Sawamura A, Hayakawa M, Gando Set al. Application of the Japanese Association for Acute Medicine disseminated intravascular coagulation diagnostic criteria for patients at an early phase of trauma. Thromb Res 2009; 124 : 706–710.
61. Gando S, Saitoh D, Ogura H et al. Disseminated intravascular coagulation (DIC) diagnosed based on the Japanese Association for Acute Medicine criteria is a dependent continuum to overt DIC in patients with sepsis. Thromb Res 2009; 123 : 715–718.
62. Payne BA, Pierre RV. Pseudothrombocytopenia: a laboratory artifact with potentially serious consequences. Mayo Clin Proc 1984; 59 : 123–125.
63. Schrezenmeier H, Muller H, Gunsilius Eet al. Anticoagulant-induced pseudothrombocytopenia and pseudoleucocytosis. Thromb Haemost 1995; 73 : 506–513.
64. Sachova L, Urgasova A, Gumulec J. Laboratory procedures following thrombocytopenia diagnosis. Vnitř Lék 2009; 55 : 290–294.
65. Aster RH, Bougie DW. Drug-induced immune thrombocytopenia. N Engl J Med 2007; 357 : 580–587.
66. Aster RH, Curtis BR, McFarland JG et al. Drug-induced immune thrombocytopenia: pathogenesis, diagnosis, and management. J Thromb Haemost 2009; 7 : 911–918.
67. George JN, Aster RH. Drug-induced thrombocytopenia: pathogenesis, evaluation, and management. Hematology Am Soc Hematol Educ Program 2009 : 153–158.
68. Warkentin TE, Chong BH, Greinacher A. Heparin-induced thrombocytopenia: towards consensus. Thromb Haemost 1998; 79 : 1–7.
69. Arepally GM,Ortel TL. Clinical practice. Heparin-induced thrombocytopenia. N Engl J Med 2006; 355 : 809–817.
70. Greinacher A. Heparin-induced thrombocytopenia. J Thromb Haemost 2009; 7: (Suppl 1): 9–12.
71. Warkentin TE, Sheppard JA, Moore JC et al. Laboratory testing for the antibodies that cause heparin-induced thrombocytopenia: how much class do we need? J Lab Clin Med 2005; 146 : 341–346.
72. Lo GK, Juhl D, Warkentin TE et al. Evaluation of pretest clinical score (4 T’s) for the diagnosis of heparin-induced thrombocytopenia in two clinical settings. J Thromb Haemost 2006; 4 : 759–75.
73. Pouplard C, Gueret P, Fouassier M et al. Prospective evaluation of the ’4Ts’ score and particle gel immunoassay specific to heparin/PF4 for the diagnosis of heparin-induced thrombocytopenia. J Thromb Haemost 2007; 5 : 1373–1379.
74. Martel N, Lee J, Wells PS. Risk for heparin-induced thrombocytopenia with unfractionated and low-molecular-weight heparin thromboprophylaxis: a meta-analysis. Blood 2005; 106 : 2710–2715.
75. Rota E, Bazzan M, Fantino G. Fondaparinux-related thrombocytopenia in a previous low-molecular-weight heparin (LMWH)-induced heparin-induced thrombocytopenia (HIT). Thromb Haemost 2008; 99 : 779–781.
76. Gao C, Boylan B, Bougie D et al. Eptifibatide-induced thrombocytopenia and thrombosis in humans require FcgRIIa and the integrin b3 cytoplasmic domain. J Clin Invest 2009; 119 : 504–511.
77. Kelton JG, Neame PB, Gauldie J et al. Elevated platelet-associated IgG in the thrombocytopenia of septicemia. N Engl J Med 1979; 300 : 760–764.
78. van der Lelie J, van der Plas-Van Dalen CM, von dem Borne AE. Platelet autoantibodies in septicaemia. Br J Haematol 1984; 58 : 755–760.
79. Stephan F, Cheffi MA, Kaplan C et al. Autoantibodies against platelet glycoproteins in critically ill patients with thrombocytopenia. Am J Med 2000; 108 : 554–560.
80. Mueller-Eckhardt C, Kayser W, Mersch-Baumert K et al. The clinical significance of platelet-associated IgG: a study on 298 patients with various disorders. Br J Haematol 1980; 46 : 123–131.
81. Kelton JG, Murphy WG, Lucarelli A et al. A prospective comparison of four techniques for measuring platelet-associated IgG. Br J Haematol 1989; 71 : 97–105.
82. Fabris F, Scandellari R, Randi ML et al. Attempt to improve the diagnosis of immune thrombocytopenia by combined use of two different platelet autoantibodies assays (PAIgG and MACE). Haematologica 2002; 87 : 1046–1052.
83. Cines DB, Liebman H, Stasi R. Patho-biology of secondary immune thrombocytopenia. Semin Hematol 2009; 46 (Suppl 2): S2–S14.
84. Mayer SA, Aledort LM. Thrombotic microangiopathy: differential diagnosis, pathophysiology and therapeutic strategies. Mt Sinai J Med 2005; 72 : 166–175.
85. Nguyen TC, Carcillo JA. Bench-to-bedside review: thrombocytopenia-associated multiple organ failure – a newly appreciated syndrome in the critically ill. Crit Care 2006; 10 : 235.
86. Gando S. Microvascular thrombosis and multiple organ dysfunction syndrome. Crit Care Med 2010; 38 (2 Suppl): S35–S42.
87. Allford SL, Hunt BJ, Rose P et al. Guidelines on the diagnosis and management of the thrombotic microangiopathic haemolytic anaemias. Br J Haematol 2003; 120 : 556–573.
88. Pereira A, Mazzara R, Monteagudo J et al. Thrombotic thrombocytopenic purpura/hemolytic uremic syndrome: a multivariate analysis of factors predicting the response to plasma exchange. Ann Hematol 1995; 70 : 319–323.
89. Crowther MA, George JN. Thrombotic thrombocytopenic purpura: 2008 update. Cleve Clin J Med 2008; 75 : 369–375.
90. Sadler JE. Thrombotic thrombocytopenic purpura: a moving target. Hematology Am Soc Hematol Educ Program 2006 : 415–420.
91. Gasser C, Gautier E, Steck A et al. Hemolytic-uremic syndrome: bilateral necrosis of the renal cortex in acute acquired hemolytic anemia. Schweiz Med Wochenschr 1955; 85 : 905–909.
92. McCrae KR, Bussel JB, Mannucci PM et al. Platelets: an update on diagnosis and management of thrombocytopenic disorders. Hematology Am Soc Hematol Educ Program 2001 : 282–305.
93. Rath W, Fischer T. The diagnosis and treatment of hypertensive disorders of pregnancy: new findings for antenatal and inpatient care. Dtsch Arztebl Int 2009; 106 : 733–738.
94. Report of the National High Blood Pressure Education Program Working Group on High Blood Pressure in Pregnancy. Am J Obstet Gynecol 2000; 183: S1–S22.
95. Sainio S, Kekomaki R, Riikonen S et al. Maternal thrombocytopenia at term: a population-based study. Acta Obstet Gynecol Scand 2000; 79 : 744–749.
96. McCrae KR, Samuels P, Schreiber AD. Pregnancy-associated thrombocytopenia: pathogenesis and management. Blood 1992; 80 : 2697–2714.
97. Sibai BM. The HELLP syndrome (hemolysis, elevated liver enzymes, and low platelets): much ado about nothing? Am J Obstet Gynecol 1990; 162 : 311–316.
98. Martin Jr. JN, Files JC, Blake PG et al. Plasma exchange for preeclampsia. I. Postpartum use for persistently severe preeclampsia-eclampsia with HELLP syndrome. Am J Obstet Gynecol 1990; 162 : 126–137.
99. Sibai BM, Ramadan MK, Usta I et al. Maternal morbidity and mortality in 442 pregnancies with hemolysis, elevated liver enzymes, and low platelets (HELLP syndrome). Am J Obstet Gynecol 1993; 169 : 1000–1006.
100. Finazzi G. The Italian Registry of Antiphospholipid Antibodies. Haematologica 1997; 82 : 101–105.
101. Cuadrado MJ, Mujic F, Munoz E et al. Thrombocytopenia in the antiphospholipid syndrome. Ann Rheum Dis 1997; 56 : 194–196.
102. Cervera R, Piette JC, Font J et al. Antiphospholipid syndrome: clinical and immunologic manifestations and patterns of disease expression in a cohort of 1,000 patients. Arthritis Rheum 2002; 46 : 1019–1027.
103. Lim W. Antiphospholipid antibody syndrome. Hematology Am Soc Hematol Educ Program 2009 : 233–239.
104. Asherson RA, Cervera R, de Groot PG et al. Catastrophic antiphospholipid syndrome: international consensus statement on classification criteria and treatment guidelines. Lupus 2003; 12 : 530–534.
105. Cervera R, Font J, Gomez-Puerta JA et al. Validation of the preliminary criteria for the classification of catastrophic antiphospholipid syndrome. Ann Rheum Dis 2005; 64 : 1205–1209.
106. Espinosa G, Bucciarelli S, Asherson RA et al. Morbidity and mortality in the catastrophic antiphospholipid syndrome: pathophysiology, causes of death, and prognostic factors. Semin Thromb Hemost 2008; 34 : 290–294.
107. Cohen AM, Cycowitz Z, Mittelman M et al. The incidence of pseudothrombocytopenia in automatic blood analyzers. Haematologia (Budap) 2000; 30 : 117–121.
108. Ledgerwood AM, Lucas CE. A review of studies on the effects of hemorrhagic shock and resuscitation on the coagulation profile. J Trauma 2003; 54 (5 Suppl): S68–S74.
109. Verma AK, Levine M, Shalansky SJ et al. Frequency of heparin-induced thrombocytopenia in critical care patients. Pharmacotherapy 2003; 23 : 745–753.
110. Gettings EM, Brush KA, Van Cott EM et al. Outcome of postoperative critically ill patients with heparin-induced thrombocytopenia: an observational retrospective case-control study. Crit Care 2006; 10: R161.
111. Kuitunen A, Suojaranta-Ylinen R, Raivio P et al. Heparin-induced thrombocytopenia following cardiac surgery is associated with poor outcome. J Cardiothorac Vasc Anesth 2007; 21 : 18–22.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2010 Issue Supplementum 1-
All articles in this issue
- Heparinem indukovaná trombocytopenie při léčbě nízkomolekulárními hepariny u dětí. Je čeho se obávat?
- Lokální intravenózní fibrinolýza u dětí a mladistvých
- Chronická imunitní trombocytopenická purpura – úspěšná léčba protilátkami anti‑CD 20
- Trombocytopenie a koagulopatie u hepatopatie: úvod do problematiky
- Monitorace parametrů koagulace a možnosti jejich ovlivnění u pacientů s jaterní cirhózou před invazivními výkony
- Imunitní trombocytopenie, diagnostika, klasifikace, diferenciální diagnostika
- Terapie imunitní trombocytopenie v graviditě
- Trombocytopenie u pacientů s průkazem antifosfolipidových protilátek nebo s antifosfolipidovým syndromem
- Diferenciální diagnostika trombocytopenie v těhotenství
- Syndrom HELLP – průběh onemocnění a aktivita markerů aktivace endotelu
- Porovnání hladin markerů aktivace endotelu v jednotlivých trimestrech.
- Využití parametru IPF (Immature platelet fraction) v laboratorní diagnostice
- Mikropartikule
- Uplatnění průtokové cytometrie v analýze trombocytů
- Změny laboratorních ukazatelů hemostázy u hepatopatií
- Úvodní slovo
- Ambulantní pacient s nově zjištěnou trombocytopenií
- Diferenciální diagnostika trombocytopenie u kriticky nemocných pacientů
- Trombocytopenie u malignit. Úvod do problematiky: příčiny, prognostický význam, význam pro terapii
- Dysplastické změny megakaryopoézy podle WHO klasifikace 2008
- Trombocytopenie u myelodysplastického syndromu
- Trombocytopenie u pacientů s akutní promyelocytární leukemií
- Využití destičkového lyzátu při kultivacích mezenchymálních kmenových buněk
- Trombocytopenie u novorozence
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Trombocytopenie a koagulopatie u hepatopatie: úvod do problematiky
- Monitorace parametrů koagulace a možnosti jejich ovlivnění u pacientů s jaterní cirhózou před invazivními výkony
- Diferenciální diagnostika trombocytopenie v těhotenství
- Využití parametru IPF (Immature platelet fraction) v laboratorní diagnostice
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


