-
Medical journals
- Career
Intervenční kardiologie: co nabízí v roce 2011
Authors: M. Želízko; B. Janek; M. Hrnčárek; V. Pořízka; V. Karmazín; J. Malý; I. Netuka
Authors‘ workplace: Přednosta: prof. MUDr. Jan Pirk, DrSc. ; Klinika kardiovaskulární chirurgie ; Klinika kardiologie ; Přednosta: prof. MUDr. Josef Kautzner, CSc. ; Institut klinické a experimentální medicíny, Praha
Published in: Prakt. Lék. 2011; 91(1): 42-48
Category: 40th Anniversary IKEM
Overview
Článek uvádí přehled současných metod intervenční kardiologie.
První část se zabývá problematikou ischemické choroby srdeční, možnostmi invazívní diagnostiky a uvádí základní informace o perkutánních koronárních intervencích (PCI) a jejich klinických indikacích.
Ve druhé části jsou uvedeny v přehledu katetrizační výkony na chlopních včetně transkatetrové implantace aortální chlopně a dále katetrizační intervence u zkratových vad srdce.Klíčová slova:
selektivní koronarografie, perkutánní koronární intervence, lékové stenty, aortální stenóza, chlopenní protéza, transkatetrová implantace, zkratová vada, alkoholová septální ablace.Úvod
Intervenční kardiologie se zabývá invazívní diagnostikou a intervenční léčbou srdečních chorob. Koronarografie je stále považována za standard pro posuzení nálezu na věnčitých tepnách a společně s perkutánní koronární intervencí (PCI) představuje nejčastěji prováděný výkon. V souvislosti s vývojem instrumentaria, jeho technickým zdokonalením a využíváním radiálního přístupu je možné většinu těchto výkonů provést i ambulantně s krátkou expektací pacienta.
Nekoronární intervence jsou početně méně časté, nicméně umožňují v současné době řešit nejčastější zkratové vady v dospělosti, mohou být řešením u některých typů chlopenních, vad včetně katetrizační implantace aortální chlopně, a nahrazují tak v řadě případů klasické kardiochirurgické operace.
V článku uvádíme základní přehled používaných metod.
1. KORONÁRNÍ NEMOC
1. 1. Invazívní diagnostické výkony
Selektivní koronarografie:
Angiografické vyšetření spočívá v selektivním nástřiku jódové kontrastní látky postupně do ústí obou věnčitých tepen. Náplň lumina je zobrazena pomocí angiografického přístroje. Je hodnocen kalibr věnčitých tepen a zúžení v jejich průběhu, přičemž za hranici významnosti je považována 50% redukce průměru (odpovídá 75% redukci plochy).
Za klinicky jednoznačně významné jsou považovány stenózy nad 70 %, jako kritické jsou popisovány stenózy nad 90 %. Stenózy v rozmezí 50–70 %, případně angiograficky nejasné nálezy, je možno dále podrobně vyšetřit dalšími metodami.
U nemocných s akutním infarktem myokardu nacházíme nejčastěji úplný uzávěr věnčité tepny trombem (v 70 %), případně kritickou stenózu, která omezuje průtok i za klidových podmínek. V případě chronického uzávěru věnčité tepny je důležité posoudit přítomnost kolaterál, které plní tepnu za místem uzávěru s ohledem na případnou revaskularizaci (PCI nebo CABG).
Setkáváme se i s anomáliemi odstupu a průběhu věnčitých tepen, kdy nejzávažnější je anomální odstup levé věnčité tepny z kmene plicnice (způsobuje ischemii myokardu již v dětství) a anomální odstup levé věnčité tepny z pravého koronárního sinu (při jedné z variant, kdy kmen levé koronární tepny probíhá mezi aortou a plicnicí, dochází k jeho externí kompresi, a tato anomalie je spojena s arytmickým rizikem náhlého úmrtí).
Koronarografické nálezy popisně hodnotíme jako
- normální (typický odstup i průběh koronárních tepen, hladké kontury a normální průtok),
- nevýznamné postižení (stenózy do 50 %), nebo jako
-
významné
postižení jednoho, dvou nebo všech tří povodí
věnčitých tepen
- ramus interventricularis anterior – RIA,
- ramus circumflexus – RC, a
- pravá věnčitá tepna – ACD),
v praxi ne zcela správně označované jako nemoc jedné, dvou nebo tří věnčitých tepen (1VD, 2VD, 3VD – z angl. vessel disease), případně jako postižení kmene levé věnčité tepny.
Při diagnostické katetrizaci je možné angiograficky zobrazit i jiné cévní oblasti, nejčastěji koronární bypassy, karotické tepny, renální tepny, pánevní tepny – viz obr. 1 a 3).
Image 1. Angiografie levé renální tepny s ostiální kalcifikovanou 70% stenózou 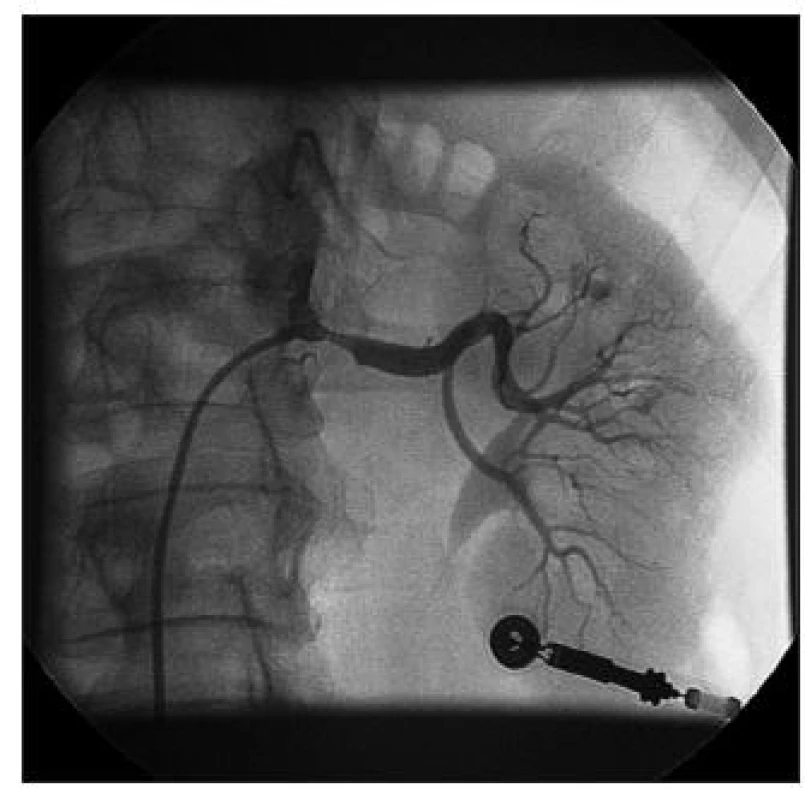
Image 2. Angiografie levé renální tepny po implantaci stentu 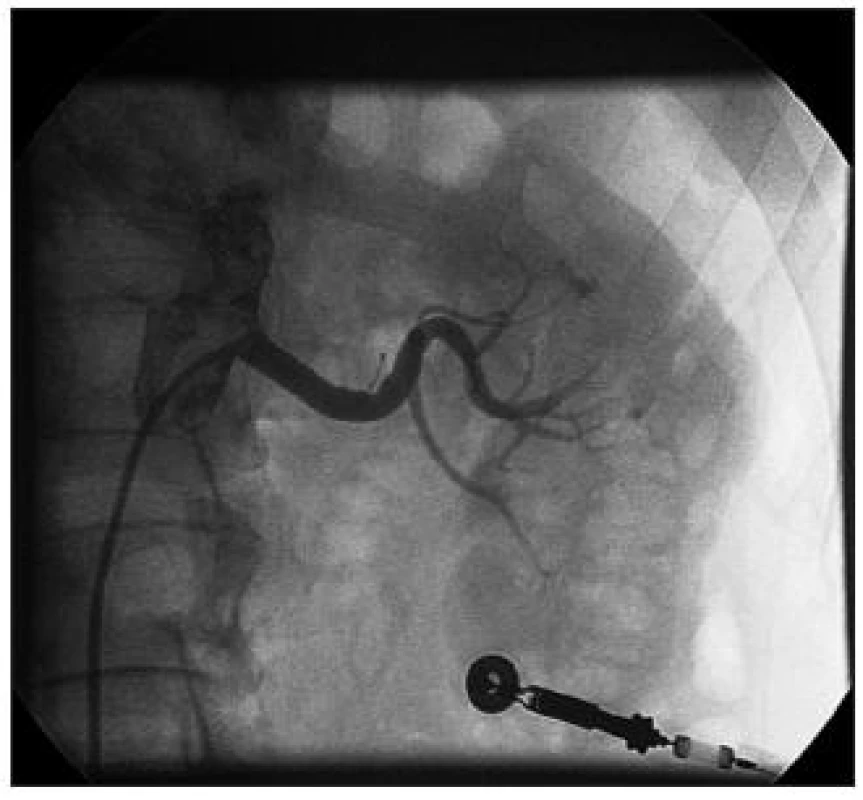
Lze provést angiografii levé komory (posouzení ejekční frakce a mitrální regurgitace), bulbu aorty (aortální regurgitace, dilatace či disekce vzestupné aorty), hrudní či břišní aorty (1).
Součástí vyšetření je i hodnocení hemodynamiky: tlakových poměrů v malém a velkém oběhu, plicní resistence, hodnocení gradientů a ploch chlopenních ústí (2).
Vzhledem k podání kontrastní látky je nutná speciální příprava u nemocných s jasnou alergickou anamnézou a dále u nemocných s renální insuficiencí (spočívá zejména v dostatečné hydrataci nemocných před vlastním vyšetřením a minimalizací množství podaného kontrastu).
Nové zobrazovací metody:
Intravaskulární ultrazvukové vyšetření (IVUS, rozlišovací schopnost 80–120 μm) umožňuje posoudit lumen cévy komplexně. Zobrazí strukturu stěny cévy včetně složení aterosklerotických plátů (kalcifikace, fibrózní pláty, trombus). Vedle přesnější kvantifikace stenózy a minimální plochy cévy v místě zúžení (hraniční je hodnota 4 mm2, u kmene pak 6 mm2) umí zobrazit i intimální trhliny, disekce a remodelaci tepny.
Indikace k IVUS vyšetření jsou u morfologicky nepřehledných lézí (bifurkační či ostiální stenózy), hraniční stenózy, stenózy kmene. Experimentálně je IVUS používán ve studiích s hodnocením možné regrese aterosklerózy.
Virtuální histologie
vychází z principu intravaskulárního ultrazvuku, zobrazuje kvalitativní složení plátu, ve kterém rozlišuje tkáň fibrózní, tukovou, kalcifikace a nekrotické hmoty. Má význam převážně v experimentálních studiích (obr. 2)Optická koherenční tomografie
zpracovává optický signál, má mnohonásobně vyšší rozlišovací schopnost ve srovnání s angiogragfií či IVUS vyšetřením (v řádu 10–20 μm). V kardiologii je metodou experimentální (endotelizace a apozice stentů, trombóza, restenóza – viz obr. 4)Image 3. Intravaskulární ultrazvuk (levá polovina obrázku) a virtuální histologie (pravá polovina obrázku) stejné stenózy. Intravaskulární ultrazvuk zobrazí lumen cévy a její původní rozměr (lamina elastica), plocha stenózy je 87 %. Virtuální histologie v barevném rozlišení určí charakter plátu a lokalizaci jednotlivých hmot 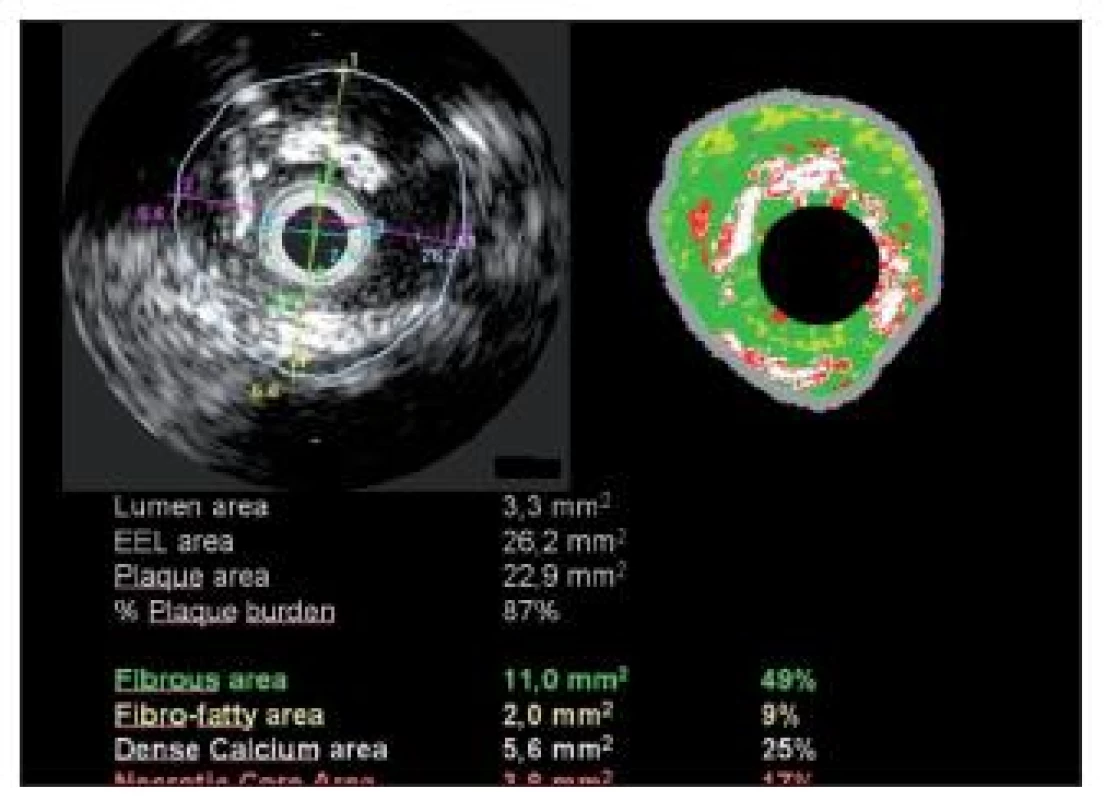
Image 4. OCT koronární tepny po implantci stentu. Oka stentu jsou pokryty tenkou vrstvou neointimy a vytvářejí optický stín 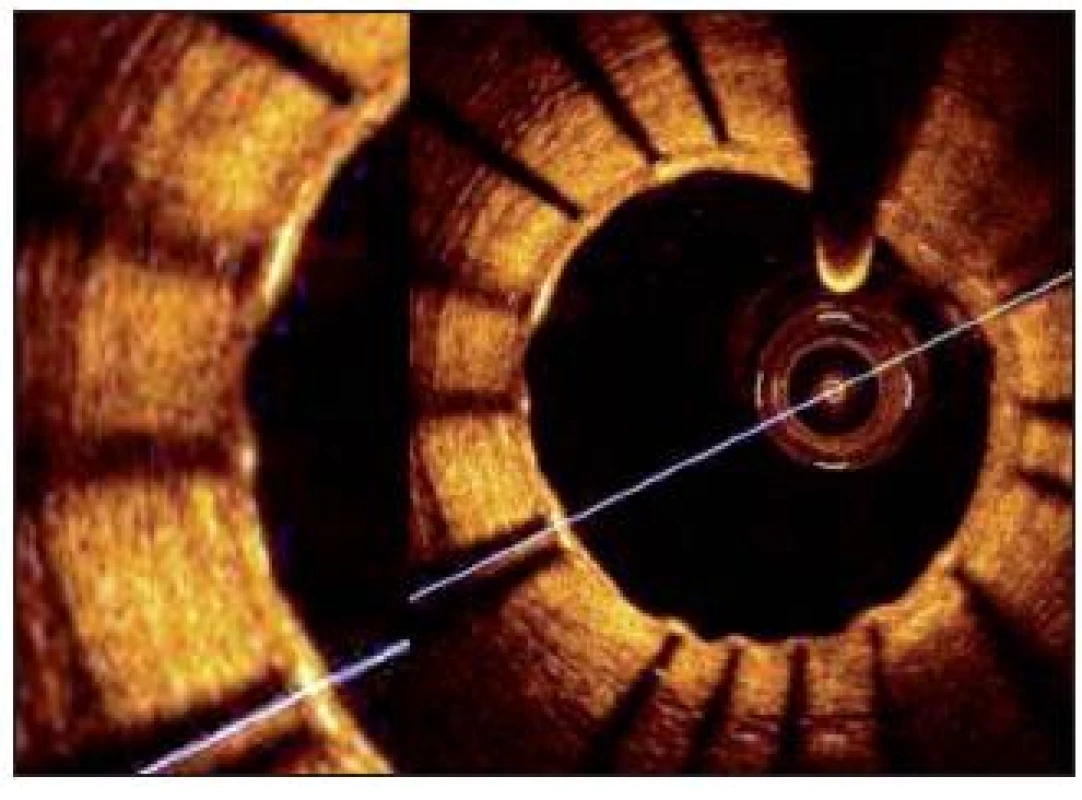
Měření tzv. frakční průtokové rezervy (FFR)
vypovídá o funkčním významu hraničních stabilních lézí, vychází z principu měření tlakového gradientu na stenóze při maximální hyperémii. Poměr středních tlaků za stenózou a před stenózou je v praxi měřen simultánně tlakovým senzorem na supertenkém vodiči (stenózu) a invazívním tlakem z vodící cévky (před stenózou), a to v klidu a po podání vasodilatačního podnětu.Hodnoty FFR <0,80 svědčí pro funkčně významnou stenózu vyžadující revaskularizaci, hodnoty FFR >0,80 svědčí pro funkčně nevýznamnou stenózu.
1. 2. Perkutánní koronární intervence (PCI)
První balonkovou koronární angioplastiku (PTCA) provedl roku 1977 Andreas Gruntzig (balonková dilatace stenózy proximálního úseku RIA), metoda se rozšířila počátkem 90. let minulého století i na nemocné s akutními koronárními syndromy (primární PTCA u akutního infarktu myokardu).
Zlom znamenalo rutinní zavedení koronárních stentů v polovině 90. let.
To umožnilo nejprve prakticky eliminovat obávané komplikace prosté balonkové dilatace – disekce tepny a riziko jejího uzávěru a současně prokázalo snížení restenózy o více než 50 % proti prosté balonkové dilataci. Následně došlo k expanzi indikací na komplexní postižení a akutní koronární syndromy. Tomu přispěly zejména informace o potřebě vysokotlakých dilatací stentů (díky poznatkům z IVUS vyšetření) a zavedení duální protidestičkové léčby ticlopidinem (později nahrazen clopidogrelem pro rychlejší nástup účinku).
Dalším významným mezníkem bylo zavedení lékových stentů (Drug eluting stents – DES), které po implantaci dlouhodobě uvolňují antiproliferativní léky a významně snížují riziko restenózy (angiograficky až o 80 %, klinicky o 50 %).
V ČR jsou dostupné od r. 2003 stenty Cypher uvolňující sirolimus a Taxus uvolňující paclitaxel, v současnosti i řada lékových stentů novějších generací, uvolňující jiné antiproliferativní látky (everolimus, zotarolimus).
Nízké riziko perkutánních koronárních intervencí provedení revaskularizace v jedné době s diagnostickou koronarografií a možnost časné dimise (při radiálním přístupu i plně ambulantní výkon) jsou pro pacienta velmi atraktivní a PCI je tak preferovanou metodou revaskularizace.
Technologická zlepšení PCI a zavedení lékových stentů posunuly indikace k PCI i na více komplexní postižení, stenózy kmene a mnohočetné nálezy a konkurují tak kardiochirurgii.
V současnosti je prováděno téměř 4x více PCI nežli koronárních bypassů (CABG), hlavní indikací k PCI jsou akutní koronární syndromy (60–70 % PCI).
Hlavní indikace k PCI (3, 4)
Akutní infarkt myokardu s elevacemi ST segmentu (STEMI)
Primární (direct) PCI u je indikována u všech nemocných s dobou ischemie do 12 hodin jakožto primární reperfúzní léčba. Struktura a síť PCI center v České republice a organizace přednemocniční diagnostiky infarktu myokardu společně s primárním transportem nemocných na PCI centrum je v praxi dostuná prakticky všem nemocným.
Trombolýza je v současnosti vyhrazena pouze nemocným v prvních dvou hodinách infarktu, kde je předpoklad velmi dlouhého transportního zdržení (doba transportu na PCI centrum delší jak 90 minut) a je možno podat trombolytikum okamžitě (prehospitalizační trombolýza bolusovým lytikem, v ČR v 1 % všech STEMI).
Výsledky primární PCI jsou velmi dobré – technická úspěšnost výkonu je nad 90 % a dále se zlepšuje při využití tzv aspiračních katetrů (trombus je nejprve z místa uzávěru věnčité tepny odsán katetrem a poté je reziduální stenóza ošetřena implantací stentu – viz obr. 5, 6 a 7).
Image 5. Uzávěr ramus interventricularis anterior (RIA) u nemocného s akutním infarktem myokardu s elevacemi ST segmentu 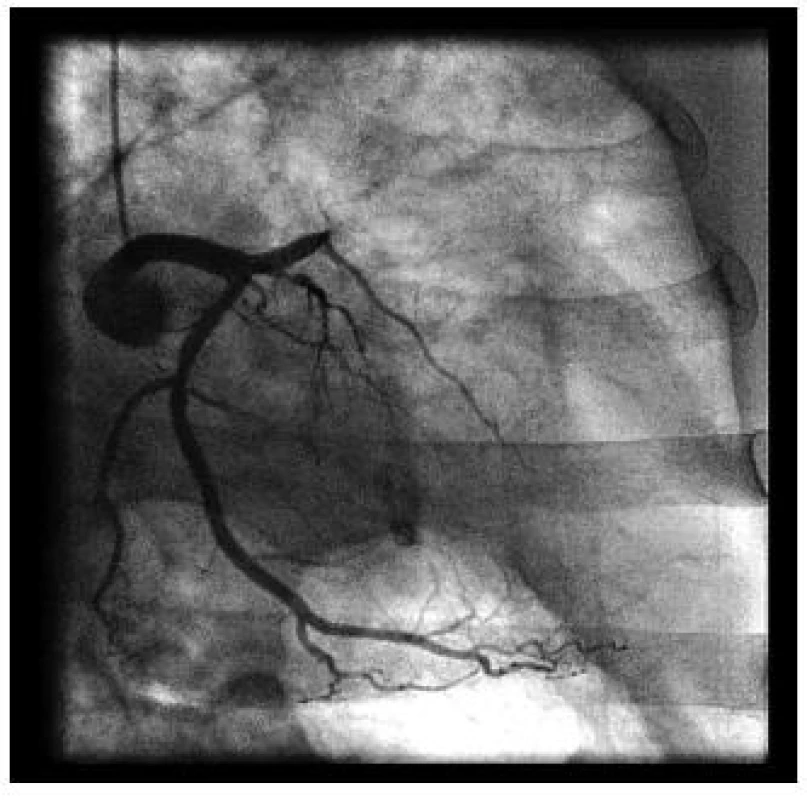
Image 6. Primární PCI: po rekanalizaci vodičem je do místa uzávěru implantován koronární stent 
Image 7. Po PCI je povodí RIA volně průchodné s normálním průtokem 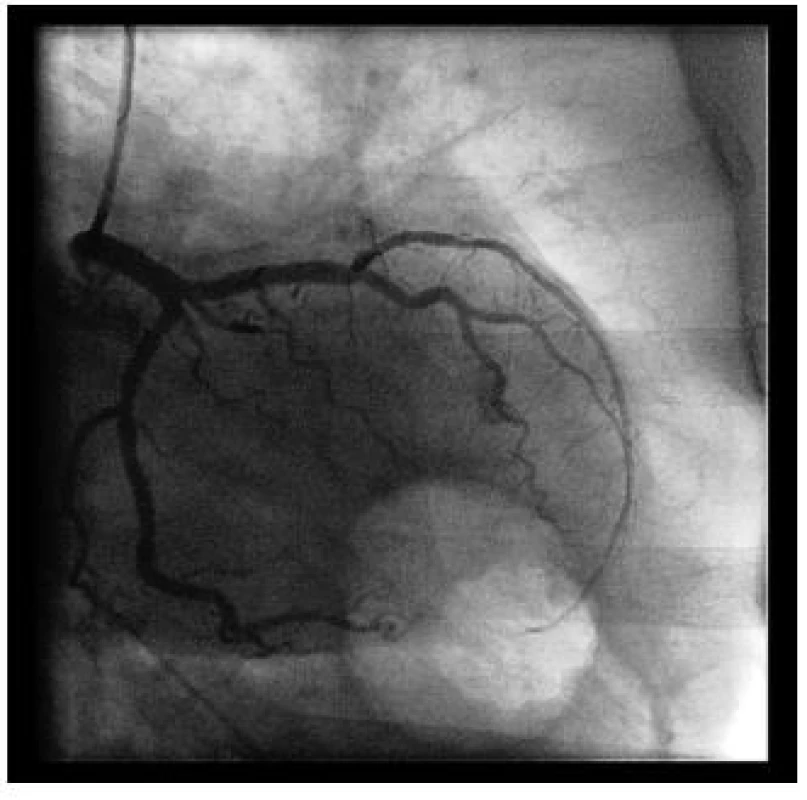
Primární PCI snížila mortalitu nemocných se STEMI o více než 50 %, recentní celorepubliková data uvádějí mortalitu všech nemocných léčených primární PCI ve 30 dni 7 % a 1-roční kolem 10 %.
Akutní koronární syndromy bez ST elevací
-
U nemocných
s klinicky vysokým rizikem
opakované klidové stenokardie,
změny v EKG,
pozitivní troponin,
srdeční selhání, nebo
maligní arytmie) je indikace k urgentní koronarografii okamžitě (nejpozději do 24 hodin); - u nemocných se středním rizikem pak časně (do 72 hodin),
-
u nemocných
s nízkým rizikem
žádné změny v EKG,
negativní troponin,
nízké klinické riziko
je možné provedení koronarografie před dimisí nebo elektivně později.
Rozhodnutí o způsobu revaskularizace závisí na závažnosti a rozsahu koronárního postižení. PCI je preferována při postižení jedné nebo dvou povodí (2/3 nemocných), CABG je pak častěji indikován u nemocných se stenózou kmene a/nebo při postižení všech 3. povodí (20 % nemocných), a to s přihlénutím k funkci levé komory srdeční a komorbiditám.
Stabilní formy ICHS
Indikace k revaskularizaci je u symptomatických nemocných s námahovou anginou pectoris. Oproti konzervativní léčbě vede revaskularizace k rychlejšímu a úplnějšímu odstranění symptomů. U nemocných s významnou stenózou kmene a/nebo postižením všech 3. povodí (prognosticky významné postižení) revaskularizace prokazatelně zlepšuje prognózu (prodlužuje přežití), u ostatních nálezů má efekt pouze na symptomy.
Rozhodnutí o způsobu PCI nebo CABG záleží na rozsahu postižení – velmi komplexní nálezy a nemocní s diabetes mellitus jsou indikováni spíše k CABG, ostatní nálezy jsou indikací k PCI.
1. 3. Ambulantní koronarografie a PCI (5)
Koronargrafie s navazující PCI je možno provést radiálním přístupem, který eliminuje riziko krvácivých komplikací, umožňuje odstranit katetr a pouzdro ihned po výkonu s časnou mobilizací pacienta (obr. 8, 9). To umožnilo provádění těchto výkonů zcela ambulantně, bez nutnosti hospitalizace, pouze s krátkou expektací po výkonu (4 hodiny).. K ambulantnímu výkonu jsou vhodní nemocní se stabilní formou ICHS, kteří nemají závažnější komorbidity (hematologické, renální, plicní, koagulační) ani přidružené kardiální postižení (chlopenní vady, stavy po CABG).
Image 8. Transradiální přístup: pouzdro 5F je zavedeno do radiální tepny 
Image 9. Transradiální přístup: po koronarografii a PCI je pouzdro odstraněno a naložena elastická bandáž, nemocný je plně mobilní 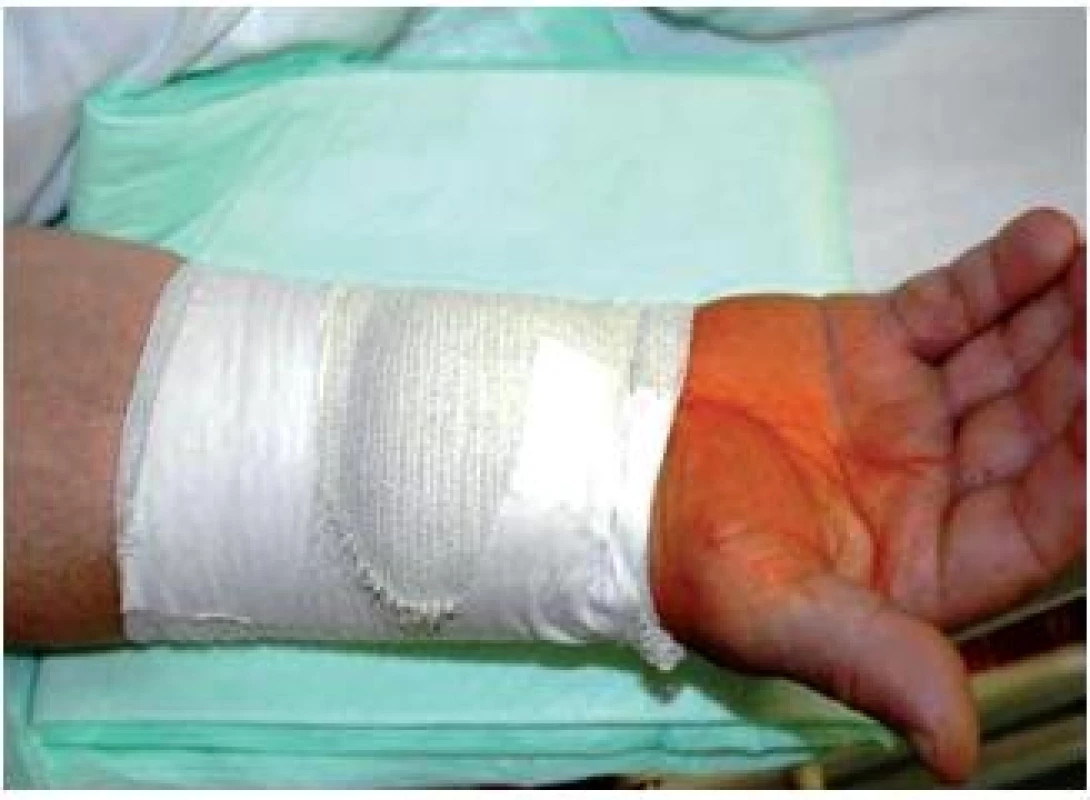
2. CHLOPENNÍ VADY SRDCE
2. 1. Perkutánní dilatace aortální stenózy
Vrozená valvulární stenóza aortální chlopně je dobrou indikací k balonkové dilataci s nízkým rizikem a dobrými krátkodobými i dlouhodobými výsledky. V dospělé populaci však převažuje degenerativní aortální stenóza, kdy prostá balonková dilatace kalcifikované aortální chlopně (Cribier, 1985) nepřináší dobré výsledky – dilatace aortálního ústí je zpravidla nedostatečná, s rizikem vzniku akutní aortální regurgitace a zejména s vysokým rizikem časné restenózy.
V 90. letech byl tento výkon prakticky opuštěn a dnes se provádí výjimečně u nemocných s pokročilou vadou, starých a polymorbidních, a to zejména jako překlenutí k případné chirurgické náhradě aortální chlopně nebo k perkutánní implantaci aortální chlopně.
2. 2. Perkutánní (transkatetrová) implantace aortální chlopně (TAVI)
Výkon spočívá v katetrizační implantaci speciálně kostruované biologické protézy aortální chlopně. Přes stenotickou aortální chlopeň je retrográdně z femorální tepny proniknuto katetrem do levé komory srdeční a zaveden vodič s vysokou oporou. Stenotická aortální chlopeň je nejprve dilatována balónkovým katetrem o průměru 22–25 mm. Princip je shodný s balonkovou dilatací aortální chlopně prováděnou kdysi jako samostatný výkon, vlastní dilatace chlopně je prováděna při rychlé stimulaci komor o frekcvenci 180/min (zabraňuje vypuzení balónku z aortální pozice). Poté je do aortálního anulu zavedena vlastní aortální bioprotéza.
V současnosti jsou komerčně dostupné dva systémy:
- chlopeň typu CoreValve, a
- chlopeň typu Sapien-Edwards.
Chlopeň CoreValve je vyrobená z prasečího perikardu, kdy 3 cípy chlopně jsou všity do nitinolového koše (obr. 10). Nitinol má termoelastickou paměť, v chladu změkne, což umožňuje celou chlopeň „sbalit“ do zaváděcího pouzdra, jehož vnější průměr je 6 mm (obr. 11, 12).
Image 10. Chlopeň typu CoreValve: v nitinolovém koši je všita vlastní trojcípá biologická chlopeň 
Image 11. Chlopeň typu Core Valve před jejím umístěním do zaváděcího pouzdra 
Image 12. Chlopeň typu CoreVlave po jejím umístění do zaváděcího pouzdra. Vnější průměr katetru je 6 mm, což umožňuje zavedení punkčí cestou 
Po zahřátí na teplotu lisdkého těla se nitinolový koš rozepne na původní velikost. Tohoto principu je využito při vlastní implantaci, kdy je chlopeň postupně vysouvána z ochranného pouzdra (obr. 13), dochází k jejímu postupnému rozvíjení, což umožňuje chlopeň přesně usadit do aortálního anulu (obr. 14).
Image 13. Schéma postupného uvolňování chlopně ze zaváděcího pouzdra do aortální pozice 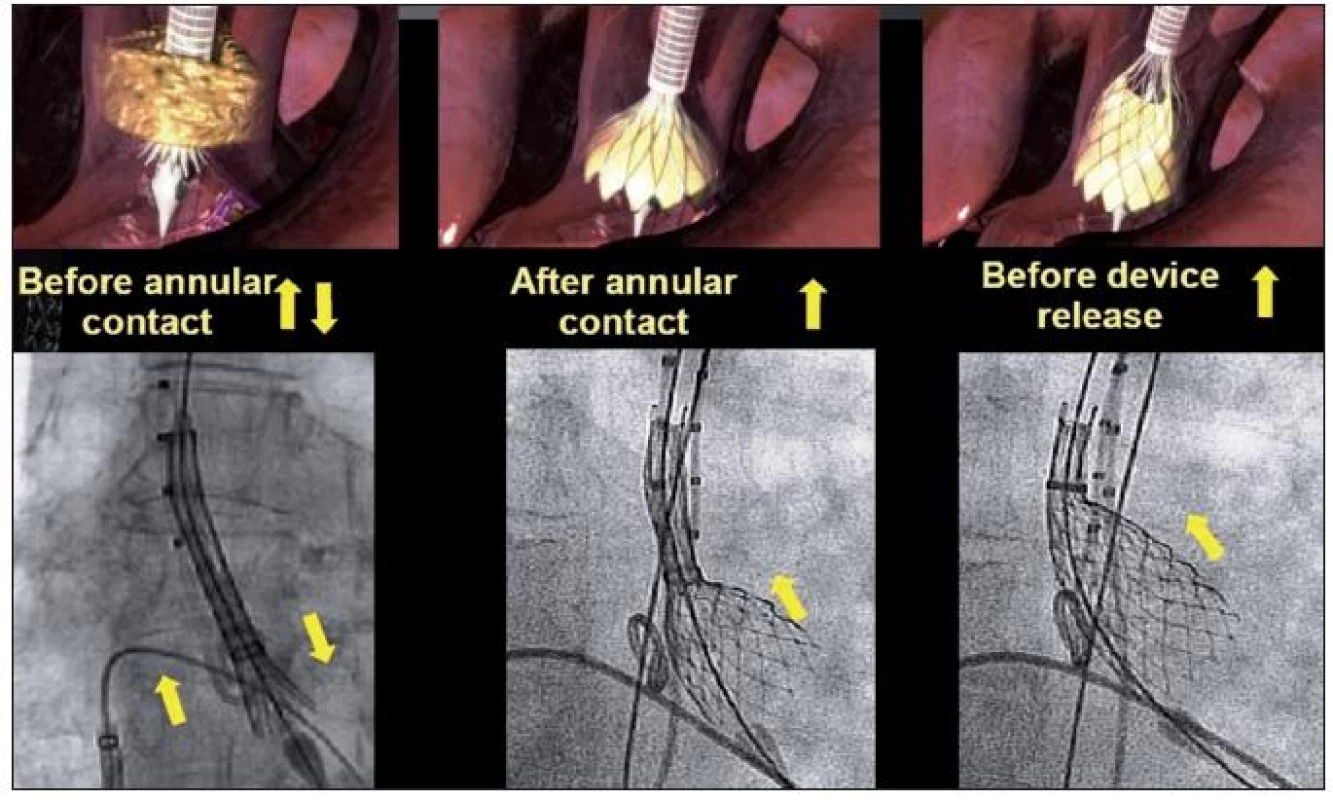
Image 14. Stav po implantaci chlopně – zaváděcí pouzdro je odstraněno, nástřik kontrastní látky do bulbu aorty prokazuje optimální pozici chlopně a nepřítomnost aortální regurgitace 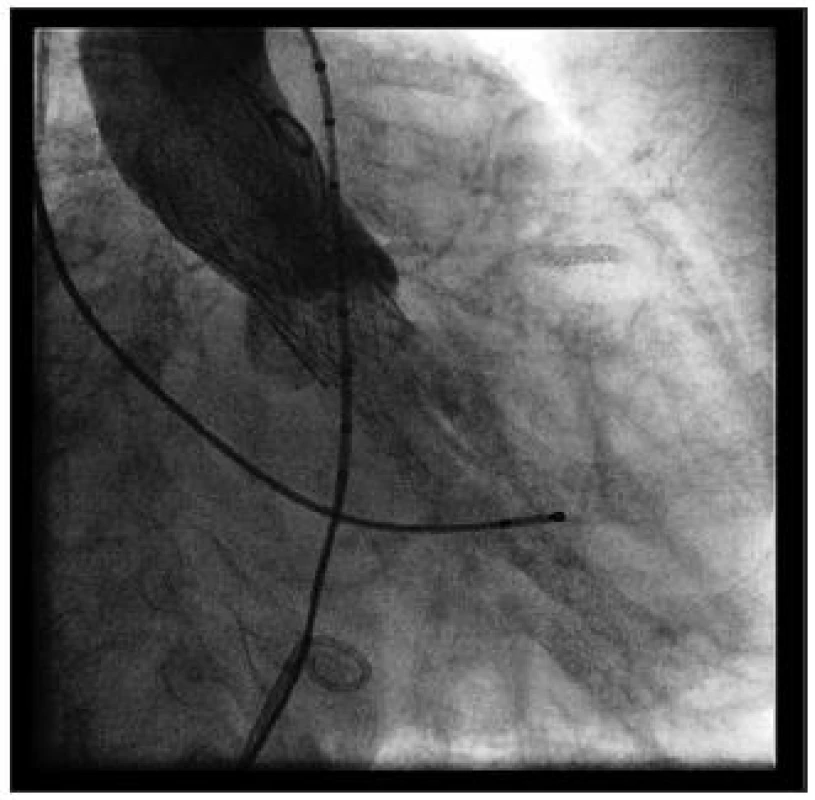
Po odstranění instrumentaria je punkční otvor ve femorální tepně uzavřen pomocí katetrizačně naložené sutury (obr. 15).
Image 15. Katetrizačně provedená sutura femorální tepny po odstranění zaváděcího pouzdra, žádné krvácení, jizva 1 cm 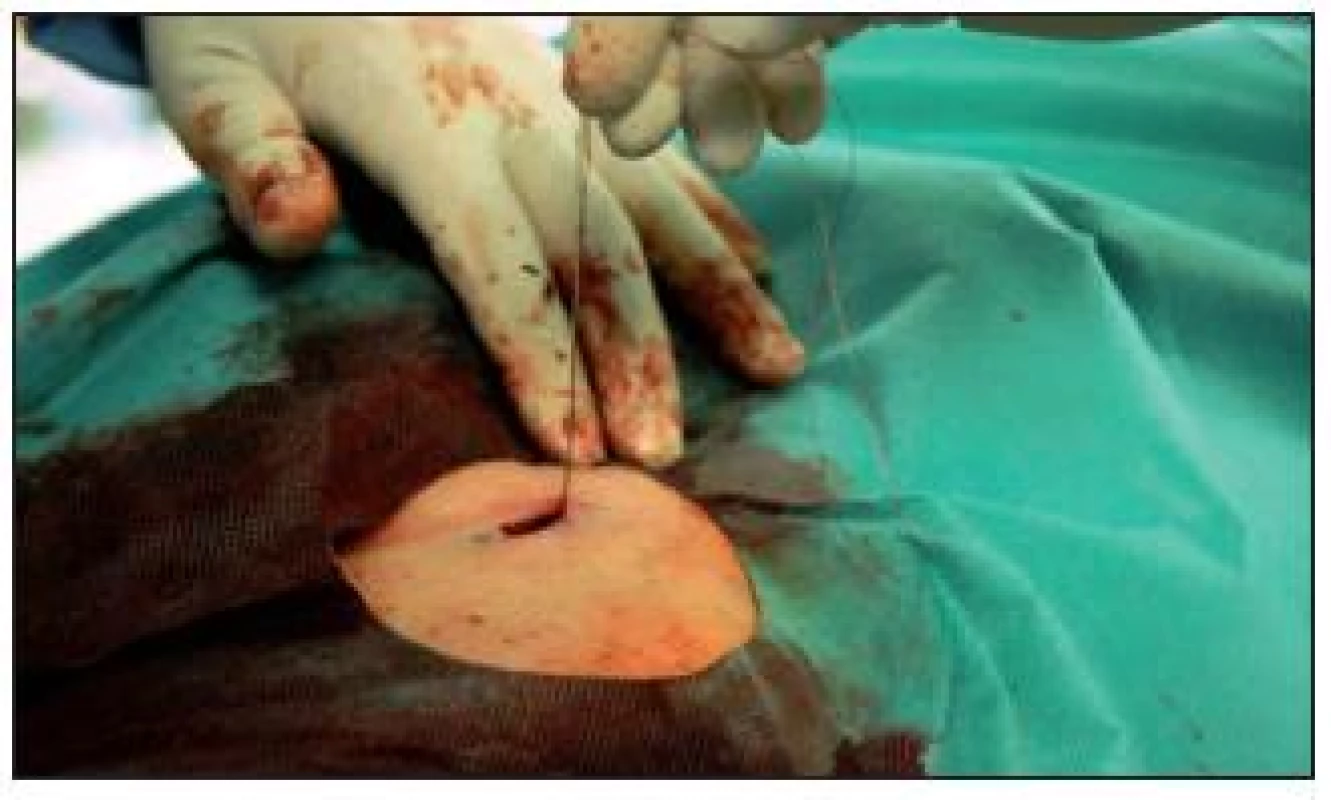
Chlopeň Sapien Edwards je vyrobena z hovězího perikardu a všita do ocelového (nová generace XT do chromkobaltového) velkého stentu. Chlopeň se stentem je umístěna na balónku a implantuje se jeho nafouknutím v aortální pozici.Tuto chlopeň je možné implantovat přístupem z femorální tepny nebo alternativně tzv. transapikálním přístupem přes hrot levé komory srdeční, kdy přístup k srdci a uzávěr otvoru v hrotu LK je však chirurgický (obr. 16).
Image 16. Chlopeň typu Sapien-Edwards a dvě přístupové cesty k implantaci: transfemorální a transapikální přes hrot levé komory 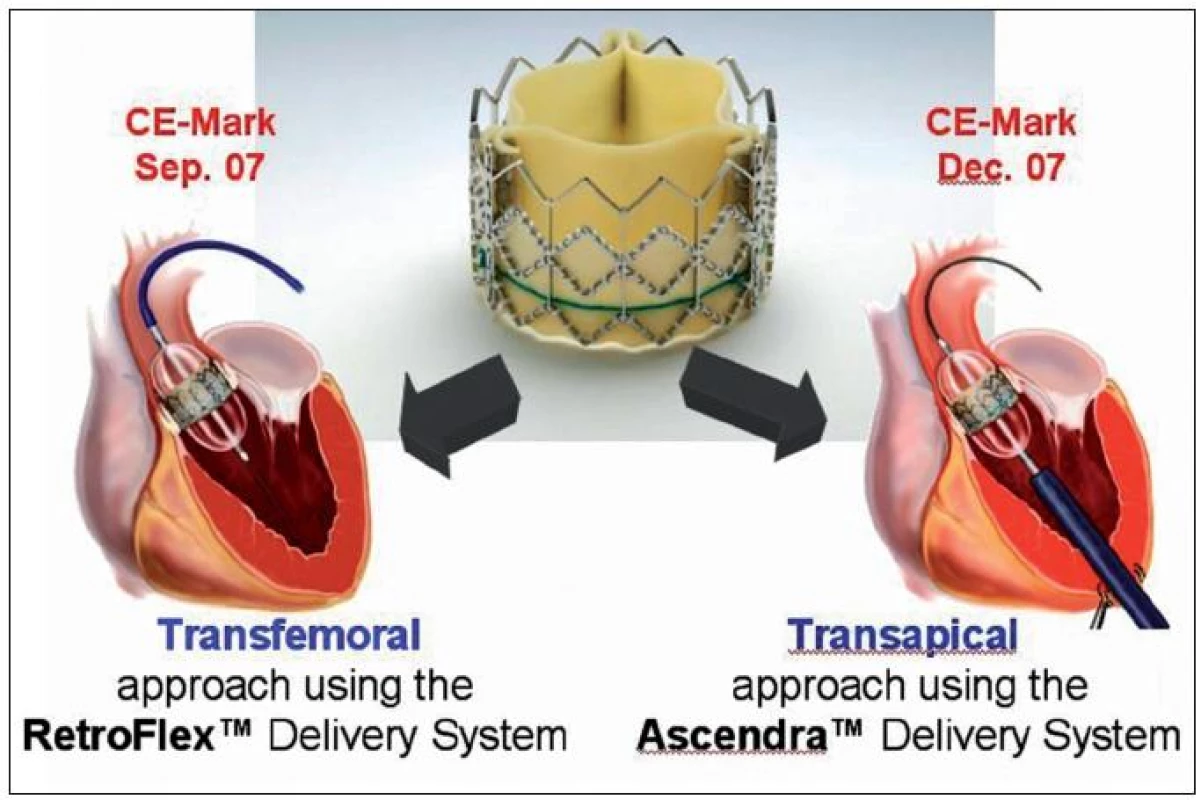
Katetrizační implantace aortální chlopně je prováděna u nemocných s významnou a klinicky symptomatickou aortální stenózou, kde klasická chirurgická operace není možná pro neúměrně vysoké riziko výkonu (věk nad 80 let, komorbidity kardiální či interní), nebo z důvodu problematického přístupu (stav po CABG, stavy po radiaci hrudníku apod).
V současné době je úspěšnost těchto výkonů nad 95 % a riziko závažných komplikací nepřesahuje 10 %. Funkce takto implatované chlopně je bezchybná po dobu 2–3 let (dosavadní doba sledování).
V České republice byl program TAVI zahájen v roce 2008 v pražském IKEMu (6) a počátkem roku 2009 v Hradci Králové (7).
2. 3. Katetrizační dilatace mitrální stenózy – perkutánní transluminální mitrální komisurotomie (PTMC)
Výkon spočívá v mechanické dilataci zúžené mitrální chlopně balónkovým katetrem – z více technik je dnes nejčastěji používána Inoue technika.
Nejprve je přístupem z femorální žíly proniknuto z pravé síně do levé síně (transseptální punkce), následně je do levé síně zaveden speciální dilatační katetr (tzv. Inoue balónek ve velikostech 24–30 mm). Nejdříve se nafukuje jeho distální část, a takto je proniknuto přes mitrální ústí. Poté se nafukuje proximální část balónku, čímž je tento fixován v mitrálním ústí. Při úplném nafouknutí se vyrovnává střední část balónku, která mechanicky oddělí srostlé cípy komisur (obr. 17).
Image 17. Katetrizační dilatace mitrální chlopně Inoue technikou 
K výkonu jsou indikováni nemocní s hemodynamicky významnou mitrální stenózou (plocha mitrálního ústí méně jak 1,5 cm2), kteří jsou limitováni námahovou dušností nebo mají již významnou plicní hypertenzi a mají vhodný anatomický nález k výkonu.
Úspěšnost výkonu je nad 90 %, excelentní výsledky jsou dosahovány zejména u mladých nemocných s těsnou stenózou a jemnou blanitou chlopní (8).
Výkon nelze provést u nemocných s těžce postiženou kalcifikovanou mitrální chlopní, při kalcifikacích v obou komisurách nebo při postižení závěsného aparátu mitrální chlopně.
Komplikací může být vznik významné mitrální regurgitace vyžadující chirurgickou náhradu chlopně (do 5 %), naopak vznik restenózy mitrální chlopně není častý. Výkony se provádějí v ČR od r. 1992, počty nemocných však v posledních letech nepřesahují desítky výkonů.
2. 4. Katetrizační dilatace stenózy chlopně plicnice – perkutánní pulmonální trasluminální valvuloplastika
Výkon spočívá v dilataci zúžené chlopně plicnice balónkovým katetrem. Ten je zpravidla snadno zaváděn přes femorální žílu do pravé síně, pravé komory a do stenotické plicnicové chloně. Jeho nafouknutím dojde k mechanickému oddělení cípů chlopně.
Výkon je indikován u nemocných s izolovanou valvulární stenózou chlopně plicnice, kdy vrcholový tlakový gradient přesahuje 50 mmHg, a klinicky je nemocný limitován námahovou duušností. Úspěšnost výkonu je prakticky 100%, komplikace minimální (9).
3. ZKRATOVÉ VADY SRDCE (10)
3. 1. Katetrizační uzávěr defektu septa síní
Defekt septa síní (DSS) je nejčastější vrozenou vadou srdce u dospělých, snad proto, že je hemodynamicky velmi dobře tolerován a klinicky se projevuje námahovou dušností nejčastěji po 20. roce života. Významný levopravý zkrat (150 % systémového průtoku a více) vede ke zvýšení průtoku plícemi a levou síní, která posléze dilatuje a vznikají suporaventrikulární arytmie. Zvýšený průtok plícemi vede k pasivní plicní hypertenzi při hyperkinetické plicní cirkulaci (námahová dušnost), hypertrofii a dilataci pravé komory, a trikuspidální regurgitaci.
Selhání pravé komory a fixovaná plicní hypertenze jsou známkou pokročilé vady. Anatomicky je nejčastěji (80 %) defekt septa síní uložen ve střední části septa (typ secundum) – tento typ je vhodný pro katetrizační uzávěr.
Pokud je defekt septa typu primum, pak je uložen spíše v dolní části septa a současně bývá postižena mitrální chlopeň (cleft) s mitrální regurgitací – tento typ je indikací ke komplexnímu kardiochirurgickému výkonu.
Katetrizačně lze uzavřít naprostou většinu DSS typu secundum (podmínkou je alespoň 5 mm okraj defektu od okolních struktur). Nejčastěji používaným instrumentariem je tzv. Amplatzův septální occluder, který se skládá ze dvou disků spojených středovou částí, která má průměr defektu a pevně vyplní celý defekt, přičemž oba disky mají pomocný fixační účinek (obr. 18).
Image 18. Amplatzův occluder používaný k uzávěru defektu septa síní 
Z femorální žíly je zaveden vodič přes defekt do levé síně, následně je velikost defektu změřena pomocí měkkého balónku naplněného ředěnou kontrastní látkou. Occluder je vyroben z nitinolu, který umožňuje zavátět jej v nataženém stavu přes poudro, které je přes defekt zavedeno do levé síně. Po vysunutí levosíňového disku tento okamžitě nabývá původního tvaru. Occluder je stažen na septum, je uvolněna jeho středová část, kterou je fixován v septu, a nakonec je vysunut i pravosíňový disk. Výsledná poloha je kontrolována pomocí jícnové (nebo intrakardiální) echokardiografie – pokud occluder těsní a je stabilní, je odpoután ze zaváděcího drátu (obr. 19 a 20).
Image 19. Echokardiografický obraz rozsáhlého defektu septa síní 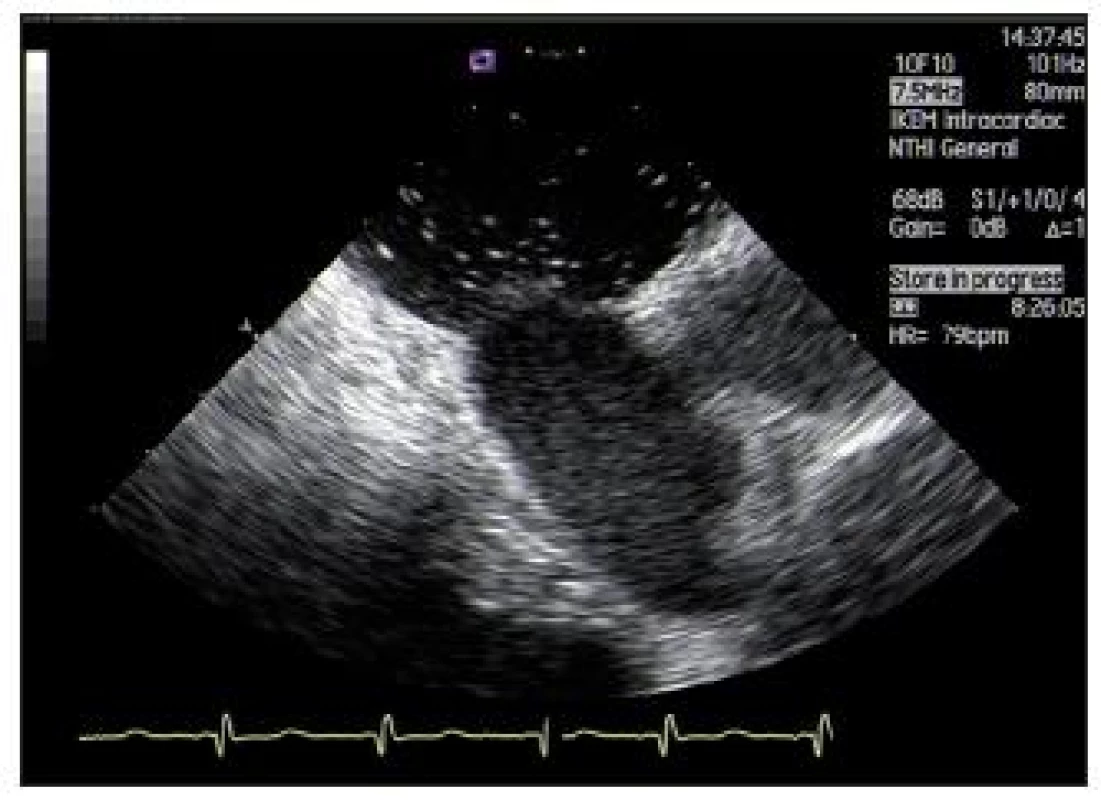
Image 20. Stejný nemocný po implantaci occluderu (dobře jsou vidět oba disky) 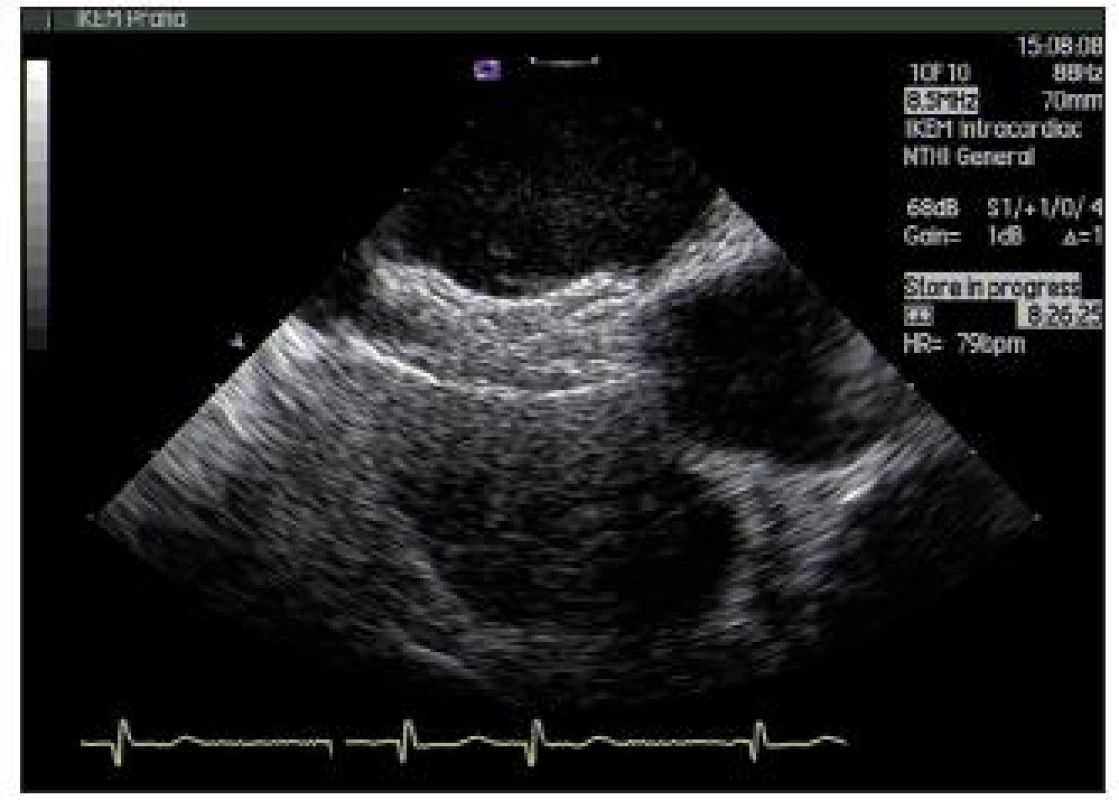
Výsledky těchto výkonů jsou vynikající, úspěšnost je nad 95 %, pouze defekty bez dostatečného okraje nebo mnohočetné defekty nelze spolehlivě uzavřít.
3. 2. Katetrizační uzávěr otevřeného foramen ovale
Foramen ovale patens (PFO) je častým nálezem v populaci (až u 15 %), nicméně ve spojení s aneuryzmaticky tenkým a vlajícím septem je častým nálezem u nemocných po prodělané mozkové příhodě embolizační etiologie. Pokud není prokázána jiná příčina, a to zejména u mladých nemocných bez známek aterosklerózy či průkazu síňových arytmií, je indikován katetrizační uzávěr PFO.
Technika je obdobná jako při uzávěru DSS, occluder má dva disky a 3 mm tenkou středovou část, odpadá měření velikosti defektu, zpravidla jde o jednoduchý výkon bez komplikací (obr. 21 a 22).
Image 21. Amplatzův occluder k uzávěru foramen ovale patens 
Image 22. RTG obraz zavedeného PFO occluderu ještě před jeho odpoutáním ze zaváděcího kabelu 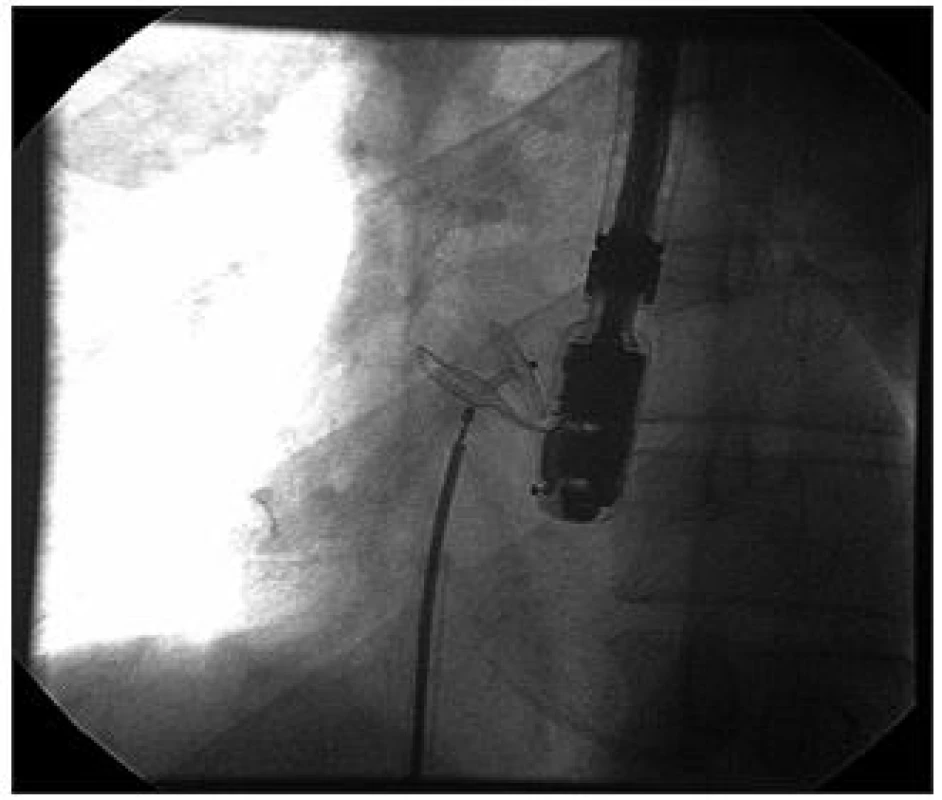
3. 3. Katetrizační uzávěry jiných (nejen zkratových) vad
Katetrizačně jze uzavírat i další zkratové vady pomocí různých typů occluderů – vděčným (i když málo častým) je uzávěr otevřené Botalovy dučeje, technicky naopak složitějším je uzávěr defektu septa komor (úspěšně lze uzavírat vrozené či rekanalizované defekty, případně neakutní poinfarktové defekty, naopak akutní defekty komorového septa vzhledem ke komplexnímu charakteru ruptury nejsou vhodné).
Mezi další možné indikace patří katetrizační uzávěr
- paravalvulárních leaků (velmi individuální úspěšnost),
- krčku pseudoaneurysmtu aorty (zpravidla u neoprabilních nemocných),
- koronární píštěle.
4. HYPERTROFICKÁ OBSTRUKČNÍ KARDIOMYOPATIE
4. 1. Alkoholová septální ablace
U nemocných s hypertrofickou kardiomyopatií dochází při rozvoji hypertrofie mezikomorového septa k dynamické obstrukci výtokového traktu, komora pak reaguje další hypertrofií na vzniklou obstrukci a vzniká námahová dušnost, případně synkopa. Extrémní hypertrofie je pak i významným arytmogenním substrátem. Odstranění subaortánní masy hypertrofického myokardu vede k ústupu gradientu ve výtokovém traktu levé komory a ústupu symptomů.
Chirurgicky prováděné myektomie jsou vzácné výkony.
Katetrizačně lze cíleně vyvolat selektivní nekrózu tohoto okrsku myokardu: nejprve je nutno provést koronarografii a zobrazit septální větev/větve, které tuto oblast septa zásobují (Obr. 23). Následně je do septální větve zaveden balónkový katetr, a tím je septální větev uzavřena (funkční test – gradient by měl vymizet), poté je luminem balonku podán echokontrast a zobrazena oblast, kterou septální větev zásobuje (anatomický test – musí se zobrazit oblast septa zodpovědná za obstrukci). Terprve poté je do septální větve injikováno malé množství (obvykle 0,5–1,5 ml) 96% ethanolu, čímž je vyvolána cílená koagulační nekróza této oblasti (obr. 24 a 25).
Image 23. Nemocný s hypertrofickou obstrukční kardiomyopatií, při koronarografii se dobře plní velká septální větev 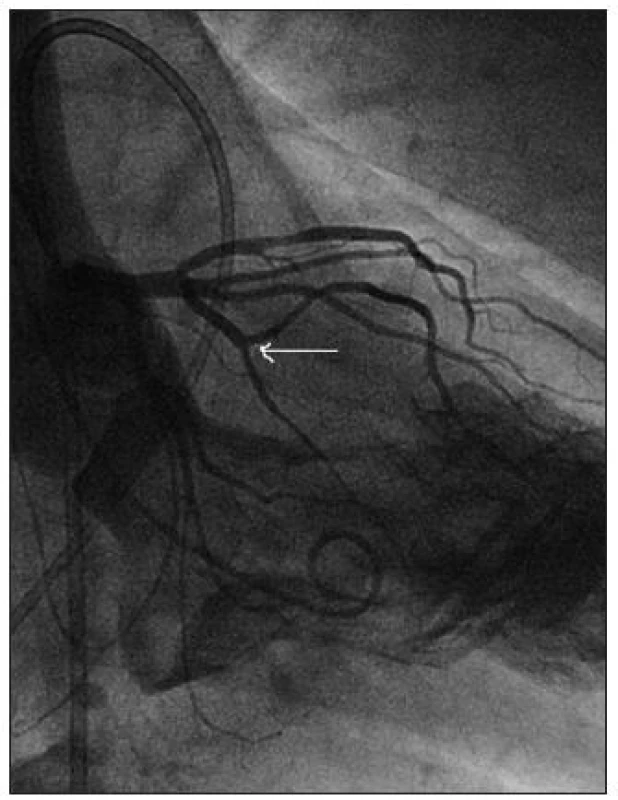
Image 24. Alkoholová septální ablace: do septální větve je zaveden balonkový katetr, po funkčním a anatomickém testu je podáno 1,0 ml 96% ethanolu 
Image 25. Nález po výkonu: septální větev je uzavřena 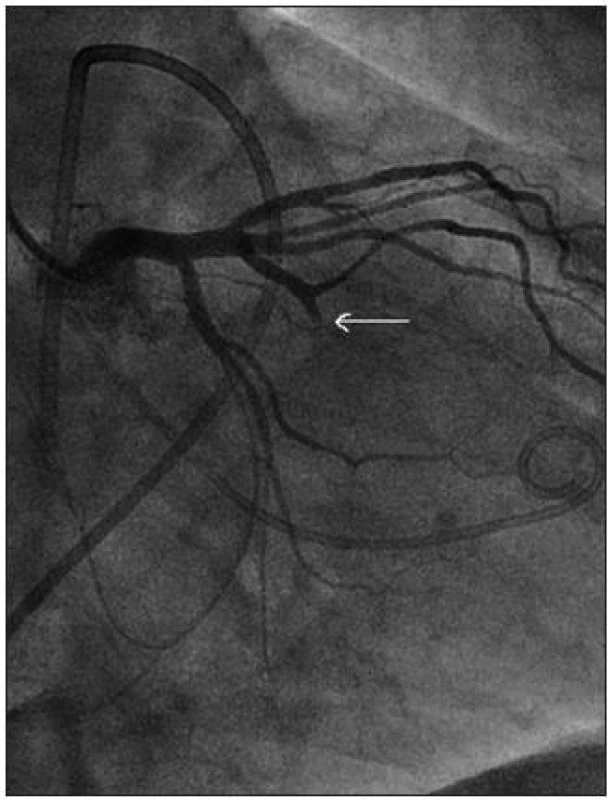
Během následujících 3 měsíců dochází k ústupu hypertrofie septa a vymizení gradientu.
Indikace jsou velmi individuální, nesmíme zapomenout, že nemocného na životě mohou u této choroby ohrožovat i maligní arytmie.
Závěr
Kardiologie prodělala velmi bouřlivý technologický rozvoj v minulých 20 letech, ať již v oblasti zobrazovacích technik (angiografie s 3D zobrazením či navigací, CT angiografie, MR, trojrozměrná echokardiografie, kombinovaná zobrazení – např. elektroanatomické mapování), či v oblasti intervencí (robotická navigace, magnetická navigace) a zejména v oblasti nových intervenčních metod.
Perkutánní implantace aortální chlopně je prvním takovým příkladem, nicméně další metody jsou již ve stadiu klinických zkoušek a nebylo možno je, vhledem k rozsahu sdělení, blíže popsat (např. katetrizační metody u mitrální regurgitace, uzávěr ouška levé síně), případně se prolínají s jinými obory (angioplastiky renálních tepen, karotických tepen apod.).
Indikace k intervenčním výkonům však zůstávají nadále individuální, vždy přísně zohledňující konkrétní riziko oproti přínosu. Jsou a budou závislé na lidském faktoru (zručnost, zkušenost ale i schopnost řešit případné komplikace), a proto by měly být prováděny pouze na takových centrech, které mají příslušné personální i technické vybavení.
MUDr. Michael Želízko, CSc.
Klinika kardiologie IKEM
Vídeňská 1958/9
140 21 Praha 4
E-mail: michael.zelizko@ikem.cz
Sources
1. Baim, D.S., Grossman, W. Cardiac Catheterization, Angiography and intervention. Fifth Edition. Baltimore, Maryland, USA: Wiliams & Wilkins,1996, p. 879. ISBN 0-683-03645-9
2. Endrys, J. Invazívní hemodynamické metody. Hradec Králové: Nucleus HK, 2005, s. 116. ISBN 80-86225-66-6.
3. Wijns, W., Kolh, P., Danchin N. et al. Guidelines on myocardial revascularization. The task force on myocardial revascularization of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). Europ. Heart. J. 2010, 38, S1-S52. Dostupné na: www.escardio.org/guidelines.
4. Želízko, M. Revaskularizace u akutních koronárních syndromů. Kardiofórum 2007, 5(3), s. 31-40.
5. Hamon, M., McFadden, E. Trans-radial approach for cardiovascular interventions. France: Europa Stethoscope Media, 2003, p. 283. ISBN: 2-9520202-0-5
6. Želízko, M., Malý, J., Janek, B. a kol. Transkatetrová implantace aortální chlopně CoreValve. Interv. Akut. Kardiol. 2010; 9(suppl. B), s. 9-13.
7. Šťásek, J., Bis, J. .Vojáček, J. a kol. Implantace balonem nesené chlopně Edwards Sapien u nemocných s aortální stenózou. Interv. Akut. Kardiol. 2010, 9(2), s. 9-13.
8. Fridrich, V., Mizera, S. Perkutánna valvuloplastika mitrálnej stenózy. Interv. Akut. Kardiol. 2010; 9 (suppl. B), s. 14-17.
9. Zelenay, J., Fridrich, V. Perkutánna translumenová valvuloplastika izolovanej chlopňovej pulmonálnej stenózy u dospelých. Interv. Akut. Kardiol. 2010, 9 (suppl. B), s. 21-24
10. Šťásek, J. Intervence chlopenních a zkratových srdečních vad dospělých. Hradec Králové: H.R.G. Litomyšl, 2006, s.100. ISBN 80-86703-18-5.
Labels
General practitioner for children and adolescents General practitioner for adults
Article was published inGeneral Practitioner

2011 Issue 1-
All articles in this issue
- Centrum diabetologie a diabetologický program v IKEM
- Přehled počtu odběrů orgánů a transplantací v IKEM v letech 1990–2009
- Transplantace pankreatu dříve a nyní
- Aktuality v prevenci a léčbě syndromu diabetické nohy; program podiatrické péče v IKEM
- Perorální antidiabetika
- Notes: minulost, současnost, budoucnost
- Vyšetření nemocných zařazovaných na čekací listinu k transplantaci ledviny
- Intervenční kardiologie: co nabízí v roce 2011
- Lékárna IKEM – součást komplexní péče o pacienty
- General Practitioner
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Vyšetření nemocných zařazovaných na čekací listinu k transplantaci ledviny
- Perorální antidiabetika
- Centrum diabetologie a diabetologický program v IKEM
- Aktuality v prevenci a léčbě syndromu diabetické nohy; program podiatrické péče v IKEM
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

