-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Dysfunkčný dialyzačný cievny prístup a jeho endovaskulárna liečba
Hemodialysis vascular access dysfunction and its endovascular treatment
Hemodialysed patients with end stage renal disease are reliant to proper function of vascular access – mostly arterio-venous fistula (AVF). AVF patency is jeopardized by stenosis formation, which needs to be treated before thrombosis. Angioplasty is primarily indicated and prolongs vascular access patency. High pressure balloons and cutting balloons aid to high technical success rate. Angioplasty needs to be repeated in order to maintain long term patency. Drug-eluting balloons prolong long term patency. Stents and stentgrafts are seldom used in inoperable patients and in selected locations. Technical advances allowed endovascular treatment in AVF thrombosis followed by angioplasty of culprit lesion. Vascular access endovascular occlusion is alternative for surgery in inoperable patients. In patients with residual renal function or iodine allergy, intervention could be ultrasound guided or carbon dioxide could be used without the need of iodine contrast.
Keywords:
Angioplasty – arterio-venous fistula stenosis – central venous stenosis – endovascular treatment – hemodialysis
Autoři: Martin Vorčák 1; Kamil Zeleňák 1; Ján Sýkora 1; Alena Ježíková 2; Marián Mokáň 2
Působiště autorů: Rádiologická klinika JLF UK a UN Martin, Slovenská republika 1; I. Interná klinika JLF UK a UN Martin, Slovenská republika 2
Vyšlo v časopise: Vnitř Lék 2020; 66(6): 14-18
Kategorie: Přehledové články
Souhrn
Hemodialyzovaní pacienti so zlyhanými obličkami sú odkázaní na fungujúci cievny prístup – najčastejšie arterio-venóznu fistulu (AVF). Jej životnosť je ohrozená vznikom stenóz, ktoré je potrebné riešiť pred vznikom trombózy. Primárnou liečbou väčšiny stenóz je angioplastika, ktorá predlžuje jej životnosť. Vysoký technický úspech je dosiahnutý pomocou vysokotlakých balónikov a balónikov s čepieľkami. Z hľadiska dlhodobej priechodnosti je potrebné angioplastiku často opakovať. Primárnu priechodnosť zvyšujú balóniky uvoľňujúce cytostatikum. Stenty a stentgrafty sa v oblasti AVF používajú zriedka u inoperabilných pacientov a vo vybraných lokalitách. Rozvoj techník umožnil endovaskulárnu liečbu trombózy fistuly, po ktorej zároveň nasleduje angioplastika príčinnej stenotickej lézie. Endovaskulárne oklúzne techniky AVF sú alternatívou chirurgie u inoperabilných pacientov. U pacientov so zachovanou funkciou obličiek alebo s alergiou je možné intervenciu navigovať bez použitia jódovej kontrastnej látky, a to pod ultrazvukovou kontrolou prípadne použitím oxidu uhličitého.
Klíčová slova:
angioplastika – centrálna venózna stenóza – dialýza – endovaskulárna liečba – stenóza arterio-venóznej fistuly
Úvod
Chronické obličkové ochorenie vo svojom poslednom (5.) štádiu končí náhradou funkcie obličiek. Metódy náhrady funkcie obličiek predstavujú: hemodialýza, transplantácia obličiek a peritoneálna dialýza. V roku 2018 bolo v Českej republike dialyzovaných 659 pacientov na milión obyvateľov (1). Na zabezpečenie dostatočnej hemodialýzy je potrebný funkčný cievny prístup, podľa možností natívna artério-venózna fistula (AVF), artério-venózny graft (AVG), centrálny venózny katéter alebo dialyzačný port. Nevýhodou dialyzačného prístupu je jeho životnosť, ktorá je nízka. Na predĺženie životnosti AVF alebo AVG volíme primárne endovaskulárne techniky, najmä angioplastiku. Napriek vysokému technickému úspechu je dlhodobá priechodnosť po angioplastike nízka a na jej udržanie sú potrebné opakované intervencie. Na prevenciu nefrotoxicity a alergických reakcií jódovej kontrastnej látky je možné intervenciu navigovať pomocou ultrasonografickej kontroly prípadne ako kontrastnú látku využiť oxid uhličitý. V článku je poskytnutý prehľad endovaskulárnych techník, ich indikácií a výsledkov v liečbe dysfunkčnej dialyzačnej fistuly.
Hemodialyzačný prístup
Typ prístupu na hemodialýzu volíme podľa predpokladaného priebehu obličkového ochorenia u konkrétneho pacienta a adekvátnosti jeho arteriálneho a venózneho systému. Použitie AVF je výrazne vyššie v Európe v porovnaní so Spojenými štátmi (83 % vs 21 %), oproti tomu zastúpenie AVG je v týchto krajinách opačné (2 % vs 24 %) (2). Po vytvorení skratu dochádza k maturácii AVF. Do 4–8 týždňov od vytvorenia by mala byť fistula ľahko palpovateľná a kanylovateľná pomocou dvoch 17 G ihiel. Primárne zlyhanie charakterizujeme ako nepoužiteľnosť AVF na dialýzu po jej chirurgickom vytvorení a dostatočnom čase na maturáciu. Podľa literárnych údajov sa jedná o značnú časť AVF (28–53 %) (3). Patogeneticky sa v tomto prípade uplatňuje najmä neointimálna hyperplázia v juxtaanastomotickej oblasti. Medián zlyhania natívnej AVF je 4,5 roka (4). V prípade neskorého zlyhania sa jedná najčastejšie o vznik stenózy na odvodnej žile, ktorá je spôsobená výrazným napätím na tenkostennú žilu a následnou fibromuskulárnou hyperpláziou, alebo opakovanými vpichmi pri kanylácii a prítomnosťou venóznych chlopní (5). Centrálne venózne stenózy vznikajú najčastejšie po zavedených hemodialyzačných katétroch. V prípade zavedenia centrálneho katétra cestou v. subclavia je výskyt významného zúženia evidentne vyšší – 42–50 % v porovnaní s 0–10 % pri zavedení cestou VJI (6). Zlyhanie fistuly na podklade arteriálnej stenózy je vzácne a zodpovedá približne 5 % pacientov (7).
Primárne zlyhanie AVG je v porovnaní s AVF nízke a vyskytuje sa približne v 20 %. Technologický pokrok materiálov používaných na vytvorenie AVG v dnešnej dobe umožňuje skorú punkciu graftu (do 48–72 hod) a zároveň znižuje komplikácie prítomné pri štandardných typoch ako sú hematómy, serómy a infekcie graftu (8). Tieto výhody sú však znevýhodnené nižšou primárnou ročnou priechodnosťou, ktorá dosahuje 30–50 % (9) a 3–7-krát vyššou mierou intervencií na udržanie priechodnosti v porovnaní s natívnou AVF (10).
Dialyzačné katétre a port katétre využívame pri akútnej či krátkodobej dialýze na preklenutie obdobia do vytvorenia definitívneho prístupu alebo v prípade nemožnosti iného cievneho prístupu pri chronickej dialyzačnej liečbe.
Monitoring cievneho prístupu
Zlyhávanie dialyzačného prístupu sa klinicky prejaví miznutím šelestu nad anastomózou, ťažkosťami pri punkcii, aspiráciou trombotického materiálu, opuchom končatiny alebo aj predĺženou dobou krvácania po dialýze. K zmenám dochádza aj v parametroch dialýzy - zmeny venózneho tlaku, recirkulácie, klesanie prietoku (11). Odporúčané je pravidelné klinické hodnotenie funkcie AVF raz týždenne, pomocou parametrov dialýzy raz mesačne. Klinické vyšetrenie napomáha pri lokalizácii stenózy v oblasti AVF, avšak môže byť aj normálne a to najmä na venóznej strane graftu – v jednej štúdii bola nameraná senzitivita takéhoto vyšetrenia 57 % (12). Známky zlyhávania funkcie AVF sú indikáciou na ultrazvukové vyšetrenie (7). Dodržiavanie prísneho monitoringu cievneho prístupu je veľmi dôležité, pretože dokáže odhaliť zlyhávajúci prístup pred jeho trombózou. Je dokázané, že životnosť AVF po rekanalizácii trombózy je nižšia ako po angioplastike, a že liečba významných stenóz pomocou PTA predlžuje použiteľnosť dialyzačného prístupu (8).
Endovaskulárna liečba dysfunkčnej dialyzačnej fistuly
Na ošetrenie sú indikované stenózy významnejšie ako 50 % (13). Medzi výhody endovaskulárneho ošetrenia stenóz dialyzačných AVF patrí vysoká technická úspešnosť procedúry s nízkou mierou komplikácií, zachovaním hlavnej odvodnej vény a v prípade technického neúspechu alebo skorého zlyhania stále zostáva dostupná možnosť sekundárneho chirurgického ošetrenia (14). Výhodou endovaskulárneho ošetrenia v porovnaní s chirurgickými technikami je aj okamžitá možnosť použitia fistuly na dialýzu, bez nutnosti zavedenia dočasného centrálneho dialyzačného katétra. Jednoduchá angioplastika s použitím balónika (plain old balloon angioplasty – POBA) má približne 90% technickú úspešnosť (15). V prípade lézie rezistentnej na liečbu pomocou POBA je vhodné použiť vysokotlakové alebo ultravysokotlakové balónikové katétre (30 ATM), alebo vykonať angioplastiku s použitím balónikového katétra s čepieľkami – cutting balloon (Obr. 1). Tieto metódy zvyšujú technickú úspešnosť blížiacu sa až 100 % (16). Primárna priechodnosť endovaskulárneho ošetrenia stenóz je u AVF 67 % po roku (15). Vysoká miera reintervencií nás núti hľadať možnosti na predĺženie intervalu medzi intervenciami. Použitie drug eluting balónikových katétrov (DEB), ktoré uvoľňujú cytostatikum (napr. paclitaxel) zabraňujúce proliferácii, sa už na tento účel osvedčilo v koronárnej a periférnej arteriálnej intervencii. Metaanalýza Kennedy et al porovnávajúca použitie POBA a DEB v oblasti AVF dokázala signifikantne vyššiu priechodnosť AVF po 3, 6, 12 a 24 mesiacoch v prípade použitia DEB (17).
Obr. 1. Angioplastika rezistentnej lézie pomocou balónika s čepieľkami
Angiografia predlaktia s rádio-cefalickou AVF s dvoma tesnými stenózami na odvodnej véne tesne za anastomózou a v jej ďalšom priebehu (A). Balónik nekompletne rozvinutý v oblasti rezistentnej lézie (B), Následná dilatácia rezistentných lézií pomocou balónika s čepieľkami s jeho kompletným rozvinutím (C) s konečným výsledkom bez reziduálnej stenózy (D)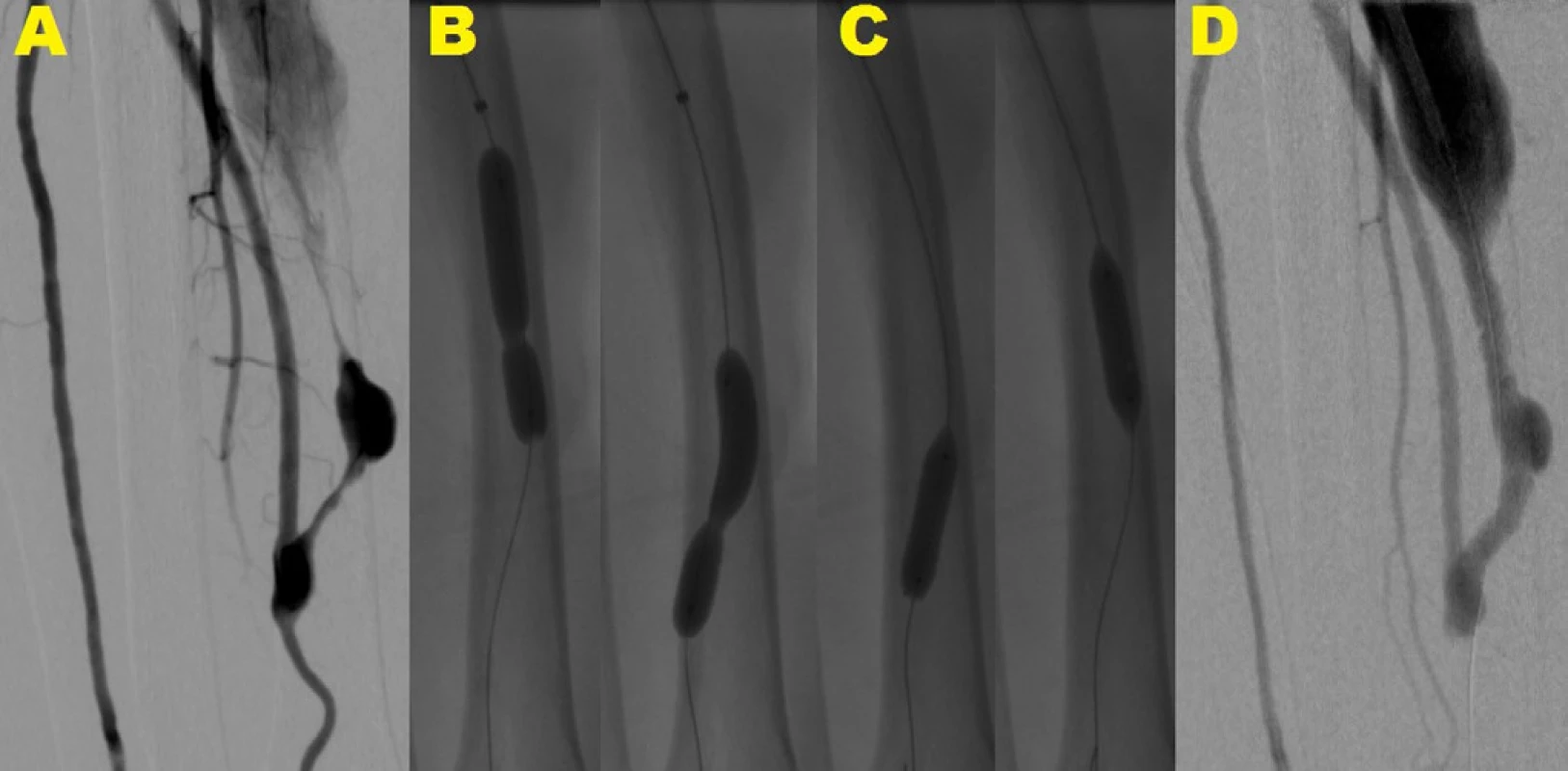
Použitie stentu je pri intervenciách na AVF vzácne a podľa štúdií výrazne nezmení priechodnosť AVF. Do úvahy prichádza ako záchranná technika u rezistentnej lézie prípadne opakovanej intervencii za obdobie kratšie ako 3 mesiace a to u pacientov, u ktorých je z rôznych príčin vyčerpaná chirurgická intervencia. Nové práce s použitím pleteného stentu Supera naznačujú jeho výhody z hľadiska primárnej priechodnosti a nízkej miery opakovaných intervencií (18).
Použitie stentgraftu je limitované, avšak novšie práce naznačujú ich využitie vo viacerých oblastiach dialyzačného okruhu. Z hľadiska priechodnosti je odporúčané ich využitie u stenóz venózneho konca graftu (19) a tiež v oblasti tzv. „cephalic arch“ stenózy v oblasti sútoku v. cephalica s v. axillaris a „swing stenózy“ v oblasti tzv. brachiálno-bazilického uhla transpozície u transponovanej brachio-bazilickej fistuly (20, 21). Samozrejmé je použitie stentgraftov v prípade ruptúry vény. V poslednej dobe sa ich použitie osvedčilo aj v prípade centrálnej venóznej stenózy (22, 23).
Centrálna venózna stenóza a uzáver
Centrálna venózna stenóza sa prejaví zvýšeným tlakom vo venóznom systéme končatiny, opuchom, zmenami koloritu končatiny, dilatáciou kolaterálnych vén na ramene a hrudníku. U dialyzovaných pacientov vznikajú stenózy v tomto segmente ako následok poranenia žily po zavedení dočasného dialyzačného katétra, ktorý je často používaný ako iniciálny cievny prístup pre dialýzu. Tieto anatomické oblasti sú veľmi zle dostupné pre chirurga, preto je angioplastika liečebnou metódou prvej voľby symptomatickej centrálnej venóznej stenózy, i keď na dosiahnutie dlhodobej priechodnosti sú často potrebné opakované intervencie (24). Primárna priechodnosť po PTA dosahuje medzi 23–63 % po 6 mesiacoch a 12–50 % po roku (25). Dilatácia asymptomatickej stenózy môže urýchliť jej progresiu a objavenie symptómov v porovnaní s konzervatívnym postupom. Asymptomatické lézie nevyžadujú liečbu a mali by byť sledované. Stentingu v oblasti centrálnych vén, najmä v oblasti v. subclavia sa snažíme vyhýbať, implantácia stentov je rezervovaná pre lézie s výrazným recoil fenoménom a pre lézie, ktoré sa objavia opakovane do 3 mesiacov od liečby (Obr. 2). Primárna priechodnosť lézií po implantácii stentov sa výrazne nelíši od priechodnosti po PTA. V liečbe symptomatických rezistentných stenóz, skorého zlyhania intervencie a restenóz po predošlej implantácii stentu boli aj v lokalite centrálnych vén odskúšané stentgrafty (22, 23). Pri uzávere centrálnych vén sa výrazne znižuje technický úspech procedúry (26).
Obr. 2. Angioplastika a stenting v. brachiocephalica vpravo
Angiografia centrálnych žíl s tesnou stenózou v. brachiocephalica vpravo, kolaterálne plnenie cestou v. brachiocephalica vľavo a v. cava superior. Angioplastika s 10 mm balónikom s nedostatočným efektom (B, C) s následnou implantáciou samoexpandovateľného stentu 14 × 40 mm s jeho dodilatáciou pomocou 12 mm balónika (D, E). Kontrolná angiografia s konečným výsledkom bez reziduálnej stenózy, bez plnenia kolaterál (F)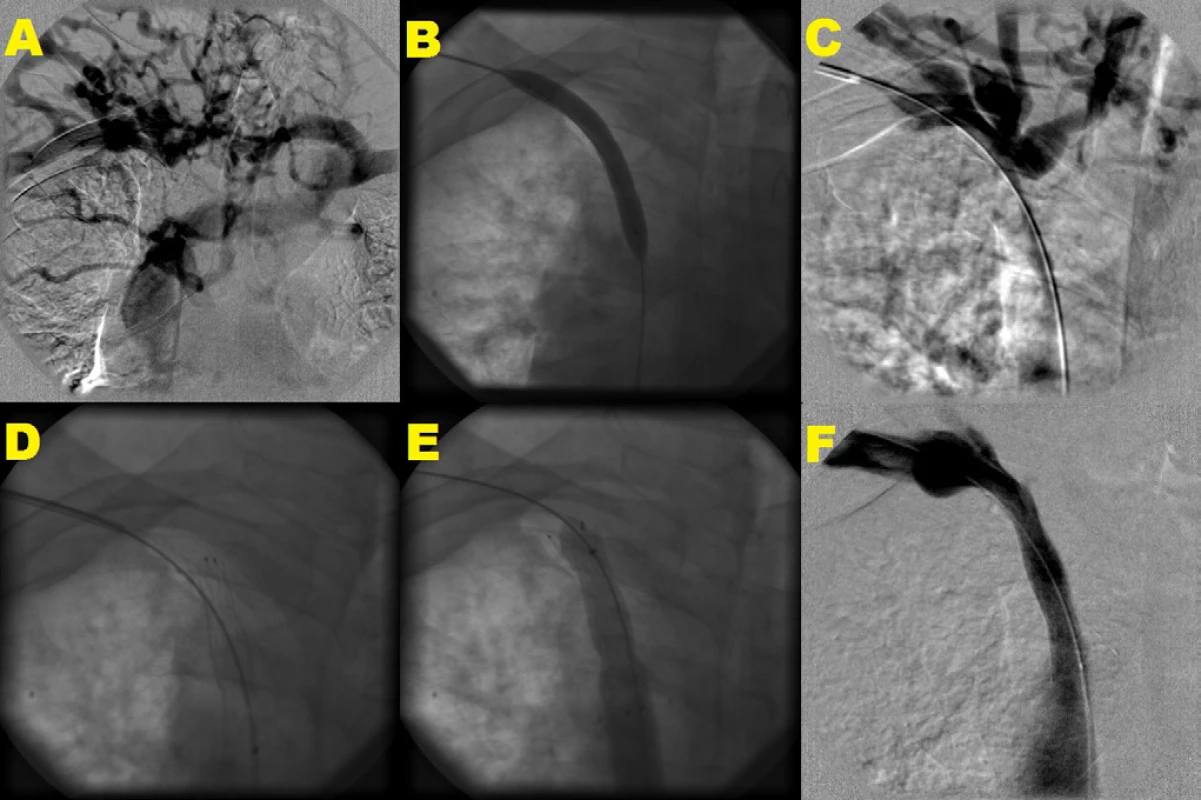
Trombóza
Endovaskulárne techniky liečby trombózy v dnešnej dobe výrazne pokročili a uplatňujú sa aj pri trombotickom uzávere venózneho prístupu. Samotná trombektómia sa vykonáva aplikáciou viacerých endovaskulárnych techník – ako pulzná spejová trombolýza, tzv. „lyse-and-wait“ technika, doplnková balóniková trombektómia pomocou Fogartyho balónika alebo techniky mechanickej a farmako-mechanickej trombektómie ako systémy Arrow-Trerotola, AngioJetTM, Argon Cleaner XTTM. Technická úspešnosť endovaskulárnej rekanalizácie trombotizovaného cievneho prístupu je nad 90 %, problémom však ostáva nízka dlhodobá priechodnosť (27). V prípade, že je trombektómia realizovaná chirurgicky, je následne odporúčaná fistulografia s angioplastikou príčinnej lézie. Odporúčaný čas do záchrany prístupu od vzniku ťažkostí je u AVF do 48 hod, u pacientov s graftom do týždňa, avšak pre vyhnutie sa zavedenia dialyzačného katétra sa odporúča vykonať trombektómiu do 48 hod. Kontraindikáciou liečby trombotizovanej AVF je fistula so známkami aktívneho zápalu, veľké aneuryzmy odvodnej vény s veľkým množstvom trombotických hmôt, zlá kardiopulmonálna rezerva, pravo-ľavý skrat a tiež skorá trombóza nedávno konštruovaného AV prístupu (28).
Endovaskulárna oklúzia v oblasti dialyzačného prístupu
Oklúzia dialyzačného prístupu je v niektorých klinických situáciách, ako sú závažný steal fenomén, kardiálna dekompenzácia, výrazný opuch končatiny pri neriešiteľnej venóznej lézii či hyperfunkčnej fistule nutná. Najčastejšie sa realizuje chirurgicky, avšak aj chirurgické postupy majú svoje limity, najmä pri zložitej anatómii a výraznom opuchu, ktorý znemožňuje hojenie rany. Oklúziu výrazných kolaterálnych a akcesórnych vén vykonávame na presmerovanie toku krvi do hlavnej drenážnej vény pri nedostatočnej funkcii fistuly, bez nálezu zúženia v jej priebehu. Alternatívou k chirurgickým technikám je u týchto pacientov endovaskulárna oklúzia celého prístupu alebo vén pomocou cievnej zátky Amplatzer (Amplazer vascular plug). Implantácia Amplatzera je jednoduchá procedúra, ktorá zabezpečí rýchly uzáver okludovanej cievy. V prípade jeho využitia pri uzávere AVF alebo kolaterálnych odvodných vén je po dôslednom multidisciplinárnom zvážení doplnkovou metódou u pacientov nevhodných k chirurgickému zákroku (29).
Endovaskulárna liečba u pacientov so zachovanou funkciou obličiek a alergiou
Endovaskulárne výkony sú štandardne realizované s použitím jódových kontrastných látok. Ich použitie je u pacientov s cievnym prístupom limitované štádiom CDK a alergickými reakciami. Kritickú skupinu pacientov predstavujú pacienti s našitou fistulou s reziduálnou funkciou obličiek, prípadne transplantovanou obličkou a pacienti s alergiou na jódovú kontrastnú látku. V tomto prípade je možné využiť na zobrazenie stenózy a realizáciu intervencie navigáciu pomocou ultrazvuku (Obr. 3) prípadne angiografiu realizovať pomocou oxidu uhličitého (CO2), ktorá je u týchto pacientov nápomocná najmä v prípade podozrenia na centrálne venózne stenózy. Technický úspech výkonov je aj v prípade využitia zobrazovacích alternatív vysoký (30).
Obr. 3. Angioplastika odvodnej vény navigovaná pomocou ultrazvuku
Zúženie odvodnej vény (A) s následnou angioplastikou tejto oblasti (B) a rozvinutím lumen vény po dilatácii (C). Úprava toku v a. brachialis – po dilatácii došlo k zvýšeniu prietoku z 396 ml/min na 645 ml/min a poklesu odporového indexu (RI) z 0,62 na 0,49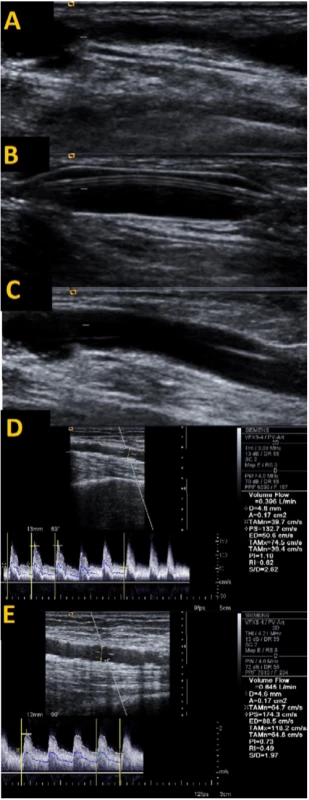
Záver
Endovaskulárne možnosti liečby dysfunkčného dialyzačného prístupu, jednak v prípade udržiavania funkcie ako aj záchrany prístupu, postupne nahradili chirurgické techniky. Ich nespornou výhodou je zachovanie liečeného venózneho segmentu vzhľadom na limitované možnosti konštrukcie AVF. Angioplastika predlžuje životnosť fistuly. Či už na periférnych, alebo na centrálnych vénach sú však na zabezpečenie dlhodobej priechodnosti potrebné opakované intervencie. Primárnou technikou liečby stenóz na AVF je angioplastika s prípadným použitím vysokotlakových balónikových katétrov, alebo balónikových katétrov s čepieľkami v prípade rezistentných lézii. Na základe pribúdajúcich dát sa pri liečbe stenóz AVF čoraz viac využívajú DEB a to vďaka dlhšej primárnej priechodnosti lézie a nižšej miere reintervencií pri rovnakej technickej úspešnosti. Implantácii stentov sa snažíme vyhýbať, v oblasti centrálnych vén je v niektorých rezistentných prípadoch ich použitie neodkladné. Použitie stentgraftov je rezervované pre prípadnú periprocedurálnu ruptúru žily, v oblasti venóznej stenózy graftu a s menšou váhou dôkazov aj v oblasti proximálnej v. cephalica, v. basilica a centrálnych vén. Vzhľadom na lepšiu životnosť fistuly po angioplastike ako po rekanalizácii trombózy je na optimálnu funkciu AVF nutný jej prísny monitoring. V prípade trombózy sa v dnešnej dobe uplatňujú mnohé rekanalizačné endovaskulárne techniky s vysokou technickou a klinickou úspešnosťou. Výhodou endovaskulárnych techník je možnosť dialýzy po zákroku, čo ochráni pacienta pred zavedením dočasného dialyzačného katétra. Oklúzne endovaskulárne techniky by mali byť použité až po pozornom zvážení pri nemožnosti chirurgickej intervencie. Na zabránenie kontrastom indukovanej nefropatie u pacientov so zostatkovou funkciou obličiek a u pacientov s alergiou na jódovú kontrastnú látku je možné intervenciu navigovať pomocou ultrazvuku prípadne ako kontrastnú látku použiť oxid uhličitý. Endovaskulárna liečba výrazne ovplyvnila manažment pacienta s dialyzačnou AVF. Jej miniinvazívny charakter umožňuje ambulantné riešenie väčšiny procedúr. Pre správnu a včasnú indikáciu je potrebné klinické a sonografické sledovanie. Úzka spolupráca nefrológa, chirurga a rádiológa prispieva k zabezpečeniu dlhodobej funkcie dialyzačného prístupu.
KORESPONDENČNÍ ADRESA AUTORA:
doc. MUDr. Kamil Zeleňák, PhD., FCIRSE, EBNI,
Rádiologická klinika JLF UK a UN
Kollárova 2,
036 01 Martin,
Slovenská republika
Cit. zkr: Vnitř Lék 2020; 66(6): e14–e18
Článek přijat redakcí: 24. 11. 2019
Článek přijat po recenzích k publikaci: 7. 1. 2020
Zdroje
1. Rychlík I, Lopot F. Statistická ročenka dialyzační léčby v České republice, 2018. Česká nefrologická společnost. (cit. 2019-10-17). Dostupné z WWW: http://www.nefrol.cz/odbornici/dialyzacni-statistika
2. Pisoni RL, Young EW, Dykstra DM, et al. Vascular access use in Europe and the United States: results from the DOPPS. Kidney Int 2002; 61 : 305–316.
3. Pajek J, Malovrh M. Preoperative ultrasound still valuable for radio-cephalic arteriovenous fistula creatio. J Vasc Access 2017; 18 : 5–9.
4. Medkouri G, Aghai R, Anabi A, et al. Analysis of vascular access in hemodialysis patients: a report from a dialysis unit in Casablanca. Saudi J Kidney Dis Transpl 2006; 17 : 516–520.
5. Nikolic B. Hemodialysis Fistula Interventions: Diagnostic and Treatment Challenges and Technical Considerations. Tech Vasc Interv Radiol 2008; 11 : 167–174.
6. Roček M. Obnovení funkce hemodialyzačního cévního přístupu. In: Krajina A, Peregrin J et al. Intervenční radiologie: miniinvazívní terapie. Olga Čermeková: Hradec Králové 2005 : 258–268.
7. Lockhart ME, Robbin ML, Needleman L, et al. ACR-AIUM-SRU Practice Parameter for the Performance of Vascular Ultrasound for Postoperative Assessment of Dialysis Access. J Ultrasound Med 2014; 33 : 1321–1332.
8. Al Shakarchi J, Inston N. Early cannulation grafts for haemodialysis: An updated systematic review. J Vasc Access 2019; 20 : 123–127.
9. Vazquez-Padron RI, Allon M. New Insights into Dialysis Vascular Access: Impact of Preexisting Arterial and enous Pathology on AVF and AVG Outcomes. Clin J Am Soc Nephrol 2016; 11 : 1495–1503.
10. Vascular Access 2006 Work Group. NKF-DOQI clinical practice guidelines for vascular access, update 2006. Am J Kidney Dis 2006; 48 : 176–306.
11. Bent CL, Sahni VA, Matson MB. The radiological management of the thrombosed arteriovenous dialysis fistula. Clinical Radiology (online) 2011; 66 : 1–12.
12. Leon C, Orozco-Vargas LC, Krishnamurthy G, et al. Accuracy of physical examination in the detection of arteriovenous graft stenosis. Semin Dial 2008; 21 : 85–88.
13. Tordoir J, Canaud B, Haage P, et al. EBPG on Vascular Access. Nephrol Dial Transplant 2007; 22 : 88–117.
14. Argyriou C, Schoretsanitis N, Georgakarakos EI, et al. Preemptive open surgical vs. endovascular repair for juxta-anastomotic stenoses of autogenous AV fistulae: a meta-analysis. J Vasc Access 2015; 16 : 454–458.
15. Macrae JM, Dipchand C, Oliver M, et al. Arteriovenous Access Failure, Stenosis, and Thrombosis. Can J Kidney Health and Dis 2016; 3.
16. Trerotola SO, Stavropoulos SW, Shlansky-Goldberg R, et al. Hemodialysis-related venous stenosis: treatment with ultrahigh-pressure angioplasty balloons. Radiology 2004; 231 : 259–262.
17. Kennedy SA, Mafeld S, Baerlocher MO, et al. Drug-Coated Balloon Angioplasty in Hemodialysis Circuits: A Systematic Review and Meta-Analysis. J Vasc Interv Radiol 2019; 30 : 483–494.
18. Thomas SD, Peden S, Crowe P, et al. Interwoven Nitinol Stents to Treat Radiocephalic Anastomotic Arteriovenous Fistula Stenosis. J Endovasc Ther 2019; 26 : 394–401.
19. Bachleda P, Janeckova J, Xinopulos P, et al. New hybrid procedures in treating occluded arteriovenous hemodialysis grafts. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub 2016; 160 : 149–152.
20. Nassar GM, Beathard G, Rhee E, et al. Management of transposed arteriovenous fistula swing point stenosis at the basilic vein angle of transposition by stent grafts. J Vasc Access 2017; 18 : 482–487.
21. Miller GA, Preddie DC, Savransky Y, et al. Use of the Viabahn stent graft for the treatment of recurrent cephalic arch stenosis in hemodialysis accesses. J Vasc Surg 2018; 67 : 522–528.
22. Jones RG, Willis AP, Jones C, et al. Long-term results of stent-graft placement to treat central venous stenosis and occlusion in hemodialysis patients with arteriovenous fistulas. J Vasc Interv Radiol 2011; 22 : 1240–1245.
23. Verstandig AG, Berelowitz D, Zaghal I, et al. Stent grafts for central venous occlusive disease in patients with ipsilateral hemodialysis access. J Vasc Interv Radiol 2013; 24 : 1280–1287.
24. Surowiec SM, Fegley AJ, Tanski WJ, et al. Endovascular management of central venous stenoses in the hemodialysis patient: results of percutaneous therapy. Vasc Endovascular Surg 2004; 38 : 349–354.
25. Agarawal A. Endovascular interventions for central vein stenosis. Kidney Res Clin Pract 2015; 34 : 228–232.
26. Buriánková E, Köcher M, Bachleda P, et al. Endovascular treatment of central venous stenoses in patients with dialysis shunts. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub 2003; 147 : 203–206.
27. Nassar GM, Rhee E, Khan AJ, et al. Percutaneous thrombectomy of AVF: immediate success and long-term patency rates. Semin Dial 2015; 28 : 15–22.
28. Quencer KB, Oklu R. Hemodialysis access thrombosis. Cardiovasc Diagn Ther 2017; 7 : 299–308.
29. Powell S, Narlawar R, Odetoyinbo T. Early experience with the Amplatzer Vascular Plug II for occlusive purposes in arteriovenous hemodialysis access. Cardiovasc Intervent Radiol 2010; 33 : 150–156.
30. Schmidli J, Widmer MK, Basile C, et al. Editor’s Choice - Vascular Access: 2018 Clinical Practice Guidelines of the European Society for Vascular Surgery (ESVS). Eur J Vasc Endovasc Surg 2018; 55 : 757–818.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2020 Číslo 6- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
- S prof. Vladimírem Paličkou o racionální suplementaci kalcia a vitaminu D v každodenní praxi
-
Všechny články tohoto čísla
- Perkutánní okluze ouška levé síně
- Současné postavení dietních opatření u pacientů s pokročilým stupněm chronického onemocnění ledvin
- Dysfunkčný dialyzačný cievny prístup a jeho endovaskulárna liečba
- Histiocytózy a neoplazie odvozené od makrofágů a dendritických buněk. Srovnání WHO klasifikace z roku 2017 a klasifikace Histiocyte society z roku 2016
- Glykovaný hemoglobín ako marker zvýšenia LDL a TAG – kohortná štúdia
- Alergie a imunopatologie – hlavní téma
- Anafylaxe – akutní a dlouhodobý management
- Potravinová alergie a intolerance
- Poruchy v komplementovém systému
- Deriváty sulfonylurey a riziko hypoglykemie u diabetiků 2. typu
- Imunosenescence – západ slunce nad imunitním systémem
- Chřipka a její komplikace
- Familiární plicní fibróza – doporučení pro diagnostiku a léčbu
- Nové dělení krystalopatií z pohledu nefrologa
- Infarkt myokardu nebo syndrom zlomeného srdce?
- Dieulafoy lézia jejuna ako zdroj život ohrozujúceho krvácania
- Co nového internistům přinášejí doporučené postupy pro diagnostiku a léčbu plicní embolie z roku 2019?
- Endoskopická diagnostika a terapie pankreatobiliárních onemocnění u osob po resekci žaludku podle Billrotha I
- Nozokomiální methemoglobinemie
- Postihnutie tráviaceho traktu pri zmiešanej chorobe spojivového tkaniva (Sharpovom syndróme)
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Infarkt myokardu nebo syndrom zlomeného srdce?
- Postihnutie tráviaceho traktu pri zmiešanej chorobe spojivového tkaniva (Sharpovom syndróme)
- Potravinová alergie a intolerance
- Poruchy v komplementovém systému
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



