-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaChirurgická léčba lokálně pokročilého karcinomu ledviny s nádorovým trombem v žilním řečišti T3b, T3c
SURGICAL MANAGEMENT OF THE RENAL CANCER WITH THE TUMOR THROMBUS IN THE VENOUS SYSTEM T3B AND T3C
Surgical management of the renal cancer with the tumor thrombus in the venous system T3b and T3c represents exacting surgical procedure. Removing of the thrombus of the II and III level and especially level IV in the right heart atrium, is always associated with high risk of the peroperative and late complications. Indication to the surgery covers excluding organ and lymphatic metastases and good performance status. The most critical phase of the surgery is the securing the thrombus and its protection against its spontaneous tearing away with fatal consequences. The tumor thrombus extraction (level II to IV) is from the radicality and safety term suitable only in case of interdisciplinary collaboration of the urologist with the thoracic surgeon or the cardio surgeon.
Key words:
renal cell carcinoma, tumor thrombus, surgical management
Autoři: P. Morávek; J. Dominik; P. Habal; P. Navrátil; J. Pacovsky; P. Žáček
Působiště autorů: FN a LF UK Hradec Králové ; Urologická klinika
Vyšlo v časopise: Urol List 2011; 9(4): 30-37
Souhrn
Chirurgická léčba karcinomu ledviny s nádorovým trombem v žilním řečišti T3b a T3c představuje náročný operační výkon. Odstranění trombu hladiny II a III z dolní duté žíly (DDŽ) a zejména hladiny IV z pravé síně (PS) je spojeno s rizikem perioperačních, pooperačních i pozdních komplikací v závislosti na výši horní hladiny trombu. Indikace k operaci předpokládá vyloučení nádorových a uzlinových metastáz a dobrý biologický stav nemocného. Za nejzávažnější část operace lze považovat zajištění trombu proti odtržení s fatálními následky v průběhu operace. Extrakce trombu hladiny II a IV je možná z pohledu radikality a bezpečnosti pro nemocného jen při interdisciplinární spolupráci urologa s hrudním chirurgem nebo kardiochirurgem dle zvolené operační taktiky.
Klíčová slova:
karcinom ledviny, nádorový trombus, chirurgická léčbaChirurgická léčba karcinomu ledviny má stále zásadní význam. Karcinom ledviny je nádor v podstatě radiorezistentní a chemorezistentní. Dosud neexistuje žádná jednoznačně účinná systémová léčba, i když v současnosti se stále více uplatňuje možnost systémové biologické léčby jako adjuvance po nefrektomii u generalizovaného onemocnění. Ta je však dosud užívána jako léčba paliativní na úrovni klinických studií.
Obr. 1. Sonografie – kulovitý trombus v pravé srdeční síni (část činkovitého trombu). 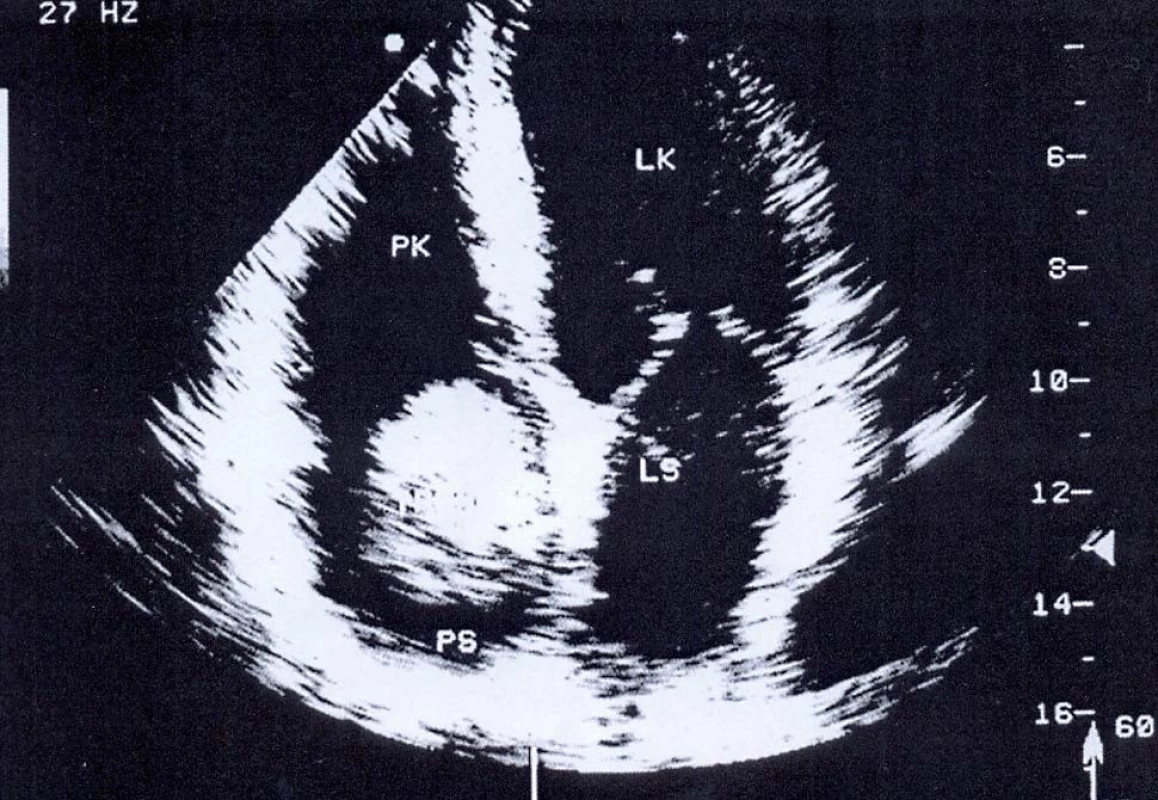
Obr. 2. Sonografie – válcovitý trombus v pravé síni. 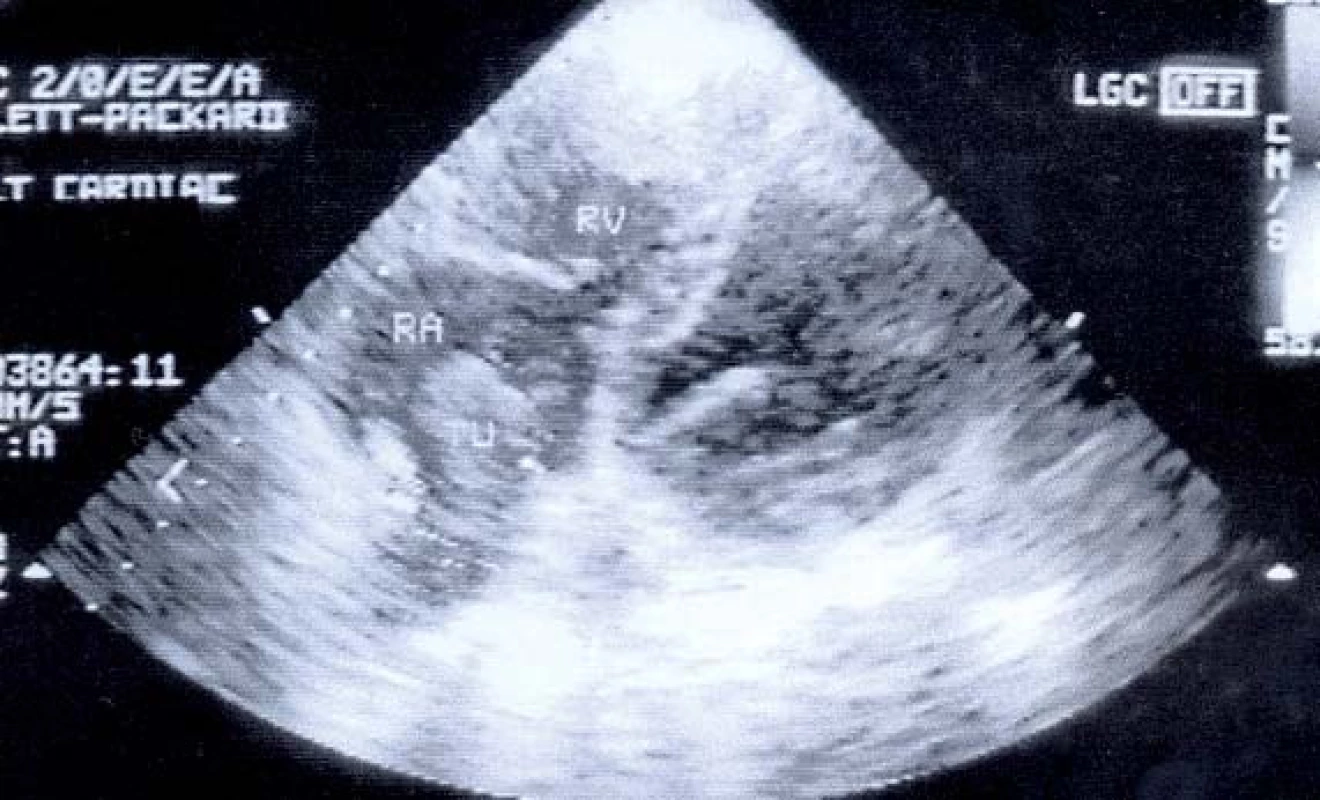
Významnou kapitolu v diskuzi o chirurgické léčbě představuje nádorový trombus karcinomu v žilním řečišti. Angioinvaze je v době operace nádoru prokázána u 4–10 % nemocných do renální žíly, dolní duté žíly a vzácně (0,5 %) do pravé srdeční síně. Nádorový trombus podle výše horní hladiny, podle invaze do žilní stěny a sekundární krevní trombózy pod křížem renálních cév je méně či více závažnou komplikací chirurgické léčby a má dosud nejasný vliv na prognózu onemocnění. Kontroverzní názory jsou zejména na indikaci chirurgické léčby nádoru T3b a T3c a na možnosti následné systémové léčby, která však patří do oblasti zájmů klinického onkologa.
Obr. 3. CT – tumor pravé ledviny s trombem v renální žíle a dolní duté žíle. 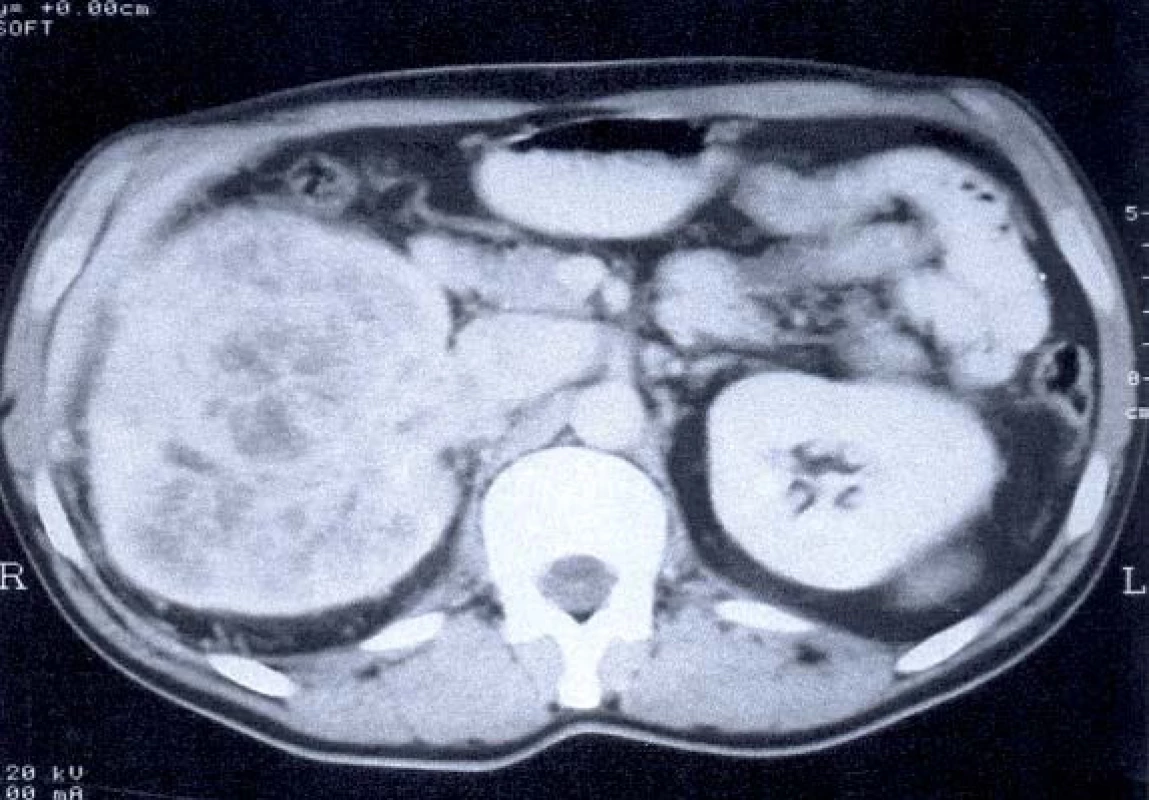
EPIDEMIOLOGIE, ETIOLOGIE, PATOLOGIE
Karcinom ledviny představuje jednu třetinu všech maligních onemocnění, jde o třetí nejčastější diagnózu, pro kterou je urologicky nemocný operován. Během posledních l5 let došlo ke zvýšení incidence onemocnění, ale zvýšilo se i pětileté přežívání u nižšího klinického stadia. Standardizovaná incidence na 100 000 obyvatel byla v ČR v roce 2003 25,66, (32,83 u mužů a 17,68 u žen), mortalita 11,86, v roce 2008 incidence 27,14 (24,9 u mužů a 19,5 u žen) a mortalita 11,13.
Obr. 4. CT – tumor levé ledviny s trombem v renální žíle a dolní duté žíle. 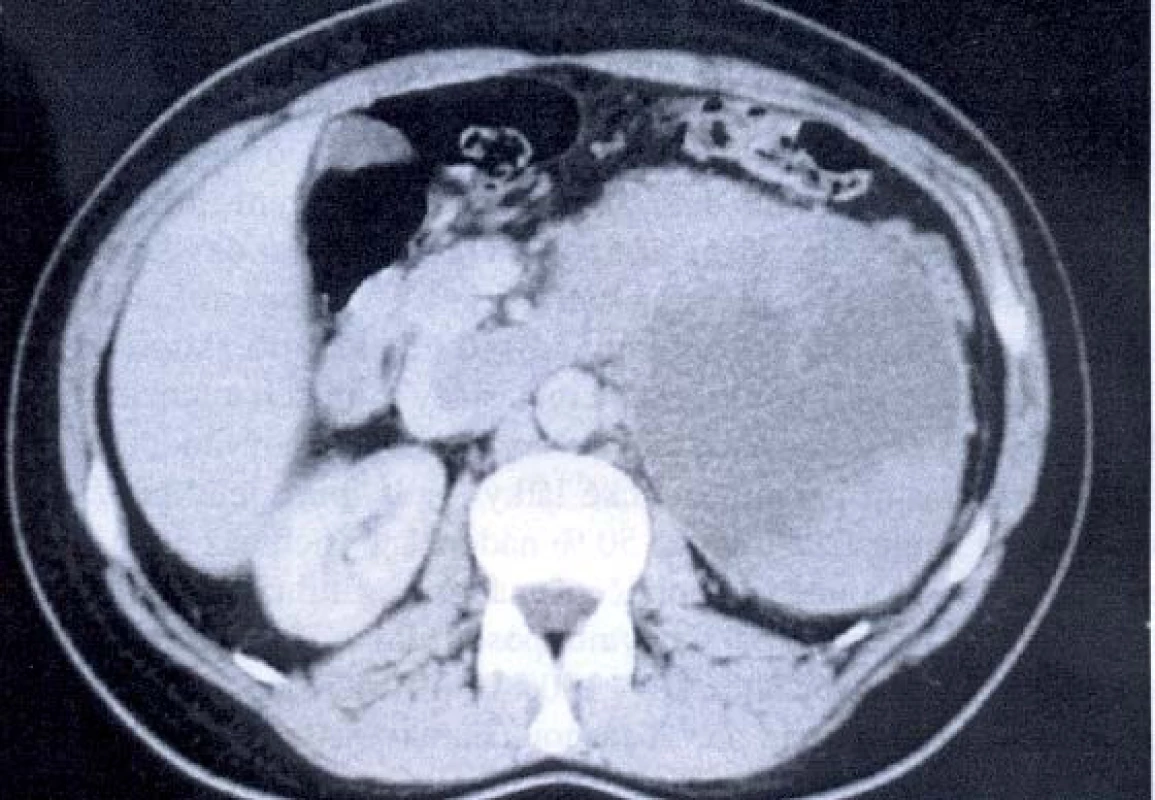
Etiologie karcinomu ledviny není známá, nejčastěji se mluví o civilizačních faktorech. Byl prokázán vliv kouření, obezity, častější výskyt u autozomálně dominantní polycystózy a u nemocných zařazených do PDL (pravidelné dialyzační léčení). Významný je zejména výskyt světlobuněčného karcinomu u Hippel-Lindau syndromu (40–50 %).
Obr. 5. Hladiny trombu dle Nesbitta. 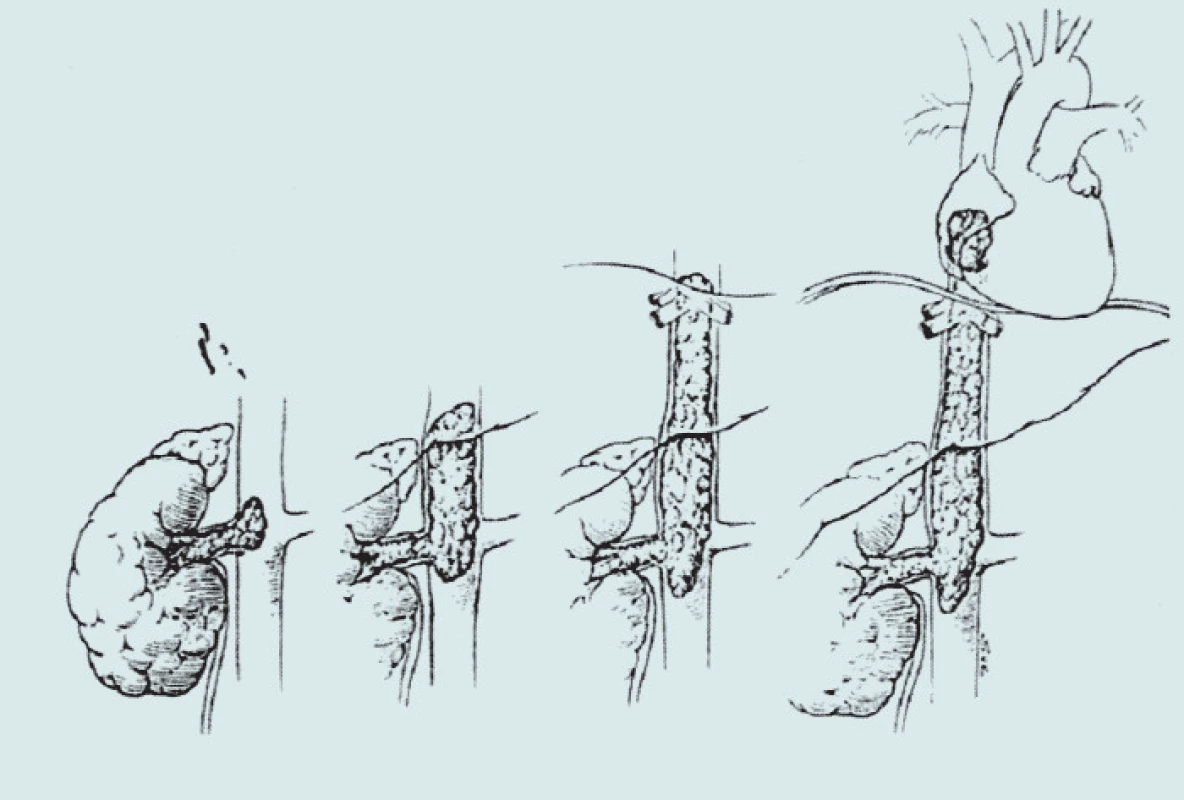
Nejčastěji používanou klasifikací dělení zhoubných nádorů parenchymu ledviny je heidelberská klasifikace, která je v současnosti modifikována. Nejčastější formou nádoru ledviny je světlobuněčný karcinom ledviny (70 %) popsaný v 19. stol. Grawitzem, (který ho mylně nazval jako hypernefrom), s pětiletým přežíváním v 65–75 %. Druhou nejčastější formou je renální papilární karcinom (10–13 %), který má dva typy. Pětileté přežívání u l. typu je 87–100 %, nesetkáváme se s metastazováním a invazí do žilního řečiště. 2. typ je charakteristický časným výskytem nekróz, vyšším potenciálem k tvorbě metastáz a velmi špatnou prognózou. V 5 % se vyskytuje chromofobní karcinom s pětiletým přežíváním v 92 %.
Obr. 6. Tumor pravé ledviny s trombem hladiny I–II (nasazení Satinského svorky) [24]. ![Tumor pravé ledviny s trombem hladiny I–II (nasazení Satinského svorky) [24].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/40a721d59dbbf219a88a2bcd704dda34.jpeg)
Nejméně příznivou prognózu má karcinom ductus Belini, medulární karcinom, sarkomatoidní typy, které mají raritní výskyt (1 %). Přežívání těchto nádorů se pohybuje řádově v měsících [1].
DIAGNOSTIKA
Prvním vyšetřením, na podkladě kterého je vysloveno podezření na nádor ledviny, je sonografie, která jistě odliší solidní expanze nad 3 cm od cystických lézí ve 100 %. Sonografické vyšetření je velmi přínosné (přínosnější než CT) pro stanovení horní hladiny nádorového trombu. Invazi trombu do stěny DDŽ a jeho migraci v žíle může ozřejmit transezofageální sonografie, která však přináší riziko uvolnění trombu během vyšetření. Trombus v pravé síni a jeho rozsah objasní nejlépe sonografie srdce.
Hlavní metodou volby pro detailní vyšetření nádoru ledviny je výpočetní tomografie (CT) a spirální CT. Objasní rozsah nádoru, vztah k okolním orgánům, postižení regionálních lymfatických uzlin, postižení nadledviny a šíření nádorového trombu do žilního řečiště. Senzitivita dosahuje až 95 %. CT je v diagnostice maligních lézí velmi efektivní díky možnosti verifikace patologické vaskularizace tumoru. Je využívána pro diagnostiku orgánových metastáz.
Obr. 7. Tumor pravé ledviny s trombem hladiny I–II (resekce DDŽ) [24]. ![Tumor pravé ledviny s trombem hladiny I–II (resekce DDŽ) [24].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/4a15fe2d63832b7429641e7a1893164b.jpeg)
Obr. 8. Tumor pravé ledviny s trombem hladiny II (naložení turniketů) [24]. ![Tumor pravé ledviny s trombem hladiny II (naložení turniketů) [24].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/94fe5f30e84f2abc6a6319371cbde3fc.jpeg)
Vysokou senzitivitu má i magnetická rezonance (MR) s použitím gadolinia. Bez použití gadolinia se nemusí zachytit až 50 % nádorů menších než 3 cm. Nevýhodou je vysoká cena, výhoda je při posouzení výšky horní hladiny nádorového trombu (100 %).
Obr. 9. Tumor pravé ledviny s trombem, hladina II (resekce DDŽ) [24]. ![Tumor pravé ledviny s trombem, hladina II (resekce DDŽ) [24].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/1d8657d8cee98eeaebb9dd04dc465c1f.jpeg)
Pozitronová emisní tomografie (PET nebo PET CT) má význam zejména v diagnostice vitálních orgánových metastáz.
Z ostatních vyšetření, indikovaných před operací nádoru T3b, T3c pro stanovení „stagingu“ jsou nutné CT plic, CT mozku, scintigrafie kostí a před operací v kardiopulmonálním bypassu (CPB) koronarografie [1].
Obr. 10. Pringleův manévr [24]. ![Pringleův manévr [24].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/9f297ec1d12735169101f398cff1d404.jpeg)
NÁDOROVÉ MARKERY, PROGNOSTICKÉ FAKTORY [1]
V současnosti neexistuje žádný specifický marker pro diagnostiku primárního tumoru, ani pro jeho sledování v pooperačním průběhu ani pro průkaz metastazování.
Z uvedených důvodů jsou v současnosti sledovány klinické a ve výzkumných klinických studiích nespecifické markery, které lze rozdělit z pohledu originality na sérové, tkáňové a genetické. Tato problematika však přesahuje téma tohoto přehledového článku.
Obr. 11. Tumor pravé ledviny s trombem hladiny III (turniket nad horní plochou jater, ostatní stejně jako u hladiny II) [24]. ![Tumor pravé ledviny s trombem hladiny III (turniket nad horní plochou jater, ostatní stejně jako u hladiny II) [24].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/43d120dd399a9b28de4c37cfa77fde34.jpeg)
Z pohledu závažnosti radikální chirurgické léčby karcinomu ledviny, a to zejména při invazi nádoru do dolní duté žíly (DDŽ) a pravé srdeční síně (PS), je nutné zmínit prognostické faktory, které určují prognózu onemocnění.
Významným faktorem je rozsah nádoru pT. Lepší prognózu má nádor, který nepřesahuje pouzdro pT1–pT2. Nepříznivým faktorem je angioinvaze do DDŽ a PS. Nebyl shledán rozdíl v pětiletém přežívání u tumorů s trombem pod játry a nad játry (pod bránicí) 57 %, pokud jsou radikálně odstraněny, na rozdíl od nádorů, které invadovaly do stěny DDŽ s pětiletým přežíváním jen 25 %.
Obr. 12. Odstraněná ledvina s nádorem a činkovitým trombem (hladina IV, operace v CPB). 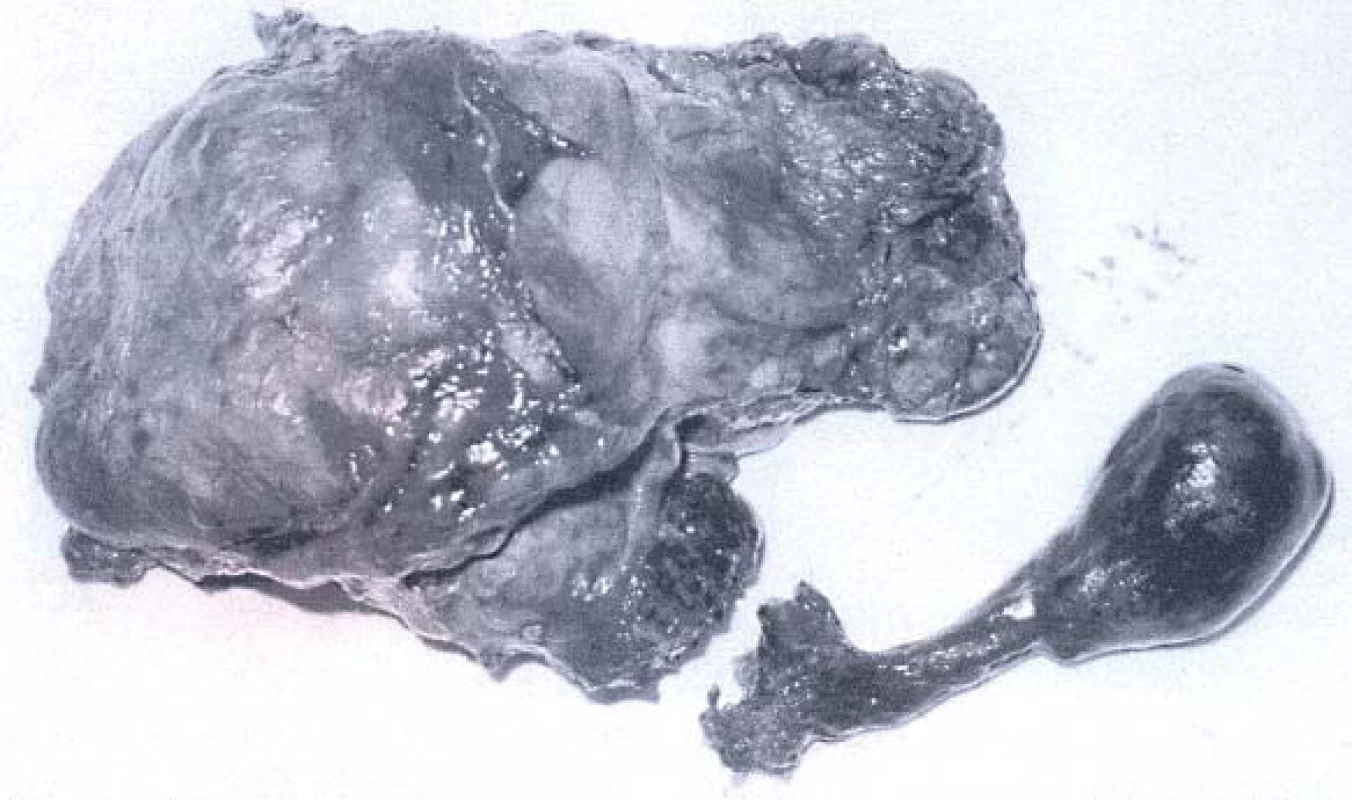
Velmi nepříznivým faktorem jsou metastázy v regionálních lymfatických uzlinách a vzdálené metastázy. Pětileté přežívání se v těchto případech pohybuje mezi 5 a 30 %.
Prognostický význam mají i histologické typy (jak už bylo výše zmíněno), grading nádoru (histologický stupeň diferenciace) podle FUHRMANOVÉ (G I–G IV) a stanovení ploidity buněk nádoru. U diploidních je pětileté přežívání 94 % a u nediploidních jen 8 %.
Nádorový trombus dosud představuje prognostický faktor nejasného významu [2–9]. Samotná přítomnost nádorového trombu nemá pro délku přežívání rozhodující význam. Pětileté přežívání u trombu hladiny II a III je obdobné jako u nádoru bez trombu (Yamashita 56–80 %, Abraham 56–60 %, Ciancio, Soloway 32–64 %, Červinka 47–69 % Morávek, Dominik 35–50 %). U hladiny trombu IV je přežívání kratší (Skinner 18–35 %, Morávek, Dominik 27–35 %).
Obr. 13. Odstraněná ledvina s nádorem a válcovitým trombem (hladina IV, operace v CPB). 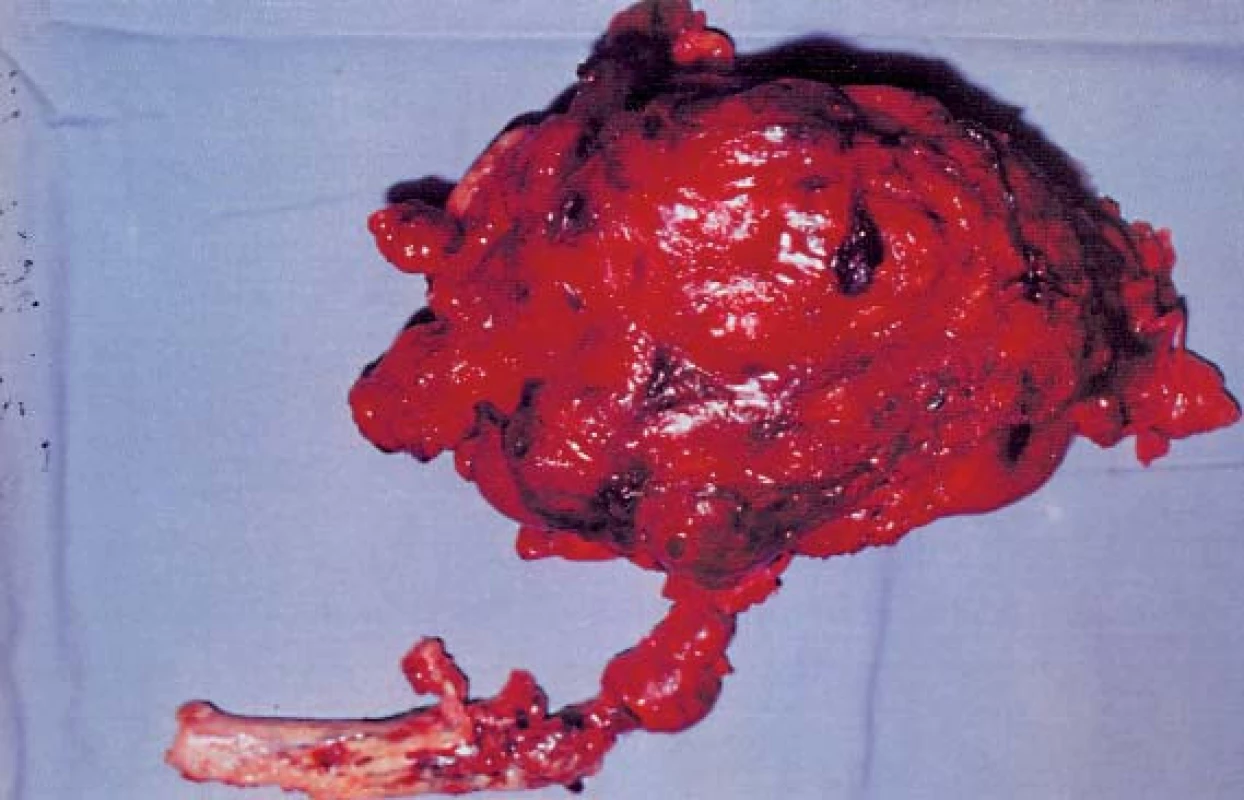
Rozhodující význam pro prognózu a délku přežití má kompletní odstranění trombu, jak již bylo zmíněno (Skinner Neves, Zinke).
Trombus je často spojen s vyšším stadiem onemocnění, s pozitivními uzlinami (26 %), metastázami v orgánech (50 % Hatcher) a s vyšším rizikem recidivy (TSUI).
Nádorový trombus v levé renální žíle způsobí poruchu odtoku krve spermatickou žilou s následným vznikem symptomatické varikokély, při obstrukci DDŽ dochází ke stáze v jejím povodí, což se projeví otokem dolních končetin, vznikem kolaterál a sekundární krevní trombózy pod úrovní trombu. Při odtoku krve z druhostranné ledviny dochází k poruše její funkce a při poruše odtoku z jaterních žil vzniká porucha funkce jater až pod obrazem BUD-CHIARI syndromu.
Obr. 14. Odstraněná ledvina s nádorem a keříčkovitým trombem (hladina IV, operace v CPB). 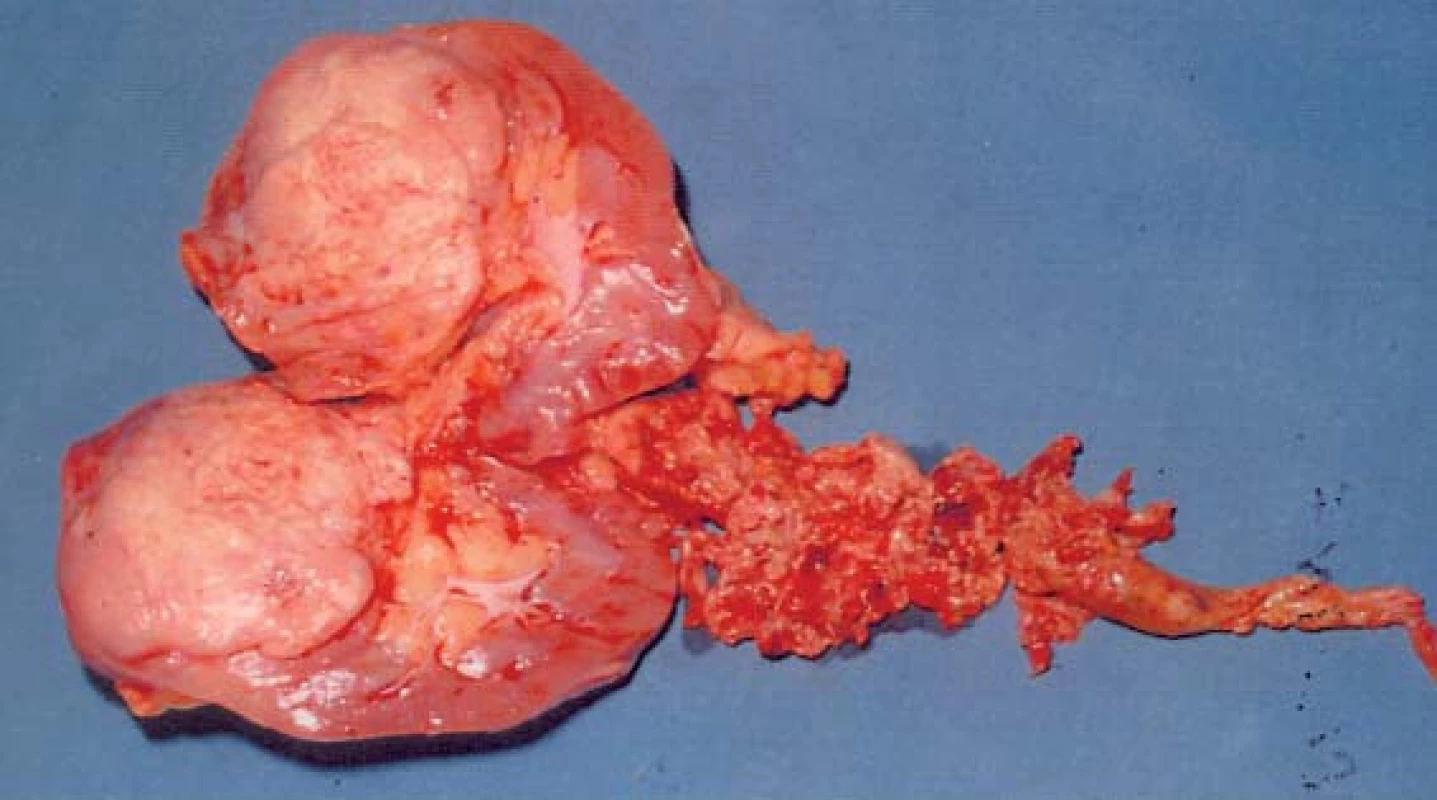
Odtržením části trombu (většinou jde o trombus smíšený) dochází k sukcesivní nebo masivní embolizaci. Při rozsáhlém trombu v pravé síni vznikají závažné hemodynamické změny, které se mohou projevit dušností a snížením minutového srdečního výdeje.
Nádorový trombus hladiny IIII a IV přináší komplikace radikální chirurgické léčby – pooperační morbiditu ve 28–41 %, pooperační mortalitu ve 13–20 % a intraoperační mortalitu v 5,5–13,0 % [10,11].
CHIRURGICKÁ LÉČBA NÁDOROVÉHO TROMBU HLADINY II, III, IV (T3B, T3C) (PŘEDPOKLADY LÉČBY, TAKTIKA – OBECNĚ)
Předpoklady pro indikaci radikální chirurgické léčby nádorového trombu hladiny II–IV:
- exaktně stanovená diagnóza – sonografie ledvin a retroperitonea včetně dolní duté žíly, sonografie srdce (hladina IV), CT ledvin, retroperitonea včetně DDŽ, CT plic, event. dle příznaků CT mozku, vždy scintigrafie kostí k vyloučení metastáz
- koronarografie – k vyloučení postižení koronárních tepen před operací trombu v síni v CPB
- akceptabilní biologická kondice nemocného (performans status)
- vypracovaný operační postup, operační taktika a technika
- multidisciplinární spolupráce urologa a hrudního chirurga (dle zvolené taktiky) u trombu hladiny III a kardiochirurga u trombu hladiny IV
Taktika léčby závisí především na výši horní hladiny trombu, na jeho tvaru (hadovitý – vlající, válcovitý, činkovitý) a na operabilitě primárního nádoru. Větší operační náročnost představují tromby vlající, křehké pro riziko uvolnění embolizace a tromby s invazí do stěny dolní duté žíly. To vyžaduje resekci celého úseku DDŽ s autologní nebo umělou polytetrafluoroethylenovou náhradou nebo bypass renální žíly zbylé ledviny na horní část resekované DDŽ, event. na slezinnou žílu za předpokladu vytvořeného kolaterálního oběhu oběhu.
CHIRURGICKÁ LÉČBA NÁDOROVÉHO TROMBU HLADINY II (SUBHEPATICKÝ) T2b [12–15]
Operace začíná radikální nefrektomií z laparotomie (lumbolaparotomie), subkostální incizí v pravém podžebří nebo v levém podžebří se stříškovitým protažením na pravou stranu (chevron incize). Důležitý je podvaz renální arterie pro kolaps žilního řečiště, který je proveden z předního nebo zadního přístupu v závislosti na velikosti nádoru, jeho umístění v ledvině a na šíři trombu. Před dokončením nefrektomie s odstraněním trombu, před ligaturou a přerušením renální žíly je třeba zajištění trombu.
Pokud trombus zasahuje do DDŽ jen v malém rozsahu, postačí naložení parciální Satinského svorky na DDŽ s trombem, provedení nástěnné resekce DDŽ a dokončení nefrektomie. Pokud sahá nádorový trombus až pod játra, je nutno obnažit DDŽ od kříže ledvinných cév po vstup do jater a naložit na ni tři turnikety (pod úrovní kříže renálních cév, pod játra a na druhostrannou renální žílu). Následuje utažení turniketů, kavotomie nebo resekce DDŽ a odstranění ledviny s trombem. Pro lepší přehlednost operačního pole je vhodné nejdříve ligovat renální žílu (arterie byla ligována v začátku preparace hilu), odstranit ledvinu s nádorem a následně trombus. Operace je dokončena provedením sutury kavotomie nebo resekce DDŽ, povolením parciální Satinského svorky, která byla po odstranění trombu nasazena na DDŽ a turnikety [12–15].
CHIRURGICKÁ LÉČBA NÁDOROVÉHO TROMBU HLADINY III (intra, suprahepatický) T3b [5,11,14–22]
Radikální operace trombu hladiny III přináší větší rizika. Trombus je často fixován při vústění renální žíly a jaterních žil, kam často invaduje. Při manipulaci s dolní dutou žilou je možné jeho odtržení, zejména u trombu vlajícího, s masivní plicní embolizací a fatálním koncem. Proto je nutné maximální jištění trombu. Zavádění kaválního filtru je v této výši nereálné. Postup operace je stejný jako u hladiny II až do fáze jištění trombu. Jisticí turniket nad horní hladinou trombu se zakládá mezi bránici a pravou síň. To předpokládá spolupráci s hrudním chirurgem, který provede torakotomii v 5. nebo 6. mezižebří, následně perikardiotomii a turniket založí. Ostatní dva turnikety jsou založeny jako u trombu hladiny II. Po utažení turniketů následuje s výhodou lepší přehlednosti ligatura ledvinné žíly s trombem a nefrektomie předem uvolněné ledviny s ligovanou arterií. V další fázi operace je provedena kavotomie nebo resekce DDŽ a extrakce trombu. Na okraje kavotomie nebo resekce jsou založeny jisticí stehy pro založení parciální Satinského svorky. Po uzavření svorky je obnoven parciální tok dolní dutou žílou a je možno povolit turnikety. Následuje sutura DDŽ a při jistotě její těsnosti odstranění turniketů. Doba uzávěru jisticího turniketu nad bránicí a ostatních je většinou 3–6 min. Úplná obturace DDŽ trombem je při této operaci přínosná. Vytvořený kolaterální oběh kompenzuje hemodynamické změny při návratu krve do pravého srdce během výkonu.
V případě ověřené invaze trombu do stěny DDŽ je nutné pro resekci stěny žíly v průběhu jater provést Pringleův manévr; laterálně a kraniálně mobilizovat pravý jaterní lalok a odklopit ho mediálně. Tím se zpřístupní retrohepatická část DDŽ. Pringleův manévr je možno s rizikem odtržení trombu provést bezprostředně po nefrektomii, horní turniket založit těsně pod bránici a operovat jen z abdominálního přístupu. Výhodou je přehlednost retrohepatické části DDŽ, nevýhodou již zmíněná možnost odtržení trombu při manipulaci s játry, zejména je-li trombus vlající, křehký (nehomogenní). Následuje založení zbylých dvou turniketů, jejich zatažení, resekce DDŽ, extrakce trombu, naložení Satinského svorky, parciální obnova toku v DDŽ, její sutura a uvolnění turniketů. Ze zkušeností je třeba říci, že žádná ze zobrazovacích metod jistě neinformuje o konzistenci, celistvosti trombu, ani o jeho invazi do stěny žíly. Invaze do žilní stěny přichází u 5 % trombů. Je třeba vždy předem zajistit spolupráci s cévním chirurgem. Z tohoto důvodu sami volíme u trombu sahajícího nad bránici operaci v CPB (mimotělním oběhu) i přes jeho rizika (viz níže). Operace trombu hladiny III v CPB není v písemnictví obecně uznávána (ZINI).
RADIKÁLNÍ CHIRURGICKÁ LÉČBA NÁDOROVÉHO TROMBU HLADINY IV (v pravé síni) T3c [4,23–34]
Tato léčba představuje nejnáročnější operační výkon spojený s intrakardiálním přístupem za spolupráce urologa a kardiochiruga. Za standardní metodu je považováno odstranění nádorového trombu z pravé síně v mimotělním oběhu (CPB – kardiopulmonální bypass), se zástavou oběhu v hluboké hypotermii (18–20 °C), ze současné atriotomie a kavotomie. Touto technikou lze odstranit všechny typy trombů. Méně invazivní je technika v normotermickém CPB (u hadovitých trombů v okraji síně) nebo v atriokaválním shuntu. Je však spojená s větší ztrátou krve a s rizikem vzduchové embolie.
Operace probíhá až do fáze zajištění trombu obligatorním způsobem jako u hladiny II a III. Po zajištění trombu v místě vstupu renální žíly do DDŽ je vena ligována, přerušena a dokončena nefrektomie. Turnikety se nezakládají. Následuje sternotomie, perikardiotomie, zavedení neúplného mimotělního oběhu (kanyly jsou zavedeny do horní duté žíly, ascendentní aorty a pravé síně), kardioplegie a chla-zení organizmu na 18–20 °C se zástavou oběhu. Hluboká hypotermie umožňuje zástavu až 20 min a bezpečné odstranění trombu v bezkrevném poli ze současné atriotomie a kavotomie (event. resekce DDŽ). Extrakce trombu je provedena kleštěmi na kámen nebo měchýřovým balonkovým katétrem, nejvýhodněji však prstem, kterým se lze snadno přesvědčit o radikalitě výkonu a neporušenosti žilní stěny. V případě potřeby invaze trombu do stěny je pro resekci možno připojit Pringleův manévr. Následuje sutura DDŽ, zavedení úplného mimotělního oběhu (kanyla ze síně do DDŽ), sutura síně, ohřívání, defibrilace a po nástupu spontánní srdeční akce zrušení CPB. Současně je provedena sutura sternotomie a laparotomie. Dle našich zkušeností je výhodou tohoto operačního postupu výborný přehled v operačním poli, maximální radikalita a minimální krevní ztráty.
Vzhledem k možným intraoperačním a pooperačním komplikacím po CPB s hlubokou hypotermií a zástavou cirkulace (mors in tabula, koagulopatie, neurologické poškození, multiorgánové selhání) někteří urologové a kardiochirurgové hledali metody bez CPB, s CPB bez chlazení a zástavy oběhu. O těchto technikách si dovolím jen stručnou informaci s literárními odkazy [19,22,35–40].
Technika s okluzí supraceliakální aorty katétrem s balonem a chlazením na 31 °C bez zástavy oběhu. Technika vakuum asistovaného CPB bez zástavy oběhu a techniky, které řeší trombus v PS bez CPB z abdominálního přístupu (Ciancio, Soloway). Podmínkou je mobilizace jater (viz technika u trombu III), nasazení turniketu na porta hepatis, maximální rotace pravého jaterního laloku doleva pro obnažení retrohepatické části DDŽ, protětí centrum tendineum bránice k ozřejmění supradiafragmatické, perikardiální části DDŽ a pravé síně. Odstranění trombu z kavotomie nebo resekce DDŽ následuje po naložení turniketů na DDŽ pod kříž ledvinných cév na druhostrannou ledvinou žílu a parciální Satinského svorky přes pravou síň. Metodu nelze využít v případě trombu činkovitého a fixovaného ke stěně síně.
ZÁVĚR
Pokročilý renální karcinom s nádorovým trombem (T3b, T3c) je velmi závažné onemocnění se špatnou prognózou. Je třeba si uvědomit, že i u tohoto onemocnění jsme schopni efektivně prodloužit nemocnému život. Chirurgická léčba je v indikovaných případech vhodná a může být radikální. S ohledem na velmi nízkou míru odpovědi na ostatní léčebné možnosti se tak stává jedinou možností léčby. Pokud se jedná o nemetastazující onemocnění, měli bychom vždy zvážit vhodnost operačního výkonu. Takový operační výkon je velice náročný, měl by být vyhrazen erudovanému pracovišti s možností mezioborové spolupráce s hrudním chirurgem a kardiochirurgem.
Indikace pro takový výkon záleží nejen na faktorech týkajících se vlastního nádoru, ale též značnou měrou na celkovém stavu nemocného a dalších komorbidit.
V současnosti neexistuje adjuvantní léčba, která by byla indikována k systémovému podání po provedení takto rozsáhlého výkonu. To je předmětem zkoumání klinických studií.
Při provádění nefrektomie s extrakcí nádorového trombu existuje reálná možnost, že trombus či jeho část nebude odstranitelný a bude muset být ponechán in situ. Lze říci, že i v takovém případě nemocný z výkonu profituje. V takovém případě je nutná trvalá antikoagulační léčba. Zkušenosti ukazují, že provedená nefrektomie významně zpomaluje progresi onemocnění a prodlužuje dobu do progrese.
Závěrem lze shrnout, že nefrektomie s odstraněním nádorového trombu zasahujícího do dolní duté žíly až nad bránici je technicky proveditelná a rizika spojená s ní jsou tváří v tvář závažnému nádorovému onemocnění akceptabilní.
doc. MUDr. Petr Morávek
Urologická klinika
FN a LF UK Hradec Králové
moravek@fnhk.cz
Zdroje
1. Morávek P. Nádory ledvin. In: Dvořáček J, Babjuk M et al. Onkourologie. 2005 Praha Galén 2005 a Karolinum: 31–44.
2. Ficarra F, Righetti R, D’Amico A. Renal vein and vena cava involvement does not affect prognosis in patiens with renal cell carcinoma. Oncolgy 2001; 61(1): 10–15.
3. Hatcher PA, Anderson EE, Paulson DF et al. Surgical management and prognosis of renal cell carcinoma invading the vena cava. J Urol 1991; 145(1): 20–24.
4. Morávek P, Dominik J. Radikale Operation wegen eines Nierenkarzinoms mit einer tumorthrombose im rechten Herzvorhof. Journal für Urologie und Gnynäkologie 2002; 9(4): 20–25.
5. Nevees RJ, Zincke H. Surgical treatment of renal cancer with vena cava extension. Br J Urol 1987; 59(5): 390–395.
6. Skinner DG, Pritchett TR, Lieskovski G et al. Vena cava involvement be renal cell carcinoma: surgical resection provides meaningful long - term survival. Ann Surg 1989; 210(3): 387–392.
7. Sosa RE, Muecke EC, Vaughan ED et al. Renal cell carcinoma extending into the IVC: the prognostic significance of the level of IVC involvement. J Urol 1984; 132(6): 1097–1100.
8. Tsuji Y, Goto A, Hara I. Renal cell carcinoma with extension of tumor thrombus into the vena Cava: surgical strategy and prognosis. J Vasc Surg 2001; 33(4): 789–796.
9. Giuliani L, Gibert C, Martorana G et al. Radical extensive surgery for renal cell carcinoma: long - term results and prognostic factors. J Urol 1990; 143(3): 468–473.
10. Nesbitt JC, Soltero ER, Dinney CP et al. Surgical management of renal cell carcinoma with inferior vena cava tumor thrombus. Ann Thorac Surg 1997; 63(6): 1952–1600.
11. Zini L, Haulon S, Decoene C et al. Renal cell carcinoma associated with tumor trombus in the inferior vena cava: Surgical strategies Ann Vasc Surg 2005; 19(4): 522–528.
12. Baše J, Navrátil P, Navrátilová J et al. Tumorous thrombosis of the inferior vena cava: Authors experience with surgical treatment. Rozhl Chir 1993; 72 : 303–306.
13. Bissada NK, Yakout HH, Babanouri A et al. Long-term experience with management of renal cell carcinoma involving the inferior vena cava. Urology 2003; 61(1): 89–92.
14. Hinnman F. Atlas urologischer Operationen Herausgeber der deutschen Augabe Herbert Ruben und Jens Altwein 1994, Ferdinand Enke Verlag Stuttgart.
15. Hohenfellner R, Fichtner J, Stein R. Ausgewahlte urologische Op - Technikem,step-by-step. 2. überarbeitete und erweitere Auflage 1997: Georg Thieme Verlag Stuttgart-New York.
16. Morávek P, Navrátil P Jr., Habal P et al. Chirurgická léčba karcinomu ledviny s nádorovým trombem v žilním řečišti hladiny III. Urológia 2006; 4 : 18–23.
17. Ciancio G, Vaida A, Savoie M et al. Management of renal cell carcinoma with level III trombus in the inferior vena cava. J Urol 2002; 168 (4 Pt 1): 1374–1377.
18. Ciancio G, Soloway M. Resection of the abdominal inferior vena cava for complicated renal cell carcinoma with tumour trombus. BJU international 2005; 96(6): 815–818.
19. Ciancio G, Soloway M. Renal cell carcinoma with tumor trombus extending above diaphragm: Avoiding cardiopulmonary bypass. Urology 2005; 66(2): 266–270.
20. Ciancio G, Hawke C, Soloway M. The use of liver transplant techniques to aim in the surgical management of urological tumors. J Urol 2000; 164 (3 Pt 1): 665–672.
21. Reissig A, Janetschek G, Eberle J et al. Renal cell carcinoma extending into the vena cava: surgical approach, technique and results. Br J Urol 1995; 75(2): 138–142.
22. Voght P, Esner R, Pretre R et al. Lessinvasive surgical treatment of renal cell carcinomas extending into the right heart and pulmonary arteries. Surgery of renal cell carcinoma, J Card Surg 1999; 14(5): 330–333.
23. Janosko EO, Powel CS, Spence PA et al. Surgical management of renal cell casrcinoma with extensive intracaval involvement using a venous bypass systém suitable for rapid conversion to total cardiopulmonary bypass. J Urol 1991; 145(3): 555–557.
24. Hashiba T, Hirokawa M, Chiba K et al. Treatment of renal cell karcinoma extending into right atrium with extra-corporeal circulation using high grade hypothermia: acase report. Hinyokika Kiyo 2000; 46(4): 255–259.
25. Klein EA, Kaye MC, Novick AC. Management of renal cell carcinoma with vena caval tumor thrombi via cardiopulmonary bypass and deep hypothermic circulatory arrest. Urol Clin North Am 1991; 18(3): 445–447.
26. Novick AC, Kaye M, Pontes JE et al. Experience with cardiopulmonary bypass and deep hypothermic circulatory arrest in the management of retroperitoneal tumors with vena caval thrombi. Ann Surg 1990; 212(4): 472–476.
27. Ochi T, Tanji N, Shimamoto K et al. Application of cardiopulmonary bypass ror resection of renal cell carcinoma and adrenocortical carcinoma extending into the right atrium. Int J Urol 2006; 13(3): 202–205.
28. Yamashita CH, Azami T, Okada M et al. Usefulness of cardiopulmoary vypase in reconstruction of inferior vena cava occupied by renal cell carcinoma tumor trombus. Angiology 1999; 50(1): 47–53.
29. Glazer A, Novick AC. Long -term follow-up after surgical treatment for renal cell carcinoma extending into the right atrium. J Urol 1996; 155(2): 448–450.
30. Kalaycioglu S, Sinci V, Aydin H et al. Cardiopulmonary vypase technique for treatment of renal cell carcinoma extending into the vena. Ann Thorac Cardiovasc Surg 1999; 5(6): 419–422.
31. Ciancio G, Soloway M. The use of natural veno-venous bypass during surgical treatment of renal cell carcinoma with inferior vena cava thrombus. Am Surg 2002; 68(5): 488–490.
32. Obadia JF, Clavel JP, Bonnefoy E. Surgery of cavoatrial extension of renal malignant tumors using a veno-venous shunt. Br J Urol 1997; 80(5): 812–814.
33. Morávek P, Dominik J, Navrátil P et al. Surgery of renal carcinoma with tumour thrombosis involving the right atrium. Rozhl Chir 1996; 75(12): 603–606.
34. Morávek P, Dominik J. Chirurgická léčba karcinomu ledviny s nádorovým trombem v pravé srdeční síni. Výsledky léčby (1993–2005). Klin Urol 2006; 2(3): 139–145.
35. Svenson LG, Crawford ES, Hess KR. Deep hypothermia with circulatory arrest: determinant of stroke and early mortality in 656 patients. J Thorac Cardiovasc Surg 1993; 106(1): 19–28.
36. Ruel M, Bedard P, Morash CR. Resection of right atriall tumor thrombi without circulatory arrest. Ann Rhorac Surg 2001; 71(2): 733–734.
37. Singhal R, Vricella LA, Mitchel RS et al. Cavoatrial tumor trombus excision without circulatory arrest. Urology 2003; 62(1): 138–140.
38. Stewart JR, Carey JA, McDougal WS et al. Cavoatrial tumor thrombectomy using cardiopulmonary bypass without circulatory arrest. Ann Thorac Surg 1991; 51(5): 717–721.
39. Cervinka WH, Ciancio G, Salerno TA et al. Renal cell cancer with invasive atrial tumor trombus excised off-pump. Urology 2005; 66(6): 1319.
40. Bassi P, Del Moro F, Ciaccia M et al. Transdiaphragmatic-intrapericardiac approach to supradiaphragmatic vena cava invasion secondary to renal cell carcinoma: a novel surgical approach. Urology 2005; 66(5): 1101–1105.
Štítky
Dětská urologie Urologie
Článek vyšel v časopiseUrologické listy
Nejčtenější tento týden
2011 Číslo 4- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Nostiriazyn – spolehlivá 1. volba u nekomplikovaných infekcí močových cest
- Nitrofurantoin s řízeným uvolňováním: osvědčená účinnost, lepší snášenlivost a méně tablet při akutní cystitidě
- Prevence opakovaných infekcí močových cest s využitím přípravku Uro-Vaxom
- Vysoká hladina PSA a její rychlý nárůst jsou nepříznivými prognostickými faktory u karcinomu prostaty
-
Všechny články tohoto čísla
- Nefron šetřící operace bez zasvorkování renálního hilu
- Minimálně invazivní laparoskopická a roboticky asistovaná parciální resekce ledviny: stručná historie a přehled
- Laparoskopická a robotická heminefrektomie a ureteroureterostomie v rámci léčby zdvojeného vývodného systému horních cest močových
- Chirurgická léčba lokálně pokročilého karcinomu ledviny s nádorovým trombem v žilním řečišti T3b, T3c
- Co nabízí dnešní medicína, když selže diagnostika karcinomu ledviny ve stadiu lokalizovaném na orgán?
- Možnosti predikce karcinomu prostaty pomocí PCA3
- Možnosti klinické aplikace kombinované léčby benigní hyperplazie prostaty
- Indikace a výsledky ablace tumoru ledviny
-
EAU Guidelines pro diagnostiku a léčbu uroteliálního karcinomu horních cest močových
aktualizace 2011 - Úvodník
- Diagnostické možnosti časného zjištění nádorů ledvin, role nádorových markerů při stanovení dalšího postupu
- EAU Guidelines pro řešení močové inkontinence
- Urologické listy
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Možnosti predikce karcinomu prostaty pomocí PCA3
- Diagnostické možnosti časného zjištění nádorů ledvin, role nádorových markerů při stanovení dalšího postupu
- Chirurgická léčba lokálně pokročilého karcinomu ledviny s nádorovým trombem v žilním řečišti T3b, T3c
- Laparoskopická a robotická heminefrektomie a ureteroureterostomie v rámci léčby zdvojeného vývodného systému horních cest močových
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



