-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Současný pohled na ureterointestinální anastomózu v močové derivaci
Ureterointestinal anastomosis in urinary diversion – current opinion
Uretero-intestinal anastomosis (UIA) is one of the most critical points for the occurrence of severe complications of intestinal urinary diversion. Perfection of the current techniques and development of new UIA methods are motivated by the effort to reduce both early and late post-surgical complications. The necessity of using antireflux UIA, especially with an orthotopic neobladder, is controversial: according to some authors, antireflux UIA of any type generally increases, in comparison with reflux UIA, the risk of obstruction that endangers renal function more than the urine reflux itself. ICUD-EAU International Consultation on Bladder Cancer 2012 does not recommend applying antireflux UIA in orthotopic bladder substitutions. In ileal conduit diversions, most surgeons use only refluxing UIA. Studer and Turner recommend antireflux UIA only in cases where urine diversion can generate great intraluminal pressure and/or where there is a high risk of permanent bacterial colonization. The flap-and-trough technique (FT) of nonrefluxing UIA represents another flap-valve method for implanting normal as well as dilated ureters into various types of urinary diversion, with a low risk of stenotic complications.
Conclusions:
A simple refluxing end-to-side UIA to a low-pressure orthotopic reservoir is a procedure of choice with low complication rates. On the other hand, the need for reflux prevention with a conduit, continent cutaneous diversion or anal diversion is well-founded.Key words:
ureterointestinal anastomosis
Autoři: J. Doležel
Působiště autorů: Oddělení urologické onkologie, Klinika operační onkologie LF Masarykovy univerzity a Masarykova onkologického ústavu, Brno přednosta: doc. MUDr. R. Šefr, Ph. D.
Vyšlo v časopise: Rozhl. Chir., 2017, roč. 96, č. 4, s. 146-150.
Kategorie: Souhrnné sdělení
Souhrn
Ureterointestinální anastomóza (UIA) je jedním z nejkritičtějších míst vzniku závažných komplikací střevní derivace moče. Zdokonalování stávajících a vývoj nových metod UIA je motivován snahou o snížení časných i pozdních pooperačních komplikací. Nutnost užití antirefluxní UIA, zejména u ortotopických náhrad měchýře, je kontroverzní. Podle některých autorů antirefluxní UIA jakéhokoliv typu obecně zvyšují, v porovnání s refluxními UIA, riziko obstrukce, která ohrožuje funkci ledvin více než reflux moče. ICUD-EAU International Consultation on Bladder Cancer 2012 nedoporučuje používání antirefluxních technik UIA u ortotopických náhrad močového měchýře. Naprostá většina urologů aplikuje refluxní UIA též u ileálních konduitů. Studer a Turner doporučují antirefluxní UIA pouze v případech derivací moče, které jsou schopny vytvářet vysoké intraluminální tlaky a/nebo je u nich velká pravděpodobnost trvalé bakteriální kolonizace. Prevence refluxu je tedy oprávněná v případě konduitů, kontinentních heterotopických derivací a análních derivací moče. Metoda flap-and-trough (FT) reprezentuje další antirefluxní UIA záklopkového typu s nízkým potenciálem stenotizace, umožňující implantace jak normálních, tak i dilatovaných močovodů prakticky do všech typů močové derivace.
Závěr:
Přímá refluxní UIA je vhodná u nízkotlakých ortotopických náhrad močového měchýře. Prevence refluxu je však opodstatněná u konduitů, heterotopických náhrad močového měchýře a análních močových derivací.Klíčová slova:
ureterointestinální anastomózaÚvod
Dokud bude léčba závažných onemocnění urogenitálního traktu (jako např. nádorů, radiačních traumat, vrozených anomálií, úrazů, neurogenních poškození…) vyžadovat rekonstrukce defektních orgánů pomocí úseků střevní trubice, potud bude vytvoření dlouhodobě spolehlivé ureterointestinální anastomózy (UIA) patřit k jednomu z nejdůležitějších požadavků rekonstrukční urologie. UIA je jedním z nejkritičtějších míst vzniku závažných komplikací střevní derivace moče či střevní substituce močových cest. Zdokonalování stávajících a vývoj nových metod UIA je motivován snahou o snížení časných i pozdních pooperačních komplikací. Nutnost užití antirefluxní UIA (zabraňující zpětnému toku moče do ureteru či ledviny), zejména u ortotopických nízkotlakých náhrad měchýře, je kontroverzní [1–6]: Podle některých autorů antirefluxní UIA jakéhokoliv typu obecně zvyšují – v porovnání s refluxními UIA – riziko obstrukce, která ohrožuje funkci ledvin více než reflux moče [4,6,7]. Studer a Turner doporučují antirefluxní UIA pouze v případech derivací moče, které jsou schopny vytvářet vysoké intraluminální tlaky a/nebo je u nich velká pravděpodobnost trvalé bakteriální kolonizace [6]. Jiní autoři pokládají prevenci refluxu za jeden z nezbytných předpokladů bezpečné derivace moče [1,3,8]. Vycházejí přitom z animálních experimentů i klinických studií [9–13]. Vyvíjejí proto metody ureterointestinálních spojení účinně zabraňujících refluxu a současně s minimální tendencí ke stenotizaci [9,14,15,16,17].
Způsob použité močové derivace tedy určuje i použití specifického typu UIA. Na základě hodnocení téměř 16 000 radikálních cystektomií provedených v předních světových centrech v letech 1971 až 2010 bylo zjištěno, že ve 42 % byla jako forma močové derivace zvolena kutánní ureteroileostomie (ileální konduit), ve 38 % ortotopická (ileální) kontinentní náhrada močového měchýře a pouze v 7,5 % anální kontinentní močová derivace [18].
Z výše uvedeného je zřejmé, že v současnosti nachází v drtivé většině uplatnění přímá refluxní ureteroileální anastomóza, aniž by bylo zcela jasné, zda je to vždy to nejlepší řešení.
Refluxní a antireflexní ureterointestinální anastomóza
Přímé, eliptické − refluxní – UIA jsou v modifikacích Nesbitově [19] či Wallaceově [20] (Obr. 1) dnes používány naprostou většinou urologů ve spojení se dvěma nejčastěji prováděnými typy močové derivace, resp. substituce močového měchýře: je to jednak ileální konduit (kutánní ureteroileostomie) (Obr. 2), jednak ortotopická ileální náhrada močového měchýře – nejčastěji typu Studer pouch [6,21] (Obr. 3), nebo modifikace W-pouche [22,23] (Obr. 4), a to jak v otevřené, tak i robotické operativě. Pokládají totiž prevenci refluxu moče do horních cest močových a ledvin za zbytečnou: kontinentní ortotopické (většinou ileální) náhrady močového měchýře jsou v době jímací fáze nízkotlaké, během močení (břišním lisem a relaxací pánevního dna) nevzniká tlakový gradient mezi střevním močovým měchýřem a horními cestami močovými, protože měchýř, díky konstrukci stěny z detubularizovaného ilea do sférického tvaru, sám aktivně negeneruje tlak schopný vyvolat reflux [6,24,25]. Horní močové cesty tak zůstávají dlouhodobě nepoškozené. Pokud je použita technika eliptické přímé anastomózy UIA, striktury vznikají, jak argumentují, u méně než 3 % pacientů [26]. Existují ovšem údaje o vyšší frekvenci stenotizace [27]. Používání ureterálních stentů zlepšuje výsledky [28]. V polovině případů se jedná o krátké striktury, které lze úspěšně řešit endourologicky [26]. Tyto poznatky stran UIA byly potvrzeny v randomizovaných studiích [29,30]. Existují domněnky, že obecně jakákoliv antirefluxní UIA má inherentně vyšší tendenci ke stenotizaci a ohrožuje funkci ledvin obstrukčními komplikacemi [6]. Přitom k poškození renálních funkcí u pacientů s ortotopickou náhradou močového měchýře za 10 roků od operace došlo v bernské studii u 21 % pacientů, ve 12 % v důsledku obstrukce [27].
Obr. 1. Ureterointestinální anastomózy: a) přímá eliptická anastomóza dle Nesbita, b) anastomóza dle Wallaceho, typ 1 (head-to-head), c) antirefluxní anastomóza „flap-and-trough“ dle Doležela Fig. 1: Uretero-intestinal anastomoses: a) Nesbit, b) Wallace, c) I Flap-and-Trough 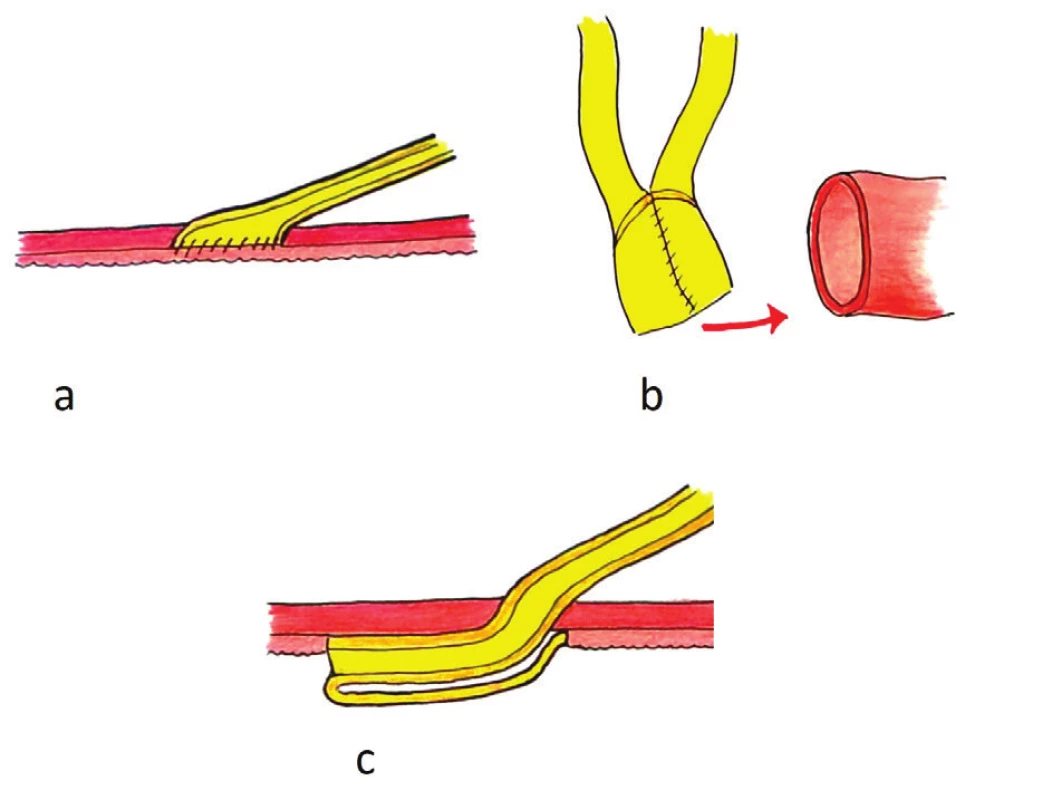
Obr. 2. Ureteroileální konduit (kutánní ureteroileostomie) – schéma Fig. 2: Ileal conduit diagram 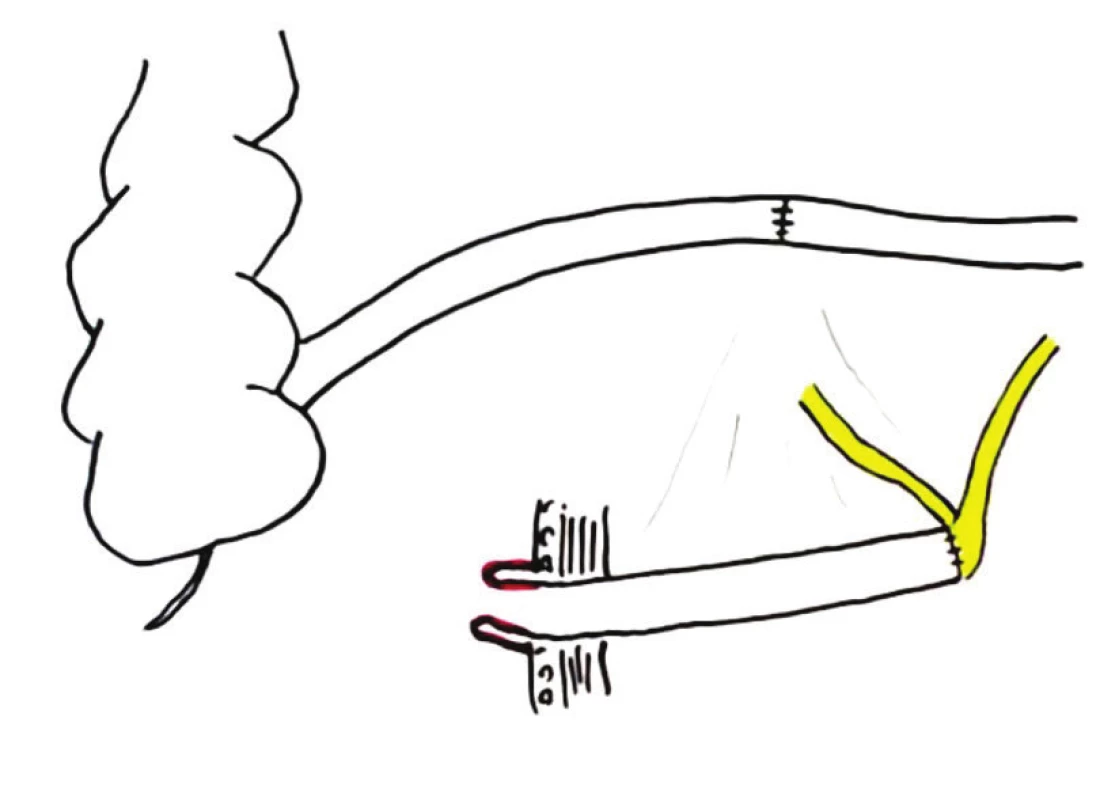
Obr. 3. Studer pouch, ileální ortotopická náhrada močového měchýře – schéma: exkludace 60 cm preterminálního ilea; detubularizace 40 cm aborálního úseku; aferentní izoperistaltický segment 20 cm, do jehož vrcholu jsou vyústěny uretery přímou anastomózou (Nesbit); sférický pouch, jehož obvod tvoří 4 obvody ilea – „cross-folded“, je na pojen na pahýl uretry Fig. 3: Studer pouch – diagram: 60 cm of excluded preterminal ileum, 40 cm detubularization, 20 cm afferent isoperistaltic segment, direct uretero-ileal anastomoses (Nesbit), spheric pouch (cross-folded configuration) connected to the urethra 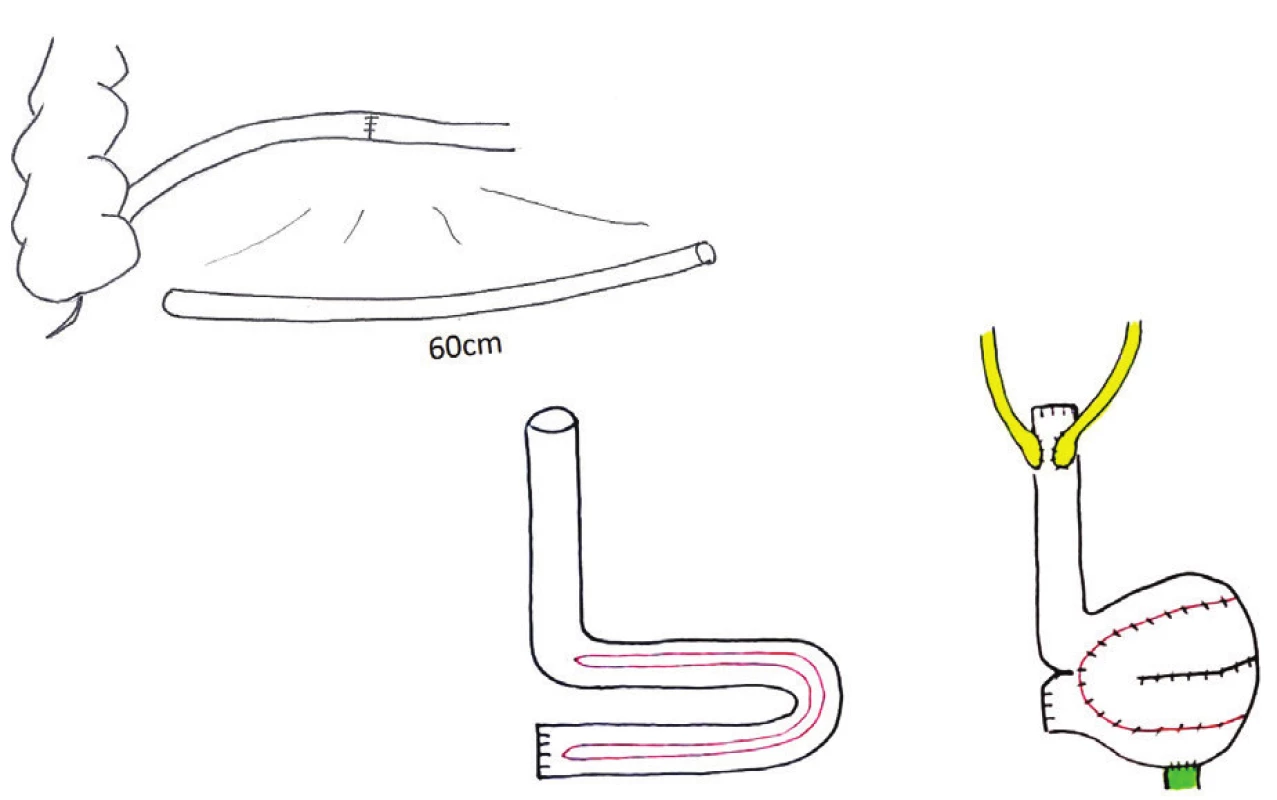
Obr. 4. W-pouch, ileální ortotopická náhrada močového měchýře – schéma: exkludace 40 cm preterminálního ilea; detubularizace s ponecháním tubulárních segmentů na koncích délky 2−3 cm; konstrukce sférického pouche napojeného na pahýl uretry; přímá implantace ureterů do otevřených konců ilea Fig. 4: W-orthotopic neobladder – diagram: 40 cm of excluded preterminal ileum, with two 2−3 cm chimneys at the ends, to which ureters are directly implanted 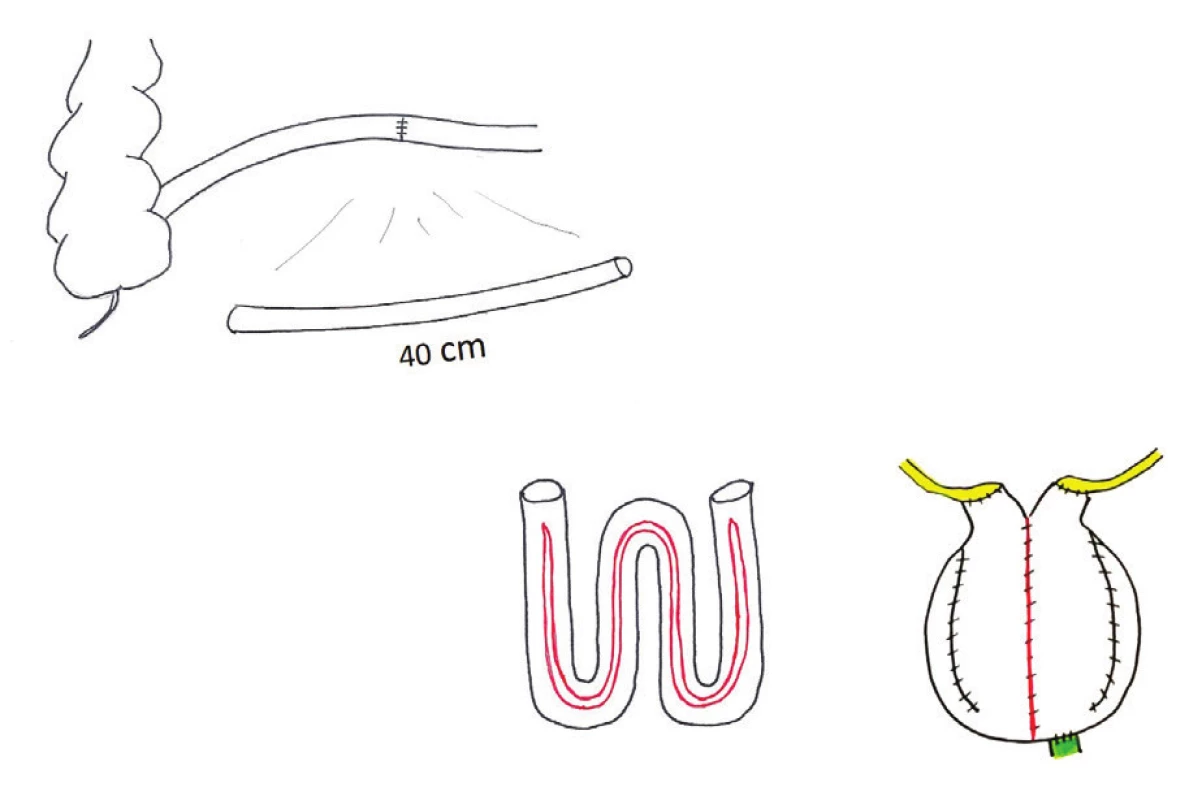
Jiní autoři pokládají prevenci vezikoureterálního refluxu za jeden z obecných nezbytných předpokladů bezpečné derivace moče či náhrady močového měchýře včetně ortotopických nízkotlakých náhrad [1,3,8]. Vycházejí přitom z animálních experimentů i klinických studií [9−13]. Poukazují na nezanedbatelný výskyt bakteriální kolonizace rezervoárů, zvláště v případě vzniku hyperkontinence (je častější u žen) s následnými močeními pomocí režimu intermitentní katetrizace a tím nebezpečí ascendentní infekce ledvin při eventuálním refluxu [31], způsobeném např. zevní kompresí naplněného rezervoáru. Mezi zastánce tohoto postoje patří i autor tohoto pojednání. Tito autoři se proto snaží vyvíjet nové metody ureterointestinálních chlopní, účinně zabraňujících refluxu a současně majících minimální tendenci ke stenotizaci. Tým autora vyvinul a klinicky úspěšně testoval originální antirefluxní UIA, kterou označuje jako metodu „laloku a žlábku“ – „flap and trough“ (FT) [15].
Používání refluxních anastomóz u ileálních konduitů, které jsou trvale bakterielně kolonizované a svojí peristaltickou aktivitou generují vysoké intraluminální tlaky, má v dnešní době především technický důvod: většina urologů pokládá konstrukci antirefluxní anastomózy u tohoto typu derivace za zbytečně riskantní, komplikovanou nebo přímo nemožnou. Z dlouhodobého hlediska však může být použití refluxní UIA u ileálních konduitů nebezpečné a může vést k ireverzibilnímu poškození funkce ledvin vysokotlakým infekčním refluxem [32]. K deterioraci renálních funkcí během 10 let od operace došlo ve výše zmíněné studii bernského týmu u 36 % pacientů s ileálním konduitem [27]. Antirefluxní anastomóza typu FT se nabízí jako možné řešení pro tyto derivace [17] (Obr. 5).
Obr. 5. Dvouhlavňová antirefluxní FT ureteroileální anastomóza do vrcholu ileálního konduitu – peroperační pohled. Fig. 5: Double-barrelled FT anastomosis at the open end of ileal conduit – intraoperative view 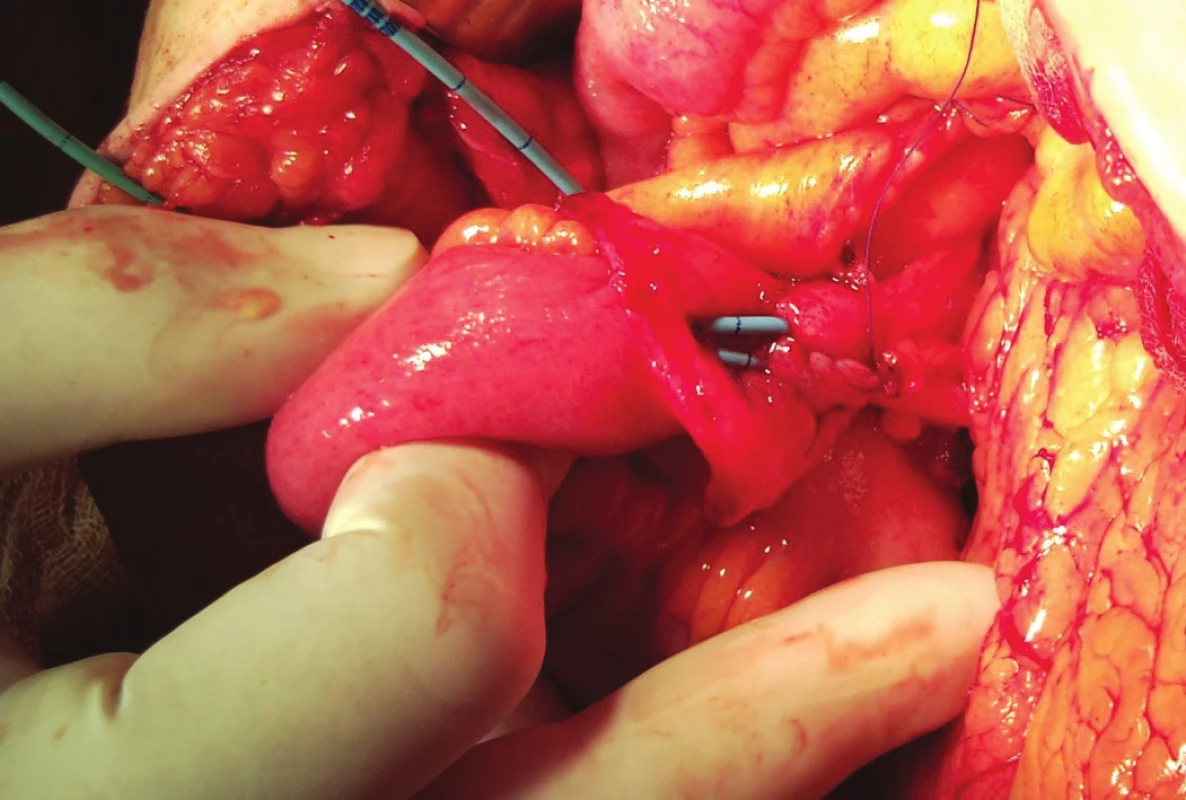
Konstrukce uretero-ileální antirefluxní anastomózy totiž představuje specifický problém: pevné spojení ileální sliznice s valvulae conniventes brání vytvoření podslizničního antirefluxního tunelu způsobem standardně uplatňovaným pro implantace ureterů do močového měchýře, colon či žaludku. V minulosti často používaná Le Ducova antirefluxní uretero-ileální anastomóza [33] je dnes považována za vyloženě nevhodnou pro vysoký výskyt komplikací – zřejmě v důsledku přímého působení moče na obnaženou adventicii intramurálního ureteru [34,35]. Podobně se ustoupilo od používání rozpolcené manžety (split cuff nipple [36,37]), protože její hojení je doprovázeno deformací následkem kontraktury rozštěpené strany manžety s možnou následnou ztrátou antirefluxního potenciálu a případně i vývojem obstrukce [15]. Serózou vystlaný extramurální tunel – serous-lined extramural tunnel (SLET) [8] – dnes používá u ileálních orotopických náhrad jen málo pracovišť [2]. Jeho slabinou je možnost dehiscence dorzální seromuskulární sutury tunelu [1]. Modifikací SLET metody je „T-pouch chlopeň“ [14]: ta bude mít pravděpodobně i podobné charakteristiky, je však technicky ještě složitější, takže se v současnosti běžně nepoužívá.
FT technika [15] (Obr. 1) zajišťuje dokonalou a okamžitou ochranu adventicie intramurálního ureteru tkání fyziologicky rezistentní k působení moče – podobně jako SLET technika a na rozdíl od Le Ducovy. Distální a proximální fixace intramurálního ureteru zajišťuje stabilní délku antirefluxního tunelu. Oba tyto prvky by měly zvyšovat její spolehlivost ve smyslu antirefluxního potenciálu a odolnosti vůči obstrukci. Navíc to, že meatus močovodu není po celém obvodu lemován suturou, může přispívat k menší tendenci k jeho stenotizaci. Místo FT anastomózy bylo vždy při endoskopických kontrolách snadno detekovatelné. Na rozdíl od SLET anastomózy antirefluxní tunel FT metody se nemůže otevřít [1]. Osa antirefluxního kanálu FT techniky může probíhat v jakémkoli směru vzhledem k ose střevní (na rozdíl od SLET), takže může vždy směřovat směrem k hrdlu neovesiky a tím usnadňovat endoskopickou sondáž [38] (Obr. 6). FT metoda umožňuje implantaci ureterů normálních i velkých kalibrů. Technika konstrukce FT anastomózy je ve srovnání s ostatními předloženými metodami technicky jednoduchá, umožňuje transluminální i extraluminální přístup, jakož i společnou implantaci dvou a více ureterů (dvou/více/hlavňová varianta) [16] (Obr. 5). Je snadno proveditelná otevřeným způsobem i roboticky asistovaně (systém daVinci®). Kromě toho lze FT metodu s výhodou využít i pro implantace do kolických derivací v případech, kdy se to jeví výhodnější než užití klasických metod využívajících podslizničních kanálů, jako je tomu např. v případech dilatovaných močovodů [39] (Obr. 7, 8). V kontrolované studii (49 pacientů, 95 renoureterálních jednotek) FT metoda nevedla ke zvýšenému výskytu obstrukčních komplikací [17].
Obr. 6. FT ureteroileální anastomóza do ortotopické neoveziky: a) 13. měsíc po implantaci, b) cystoskopický pohled 68. měsíc po operaci. Fig. 6: FT UIA into the ileal neobladder: a) 13 months, and 68 months, b) after the procedure 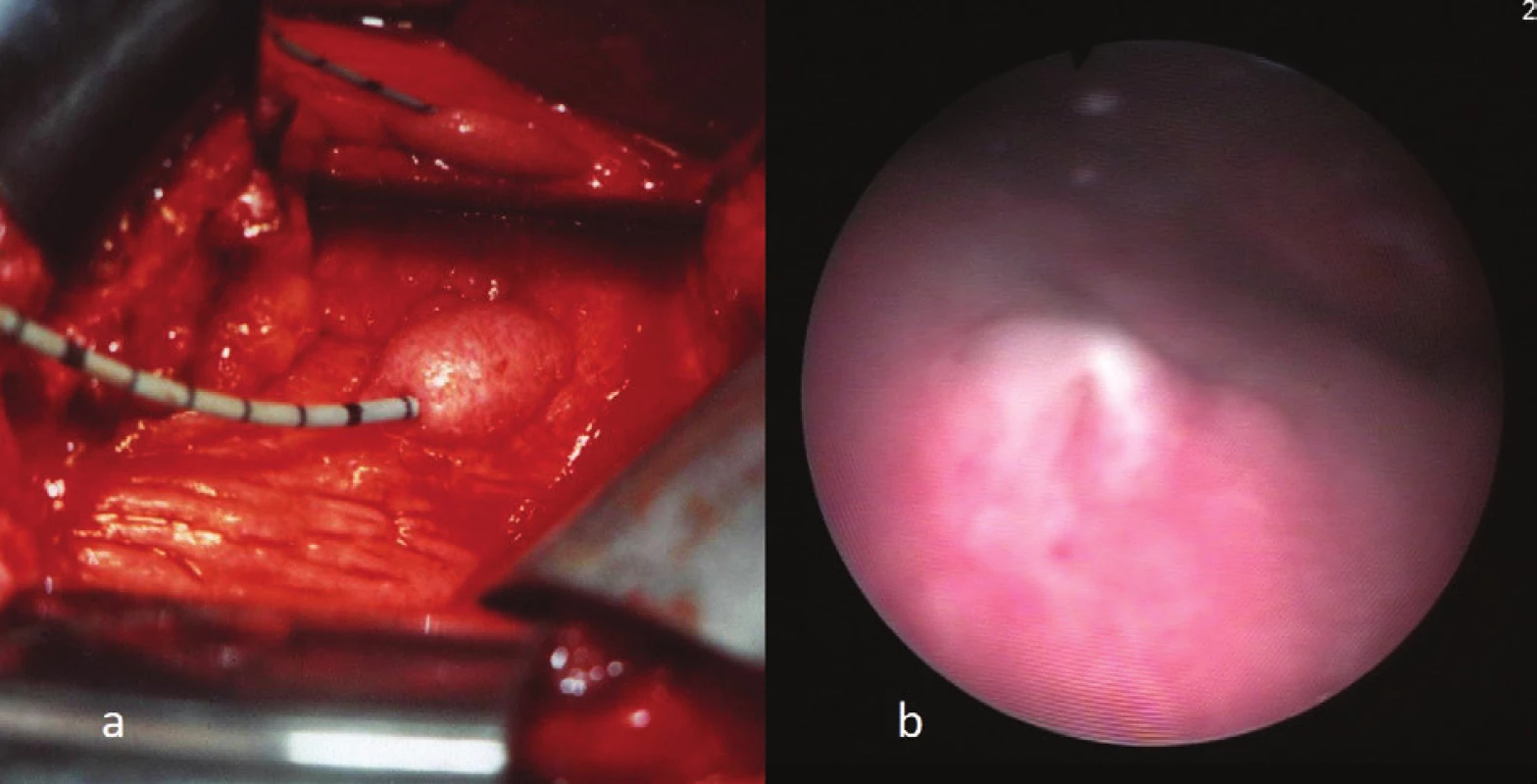
Obr. 7. Sigma-rectum pouch (Mainz Pouch II) – shema: detubularizace 20 cm sigmatu nad rektosigmatickým přechodem; konstrukce sférického pouche, do jehož dorzální stěny jsou antirefluxně vyústěny uretery metodou FT. Kontinenci moče (a stolice) zajišťuje anální svěrač. Fig. 7: Sigma-rectum pouch (Mainz pouch II) – diagram: 20 cm of detubularization, spheric configuration, antirefluxing FT UIA at the dorsal wall 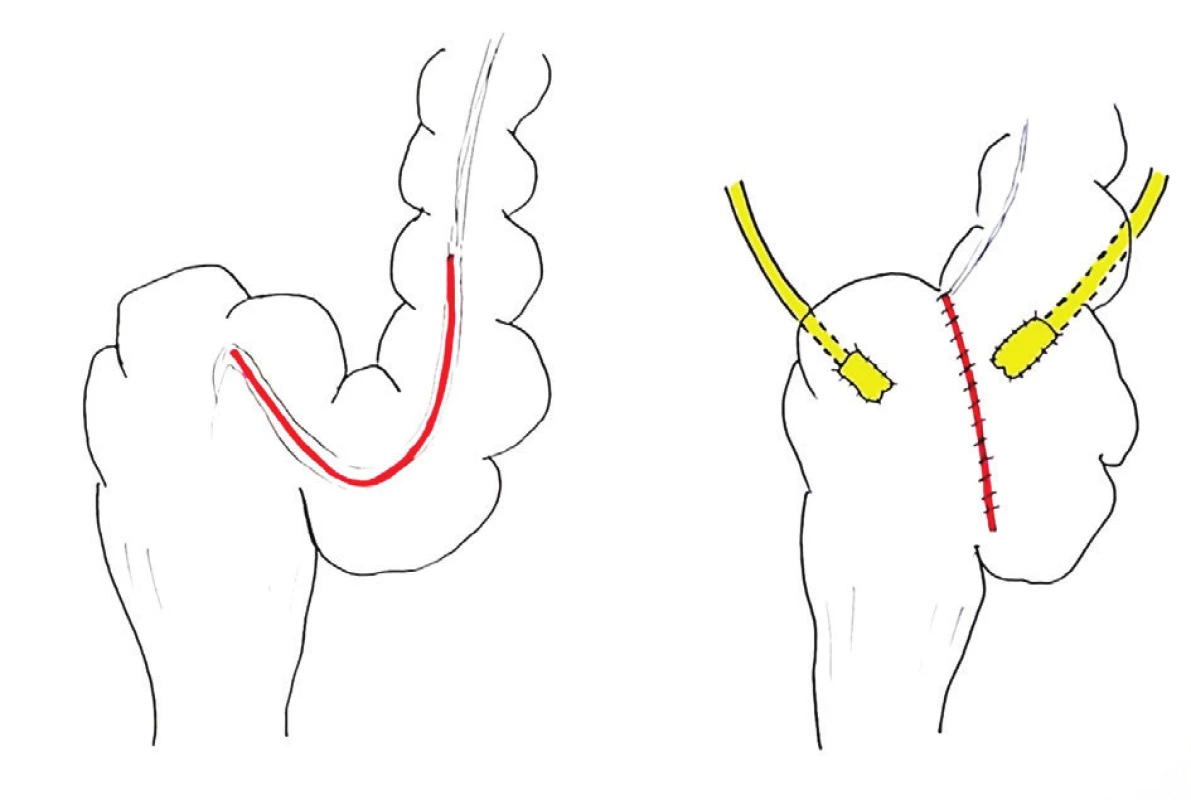
Obr. 8. FT – ureterosigmatické anastomózy do sigma-rektum pouche: a) peroperační pohled, b) kolonoskopický pohled 60. měsíc po operaci. Fig. 8: FT anastomoses to the sigma-rectum pouch: a) peroperation view, b) 60 months after the procedure (colonoscopy) 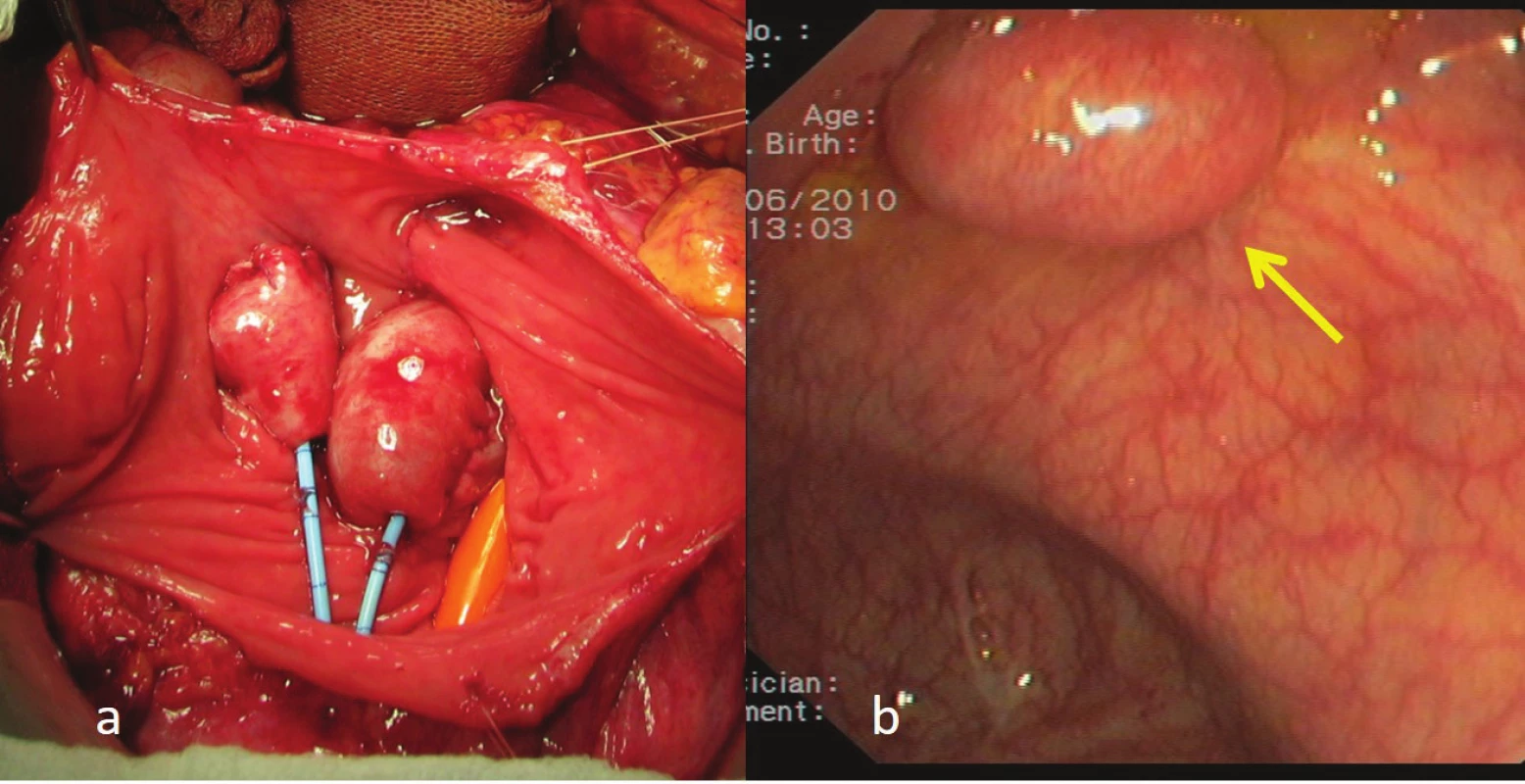
Závěr
U ortotopických ileálních náhrad močového měchýře je pravděpodobně používání přímých refluxních ureterointestinálních anastomóz ve většině případů relativně bezpečné. U střevních močových derivací, které jsou schopné generovat vysoké intraluminální tlaky a/nebo jsou trvale bakteriálně kolonizované, má konstrukce antirefluxní ureterointestinální anastomózy zřejmě opodstatnění. Rozřešit současné debaty ohledně vhodnosti aplikace antirefluxní či refluxní UIA v různých typech močové derivace však může pouze dobře vedená randomizovaná multicentrická prospektivní studie.
Podpořeno MZ ČR-RVO ( MOÚ,00209805).
Konflikt zájmů
Autor článku prohlašuje, že není v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise.
Doc. MUDr. Jan Doležel, PhD.
Františky Stránecké 541/3
602 00 Brno
e-mail: dolezel@mou.cz
Zdroje
1. Månsson W. Comment. In Hohenfellner R, Novick A, Fichtner J, editors. Innovations in Urologic Surgery. 2nd ed. Oxford: Isis Medical Media. 1997 : 622−3.
2. Abol-Enein H, Ghoneim MA. Functional results of orthotopic ileal neobladder with serous-lined extramural ureteral reimplantation: Experience with 450 patients. J Urol 2001;165 : 1427−32.
3. Kristjánsson A, Månsson W. Refluxing or nonrefluxing ureteric anastomosis. BJU Int 1999;84 : 905−10.
4. Hohenfellner R, Black P, Leissner J, et al. Refluxing ureterointestinal anastomosis for continent cutaneous urinary diversion. J Urol 2002;168 : 1013−7.
5. Ghoneim MA. Editorial comment. In Hohenfellner R, Black P, Leissner J, et al. Refluxing ureterointestinal anastomosis for continent cutaneous urinary diversion. J Urol 2002;168 : 1013−7.
6. Studer UE, Turner WH. Is reflux prevention important in urinary diversion? In Webster GD, Goldwasser B, editors. Urinary diversion: Scientific foundations and clinical practice. Oxford, Isis Medical Media 1995 : 282−93.
7. Waidelich R, Rink F, Kriegmair M, et al. A study of reflux in patients with an ileal orthotopic bladder. Br J Urol 1998;81 : 241–6.
8. Abol-Enein H, Ghoneim MA. A novel uretero-ileal reimplantation technique: The serous lined extramural tunnel. A preliminary report. J Urol 1994;151 : 1193−7.
9. Kristjánsson A, Abol-Enein H, Alm P, et al. Long-term renal morphology and function following enterocystoplasty (refluxing or antireflux anast.): an experimental study. Br J Urol 1996;78 : 840−6.
10. Richie JP, Skinner DG. Urinary diversion: the physiological rationale for non-refluxing colonic conduits. Br J Urol 1975;47 : 269−75.
11. Duggan FJ, Sanford EJ, Rohner TJ. The disadvantages of reflux in uretero-ileal cutaneous anastomoses for supravesical urinary diversion. Urol Res 1974;2 : 85−90.
12. Kristjánsson A, Wallin L, Månsson W. Renal function up to 16 years after conduit (refluxing or anti-reflux anastomosis) or continent urinary diversion. 1. glomerular filtration rate and patency of uretero-intestinal anastomosis. Br J Urol 1995;76 : 539−45.
13. Kristjánsson A, Bajc M, Willin L, et al. Renal function up to 16 years after conduit (refluxing or antireflux anast.) or continent urin. diversion. 2. Renal scaring and location of bacteriuria. Br J Urol 1995;76 : 546−50.
14. Stein JP, Lieskovsky G, Ginsberg DA, et al. The T pouch: an orthotopic ileal neobladder incorporating a serosal lined ileal antireflux technique. J Urol 1998;159 : 1836−42.
15. Doležel J. Uretero-ileal anastomosis: a preliminary report of novel modification - the flap-and-trough technique. BJU Int 2001;88(cr3):299.
16. Doležel J, Sutorý M, Navrátil P. Antireflux uretero-intestinal anastomosis – Flap-and-Trough technique − applicable to ileum: Early clinical experience. Eur Urol 2004;46 : 598−603.
17. Doležel J, Čapák I, Valík D, et al. The effect of uretero-intestinal anastomosis on renal function and morbidity in intestinal urinary diversion. Scand J Urol 2013;47 : 225−9.
18. Hautmann ER, Abol-Enein H, Davidsson T, et al. ICUD-EAU International Consultation on Bladder Cancer 2012: Urinary diversion. Eur Urol 2013;63 : 67−80.
19. Nesbit RM. Uretero-sigmoid anastomosis by direct elliptical anastomosis. J Urol 1949;61 : 728−34.
20. Wallace DM. Ureteric diversion using a conduit: a simplified technique. Br J Urol 1966 : 38 : 522−7.
21. Studer UE, Ackermnn D, Casanova GA. Three years’ experience with an ileal low pressure bladder substitute. Br J Urol 1989;63 : 43−52.
22. Hautmann RE, de Petriconi RC, Volkmer BG. 25 years of experience with 1,000 neobladders: long-term complications. J Urol. 2011;85 : 2207–12.
23. Elbendary M, El Gamal OM, Tawfik AM, et al. Simple modification in Hautmann neobladder to carry out left ureteroileal anastmosis without mobilization of the ureter. Int J Urol 2014;21 : 413−5.
24. Waidelich R, Rink F, Kriegmair M, et al. A study of reflux in patients with an ileal orthotopic bladder. Br J Urol 1998;81 : 241–6.
25. Studer UE, Turner WH. The ileal orthotopic bladder. Urology 1995;45 : 185−9.
26. Studer UE, Burkhard FC, Schumacher M, et al. Twenty years experience with an ileal orthotopic low pressure bladder substitute – lessons to be learned. J Urol 2006;176 : 161–6.
27. Jin XD, Roethlisberger S, Burkhard FC, et al. Long-term renal function after urinary diversion by ileal conduit or orthotopic ileal bladder substitution. Eur Urol 2012;61 : 491–7.
28. Mattei A, Birkhaeuser FD, Baermann C, et al. To stent or not to stent perioperatively the ureteroileal anastomosis of ileal orthotopic bladder substitutes and ileal conduits? Results of a prospective randomized trial. J Urol 2008;179 : 582–6.
29. Kessler TM, Burkhard FC, Perimenis P, et al. Attempted nerve sparing surgery and age have a significant effect on urinary continence and erectile function after radical cystoprostatectomy and ileal orthotopic bladder substitution. J Urol 2004;172 : 1323–7.
30. Shaaban AA, Abdel-Latif M, Mosbah A, et al. A randomized study comparing an antireflux system with a direct ureteric anastomosis in patients with orthotopic ileal neobladders. BJU Int 2006;97 : 1057–62.
31. Gakis G, Stenzl A. Ileal neobladder and its variants. Eur Urol 2010;745−53.
32. Neal DE, Urodynamic investigation of the ileal conduit: upper tract dilatation and the effects of revision of the conduit. J. Urol 1989;142 : 97−100.
33. Le Duc A, Camey M, Teillac P. An original antireflux uretero-ileal implantation technique: long-term follow-up. J Urol 1987;137 : 1156−8.
34. Nagele U, Sievert KD, Merseburger AS, et al. A. Urinary diversion following cystectomy. EAU Update Series 2005 : 129−37.
35. Shaaban AA, Gaballah MA, El-Diasty TA, et al. Urethral controlled bladder substitution: a comparison between the intussusc. nipple valve and the technique of Le Duc as antireflux procedures. J Urol 1992;148 : 1156−61.
36. Heitz-Boyer M, Hovelacque A. Creation d´une nouvelle vessie et d´un nouvel uretre. J d´Urol Med Chir 1912;18 : 237−58.
37. Sagalowsky AI Further experience with split-cuff nipple ureteral reimplantation in urinary diversion. J Urol 1998;159 : 1843−4.
38. Stenzl A, Sherif H, Kuczyk M. Radical cystectomy with orthotopic neobladder for invasive bladder cancer: A critical analysis of long term oncological, functional and quality of life results. Int Brazil J Urol 2010;36 : 537−47.
39. Doležel J, Čapák I, Staník, et al. Vlastní modifikace uretero-intestinální resp. uretero-neocystoanastomózy v onkochirurgii a rekonstrukční urologii. In: Abrahamová J, editor. Vybrané otázky onkologie XIV. Praha, Galén 2010 : 32−3.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2017 Číslo 4- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Stillova choroba: vzácné a závažné systémové onemocnění
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Vzpomínka na profesora Miloše Hájka
- Editorial
- Současný pohled na ureterointestinální anastomózu v močové derivaci
- Hemangiomy jater – kdy indikovat invazivní léčbu?
- Léčba avulzních zlomenin v oblasti pánve a kyčle u dětí a dospívajících
- K životnímu jubileu docenta Leopolda Plevy
- Solidní pseudopapilární tumor pankreatu
- Traumatická ruptura dolní duté žíly s odloženým ošetřením po překladu na specializované pracoviště
- Odešel profesor Miroslav Slavík
- Resekce jater pro recidivující sarkom s náhradou infiltrované dolní duté žíly aortálním allograftem – kazuistika a přehled literatury
- Polymastia v neobvyklej lokalizácii počas gravidity
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Hemangiomy jater – kdy indikovat invazivní léčbu?
- Léčba avulzních zlomenin v oblasti pánve a kyčle u dětí a dospívajících
- Solidní pseudopapilární tumor pankreatu
- Polymastia v neobvyklej lokalizácii počas gravidity
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



