-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Sarkom hrudní stěny po ozáření pro karcinom prsu − kazuistika
Sarcoma of the chest wall after radiotherapy for breast carcinoma – a case report
Introduction:
Sarcoma occurring in soft tissues after radiotherapy is a rare complication of radiation treatment of tumours. It was most often described after treatment for breast cancer as well as for non-Hodgkin lymphoma and cervical carcinoma. The time interval between the radiation therapy and the development of the sarcoma can be very wide. Treatment demands radical surgical resection of the sarcoma with the edge of the resected tissue without tumour cells. In some cases, this is followed by chemotherapy or radiotherapy. The median survival time is 23 months, the longest survival being associated with sarcomas removed in a radical way.Case report:
We present the case of a female patient with recurring leiomyosarcoma of the chest wall after radiotherapy for cancer of the right breast. In 2006, this 62-year-old patient was operated on to keep her right breast with axilla exenteration. After the surgery, hormonal therapy was followed by adjuvant radiotherapy of the right breast and the adjacent axilla. We used a linear accelerator and the total amount of radiation was 50 Gy (2 Gy fractionally once a day, five days a week). Four years after the operation, leiomyosarcoma was diagnosed in the pectoral muscle at the site where the tumour of the right breast had been excised. Between 2011 and 2013, a total of five operations of reoccurring sarcoma were performed – two excisions of the tumour, a mastectomy, rib resection and, at last, block resection of the chest wall. Adjuvant oncological treatment was not indicated. The patient, now being 69 years old, is still in a good physical and mental condition without any generalization of the disease.Conclusion:
Sarcoma of the chest wall is a relatively rare consequence of radiotherapy for breast cancer. Sarcoma treatment involves radical surgical resection of the tumour whenever possible. The surgery is mostly followed by radiotherapy which, however, is impossible in a patient after breast-preserving surgery for carcinoma with radiotherapy. Chemotherapy is not very effective in sarcomas. Therefore, the operation needs to be performed by an experienced surgeon in a sufficiently radical way.Key words:
breast cancer – radiotherapy – sarcoma after radiotherapy
Autoři: I. Zedníková 1; J. Šafránek 1
; M. Hlaváčková 2; O. Hes 3; T. Svoboda 4
Působiště autorů: Chirurgická klinika FN Plzeň-Lochotín, přednosta: prof. MUDr. V. Třeška, DrSc. 1; Klinika zobrazovacích metod FN Plzeň-Lochotín, přednosta: doc. MUDr. B. Kreuzberg, CSc. 2; Šiklův patologicko-anatomický ústav FN Plzeň, přednosta: prof. MUDr. M. Michal 3; Onkologické a radioterapeutické oddělení FN Plzeň, přednosta: prof. MUDr. J. Fínek, Ph. D. 4
Vyšlo v časopise: Rozhl. Chir., 2014, roč. 93, č. 7, s. 396-400.
Kategorie: Kazuistika
Souhrn
Úvod:
Sarkom vzniklý v měkkých tkáních po ozáření je vzácnou komplikací radiační léčby nádorů. Byl nejčastěji popsán po léčbě pro karcinom prsu, dále pro non-Hodgkinův lymfom a karcinom děložního čípku. Vzniká v širokém časovém rozmezí po ozáření. V léčbě je nejdůležitější radikální chirurgické odstranění sarkomu s okrajem resekátu bez nádorových buněk. V některých případech následují chemoterapie nebo ozáření. Medián přežití je 23 měsíců, kdy nejdelší přežití je u sarkomů radikálně odstraněných.Kazuistika:
Prezentujeme případ pacientky s recidivujícím leiomyosarkomem hrudní stěny po ozáření pro karcinom pravého prsu. Pacientka byla v roce 2006 po záchovné operaci pravého prsu s exenterací axily ve věku 62 let. Po operaci byla nasazena hormonální terapie a následovalo adjuvantní ozáření pravého prsu a přilehlé axily. Ozáření proběhlo na lineárním urychlovači, celková dávka záření byla 50 Gy (2 Gy frakcionovaně 1krát denně, 5 dní v týdnu). 4 roky po operaci byl diagnostikován leiomyosarkom v pektorálním svalu v místě excize tumoru pravého prsu. V letech 2011−2013 bylo provedeno celkem 5 operací recidivujícího sarkomu – 2krát excize tumoru, mastektomie, resekce žebra a nakonec bloková resekce hrudní stěny. Adjuvantní onkologická léčba nebyla indikována. Pacientka, nyní 69letá, je stále v dobré fyzické i psychické kondici, bez generalizace onemocnění.Závěr:
Sarkom hrudní stěny je poměrně vzácným následkem radioterapie karcinomu prsu. Základem léčby sarkomů je radikální chirurgické odstranění nádoru. Po operaci většinou následuje ozáření, které však u pacientky po záchovné operaci prsu pro karcinom s ozářením již není možné. Chemoterapie není u sarkomů příliš účinná. Proto je nutné, aby operace byla provedena zkušeným chirurgem dostatečně radikálně.Klíčová slova:
karcinom prsu – radioterapie – sarkom po ozářeníÚVOD
Sarkomy jsou heterogenní skupinou zhoubných nádorů vznikajících z pojivových tkání v různých místech organismu. V současné době je známo asi 40 typů sarkomů, které se liší agresivitou a prognózou. Nejčastěji postihují končetiny, méně trup, retroperitoneum, hlavu a krk. Incidence v České republice je asi 350 případů ročně, což je méně než 1 % všech zhoubných nádorových onemocnění [1].
Jediným příznakem sarkomu je v časném stadiu nebolestivá bulka, která se zvětšuje. Retroperitoneální sarkomy se projeví nespecifickými bolestmi břicha či zad. Sarkomy ohrožují nemocného místním prorůstáním do okolních struktur a orgánů a metastazováním, zejména do plic. Prognózu onemocnění ovlivňuje především histologický typ sarkomu, jeho fenotyp, grading, stadium nemoci, lokalizace léze a léčebný postup. V diagnostice se uplatňuje sonografické vyšetření, při podezření na tumor následované počítačovou tomografií (CT) nebo magnetickou rezonancí (MR). K léčbě přistupujeme až po histologické verifikaci sarkomu core-cut biopsií [2]. Základem léčby je radikální chirurgické odstranění nádoru. Po operaci většinou následuje adjuvantní radioterapie. Systémová léčba – chemoterapie a biologická léčba – není u sarkomů příliš účinná. S ohledem na malý počet sarkomů v porovnání s karcinomy by měla být jejich léčba soustředěna do komplexních onkologických center, kde jsou k této léčbě podmínky, co se týče vybavení i zkušeností [3].
Zvláštní skupinu tvoří sarkomy vzniklé v ozářené tkáni a jsou vzácnou komplikací radiační léčby nádorů. Zahrnují 0,5−5,5 % všech sarkomů. Byly nejčastěji popsány po léčbě pro karcinom prsu, dále pro non-Hodgkinův lymfom a karcinom děložního čípku [4,5]. Radiačně indukované sarkomy, konkrétně fibrosarkom a osteosarkom, po radioterapii karcinomu prsu byly poprvé literárně popsány Warrenem a Sommerem v roce 1936 [6]. Vznikají v širokém časovém rozmezí po ozáření. Nejčastějšími histologickými typy jsou osteosarkom, maligní histiocytom, fibrosarkom a angiosarkom [7]. V léčbě je nejdůležitější radikální chirurgické odstranění sarkomu s okrajem resekátu bez nádorových buněk. V některých případech následují chemoterapie nebo ozáření. Prognóza tohoto onemocnění je velmi špatná, pětileté přežití se uvádí 27−36 % [8]. Medián přežití je 23 měsíců, kdy nejdelší přežití je u sarkomů radikálně odstraněných [9,10].
Za posledních 10 let se na našem pracovišti vyskytly pouze 4 případy radiačně indukovaných sarkomů prsu či hrudní stěny po léčbě pro karcinom prsu [6]. Ve třech případech se jednalo o angiosarkom, v jednom případě o leiomyosarkom. Případ ženy s leiomyosarkomem je cílem našeho sdělení.
Kazuistika
Žena, léčená pro arteriální hypertenzi a astma bronchiale, byla v srpnu 2006 operovaná pro karcinom pravého prsu ve věku 62 let. Byla provedena parciální resekce s exenterací axily. Histologie: duktální invazivní karcinom, velikost 9 mm, resekční okraje bez tumoru – do spodiny 4 mm, do stran 20 mm, grade 2, imunohistochemické vyšetření – estrogenové receptory pozitivní v 90 % nádorových buněk, progesteronové receptory pozitivní v 80 % nádorových buněk, proliferační aktivita nízká, 15 uzlin z levé axily bez metastatického postižení, bez průkazu vzdálených metastáz. TNM klasifikace pT1bN0M0 – stadium I. V září 2006 byla zahájena hormonální terapie inhibitory aromatáz (anastrozol). V rozmezí 14. 12. 2006 – 26. 1. 2007 byl nemocné ozářen pravý prs a přilehlá etáž axily. Ozáření proběhlo na lineárním urychlovači, celková dávka záření byla 50 Gy (2 Gy frakcionovaně 1krát denně, 5 dní v týdnu). Pacientka byla dále dispenzarizovaná na Onkologickém a radioterapeutickém oddělení FN Plzeň, měla pravidelně prováděnou mamografii a sonografii prsů a axil 1krát ročně. Mamografie a sonografie v březnu 2010 byly bez známek tumoru. Od září 2010 začala pacientka pociťovat bolesti pravého prsu a v pravé axile s mírným lymfedémem pravé horní končetiny. V listopadu 2010 byl na sonografii popsán tumor na rozhraní zevních kvadrantů pravého prsu nasedající na pektorální fascii, odebraná Core cut biopsie prokázala vřetenobuněčný sarkom s myxoidním fenotypem – leiomyosarkom.
Obr. 1. Struktury leiomyosarkomu s invazí do tukové a svalové tkáně (pravá polovina fotky) Hematoxylin-eosin, zvětšení 100x. Fig. 1: Structures of leiomyosarcoma invading the fatty and muscle tissue (the right half of the photograph). Hematoxylin-Eosin, 100x magnification. 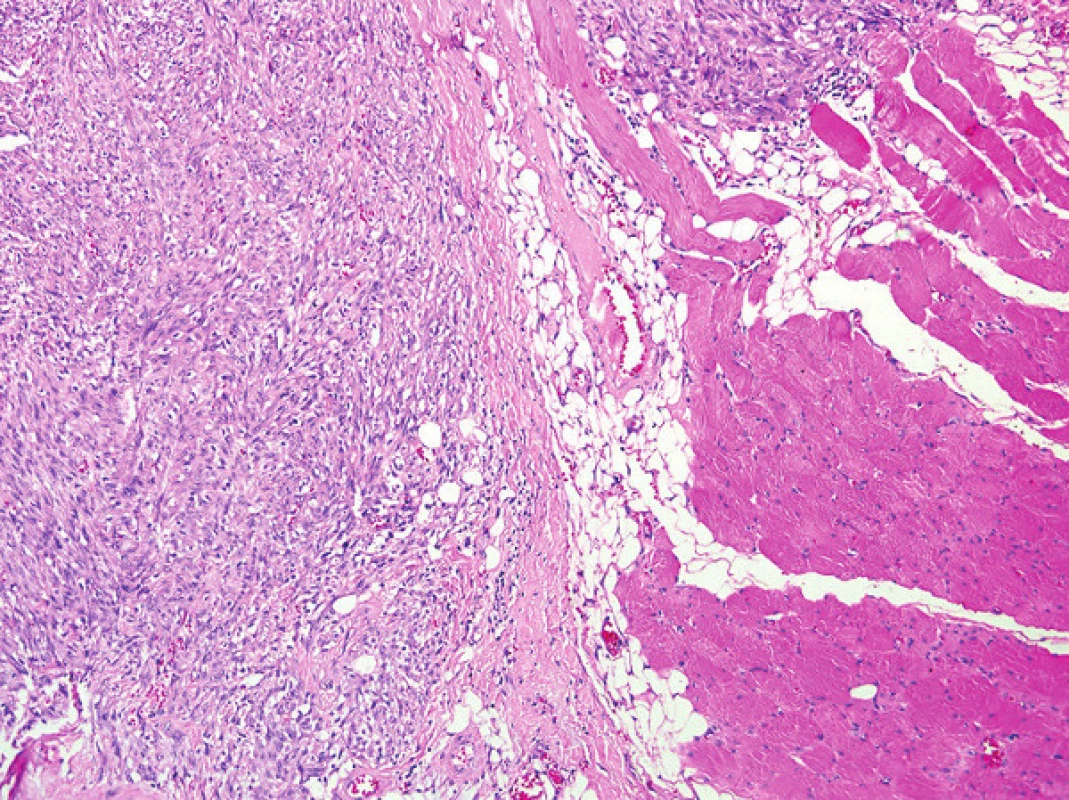
Obr. 2. Leiomyosarkom s bizarními buňkami Hematoxylin-eosin, zvětšení 100x. Fig. 2: Leiomyosarcoma with bizarre cells Hematoxylin-Eosin, 100x magnification. 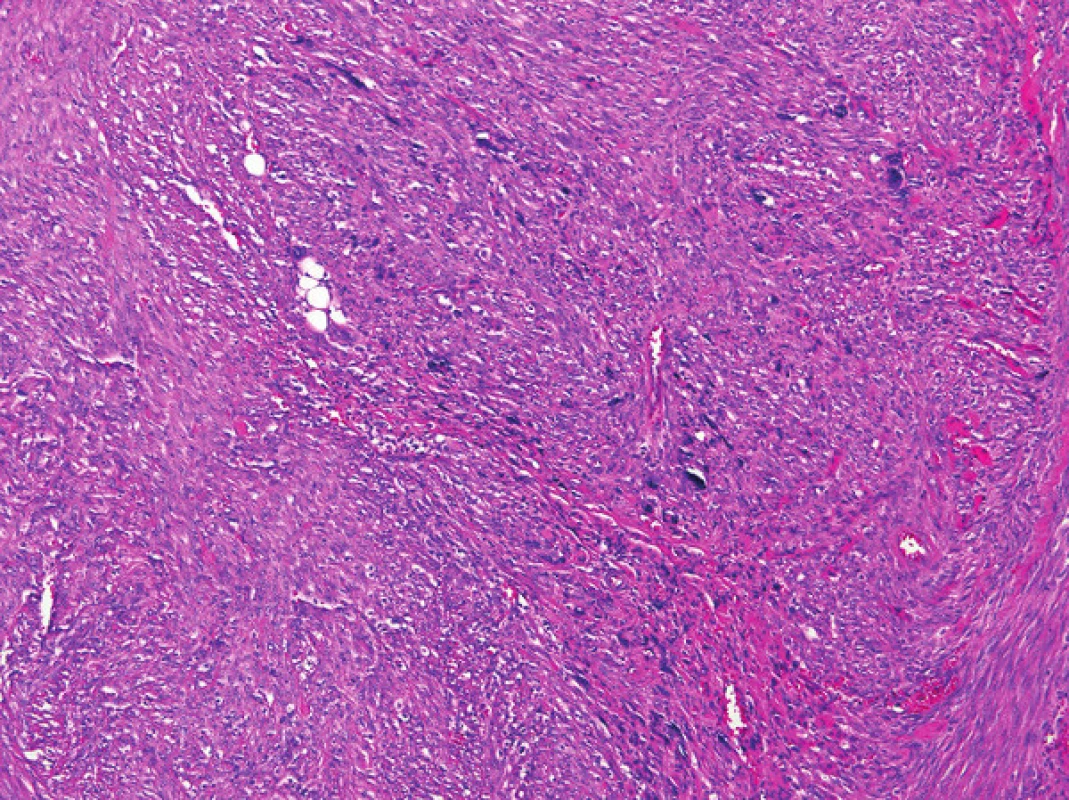
V prosinci 2010 byl na CT hrudníku potvrzen expanzivní útvar v pravém prsu, bez prorůstání do hrudní stěny, bez průkazu plicních metastáz.
Obr. 3. CT hrudníku v prosinci 2010 Fig. 3: Chest CT scan in December 2010 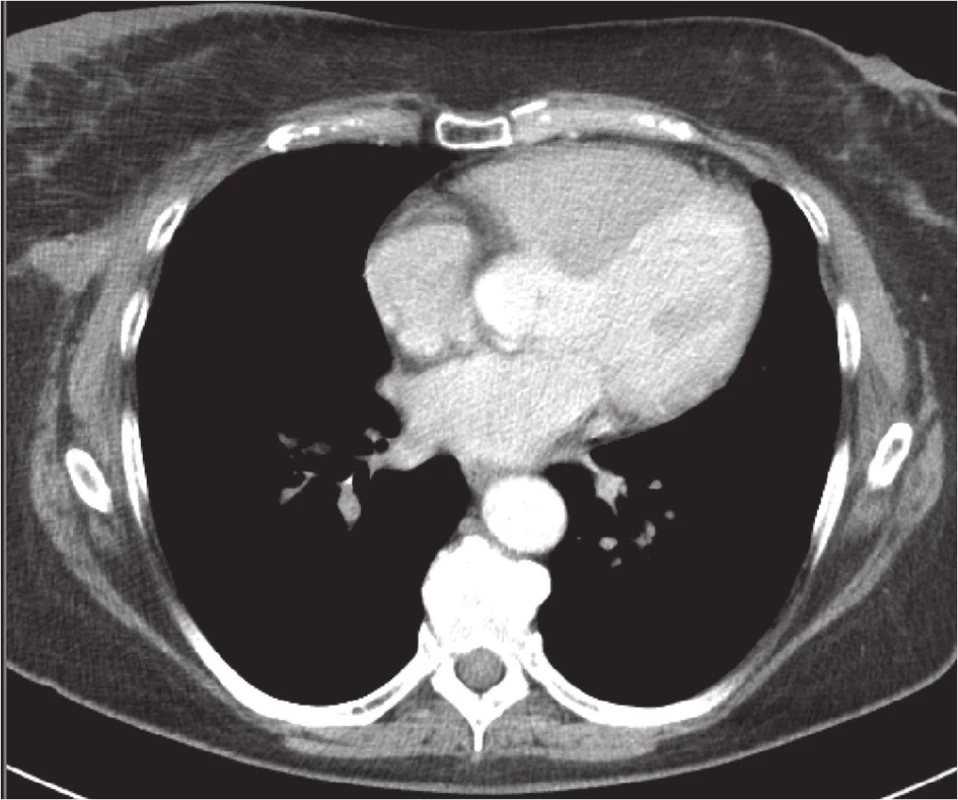
Pacientka byla indikovaná k excizi sarkomu, která byla provedena 31. 1. 2011 radikálně, tumor odstraněn celý, resekční okraje bez nádorových buněk, jeho velikost byla 25x25x17 mm. Imunohistochemické vyšetření – estrogenové a progesteronové receptory negativní, exprese HER2/neu negativní, proliferační aktivita vysoká. Jelikož byla oblast pravého prsu již ozářena po záchovné operaci pro karcinom, nebylo možné provést po operaci ozáření. Onkology byla doporučena pouze dispenzarizace. V květnu 2011 si pacientka sama opět vyhmatala rezistenci v jizvě na pravém prsu, byla provedena sonografie s nálezem suspektní recidivy sarkomu 10x5 mm, poté MR prsů a 25. 7. 2011 opět chirurgická excize recidivy leiomyosarkomu, mikroskopicky opět nádorové struktury nedosahovaly do okraje excize. Jednalo se o recidivu časnou – 3 měsíce od předchozího výkonu.
Obr. 4. MR prsů v červnu 2011 Fig. 4: Breast MRI in June 2011 
Obr. 5. PET/CT vyšetření v říjnu 2012 Fig. 5: PET/CT scan in October 2012 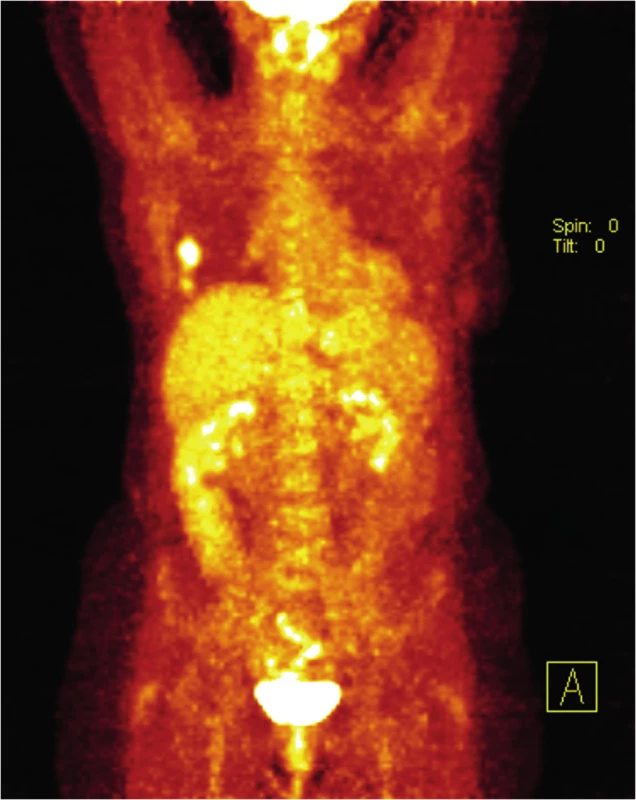
V říjnu 2011 bylo provedeno PET/CT bez zvýšené metabolické aktivity v pravém prsu. V květnu 2012 si pacientka opět vyhmatala rezistenci v jizvě na pravém prsu, byla provedena sonografie a pro podezření na recidivu sarkomu Core cut biopsie, která recidivu potvrdila. 2. 7. 2012 byla provedena pravostranná mastektomie s odstraněním pektorální fascie a části pektorálního svalu pod tumorem s nálezem leiomyosarkomu velikosti 45x25x12 mm, s prorůstáním do pektorálního svalu. Již v září 2012 pacientka opět hmatá rezistenci pod jizvou na hrudní stěně, biopticky byla potvrzena recidiva sarkomu, provedeno PET/CT s nálezem tumoru ve svalu před IV. žebrem, bez generalizace.
28. 11. 2012 jsme provedli resekci části IV. žebra vpravo, histologie – leiomyosarkom dosahující těsně k okraji resekátu, prorůstající do žebra. V dubnu 2013 bylo na kontrolním PET/CT podezření na recidivu sarkomu ve svalech před III. a V. žebrem vpravo. Bez generalizace.
27. 5. 2013 byla provedena resekce hrudní stěny v rozsahu III.−VI. žebra vpravo s náhradou síťkou.
Obr. 6. PET/CT vyšetření v dubnu 2013 Fig. 6: PET/CT scan in April 2013 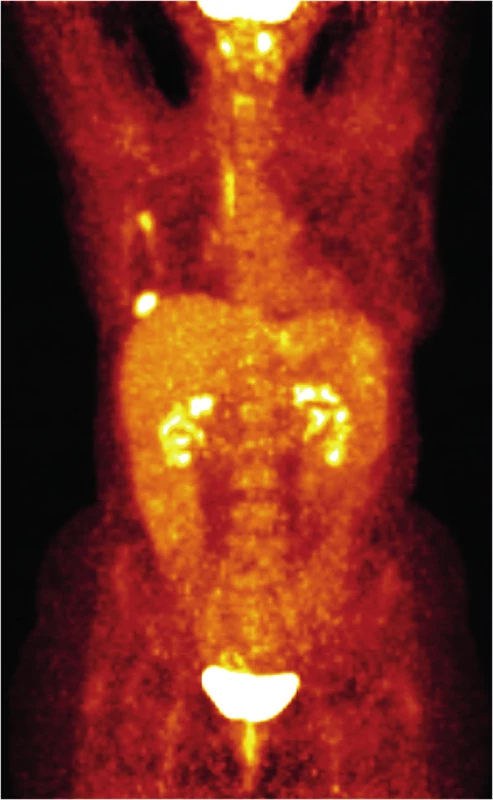
Obr. 7. Rekonstrukce resekované hrudní stěny síťkou Fig. 7: Reconstruction of the resected chest wall with mesh 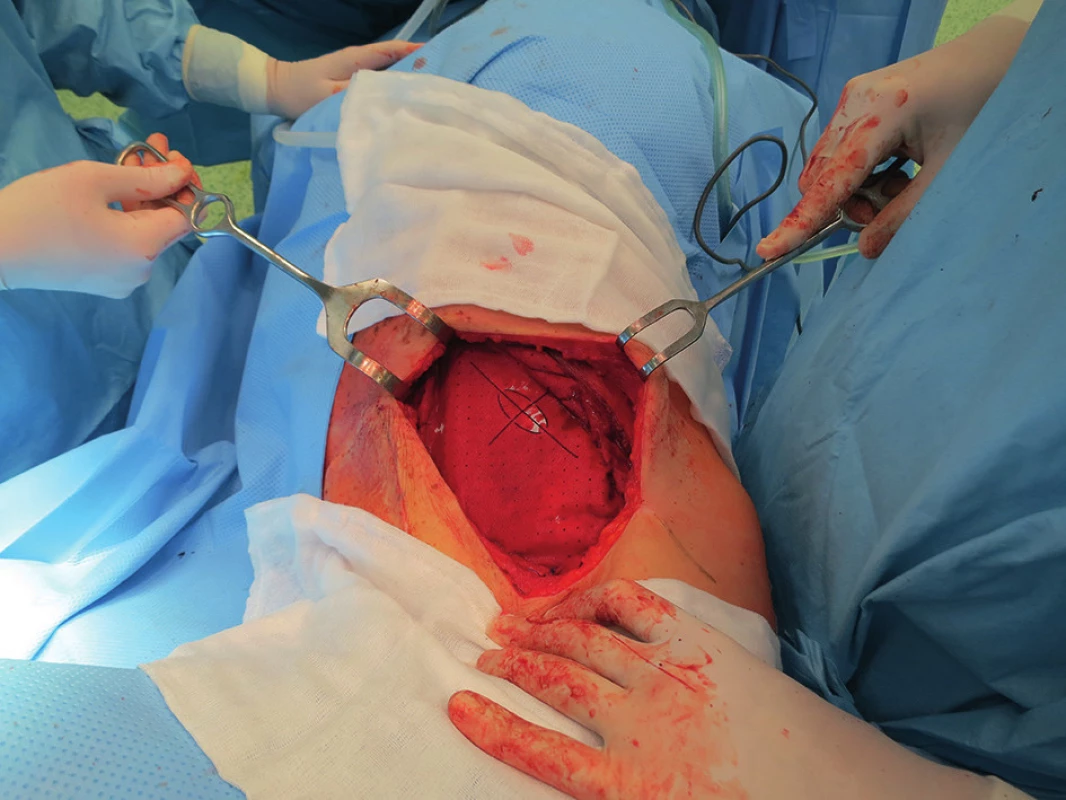
Histologie: nalezeny dva tumory – 40 a 25 mm, okraje resekátu bez nádorové infiltrace, do žeber tumory neprorůstaly. Pacientka, nyní 69letá, je 7 let po operaci pravého prsu pro karcinom, 32 měsíců od stanovení diagnózy sarkomu hrudní stěny, po 5 operacích lokálně recidivujícího sarkomu, stále v dobré fyzické i psychické kondici.
Obr. 8. Výsledný efekt operace Fig. 8: Final effect of the surgery 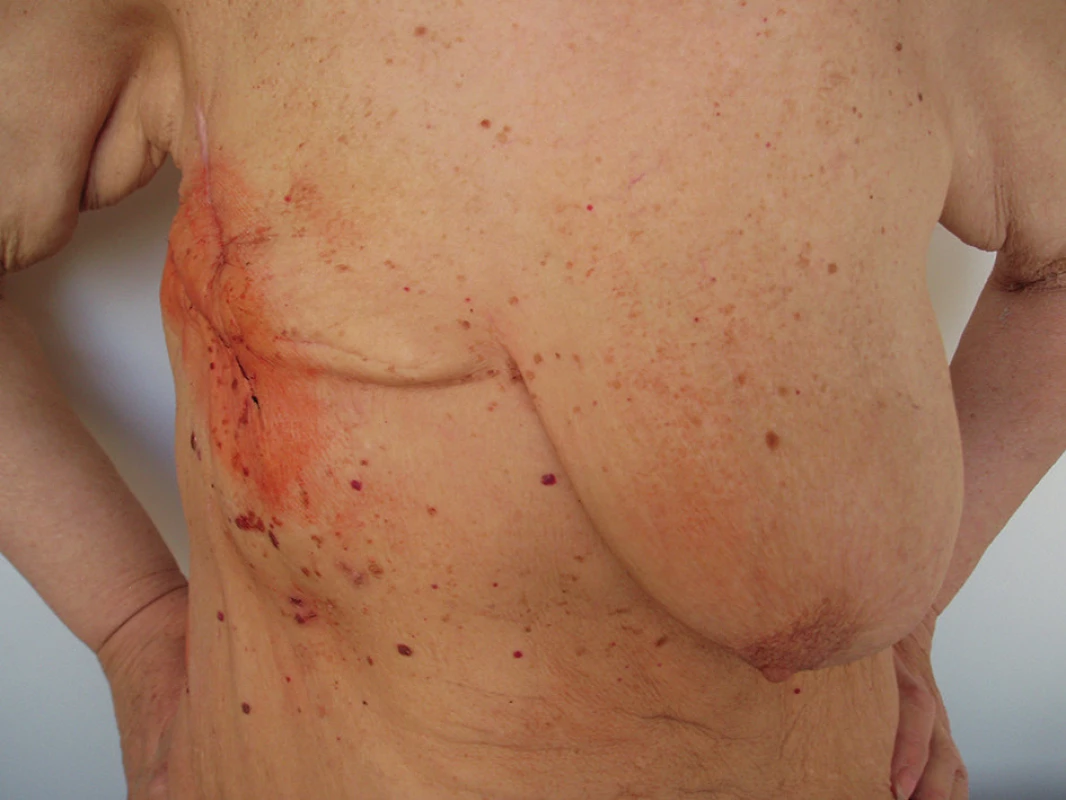
DISKUZE
Žen s karcinomem prsu stále přibývá. Se zlepšující se diagnostikou a léčbou tohoto onemocnění je stále více žen po záchovné operaci prsu s nutností adjuvantního ozáření. Proto musíme počítat i se vzrůstajícím počtem sarkomů vznikajících v ozářené tkáni [11]. Z hlediska etiologie rozlišujeme sarkomy, které v prsu vznikají jako primární nádor, a sarkomy sekundární [12]. Ty dělíme na sarkomy vzniklé následkem chronického lymfedému ipsilaterální horní končetiny a sarkomy vzniklé po léčebném ozáření prsu při léčbě karcinomu [13]. Riziko vzniku sarkomu v ozářené oblasti je velmi malé, uvádí se asi 0,5 % během 15 let [14,15]. Abychom mohli sarkom prohlásit za postradiační, měl by splňovat klasická Cahanova kritéria radiací indukovaného sarkomu, a to histologicky potvrzený sarkom vyrůstající z ozářené oblasti po dlouhé periodě latence [6]. Sekundární sarkomy mají multifaktoriální etiologii, nejzkoumanějšími faktory jsou chronické edematózní a fibrotické změny prsu po operačním výkonu s následnou radioterapií. Navíc zde hraje roli přímé poškození struktury DNA ionizujícím zářením [16,17].
Ženy po léčbě pro karcinom prsu mají tu výhodu, že jsou pečlivě dispenzarizované, mají pravidelné klinické, mamografické a sonografické vyšetření. Jsou také poučeny o nutnosti samovyšetřování. Proto se na diagnózu sarkomu prsu či hrudní stěny přijde včas. Po mamografii a sonografickém vyšetření prsů s nejasným nálezem by měla následovat Core cut biopsie ložiska. Je-li zjištěna diagnóza sarkomu, musí následovat CT hrudníku k určení rozsahu postižení a ev. prorůstání do hrudní stěny [18]. Důležité je také vyloučení vzdálených metastáz [19]. V současné době je jediná účinná léčba sarkomů chirurgická [3]. V případě sarkomu prsu je dostačující excize tumoru, mastektomie nezlepšuje prognózu [20]. Mastektomii provádíme pouze v případě deformace prsu opakovanými operacemi, jako tomu bylo u naší pacientky, nebo na přání nemocné. Prognóza je závislá na mikroskopicky negativních okrajích resekátu. I přesto sarkomy často recidivují [7,12].
Leiomyosarkom prsu či hrudní stěny popsaný v naší kazuistice je extrémně vzácná diagnóza. V literatuře byly zatím popsány pouze desítky případů. Leiomyosarkom v prsní žláze či hrudní stěně vzniká v naprosté většině případů z cévní stěny. Na rozdíl od jiných sarkomů prsu je méně agresivní a má lepší prognózu [14]. Jedná se o pomalu rostoucí tumor, ale s tendencí prorůstat do kůže a pektorálního svalu. V našem případě však leiomyosarkom nebyl pomalu rostoucím tumorem, naopak k recidivám docházelo velmi rychle. Literární údaj o častých lokálních recidivách je patrný i z našeho případu [15]. Informace o tomto typu sarkomu jsou však, vzhledem k malému počtu případů, omezené [16].
Závěr
Z praktického hlediska je důležité na možnost vzniku postradiačního sarkomu prsu myslet, včas ho diagnostikovat a léčit. Ozáření je důležitou součástí léčby karcinomu prsu a jeho profit převyšuje rizika. Navíc riziko vzniku sarkomu v ozářené oblasti je zde velmi malé. V současné době je jediná úspěšná léčba sarkomů chirurgická. Možnosti chemoterapie a radioterapie jsou velmi omezené. Operační výkon by proto měl být pečlivě naplánován a proveden zkušeným operatérem.
Forscher CA, Casciato DA, Territo MC. Manual of Clinical Oncology. Lippincott Williams and Wilkins, Philadelphia 2009;384−396.
NCCN Clinical Practise Guidlines in Oncology. Soft Tissues Sarcoma, V. 1/2011 (dostupný na www.nccn.org).
MUDr. Zedníková Ilona
Chirurgická klinika FN Plzeň-Lochotín
300 00 Plzeň
e-mail: zednikovai@fnplzen.cz
Zdroje
1. Žaloudík J. Chirurgické aspekty léčby sarkomů měkkých tkání. Onkologie 2010;4 : 297−301.
2. Berg JW, Hutter RV. Breast cancer. Cancer 1995;75 : 257−259.
3. Mark RJ, Poen J, Tran LM, et al. Postradiation sarcoma: A single institution study nad review of the literature. Seminars in Oncology 1997;24 : 504−514.
4. Vojtíšek R, Kinkor Z, Fínek J. Sekundární angiosarkomy po konzervativní léčbě nádorů prsu, Klin Onkol 2011;24 : 382−388.
5. Laskin WB, Silverman TA, Enzinger FM. Postradiation soft tissue sarcoma: A analysis of 53 cases. Cancer 1994;73 : 2653−2662.
6. Karlsson P, Holmberg E, Johansson KA, et al. Soft tissue sarcoma after treatment for breast cancer. Radiother Oncol 1996;38 : 25−31.
7. Lagrange JL, Ramaioli A, Chateau MC, et al. Sarcoma after radiation therapy: retrospective multiinstitutional study of 80 histologically confirmed cases. Radiology 2000;216 : 197−200.
8. Blanchard DK, Reynolds C, Grant CS, et al. Radiation-induced breast sarcoma. Am J Surg 2002;184 : 356−358.
9. Huang J, Mackillop WJ. Increased risk of soft tissue sarcoma after radiotherapy in women with breast carcinoma. Cancer 2001;92 : 172−180.
10. McGowan TS, Cummings BJ, O´Sullivan B, et al. An analysis of 78 breast sarcoma patients without distant metastases at presentation. Int J Radiat Oncol Biol Phys 2000;46 : 383−390.
11. Yamashina M. Primary Leiomyosarcoma in the Breast. Japanese Journal of Clinical Oncology 1987;17 : 71−77.
12. Markaki S, Sotiropoulou M, Hanioti C, Lazaris D. Leiomyosarcoma of the breast – A clinicopathologic and immunohistochemical study. European Journal of Obstetrics and Gynecology and Reproductive Biology 2003;2 : 233−236.
13. Shinto O, Yashiro M, Yamada N, Matsuoka T, Ohira M, et al. Primary Leiomyosarcoma of the Breast: Report of a Case. Surgery Today 2002;8 : 716−719.
14. Yap J, Chuba PJ, Thomas R, et al. Sarcoma as a second malignancy after treatment for breast cancer. International Journal of Radiation Oncology Biology Physics 2002;52 : 1231−1237.
15. Kirova YM, Vilcoq JR, Asselain B, Sastre-Garau X, Fourquet A. Radiation-induced sarcomas after radiotherapy for breast carcinoma: a large-scale single-institution review. Cancer 2005;68 : 356−363.
16. Kuten A, Sapir D, Cohen Y, Haim N, Borovik R, et al. Postirradiation soft tissue sarcoma occuring in breast cancer patients: report of seven cases and results of combination chemotherapy. Journal of Surgical Oncology 1985;28 : 168−171.
17. Olicina M, Merck B, Gimenez-Climent MJ, Almenar S, Sancho-Merle MF, et al. Radiation-Induced Leiomyosarcoma after Breast Cancer Treatment and TRAM Flap Reconstruction. Sarcoma 2008 : 3 pages.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2014 Číslo 7- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Stillova choroba: vzácné a závažné systémové onemocnění
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Bariatrie – enfant terrible chirurgie?
- Léčebná taktika ruptury výdutí břišní aorty
- Interdisciplinární evropská doporučení metabolické a bariatrické chirurgie
- Pankreatická píštěl a akutní pooperační pankreatitida po proximální pankreatoduodenektomii
- Rizika a komplikace operačních výkonů u urologických pacientů ve vyšším věku
- Etapovitý menežment otvorených zlomenín proximálnej tíbie s defektom mäkkých častí
- Sarkom hrudní stěny po ozáření pro karcinom prsu − kazuistika
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Sarkom hrudní stěny po ozáření pro karcinom prsu − kazuistika
- Léčebná taktika ruptury výdutí břišní aorty
- Rizika a komplikace operačních výkonů u urologických pacientů ve vyšším věku
- Pankreatická píštěl a akutní pooperační pankreatitida po proximální pankreatoduodenektomii
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



