-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Akutní endovaskulární řešení disekce hrudní aorty a následné ischemie dolních končetin
Urgent Endovascular Management of the Thoracic Aorta Dissection and Subsequent Lower Extremity Ischemia
Situation:
Insertion of tubular stentgrafts in the management of acute type B dissection of the thoracic aorta has recently become a popular alternative to open surgeries. The classical surgical procedure in complicated dissections is associated with mortality rates of up to 50% and prolonged intensive care hospitalization. However, endovascular procedures have been associated with significantly lower morbidity and mortality rates. There is insufficient experience with the stentgraft implantation outcome concerning both the septum dissection and the lumini.Case Review:
A tubular stentgraft has been implanted to a forty-nine-year-old patient with acute, type B dissection. Immediate ischemic and neurological complications, requiring reoperation and prolonged intensive care, were recorded postoperatively. The causes and the management are discussed.Conclusion:
Endovascular management of the type B dissection is a popular, more patient-saving and healthcare professionals-saving procedure, compared to classical open surgery. Pressure changes in the true and false aortic lumen may result in rapid reduction of the organ and limb perfusion flow. These complications should be expected and must be managed urgently. Such surgeries should be performed in clinical centres with appropriate facilities.Key words:
type B dissection – endovascular management – hybrid procedure
Autoři: P. Šedivý 1; P. Šebesta 1; T. Mach 2
Působiště autorů: Oddělení cévní chirurgie, primář doc. MUDr. P. Štádler, Ph. D., Nemocnice na Homolce, Praha 1; Radiodiagnostické oddělení, primář doc. MUDr. J. Vymazal, D. Sc., Nemocnice Na Homolce, Praha 2
Vyšlo v časopise: Rozhl. Chir., 2008, roč. 87, č. 4, s. 171-175.
Kategorie: Monotematický speciál - Původní práce
Souhrn
Situace:
Řešení akutní disekce typu B hrudní aorty implantací tubulárního stentgraftu se v posledních letech stalo atraktivní alternativou případné otevřené operace. Klasický operační výkon je u komplikovaných disekcí provázen až 50% mortalitou a protrahovaným pobytem pacienta na JIP. Při endovaskulárním výkonu je morbidita i mortalita výrazně nižší. Zatím není dostatek zkušeností, jak se septum disekce a obě lumina budou po zavedení stentgraftu chovat.Popis případu:
Implantovali jsme tubulární stentgraft čtyřicetidevítiletému pacientovi s akutní disekcí B. Po operaci došlo k bezprostředním ischemickým a neurologickým komplikacím, které si vyžádaly reoperaci a prodloužený pobyt na JIP. Jsou rozebrány příčiny a popsán způsob řešení.Závěr:
Endovaskulární řešení disekce B je atraktivní a pro pacienta i personál méně náročný operační výkon ve srovnání s klasickou otevřenou operací. Při změnách tlaků v pravém a nepravém luminu aorty může dojít k náhlým změnám perfuze orgánů nebo končetin. Tyto komplikace je nutno očekávat a neodkladně řešit. Operace tohoto typu je vhodné provádět v klinických centrech s patřičným zázemím.Klíčová slova:
disekce B – endovaskulární řešení – hybridní výkonÚVOD
Řešení akutní disekce hrudní aorty typu B pomocí implantace stentgraftu je postup, který v posledních letech nabývá na vážnosti [5, 6, 8, 13]. Dosud byla doporučovaným postupem při nekomplikovaném průběhu konzervativní léčba. Ta spočívala v razantním snížení krevního tlaku betablokátory a sledování vývoje poruch prokrvení orgánů nebo končetin nebo případného vzniku jiných komplikací. Teprve při nezvládnutelné hypertenzi, po vzniku kryté nebo otevřené ruptury či viscerální, renální nebo končetinové ischemie, se stav považoval za indikovaný k operačnímu výkonu [1, 14].
Operační výkon je u komplikovaných disekcí provázen až 50% mortalitou a protrahovaným pobytem pacienta na JIP [4, 15]. Nezřídka je komplikován paraplegií zapříčiněnou hypoperfuzí míchy [11]. Při konzervativním postupu je procento časných komplikací poměrně malé a až 50 % pacientů se dožívá 10 let od příhody. V poslední době ale dlouhodobé sledování pacientů ukazuje na téměř pravidelný vznik pozdních komplikací chronické disekce [2, 3, 16, 17]. Dominují mezi nimi zejména dilatace a pozdní ruptury falešného lumen, pleurální výpotky, pozdní neurologické komplikace a orgánové ischemie vzniklé vývojem disekce.
Chování septa a obou lumin disekce po implantaci stentgraftu není dosud podrobněji popsáno. Publikované výsledky ze světových pracovišť umožňují hodnotit slibné střednědobé výsledky endovaskulární léčby [7, 18, 19, 20].
Na našem pracovišti se endovaskulárními přístupy při léčbě chirurgických onemocnění hrudní i abdominální aorty zabýváme od roku 1994. Od roku 2001 jsme zavedli 115 hrudních stentgraftů pro aortální postižení různé etiologie. Disekci B jsme tímto způsobem ošetřili u 31 postižených. Tři pacienti (9,7 %) s celkovým nejvyšším operačním rizikem během pooperačního průběhu zemřeli.
POPIS PŘÍPADU
Dovolujeme si popsat ne zcela obvyklý případ pacienta s akutní disekcí hrudní aorty typu B a se současným proměnlivým obrazem ischemie dolních končetin.
Čtyřicetidevítiletý muž, kuřák, bez anamnézy sledovaných chorob a bez významnější chronické medikace, pocítil z plného zdraví nejprve mírnou bolest v okolí levé mammily. Hodinu poté se již velmi intenzivní bolesti šířily do zad podél páteře ve výši lopatek. Vědomí alterováno nebylo, bolest se mírně měnila s nádechem. Převezen vozem RZP na kardiologickou kliniku FN KV, kde naměřena hypertenze 190/120 a echograficky a CT diagnostikována disekce hrudní aorty B. Následně byl přeložen na JIP Oddělení cévní chirurgie Nemocnice Na Homolce.
Ze snímků CT AG bylo zřejmé, že se disekce šíří od levé a. subclavia v celém rozsahu hrudní, viscerální a abdominální aortou. Vlevo falešné lumen končilo na odstupu a. iliaca comm. a dále se plnilo jen lumen pravé, vpravo naopak pravé lumen končilo u ústí a. iliaca comm. a distální perfuzi zajišťovalo již jen široké falešné lumen. Viscerální tepny odstupovaly všechny z pravého lumen vyjma pravé a. renalis. Pravé lumen bylo ve viscerálním a subrenálním úseku výrazně utlačeno (Obr. 1 a 2).
Obr. 1. Falešné ústí začíná těsně pod levou a. subclavia Fig. 1. A false orifice starting under the left subclavian artery 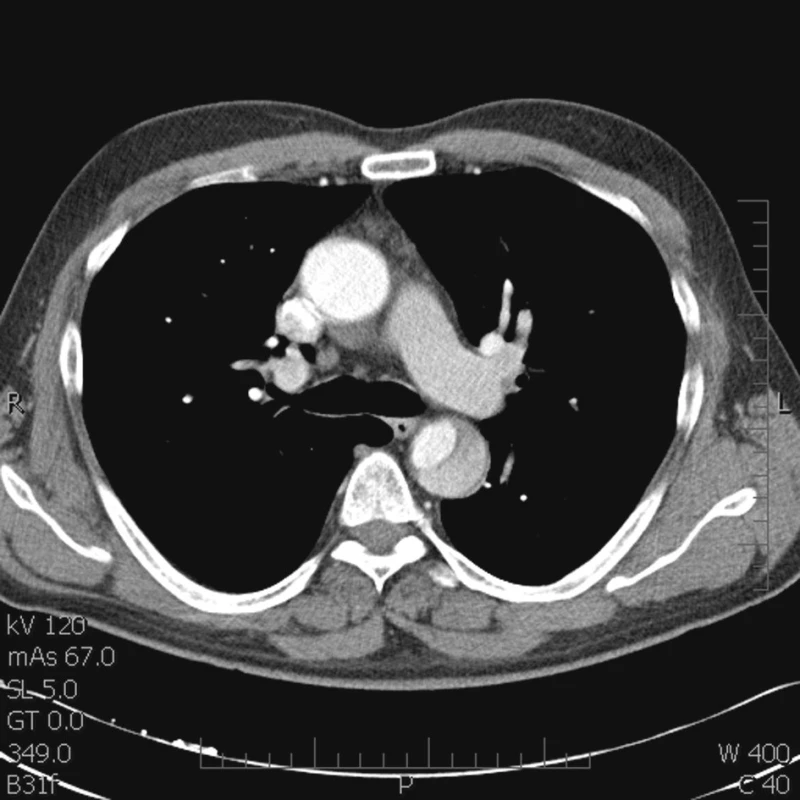
Obr. 2. Odstup a. mesenterica sup. z pravého lumen Fig. 2. The a. mesenterica sup., branching off the true lumen 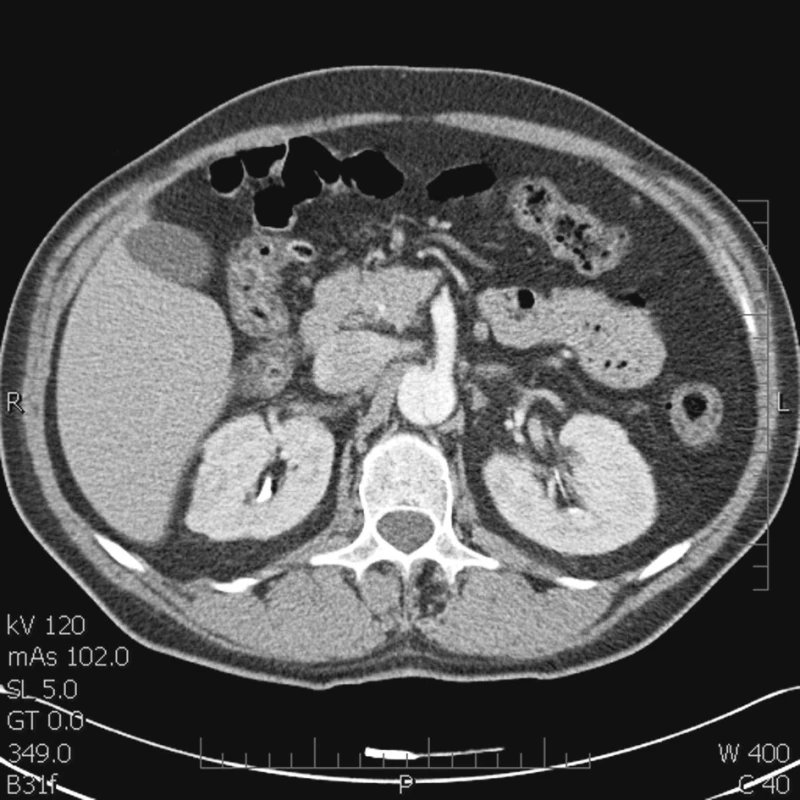
Na našem pracovišti jsme při fyzikálním vyšetření zjistili oslabenou pulzaci na a. femoralis l. dx., končetina však byla bez projevů závažnější ischemie a obě periferní tepny byly hmatné. Neurologický stav pacienta nebyl také nijak alterován. Trvala ovšem úporná hypertenze a typické bolesti v zádech i přes maximální medikamentózní terapii (urapidil (Ebrantil) + nitroprussid + metoprolol (Betaloc) + sufentanil (Sufenta)). Diuréza byla 50 ml/hod. Krevní obraz mimo leukocytózu 16,2 x 109/l byl normální. Pro přetrvávající bolesti a hypertenzi jsme se rozhodli k endovaskulárnímu řešení.
Primární operace
Ve spolupráci s radiologem jsme cestou levé a. femoralis implantovali tubulární stentgraft Endofit (LeMaitre Vascular Inc., Burlington, USA), složený ze dvou segmentů od levé a. subclavia (AS) do vzdálenosti 4 cm nad tr. coelicaus. Ústí levé a. subclavia jsme záměrně překryli s cílem získat lepší kotvicí zónu (Obr. 3). V rozsahu stentgraftu došlo k promptní expanzi pravého lumen a falešné lumen se plnit přestalo. Ve viscerálním a abdominálním úseku obě lumina přetrvala bez zjevných změn, pulzace v tříslech se nezměnila.
Obr. 3. Stentgraft hrdlem překrývá levou a. subclavii a končí nad viscerálním segmentem Fig. 3. A stentgraft covering the left subclavian artery and ending cranial to the visceral segment 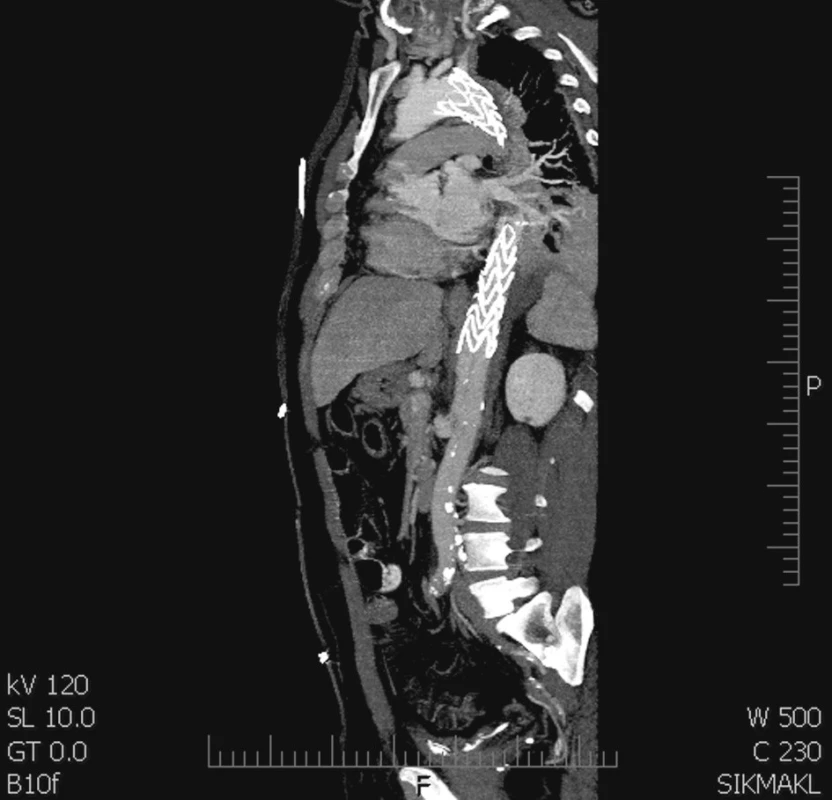
Reoperace pro ischemickou komplikaci
Bezprostředně po výkonu byla hybnost dolních končetin dobrá a neurolog hodnotil pooperační nález jako normální. Během dvou hodin došlo k rozvoji těžké ischemie levé dolní končetiny se ztrátou pulzace v třísle. Provedli jsme novou CT angiografii a zjistili změnu krevního průtoku v pánevních tepnách. Došlo ke kompresi pravého lumen v abdominální aortě.
Pacient byl znovu převezen na operační sál. Po rozpuštění operační rány nalezena netepající levá a. femoralis, bez přítomnosti trombózy. Sondáží vodičem proniknuto do pravého lumen a posléze až do hrudního stentgraftu. Rozhodli jsme se situaci řešit hybridním výkonem, implantovali aortouniiliacký stentgraft Gore Excluder (W.L.Gore & Associates, Inc., Flagstaff, USA), vlevo, subrenální s nekrytým suprarenálním kotvením, distálně zakončený bezpečně v pravém lumen nad větvením společné iliky.
V pravé společné femorální tepně jsme nalezli a prošitím ošetřili ukončení disekce. Perfuzi pravé dolní končetiny jsme zajistili provedením extraanatomického femoro-femorálního zkříženého bypassu armovanou PTFE protézou (Vascutek Terumo, Inchinnan, VB) (Obr. 4). Zevní pánevní tepnu vpravo jsme nad tříselným vazem a nad odstupem a. circumflexa ilium podvázali, abychom zabránili zpětnému plnění falešného lumen v subrenální aortě. Krevní ztráta byla 800 ml a pacient neměl ani při jedné operaci hypotenzi, mimo několikavteřinové snížení TK během kotvení proximálního hrdla hrudního stentgraftu.
Obr. 4. Aortouniiliacký stentgraft s nekrytým suprerenálním hrdlem a femorofemorální zkřížený bypass Fig. 4. An aortouniiliac stentgraft with an open suprarenal column and a femoro-femoral cross-over bypasss 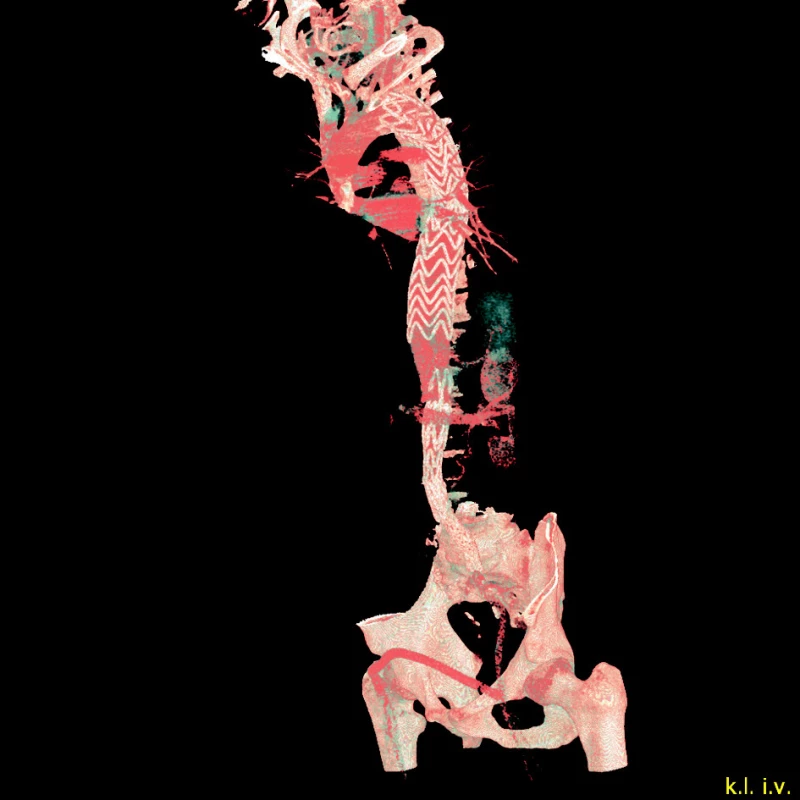
Po výkonu byly oboustranně dobře hmatné pulzace na obou periferních tepnách dolních končetin a obě končetiny byly normálně hybné. Překrytí levé AS přes vymizení periferních pulzací (na kontrolním CT AG dokumentováno plnění levé AS stealem přes levou a. vertebralis) nevedlo k žádným ischemickým projevům.
Neurologická komplikace
S prodlevou 24 hodin po této dvojité operaci došlo k rozvoji paraplegie. V kontinuální infuzi byl podán solumedrol ve vysoké dávce, (400 mg/hod., 0,08 mg/kg/min.) v úrovni Th 11 byla provedena drenáž mozkomíšního prostoru a pacient plně heparinizován. NMR angiografie vyloučila krvácení do páteřního kanálu, kompresi míchy i závažnější míšní ischemii.
Během dalších 24 hodin se upravila hybnost PDK k normě, plegie LDK přetrvala, ale čití levé dolní končetiny bylo prakticky normální. Hypertenze se postupně stabilizovala během prvého pooperačního týdne. Po extrakci močového katétru byl pacient kontinentní. Během 3 pooperačních týdnů plegie LDK přešla v parézu II. stupně. Nemocného jsme přeložili na rehabilitační kliniku.
Na ambulantní kontrolu po 3 měsících přišel pacient sám, s oporou jedné hole. Hybnost LDK se obnovila téměř k normálu, přetrvává jen určitá slabost a neobratnost. Pulzace na PHK a obou DK jsou na všech periferních tepnách dobře hmatné, LHK není subjektivně ischemická.
DISKUSE
Podle dlouhodobého sledování výsledků konzervativního a operačního postupu u pacientů s nekomplikovanou disekcí B přináší v poslední době lepší výsledky aktivní operační přístup. Časná nemocniční mortalita během konzervativní léčby je i přes agresivní antihypertenzní terapii vysoká. Stav disekované tepny si mnohdy během několika let vynutí operační řešení kvůli expanzi nebo perforaci falešného lumen, rozvoji orgánové ischemie, recidivujícím bolestem, nebo špatně léčitelné hypertenzi [2, 3, 4, 5, 6, 7, 8, 13].
Implantace SG do disekce B hrudní aorty je efektivní a technicky dobře proveditelný výkon s menší zátěží pro pacienta i personál ve srovnání s klasickou operací. Je spojen s výrazně nižší morbiditou a mortalitou a s menším rizikem vzniku neurologických komplikací. Krevní ztráty jsou při endovaskulárním postupu výrazně nižší [5, 6, 7, 8].
Implantaci stentgraftu do obou etáží disekované aorty (tedy do hrudní descendentní a současně do infrarenální aorty) v jedné době brání oprávněné obavy z rozvoje ischemického postižení míchy [9, 10, 11, 12]. I při překrytí pouze hrudního úseku disekce je vhodné ponechat nekrytý alespoň jeden pár z těch supraviscerálních interkostálních tepen, které odstupují zhruba v úseku 10 cm proximálně od tr. coeliacus. Někdy mohou překrytí těchto tepen kompenzovat přítomné intersegmentální kolaterály [10]. Významný kolaterální přítok interkostálních tepen poskytuje průchodná a. thoracica interna. Pokud nejsou kaudální interkostální tepny angiograficky prokazatelné, pak je pravděpodobně možné překrýt celou descendentní aortu až těsně k odstupu tr. coeliacus. Obdobně ve viscerálním úseku, nejsou-li lumbální tepny viditelné, je zřejmě možno s přijatelnou hladinou rizika implantovat bifurkační SG, pokud se zachová průchodnost vnitřních pánevních tepen. Možný vznik ischemických orgánových nebo končetinových komplikací vyžaduje bedlivou pooperační monitoraci [21].
Naše zkušenost dokládá literaturní údaje, že bezprostřední neurologická komplikace z míšní hypoperfuze může být reverzibilní po podávání kortikoidů, drenáži cerebrospinálního moku a elevaci systémového krevního tlaku [11, 12]. Přesto je výskyt neurologických komplikací řádově nižší, než po otevřeném operačním řešení.
Nejslibnějším postupem je řešit disekci B endovaskulárně časně po jejím vzniku, jak dokládají výsledky naše i z jiných pracovišť [7, 8, 13, 14, 20]. Septum není v té době hypertrofované a je velmi mobilní, falešné lumen se ochotně komprimuje a při následných kontrolách stěna aorty těsně konturuje obvod stentgraftu.
Zhodnocení dlouhodobých změn aortální stěny a porovnání dlouhodobých výsledků všech léčebných modalit si žádá sledování větších počtů pacientů v delších časových intervalech, nejlépe v rámci randomizovaných studií [19].
ZÁVĚR
Endovaskulární řešení disekce B je atraktivní a pro pacienta i zdravotníky méně náročný operační výkon ve srovnání s klasickou otevřenou operací. Při změnách tlaků v pravém a nepravém luminu aorty může dojít k fatálním změnám perfuze orgánů nebo končetin. Pooperační monitorování na JIP umožňuje tyto komplikace bezprostředně zjistit a neodkladně řešit.
MUDr. P. Šedivý
Oddělení cévní chirurgie Nemocnice na Homolce
Roentgenova 2
150 00 Praha 5
e-mail: petr.sedivy@homolka.cz
Zdroje
1. DeBakey, M. E., McCollum, C. H., Crawford, E. S., Morris, G. C. Jr., Howell, J., Noon, G. .P, Lawrie, G. Dissection and dissecting aneurysms of the aorta: twenty-year follow-up of five hundred twenty-seven patients treated surgically. Surgery, 1982, Dec; 92(6): 1118–1134.
2. Greenberg, R., Khwaja, J., Haulon, S., Fulton, G. Aortic dissections: new perspectives and treatment paradigms. Eur. J. Vasc. Endovasc. Surg., 2003, Dec; 26(6): 579–586.
3. UmaĖa, J. P., Lai, D. T., Mitchell, R. S., Moore, K. A., Rodriguez, F., Robbins, R. C., Oyer, P. E., Dake, M. D., Shumway, N. E., Reitz, B. A., Miller, D. C. Is medical therapy still the optimal treatment strategy for patients with acute type B aortic dissections? J. Thorac. Cardiovasc. Surg., 2002, Nov; 124(5): 896–910.
4. Gysi, J., Schaffner, T., Mohacsi, P., Aeschbacher, B., Althaus, U., Carrel, T. Early and late outcome of operated and non-operated acute dissection of the descending aorta. Eur. J. Cardiothorac. Surg., 1997, Jun; 11(6): 1163–1169.
5. Stone, D. H., Brewster, D. C., Kwolek, C. J., LaMuraglia, G. M., Conrad, M. F., Chung, T. K., Cambria, R. P. Stent-graft versus open-surgical repair of the thoracic aorta: mid-term results. J. Vasc. Surg., 2006, Dec; 44(6): 1188–1197.
6. Amabile, P., Collart, F., Gariboldi, V., Rollet, G., Bartoli, J. M., Piquet, P. Surgical versus endovascular treatment of traumatic thoracic aortic rupture. J. Vasc. Surg., 2004, Nov; 40(5): 873–879.
7. Eggebrecht, H., Nienaber, C. A., Neuhäuser, M., Baumgart, D., Kische, S., Schmermund, A., Herold, U., Rehders, T. C., Jakob, H. G., Erbel, R. Endovascular stent-graft placement in aortic dissection: a meta-analysis. Eur. Heart. J., 2006, Feb; 27(4): 489–498.
8. Kahn, S. L., Dake, M. D. Stent graft management of stable, uncomplicated type B aortic dissection. Perspect. Vasc. Surg. Endovasc. Ther., 2007, Jun; 19(2): 162–169.
9. Gravereaux, E. C., Faries, P. L., Burks, J. A., Latessa, V., Spielvogel, D., Hollier, L. H., Marin, M. L. Risk of spinal cord ischemia after endograft repair of thoracic aortic aneurysms. J. Vasc. Surg., 2001, Dec; 34(6): 997–1003.
10. Schurink, G. W., Nijenhuis, R. J., Backes, W. H., Mess, W., de Haan, M. W., Mochtar, B., Jacobs, M. J. Assessment of spinal cord circulation and function in endovascular treatment of thoracic aortic aneurysms. Ann. Thorac. Surg., 2007, Feb; 83(2): S877–881.
11. Griepp, R. B., Ergin, M. A., Galla, J. D., Klein, J. J., Spielvogel, D., Griepp, E. B. Minimizing spinal cord injury during repair of descending thoracic and thoracoabdominal aneurysms: the Mount Sinai approach. Semin. Thorac. Cardiovasc. Surg., 1998, Jan; 10(1): 25–28.
12. Khoynezhad, A., Donayre, C. E., Bui, H., Kopchok, G. E., Walot, I., White, R. A. Risk factors of neurologic deficit after thoracic aortic endografting. Ann. Thorac. Surg., 2007, Feb; 83(2): S882–889; discussion S890–892.
13. Schoder, M., Czerny, M., Cejna, M., Rand, T., Stadler, A., Sodeck, G. H., Gottardi, R., Loewe, C., Lamme, J. Endovascular repair of acute type B aortic dissection: long-term follow-up of true and false lumen diameter changes. Ann. Thorac. Surg., 2007, Mar; 83(3): 1059–1066.
14. Jex, R. K., Schaff, H. V., Piehler, J. M., King, R. M., Orszulak, T. A., Danielson, G. K., Pairolero, P. C., Pluth, J. R., Ilstrup, D. Early and late results following repair of dissections of the descending thoracic aorta. J. Vasc. Surg., 1986, Feb; 3(2): 226–237.
15. Cambria, R. P. Surgical treatment of complicated distal aortic dissection. Semin. Vasc. Surg., 2002, Jun; 15(2): 97–107.
16. Sueyoshi, E., Sakamoto, I., Hayashi, K., Yamaguchi, T., Ikara, T. Growth rate of aortic diameter in patients with type B aortic dissection during the chronic phase. Circulation, 2004, Sep 14; 110(11 Suppl 1): II256–261.
17. UmaĖa, J. P., Lai, D. T., Mitchell, R. S., Moore, K. A., Rodriguez, F., Robbins, R. C., Oyer, P. E., Dake, M. D., Shumway, N. E., Reitz, B. A., Miller, D. C. Is medical therapy still the optimal treatment strategy for patients with acute type B aortic dissections? J. Thorac. Cardiovasc. Surg., 2002, Nov; 124(5): 896–910.
18. Attia, C., Villard, J., Boussel, L., Farhat, F., Robin, J., Revel, D., Douek, P. Endovascular repair of localized pathological lesions of the descending thoracic aorta: midterm results. Cardiovasc. Intervent. Radiol., 2007, Jul-Aug; 30(4): 628–637.
19. Bergeron, P., Inglese, L., Gay, J. Setting up of a multicentric European registry dealing with type B dissections in chronic and acute phases with thoracic EndoFit(R) devices. J. Cardiovasc. Surg. (Torino), 2007, Dec; 48(6): 689–695.
20. Stone, D. H., Brewster, D. C., Kwolek, C. J., Lamuraglia, G. M., Conrad, M. F., Chung, T. K., Cambria, R. P. Stent-graft versus open-surgical repair of the thoracic aorta: mid-term results. J. Vasc. Surg., 2006, Dec; 44(6): 1188–1197.
21. Lauterbach, S. R., Cambria, R. P., Brewster, D. C., Gertler, J. P., Lamuraglia, G. M., Isselbacher, E. M., Hilgenberg, A. D., Moncure, A. C. Contemporary management of aortic branch compromise resulting from acute aortic dissection. J. Vasc. Surg., 2001, Jun; 33(6): 1185–1192.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2008 Číslo 4- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Stillova choroba: vzácné a závažné systémové onemocnění
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Akutní endovaskulární řešení disekce hrudní aorty a následné ischemie dolních končetin
- Výskyt a řešení prolongovaného úniku vzduchu po plicní lobektomii
- Biopsie sentinelové uzliny u karcinomu prsu v klinické praxi
- Hluboká žíla dolní končetiny jako tepenná náhrada při řešení infekce cévní protézy
- Skúsenosti s plastikou ventrálnych hernií podľa Chevrela s „on lay“ prolénovou sieťkou
- Naše zkušenosti s resekčními výkony na pankreatu. Retrospektivní analýza
- Chronická pankreatitída, indikácie k resekčným výkonom a pooperačné komplikácie
- Kvalita života pacientov po resekčných výkonoch pre chronickú pankreatitídu
- Epidemiologie a ekonomie zlomenin proximálního femuru, proximálního humeru, distálního radia a luxačních zlomenin hlezna
- Prof. MUDr. Václav Vojtěch Tošovský, DrSc., zemřel ve věku 95 let
- Životní jubileum prof. MUDr. Vl. Krále, CSc. (29. 3. – 70 let)
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Kvalita života pacientov po resekčných výkonoch pre chronickú pankreatitídu
- Skúsenosti s plastikou ventrálnych hernií podľa Chevrela s „on lay“ prolénovou sieťkou
- Chronická pankreatitída, indikácie k resekčným výkonom a pooperačné komplikácie
- Naše zkušenosti s resekčními výkony na pankreatu. Retrospektivní analýza
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



