-
Články
- Vzdělávání
- Časopisy
Top články
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Volná místa
Doporučené pozice
Reklama- Praxe
Výsledky liečby gestačnej trofoblastovej neoplázie v Slovenskej republike v rokoch 1993–2017
Results of treatment of gestational trophoblastic neoplasia in the Slovak Republic in the years 1993–2017
Objective: Gestational trophoblastic neoplasia epidemiology and treatment results in the Slovak Republic in the years 1993–2017. Methods: Retrospective analysis results of gestational trophoblastic neoplasia treatment in the Centre for gestational trophoblastic disease in the Slovak Republic in Bratislava in the years 1993–2017 according to prognostic scoring and staging system FIGO/WHO (International Federation of Gynecology and Obstetrics/World Health Organization). Results: The Centre for Gestational Trophoblastic Disease was created in the Slovak Republic in the year 1993, after the split of former Czechoslovakia. A total of 100 patients with gestational trophoblastic neoplasia were treated in this Centre in the years 1993–2017. According to prognostic scoring and staging system FIGO/ WHO, 74% patients were at a low risk and 26% of patients were at a high-risk of gestational trophoblastic neoplasia. There were 56, 2, 32 and 10% patients in stages I, II, III, and IV, respectively. The total curability and mortality rates were 96 and 4%, respectively. The curability rate 100% was achieved in stages I–III and in all placental site trophoblastic tumours, and the curability rate 60% was achieved in stage IV. In the years 1993 –2017, the incidences were 1 in 59,315 pregnancies and 1 in 42,299 deliveries for choriocarcinoma, 1 in 489,348 pregnancies and 1 in 348,965 deliveries for placental site trophoblastic tumours, 1 in 139,814 pregnancies and 1 in 99,704 deliveries for invasive mole, and 1 in 39,947 pregnancies and 1 in 28,487 deliveries for persistent gestational trophoblastic neoplasia. In the Czech Republic in the same period of time, there were treated 281 (301) patients with the curability rate 98.6% (98.7%). Conclusion: The results of the treatment of gestational trophoblastic neoplasia in the Slovak Republic are comparable with those achieved by leading centers specialized for the treatment of this disease in Europe and in the world. Early detection and centralisation of the treatment are crucial points for successful treatment, as the high curability rate of gestational trophoblastic neoplasia is achieved by effective therapy.
Keywords:
gestational trophoblastic neoplasia – choriocarcinoma – placental site trophoblastic tumour – epithelioid trophoblastic tumour – invasive mole – curability – mortality – reproductive outcomes
Autoři: Korbeľ M. 1,2; Iarsky Šufl J. 1,3; Danihel Ľ. 1,4; Nižňanská Z. 1,2
Působiště autorů: Centrum pre gestačnú trofoblastovú chorobu Slovenskej republiky, Bratislava, Slovenská republika 1; I. gynekologicko-pôrodnícka klinika LF UK a UN Bratislava, Slovenská republika 2; Oddelenie klinickej onkológie A, II. onkologická klinika LF UK a NOÚ Bratislava, Slovenská republika 3; Ústav patologickej anatómie, LF UK a UN Bratislava, Slovenská republika 4
Vyšlo v časopise: Ceska Gynekol 2021; 86(2): 94-101
Kategorie: Původní práce
doi: https://doi.org/10.48095/cccg202194Souhrn
Cieľ štúdie: Analýza výsledkov liečby a epidemiologických aspektov gestačnej trofoblastovej neoplázie v Slovenskej republike v rokoch 1993–2017. Metodika: Retrospektívna analýza výsledkov liečby gestačnej trofoblastovej neoplázie podľa prognostického skórovacieho systému a stagingu FIGO/WHO (International Federation of Gynecology and Obstetrics/World Health Organization) v Centre pre gestačnú trofoblastovú chorobu Slovenskej republiky v Bratislave v rokoch 1993–2017. Výsledky: Centrum pre gestačnú trofoblastovú chorobu v Slovenskej republike bolo vybudované v roku 1993, kedy došlo k rozdeleniu Československej republiky. Celkovo bolo v centre v rokoch 1993–2017 liečených 100 pacientok s gestačnou trofoblastovou neopláziou. Podľa prognostického skórovacieho systému a stagingu FIGO/ WHO bolo 74 % pacientok v štádiu nízkeho rizika a 26 % vysokého rizika. V I. štádiu bolo 56 %, v II. štádiu 2 %, v III. štádiu 32 % a v IV. štádiu 10 % pacientok. Celková kurabilita bola 96 % a mortalita 4 %. Kurabilita 100 % bola v I.–III. štádiu a všetkých trofoblastových tumorov placentového lôžka a 60 % v IV. štádiu. V Slovenskej republike v rokoch 1993–2017 bola incidencia choriokarcinómu 1 : 59 315 tehotností a 1 : 42 299 pôrodov, trofoblastového tumoru placentového lôžka 1 : 489 348 tehotností a 1 : 348 965 pôrodov, invazívnej moly 1 : 139 814 tehotností a 1 : 99 704 pôrodov, perzistujúcej gestačnej trofoblastovej neoplázie 1 : 39 947 tehotností a 1 : 28 487 pôrodov. V Českej republike bolo v rokoch 1993–2017 liečených 281 (301) pacientok s gestačnou trofoblastovou neopláziou a kurabilita bola 98,6 % (98,7 %). Záver: Výsledky liečby gestačnej trofoblastovej neoplázie v Slovenskej republike sú porovnateľné s výsledkami ktoré dosahujú popredné pracoviská špecializujúce sa na liečbu tohto ochorenia v Európe a vo svete. Nevyhnutnou podmienkou úspešnej liečby je včasná diagnostika a centralizácia liečby, pretože účinnou terapiou sa dosahuje vysoká kurabilita gestačnej trofoblastovej neoplázie.
Klíčová slova:
gestačná trofoblastová neoplázia – choriokarcinóm – trofoblastový tumor placentového lôžka – epiteloidný trofoblastový tumor –invazívna mola – kurabilita – mortalita – reprodukčné výsledky
Úvod
Gestačná trofoblastová neoplázia (tj. malígne formy gestačnej trofoblastovej choroby kam patrí choriokarcinóm, trofoblastový tumor placentového lôžka, epitelový trofoblastový tumor a invazívna mola), bola do roku 1955 ochorením s mortalitou takmer 100 % a jediná modalita liečby bola chirurgická. Za 6 desaťročí sa z tohto smrtiaceho ochorenia stala najlepšie liečiteľná neoplázia, ktorej kurabilita sa v súčasnosti blíži k 99–100 % a po liečbe je možná aj úspešná gravidita [1–7].
História liečby gestačnej trofoblastovej neoplázie (GTN) v Československu siaha do roku 1955, kedy bolo na I. gynekologicko-pôrodníckej klinike 1. lekárskej fakulty Univerzity Karlovy (LF UK) v Prahe (gynekologická časť kliniky bola na Karlovom námestí) kreované Celostátní centrum pro léčbu a výzkum trofoblastické nemoci (CTN) Československej socialistickej republiky. V CTN boli liečené aj pacientky zo Slovenska. Časť pacientok s GTN bola liečená na gynekologicko-pôrodníckej klinike LF Palackého univerzity v Olomouci, pretože pracovisko malo v tom čase vlastné skúsenosti a dobré výsledky. V rokoch 1975–1988 bola vybudovaná sieť krajských odborníkov pre trofoblastovú chorobu po celom Československu, ktorú v rokoch 1988–1992 vymenila nová generácia krajských odborníkov. Výnosom Ministerstva zdravotníctva (MZ) v roku 1986 získalo CTN štatút celoštátneho referenčného pracoviska pre trofoblastovú chorobu a odvtedy sa liečba pacientok s GTN z Čiech, Moravy a Slovenska sústredila do pražského CTN [8–12]. Po rozdelení republiky v roku 1993 pokračovalo pražské Centrum pro trofoblastickou nemoc (CTN) v liečbe pacientok z Českej republiky (ČR). Doteraz ostatným výnosom MZ ČR z roku 1998 bol za CTN vymenovaný Ústav pro péči o matku a dítě (ÚPMD) v Praze-Podolí, kde sa liečila prevažná časť pacientok s GTN z ČR. V rokoch 1996–2012 boli na gynekologicko-pôrodníckej klinike 2. LF UK a FN v Motole ročne liečené približne 3–4 pacientky s GTN (v tom čase ako prednosta kliniky pôsobil prof. Rob). Od roku 2017 sa časť pacientok s GTN liečila aj na gynekologicko-pôrodníckej klinike 3. LF UK a FN Královské Vinohrady, kde sa stal prof. Rob prednostom. Prof. Rob v počiatkoch svojej kariéry pôsobil v CTN na Karlovom námestí a venoval sa klinickému manažmentu pacientok s GTN [3,13,14].
V Slovenskej republike (SR) bolo v roku 1993 vytvorené špecializované pracovisko na liečbu GTN – Centrum pre trofoblastovú chorobu SR (CTCH SR). CTCH SR bolo vytvorené v spolupráci 4 pracovísk: I. gynekologicko-pôrodnícka klinika Lekárskej fakulty Univerzity Komenského (LF UK) a Fakultnej nemocnice (FN), Ústav patologickej anatómie LF UK a FN, Ústav lekárskej biológie LF UK a Národný onkologický ústav v Bratislave. Uvedené pracoviská boli v roku 2011 oficiálne ustanovené ako špecializované pracovisko „Centrum pre gestačnú trofoblastovú chorobu MZ SR“ (CGTCH MZ SR) a v rokoch 2017 bolo MZ SR preklasifikované na „Pracovisko pre zriedkavé choroby v SR – Centrum pre gestačnú trofoblastovú chorobu“ (CGTCH SR) [4,13,15,].
Materiál a metodika
Z databázy CGTCH MZ SR boli retrospektívne analyzované výsledky liečby GTN v rokoch 1993–2017 podľa WHO a FIGO prognostického skórovacieho systému a stagingu z roku 2000 s modifikáciou v roku 2002 (tab. 1). Retrospektívne boli preklasifikované prípady GTN dovtedy liečené podľa prognostického skórovacieho systému Svetovej zdravotníckej organizácie (WHO) z roku 1983 [4,6,16–18]. Histologická klasifikácia GTN v SR bola robená podľa kritérií WHO [19,20].
Tab. 1. FIGO/WHO staging a prognostický skórovací systém [16]
Tab. 1. FIGO/WHO staging and prognostic scoring system [16].![FIGO/WHO staging a prognostický skórovací systém [16]<br>
Tab. 1. FIGO/WHO staging and prognostic scoring system [16].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/b69536d9ecdc406021d9f173415d2563.png)
Histologická klasifikácia GTN v ČR vychádzala zo Zavadilovej klasifikácie [11,12]. V príspevku je aj stručné zhrnutie niektorých dostupných výsledkov liečby GTN na základe publikovaných a nepublikovaných dát získaných od kompetentných pracovníkov z ÚPMD, z Motola a z Královských Vinohrad [19,21]. V Motole boli v rokoch 1996–2012 liečené 3–4 pacientky ročne tj. približne 52–68 pacientok (presné údaje žiaľ absentujú).
Výsledky
V CGTCH MZ SR bolo v období rokov 1993–2017 evidovaných 684 prípadov GTCH, z nich 247 bolo liečených (tab. 2). Z pacientok s GTN malo 14 invazívnu molu, 30 choriokarcinóm, 49 perzistujúcu gestačnú trofoblastovú neopláziu (PGTN) vyžadujúcu chemoterapiu a 4 trofoblastový tumor placentového lôžka (PSTT).
Tab. 2. Prehľad pacientok liečených v Centre pre gestačnú trofoblastovú chorobu Slovenskej republike v rokoch 1993–2017.
Tab. 2. Overview of patients treated at the Center for Gestational Trophoblastic Disease of the Slovak Republic in the years 1993–2017.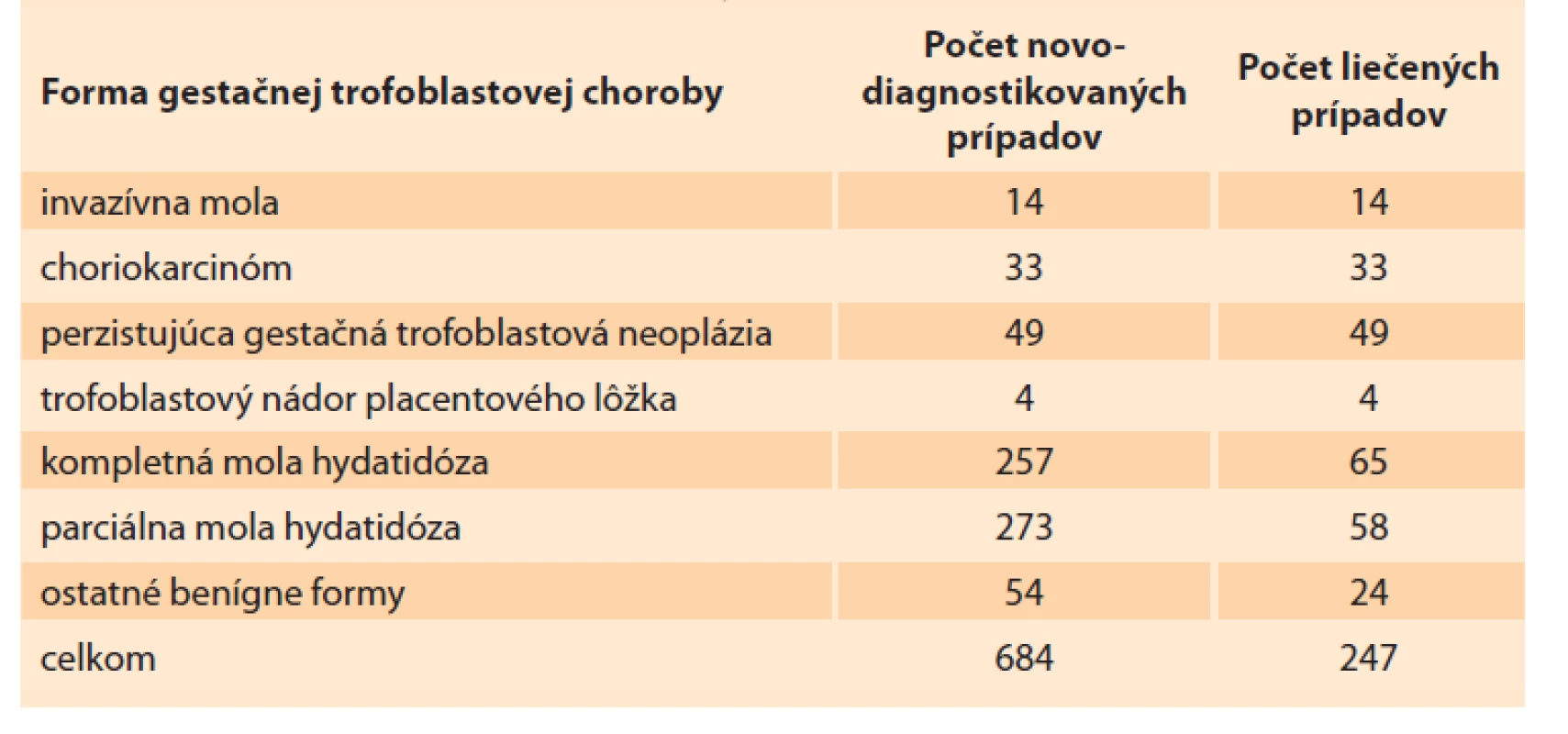
V sledovanom období bolo liečených 100 pacientok s GTN s celkovou kurabilitou 96 % (tab. 3). Jedna pacientka exitovala hneď po príchode do centra na masívne intrakraniálne krvácanie skôr ako bolo možné začať liečbu. Chemoterapiou bolo liečených 89 pacientok, z toho 3 pacientky (jedna FIGO III: nízkeho rizika a dve FIGO IV: vysokého rizika) s priaznivým poklesom hCG, ale nie do negativity, liečbu odmietli dokončiť. K 31. 12. 2020 všetky tri žili, pričom jedna z nich (Rómka) porodila zdravé dieťa v termíne. Záchrannou liečbou bola zvládnutá recidíva ochorenia u 3 zo 4 pacientok. Exitovali 4 pacientky (4 %) v IV. štádiu FIGO na masívne krvácanie z mozgových metastáz (pri dobrej odpovedi na kombinovanú chemoterapiu). U jednej postmenopauzálnej pacientky po evakuácii kompletnej moly ochorenie progredovalo zo I. štádia do IV. štádia a skočilo exitom, napriek kombinovanej intravenóznej, intrathekálnej a salvage chemoterapii, chirurgickej terapii a rádioterapii. Kurabilita 100 % bola v I.–III. štádiu a všetkých PSTT, ale v IV. štádiu bola iba 60 %. Od roku 2008 neumrela na GTN v SR žiadna pacientka.
Tab. 3. Výsledky liečby gestačnej trofoblastovej neoplázie v Slovenskej republike v rokoch 1993–2017.
Tab. 3. Results of treatment of gestational trophoblastic neoplasia in the Slovak Republic in the years 1993–2017.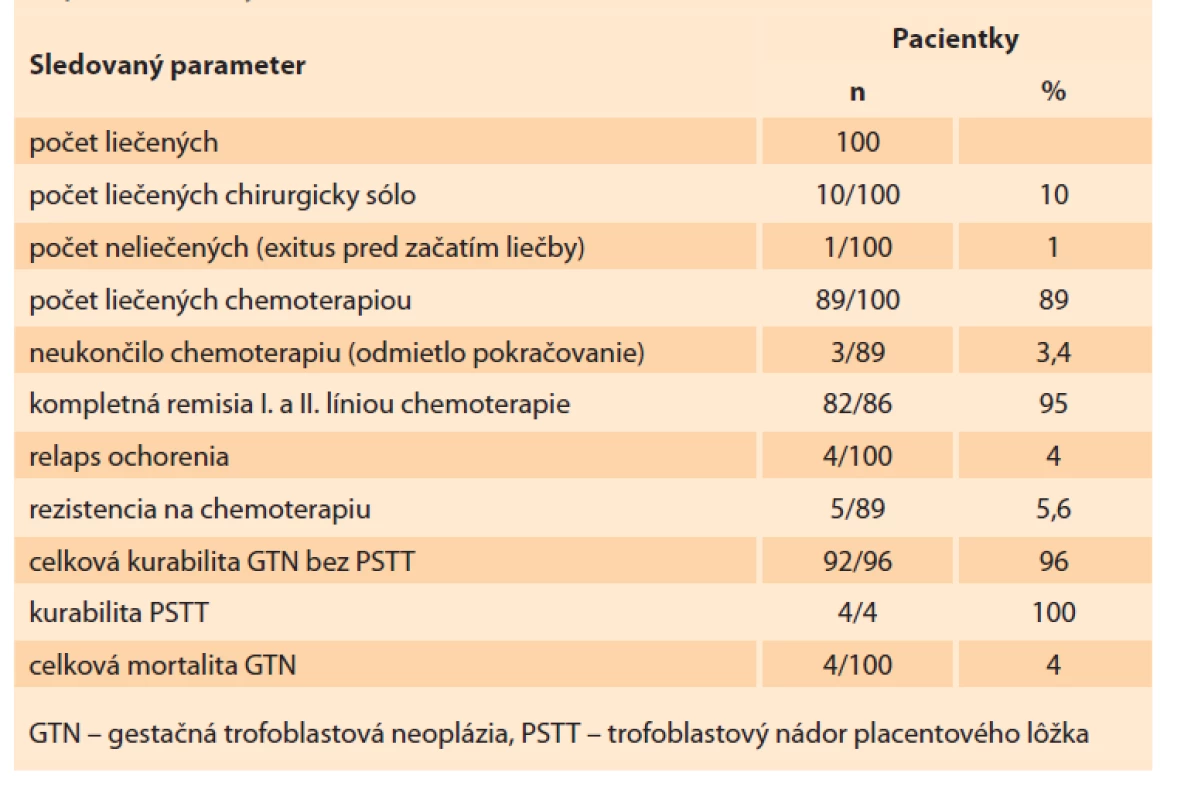
Zo 100 pacientok bolo chemoterapiou liečených celkom 89, z toho len sólo chemoterapiou 64 a kombináciou chemoterapie s chirurgickým výkonom 22 pacientok. Intratekálna chemoterapia bola aplikovaná 5 pacientkam a rádioterapia 5 pacientkam. Chirurgicky bolo liečených celkom 37 pacientok. Z gynekologických výkonov bola urobená abdominálna hysterektómia u 25 a salpingektómia u 2 pacientok. Resekcia pľúcnych metastáz bola robená u 5, mozgových metastáz u 2, krvácajúcich metastáz v pečeni a splenektómia bola robená u 2 pacientok a resekcia rekta u 1 pacientky. U 2 pacientok vznikla GTN po viacplodovej gravidite s koexistujúcou kompletnou molou a normálnym plodom (CHMCF – complete hydatidiform mole and coexisting normal fetus). Jedna z týchto gravidít skončila termínovým pôrodom zdravého dieťaťa a druhá potratom v II. trimestri gravidity. Incidencia CHMCF v SR bola 1 na 978 692 gravidít, čo je nepomerne nižšia ako vo svete udávaná – 1 prípad na 20 000–100 000 [22].
Z nežiaducich účinkov chemoterapie sa vyskytla slizničná toxicita a hepatotoxicita zhodne po 39 %, hematologická u 47 %, nefrotoxicita u 4 %, lokálna u 1 % a sekundárne malignity u 4 % pacientok (z nich 3 mali duktálny karcinóm in situ).
Podľa FIGO stagingu [1,6,16,17] v I. štádiu bolo 56 %, II. štádiu boli 3 %, v III. štádiu bolo 32 % a v IV. štádiu bolo 11 % pacientok (tab. 4).
Tab. 4. FIGO staging pacientok liečených pre gestačnú trofoblastovú neopláziu v Slovenskej republike v rokoch 1993–2017.
Tab. 4. FIGO staging of patients treated for gestational trophoblastic neoplasia in the Slovak Republic in 1993–2017.
Podľa prognostického skórovacieho systému WHO/ FIGO, 2 000 bolo v nízkom stupni rizika 74 % pacientok s GTN a vo vysokom stupni rizika 26 % (pre PSTT FIGO prognostický skórovací systém neplatí). Podľa prognostického skórovacieho systému WHO z roku 1983 [18] by bolo 69 % pacientok s GTN zaradených do nízkeho stupňa rizika, 16 % do stredného a 16 % do vysokého stupňa rizika (tab. 5).
Tab. 5. Distribúcia gestačnej trofoblastovej neoplázie v Slovenskej republike v rokoch 1993–2017 podľa FIGO/WHO prognostického skórovacieho systému.
Tab. 5. Distribution of gestational trophoblastic neoplasia in the Slovak Republic in 1993–2017 according to the FIGO/WHO prognostic scoring system.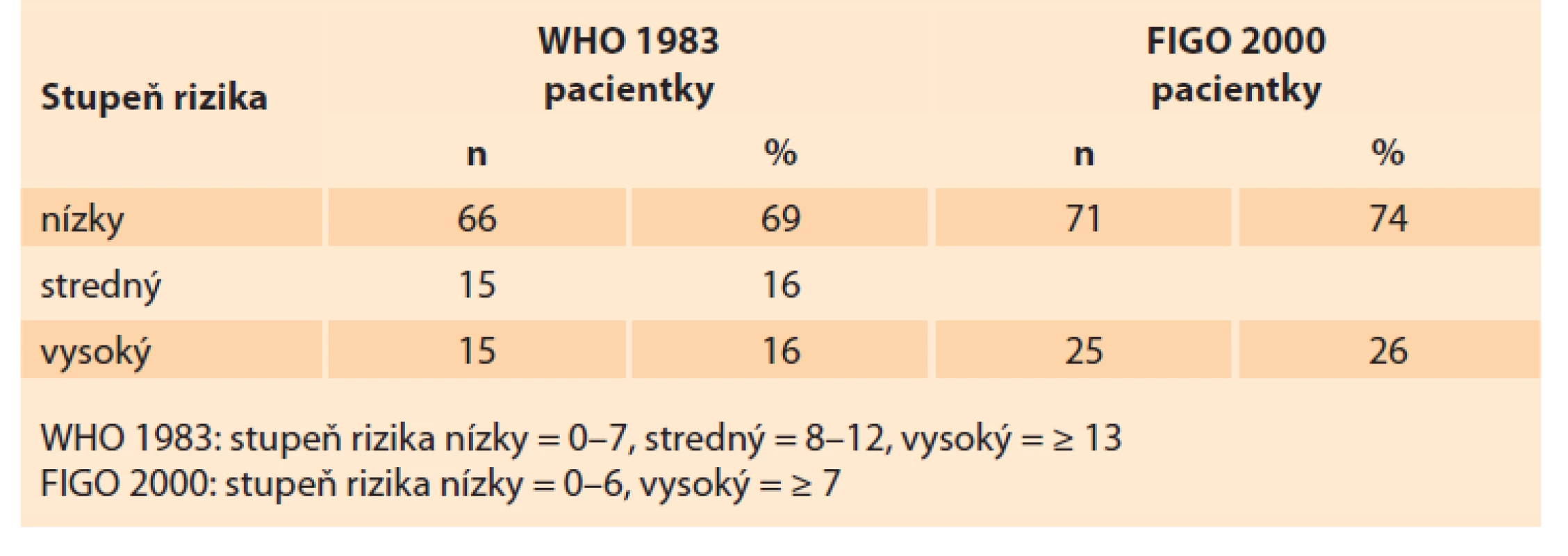
GTN sa vyskytla u 13 % pacientok pod 20 rokov, medzi 20. a 29. rokom u 40 % pacientok, medzi 30. a 39. rokom u 31 % pacientok a u 16 % starších ako 40 rokov. Priemerná incidencia GTN na 100 000 živonarodených detí bola 7, nižšia bola vo vekových kategóriách 20–34 rokov, vyššia vo veku pod 20 a vo veku 35 a viac rokov (tab. 6).
Tab. 6. Incidencia gestačnej trofoblastovej neoplázie podľa veku v Slovenskej republike v rokoch 1993–2017.
Tab. 6. Incidence of gestational trophoblastic neoplasia by age in the Slovak Republic in 1993–2017.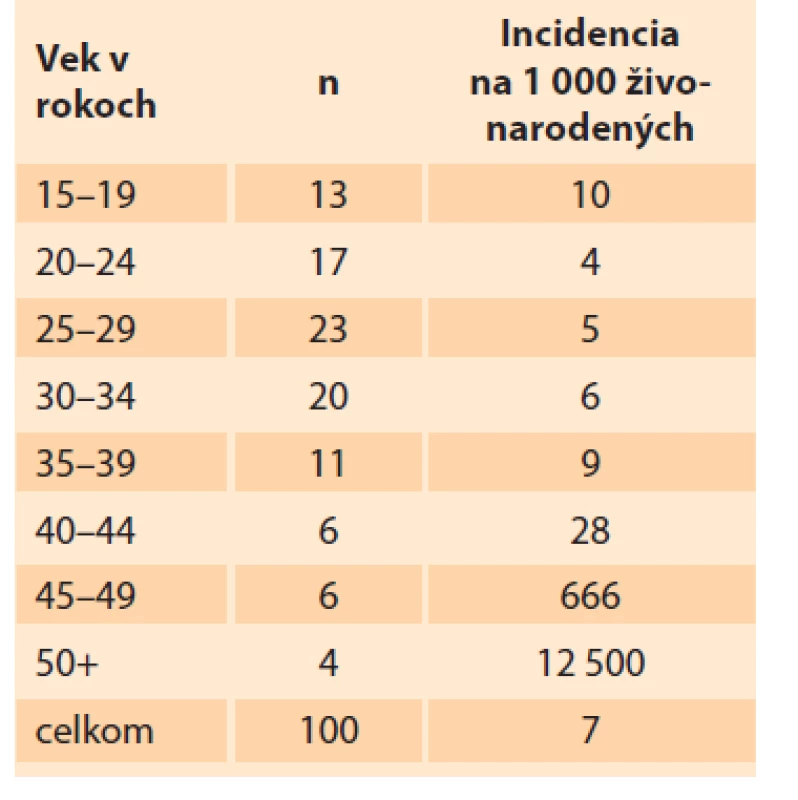
Celková incidencia GTN v SR v rokoch 1993–2017 na 1 000 tehotností bola 0,051 a na 1 000 pôrodov 0,072 (tab. 7). Najvyššiu incidenciu vykazovala PGTN – išlo o pacientky v reprodukčnom veku, kde bola snaha o zachovanie fertility. Najnižšia incidencia bola pri PSTT, podobne ako je to aj vo svete. V sledovanom období v SR boli každoročne diagnostikované v priemere 4 nové prípady GTN [4,13].
Tab. 7. Incidencia gestačnej trofoblastovej neoplázie v Slovenskej republike v rokoch 1993–2017.
Tab. 7. Incidence of gestational trophoblastic neoplasia in the Slovak Republic in 1993–2017.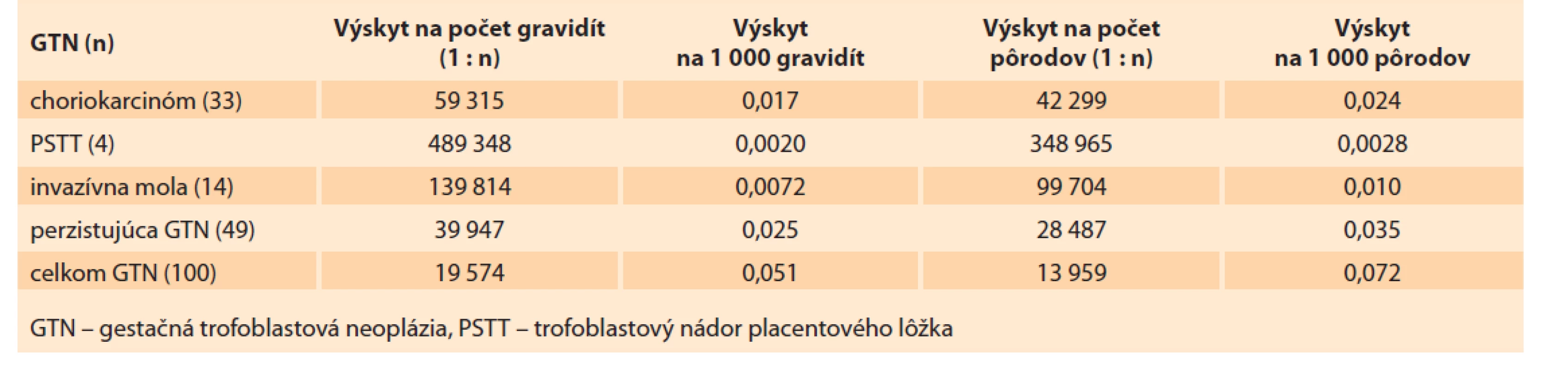
Diskusia
Prelom v liečbe GTN nastal v roku 1956, kedy bola zverejnená prvá publikácia o úspešnej liečbe choriokarcinómu metotrexátom [18]. Historický vývoj kurability a mortality GTN v Československu od roku 1955 kopíroval trendy liečby vo svete. V rokoch 1955–1963 bola kurabilita nízka (5,5 %) a jedinou účinnou liečbou bolo odstránenie postihnutého orgánu. Zavedením chemoterapie sa v rokoch 1963–1980 zvýšila kurabilita na 56,4 %. Pokroky v medicíne a centralizácia liečby ochorenia posunuli v rokoch 1980–2000 kurabilitu na 94,2 % [3]. V rokov 1993–2012 sa kurabilita GTN ešte zlepšila – v ÚPMD 97,7 %, v Motole 100 % (celá ČR 98,2–98,3 %) a SR 94,7 % (tab. 8). Najúspešnejšou etapou bolo 5-ročné obdobie 2013–2017 kedy zhodne tri pracoviská v ČR a CGTCH SR vykázali 100% kurabilitu GTN. V dátach z ČR je však diskrepancia medzi gynekologicko-pôrodníckymi pracoviskami a ÚZIS (Ústav zdravotnických informací a statistiky) ČR. Podľa zverejnených dát ÚZIS (SVOD – software pro vizualizaci onkologických dat) bolo v rokoch 1993–2017 liečených na diagnózu C58 (zhubný nádor placenty) iba 99 pacientok, z ktorých 7 umrelo, čo by znamenalo mortalitu 7,1 % [23]. Údaj o počte liečených pacientok v dátach ÚZIS je zjavne veľmi nepresný, pretože by to mal byť trojnásobný počet (teoretický predpoklad na základe incidencie v Európe, ČR a SR na počet gravidít). Zjavne je to v dôsledku zlyhávania hlásenia týchto prípadov. Údaj ÚZIS o mortalite týchto pacientok možno však považovať za spoľahlivejší ako údaje z gynekologicko-pôrodníckych pracovísk liečiacich toto ochorenie, hoci sa nám nepodarilo zistiť (napriek opakovaným snahám), či išlo o úmrtia v priamej súvislosti s diagnózou C58, alebo z inej príčiny (tab. 8, 9).
Tab. 8. Kurabilita a mortalita pacientok s gestačnou trofoblastovou neopláziou v Českej republike v rokoch 1993–2017.
Tab. 8. Curability and mortality of patients with gestational trophoblastic neoplasia in the Czech Republic in 1993–2017.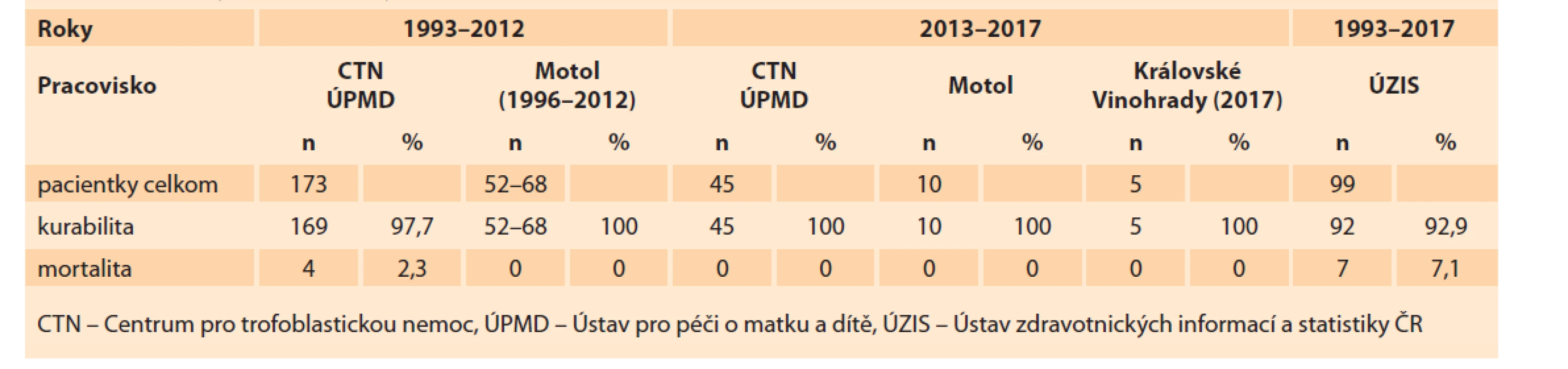
Tab. 9. Kurabilita a mortalita pacientok s gestačnou trofoblastovou neopláziou v Českej a Slovenskej republike v rokoch 1993–2017.
Tab. 9. Curability and mortality of patients with gestational trophoblastic neoplasia in the Czech Republic and Slovak Republic in 1993–2017.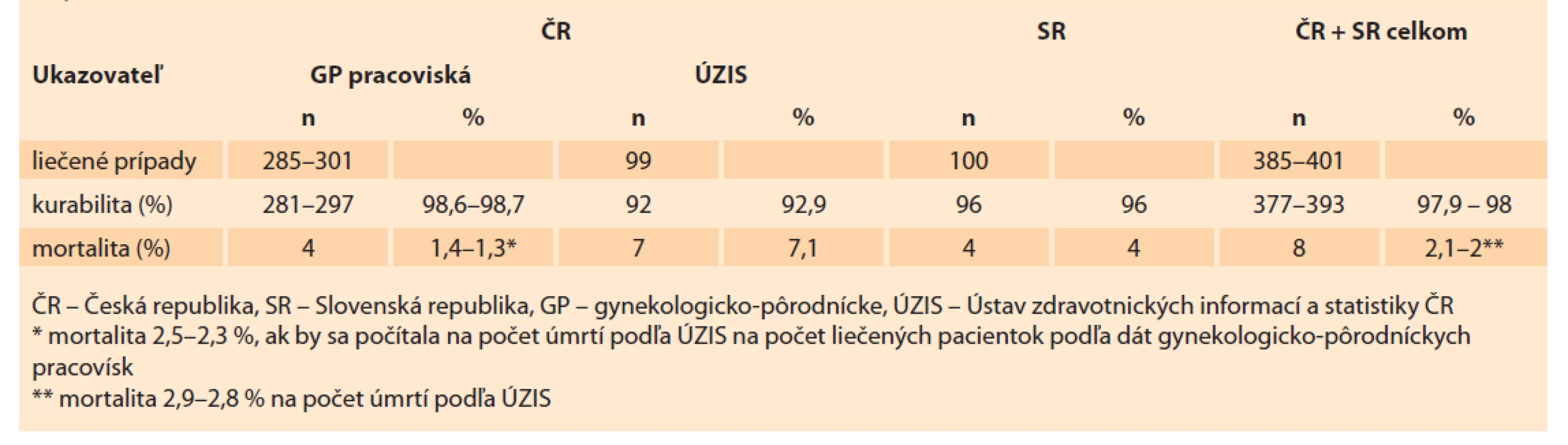
Keby sa výsledky liečby GTN v ČR a SR v rokoch 1993–2017 previedli na spoločného menovateľa (tab. 9), tak za 25 rokov bolo v oboch štátoch liečených 385–401 pacientok s celkovou kurabilitou 97,9–98 % a mortalitou 2,1–2 % (2,9–2,8 % pri počítaní na mortalitu podľa ÚZIS). V ÚPMD, v Motole aj v Královských Vinohradech sa pokračovalo v 40-ročnej tradícii diagnostiky a liečby GTN a zúročili sa historické skúsenosti a systematická práca. Novovybudovanému slovenskému centru chýbali historické skúsenosti, muselo prekonať nielen svoju „learning curve“, ale aj viaceré „reformy“ slovenského zdravotníctva a zápasiť s organizačnými aj ekonomickými problémami [4,13,15]. Výsledky slovenského centra však možno považovať za výborné. Zo štyroch úmrtí sa 3 pacientky dostali do centra v infaustnom stave a len 1 prípad sa nepodarilo terapeuticky zvládnuť (choriokarcinóm metastázoval napriek intenzívnej multimodalitnej terapii). Skoršie odoslanie 3 pacientok do centra by posunulo celkovú kurabilitu na 99 %. V čase úmrtí týchto pacientok vysokého rizika (FIGO IV: ultra high risk) však ešte neboli vedomosti o indukčnej liečbe nízko dávkovaným etopozidom a cisplatinou ani o imunoterapii [24,25]. Potešujúca je aj skutočnosť, že od roku 2008 v SR nebolo zaznamenané žiadne úmrtie pacientky na GTN.
Ostatné desaťročia priniesli ďalšie zlepšenie kurability, čo prispelo k zníženiu mortality na GTN [6,24,26–29]. Spektrum histologických a nehistologických diagnóz GTN sa už niekoľko dekád mení. Kým v minulosti v spektre GTN dominovala histopatologická diagnóza choriokarcinóm, v ostatných desaťročiach prevažuje nehistologická diagnóza – perzistujúca GTN. Vyplýva to zo skutočnosti, že mnoho žien posúva svoje reprodukčné snahy do vyššieho veku, kedy sa ale riziko GTN zvyšuje. Pri absencii histopatologickej diagnózy (keď taktika liečby musí zohľadniť zachovanie uteru i keď je v myometriu lokalizovaný trofoblastový tumor), je vedúcou modalitou liečby chemoterapia podľa prognostického skórovacieho systému a stagingu ako pri choriokarcinóme [3,4,13]. Najoptimálnejší vek na rodenie je jednoznačne medzi 20–30 rokom života ženy, kedy sú aj perinatologické ukazovatele najlepšie a riziko GTN je najnižšie (potvrdzujú to aj slovenské epidemiologické dáta).
V období rokov 1993–2017 v SR prevažovala u 100 liečených pacientok PGTN 49 %, nasledoval choriokarcinóm 33 %, invazívna mola 14 % a PSTT 4 % (tab. 10). V tom istom období u 233 pacientok liečených v pražských pracoviskách (tab. 10) prevažoval choriokarcinóm 42 %, nasledovala PGTN 41 %, invazívna mola 10 %, PSTT 9 % a epiteloidný trofoblastový tumor (ETT) 3 %.
Tab. 10. Frekvencia jednotlivých foriem gestačnej trofoblastovej neoplázie v Slovenskej a Českej republike v rokoch 1993–2017.
Tab. 10. Frequency of individual forms of gestational trophoblastic neoplasia in the Slovak Republic and Czech Republic in the years 1993–2017.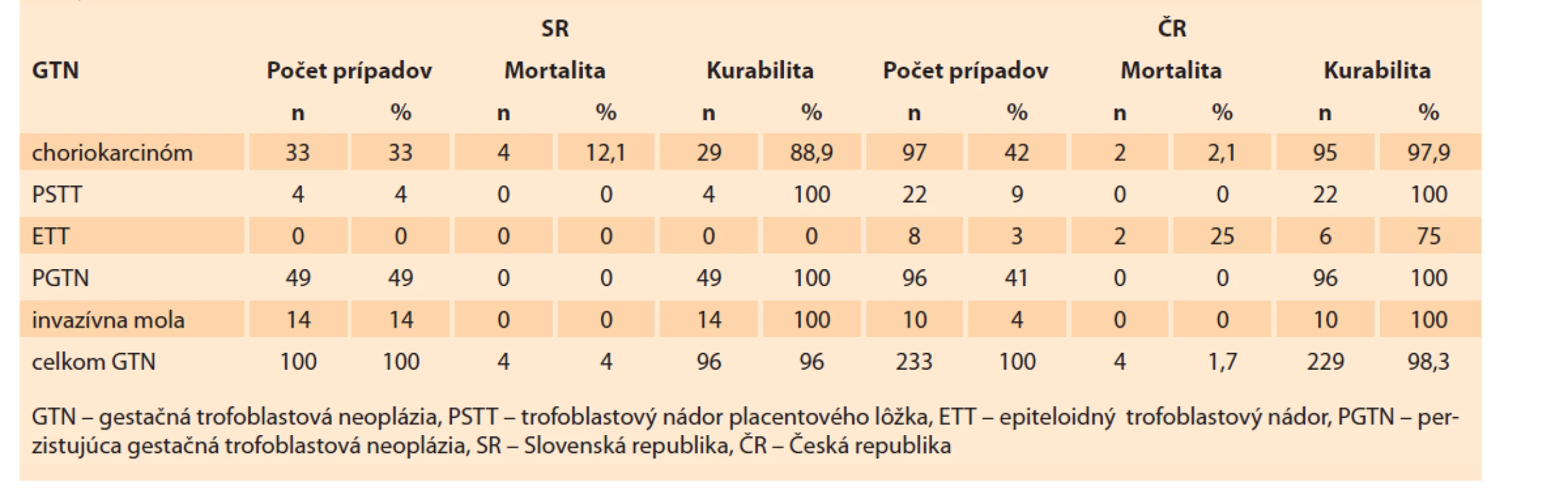
Výsledky liečby GTN v ČR aj v SR sú porovnateľné s výsledkami popredných centier pre GTD vo svete. Pozitívnym javom je 100% kurabilita v skupine pacientok s PGTN, invazívnou molou a PSTT v SR aj ČR. PSTT patrí k najmalígnejším formám GTN a preto 100% kurabilita v ČR aj SR je pozoruhodný výsledok (i keď pri menšom počte pacientok). U pacientok s PGTN sa chemoterapiou podarilo zachovať aj fertilitu a dať šancu na pôrod dieťaťa [3,4,13].
Publikované údaje o graviditách po chemoterapii z ČR aj SR sú porovnateľné a veľmi optimistické (tab. 11, 12). Veľmi pozitívna správa pre ženy s GTN je, že v ČR aj SR sa pacientkam po chemoterapii narodili všetky deti živé a zdravé (bez vrodených malformácií) [4,14,21].
Tab. 11. Fertilita pacientok po chemoterapii pre gestačnú trofoblastovú neopláziu v Českej a Slovenskej republike.
Tab. 11. Fertility of patients after chemotherapy for gestational trophoblastic neoplasia in the Czech Republic and Slovak Republic.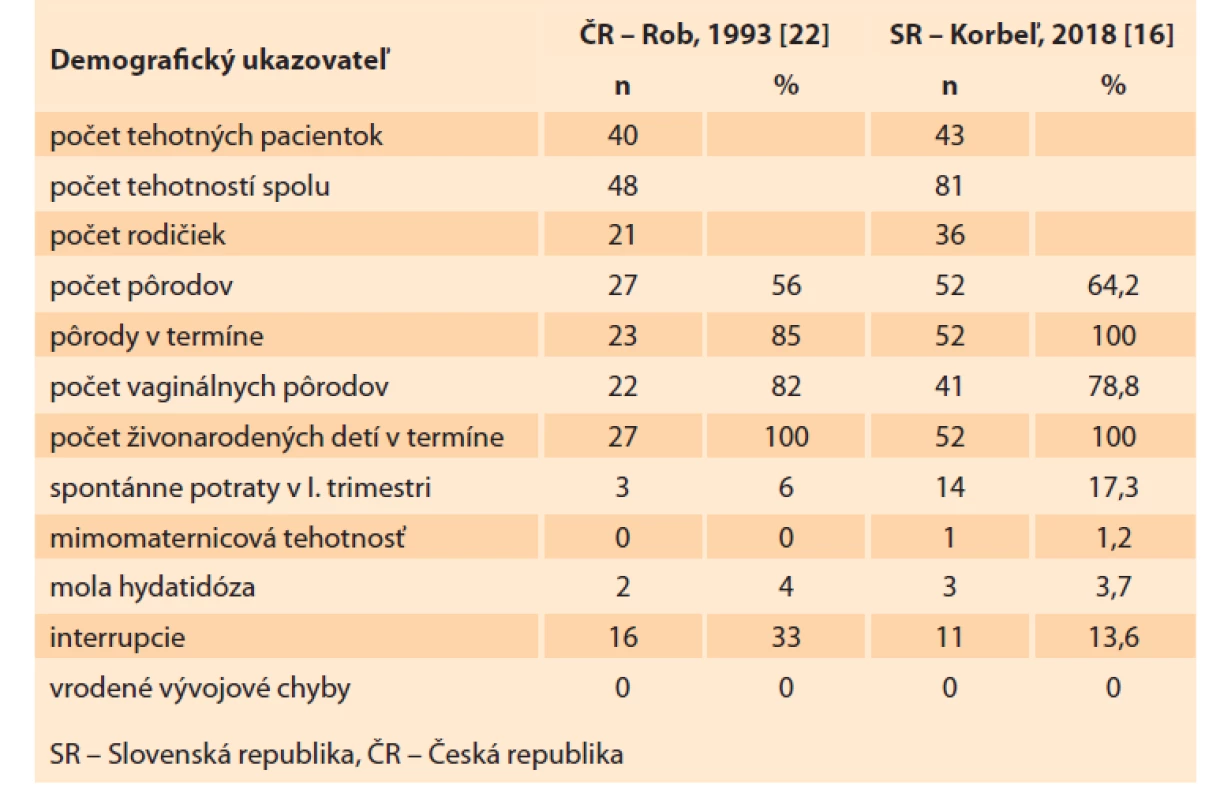
Tab. 12. Tehotnosti po liečbe gestačnej trofoblastovej neoplázie – dáta zo sveta, Česká a Slovenská republika.
Tab. 12. Pregnancy after the treatment of gestational trophoblastic neoplasia – data from the world, Czech Republic and Slovak Republic.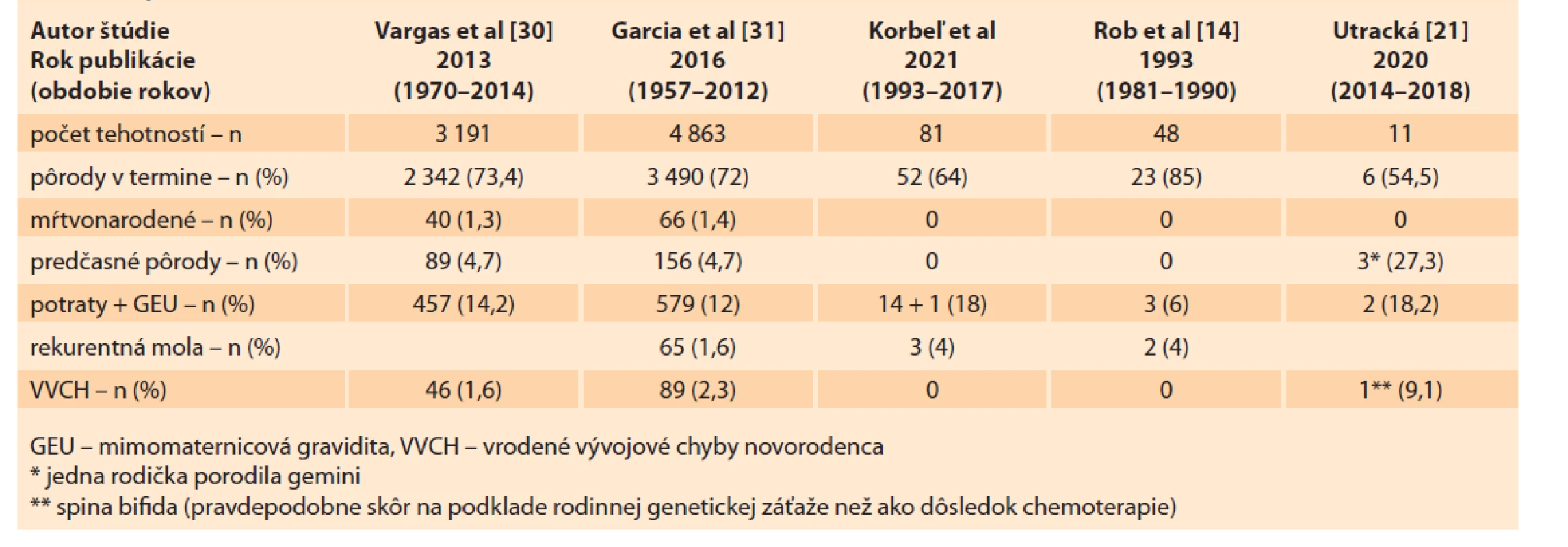
V roku 2014 Vargas et al publikovali sumár výsledkov 3 191 gravidít po liečbe GTN z 11 svetových pracovísk publikovaných v rokov 1970–2014 [30] a v roku 2016 Garcia et al sumár 4 863 gravidít po liečbe GTN zo 16 svetových pracovísk publikovaných v rokov 1984–2014 [31].Každé z citovaných pracovísk vykazovalo buď predčasné pôrody, alebo mŕtvorodenosť alebo vrodené malformácie [30,31]. V malom súbore gravidít z CTN Podolí v rokoch 2014–2018 sa žiadne dieťa nenarodilo mŕtve, ale 4 deti predčasne (z toho jedny gemini) a 1 dieťa so spinou bifidou, ktorá vznikla pravdepodobne na podklade rodinnej genetickej záťaže ako dôsledok chemoterapie (tab. 12) [21].
Na GTN treba myslieť v diferenciálnej diagnostike všetkých nejasných stavov u žien s anamnézou akejkoľvek gravidity v minulosti, ktoré prichádzajú s nepravidelným krvácaním, metastázami nejasnej genézy, či pozitivitou alebo pretrvávajúcimi nízkymi hladinami hCG [13]. Pri vysokej kurabilite GTN sa dá veľa zachrániť, ale nesprávnym manažmentom aj veľa pokaziť. Stále platí to, čo Mogensen napísal v roku 1973, že „nie je jednoduché určiť štandardný priebeh ochorenia, zvraty stavu sú nečakané, prekvapivé a nemožno ich vôbec predvídať“ platia doteraz [32].
Záver
Kvalita starostlivosti o pacientky s GTN v SR aj ČR je na vysokej úrovni, porovnateľnej s inými špecializovanými centrami vo svete. Základom úspešnej liečby GTN je včasné odoslanie pacientok na riešenie do centra. Úspešná liečba GTN, ktorá sa v súčasnosti blíži k hranici 99–100 %, dáva ženám vo fertilnom veku šancu na pôrod zdravého dieťaťa.
Doručené/ Submitted: 16. 2. 2021
Prijaté/ Accepted: 3. 3. 2021
doc. MU Dr. Miroslav Korbeľ, CSc.
I. gynekologicko-pôrodnícka klinika
LF UK a UN Bratislava
Antolská 11
851 07 Bratislava
Slovenská republika
Publikačné etika: Redakčná rada potvrdzuje, že rukopis práce splnil ICMJE kritériá pre publikácie zasielané do biomedicínskych časopisov.
Publication ethics: The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Konflikt záujmov: Autori deklarujú, že v súvislosti s predmetom štúdie/ práce nemajú žiadny konflikt záujmov.
Conflict of interests: The authors declare they have no potential conflicts of interest concerning the drugs, products or services used in the study.
Poďakovanie: Za poskytnutie dát o GTN v ČR od roku 1993 ďakujeme MU Dr. F. Hronovi, MU Dr. E. Utrackej a doc. MU Dr. J. Feyereislovi, CSc. z CTN ÚPMD Praha-Podolí, prof. MU Dr. L. Robovi, CSc. z gynekologicko-porodnické kliniky 2. LF UK a FN Motol Praha a z gynekologicko-porodnické kliniky 3. LF UK a FN Královské Vinohrady Praha a prim. MU Dr. M. Plutovi, Ph.D. z gynekologicko-porodnické kliniky 2. LF UK a FN Motol Praha.
Poďakovanie patrí aj všetkým bývalým i terajším spolupracovníkom CGTCH SR za ich dlhoročnú obetavú prácu pri manažovaní pacientok s GTN.
Acknowledgment: We thank F. Hron, MD, E. Utracka, MD and Assoc. Prof. MU Dr. J. Feyereisl, PhD, from CTN ÚPMD Prague-Podolí, Prof. L. Rob, MD, PhD, from Gynecology and Obstetrics Clinic of 2nd Medical Faculty of Charles University and Motol University Hospital in Prague, and from Gynecology and Obstetrics Clinic of 3rd Medical Faculty of Charles University and Královské Vinohrady University Hospital in Prague, and M. Pluto, MD, PhD, from Gynecology and Obstetrics Clinic of 2nd Medical Faculty of Charles University and Motol University Hospital in Prague for providing data on GTN in the Czech Republic since 1993.
Thanks also go to all former and current collaborators of CGTCH SR for many years of their dedicated work in managing patients with GTN.
Zdroje
1. Braga A, Mora P, de Melo AC et al. Challenges in the diagnosis and treatment of gestational trophoblastic neoplasia worldwide. World J Clin Oncol 2019; 10(2): 28–37. doi: 10.5306/ wjco.v10.i2.28.
2. Brown J, Naumann RW, Seckl MJ et al. 15 years of progress in gestational trophoblastic disease: scoring, standardization, and salvage. Gynecol Oncol 2016; 144(1): 200–207. doi: 10.1016/ j.ygyno.2016.08.330.
3. Hron F, Feyereisl J, Zavadil M. Výsledky léčby gestačních trofoblastických tumorů v ČR. Gynekol Prax 2014; 12(3): 127–131.
4. Korbeľ M, Šufliarsky J, Danihel Ľ et al. Liečba gestačných trofoblastových tumorov v Slovenskej republike v rokoch 1993–2012. Gynekol Prax 2014; 12(3): 132–135.
5. Li MC, Hertz R, Spencer DB. Effect of methotrexate therapy upon choriocarcinoma and chorioadenoma. Proc Soc Biol Med 1956; 93(2): 361–369. doi: 10.3181/ 00379727-93-22757.
6. Ngan HY, Seckl MJ, Berkowitz RS et al. Update on the diagnosis and management of gestational trophoblastic disease. Int J Gynaecol Obstet 2018; 143(Suppl 2): 79–85. doi: 10.1002/ ijgo.12615.
7. Seckl MJ, Sebire NJ, Fischer RA et al. Gestational trophoblastic disease: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2013; 24(Suppl 6): vi39–vi50. doi: 10.1093/ annonc/ mdt345.
8. Gazárek F, Kudela M, Lindner E. Naše zkušenosti s léčbou choriokarcinomu. Ceska Gynekol 1976; 41 : 273–275.
9. Kudela M, Gazárek F, Fingerova H. Diagnostik und terapie bösartiger trofoblasttumoren. Acta Univ Palacky Olom 1979; 90 : 213–216.
10. Skřivan J, Zavadil M, Jakoubková J et al. Péče o ženy s trofoblastickou nemocí (choriokarcinomem) v ČSSR. Prakt Lék 1982; 62(18): 546–547.
11. Zavadil M, Skřivan J, Rob L et al. Centrum pro trofoblastickou nemoc (CTN). Ceska Gynekol 1988; 53(9): 695–700.
12. Zavadil M, Feyereisl J, Krofta L et al. Perzistující trofoblastická nemoc v Centru pro trofoblastickopu nemoc v ČR v létech 1955–2007. Ceska Gynekol 2008; 73(2): 73–79.
13. Korbeľ M, Šufliarsky J, Danihel Ľ et al. Výsledky liečby gestačnej trofoblastovej neoplázie v Slovenskej republike v rokoch 1993–2012. Ceska Gynekol 2016; 81(1): 6–13.
14. Rob L, Zavadil M, Vlachová J. Těhotenství po chemoterapii u maligních forem gestační trofoblastické nemoci. Sborník Lékařský 1993; 94(2): 185–189.
15. Korbeľ M, Danihel Ľ, Vojtaššák J et al. Centrum pre trofoblastovú chorobu Slovenskej republiky – 10 rokov činnosti. Slov Gynek Pôrod 2003; 10(2): 56–61.
16. FIGO Oncology Committee. FIGO staging for gestational trophoblastic neoplasia 2000. Int J Gynecol Obstet 2000; 77(3): 285–287. doi: 10.1016/ s0020-7292(02)00063-2.
17. Kohorn EI. Negotiating a staging and risk factor scoring system for gestational trophoblastic neoplasia. A progress report. J Reprod Med 2002; 47(6): 445–500.
18. WHO. Gestational trophoblastic diseases: report of a WHO scientific group. World Health Organ Tech Rep Ser 1983; 692 : 7–81.
19. Danihel Ľ, Čierna Z, Šišovský V et al. Histopatologická diagnostika gestačných trofoblastových tumorov. Gynekol Prax 2014; 12(3): 150–153.
20. Genest DR, Berkowitz RS, Fisher RA et al. Gestational trophoblastic disease. In: Tavassoli FA, Devilee P, WHO classification of tumours (eds). Pathology and genetics, tumours of the breast and female genital organs. Tumours of the uterine corpus. 3rd ed. Lyon: IARC Press 2003 : 250–254.
21. Utracká E. Fertilita po chemoterapii pro gestační trofoblastickou nemoc. Gyn Por 2020; 4(1): 30–32.
22. Lin LH, Maestá I, Braga A et al. Multiple pregnancies with complete mole and coexisting normal fetus in North and South America: a retrospective multicenter cohort and literature review. Gynecol Oncol 2017; 145(1): 88–95. doi: 10.1016/ j.ygyno.2017.01.021.
23. SVOD. Epidemiologie zhoubných nádorů v České republice. 2021 [online]. Dostupné na: www.svod.cz.
24. Alifrangis C, Agarwal R, Short D et al. EMA/ CO for high-risk gestational trophoblastic neoplasia: good outcomes with induction low-dose etoposide-cisplatin and genetics analysis. J Clin Oncol 2013; 31(2): 280–286. doi: 10.1200/ JCO.2012.43.1817.
25. Bolze PA, Patrier S, Massardier J et al. PD-L1 expression in premalignant and malignant trophoblasts from gestational trophoblastic diseases is ubiquitous and independent of clinical outcomes. Int J Gynecol Cancer 2017; 27(3): 554–561. doi: 10.1097/ IGC.0000000000000892.
26. Bolze PA, Attia J, Massardier J et al. Formalised consensus of the European Organisation for Treatment of Trophoblastic Diseases on management of gestational trophoblastic diseases. Eur J Cancer 2015; 51(13): 1725–1731. doi: 10.1016/ j.ejca.2015.05.026.
27. Clair KH, Gallegos N, Bristow RE. Succesful treatment of metastatic refractory gestational choriocarcinoma with pembrolizumab: a case for immune checkpoint salvage therapy in trophoblastic tumors. Gynecol Oncol Rep 2020; 34 : 100625. doi: 10.1016/ j.gore.2020.100625.
28. Sharami SR, Saffarieh E. A review on management of gestational trophoblastic neoplasia. J Family Med Prim Care 2020; 9(3): 1287–1295. doi: 10.4103/ jfmpc.jfmpc_876_19.
29. You B, Bolze PA, Lotz JP et al. Avelumab in patients with gestational trophoblastic tumors with resistance to single-agent chemotherapy: cohort A of the TROPHIMMUN phase II trial. J Clin Oncol 2020; 38(27): 3129–3137. doi: 10.1200/ JCO.20.00803.
30. Vargas R, Barroilhet LM, Esselen K et al. Subsequent pregnancy outcome after complete and partial molar pregnancy, recurrent molar pregnancy, and gestational trophoblastic neoplasia: an update from the New England Trophoblastic Disease Center. J Reprod Med 2014; 59(5–6): 188–194.
31. Garcia MT, Lin LH, Fushida K et al. Pregnancy outcomes after chemotherapy for frophoblastic neoplasia. Rev Assoc Med Bras 2016; 62(9): 837–842. doi: 10.1590/ 1806-9282.62.09.837.
32. Mogensen B. Invasive mole and gestational choriocarcinoma in Denmark, 1940–1969: biological and clinical aspects. Acta Obstet Gynec Scand 1973; 52(3): 211–220. doi: 10.3109/ 00016347309158317.
Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicína
Článek vyšel v časopiseČeská gynekologie
Nejčtenější tento týden
2021 Číslo 2- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- INFOGRAFIKA: Algoritmus individualizované léčby obezity dle EASO 2025
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Magnosolv a jeho využití v neurologii
- Isoprinosin je bezpečný a účinný v léčbě pacientů s akutní respirační virovou infekcí
-
Všechny články tohoto čísla
- Analýza vybraných perinatologických ukazovateľov v Slovenskej republike v rokoch 2007–2018
- “Bloodless surgery” a gynekologické pacientky hlásící se k víře Svědků Jehovových
- Obrovský fibroadenom prsu v těhotenství
- Poranění análního sfinkteru při porodu a anální inkontinence
- Současné možnosti prevence a terapie ovariálního hyperstimulačního syndromu
- Kvalita života a sexualita u žen s močovou inkontinencí
- Obštrukcia dolného močového traktu plodu: aktuálny prehľad možnosti intrauterinnej diagnostiky a liečby
- Řešená problematika reprodukční medicíny v České republice 2020
- Význam měření pupečníkového interleukinu-6, prokalcitoninu a C-reaktivního proteinu v diagnostice systémové zánětlivé odpovědi plodu
- Nový nástroj pro personalizaci ovariální stimulace: výsledky studie CERES při použití nového gonadotropinu – folitropinu delta
- Výsledky liečby gestačnej trofoblastovej neoplázie v Slovenskej republike v rokoch 1993–2017
- Česká gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Současné možnosti prevence a terapie ovariálního hyperstimulačního syndromu
- Obrovský fibroadenom prsu v těhotenství
- Poranění análního sfinkteru při porodu a anální inkontinence
- Nový nástroj pro personalizaci ovariální stimulace: výsledky studie CERES při použití nového gonadotropinu – folitropinu delta
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



