-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaPorovnání incizionální a epidurální analgezie v léčbě pooperační bolesti po císařském řezu
Comparison of incisional and epidural analgesia in the treatment of postoperative pain after cesarean section
Objective:
Comparison of incisional and epidural analgesia in the treatment of postoperative pain after cesarean sectio.
Design:
Prospective cohort study in the period from 2015 to 2016.
Setting:
Department of Obstetric and Gynecology, Masaryk University, University Hospital Brno.
Material and methods:
The group included 72 patients in the 38th–41st. week of pregnancy. They were divided at the time of indication to the cesarean section (SC) into two groups according to the selected type of analgesia (epidural/incisional). Women with epidural analgesia (EA) received bupivacaine and sufentanil after surgery in the epidural catheter. A second group was patients during general anesthesia SC introduced into the surgical wound IA Painfusor which was continuously administered bupivacaine. The intensity of the patient‘s pain was evaluated on the visual analogue scale (VAS). If the VAS exceeded 4, the dose of the opioid analgesic piritramide (additional dose of DDA analgesic) was administered intravenously. The intensity of pain and the number of DDAs required were evaluated 24 hours after SC. Satisfaction with pain relief, sleep quality, and patient side effects were assessed using a questionnaire.
Results:
Patients in the EA group (n = 36) evaluated postoperative pain (PB) value of 4.4 ± 1.8 according to VAS, women in group IA (n = 36) reported a PB according to VAS of 4.4 ± 1.3 (p = 0.972). The difference in the number of applied DDA was not statistically significant compared groups (2.3 ± 0.9 EA vs. 2.4 ± 0.9 IA, p = 0.301). By comparing the other parameters evaluated by the questionnaire statistically significant more vertigo cases were found in women with IA (22.2% EA vs. 72.2% IA, p < 0.001). In the other evaluated parameters the differences between the two methods were not statistically significant.
Conclusion:
Epidural and incisional analgesia are comparable methods in the effectiveness of pain management during the first day of the cesarean section. Except for vertigo, both methods were also comparable in terms of the occurrence of undesirable effects.
Keywords:
cesarean section, postoperative analgesia, epidural analgesia, incisional analgesia, Painfusor
Autoři: I. Meixnerová 1; Martin Huser 1
; D. Seidlová 2,3; Petr Janků 1
; P. Štourač 4; R. Gál 2
Působiště autorů: Gynekologicko-porodnická klinika LF MU a FN, Brno, přednosta prof. MUDr. P. Ventruba, DrSc., MBA 1; Klinika anesteziologie, resuscitace a intenzivní medicíny LF MU a FN, Brno, přednosta prof. MUDr. R. Gál, Ph. D. 2; II. anesteziologicko-resuscitační oddělení FN, Brno, primářka MUDr. D. Seidlová, Ph. D. 3; Klinika dětské anesteziologie a resuscitace LF MU a FN, Brno, přednosta doc. MUDr. P. Štourač, Ph. D. 4
Vyšlo v časopise: Ceska Gynekol 2018; 83(3): 182-187
Souhrn
Cíl studie:
Porovnání incizionální (IA) a epidurální (EA) analgezie v léčbě pooperační bolesti u žen po císařském řezu (SC). Srovnání parametrů objektivních (intenzita bolesti, počet dodatečných dávek analgetik, nežádoucí účinky) a subjektivních (spokojenost s metodou, poruchy spánku).
Typ studie:
Prospektivní kohortová studie v letech 2015–2016.
Název a sídlo pracoviště:
Gynekologicko-porodnická klinika LF MU a FN Brno.
Soubor a metodika:
Soubor zahrnoval 72 pacientek ve 38. až 41. týdnu těhotenství. Byly rozděleny v době indikace k císařskému řezu do dvou skupin podle volby typu analgezie (epidurální/incizionální). Ženy s EA dostávaly po operaci do epidurálního katétru bupivakain a sufentanil. Druhé skupině pacientek byl v průběhu SC v celkové anestezii zaveden do operační rány IA Painfusor, kterým byl po operaci kontinuálně podáván bupivakain. Intenzitu bolesti pacientky hodnotily na vizuální analogové škále (VAS). Pokud VAS přesáhla 4, byla intravenózně aplikována dávka opioidního analgetika piritramid (dodatečná dávka analgetika DDA). Ve sledovaném období 24 hodin po SC byla hodnocena intenzita bolesti a počet vyžadovaných DDA. Spokojenost s tlumením bolesti, kvalitu spánku a nežádoucí účinky pacientky hodnotily pomocí dotazníku.
Výsledky:
Pacientky ve skupině EA (n = 36) hodnotily pooperační bolest (PB) hodnotou 4,4 ± 1,8 podle VAS, ženy ve skupině IA (n = 36) udávaly hodnotu PB podle VAS 4,4 ± 1,3 (p = 0,972). Rozdíl v počtu aplikovaných DDA nebyl ve srovnávaných skupinách statisticky významný (2,3 ± 0,9 EA vs. 2,4 ± 0,9 IA, p = 0,301). Při srovnávání dalších parametrů hodnocených dotazníkem bylo zjištěno statisticky signifikantně více případů vertiga u žen s IA (22,2 % EA vs. 72,2 % IA, p < 0,001). V ostatních hodnocených parametrech nebyly rozdíly mezi oběma metodami statisticky významné.
Závěr:
Epidurální a incizionální analgezie jsou srovnatelné metody v efektivitě léčby bolesti v období prvního dne po císařském řezu. S výjimkou vertiga byly obě metody srovnatelné také z hlediska výskytu nežádoucích účinků.
Klíčová slova
císařský řez, pooperační analgezie, epidurální analgezie, incizionální analgezie, Painfuso
ÚVOD
Císařský řez je nejčastější porodnickou operací. V České republice se v roce 2016 narodilo 24,9 % dětí císařským řezem [15]. Frekvence císařských řezů souvisí s rostoucím podílem starších rodiček, počtem předčasných porodů a vícečetných těhotenství. Významným faktorem je také předchozí porod císařským řezem [3, 9]. Tato abdominální operace je spojena s vnímáním akutní bolesti v časném pooperačním období. Dobře nastavená pooperační analgezie snižuje morbiditu pacientky, umožňuje časnou mobilizaci, a tím snižuje rizika tromboembolické choroby. Naopak nedostatečná analgezie má negativní vliv na pooperační průběh. Vede k aktivaci sympatiku, zvýšené spotřebě kyslíku, tachykardii a hypertenzi [4].
Bolest je symptom, který informuje organismus o hrozícím či probíhajícím tkáňovém inzultu. Jedná se o nepříjemný prožitek spojený se strachem, úzkostí a fylogeneticky starou obrannou nebo únikovou vegetativní reakcí. Pokud není akutní bolest dostatečně léčena, může se na podkladě periferní a centrální senzitizace nervového systému v řádu měsíců rozvinout v bolest chronickou [7]. Intenzita bolesti je nejčastěji sledována podle vizuální analogové škály (VAS). Další možností hodnocení je kategoriální stupnice – Melzackova škála, intenzita současné bolesti (present pain intensity), kde 0 je žádná, 1 mírná, 2 středně silná, 3 silná, 4 krutá a 5 nesnesitelná [7].
Předpokládaná intenzita pooperační bolesti po císařském řezu je střední až vysoká. Proto je v pooperační analgezii vhodné použití multimodální analgezie – kombinace analgetik různých skupin – zajišťující aditivní účinek a snižující nežádoucí účinky. Účinek monoterapie neopiodními analgetiky je v léčbě bolesti zpravidla nedostatečný [4]. Jednou z účinných možností, a na našem pracovišti nejrozšířenější, je kombinace nesteroidního antiflogistika (NSA) s krátkým biologickým poločasem, a to především diklofenaku, se silným opioidem (piritramid). První volbou z neopioidních analgetik v celém peripartálním období je paracetamol. Jednou z možných alternativ, zejména v rámci multimodální analgezie, je kombinace NSA či paracetamolu s metamizolem. Tato kombinace se u nás také používá, i když podle souhrnu údajů o léčivém přípravku není podávání metamizolu v době kojení doporučováno. Absolutní kontraindikace jeho podání se týká ale především třetího trimestru těhotenství pro jeho slabý, ale patrný účinek na inhibici prostaglandinů [12, 19].
Nejúčinnější metodou pooperační analgezie po císařském řezu je nesporně epidurální analgezie (EA). Do epidurálního prostoru (v oblasti bederní páteře) je zaveden anesteziologem již předoperačně katétr, jímž je podávána nejčastěji směs lokálního anestetika a opiátu. EA lze samozřejmě zahájit již během porodu, s možností přechodu do epidurální anestezie a následnou pooperační analgezií. Tato analgezie je bez negativního vlivu na plod, lze ji použít u rizikových pacientek (hypertenze, asthma bronchiale, preeklampsie apod.) [16, 18, 21].
Další možností je incizionální analgezie (IA) v místě operační rány. Tato technika je založená na opakované instilaci lokálního anestetika do operační rány katétrem, který zavádí chirurg při šití rány. Je možno použít epidurální katétr o velikosti 18 G (průměr 1,3 mm) nebo 16 G (průměr 1,7 mm) [10]. Lokální anestetikum je dávkováno v bolusech, kontinuálně dávkovačem nebo systémem PCA (pacient contolled analgesia) elastomerickou pumpou. V naší studii jsme používali Painfusor (Baxter), tedy perforovaný katétr napojený na pumpu s analgetiky (Infusor) s kontinuálním či regulovatelným průtokem. Délka katétru je volitelná podle velikosti operační rány od 7,5 do 30,0 cm. Zavádí jej operatér subfasciálně v průběhu operačního výkonu. Po dokončení sutury rány aplikuje do Painfusoru bolus 20 ml lokálního anestetika. Infusor se zásobou lokálního anestetika určený k postupnému uvolňování napojí sestra na pooperačním oddělení.
Cílem naší práce je porovnání účinnosti IA a EA v léčbě pooperační bolesti u žen v období 24 hodin po císařském řezu pomocí objektivních a subjektivních parametrů pro měření intenzity bolesti a sledování výskytu vybraných nežádoucích účinků těchto analgetických technik.
MATERIÁL A METODIKA
Do studie bylo zařazeno celkem 72 pacientek indikovaných k porodu císařským řezem v období leden 2015 až leden 2016 na Gynekologicko-porodnické klinice LF MU a FN Brno ve spolupráci s kolegy z Kliniky anesteziologie, resuscitace a intenzivní medicíny LF MU a FN Brno a II. anesteziologicko-resuscitačního oddělení FN Brno. Do souboru byly zařazeny pacientky s jednočetnou termínovou graviditou (38.–42. týden gravidity) indikované k akutnímu či plánovanému císařskému řezu. Pacientky měly nízký stupeň rizika anestezie (stupeň I nebo II), hodnocený pomocí klasifikace fyzického stavu nemocného ASA (American Society of Anesthesiologist) [1]. V době indikace císařského řezu byly pacientky rozděleny do dvou skupin. Do skupiny epidurální analgezie byly zařazeny pacientky, které měly EA již během první doby porodní a pacientky indikované k primárnímu císařskému řezu s možností podání epidurální anestezie. Dále pacientky, které si EA přály a nebylo zde riziko z prodlení. Skupina incizionální analgezie zahrnovala pacientky, u kterých byla EA kontraindikována, EA si nepřály nebo hrozilo riziko z prodlení.
Pacientkám ve skupině EA byla podána standardní dávka směsi bupivakainu a sufentanilu pro epidurální anestezii k císařskému řezu. Pooperačně pak byla podávána naředěná směs bupivakainu a sufentanilu (0,5% Marcaine + 100 µg Sufenta + 38 ml F1/1) rychlostí 6 ml/hod po dobu 24 hodin po operaci. Skupině IA byla na konci operace provedena inzerce katétru Painfusor subfasciálně pomocí zaváděcí jehly a poté byla dokončena sutura rány. Po aplikaci bolusu bupivakainu 20 ml (0,25% Marcaine) byla připojena pumpa Infusor a pokračováno v aplikaci bupivakainu (0,25% Marcaine) z Infusoru rychlostí 5 ml/hod po dobu 24 hodin.
Všechny pacientky byly po operaci sledovány a poučeny o způsobu vyjádření intenzity bolesti pomocí vizuální analogové škály VAS. Pacientky hodnotily intenzitu popisované bolesti na numerické stupnici, na které jsou číslice od 0 do 10. Číslice 0 odpovídá nulové bolesti a číslice 10 maximální bolesti, jakou si pacient dokáže představit. Hlavní sledovaný parametr byla intenzita bolesti v období 24 hodin po operaci. Při pooperační bolesti stupně VAS < 4 byla podána dávka piritramidu 0,2 mg/kg s.c. a zaznamenána jako dodatečná dávka analgetika (DDA). Počet dodatečných dávek analgetik byl hodnocen jako další a zcela objektivní sledovaný parametr hodnocení pooperační bolesti. Pacientky dále ještě subjektivně hodnotily celkovou spokojenost s léčbou pooperační bolesti v období prvních 24 hodin po výkonu na stupnici 1–5 jako ve škole (1 – výborně, 5 – nedostatečně). Pomocí dotazníku pacientky dále ve stejném období hodnotily kvalitu spánku a možné nežádoucí účinky pooperační analgezie – nevolnost, zvracení, bolesti hlavy, vertigo, nadměrné pocení, třesavku a nechutenství.
K vyloučení selekční chyby byly obě srovnávané skupiny pacientek porovnány z hlediska věku, parity a body mass indexu. Ke statistickému srovnání obou analgetických metod (EA a IA) byl použit Fisherův exaktní test pro data kategoriální a Mannův-Whitneyho U test pro data spojitá. Jako hladina statistické významnosti byla ve všech testech použita hodnota α = 0,05. Ke statistickému zpracování byl použit software Statistica (TIBCO Software Inc.).
VÝSLEDKY
Obě srovnávané skupiny pacientek (EA a IA) byly před dalším statistickým zpracováním porovnány z hlediska věku, parity a body mass indexu. V žádné z obou skupin nebyl nalezen statisticky signifikantní rozdíl (tab. 1). Průměrný věk pacientek s EA byl 30,4 ± 6,4 let, pacientky s IA byly průměrného věku 30,3 ± 4,4 let (p = 0,423). Rodičky s EA měly body mass index 30,1 ± 3,0, body mass index pacientek s IA byl 29,4 ± 4,8 (p = 0,647). Průměrná parita žen ve skupině EA byla 1,8 ± 0,4 dítěte, ve skupině IA měly ženy 1,9 ± 0,5 dítěte (p = 0,532).
Tab. 1. Srovnání obou skupin z hlediska věku, indexu tělesné hmotnosti a parity 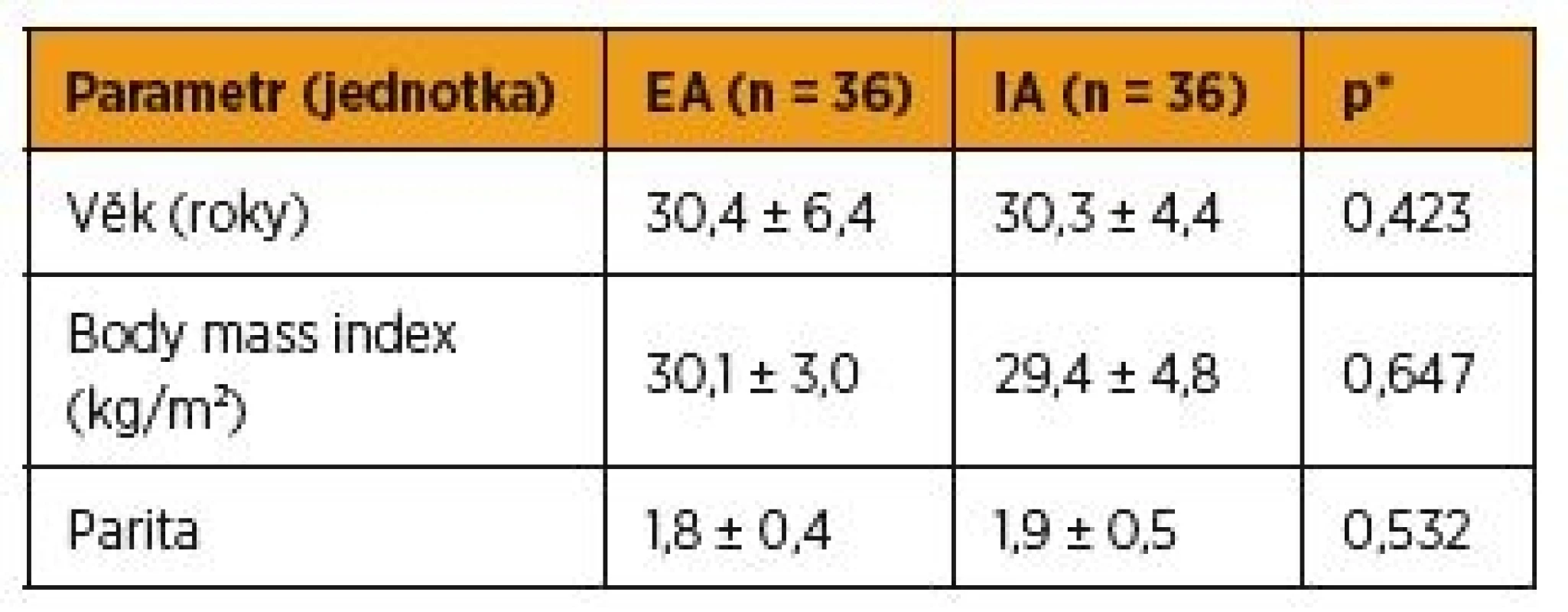
*Mannův-Whitneyho U test Pacientky, které měly EA po císařském řezu, hodnotily pooperační bolest hodnotou 4,4 ± 1,8 podle vizuální analogové škály. Ženy ve skupině IA (n = 36) udávaly hodnotu pooperační bolesti podle VAS 4,4 ± 1,3 (p = 0,972). Při srovnání obou skupin v počtu aplikovaných dodatečných dávek analgetika nebyl rovněž rozdíl mezi oběma srovnávanými skupinami pacientek statisticky významný (p = 0,301). Pacientkám ve skupině EA bylo podáno 2,3 ± 0,9 DDA. Ženy v souboru IA dostaly 2,4 ± 0,9 DDA. Pacientky dále hodnotily celkovou spokojenost s příslušnou metodou pooperační analgezie známkou od 1 do 5. EA hodnotily průměrnou známkou 2,2 ± 0,8, IA byla pacientkami průměrně hodnocena známkou 2,3 ± 0,8. Rozdíl v subjektivním hodnocení obou srovnávaných metod pooperační analgezie také nebyl statisticky významný (p = 0,319) (tab. 2). Hodnocení nežádoucích účinků obsahuje tabulka 3.
Tab. 2. Hodnocení účinnosti léčby pooperační bolesti a spokojenosti pacientek 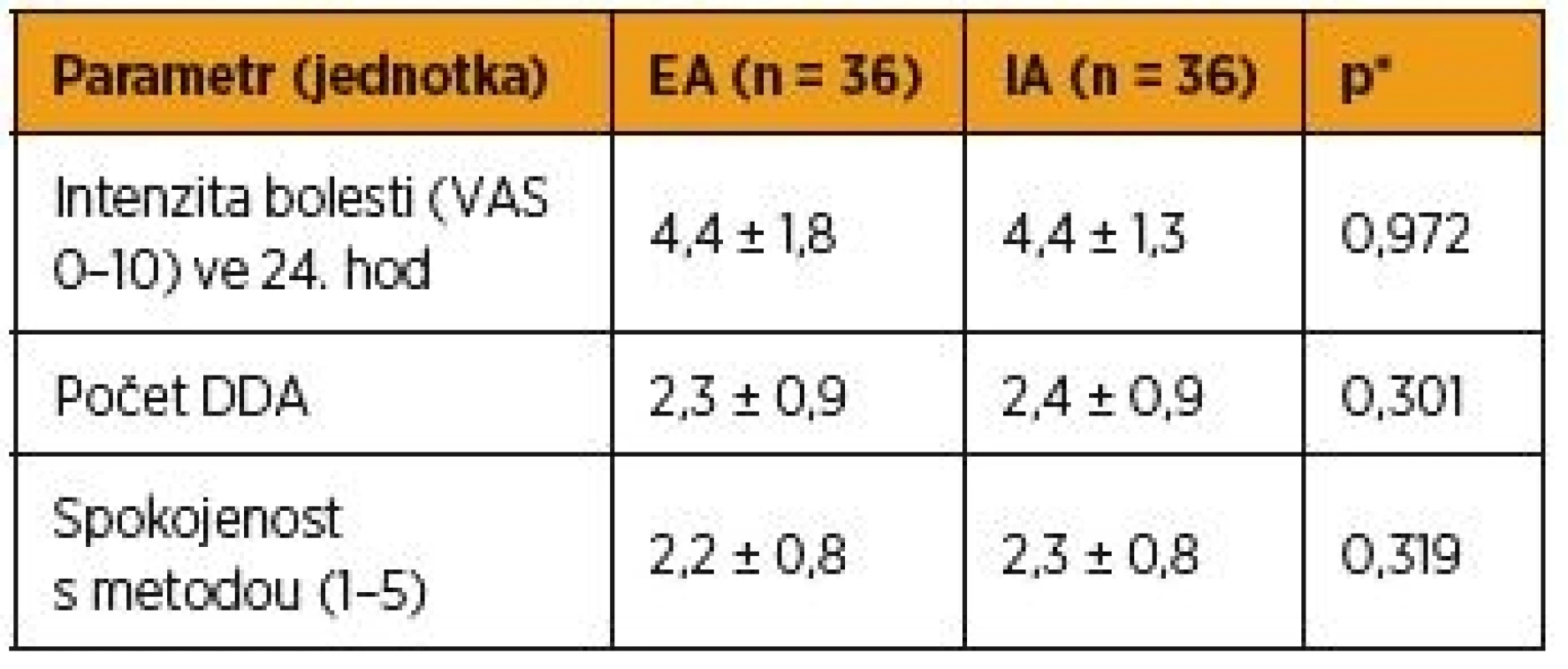
*Mannův-Whitneyho U test Tab. 3. Hodnocení výskytu nežádoucích účinků 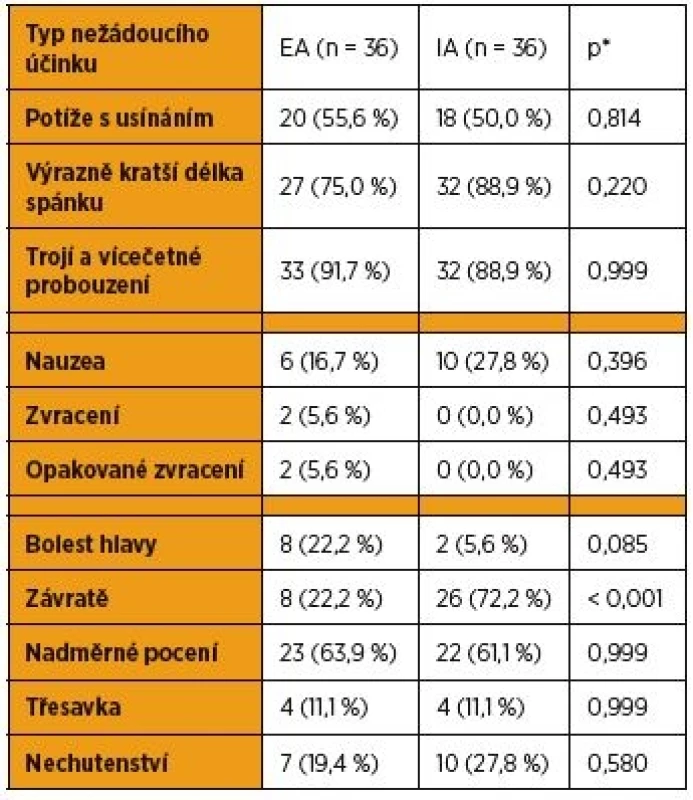
*Fisherův exaktní test DISKUSE
Nejdůležitějším zjištěním studie je, že účinnost incizionální analgezie po císařském řezu je srovnatelná s epidurální analgezií. Proto může být její použití metodou volby tam, kde epidurální katétr není zaveden (subarachnoidální a celková anestezie). Míra intenzity pooperační bolesti hodnocená stupnicí VAS v období 24 hodin po císařském řezu byla shodná ve srovnávaných skupinách epidurální i incizonální analgezie. Při srovnání počtu aplikovaných dodatečných dávek analgetik nebyl zaznamenán mezi oběma skupinami statisticky významný rozdíl. Hodnocení celkové spokojenosti pacientek s metodou analgezie bylo srovnatelné. Rozdíly v kvalitě spánku a výskytu nežádoucích účinků, jako nauzea, zvracení, bolesti hlavy, nadměrné pocení, třesavka a nechutenství, nebyly statisticky významné. Bylo zjištěno statisticky signifikantně více případů vertiga u žen s incizionální analgezií. Lze předpokládat, že i když celková denní dávka bupivakainu nepřekročila dávku maximální (byla však vyšší než u pacientek s EA), mohly se již projevit nežádoucí účinky lokálního anestetika, mezi které vertigo standardně patří. Limitujícím faktorem naší studie byla také velikost souboru 72 pacientek, výsledky mohou být ovlivněny malým počtem žen ve srovnávaných skupinách. Výhodou byla prospektivní metoda srovnání, kdy jsme vytvořili dva soubory rodiček, srovnatelných z hlediska věku, indexu tělesné hmotnosti a parity v termínovém těhotenství, a sledovali je v čase 24 hodin po porodu císařským řezem.
V literatuře byla publikována práce Ranta et al., která se zabývá srovnáním EA a IA v období 72 hodin po císařském řezu v souboru 40 pacientek. Hodnocení bolesti během prvních čtyř hodin po operaci ukázalo průměrnou intenzitu bolesti podle VAS ve skupině EA nižší. Ve 24 hodinách po operačním výkonu byla intenzita bolesti v obou skupinách srovnatelná. Výskyt nežádoucích účinků byl minimální [13]. V našem souboru 72 pacientek jsme hodnotili intenzitu bolesti pouze ve 24. hodině, kdy byla míra bolesti ve skupině EA i IA srovnatelná, tento výsledek koreluje s prací Ranta et al. Metaanalýzu devíti studií o celkovém počtu 505 pacientů srovnávající epidurální a incizionální analgezii v terapii bolesti po abdominálních operacích publikovali Ventham et al. Pacienti byli sledováni v období 48 hodin po operaci. V hodnocení stupně bolesti ve 24. a 48. hodině po operačním výkonu nebyl nalezen žádný signifikantní rozdíl mezi EA a IA [20]. Výsledky tedy korelují s našimi závěry.
Epidurální analgezie se řadí mezi nejúčinnější metody pooperační analgezie po císařském řezu [16, 18, 21]. Tato metoda je invazivní a technicky náročná. Její zavedení pouze z důvodu tlumení pooperační bolesti po císařském řezu není indikováno z důvodu možných komplikací. Je tedy omezena na pacientky, které jsou operovány ve svodné epidurální anestezii nebo EA vyžadují již během porodu. Zavedení EA je limitováno přítomností anesteziologa na porodním sále. Kontraindikací jsou poruchy koagulace, trombocytopenie, aplikace LMWH v posledních deseti hodinách, alergie na lokální anestetika, neléčená bakteriémie a infekční léze v místě vpichu. Relativní kontraindikací mohou být onemocnění mozku a míchy, těžké deformity páteře, silné bolesti hlavy a zad v anamnéze, obtížná spolupráce s rodičkou, případně technické aspekty – obezita, poúrazové stavy, tetování [4, 5]. Běžnou komplikací je hypotenze pacientky z blokády sympatiku [17]. Prevencí je včasná instilace krystaloidu 500–1000 ml i.v. Dalším rizikem je možnost perforace dura mater s aplikací lokálního anestetika do subdurálního prostoru (totální spinální anestezie) [11] nebo při pouhém poranění dura mater pak vznik postpunkční cefaley.
Incizionální analgezie v místě operační rány není přes svůj analgetický potenciál v porodnictví příliš využívána. Důvodem je nedostatek zkušeností s touto technikou, ekonomický aspekt a v neposlední řadě také absence vlastního Painfusoru na porodním sále. Její účinnost u císařského řezu také není jednoznačně podepřena recentně publikovanými pracemi, případně je i zpochybňována [8]. Hlavními výhodami této metody jsou redukce množství podaných analgetik a opiátů v časném pooperačním období, snížení výskytu průlomové bolesti, urychlení mobilizace a zkrácení doby hospitalizace. Nezvyšuje výskyt infekcí operační rány a nezhoršuje hojení [2, 6, 8]. V literatuře se setkáme i s aplikací NSA do oblasti operační rány, kde zabráněním vzniku hyperalgezie dochází ke snížené spotřebě opioidů v pooperačním období [4]. Subfasciální katétr Painfusor zavádí operatér sám v průběhu operačního výkonu. Je třeba, aby byl edukován v technice zavedení. Zavádění je technicky snadné. Nutnost nošení infuzoru snášely pacientky dobře. Využití obou metod lokální analgezie snižuje množství intravenózně podaných dávek analgetik v časném pooperačním období [20].
ZÁVĚR
Z uvedených výsledků vyplývá, že obě metody (EA i IA) jsou srovnatelné v efektivitě léčby bolesti, počtu užití dalších analgetik i z hlediska výskytu nežádoucích účinků. Systém incizionální analgezie v místě operační rány lze s výhodou využít u pacientek, které měly jiný typ anestezie než epidurální. Tedy všechny pacientky, které podstupují císařský řez, ať v subarachnoidální, nebo v celkové anestezii, by z této metody mohly profitovat.
Práce vznikla za podpory Ministerstva zdravotnictví ČR - RVO č. FNBr 65269705.
MUDr. Ivana Meixnerová
Gynekologicko-porodnická klinika
LF MU a FN
Jihlavská 20
625 00 Brno
e-mail: meixnerova.ivana@fnbrno.cz
Zdroje
1. Adamus, M., Herold, I., Trenkler, Š., et al. Klasifikace fyzického stavu nemocného podle ASA – dozrál čas na změnu? Anest intenz Med, 2007, 18, 1, s. 9–23.
2. Bianconi, M., Ferraro, L., Ricci, R., et al. The pharmacokinetics and efficacy of ropivacaine continuous wound instillation after spine fusion surgery. Anesth Analg, 2004, 98, 1, p. 166–172.
3. Bláha, J. Porodnická anestezie – Česká republika versus svět. Prakt Gynek, 2013, 17, 4, s. 287–292.
4. Bláha, J., Klozová, R., Nosková, P., et al. Současné postupy v porodnické anestezii V. – pooperační péče po císařském řezu. Anest intenz Med, 2015, 26, 2, s. 87–98.
5. Bláha, J., Kolníková, I., Nosková, P. Císařský řez, ale jaká anestezie? Prakt Gynek, 2011, 15, 3–4, s. 187–191.
6. Fredman, B., Shapiro, A., Zohar, E., et al. The analgesic efficacy of patient controlled ropivacaine instillation after Cesarean delivery. Anesth Analg, 2000, 91, 6, p.1436–1440.
7. Gabrhelík, T., Pieran, M. Léčba pooperační bolesti. Interní medicína pro praxi, 2012, 14, 1, s. 23–25.
8. Gottschalk, A., Burmeister, MA., Radtke, P., et al. Continuous wound infiltration with ropivacaine reduces pain and analgesic requirement after shoulder surgery. Anesth Analg, 2003, 97, 4, p. 1086–1091.
9. Hruban, L., Janků, P., Ventruba, P., et al. Vedení porodu po předchozím císařském řezu, analýza výsledků z let 2007–2010. Čes Gynek, 2012, 77, 2, s. 127–132.
10. Mach, D. Periferní nervové blokády: pro klinickou praxi včetně ultrazvukového navádění. Praha, Grada, 2010, s 178.
11. Nosková, P., Bláha, J., Klozová, R., et al. Postpunkční cefalea v porodnictví. Anest intenz Med, 2014, 25, 3, s. 194–202.
12. Novalgin Injekce, Státní ústav pro kontrolu léčiv. [online]. [cit. 2017-12-18]. Dostupné z: http://www.sukl.cz/download/spc/SPC14383.pdf.
13. Ranta, PO., Ala-Kokko, TI., Kukkonen, JE., et al. Incisional and epidural analgesia after caesarean delivery: a prospective, placebo controlled, randomized clinical study. Int J Obstet Anesth, 2006,15, p. 189–194.
14. Royakkers, AA., Willigers, H., van der Ven, AJ., et al. Catheter-related epidural abscesses – don‘t wait for neurological deficits. Acta Anaesthesiol Scand, 2002, 46, 5, p. 611–615.
15. Sekce perinatologie a fetomaternální medicíny, České gynekologické a porodnické společnosti. XXXIV. celostátní konference, 6.–8. 4. 2017, Karlovy Vary.
16. Štourač, P., Bláha, J., Klozová, R., et al. Anesthesia for cesarean delivery in the Czech Republic: a 2011 national survey. Anesth Analges, 2015, 120, 6, s. 1303–1308.
17. Štourač, P., Bláha, J., Nosková, P., et al. Současné postupy v porodnické anestezii IV. – anesteziologické komplikace u císařského řezu. Anest intenz Med, 2014, 25, 2, s. 123–134.
18. Štourač, P., Kuchařová, E., Křikava, I., et al. Establishment and evaluation of a post caesarean acute pain service in a perinatological center: retrospective observational study. Čes Gynek, 2014, 79, 5, s. 363–370.
19. Štourač, P., Seidlová, D., Bártíková, I., et al. Srovnání opioidní a neopioidní analgezie po císařském řezu v celkové anestezii – prospektivní observační studie. Anest intenz Med, 2014, 25, 1, s. 8–16.
20. Ventham, NT., Hughes, M., O‘Neill, S., et al. Systematic review and meta-analysis of continuous local anaesthetic wound infiltration versus epidural analgesia for postoperative pain following abdominal Sumery. Brit J Surg, 2013, 14, 9, p. 1280–1289.
21. Wu, CL., Cohen, SR., Richman, JM., et al. Efficacy of postoperative patient-controlled and continuous infusion epidural analgesia versus intravenous patient-controlled analgesia with opioids: a meta-analysis. Anesthesiology, 2005, 103, 5, p. 1079–1088
Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicína
Článek vyšel v časopiseČeská gynekologie
Nejčtenější tento týden
2018 Číslo 3- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Isoprinosin je bezpečný a účinný v léčbě pacientů s akutní respirační virovou infekcí
-
Všechny články tohoto čísla
- Jak dlouho přetrvává léčba mirabegronem u úspěšně léčených pacientů s hyperaktivním močovým měchýřem? Analýza multicentrické studie
- Význam hladin bazického fibroblastového růstového faktoru u pacientek s tumorem ovaria
- Ovlivňuje použití transferového média EmbryoGlue úspěšnost embryotransferu?
- Porovnání incizionální a epidurální analgezie v léčbě pooperační bolesti po císařském řezu
- Hodnocení sestupu a mobility uretrovezikální junkce u žen se stresovou inkontinencí moči – ultrazvuková studie
- Roboticky asistovaná laparoskopická abdominální cerkláž: dvě kazuistiky
- Primární maligní melanom pochvy, kazuistika a review z literatury
- Plánovaný domácí porod – Česká republika 2018
- Obezita a snížení plodnosti mužů
- Vakcinace proti HPV a výhled nových možností
- Potenciál survivínu pre liečbu gynekologických tumorových ochorení
- Prolaktin a poruchy reprodukce
- Zápis z jednání volební komise pro volby výboruSekce perinatologie a fetomaternální medicínyČeské gynekologické a porodnické společnosti ČLS JEP
- Zápis z jednání volební komise pro volby výboru Onkogynekologické sekce České gynekologické a porodnické společnosti ČLS JEP
- Česká gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Prolaktin a poruchy reprodukce
- Ovlivňuje použití transferového média EmbryoGlue úspěšnost embryotransferu?
- Vakcinace proti HPV a výhled nových možností
- Plánovaný domácí porod – Česká republika 2018
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



