-
Medical journals
- Career
Analýza a srovnání souborů nositelů implantabilního kardioverteru - defibrilátoru v primární a sekundární prevenci
Authors: L. Křivan; M. Kozák; M. Sepši; J. Vlašínová; P. Lokaj; J. Špinar
Authors‘ workplace: Interní kardiologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MU Dr. Jindřich Špinar, CSc., FESC
Published in: Vnitř Lék 2010; 56(2): 99-105
Category: Original Contributions
Overview
Cíl:
Cílem práce bylo provedení analýzy skupiny nemocných s primárně preventivní implantací (PP) kardioverteru ‑ defibrilátoru (ICD) v dlouhodobém sledování a porovnání výsledků s daty získanými u nemocných s implantací ICD v sekundární prevenci (SP).Soubor pacientů a metody:
Celkem bylo sledováno 73 pacientů s PP implantací a 138 nemocných s SP implantací. Převážnou většinu tvořili muži 88 % v PP a 78 % v SP s průměrným věkem 63 let. Většina nemocných trpěla ICHS jako základním srdečním onemocněním. Průměrná ejekční frakce levé komory (EF LK) byla 28 % u PP a 38 % u SP pacientů. Míra postižení koronárních tepen a doprovodná medikace byla u obou souborů obdobná. Byl porovnán výskyt přidružených onemocnění, výskyt maligních arytmií i nevhodné terapie, důvody rehospitalizací a přežívání pacientů.Výsledky:
Pacienti v souboru PP implantací měli nižší EF LK (p < 0,001), vyšší podíl revaskularizace koronárních tepen (p < 0,001), stejně tak nižší výskyt nevhodné terapie a arytmické bouře (p < 0,001). Ve skupině PP implantací byl vyšší výskyt nemocných s cukrovkou (p = 0,009), hyperlipidemie (p < 0,001) a cévního onemocnění mozku (p = 0,017). Přítomnost renální insuficience je spojena s vyšším rizikem úmrtí.Závěry:
Pacienti s primárně preventivní indikací ICD mají nižší EF LK a více přidružených onemocnění než nemocní léčení sekundárně preventivní implantací ICD. Jsou také častěji léčeni revaskularizací myokardu a mají nižší výskyt nevhodných terapií. Arytmická bouře se zdá být typickým rysem pro sekundárně preventivní ICD implantace.Klíčová slova:
implantabilní kardioverter ‑ defibrilátor – primární prevence – sekundární prevence – nevhodná terapie – náhlá smrtÚvod
V roce 1980 byl poprvé implantován kardioverter-defibrilátor (ICD) pacientovi s vysokým rizikem náhlé srdeční smrti (NSS) [1]. Multicentrické studie následujících let prokázaly jednoznačný profit z ICD u pacientů v sekundární prevenci. Podle doporučení České kardiologické společnosti byly v letech 1994 – 2005 prováděny implantace ICD pouze u nemocných, kteří již prodělali maligní arytmii a byli úspěšně resuscitováni. Od roku 2005 vstoupila v platnost v ČR nová doporučení umožňující indikovat k implantaci i nemocné, kteří dosud maligní arytmii neprodělali, ale jsou ve vysokém riziku NSS. Jednalo se o nemocné po infarktu myokardu (IM) s ejekční frakcí levé komory (EF LK) pod 35 % a přítomností nesetrvalých komorových tachykardií (NSKT). Tito nemocní byli podrobeni programované stimulaci komor (PSK), a pokud byl výsledek pozitivní, byli indikováni k implantaci ICD [2]. V období let 2005 – 2008 bylo na Interní kardiologické klinice LF MU a FN Brno Bohunice implantováno ICD u 73 pacientů z primárně preventivní indikace. Jednalo se převážně o nemocné s ischemickou chorobou srdeční (ICHS). Naším cílem bylo analyzovat základní charakteristiky souboru nemocných s primárně preventivní implantací ICD a porovnat je s historickými daty souboru pacientů implantovaných ze sekundárně preventivních důvodů.
Metody
U všech pacientů jsme v léčbě a sledování postupovali podle jednotného protokolu. Nemocní měli před implantací ICD provedeno echokardiografické vyšetření se stanovením EF LK, selektivní koronarografií (SKG) s posouzením významnosti postižení koronárního řečiště a snahou o maximální možnou revaskularizaci. Podle výsledku byli rozděleni do skupin s postižením jedné, dvou a více tepen. U všech nemocných bylo provedeno základní elektrofyziologické vyšetření se stanovením převodních parametrů, vyloučením přítomnosti supraventrikulární reentry tachykardie a PSK. Zaznamenali jsme doprovodnou antiarytmickou medikaci a doprovodná onemocnění (diabetes – DM, hypertenzi, ischemickou chorobu dolních končetin – ICHDKK, cévní onemocnění mozku – COM, hyperlipoproteinemii – HLP a renální insuficienci s retencí N látek s kreatininem převyšujícím 120 μmol/ l). Protokol implantací ICD se řídil podle standardních zvyklostí, vždy bylo provedeno 2krát testování defibrilačního prahu šokovou energií o 10 J nižší než maximum přístroje. Po propuštění byli pacienti sledováni v 3 - nebo 6měsíčních intervalech podle klinického stavu. Při kontrolách ICD vždy proběhla analýza epizod arytmií z paměti ICD s rozdělením na adekvátní a nevhodnou terapii. U adekvátní terapie byla stanovena frekvence arytmie, způsob terapie ICD a počet arytmických epizod. Sledovali jsme dobu od implantace do první udělené adekvátní terapie. Zaznamenávali jsme případné rehospitalizace pacientů, jejich počet a příčinu. Takto získaná data jsme posléze porovnali s údaji staršího souboru nemocných z let 1994 – 2001, kteří byli indikováni k implantaci ICD ze sekundárně preventivních důvodů. Oba soubory nemocných se nepřekrývají, vychází z jednoho pracoviště. Data jsou získána podle stejného protokolu. Implantace i kontroly ICD prováděli u obou souborů nemocných stejní lékaři.
Statistické metody
Pro popis souboru byly použity základní deskriptivní statistické metody. Spojitá data jsou prezentována jako průměr ± směrodatná odchylka.
Pro srovnání dvou skupin pacientů (PP vs SP, zemřelí vs žijící) v kategoriálních proměnných se dvěma kategoriemi byl použit Fisherův test, pro proměnné s více kategoriemi M - L χ2 test. V případě srovnávání spojitých proměnných, mezi dvěma skupinami pacientů splňujících předpoklad normálního rozložení byl použit t test, při porušení tohoto předpokladu neparametrický Mann Whitney test.
Pro celkové přežití pacientů a dobu do 1. terapie maligní arytmie byl použit Kaplan - Meierův odhad křivky přežití. Pro srovnání přežití mezi jednotlivými skupinami pacientů byl použit log rank test. Relativní riziko úmrtí (RR) mezi dvěma skupinami pacientů bylo stanoveno použitím Coxova regresního modelu. Veškeré statistické testy byly provedeny na hladině významnosti α = 0,05.
Soubor nemocných
Ve sledovaném období byl ICD implantován 73 pacientům z primárně preventivních (PP) důvodů. Jednalo se o 64 mužů a 9 žen průměrného věku 63,5 ± 9,4 roku. Jednodutinový ICD mělo 29 (39,7 %), dvoudutinový ICD 16 (21,9 %) a resynchronizační terapii 28 (38,4 %) pacientů. Medián sledování byl 17,45 měsíců.
Skupina nemocných, kteří byli indikováni k ICD ze sekundárně preventivních (SP) důvodů v letech 1994 – 2001, měla 138 pacientů. Jednalo se o 108 (78,3 %) mužů a 30 (21,7 %) žen se smíšenou etiologií srdečního onemocnění (ICHS, dilatační kardiomyopatie – DKMP, arytmogenní kardiomyopatie pravé komory – ARVC, syndrom dlouhého QT – LQT), i pacienty bez zjištěné organické příčiny arytmií. Průměrný věk nemocných byl 62,0 ± 12,7 let. Průměrná EF LK byla 38 %. Medián sledování byl 47,35 měsíců (tab. 1).
Table 1. Obecná charakteristika souborů. 
Výsledky
V následujícím textu jsou uváděny výsledky získané analýzou nového souboru pacientů s PP implantací ICD. V tabulkách jsou pro srovnání vždy uváděny odpovídající údaje získané u souboru s SP indikací.
Průměrná EF LK byla v našem souboru28,0 ± 6,4 %. 69 nemocných (94,5 %) trpělo ICHS, u 4 nemocných (5,5 %) se jednalo o koincidenci ICHS a DKMP. Postižení koronárních tepen, revaskularizace, doprovodná onemocnění a medikace jsou zaznamenány v tab. 2 a tab. 3.
Table 2. Postižení koronárních tepen, revaskularizace a medikace. 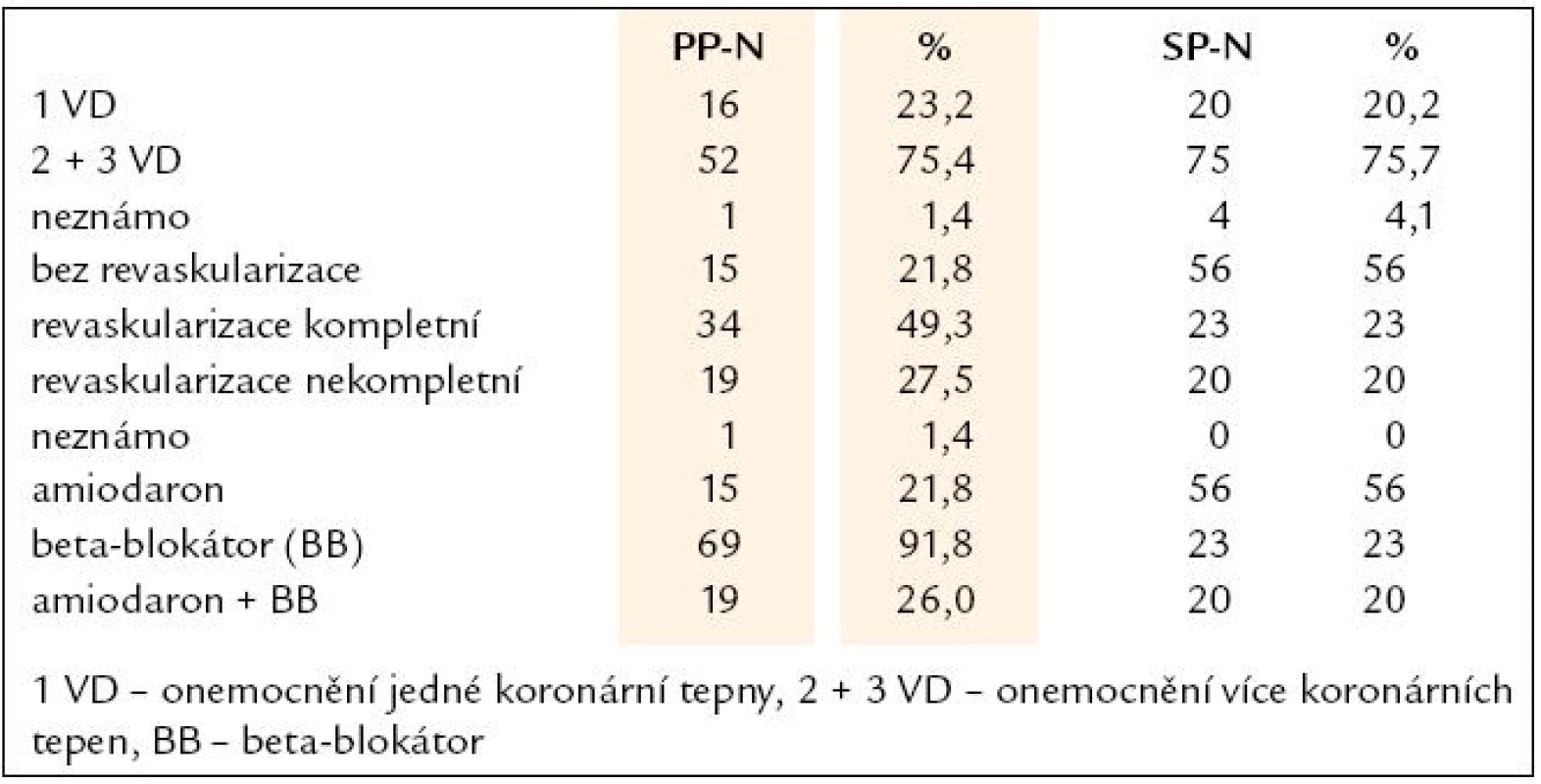
Table 3. Doprovodná onemocnění. 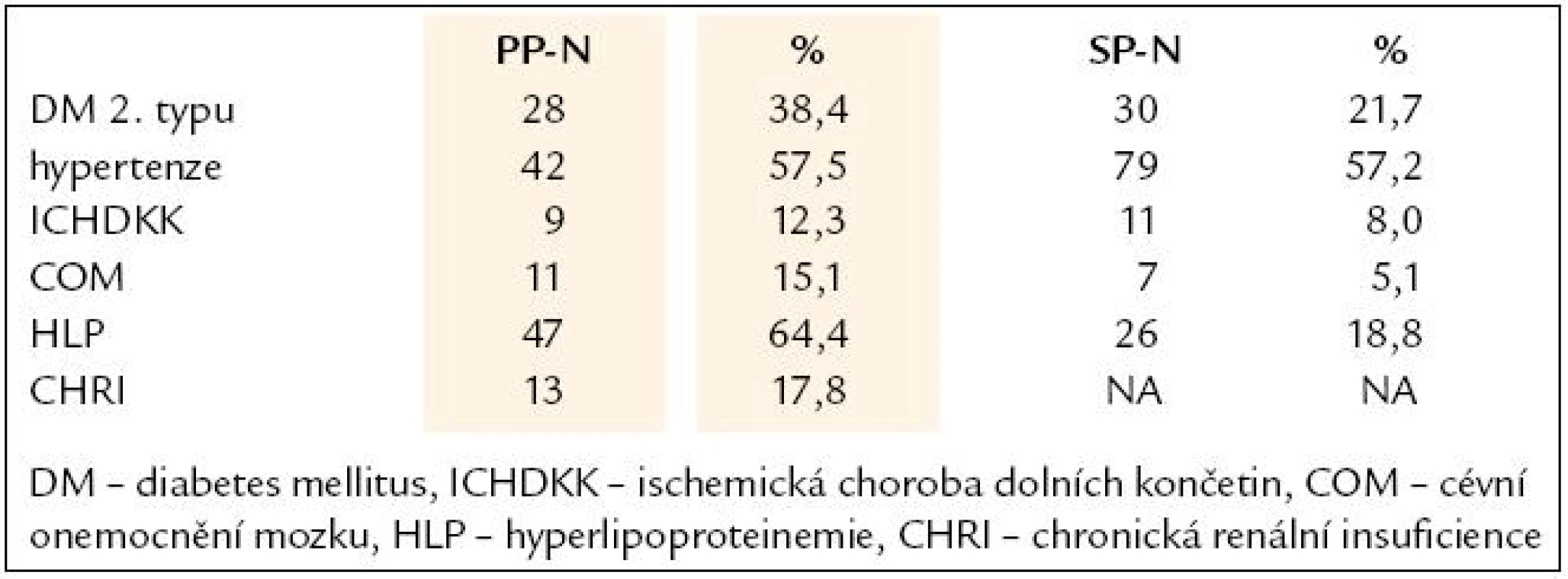
V zastoupení antiarytmické terapie převažoval beta blokátor a amiodaron. Tyto dva léky byly také nejčastější antiarytmickou kombinací u 19 (26,0 %) nemocných. Nejčastějšími přidruženými onemocněními byla HLP a hypertenze. Bez přidružených onemocnění byli pouze 3 (4,1 %) pacienti. Nejčastěji se vyskytovala souběžně dvě přidružená onemocnění (37,0 % pacientů).
V průběhu sledování byla zaznamenána maligní arytmie u 19 (26 %) pacientů. Z toho komorová tachykardie u 17 (23,3 %) pacientů. 54 (74 %) nemělo žádnou maligní arytmii. Minimální počet KT byl 1 u osmi pacientů a maximální byl 78 epizod jednoho nemocného. Průměrná TF KT byla 199/ min. Frekvence KT > 200/ min byla zaznamenána u 8 (47,1 %) pacientů. U 7 nemocných (41,2 %) byla tepová frekvence KT < 200/ min a u 2 zbývajících pacientů se frekvenci KT nepodařilo zjistit. 4 pacienti (5,5 %) prodělali fibrilaci komor, 2 z nich však měli současně i komorovou tachykardii. Nesetrvalé komorové tachykardie se vyskytly u 16 (21,9 %) pacientů. Arytmická bouře byla zaznamenána pouze u 1 pacienta (tab. 4 a 5).
Table 4. Zastoupení jednotlivých typů arytmie. 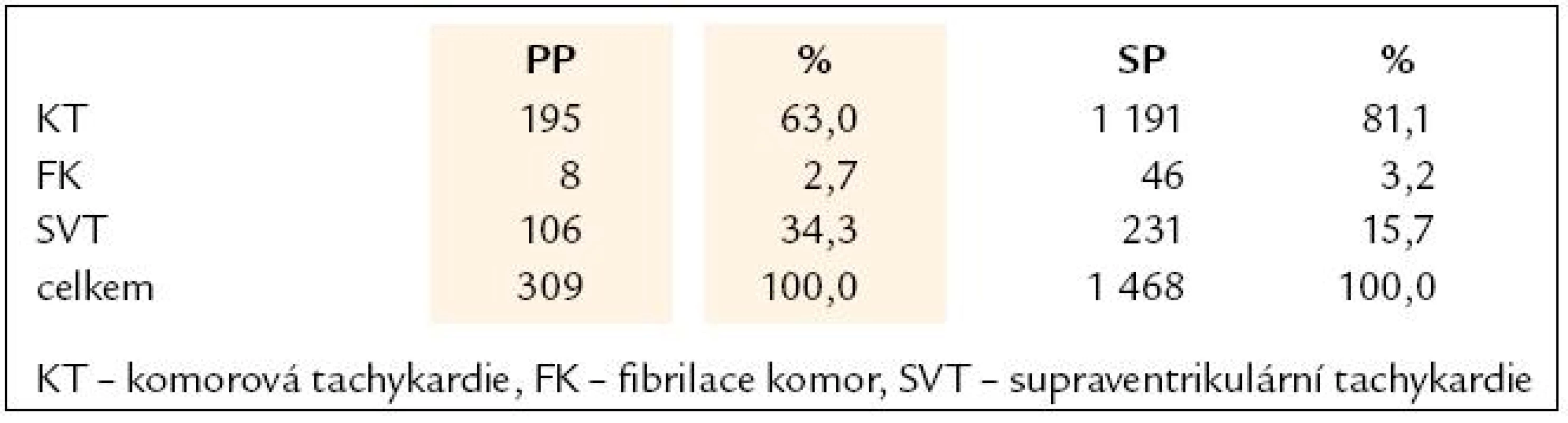
Table 5. Výskyt nevhodné terapie a arytmické bouře. 
Supraventrikulární tachykardie detekovaná přístrojem v pásmu KT se vyskytla celkem u 18 (24,7 %) pacientů. Průměrná tepová frekvence těchto tachykardií byla 163,1/ min. 11 nemocných (15 %) mělo výskyt SVT i maligní arytmie. Nevhodná terapie způsobená SVT byla zaznamenána pouze u 7 (9,6 %) pacientů. Nejvyšší počet nevhodných terapií u jednoho pacienta byl 28. Nevhodná terapie byla udělena průměrně ve 21,3 % případů výskytu SVT. U 2 pacientů byla nevhodná terapie při všech výskytech SVT (tab. 5).
Dobu od primoimplantace do 1. léčby maligní arytmie bylo možno stanovit u 72 pacientů. Medián doby do 1. léčby maligní arytmie nebylo možné stanovit. 25% percentil doby do 1. léčby maligní arytmie byl 24,5 měsíců. Kumulativní podíl pacientů bez léčby maligní arytmie po jednom roce sledování byl 90 %.
U pacientů nebyl prokázán statisticky významný rozdíl v celkovém přežití pacientů podle počtu postižených tepen (p = 0,428). Nebyl prokázán statisticky významný rozdíl v celkovém přežití pacientů podle výskytu komorové tachykardie (p = 0,363) ani podle výskytu nesetrvalé komorové tachykardie (p = 0,444) (grafy 1, 2 a 3).
Graph 1. Přežívání podle počtu postižených tepen. 
Graph 2. Přežívání podle výskytu komorové tachykardie. 
Graph 3. Přežívání podle výskytu NSKT. 
Celkem bylo zaznamenáno 47 rehospitalizací u 25 (34,2 % sledovaných) pacientů.
Tab. 6 ukazuje příčiny rehospitalizací. Z důvodu srdečního onemocnění (AKS, progrese srdečního selhání či arytmické bouře) to bylo 19 rehospitalizací, 2 byly z důvodu komplikací způsobených ICD a 26 příčin bylo nekardiálních (tab. 6).
#tab:6#
Celková doba přežití (OS) byla stanovena jako doba od primoimplantace do úmrtí nebo do 30. 4. 2009 v případě cenzorovaných pacientů. V průběhu sledování zemřelo 11 pacientů, u jednoho nemocného nebylo možné stanovit, zda zemřel, 61 bylo k datu hodnocení žijících. Kumulativní podíl přežívajících po 1 roce byl 94 %, po 2 letech 91 %, po 3 letech 87 % a ve 4 letech 83 %.
Mezi skupinami žijících a zemřelých pacientů nebyl nalezen statisticky významný rozdíl ve výskytu přidružených onemocnění HT, DM, COM, HLP a ICHDKK (p = 0,914). Pacienti s renální insuficiencí mají statisticky významně vyšší riziko úmrtí než nemocní bez renální insuficience (p = 0,015, RR = 5,02) (graf 4).
Graph 4. Přežívání pacientů s renální insuficiencí. 
Srovnání souborů ICD nositelů v PP a SP
Z obecných charakteristik souboru je patrné, že v PP je zastoupení žen téměř poloviční než v SP, nicméně tento rozdíl není statisticky významný (p = 0,135). Soubory se neliší průměrným věkem. V souboru PP nemocných je významně nižší EF LK (p < 0,001). Postižení koronárních tepen je u obou souborů obdobné, avšak počet revaskularizovaných pacientů je ve skupině PP statisticky významně vyšší (p < 0,001). V doprovodné antiarytmické medikaci převažuje u souboru SP amiodaron, zatímco u PP nemocných je to beta blokátor. V souboru PP byl statisticky významně vyšší výskyt přidružených onemocnění DM (p = 0,009), HLP (p < 0,001) a COM (p = 0,017). Ve výskytu ICHDKK a hypertenze nebyl významný rozdíl. Výskyt renální insuficience nebyl u historického souboru SP hodnocen, proto jsme porovnání provést nemohli. V souboru PP implantací byl zaznamenán statisticky významně nižší výskyt nevhodné terapie i arytmické bouře (p < 0,001).
Diskuze
Oba soubory nemocných se významně nelišily věkem. Rozdílné bylo však zastoupení jednotlivých druhů srdečního onemocnění. Ve skupině SP sice převažovala ICHS jako etiologie maligních arytmií, avšak téměř 30 % nemocných trpělo jiným onemocněním (DKMP, ARVC, LQT syndrom apod.). Skupina pacientů s PP implantací naproti tomu byla uniformní, jednalo se pouze o nemocné s ICHS po prodělaném IM. S tím souvisí i významně nižší průměrná EF LK nemocných v PP. Průměrná EF LK byla v našem souboru 28 %. Je to méně, než udávají doporučení pro PP implantace, kde je stanovena hranice EF LK ≤ 35 %. Tato nižší hodnota koresponduje s reálnou EF LK zjištěnou v primárně preventivních ICD studiích MADIT I – 26 %, MADIT II – 23 %, MUSTT – 29 % [3].
Přidružená onemocnění neměla ve skupině PP vliv na přežívání pacientů, s výjimkou renální insuficience, která signifikantně více než 5krát zvyšuje riziko úmrtí. Literatura uvádí, že nejsilnější rizikové faktory pro úmrtí u pacientů s implantovaným ICD v rámci primární prevence jsou: renální insuficience, věk nad 70 let, EF LK pod 20 %, NYHA klasifikační třída III – IV, přítomnost fibrilace síní a diabetes mellitus [4]. Při porovnání skupin PP a SP implantací je v prvně jmenované významně vyšší výskyt hyperlipoproteinemie, diabetu a onemocnění mozkových tepen. Ačkoliv je u těchto nemocných vyšší procento revaskularizovaných pacientů, lze předpokládat difuznější postižení koronárních tepen, které je ovlivněno přidruženými chorobami.
Výskyt maligní arytmie nebyl v našem souboru spjat se zvýšenou mortalitou pacientů, jak naznačují některé údaje. Ve studii DINAMIT byli léčeni pomocí ICD pacienti s nedávno proběhlým IM (6 – 40 dní) a EF LK < 30 % s nálezem nízké variability srdeční frekvence. Redukce náhlé smrti o 58 % pomocí ICD byla bohužel negativně vyvážena vzestupem „nearytmické“ smrti v ICD větvi. Velmi silným predikátorem takového úmrtí byl výskyt adekvátní ICD terapie [5]. V našem souboru nebyl výskyt setrvalé komorové tachykardie, a tedy adekvátní terapie z ICD spojen s vyšším rizikem úmrtí. Některé práce prokazují, že samotný výskyt komorové tachykardie, nesetrvalé i setrvalé, nemusí být spojen s vyšším rizikem úmrtí [6].
Délka sledování, ve kterém bude mít 25 % pacientů s PP implantací alespoň jednu adekvátní ICD terapii, v našem souboru těsně přesahuje 2 roky. V prodlouženém sledování, které by odpovídalo průměrné životnosti ICD (4 – 5 let), lze tedy očekávat další zvýšení počtu adekvátně léčených pacientů. V literatuře se vyskytují údaje o pozdním výskytu maligní arytmie po IM, které dokumentují zvyšující se profit z implantace ICD v závislosti na délce sledování [3]. Tento trend narůstajícího výskytu maligní arytmie v průběhu sledování souvisí patrně s dlouhodobou elektrickou remodelací srdce a progresí ICHS [7].
V našem souboru bylo celkem zaznamenáno 309 arytmických epizod. Více než třetinu přístroje klasifikovaly jako SVT. Z této skupiny 106 SVT byla v 21 % případů udělena nevhodná terapie. Celkem prodělalo nevhodnou terapii 7 pacientů (9,6 %). Srovnání těchto údajů u souborů SP a PP implantací je problematické, protože neznáme počet všech supraventrikulárních arytmií, které pacienti prodělali. Navíc starší typy přístrojů nebyly vybaveny monitorovací zónou či ukládáním záznamů neléčených SVT do paměti. Počet pacientů, kteří prodělali NT, byl však v souboru nemocných s PP implantací významně nižší. Kreuz et al udává výskyt NT u 9 % epizod a 18 % pacientů splňujících MADIT II kritéria při současném výskytu adekvátní terapie u 50 % nemocných v průběhu 33 měsíců sledování [8]. Důvodem může být kratší doba sledování PP souboru i sofistikovanější algoritmy k potlačení nevhodné terapie, kterými jsou moderní ICD vybaveny. Významnou roli v redukci nevhodné terapie a arytmických bouří patrně hraje i vyšší procento revaskularizace u PP skupiny [9,10] a zejména vysoký podíl beta blokátorů v doprovodné medikaci. Beta blokátory nejen snižují výskyt supraventrikulárních arytmií, ale u fibrilace síní jako hlavní příčiny nevhodné terapie zpomalují převod atrioventrikulárním uzlem a brání dosažení vysoké komorové frekvence. Vliv beta blokátorů na snížení celkové i arytmické mortality u pacientů s ICHS je znám dlouhodobě.
Při sledování rehospitalizací je patrný trend k poklesu počtů rehospitalizovaných pacientů z důvodu srdečního selhání, akutního koronárního syndromu nebo arytmické bouře. Tento pokles je „vyvážen“ nárůstem hospitalizací z nekardiálních důvodů. Svou roli v tom zřejmě hraje významně vyšší výskyt některých přidružených onemocnění v PP souboru (viz výše).
Přežívání nemocných s ICD v našem souboru bylo srovnatelné s velkými multicentrickými studiemi. V našem souboru pacientů s PP implantací bylo přežívání v 1. roce 94 % a ve 3 letech 87 %. Ve studii SCD - HeFT to bylo 94 %, resp. 83 %, a ve studii MADIT II 91 %, resp. 78 % [11,12]. Vysoký počet přežívajících pacientů je umožněn díky komplexní péči o rizikové nemocné, kam patří revaskularizace u většiny pacientů s ICHS, léčba srdečního selhání a v neposlední řadě odvrácení arytmické náhlé smrti pomocí ICD.
Hodnocení efektivity ICD terapie bývá založeno na počtu adekvátních ICD terapií. Toto číslo však není totožné s počtem zachráněných životů. Některé komorové tachykardie správně léčené ICD by totiž nemusely vést k fatálním následkům a úmrtí pacienta. V některých případech je i samotná přítomnost ICD proarytmickým faktorem [13]. Lze však předpokládat, že u pacientů léčených ICD pro rychlou komorovou tachykardii (> 250/ min) by byla mortalita vysoká a u nemocných léčených pro fibrilaci komor téměř 100% při předpokládané účinnosti kardiopulmonální resuscitace v terénu 1 – 5 % [14]. V našem souboru prodělalo maligní arytmii léčenou adekvátní ICD terapií celkem 26 % nemocných. Z této skupiny mělo 7 pacientů, tj. 9,6 %, buď fibrilaci komor, nebo KT s frekvencí nad 250/ min. Lze tedy konstatovat, že i za krátkou dobu sledování byla již odvrácena náhlá arytmická smrt u zhruba 10 % našich nemocných.
Závěry
- Pacienti s primárně preventivní indikací ICD mají nižší EF LK a více přidružených onemocnění než nemocní léčení sekundárně preventivní implantací ICD.
- Jsou častěji léčeni revaskularizací myokardu a mají nižší výskyt nevhodných terapií.
- Arytmická bouře je typickým rysem pro sekundárně preventivní ICD implantace.
- Renální insuficience je rizikovým faktorem úmrtí.
Současné implantabilní defibrilátory jsou z pohledu primární prevence bezpečné s malým výskytem nevhodné terapie a při 5leté odhadované životnosti přístrojů lze počítat i s vysokou efektivitou v léčbě maligních komorových dysrytmií. Celkové přežívání pacientů s ICD v PP je i po 4 letech vysoké. Nedílnou součástí léčby pacientů s vyšším rizikem NSS je komplexní farmakoterapie, zejména užití beta blokátorů.
Limitace
Jistou limitací naší práce je kratší délka sledování u skupiny nemocných s PP indikací ICD. Určitým problémem se může jevit srovnání souborů sledovaných v různém období. Na druhé straně se jedná vždy o nemocné z jednoho pracoviště, kteří byli léčeni a sledováni stejným týmem lékařů, podle jednotného protokolu a zvyklostí.
MUDr. Lubomír Křivan, Ph.D.
www.fnbrno.cz
e-mail: lkrivan@fnbrno.czDoručeno do redakce: 25. 9. 2009
Přijato po recenzi: 4. 11. 2009
Sources
1. Mirowski M, Reid P, Mower M et al. Termination of malignant ventricular arrhythmias with an implanted automatic defibrillator in human beings. N Engl J Med 1980; 303 : 322 – 324.
2. Táborský M. Zásady pro implantace kardiostimulátorů, ICD a SRL. Cor Vasa 2005; 47 : 59 – 68.
3. Dorian P, Takajíc M, Tang A. Implantable cerdioverter defibrillators for the prevention of sudden death. Can J Cardiol 2005; 21 (Suppl A): 31A – 36A.
4. Goldenberg I, Vyas AK, Hall WJ et al. Risk stratification for primary implantation of a cardioverter defibrillator in patients with ischemic left ventricular dysfunction. J Am Coll Cardiol 2008; 51 : 288 – 296.
5. Dorian P, Connolly SJ, Hohnloser SH et al. On behalf of the DINAMIT investigators. Why don’t ICDs decrease all‑cause mortality after MI? Insights form the DINAMIT study. Circulation 2004; 110 (Suppl III): III – 502.
6. Chow T, Kereiakes DJ, Onufer J et al. Does Microvolt T - Wave Alternans Testing Predict Ventricular Tachyarrhythmias in Patients With Ischemic Cardiomyopathy and Prophylactic Defibrillators? The MASTER (Microvolt T Wave Alternans Testing for Risk Stratification of Post‑Myocardial Infarction Patients) Trial. J Am Coll Cardiol 2008; 52 : 1607 – 1615.
7. Passman R, Kadish A. Sudden death prevention with implantable device. Circulation 2007; 116 : 561 – 571.
8. Kreuz J, Balta O, Liliegren N et al. Incidence and characteristics of appropriate and inappropriate therapies in recipients of ICD implanted for primary prevention of sudden cardiac death. PACE 2007; 30: S125 – S127.
9. Hutyra M, Skála T, Kamínek M et al. Význam stanovení viability myokardu před revaskularizací u pacientů s ischemickou kardiomyopatií a systolickou dysfunkcí levé komory srdeční. Vnitř Lék 2008; 54 : 395 – 401.
10. Toman O, Poloczek M, Pařenica J et al. Ischemická choroba srdeční s předčasnou manifestací u mladých pacientů. Vnitř Lék 2008; 54 : 810 – 816.
11. Kenji A, Yoshimitsu S, Masahiko G et al. Long term clinical follow up of japanese heart failure patients received ICD therapy dor primary prevention of sudden cardiac death. J Card Fail 2008; 14: S140 – S141.
12. Stiles S. ALTITUDE: Survival with primary prevention ICDs better than ever in remotely monitored „real - world“ population. www.mespe.net/ .../ 01 ICD in primary prevention.pdf.
13. Křivan L, Kozák M, Sepši M et al. Specifické komplikace terapie implantabilními kardiovertery defibrilátory. Čas Lék Čes 2004; 143 : 521 – 525.
14. Zhi - Jie Z, Drift JB, Gilda WH et al. Sudden cardiac death in the United States, 1988 – 1998. Circulation 2001; 104 : 2158 – 2163.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2010 Issue 2-
All articles in this issue
- Výskyt revmatických manifestací a orgánově nespecifické autoimunity u nemocných s autoimunitní tyreopatií – editorial
- Několik poznámek k problematice infikovaného myxomu – editorial
- Analýza a srovnání souborů nositelů implantabilního kardioverteru- defibrilátoru v primární a sekundární prevenci
- Výskyt reumatických manifestácií a orgánovo nešpecifickej autoimunity u chorých s autoimunitnou tyreopatiou
- Probiotika u akutní pankreatitidy – randomizovaná, placebem kontrolovaná, dvojitě slepá studie
- Rizika dlouhodobé antisekreční terapie
- Přímý inhibitor reninu aliskiren v léčbě kardiovaskulárních a renálních onemocnění
- Endokanabinoidní systém a ovlivnění trombogeneze
- Antitrombotická terapie v graviditě
- Centrální diabetes insipidus u dospělých osob – první příznak histiocytózy z Langerhansových buněk a Erdheimovy‑Chesterovy choroby. Popis tří případů a přehled literatury
- Kazuistika mladého pacienta s konstriktivní perikarditidou se subakutním průběhem
- Infikovaný myxom jako příčina akutní infekční endokarditidy
- Přehodnocení doporučení pro diagnostiku a léčbu hypertenze
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Centrální diabetes insipidus u dospělých osob – první příznak histiocytózy z Langerhansových buněk a Erdheimovy‑Chesterovy choroby. Popis tří případů a přehled literatury
- Rizika dlouhodobé antisekreční terapie
- Kazuistika mladého pacienta s konstriktivní perikarditidou se subakutním průběhem
- Přímý inhibitor reninu aliskiren v léčbě kardiovaskulárních a renálních onemocnění
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

