-
Medical journals
- Career
Sarkoidóza – systémová nemoc. Co je nového?
Authors: M. Vašáková; M. Šterclová; J. Anton
Authors‘ workplace: Primářka: MUDr. Martina Vašáková, Ph. D. ; Fakultní Thomayerova nemocnice s poliklinikou, Praha ; Přednostka: MUDr. Václava Bártů ; Pneumologická klinika 1. LF UK
Published in: Prakt. Lék. 2008; 88(4): 208-212
Category: Various Specialization
Overview
Sarkoidóza, ačkoli obvykle vnímaná jako plicní onemocnění, je klasickou systémovou nemocí. Etiopatogeneticky je charakterizována tvorbou nekazeifikujících granulomů, které mohou postihovat většinu orgánů v těle, některé klinicky manifestně a některé asymptomaticky. Kromě orgánově specifických manifestací má sarkoidóza i imunopatologické a metabolické projevy. Jedním z nejobtížněji ovlivnitelných systémových symptomů sarkoidózy je chronická únava. Obecně lze říci, že prognosticky jsou příznivější formy sarkoidózy s akutní manifestací s převahou v plicích, kdy dochází často ke spontánní regresi onemocnění, horší prognózu mají formy onemocnění chronické, plíživé a formy se závažným mimoplicním postižením, hlavně srdečního svalu a centrálního nervového systému. Léčba sarkoidózy spočívá v podávání středních dávek kortikoidů, alternativou léčby jsou antimalarika a imunosupresiva. V některých případech je nově zkoušena léčba biologická, zaměřená proti TNF-alfa mediované imunopatologické odpovědi.
Klíčová slova:
sarkoidóza, granulomy, multiorgánové postižení, prognóza, léčba.Úvod
Sarkoidóza je multisystémové granulomatózní onemocnění nejasné etiologie. Obvykle postihuje nemocné mladého a středního věku a projevuje se nejčastěji nitrohrudním postižením s bilaterální hilovou lymfadenopatií, někdy i s plicními infiltráty, z mimoplicních lokalizací pak nejčastěji očními a kožními lézemi. K dalším postižený orgánům patří játra, slezina, lymfatické uzliny, slinné žlázy, srdce, nervový systém, svaly a kosti, ale mohou být postiženy i další orgány (12) (tab. 1)
Kožní léze způsobené sarkoidózou byly popsány poprvé v roce 1877 Jonathanem Hutchinsonem, v roce 1889 Caesar Besnier zveřejnil popis lupus pernio, Osler popsal 1898 postižení slzných a příušních žlaz, 1904 byly Kreibichem publikovány cystické kostní změny v kontextu s lupus pernio, Heerfordt zachytil v roce 1909 uveitidu a parotitidu způsobenou sarkoidózou, multisystémové postižení (kůže, lymfatické uzliny, kosti, plíce) uveřejnil poprvé Schaumann v roce 1914 pod názvem benigní lymfogranulomatóza a rok poté popsali multisystémové postižení také Bittorf a Kuznitzky.
Epidemiologie sarkoidózy
Prevalence sarkoidózy se značně liší mezi jednotlivými regiony, od méně než jednoho případu na 100 000 obyvatel až ke 40/100 000 obyvatel. V České republice je prevalence této nemoci 10/100 000 obyvatel. Česká republika patří k zemím s čas-tějším výskytem sarkoidózy, tak jako ostatní země Střední Evropy, skandinávské země, Spojené státy americké a Japonsko. Méně častá je v jněkterých asijských zemích, ve Střední a Jižní Americe a Africe.
Nejzávažnějšími formami onemocnění trpí Afroameričané, kavkazská rasa mívá častěji asymptomatický průběh onemocnění. Mortalita všech forem sarkoidózy je 1–5 %.
Nejčastěji nemoc postihuje nemocné ve 3. a 4. dekádě života, a to častěji ženy než muže, nekuřáky spíše než kuřáky (7).
Etiopatogeneze sarkoidózy
Etiologie sarkoidózy je stále neznámá. Je však velmi pravděpodobné, že nemoc se vyvíjí po expozici specifickým antigenům zevního prostředí u geneticky náchylných jedinců. Jako podezřelé zevní antigeny byly v souvislosti se sarkoidózou zmiňovány nejčastěji tyto noxy:
- mykobakteria,
- Propionebacter acne,
- berylium,
- pyly stromů,
- zplodiny hoření,
- insekticidy,
- plísně.
Po stránce genetické je náchylnost k sarkoidóze a sklon k chronicitě onemocnění významně ovlivněn variabilitou v oblasti genu pro molekuly HLA I. a II. třídy. Také některé formy nemoci, jako je kupříkladu Lofgrenův syndrom, jsou vázané na určitý typ HLA alel. Hypotézu o genetické podmíněnosti sklonu k sarkoidóze podporují i rodinné studie a studie ACCESS (Case Control Etiologic Sarcoidosis Study), kde byla prokázána u pacientů se sarkoidózou 5 krát vyšší četnost stejného onemocnění u pokrevních příbuzných v porovnání se zdravou populací (13).
Sarkoidóza je charakterizována imunopatologicky nahromaděním aktivovaných TH1 lymfocytů a makrofágů v cílových orgánech nebo systémech, a to hlavně v plicích. To podporuje hypotézu o imunopatologické TH1 odpovědi na specifické antigeny, během které se uvolňují ve zvýšené míře TH1 cytokiny, a to hlavně interleukin-2 (IL-2) a interferon-gamma (IFN-gamma) a dochází ke zvýšené proliferaci imunokompetentních B buněk, a tím i ke zvýšené produkci imunoglobulinů. Tyto procesy jsou podkladem pro typický laboratorní imunologický obraz u sarko-idó-zy, kdy v postižené tkáni nebo orgánu jsou nakupeny CD4+T lymfocyty, ale na-opak v periferní krvi je relativní lymfopénie s převahou CD8+ T lymfocytů a hy-pergamaglobulinémie.(7) Anergie kožního tuberkulinového testu je pak funkčním obrazem tohoto sekundárního defektu buněčné imunity.
Aktivované makrofágy v granulomech jsou odpovědné za sekundární metabolické projevy sarkoidózy, jako je porucha metabolismu vápníku s hyperkalcémií a hyperkalciurií při nadprodukci 1,25-dihydroxycholekalciferolu, čili vitaminu D3 (15). Také produkují ve zvýšené míře tumor nekrotizující faktor - alfa (TNF-alfa) a angiotensin konvertující enzym (ACE), který se tak stává jedním z měřitelných markerů míry aktivity sarkoidózy. Při přechodu nemoci do chronicity a hlavně při přechodu ze stádia granulomatózních změn do stádia fibrózy (25 % pacientů s plicním postižením u sarkoidózy) dochází ke změně cytokinového spektra se sklonem k převaze cytokinů TH2 typu, typicky interleukinu - 4 (IL-4). Pacienti, kteří zvýšeně exprimují transformující růstový faktor beta (TGF-beta), mají sklon ke spontánní remisi onemocnění.
Klinický obraz sarkoidózy
Klinický obraz onemocnění není jednotný a závisí do značné míry na tom, zda jde o onemocnění chronické nebo akutní a jaké orgány a systémy jsou predilekčně postiženy (viz. tab. 1) Onemocnění často může probíhat asymptomaticky a může být poprvé zachyceno až na provedeném zadopředním skiagramu hrudníku, který je zhotoven kupříkladu v rámci vstupní prohlídky či předoperačního vyšetření. U symptomatických průběhů bývají v popředí systémové projevy onemocnění, jako je únava, noční pocení a váhový úbytek. Další projevy jsou pak specifické pro dané orgánové postižení. Při akutním průběhu sarkoidózy se nemoc manifestuje pod obrazem tzv. Lofgrenova syndromu (9 až 34 % pacientů):
- artritidy (hlavně v hlezenných kloubech),
- erythema nodosum, a
- bilaterální hilové adenopatie na skiagramu hrudníku.
Pokud je dán nemoci přirozený průběh, pak onemocnění spontánně regreduje u dvou třetin pacientů v průběhu 10 let od stanovení diagnózy, z toho u více než poloviny pacientů do 3 let. Zbylá třetina pacientů má bohužel progredující onemocnění a 5 % pacientů na onemocnění umírá, a to buď na respirační selhání při plicní fibróze, nebo na srdeční zástavu při postižení myokardu nebo na neurologické postižení (7).
Systémové projevy sarkoidózy
Až u 70 % pacientů se sarkoidózou je dominujícím a velmi obtěžujícím příznakem únava. Podle Sharmy (1999) může mít únava u sarkoidózy několik forem a těmi jsou:
- časná ranní únava, která znemožňuje pacientovi vstát ráno z postele,
- mírnější formou je pocit nevyspání s intermitentní únavou, kdy pacient sice nemá problémy se vstáváním, ale je vyčerpán po několika hodinách činnosti,
- poslední formou je pak odpolední únava, kdy pacient má chřipkové příznaky a obvykle musí jít brzo spát, protože se cítí unaven.
Zvláštní manifestací únavového syndromu u sarkoidózy je tzv. chronický únavový syndrom po prodělané sarkoidóze, který má mnoho synonym a projevuje se nejčastěji jako soubor příznaků:
- fibromyalgie,
- myalgie, a
- deprese.
Častým steskem je svalová slabost, která může být způsobena primárně granulomatózním postižením při sarkoidóze (u pacientů se sarkoidózou v 50–75 % svalových biopsií), ale může být indukována i léčbou kortikoidy (16, 19). Je třeba příčinu svalové slabosti zvážit, neboť při postižení granulomatózním zánětem je na místě léčba kortikoidy, ale při steroidní myopatii naopak kortikoidy musíme vysadit, nebo alespoň snížit a pokusit se eventuálně přejít na jinou formu léčby sarkoidózy. Často si na svalovou slabost stěžují pacienti, kteří mají zároveň pocit únavy při sarkoidóze, někdy popisují nemožnost fyzické zátěže hlavně pro svalovou únavu, a to hlavně dolních končetin. Výrazné, klinicky manifestní, svalové syndromy má však minimum pacientů se sarkoidózou.
Jedná se o dva syndromy:
- akutní polymyozitidu (popsáno doposud 18 případů) postihující proximální svalové skupiny pažní a pánevní, kdy je onemocnění spojeno s teplotami, erythema nodosum a polyartralgiemi, a
- chronickou myopatii (méně než 0,5 % pacientů, ACCESS 2003 – 1 z 215 pacientů) (13).
Diagnosticky nám v těchto dvou případech pomůže elektromyografické vyšetření, magnetická rezonance a svalová biopsie. Nezřídka bývají zvýšené teploty, většinou subfebrilie, ale občas i teploty dosahující 40°C. Při vyšetřování pacienta pro febrilie nejasné etiologie proto musíme mj. zvážit diferenciálně diagnosticky i sarkoidózu. Častý bývá úbytek hmotnosti dosahující až 2–6 kg za 10 až 12 týdnů.
Plicní postižení u sarkoidózy
Nejčastějším cílovým orgánem u sarkoidózy jsou plíce a uzliny v mezihrudí, které jsou postiženy prakticky u všech pacientů se sarkoidózou. Plicní postižení se obvykle manifestuje kašlem, pocitem diskomfortu na hrudi, dušností a případně i distančními pískoty.
Dle radiologického obrazu na zadopředním skiagramu hrudníku lze nitrohrudní sarkoidózu rozdělit do 5 stádií (tab. 2). Funkčně se plicní postižení může projevovat různým typem ventilační poruchy nebo může být funkčně asymptomatické. Přibližně 65 % pacientů má poruchu ventilace ve smyslu restrikce, z toho 50 % pacientů má také obstrukční ventilační poruchu, u řady pacientů jsou přítomny i známky bronchiální hyperreaktivity. Difúzní kapacita bývá snížena při manifestním postižení plicního parenchymu, její výrazné snížení je patrné ve stádiu fibrózy. Plicní hypertenze může být projevem jednak pokročilého onemocnění s fibrózními změnami, ale bylo také popsáno granulomatózní postižení plicních arteriol bez výrazného postižení plicního parenchymu (2).
Podrobnější zobrazení změn u u nitrohrudní sarkoidózy umožňuje CT hrudníku s vysokou rozlišovací schopností (HRCT), které lépe stanoví rozsah postižení plicní tkáně a jeho dynamiku v čase a rozliší fibrózní (irreverzibilní změny) od změn granulomatózních a infiltrativních (reverzibilních). Také nám pomůže v případě diferenciálně diagnostických rozpaků (1, 11).
Další z vyšetřovacích metod, kterou indikujeme při plicním postižení u sarkoidózy je bronchoskopie s bronchoalveolární laváží (BAL), endobronchiální a transbronchiální biopsií a perbronchiální punkcí uzlin. Typicky v tekutině získané BAL (BALTe) zachytíme převahu T lymfocytů, a to hlavně CD4 pozitivních, takže poměr CD4+/CD8+ T lymfocytů bývá obvykle větší než 3,5. V poslední době se dostává ke slovu i vyšetření nebuněčných součástí BALTe, a to hlavně cytokinů a chemokinů, které by mohly do budoucna mít i klinický význam při stanovení aktivity a prognózy plicního postižení u sarkoidózy (9, 18).
Postižení mimoplicních orgánů u sarkoidózy
Sarkoidóza je svým charakterem systémové onemocnění s multiorgánovým postižením. Nejčastěji postiženým orgánem jsou sice plíce a nitrohrudní uzliny, ale velmi často jsou postižena i játra, oči, kůže, slinné a slzné žlázy, myokard, nervy a svaly (tab. 1). Obecně, sarkoidóza může postihnout každý orgán a v případě řady orgánů může jít o funkčně nevýznamné a klinicky němé postižení. Nicméně v některých orgánových lokalizacích může znamenat nezjištěné, a tudíž neléčené postižení smrt pacienta, jako je to například v případě postižení myokardu, které se může manifestovat primárně náhlou smrtí z maligní arytmie způsobené poruchou převodu (4).
Table 1. Četnost postižení jednotlivých orgánů a systému u sarkoidózy 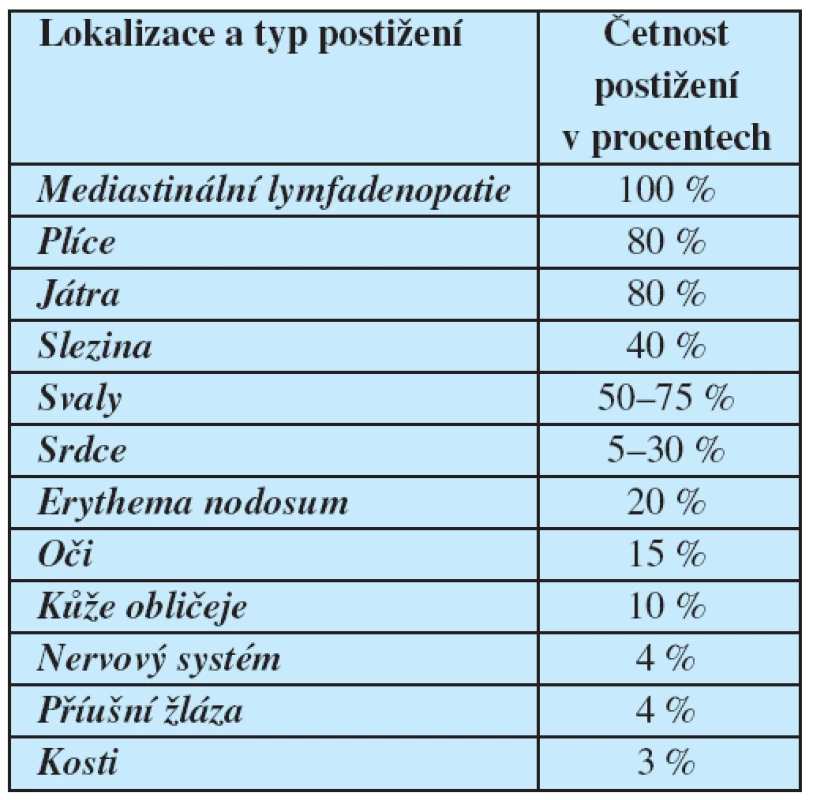
Játra jsou jedním z nejčastěji postižených extratorakálních orgánů. Granulomy jsou v nich zjišťovány v případě 50–80 % biopsií u pacientů se sarkoidózou. Ve 20 % pacientů jsou játra zvětšena i při fyzikálním vyšetření, laboratorně bývá patrné zvýšení alkalické fosfatázy a aminotransferáz až v 30 % nemocných. Zřídka ale bývá jaterní postižení příčinou portální hypertenze či jaterního selhání. Postižení jater obvykle nebývá závažné a většinou nevyžaduje léčbu (8).
Oční postižení je velmi variabilní a vídáme jej u 11–83 % pacientů. Nejčastější formou očního postižení je uveitida. Je třeba na toto postižení myslet, neboť při chronickém neléčeném průběhu může vyvolat těžké granulomatózní změny, zákal a slepotu. Méně časté je postižení spojivky (keratoconjunctivitis sicca), slzných žlaz (dacryocystitis) a cév sítnice (vaskulitida retinálních cév) (3).
Sarkoidóza postihuje klinicky manifestně nervový systém u méně než 10 % pacientů. Predilekční lokalizací postižení bývají bazální partie mozku s nejčastějším postižením hlavových nervů, hypothalamu a hypofýzy. Toto postižení se objevuje obvykle časně v průběhu sarkoidózy a je dobře ovlivnitelné léčbou. Horší prognózu má postižení, které se manifestuje později v průběhu onemocnění a má tendenci ke chronicitě. Patří k němu tumoriformní masy v mozku, periferní neuropatie a neuromuskulární postižení. Hlavním diagnostickým nástrojem je zde CT mozku, nebo lépe magnetická rezonance, která zachytí zvláště difúzní a diskrétní změny časněji a pak také samozřejmě punkce mozkomíšního moku k vyloučení jiných příčin granulomatózních lézí nervového systému (tuberkulózy a mykóz) (16).
Postižení kloubů ve smyslu artralgií se objevuje u 25–40 % pacientů, deformační změny jsou ale naštěstí velmi vzácné. Klinicky manifestní svalové postižení se objevuje velmi zřídka a obvykle se setkáme pouze se svalovou únavou v rámci únavy celkové (viz výše). Kostní cysty pozorujeme většinou pouze v souvislosti s chronickým kožním postižením (19).
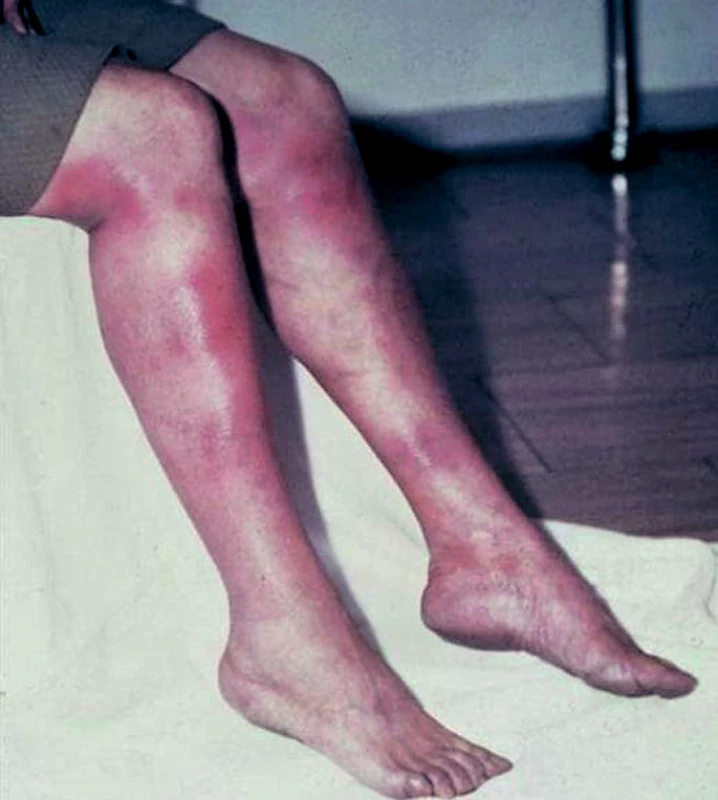
Kožní postižení je popisováno u 25 % pacientů. Nejfrekventnějším kožním projevem je erythema nodosum, nejčastěji jej můžeme vidět u nemocných se sarkoidózou v Severní Evropě, Portoriku a Mexiku. Podkladem nejsou granulomatózní léze, ale nekrotizující vaskulitida, a symptom není specifický pouze pro sarkoidózu (obr. 1).
Závažným postižením je tzv. „lupus pernio“, který se s nejvyšší četností vyskytuje u afroamerických žen se sarkoidózou a postihuje centrální části obličeje, nos, tváře, rty a uši, a je spojen s chronickým průběhem sarkoidózy, s kostním cystickým postižením a s plicní fibrózou. Prakticky nikdy nedochází v těchto případech ke spontánní remisi, průběh onemocnění je chronický, často nepříznivý. Mírnějšími formami kožního postižení jsou plaky, makulopapulární výsevy, podkožní uzlíky a sarkoidóza v oblasti jizev (5).
Mezi méně závažná postižení patří poruchy krvetvorby v rámci sarkoidózy, a to anémie ve 4–20 %, vzácně i hemolytického typu, dále pak leukopenie až ve 40 %, obvykle nezávažná, pouze obráží relativní depleci T lymfocytů. Periferní lymfatické uzliny bývají hmatné ve 30 až 40 %. Gastrointestinální trakt bývá postižen u méně než 1 % nemocných. Velmi vzácné je také postižení ledvin, které se může manifestovat ve formě granulomatózní intersticiální nefritidy, častěji však bývají ledviny postiženy sekundárně při hyperkalcémii a s ní spojené nefrokalcinóze (8, 15).
Diagnostika sarkoidózy
Je nutné si uvědomit, že neexistuje žádný izolovaný test, který by potvrdil jednoznačně diagnózu sarkoidózy, a to ani histologické vyšetření vzorku postižené tkáně. Nekazeifikující granulomy, které jsou patologickým obrazem sarkoidózy v orgánech a tkáních jsou samy o sobě nespecifické a stanovit diagnózu pouze na základě histologie není možné. (obr. 2). Z tohoto důvodu byla stanovena diagnostická kritéria sarkoidózy (tab. 3 a 4).
Image 2. Histologický obraz granulomu u sarkoidózy 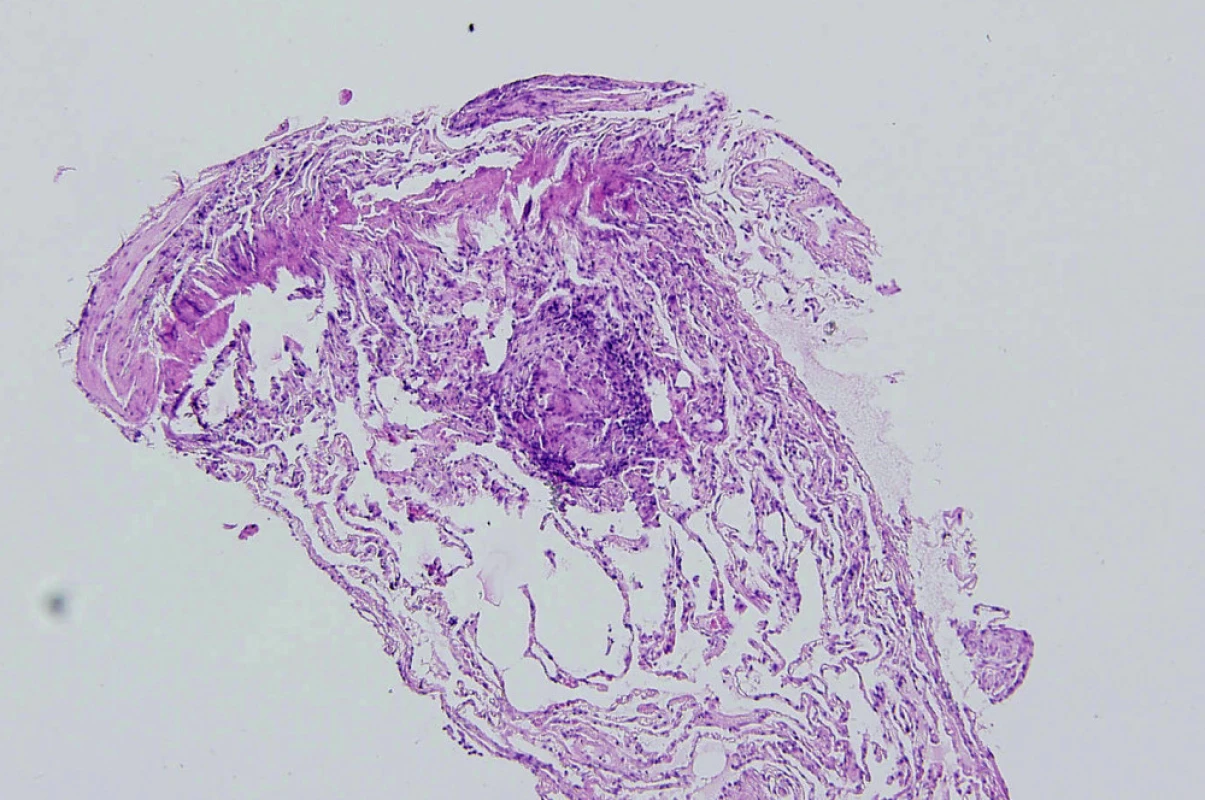
Table 2. Diagnostická kritéria sarkoidózy 
Table 3. Doporučený diagnostický soubor u sarkoidózy 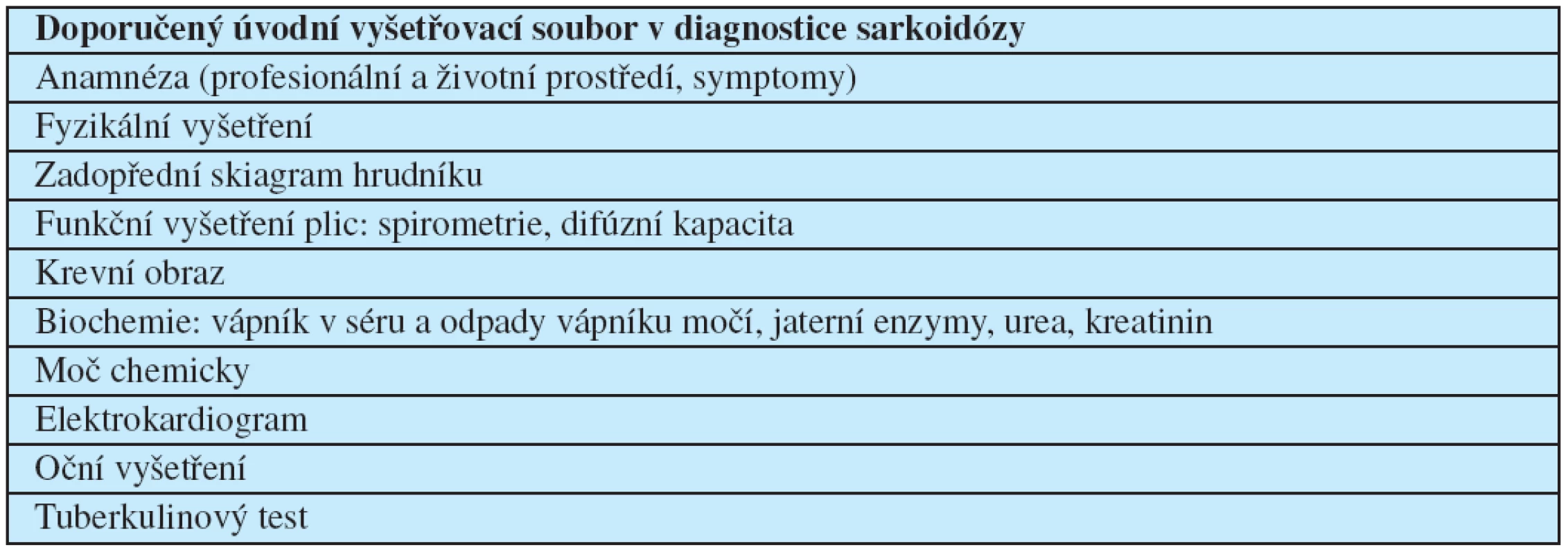
V radiologickém obraze sarkoidózy je nejtypičtější obraz postižení hilových a mediastinálních uzlin, v pokročilejších stádiích sarkoidózy spojený s plicním parenchymatózním postižením ve smyslu nodulací a infiltrátů. Při přechodu do jizvení se objevuje obraz retikulací, který je odrazem fibrózních změn a mediastinální a hilová adenopatie pak již může chybět (tab. 2, str. 209).
Table 4. Stádia plicního postižení dle zadopředního skiagramu hrudníku 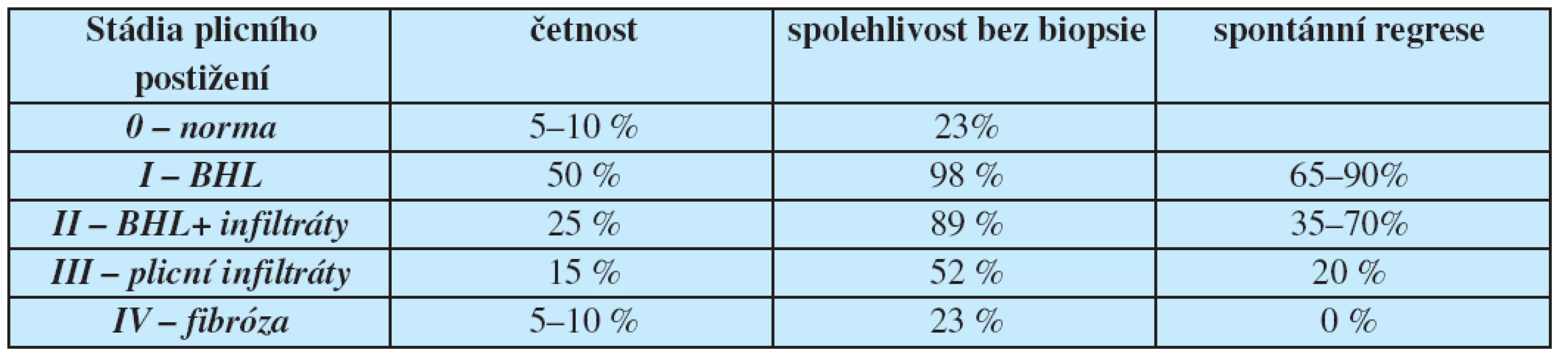
BHL: bilaterální hilová lymfadenopatie Jedním z typických laboratorně diagnostikovatelných projevů aktivní sarkoidózy jsou zvýšené hladiny vápníku v séru a zvýšené odpady vápníku močí. Také je zvýšen sérový ACE jako obraz aktivace makrofágů v sarkoidních granulomech (15).
V imunologických parametrech je patrna porucha buněčné imunity charakterizovaná většinou snížením CD4+ T lymfocytů a zároveň hypergamaglobulinémie. Z cytokinů bývá zvýšen IL-2 a solubilní receptor pro IL-2 (s IL-2R) jako marker aktivní sarkoidózy.
Z kožních testů je přítomna tuberkulinová anergie, naopak je pozitivní tzv. Kveim-Siltzbachův test. Technicky test spočívá v intradermální aplikaci homogenátu lidské sarkoidní tkáně získávané obvykle z resekovaných slezin nemocných se sarkoidózou, po 4 týdnech je pak excidována papula vzniklá v místě vpichu a histologicky vyšetřena. Tento test ale většina pracovišť opouští, a to hlavně pro nutnost vpravování nestandardizovaného humánního materiálu z odlišného jedince do těla pacienta. Proto je dnes jeho použití vyhrazeno pro diagnosticky nejasné stavy s nemožností získat pro biopsii část nepřístupné či obtížně přístupné postižené tkáně či orgánu (2).
Z nukleárně medicínských metod je již léta užíván pro diagnostiku sarkoidózy galiový scan, který v typickém případě zobrazí v oblasti hlavy a krku postižené slinné a slzné žlázy s obrazem „panda“ a v oblasti hrudníku lymfatické uzliny s obrazem „lambda“. Jedním z novějších diagnostických nástrojů je F-fluorodeoxyglukózová pozitronová emisní tomografie (FDG-PET), která stanoví rozsah orgánového postižení u sarkoidózy (17).
Co se týče vhodné lokalizace tkáňové biopsie při histologické diagnostice sarkoidózy, pak je nejlepší bioptovat zevně přístupnou tkáň (kožní léze, uzlina, spojivka). Pokud tyto tkáně nejsou postiženy, pak v případě změn na skiagramu hrudníku provedeme bronchoskopii s bronchoalveolární laváží, transbronchiální punkcí uzlin a endobronchiální či transbronchiální biopsií.
Pokud jsou výsledky vyšetření nediagnostické, pak volíme mediastinoskopii, eventuálně videoasistovanou thorakoskopickou biopsii (VATS). V případě normálního zadopředního skiagramu hrudníku bioptujeme přímo cílový (postižený) orgán: játra, svaly, nervový systém, otolaryngeální oblast, srdce, nitrobřišní uzliny.
Léčba sarkoidózy
Před zahájením léčby u pacienta se sarkoidózou je nutné vždy zvážit, zda pacientův stav a rozsah onemocnění vůbec léčbu vyžaduje, či nikoliv. Samotná léčba totiž pacientovi může přinést větší diskomfort než vlastní onemocnění. Zásadní otázkou před zahájením léčby je tedy, zda je ohrožena funkce postiženého orgánu natolik významně, aby měla léčba svoje opodstatnění a profit z léčby převážil nežádoucí účinky léků. Léčbu většinou zahajujeme perorálním prednisonem v dávce 20 až 40 mg denně (odpovídá přibližně dávkování 0, 5 mg/kg). Efekt léčby vyhodnocujeme obvykle po 1 až 3 měsících.
Při pozitivní léčebné odezvě snižujeme prednison na 5 až 15 mg denně, a tuto dávku pak ponecháme dalších 9 až 12 měsíců. Pokud není pozitivní efekt po 3 měsících léčby, buď jde o nemoc s ireverzibilním postižením (fibróza), neadekvátní dávku prednisonu nebo non-adherenci pacienta k léčbě (6).
Alternativním lékem je hydroxychlorochin, a to zvláště u pacientů s hyperkalcémií, kožním a neurologickým postižením. Metotrexát je obvykle používán u rezistentních forem onemocnění, často v kombinaci s kortikoidy, u nichž pomáhá redukovat dávky nutné k dosažení léčebného efektu. Z imunosupresiv se v případě chronických a multiorgánových forem onemocnění používá azathioprin, a to také v kombinaci s kortikoidy. Byl také popsán efekt minocyklinu při léčbě kožních forem sarkoidózy (5). Vzhledem k tomu, že kruciální roli v etiopatogenezu sarkoidózy hraje TNF alfa, dá se předpokládat léčebný efekt látek inhibujících tento cytokin, jeho produkci či dráhu jeho působení. Mezi takové léky patří kupříkladu thalidomid a pentoxifylin, které suprimují produkci TNF-alfa. Z léků blokujících účinek TNF-alfa jsou u sarkoidózy zkoušeny infliximab a etanercept, které jsou zatím rezervovány pro léčbu refrakterních nebo chronických forem sarkoidózy (10, 14) (tab. 5).
Table 5. Úvodní léčba v závislosti na postiženém orgánu a klinickém stavu pacienta 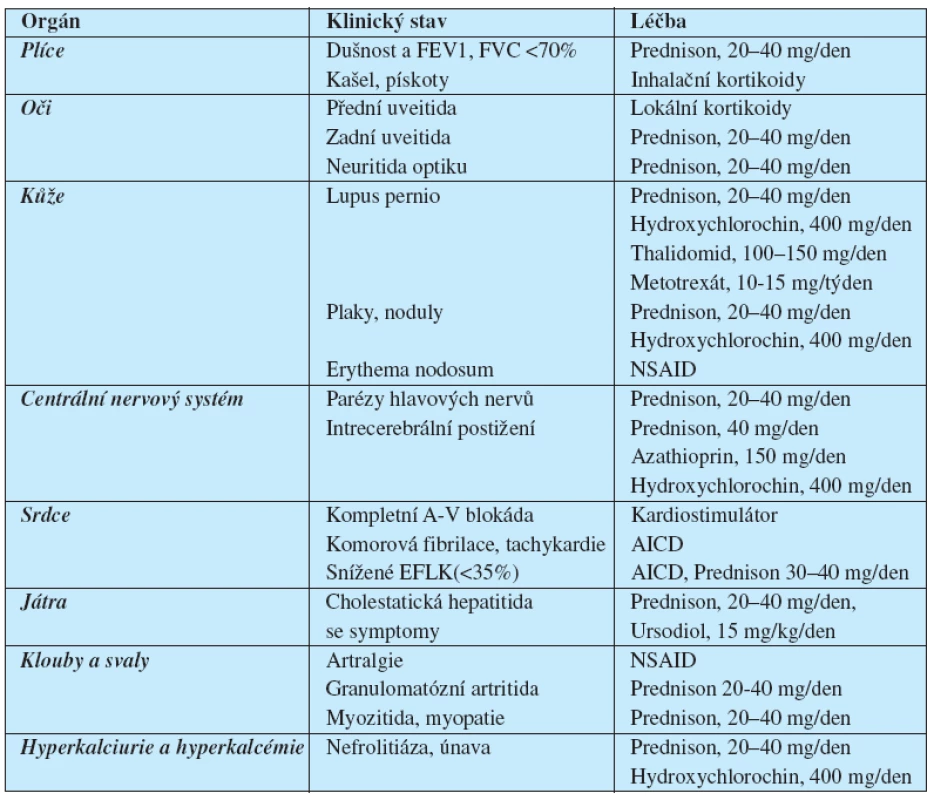
AICD – implantabilní srdeční defibrilátor NSAID – nesteroidní antirevmatika V případě nitrohrudní sarkoidózy se z pacientů rekrutují pouze 3 % z celkového počtu všech adeptů transplantace plic a méně než 1% adeptů transplantací srdce.
Závěr
Sarkoidóza je relativně benigním systémovým a multiorgánovým onemocněním a v oblasti Střední Evropy se obvykle nesetkáme se závažnými průběhy této nemoci. Nicméně, některé její formy, jako je například rozsáhlé plicní postižení s přechodem do fibrózy nebo postižení srdce, či centrálního nervového systému, mohou, a to zvláště jsou-li nerozpoznány, a tudíž neléčeny, ohrozit pacienta na životě, nebo jej výrazně zkrátit.
MUDr. Martina Vašáková, Ph.D.
Pneumologická klinika 1. LF UK
Fakultni Thomayerova nemocnice s poliklinikou
Vídeňská 800
140 59 Praha 4
Tel.: 26108 2372, Fax: 26108 2206,
e-mail: martina.vasakova@ftn.cz
Sources
1. Akira, M. Kozuka, T. Inoue, Y. et al. Long-term follow-up CT scan evaluation in patients with pulmonary sarcoidosis. Chest 2005, 127, 1, p. 185-191.
2. American Thoracic Society, European Respiratory Society, World Association of Sarcoidosis and Other Granulomatous Disorders. Statement on sarcoidosis. Am. J. Respir. Crit. Care Med. 1999, 160, p. 736-755.
3. Bradley, D., Baughmann, RP. Raymond, L. et al. Ocular manifesation of sarcoidosis. In Extrapulmonary sarcoidosis. Seminars in Respiratory and Critical Care Medicine 2002, 23, 6, p. 543-548.
4. Deng, J.C., Baughmann, R.P., Lynch, J.P. Cardiac involvement in sarcoidosis. In Extrapulmonary sarcoidosis. Seminars in Respiratory and Critical Care Medicine, 2002, 23, 6, p. 513-527.
5. Epstein, W. Cutaneous Sarcoidosis. In Extrapulmonary sarcoidosis. Seminars in Respiratory and Critical Care Medicine, 2002, 23, 6, p. 571-577.
6. Grutters, J.C., van den Bosch, M.M. Corticosteroid treatment in sacoidosis. Eur. Respir. J. 2006, 2, p. 627-636.
7. Iannuzzi, M.C., Rybicki, B.A., Teirstein, A.S. Sarcoidosis. N. Engl. J. Med. 2007, 357(21), p. 2153-2165.
8. Judson, M.A. Hepatic, splenic, and gastrointestinal involvement with sarcoidosis. In Extrapulmonary sarcoidosis. Seminars in Respiratory and Critical Care Medicine 2002, 23, 6, p. 529-541.
9. Kriegova, E. Melle, C. Kolek, V. Protein profiles of bronchoalveolar lavage fluid from patients with pulmonary sarcoidosis. Am. J. Respir. Crit. Care Med. 2006, 173, p. 1145 - 1154.
10. Martin, W.J., Iannuzzi, M.C., Gail, D.B. et al. Future directions in sarcoidosis research. Summary of an NHLBI Working Group. Am. J. Respir. Crit. Care Med. 2004, 170, p. 567-571.
11. Polák, J., Vašáková, M., Bártů, V. a kol. Význam vysoce rozlišující výpočetní tomografie/HRCT/ při sledování nemocných s plicní sarkoidózou. Stud. Pneumol. Phtiseol. 1994, 54, 6, s. 424-433.
12. Proceedings of XII. World Congress Sarcoidosis 1991. Sarcoidosis, 1992, 9, (Suppl 1), p. 34.
13. Rybicki, B.A., Ianuzzi, M.C., Frederick, M.M. et al. Familial aggregation of sarcoidosis: A Case-Control Etiologic Study of Sarcoidosis (ACCESS). Am. J. Respir. Crit. Care Med. 2001, 164, p. 2085-2091.
14. Saleh, S., Ghodsian, S., Yakimova, V. et al. Effectiveness of infliximab in treating selected patients with sarcoidosis. Respiratory Medicine 2006, 100, p. 2053-2059.
15. Sharma, O.P., Vučinič, V. Sarcoidosis of the thyroid and kidneys and calcium metabolism. In Extrapulmonary sarcoidosis. Seminars in Respiratory and Critical Care Medicine 2002, 23, 6, p. 579-588.
16. Teirstein, A. Neuromuscular sarcoidosis. In Extrapulmonary sarcoidosis. Seminars in Respiratory and Critical Care Medicine, 2002, 23, 6, p. 505-512.
17. Teirstein, A.S., Machac, J., Almeida, O. et al. Results of 188 whole-body fluorodeoxyglukose positron emission tomography scans in 137 patients with sarcoidosis. Chest 2007, 132, 6, p. 1949-1953.
18. Ziegenhagen, M.W., Rothe, M.E., Schlaak, M. et al. Bronchoalveolar and serological parameters reflecting the severity of sarcoidosis. Eur. Respir. J. 2003, 21, p. 407-413.
19. Zisman, D.A., Shor, A.F., Lynch, J.P. Sarcoidosis involving the musculosceletal system. In Extrapulmonary sarcoidosis. Seminars in Respiratory and Critical Care Medicine 2002, 23, 6, p. 555-570.
Labels
General practitioner for children and adolescents General practitioner for adults
Article was published inGeneral Practitioner

2008 Issue 4-
All articles in this issue
- Prevence a časný záchyt cévních komplikací diabetu
- Místní léčba revmatických chorob nesteroidními antirevmatiky
- Historie vývoje poznatků o potravinách a významu živin ve výživě člověka
- Sluchové poznávání a jeho poruchy
- Sarkoidóza – systémová nemoc. Co je nového?
- Fotoalergické kožní reakce po systémovém podávání léků
- Sezónní práce v zemědělství – riziko organofosfátů
- Kotníkové indexy a riziko kardiovaskulárních komplikací
- Třírovinná zlomenina distální tibie u dětí
- Prenatální diagnostika a její úspěšnost v České republice
- Automutilace a poranění zevního genitálu u mužů
- Letální abscedující pneumonie vyvolaná kmenem Staphylococcus aureus oxacilin rezistentním s produkcí Pantonova-Valentinova leukocidinu
- Mimostřevní projevy při celiakii
- General Practitioner
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Mimostřevní projevy při celiakii
- Sarkoidóza – systémová nemoc. Co je nového?
- Třírovinná zlomenina distální tibie u dětí
- Letální abscedující pneumonie vyvolaná kmenem Staphylococcus aureus oxacilin rezistentním s produkcí Pantonova-Valentinova leukocidinu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career