-
Medical journals
- Career
Mimostřevní projevy při celiakii
: L. Franeková; M. Sedláčková
: Fakultní Thomayerova nemocnice s poliklinikou, Praha ; Primář: MUDr. Marie Sedláčková ; Revmatologické a rehabilitační oddělení
: Prakt. Lék. 2008; 88(4): 240-243
: Case Report
Celiakální sprue je autoimunitní onemocnění navozené gliadinovou frakcí lepku. V dospělosti mohou být klinické střevní projevy nemoci nevýrazné a dominují mimostřevní příznaky. V práci se zabýváme metabolickými a zánětlivými kloubními příznaky, které ke správné diagnóze celiakie, a tedy i odpovídající terapii mohou vést. K ilustraci uvádíme dvě kazuistiky, které problematiku diagnostiky podrobně popisují.
Klíčová slova:
celiakie, malabsorpce, osteomalácie, protilátky proti transglutamináze, endomysiální protilátky, sakroileitida, Looserova pseudofraktura.Úvod
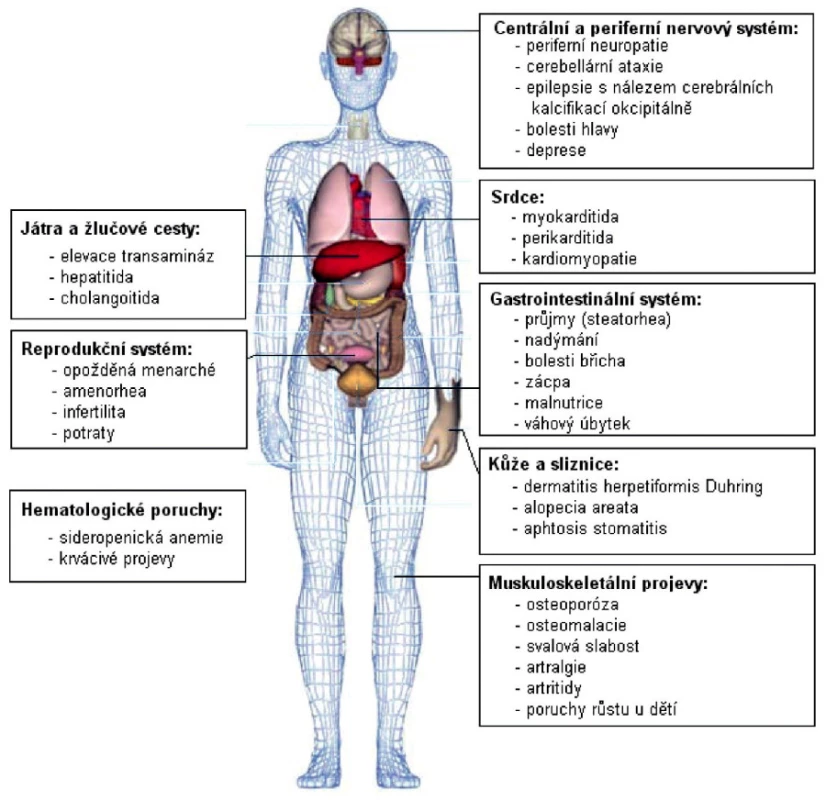
Celiakie (celiakální sprue, glutenová enteropatie) je autoimunitní onemocnění navozené u geneticky disponovaných osob (nositelé HLA DQ2 a DQ8) gliadinovou frakcí lepku. Onemocnění postihuje primárně střevní sliznici a projevuje se malabsorpčním syndromem různé intenzity, ale také celou řadou mimostřevních projevů – jako jsou projevy kožní, kardiální, neurologické, kloubní či gynekologické (obr. 1) (3, 4).
Manifestace celiakie má dva vrcholy – nejčastěji se diagnostikuje v druhém roce života nebo ve 4. dekádě. I klinický obraz se v dětském a dospělém období liší: v dětském věku dominují průjmy a neprospívání dítěte, u dospělých převažují mimostřevní projevy onemocnění a střevní obtíže mohou být necharakteristické ( bolesti břicha, nadýmání, nechutenství, jen občasné průjmy nebo naopak zácpa), nebo nemusí být vyjádřeny vůbec.
Značná variabilita klinických projevů a fakt, že se na toto nemocnění v dospělém věku nemyslí, je příčinou nedostatečné diagnostiky celiakie v populaci. Na každého diagnostikovaného nemocného se odhaduje dalších 5–10 s nepoznaným onemocněním (5). Z důvodů zvýšeného rizika malignit gastrointestinálního traktu nebo osteoporotických zlomenin u pacientů s nepoznaným onemocněním se doporučuje pacienty aktivně vyhledávat v rizikových skupinách osob.
Při podezření na celiakii je třeba vyšetřit v séru protilátky pro toto nemocnění vysoce specifické – protilátky endomyziální a proti tkáňové transglutamináze. Diagnostika celiakie je postavena na bioptickém průkazu u dospělých z duodena) atrofie klků střevní sliznice, lymfoplazmocytární infiltrace, hypertrofie krypt a zmnožení intraepiteliálních lymfocytů. Základem terapie je bezlepková dieta a substituce minerálů a vitamínů.
Vzhledem k širokému spektru klinických projevů se může ve své ordinaci praktický lékař setkat i s nemocnými s dosud nediagnostikovaným onemocněním, a to především u osob s osteoporózou či osteomalácií (v rámci malabsorpčního syndromu), dále u pacientů bolestmi kloubů a artritidami nebo s projevy neurologickými a kardiálními. V našem sdělení bychom rádi prezentovali dvě kazuistiky, ve kterých správná diferenciální diagnóza kostní a kloubní nemoci vede přímo k cíli, k průkazu celiakie.
Vlastní pozorování
Kazuistika č. 1:
Anamnéza:
Žena, 72 let, v rodinné anamnéze údaj o chronickém průjmovém onemocnění otce. Pacientka sama od dětství trpěla na nadýmání a průjmy, jejichž příčinu se nepodařilo zjistit. Dvakrát byla pro průjmy hospitalizována se závěrem, že etiologie průjmu je infekční. Kromě laktózové intolerance nebyl jiný provokační moment vypozorován.
V osobní anamnéze byla nápadná informace o mnohočetných zlomeninách – fraktuře klíční kosti, pravého předloktí, mnohočetných kompresivních frakturách hrudních obratlů a prvního bederního obratle.
Subjektivní obtíže:
Pacientka (156 cm, 45 kg) si stěžovala na bolesti dlouhých kostí, žeber, kloubů, váhový úbytek 12 kg za posledních 7 let, únavu a zhoršující se chůzi. V době přijetí k diagnostické hospitalizaci na naše oddělení udávala 5 průjmovitých světlých stolic za den.
Objektivní nález:
V objektivním nálezu dominoval bledý kolorit kůže, astenický habitus, kolébavá chůze, perimaleolární otoky, jinak byl nález fyziologický. V kloubním nálezu nebyly známky artritidy, bérce i páteř byly na poklep bolestivé, páteř s obrazem kyfoskoliózy.
Výsledky vyšetření:
Vyšetřením biochemických markerů kostního metabolismu byly zjištěny výsledky typické pro osteomalácii: hypokalcemie 1,4 mmol/l, výrazná hypokalciurie 0,36 mmol/24 hod, sérová hladina fosforu při dolní hranici normy, zvýšená aktivita alkalické fosfatázy 10,5 (norma do 2,4), respektive jejího kostního izoenzymu 5,84 μkat/l (norma do 1,2), osteokalcin 29,4 ng/l (norma do 16,3), hladina kalcidiolu 17,2 nmol/l (dolní hranice normy je 50), parathormon 237 pg/ml (norma do 55).
V laboratorních vyšetřeních byly dále zřetelné projevy malabsorpčního syndromu (anémie s hemoglobinem 89 g/l, hyposideremie, hypomagnezémie, hypalbuminemie 30,2 g/l, prodloužení protrombinového času na INR 5,6 jako projev deficitu K vitamínu), zvýšená sedimentace (FW 75 mm/hod) a hyperimunoglobulinemie. Vyšetřením protilátek typických pro celiakii byl zjištěn desetinásobný titr IgG antigliadinových protilátek, trojnásobný titr IgA endomyziálních protilátek, v IgG třídě byly tyto protilátky negativní. V době přijetí pacientky na naše oddělení jsme ještě neměli možnost vyšetřit protilátky proti tkáňové transglutamináze.
Rentgenovým vyšetřením byly prokázány pro osteomalácii typické Looserovy zóny (pseudofraktury) na obou fibulách (obr. 2), dolním raménku kosti stydké vpravo, krčku levého femuru, pravém předloktí a žebrech. Denzitometrickým měřením byl stanoven těžký stupeň demineralizace: T-score v oblasti krčku femuru bylo – 4,73. Bioptické a histochemické vyšetření makroskopicky atrofické sliznice duodena prokázalo floridní celiakii.
2. Obraz Looserovy pseudofraktury na fibule (známka osteomalácie). 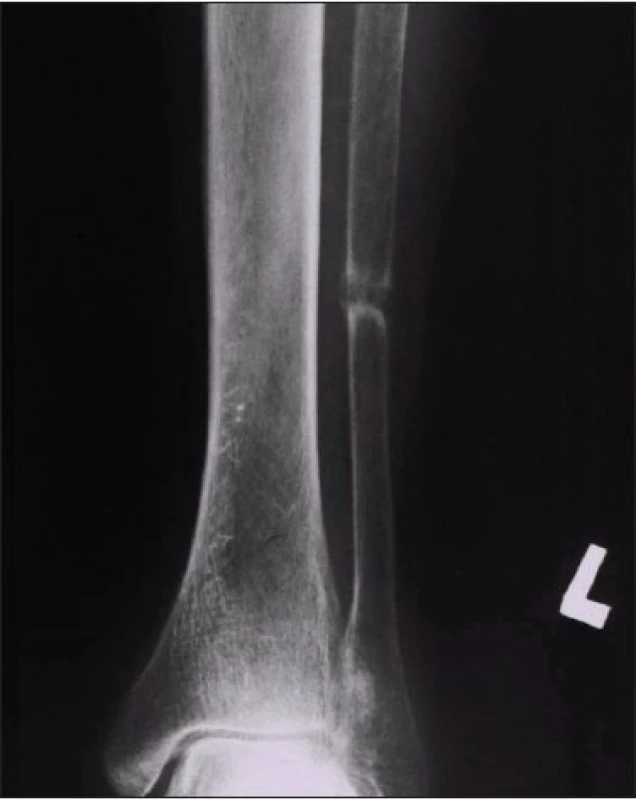
Diagnostický závěr:
Těžký malabsorpční syndrom s osteomalácií, anémií, hypalbuminemickými otoky dolních končetin, deficitem Fe, Mg, K vitamínu, na podkladě celiakie.
Léčba a její výsledky:
Terapeuticky byla zavedena bezlepková dieta, parenterálně substituce kalcia 5 amp/den, ergokalciferolu (zpočátku v dávce 300 tis IU i.m. obden, poté v delších časových intervalech v závislosti na hodnotě ALP, kalcémie a kalciurie), perorální substituce železa a K vitamínu. Za 6 měsíců byla pacientka již bez únavy, bez bolestí, stolici měla jen 1x denně, přibrala 7 kg na váze, došlo již k normalizaci kalciového metabolismu, markerů kostního obratu a krevního obrazu. Při kontrole za 2 roky byl celkový váhový přírůstek 20kg.
Diskuse
Diferenciální diagnostika chronického průjmovitého onemocnění zahrnuje pátrání po infekčních (zejména bakteriálních a parazitárních) a endokrinních příčinách, idiopatických střevních zánětech, potravinové alergii, divertikulitidě, pankreatické insuficienci, ale také je třeba vždy myslet i na celiakii. Celiakie je v dospělosti diagnostikována spíše výjimečně pro netypické obtíže a nedostatečnou informovanost o mimostřevních symptomech. Teprve po vyloučení všech organických příčin lze označit průjmové onemocnění za dráždivý tračník.
Proč u 72leté ženy s typickými příznaky celiakie od dětství nebylo toto nemocnění dosud diagnostikováno vysvětluje fakt, že v době dětství pacientky ještě nebyla známa etiopatogenetická souvislost gliadinu s průjmy s nutností jeho vyloučení ze stravy. Ta byla objevena Dickem teprve koncem 40. let 20. století.
U pacientů se zjištěnou demineralizací skeletu je třeba provádět důslednou diferenciální diagnostiku metabolické osteopatie, t.j. odlišit osteomalácii od osteoporózy na základě vyšetření kalciového metabolismu a markerů kostního obratu a při podezření na osteomalácii pak pátrat po Looserových pseudofrakturách v oblasti pánve, eventuálně žeber a dlouhých kostí. Hyperparatyreóza je v tomto případě pouze sekundární, navozená hypokalcémií. Rozlišení osteoporózy od osteomalácie je důležité z hlediska strategie léčby. Každý pacient s osteoporózou nebo dokonce s osteoporotickou frakturou by měl být podroben vyloučení sekundárních příčin osteoporózy, ke kterým kromě endokrinopatií, hematoonkologických malignit, idiopatické hyperkalciurie, patří i malabsorpční stavy včetně celiakie. Screening celiakie se doporučuje provádět (stanovením protilátek endomyziálních a proti tkáňové transglutamináze) u pa-cientů s osteoporózou, kteří udávají jakékoliv dyspeptické obtíže, u mužů, premenopauzálních žen, dále u příbuzných pacientů s celiakií a pacientů, kteří jsou léčeni pro nevysvětlenou sideropenickou anémii (4, 9).
Kazuistika č. 2:
Anamnéza:
Jedná o 24letou pacientku bez rodinné zátěže revmatických či střevních chorob, dosud zdravou a bez střevních obtíží.
Subjektivní obtíže:
Obtíže ve smyslu bolestí dolní části zad (low back pain) s maximem v oblasti obou sakroiliakálních kloubů, zejména nočními, se u pacientky poprvé objevily na jaře roku 2006. Pro tyto týden trvající intenzivní obtíže byla přijata na neurologické oddělení. V objektivním neurologickém nálezu nebyly patrny senzitivní ani motorické výpadky. RTG obraz bederní páteře byl bez zjevné patologie. Na rentgenu sakroiliakálních kloubů byla popsána jen lehká sklerotizace levého kloubu kraniálně.
V laboratorních výsledcích byl zřetelný vzestup zánětlivých parametrů (FW 42/80, CRP 42), jehož příčina nebyla objasněna. Vzhledem k neustupujícím obtížím při analgetickomyorelaxační infuzní léčbě byla doplněna lumbální punkce, CT a poté i MRI bederní páteře. Diskrétní nález protruze disku L4/5 a normální likvorový nález nevysvětlily obtíže pacientky. Pacientka jen s minimální úlevou byla propuštěna do domácího léčení. S odstupem 6 týdnů, kdy se obtíže spontánně podstatně zlepšily, byla vyšetřena revmatologem, který již neshledal bolestivost v oblasti SI kloubů, konstatoval normalizaci parametrů zánětu a HLA B 27 negativitu.
V září 2006 došlo k recidivě bolestí SI kloubů se subfebriliemi a opětovnou elevací markerů zánětu (CRP 50). Bylo pátráno i po dalších infekčních fokusech s negativními výsledky. K dovyšetření byla pacientka přeložena na naše oddělení.
Objektivní nález při přijetí:
Objektivní kožní a interní nález byl fyziologický. Kloubní nález byl na periferních kloubech normální, bederní páteř bez bolestivosti, rozvíjení páteře v předklonu nevyšetřitelné pro výrazné bolesti SI kloubů s typickým nočním maximem (zánětlivá bolest).
Výsledky vyšetření:
Klinické podezření na sakroileitidu jsme ověřili magnetickou rezonancí, kde nález kostního edému obklopujícího sakroiliakální klouby a subchondrální sklerotizace byly přesvědčivým důkazem oboustranné sakroileitidy (obr. 3).
3. MR obraz oboustranné sakroileitidy (kostní edém obklopující sakroiliakální klouby a subchondrální skleróza kosti) 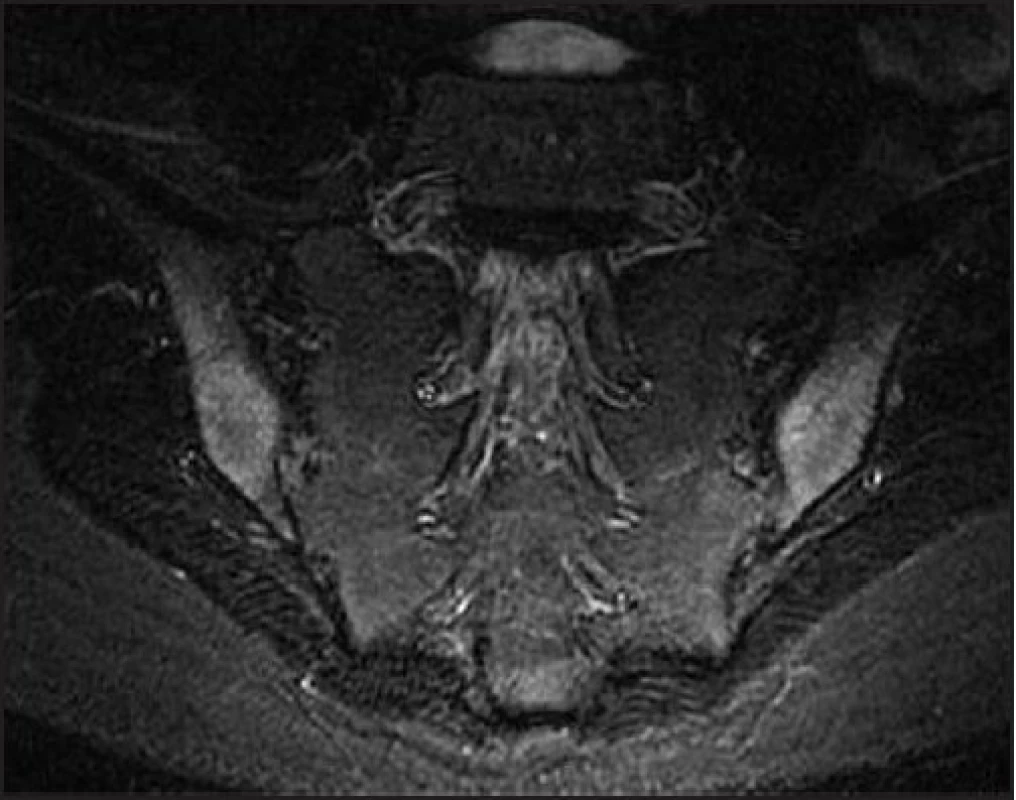
V dalším vyšetřovacím programu jsme se zaměřili na průkaz infekce Chlamydia trachomatis, pro kterou nepřímo svědčily dvojnásobné titry protilátek ve třídě IgA a IgG. Kultivačně však stěrem z děložního čípku Chlamydie prokázána nebyla, vyšetření Chlamydií v moči metodou PCR bylo rovněž negativní. Základní imunologická vyšetření jako hladiny imunoglobulinů, cirkulující imunokomplexy, komplement, byly v normě, autoprotilátky (ANA, RF, ENA, ACLA, ds DNA, ANCA) jsme neprokázali.
Při pátrání po důvodu sakroileitidy u HLA B 27 negativní pacientky jsme uvažovali i o celiakii, a proto provedli screening, přičemž antigliadinové protilátky byly v normě, ale protilátky proti tkáňové transglutamináze byly ve třídě IgA čtyřnásobné a ve třídě IgG dvojnásobné. Na doporučení gastroenterologa byla následně provedena enteroskopie s bioptickým odběrem z proximálního jejuna. V histologickém obraze byl patrný nepravidelný slizniční reliéf se zvýšeným počtem intraepiteliálních lymfocytů (Marsh I – infiltrativní typ) a známky mírného autoimunitního poškození sliznice (zvýšený počet T-lymfocytů). Gastroenterolog uzavřel diagnózu jako pravděpodobnou celiakální sprue.
Diagnostický závěr:
Enteropatická artritida s axiálním postižením II. stadia (sakroileitidou) u pacientky s celiakií.
Terapie:
Pacientku jsme v první fázi léčili nesteroidními antirevmatiky v plné protizánětlivé dávce a provedli jsme lokální obstřik sakroiliakálních kloubů s depotním kortikoidem. Tato léčba vedla k úlevě obtíží, které však brzy recidivovaly. Proto jsme přešli k celkové léčbě kortikoidy a Sulfasalazinem v dávce 2g/den. Poté, co byla prokázána celiakie, byla pacientka instruována ohledně bezlepkové diety a zařazena do sledování v gastro-enterologické poradně. Kortikoidy i Sulfasalazin byly po 6 měsících trvající remise postupně vysazeny. Ponechána byla pouze léčba nesteroidními antirevmatiky podle potřeby.
Diskuse
Průkaz zánětu v oblasti sakroiliakálních (křížokyčelních) kloubů může být diagnostickým problémem, a to zejména proto, že rentgenové vyšetření pro časnou diagnostiku zánětu není dostatečně citlivé. Typické RTG známky sakroileitidy se subchondrální sklerotizací a erozemi se vytvářejí se zpožděním minimálně 6 měsíčním. Suverénní metodou průkazu časných zánětlivých změn je MRI vyšetření. Pacient trpí bolestí dolní části zad zánětlivého charakteru, která je typicky klidová a noční, budí nemocného ze spánku, úlevu mu přináší rozcvičení, ráno se pacient budí s pocitem ranní ztuhlosti delší než půl hodiny. Pokud při těchto obtížích je palpace na sakroiliakální klouby výrazně bolestivá, a laboratorně jsou vyjádřeny laboratorní markery zánětu, pak diagnóza sakroileitidy je velmi pravděpodobná. Scintigrafické vyšetření skeletu prokáže zvýšenou akumulaci radiofarmaka v sakroiliakálních kloubech.
K sakroileitidám dochází nejčastěji po proběhlém infekčním střevním onemocnění nebo infekci urogenitálního traktu (zejména infekci Chlamydia trachomatis), dále u pacientů se nespecifickými střevními záněty (idiopatická proktokolitida, M. Crohn), lupénkou a ankylozující spondylitidou (8). Všechna tato onemocnění patří do skupiny tzv. séronegativních spondylartropatií. Revmatoidní faktor je u těchto pacientů obvykle negativní a různě silná je jejich asociace s HLA antigenem B 27. Pokud je důvod onemocnění nejasný, hovoříme o nediferencovaných spondylartropatiích. Málo známá je skutečnost, že i pacienti s celiakií jsou ohroženi rozvojem sakroileitidy (10) a eventuálně i spondy-litidy, ale také artritidami periferních kloubů. Typicky jde o symetrickou polyartritidou velkých kloubů (ramena, kyčle, kolena) (6).
Je doložena řada kazuistik i s jiným obrazem periferních artritid (mono, oligoartritid), jejichž příčinou byla celiakie. Asociace s HLA B 27 u těchto pacientů prokázána nebyla. V diferenciální diagnostice pacientů se sakroileitidou, zejména jednostrannou a HLA B 27 neg., bychom měli proto uvažovat i o celiakii a vyšetřit protilátky typické pro celiakii (endomyziální a proti tkáňové transglutamináze). Při záchytu těchto protilátek se gastroenterolog rozhodne, zda provést bioptický odběr.
V uvedené kazuistice pacientky s oboustrannou sakroileitidou, HLA B 27 neg., špatně reagující na léčbu, předpokládáme souvislost s prokázanou celiakií.
Terapeutický přístup je obdobný při axiálním postižení při všech séronegativních spondylartropatiích. Základem terapie jsou nesteroidní antirevmatika, a u případů rezistentních na tuto léčbu i kortikoidy lokálně i systémově. Předpokládáme, že pacientka bude ze zavedení bezlepkové diety profitovat z hlediska možného rozvoje malabsorpčního syndromu, s ním i osteoporózy, nebude vystavena zvýšenému riziku malignit trávicího traktu, a také snížíme pravděpodobnost recidivy sakroileitidy a eventuálně pokračujícího zánětlivého postižení páteře s omezením hybnosti podobné ankylozující spondylitidě. Literární údaje uvádějí efekt bezlepkové diety na kloubní obtíže u 79 % pacientů s prokázanou celiakií (2, 7). Opětovná expozice lepku navodila u pacientů relaps periferní artritidy či sakroileitidy (1).
Závěr
Podrobné vyšetření pacientů s metabolickými osteopatiemi (osteomalácií a osteoporózou), artralgiemi, artritidou, nebo se současnou sakroileitidou, může vést i k odhalení dosud nediagnostikované celiakie a vyloučením lepku ze stravy k naději na remisi jinak špatně ovlivnitelného onemocnění.
MUDr. Lenka Franeková
Revmatologické a rehabilitační odd. Fakultní Thomayerovy nemocnice
Vídeňská 800,
Praha 4 – Krč, 140 59
Sources
1. Bourne, J.T., Kumar, P., Huskisson, E.C. et al. Arthritis and celiac disease. Ann. Rheum. Dis. 1985, 44, p. 592-898.
2. Collin, P., Korpela, M., Hällstrom, O. et al. Rheumatic complaints as a presenting symptom in patients with coeliac disease. Scand. J. Rheumatol. 1992, 21, p. 20-23.
3. Dewar, D.H., Ciclitira, P.J. Clinical features and diagnosis of celiac disease. Gastroenterology 2005, 128, Suppl 1, p. 19-24.
4. Franeková, L., Philipp, T., Sedláčková, M. Muskuloskeletální projevy při celiakii. Čes. Revmatik. 2007, 15, s. 190-196.
5. Heel, D.A., West, J. Recent advances in coeliac disease. Gut 2006, 55, p. 1037-1046.
6. Holden, W., Orchard, T., Wordsworth, P. Enteropathic arthritis. Rheum. Dis. N. Am. 2003, 29, p. 513-530.
7. Lubrano, E., Ciacci, C., Ames, P.R.J. et al. Arthritis of coeliac disease: prevalence and pattern in 200 adult patients. Br. J. Rheumatol. 2000, 29, p. 260-263.
8. Peterová, V., Forejtová, Š. Komplexní morfologická vyšetření u nemocných s ankylozující spondylitidou. Čes. Revmatik. 2006, 14 (2), s. 70-78.
9. Selby, P.L., Davies, M., Judith, E.A. et al. Bone loss in celiac disease is related to secondary hyperparathyroidism. J. Bone. Miner. Res. 1999, 14 (4), p. 652-657.
10. Usai, P., Boi, M.F., Piga, M. et al. Adult celiac disease is frequently associated with sacroiliitis. Dig. Dis. Sci. 1995, 40, p. 1906-1908.
Labels
General practitioner for children and adolescents General practitioner for adults
Article was published inGeneral Practitioner

2008 Issue 4-
All articles in this issue
- Prevention and early detection of the vascular complications of diabetes
- Topical treatment of rheumatic diseases by non steroidal anti-inflammatory drugs
- The history of the development of our understanding of food and the importance of nutrients in human nutrition
- Auditory system and its disturbances
- Sarcoidosis- a systemic disease. What is new?
- Photoallergic skin reactions due to systemic application of drugs
- Seasonal work in agriculture – risk of organophosphates
- Ankle-brachial indices and risk of cardiovascular complications
- Triplane fracture of distal tibia in children
- Prenatal diagnostics and its success in the Czech Republic
- Self-mutilation and male external genitalia injury
- Fatal abscessing pneumonia caused by oxacillin-resistant Staphylococcus aureus producing Panton-Valentine leukocidin
- Extraintestinal symptoms of coeliac disease
- General Practitioner
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Extraintestinal symptoms of coeliac disease
- Sarcoidosis- a systemic disease. What is new?
- Triplane fracture of distal tibia in children
- Fatal abscessing pneumonia caused by oxacillin-resistant Staphylococcus aureus producing Panton-Valentine leukocidin
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career