-
Medical journals
- Career
Léčba komplikované Crohnovy choroby vedolizumabem
Authors: B. Pipek 1; P. Falt 1–3
Authors‘ workplace: Centrum péče o zažívací trakt, Vítkovická nemocnice, a. s., Ostrava 1; LF OU v Ostravě 2; Katedra interních oborů, LF UK v Hradci Králové 3
Published in: Gastroent Hepatol 2018; 72(2): 143-147
Category: IBD: Case Report
doi: https://doi.org/10.14735/amgh2018csgh.info02Overview
Crohnova choroba je chronické zánětlivé onemocnění trávicího traktu ne zcela jasné etiologie, kdy se u mnoha nemocných setkáváme s těžkým progredujícím průběhem s četnými komplikacemi. Novým biologickým léčivem, které je od roku 2016 dostupné na českém trhu, je antiintegrinová protilátka vedolizumab. Vedolizumab je humanizovaná monoklonální protilátka proti integrinovým receptorům (α4β7) na povrchu aktivovaných leukocytů, která selektivně zabraňuje vycestování lymfocytů z kapilární sítě do gastrointestinálního traktu. Díky této selektivitě je léčba provázena nízkým rizikem nežádoucích účinků. Je indikován k léčbě dospělých pacientů se středně těžkou až těžkou aktivní Crohnovou chorobou nebo ulcerózní kolitidou, u nichž buď nastala neadekvátní odpověď na konvenční terapii nebo na antagonistu tumor nekrotizujícího faktoru α (TNF-α) nebo došlo ke ztrátě odpovědi na léčbu nebo u pacientů, kteří uvedenou léčbu netolerují. Prezentujeme kazuistiku 43leté pacientky s těžce a komplikovaně probíhající Crohnovou chorobou, po četných resekčních výkonech, po selhání dvou anti-TNF léků a s rozvinutou kortikodependencí. Po podání vedolizumabu došlo k postupnému zlepšení klinického stavu pacientky, normalizaci endoskopického nálezu i těžké sideropenické anémie. Podařilo se nám zcela vysadit kortikoidy. Aktuálně je pacientka po roční léčbě vedolizumabem v hluboké remisi onemocnění.
Klíčová slova:
Crohnova choroba – vedolizumab – ileceocekální resekce – endoskopická dilatace pooperační striktury – biodegradabilní stentPopis případu
V našem sdělení prezentujeme kazuistiku dnes 43leté pacientky léčené s Crohnovou chorobou (CD – Crohn’s disease) od roku 2002. Jedná se o CD diagnostikovanou ve 28 letech s penetrujícím a strikturujícím postižením terminálního ilea a colon (dle Montreálské klasifikace A2 – diagnostikovaná v 28 letech, L3 s postižením terminálního ilea + colon, B2 + 3 strikturující a penetrující postižení). V roce 2009 prodělala pacientka ileocekální resekci, která byla provedena pro zánětlivý konvolut v pravém podbřišku zaujímající pravá adnexa i ureter, který následně vedl k rozvoji pravostranné hydronefrózy. Pravá ledvina musela být pro přetrvávající strikturu ureteru opakovaně stentována a vzhledem k tomu, že stentáže nevedly k ústupu obtíží a zlepšení nálezu na pravé ledvině, přistoupilo se na podzim roku 2010 k pokusu o autotransplantaci pravé ledviny do levé jámy kyčelní. Po 4 dnech došlo k selhání funkce štěpu, a proto bylo provedeno jeho chirurgické odstranění. Z histologického resekátu se jednalo o nekrózu tkáně ledviny, bez průkazu tumorózních změn či jiné patologie. Pacientka užívala mesalazin od doby diagnózy nemoci v dávce 4 g/den, intermitentně dle klinických obtíží prednison v dávce od 10–20 mg/den, dále pak azathioprin od roku 2003.
Do roku 2012 byla pacientka na zavedené medikaci relativně bez obtíží, kontrolní koloskopie neprokázaly aktivitu nemoci. Neměla bolesti břicha ani průjmy, nehubla. Od konce roku 2012 však došlo k postupnému zhoršování stavu, pacientka udávala až 10 hlenovitých stolic denně s pravidelnou příměsí krve, ubyla na váze (7 kg/3 měsíce), limitovaly ji i bolesti břicha vázáné na defekaci. Laboratorně byla zjištěna těžká sideropenická anémie (hemoglobin 66 g/l), hypalbuminemie (albumin 26 g/l) a vysoký kalprotektin (> 1 800 µg/g). Byla provedena koloskopie, která prokázala těžké postižení tračníku s endoskopicky průchodným zúžením v oblasti ileokolické anastomózy a s těžkým postižením neoterminálního ilea (Rutgeerts i4). Pacientka byla vzhledem k celkovému klinickému stavu a koloskopickému nálezu těžkého postižení tračníku a rekurence v neoterminálním ileu indikována k biologické terapii adalimumabem. Pro výše zmíněnou léčbu bylo rozhodnuto i vzhledem k preferencím pacientky a jejímu chabému perifernímu žilnímu přístupu. Byl podán ve standardním dávkování v kombinované terapii s azathioprinem. Stav pacientky se po indukční fázi biologické léčby částečně zlepšil, ustoupily bolesti břicha, ale přetrvávaly průjmy. V laboratorních odběrech nadále dominovala sideropenická anémie (hemoglobin 70 g/l, železo 5 µmol/l, feritin 4µg/l, saturace transferinu 3 %) a vysoký kalprotektin (1 800 µg/g). Kontrolní koloskopie prokázala úplné vyhojení transverza a descendens, ale přetrvávalo těžké zánětlivé postižení sigmatu a oblasti anastomózy. Z medikace byl pro neúčinnost vysazen azathioprin a přidán metotrexát, který však byl po 5 měsících vysazen pro inefektivitu. S odstupem několika měsíců u pacientky progredovaly křečovité bolesti břicha. Kontrolní koloskopie prokázala těsnou strikturu ileokolické anastomózy (obr. 1). Byla provedena endoskopická balonková dilatace (obr. 2), která měla u pacientky významnou klinickou odezvu, ustoupily bolesti břicha a celkově se cítila lépe. Druhé plánované sezení dilatace následovalo s odstupem několika týdnů, opět s výborným bezprostředním klinickým projevem. Vzhledem k nutnosti opakovaných endoskopických dilatací a ve snaze efekt těchto dilatací prodloužit jsme se rozhodli k zavedení biodegradabilního stentu do striktury. Samotný výkon proběhl bez zásadních komplikací, ale již den po výkonu došlo k migraci stentu do sigmatu pod obrazem ileózního stavu. Byla nutná endoskopická extrakce stentu. Koloskopie provedená na podzim 2013 znovu prokázala vysokou zánětlivou aktivitu v tračníku, kdy v sigmatu a descendens byly nalezeny hluboké vředy, celé lumen bylo stenotické a totální koloskopii jsme nebyli schopni provést ani v celkové anestezii pro riziko perforace (obr. 3). Vzhledem k výrazné intraluminární aktivitě nemoci a farmokologicky dále neřešitelné chorobě byla pacientka indikována k operačnímu výkonu. V lednu 2014 byla provedena resekce stenotické anastomózy s ileoascendentoanastomózou a levostrannou hemikolektomií s transverzosigmoideoanastomózou. Koloskopie provedená pro rozvoj pooperačního ilea ukázala reziduální vysoce aktivní zánětlivé postižení v oblasti sigmoidea a transverza a volně prostupné obě anastomózy. Vzhledem k endoskopickému nálezu, rizikovému profilu pacientky a předchozímu selhání léčby adalimumabem byla časně po operaci zahájena biologická léčba infliximabem. Přes podávanou léčbu došlo znovu k postupnému zhoršení klinického stavu, a proto byl infliximab po 6 měsících vysazen a byla zahájena systémová kortikoterapie. Po vyčerpání všech dostupných léčebných možností u pacientky refrakterní k anti-TNF léčbě, s rozvinutou kortikodependencí, bylo přistoupeno k léčbě vedolizumabem. Vedolizumab byl podán v doporučeném dávkovacím indukčním režimu 300 mg léčiva v intravenózní infuzi v 0., 2., 6. a 10. týdnu a nadále je podáván každých 8 týdnů. Aktuálně je pacientka po roční léčbě vedolizumabem bez obtíží, má dvě formované stolice za den, váhově přibrala (5 kg/12 měsíců) a cítí se velmi dobře. Kortikoidy byly postupně zcela vysazeny. Laboratorně došlo k normalizaci výrazné sekundární anémie (aktuální hemoglobin 123 g/l), která si vyžádala opakované krevní převody a parenterální substituce železa. Koloskopicky (únor 2017) je bez známek rekurence nemoci (obr. 4–6).
Image 1. Striktura ileokolické anastomózy. Fig. 1. Stricture of ileocolic anastomosis. 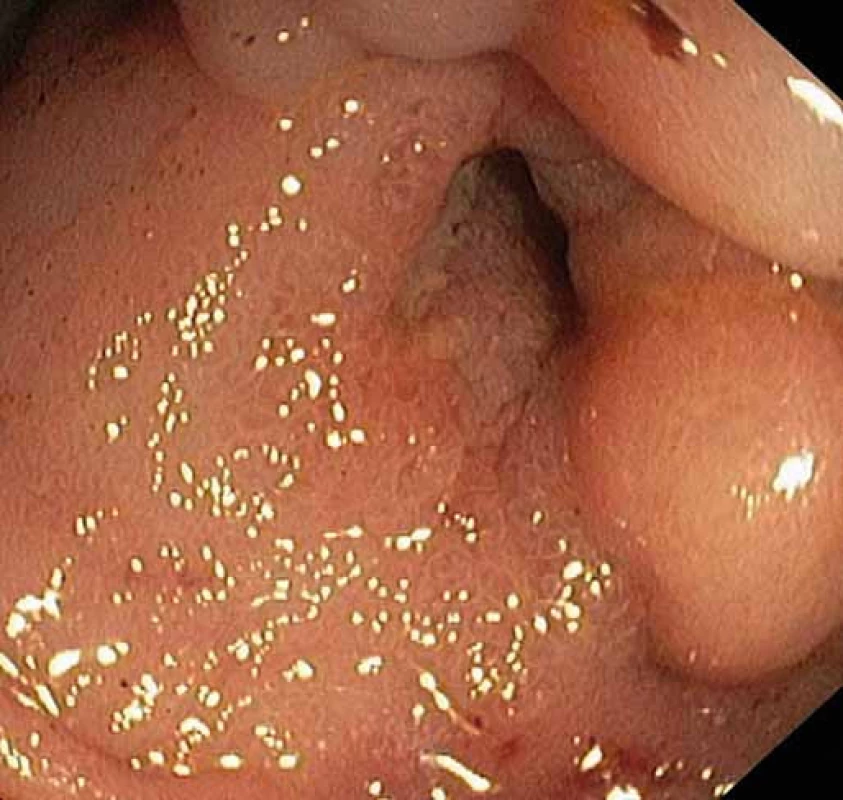
Image 2. Striktura ileokolické anastomózy po endoskopické balonkové dilataci. Fig. 2. Stricture of ileocolic anastomosis after endoscopic ballon dilatation. 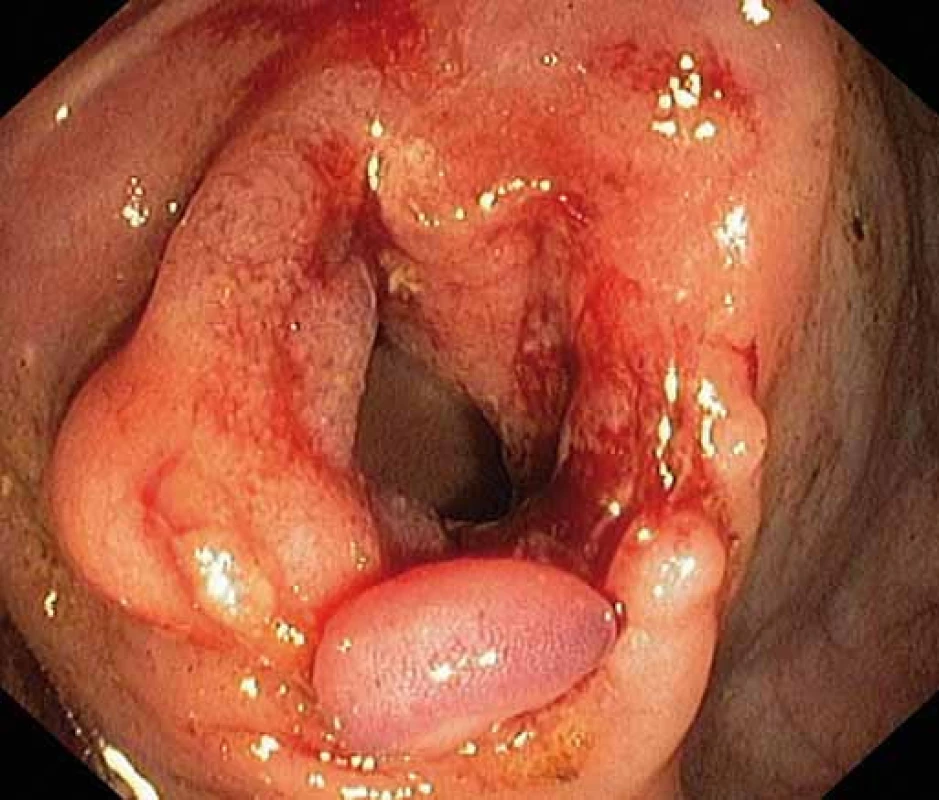
Image 3. Endoskopický obraz vysoké zánětlivé aktivity v tračníku, stenotické lumen neprostupné pro endoskop (hluboké vředy převážně sigmatu) pro riziko perforace. Fig. 3. Endoscopic image of high inflammatory activity in the colon, stenotic lumen (deep ulcer predominantly in sigmoideum), not accessible with endoscope because of a high risk of perforation. 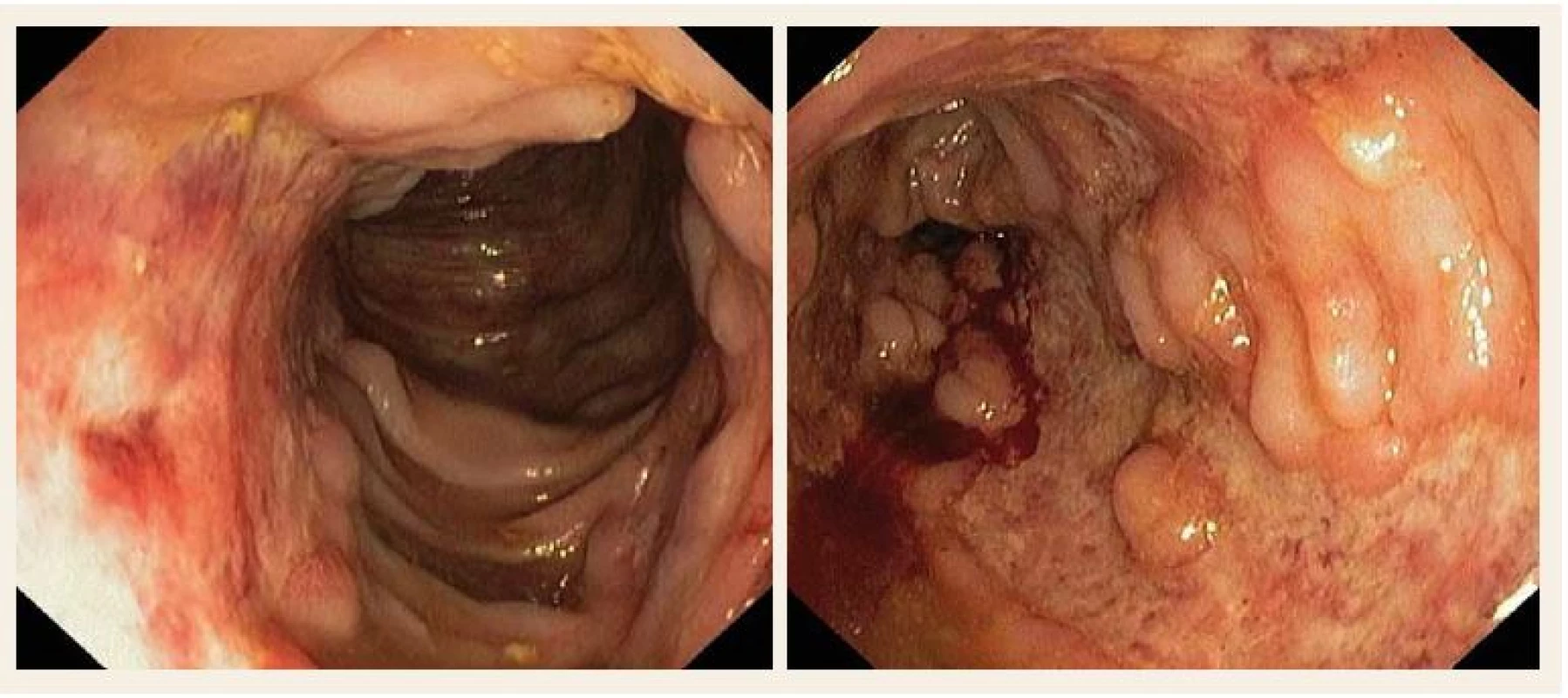
Image 4. Koloskopicky bez známek rekurence nemoci – oblast ileokolické anastomózy. Fig. 4. Coloscopic image without evidence of disease recurrence – ileocolic anastomosis. 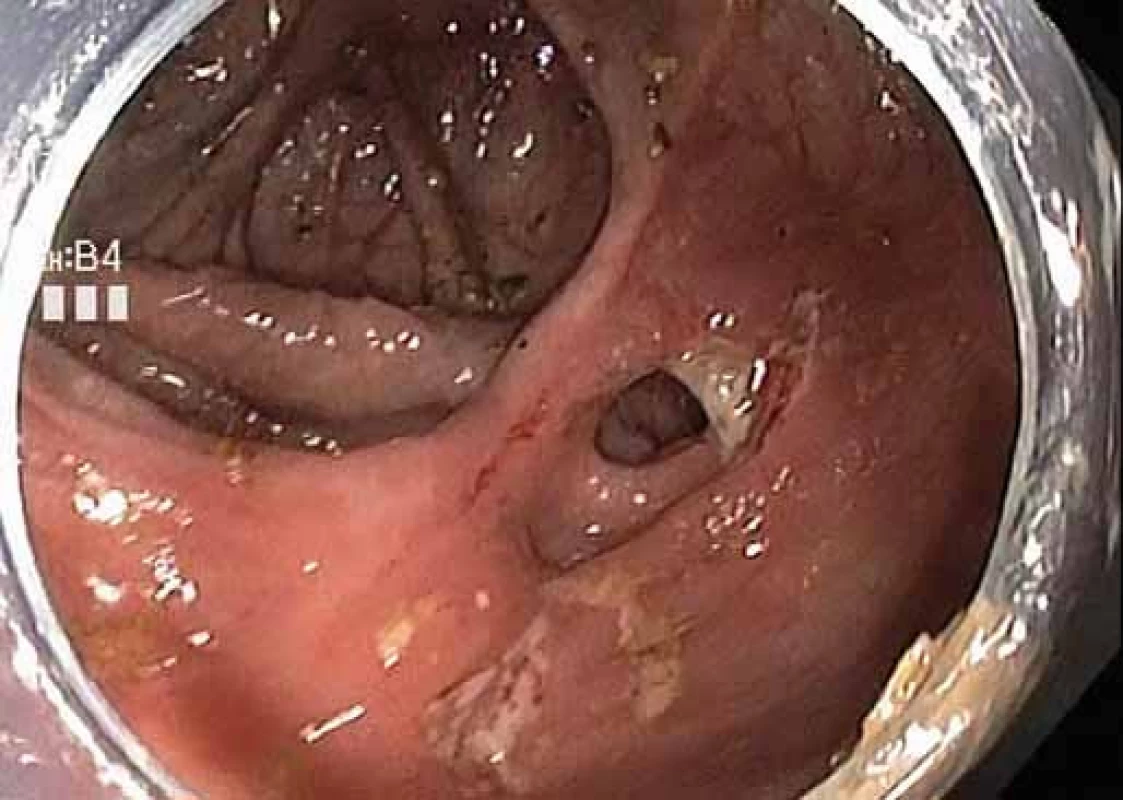
Image 5. Normální nález po 5měsíční léčbě vedolizumabem, tlusté střevo. Fig. 5. Normal finding after 5 months of treatment with vedolizumab, large intestine. 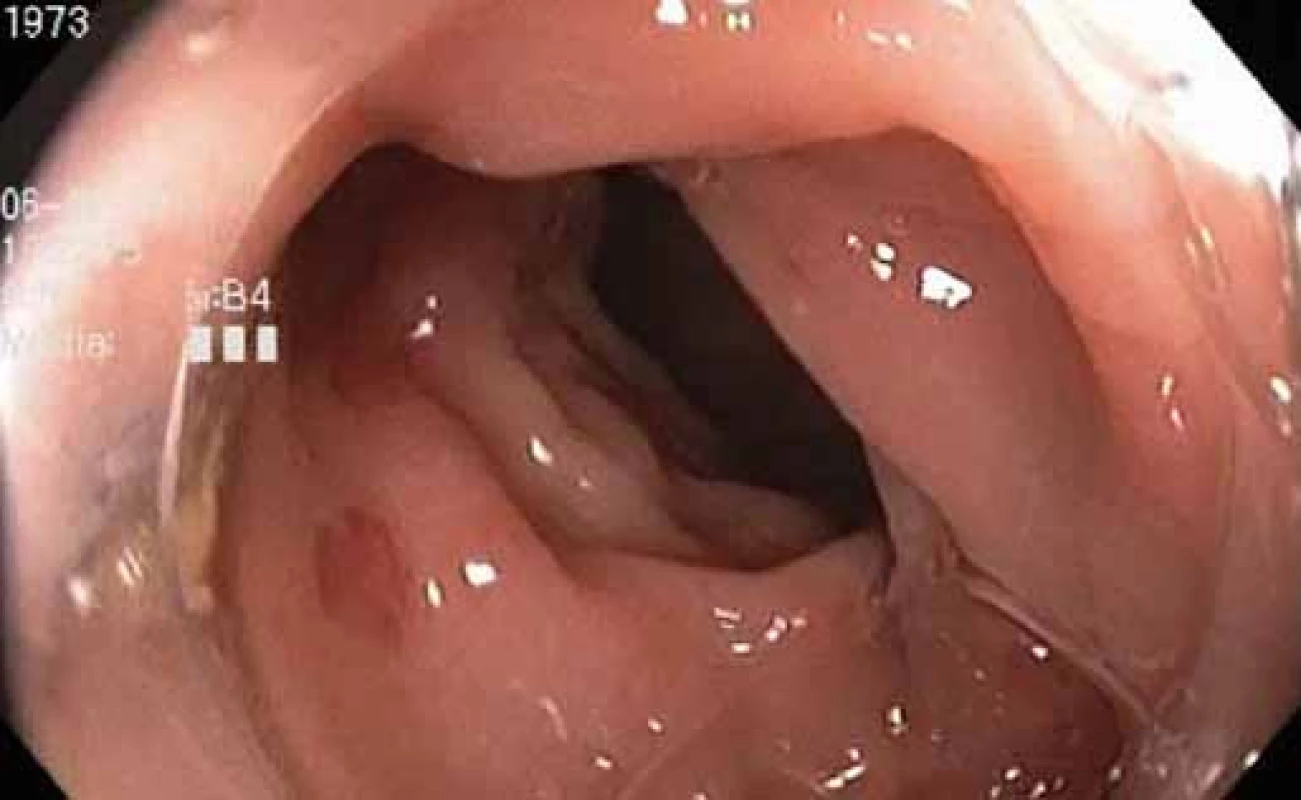
Image 6. Neoterminální ileum s klidovým nálezem po 5měsíní léčbě vedolizumabem. Fig. 6. Healed neoterminal ileum with finding after 5 months of treatment with vedolizumab. 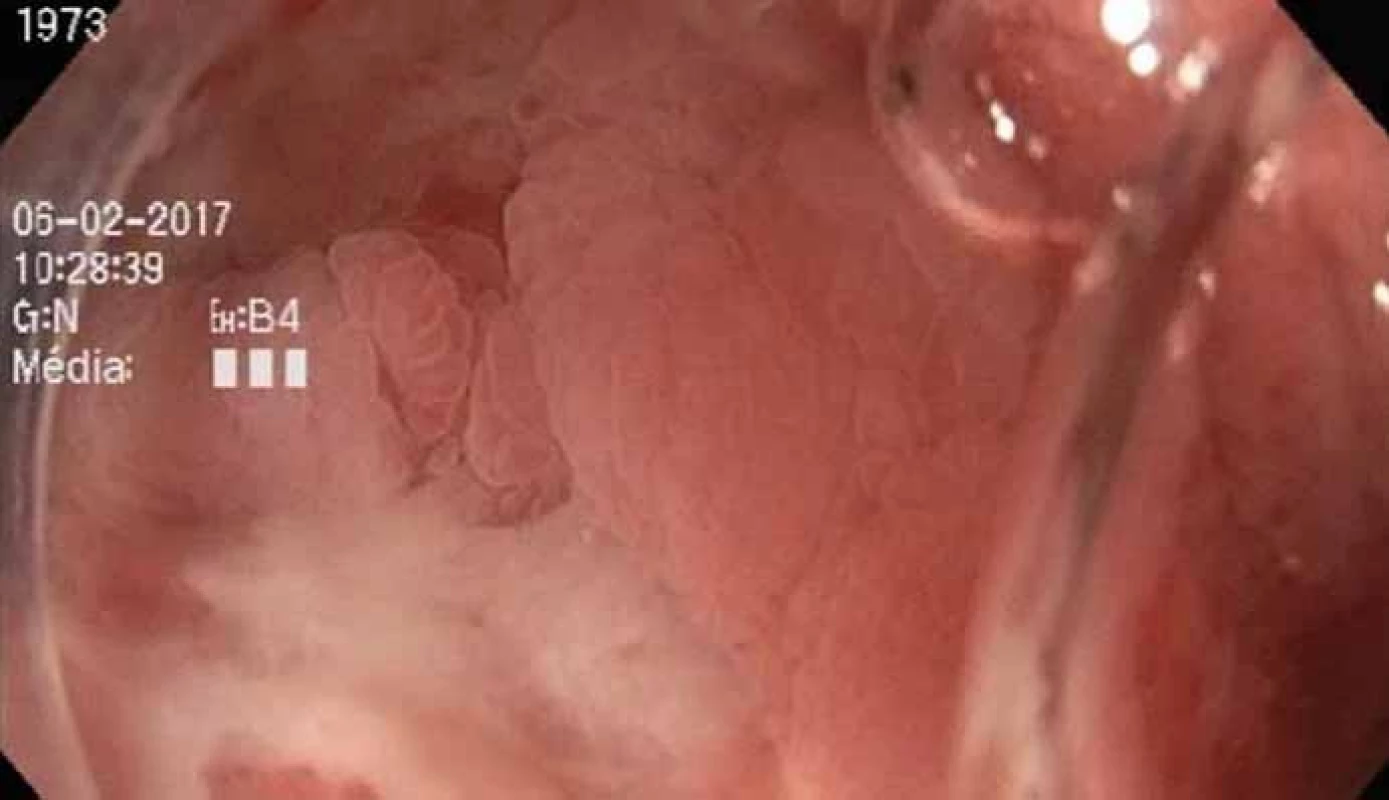
Diskuze
CD má u prezentované pacientky velmi těžký a komplikovaný průběh, došlo k selhání dosavadní farmakologické léčby vč. anti-TNF terapie a k rozvoji kortikodependence. Indikace k rozsáhlému operačnímu řešení u takto komplikovaného průběhu nemoci bylo jediným možným východiskem. Jednalo se o záchrannou operaci pro těžkou intraluminární, ale farmakologicky neřešitelnou chorobu. Operačním výkonem se odstranila stenotická anastomóza, která činila pacientce výrazné pasážové obtíže, byla vytvořena nová ileokolická anastomóza a současně byla provedena levostranná hemikolektomie, kdy se odstranila zánětem nejvíce postižená a stenotizující část tlustého střeva. Za jisté riziko můžeme považovat založení dvou anastomóz (ileoascendento-a transverzosigmoideoanastomózy), ale díky nim došlo k zachování funkční části tlustého střeva.
Na bezpečnost a účinnost vedolizumabu byly provedeny rozsáhlé klinické studie u nemocných s ulcerózní kolitidou (UC) a CD [1,2]. Projekt označený názvem GEMINI zahrnoval několik tisíc nemocných s idiopatickými střevními záněty a proběhl ve třech stovkách center na pěti kontinentech [3,4]. Fáze studie GEMINI III sledovala pacienty s CD, u nichž selhala předcházející anti-TNF léčba [5].
Dnes je již k dispozici řada prací, které hodnotí léčbu vedolizumabem v klinické praxi a které jsou nezbytné pro posouzení účinnosti přípravku. Informace o dlouhodobém sledování v klinické praxi zatím nejsou k dispozici, data se tedy týkají hlavně indukčních fází léčby a zatím potvrzují výsledky studií GEMINI.
Účinnost léčby vedolizumabem s ohledem na předcházející léčbu anti-TNF protilátkami u pacientů s CD hodnotila metaanalýza tří studií, která zahrnovala 1 716 pacientů s těžkým průběhem CD [6]. Cílem bylo zjistit poměr nemocných na terapii vedolizumabem, kteří dosáhli klinické odpovědi v 8. týdnu od zahájení léčby. Metaanalýza potvrdila, že účinnost vedolizumabu je v indukci remise vyšší oproti placebu a léčba je účinnější u nemocných po selhání předcházející anti-TNF léčby.
Účinnost a bezpečnost vedolizumabu ve fázi indukce u celkem 173 pacientů s CD a 121 s UC, u kterých selhala anti-TNF léčba, prospektivně sledovali Amiot et al [7]. Podíl klinických remisí (týden 6 a 14) byl u obou skupin srovnatelný, benefit podávané konkomitantní terapie nebyl prokázán.
Využití biodegradabilních stentů u pacientů s CD a s fibrotickou strikturou je metodou experimentální, která není v běžné klinické praxi rutinně využívána. Zavedení stentu je ke zvážení u pacientů, kteří těží z opakovaných endoskopických balonkových dilatací. Je potřeba si uvědomit vysoké riziko migrace stentu a tuto metodu nelze považovat za standardní terapii fibrotického postižení. Soubor 11 pacientů se stenotizující CD prezentovali v prospektivní studii Rejchrt et al publikované v časopise Endoscopy v roce 2011 [8]. U tří pacientů z tohoto souboru došlo k migraci stentu, u dvou po 2 dnech, u třetího po 8 týdnech. Další vývoj a zlepšování designu jednotlivých stentů by mohl do budoucna limitovat jejich vycestování. Obdobnou práci prezentovali v roce 2016 Karstensen et al, opět však na malém souboru pacientů. Uvádí zavedení biodegradabilního stentu u pěti pacientů, k migraci stentu došlo u jednoho pacienta ze souboru [9].
Závěr
Cílem této kazuistiky je prezentovat případ pacientky s těžce a komplikovaně probíhající CD refrakterní k imunosupresivní i anti-TNF terapii, po komplikovaných resekčních výkonech, po opakovaných endoskopických balonkových dilatacích ileocekální anastomózy, po zavedení biodegradabilního stentu do krátké fibrotické stenózy a jeho následnou migrací, s rozvinutou kotikodependencí. Upozorňujeme na možnost využití nové biologické terapie vedolizumabem, jehož jedinečnost tkví v odlišném mechanizmu účinku oproti anti-TNF terapii a díky jeho selektivitě i v dobrém bezpečnostním profilu. Vzhledem k pomalému nástupu účinku ve srovnání s jinými biologickými léčivy je většinou nutné pacienty léčit kortikoidy a ty postupně vysazovat až po předpokládaném nástupu účinku. Naše kazuistika demonstruje účinnost vedolizumabu u komplikované formy intraluminární CD. Pacientka je po roční léčbě vedolizumabem v hluboké remisi onemocnění.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 9. 8. 2017
Přijato: 27. 9. 2017
MUDr. Barbora Pipek
Centrum péče o zažívací trakt
Vítkovická nemocnice, a. s.
Zalužanského 1192/15
703 84 Ostrava
Sources
1. Lukáš M. Vedolizumab v léčbě Crohnovy choroby. Gastroent Hepatol 2015; 69 (2): 146–150. doi: 10.14735/amgh2015146.
2. Bortlík M. Vedolizumab – nová antiintegrinová protilátka s vysokou gastrointestinální selektivitou. Gastroent Hepatol 2014; 68 (6): 481–484. doi: 10.14735/amgh2014481.
3. Falt P. Léčba vedolizumabem u pacientů s idiopatickými střevními záněty v České republice. Gastroent Hepatol 2017; 71 (1): 19–23. doi: 10.14735/amgh201719.
4. Sandborn WJ, Feagan BG, Rutgeerts P et al. Vedolizumab as induction and maintence therapy for Crohn’s disease. N Engl J Med 2013; 369 (8): 711–721. doi: 10.1056/NEJMoa1215739.
5. Sands BE, Feagan BG, Rutgeerts P et al. Effects of vedolizumab induction therapy for pacients with Crohn’s disease in whom tumor necrosis factor antagonist treatment failed. Gastroenterology 2014; 147 (3): 618–627. doi: 10.1053/j.gastro.2014.05.008.
6. Lam MCW, Fu N, Bressler B et al. Vedolizumab for induction of remission in Crohn‘s disease in adults. A systematic review and meta analysis. JCC 2015: S227. Abstract P301.
7. Amiot A, Grimaud JC, Peyrin-Biroulet L et al. Effectiveness and safety of vedolizumab induction therapy for pacients with inflammatory bowel disease. Clin Gastroenterol Hepatol 2016; 14 (11): 1593–1601. doi: 10.1016/j.cgh.2016.02.016.
8. Rejchrt S, Kopacova M, Brozik J et al. Biodegradable stents for treatment of benign stenoses of small and large intestines. Endoscopy 2011; 43 (10): 911–917. doi: 10.1055/s-0030-1256405.
9. Karstensen JG, Christensen KR, Brynskov J et al. Biodegradable stents for the tratment of bowel strictures in Crohn‘s disease: technical results and challenges. Endosc Int Open 2016; 4 (3): E296–E300. doi: 10.1055/s-0042-101940.
Labels
Paediatric gastroenterology Gastroenterology and hepatology Surgery
Article was published inGastroenterology and Hepatology
2018 Issue 2-
All articles in this issue
- Akutní poškození ledvin u pacientů s akutní pankreatitidou
- Kombinace endoskopické slizniční resekce a „full-thickness“ resekce v léčbě adenomu ascendens s příznakem „non-liftingu“
- Populární sleeve gastrectomy – tubulizace žaludku v chirurgické léčbě těžké obezity a cukrovky 2. typu
- Esomeprazol – S-izomer omeprazolu s výhodnějšími farmakologickými vlastnostmi a silnějším farmakodynamickým účinkem
- Gastrointestinálne prejavy familiárnej stredomorskej horúčky – problém aj v strednej Európe?
- Životní jubileum prof. Zdeňka Marečka
- Pohľad na XXIII. Gastrofórum, Štrbské Pleso, 2018
- 6th Conference of Central European Hepatologic Col laboration
- Výběr z mezinárodních časopisů
- Hepatologie
- Primární biliární cholangitida – doporučený postup České hepatologické společnosti ČLS JEP pro diagnostiku a léčbu
- Neobvyklá příčina zvětšování břicha
- Terlipresin – stále nepostradatelný ve dvou indikacích
- Léčba komplikované Crohnovy choroby vedolizumabem
- Infekce jaterní cysty při polycystóze jater jako zdroj sepse
- Hepatocelulárny karcinóm na strednom Slovensku – analýza kohorty 207 pacientov v nemocnici 3. stupňa
- Gastroenterology and Hepatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Terlipresin – stále nepostradatelný ve dvou indikacích
- Primární biliární cholangitida – doporučený postup České hepatologické společnosti ČLS JEP pro diagnostiku a léčbu
- Infekce jaterní cysty při polycystóze jater jako zdroj sepse
- Neobvyklá příčina zvětšování břicha
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

