-
Medical journals
- Career
Nekrotizující enterokolitida v Perinatologickém centru FN Hradec Králové 2010–2017
Authors: Ondřej Dvořák 1; R. Štichhauer 2,3; A. Šafus 2,3; T. Matějek 1; J. Koudelka 2; Z. Kokštein 1,3; J. Malý 1,3
Authors‘ workplace: Dětská klinika, Fakultní nemocnice, Hradec Králové 1; Oddělení dětské chirurgie a traumatologie, Fakultní nemocnice, Hradec Králové 2; Lékařská fakulta, Univerzita Karlova, Hradec Králové 3
Published in: Čes-slov Pediat 2018; 73 (8): 486-493.
Category:
Overview
Úvod:
Nekrotizující enterokolitida (NEC) je závažné zánětlivé onemocnění postihující převážně nezralé novorozence. I přes pokrok v přístupu k takto ohroženým novorozencům, poznatkům v oblasti prevence a zlepšující se diagnostice, zůstává NEC jednou z vedoucích příčin mortality i morbidity předčasně narozených novorozenců.
Metodika:
Retrospektivní kohortová analýza.
Výsledky:
Ve spádovém regionu Perinatologického centra FN Hradec Králové se v letech 2010–2017 narodilo 100 233 novorozenců, z toho 7165 novorozenců s porodní hmotností <2500 g, 907 novorozenců s porodní hmotností <1500 g a 119 novorozenců s porodní hmotností <750 g. Klasifikace NEC (IIa a vyšší) dle modifikované Bellovy stupnice byla realizována při stanovení diagnózy, v průběhu konzervativní léčby mohla progredovat.
NEC byla diagnostikována v 86 případech (incidence 0,86 ‰). Incidence NEC v hmotnostní kategorii <1500 g byla v našem regionu 5,6 %, v hmotnostní kategorii <1000 g 10,5 %, u novorozenců s porodní hmotností <750 g 12,6 %. Letalita novorozenců s porodní hmotností <750 g dosahovala 53 %, u novorozenců s hmotností <1500 g 24,5 %; v celém souboru 86 pacientů s NEC činila 23 %. Letalita podle gestačního stáří byla ve skupině novorozenců narozených mezi 24. až 28. týdnem 33,3 %, u novorozenců narozených mezi 29. až 32. gestačním týdnem 22,7 % a ve skupině novorozenců narozených po 33. týdnu těhotenství 10,7 %. Stadium II jsme diagnostikovali celkem 58krát, stadium III 28krát.
Konzervativně bylo léčeno 22 pacientů, zbývajících 64 pacientů podstoupilo chirurgickou léčbu. Mezi chirurgicky léčenými pacienty byla souhrnná letalita 30 %, mezi konzervativně léčenými pacienty byla souhrnná letalita 4,5 %. Průměrná délka hospitalizace u konzervativně léčených pacientů byla 49 dní, u pacientů léčených chirurgicky 84 dní.
Závěr:
Výše uvedená data jsou srovnatelná s výsledky publikovanými v západní Evropě a Severní Americe. V posledních letech lze v našem souboru pozorovat trend mírného poklesu výskytu tohoto onemocnění, i tak zůstává nekrotizující enterokolitida velmi závažným onemocněním, které zásadně ovlivňuje přežití i dlouhodobou prognózu předčasně narozených novorozenců.
KLÍČOVÁ SLOVA:
NEC, operace, stomie, anastomóza, incidence
ÚVOD
Nekrotizující enterokolitida (NEC) je nejčastější etiologickou příčinou náhlé příhody břišní u novorozence. Jedná se o často perakutně progredující zánětlivé postižení trávicí trubice postihující především novorozence s nízkou porodní hmotností. První zmínky o chorobě nápadně připomínající dnešní NEC pocházejí z první poloviny 19. století [1], ale do širšího povědomí se onemocnění dostalo až s rozvojem novorozenecké intenzivní péče v posledních 50 letech. Prevalence kolísá napříč různými státy světa a dosahuje 7 % v kategorii dětí s porodní hmotností <1500 gramů s letalitou mezi 20–40 % [2–5]. Asi v 7–10 % postihuje donošené novorozence, ve zbylé většině se jedná o novorozence s nízkou porodní hmotností, přičemž incidence onemocnění stoupá s klesající porodní hmotností.
Přestože jde primárně o postižení trávicího traktu, mají postižení novorozenci výrazně zvýšené riziko neurovývojového opoždění [6, 7]. Kromě toho je intestinální resekce spojena s rizikem rozvoje syndromu krátkého střeva s celou řadou možných navazujících komplikací [8]. Přestože je NEC předmětem intenzivního výzkumu, jsou její patogeneze a hlavně příčiny rozvoje u jednotlivých konkrétních pacientů velmi nejasné [9] (tab. 1). I to je zřejmě důvodem, proč se léčba NEC za poslední 4 dekády prakticky nezměnila a přes velmi citelně vnímané nedostatky i nadále vychází z modifikované Bellovy klasifikace [10, 11].
Table 1. Uvažované faktory podílející se na rozvoji nekrotizující enterokolitidy. 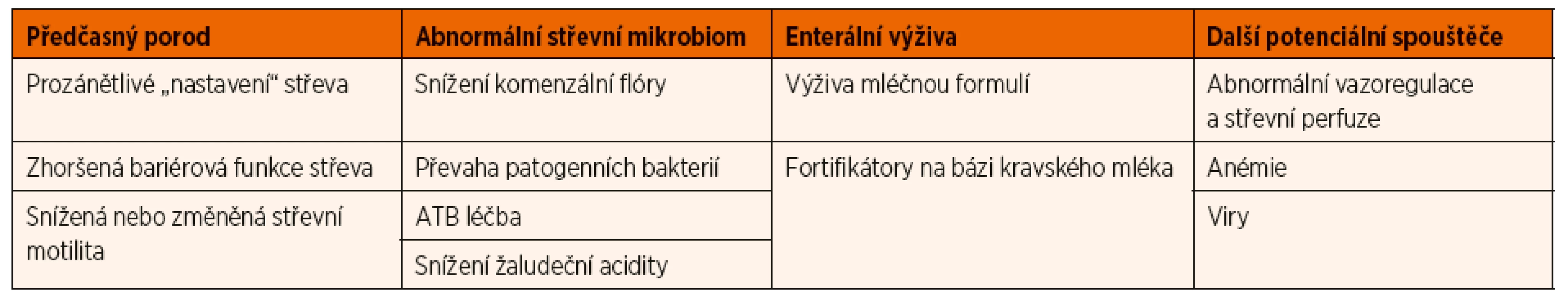
Onemocnění se prezentuje celou řadou nespecifických příznaků, přičemž vedoucí triádou bývá intolerance krmení/zvracení, distenze břicha a enteroragie. Kromě toho bývají pozorovány, podobně jako v případě jakékoliv jiné novorozenecké sepse, tachykardie/bradykardie, apnoe, poklesy saturace, poruchy prokrvení, teplotní nestabilita a další. Laboratorní parametry zánětu v iniciál-ní fázi onemocnění nemusí být zvýšené; prognosticky závažným znamením bývá leukopenie a prohlubující se metabolická acidóza, často provázená hyperglykémií. Patognomonickým, i když iniciálně mnohdy diskrétním, je nález pneumatosis cystoides intestini – PCI (pneumatosis intestinalis) a/nebo přítomnost plynu ve větvích v. portae (PVG) při nativním rentgenovém snímku břicha (obr. 1). Při nálezu pneumoperitonea je nutné odlišit, zda jde o NEC v pokročilém stadiu onemocnění, či nález volného vzduchu při spontánní intestinální perforaci, což je stav klinicky, patofyziologicky i prognosticky zcela odlišný od NEC. V rukou zkušeného sonografisty poskytuje obdobný nález i ultrazvukové vyšetření břicha [12].
Image 1. Nativní RTG s nálezem NEC – červené šipky označují PCI (pneumatosis cystoides intestini), modrá šipka znázorňuje přítomnost plynu ve větvích v. portae (PVG).
Fig. 1. Abdominal X-ray in NEC patient. Intramural bowel gas (PCI) – red arrows; gas in the branches of portal vein (PVG) – blue arrow.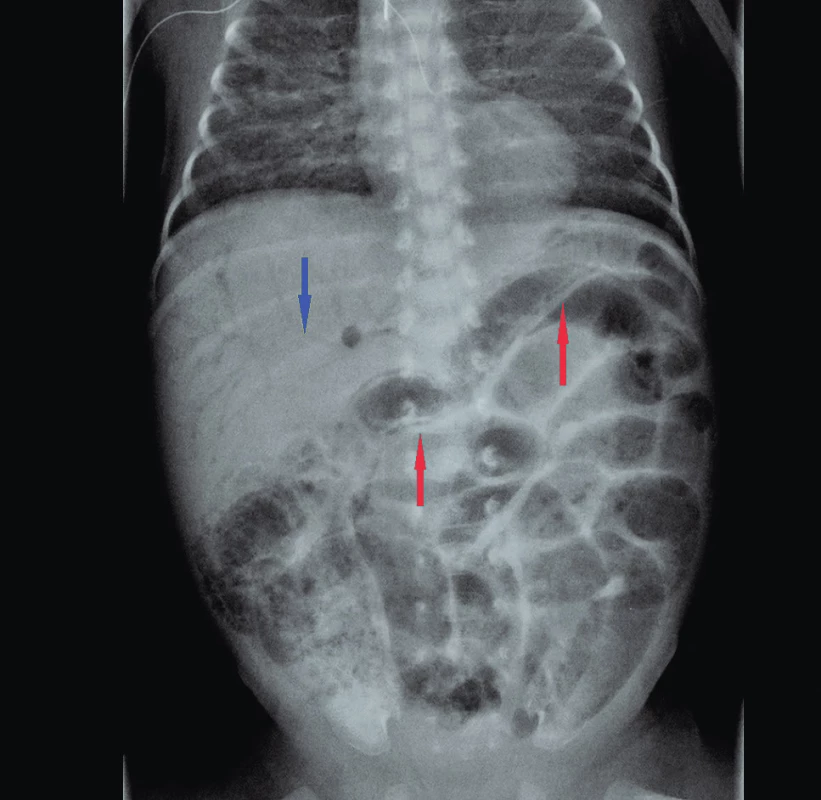
Léčba nekrotizující enterokolitidy je s ohledem na stadium onemocnění a stav pacienta konzervativní (přerušení krmení, zavedení žaludeční sondy k dekompresi, podání antibiotik, podpora oběhu/ventilace, léčba poruch vnitřního prostředí včetně DIC), resp. konzervativní rozšířená o léčbu chirurgickou. Nejčastějším operačním výkonem je resekce postiženého nekrotického střevního úseku s následným vyvedením enterostomie k derivaci trávicího traktu, event. je střevní resekce následována primární střevní anastomózou se zachováním konti-nuity GIT. Jako jedna ze stále využívaných chirurgických metod je popisována primární drenáž břišní dutiny, a to buď jako izolovaný výkon, nebo následována klasickou laparotomií [3, 13].
Přestože není NEC vzácným onemocněním na novorozeneckých odděleních s JIRP, je velmi nesnadné získat v domácím písemnictví informace o prevalenci event. výsledcích péče v ČR [14, 15]. Cílem předkládané práce je proto zhodnocení základních epidemiologických dat a výsledků péče v Perinatologickém centru FN Hradec Králové v letech 2010–2017.
MATERIÁL A METODA
Předkládaná práce je retrospektivní observační kohortovou studií. Soubor tvoří pacienti hospitalizovaní a léčení pro nekrotizující enterokolitidu na Dětské klinice LF UK a FN Hradec Králové v letech 2010–2017. Nekrotizující enterokolitida byla definována jako onemocnění ve stadiu IIa a vyšším dle modifikované Bellovy klasifikace [11] (tab. 2). Onemocnění bylo klasifikováno při stanovení diagnózy, v dalším průběhu konzervativní léčby mohlo progredovat. Informace o pacientech byly získány z prospektivně vedené databáze jednoho z autorů (JM) a dále ze zdravotnické dokumentace jednotlivých pacientů. Rentgenová obrazová dokumentace byla získána z archivu Radiologické kliniky FN Hradec Králové a peroperační fotodokumentace z obrazového archivu Oddělení dětské chirurgie a traumatologie FN Hradec Králové. Data o lokalizaci onemocnění byla získána z operačních protokolů chirurgicky léčených pacientů.
Table 2. Modifikovaná Bellova kritéria stupňů NEC (dle Walsheové a Kliegmanna). 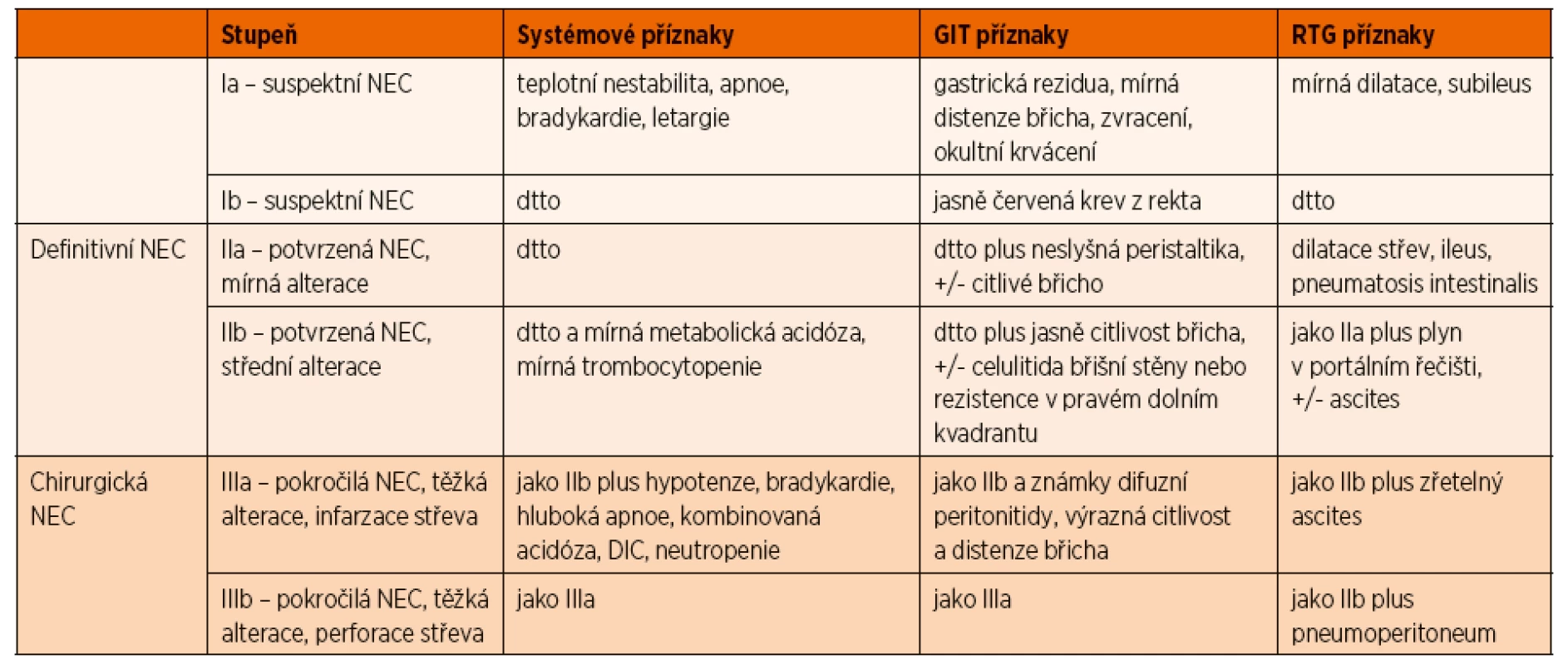
Upraveno dle Kalousová J, Fryč R. In: Šnajdauf J, Škába R. Dětská chirurgie. Praha: Galén, 2005 [16]. VÝSLEDKY
Ve spádovém regionu Perinatologického centra FN Hradec Králové se v letech 2010–2017 narodilo 100 233 novorozenců, z toho 7165 novorozenců s porodní hmotností <2500 g. 907 novorozenců mělo porodní hmotnost <1500 g, 119 novorozenců mělo porodní hmotnost <750 g. NEC ve stadiu IIa a vyšší byla diagnostikována v 86 případech (incidence 0,86 ‰). Medián porodní hmotnosti byl u našich pacientů 1285 (440–3290) gramů, medián gestačního věku 30 (24–40) gestačních týdnů. Medián postnatálního stáří při stanovení diagnózy byl 11 (1–101; interkvartilové rozpětí (IQR) 6–22) dní.
Stadium onemocnění IIa nebo IIb bylo iniciálně diagnostikováno v 58 případech (67 %), stadium IIIa nebo IIIb ve 28 (33 %) případech, přičemž četnost nejzávažnějších stadií s klesající porodní hmotností stoupala. V kategorii gestačně nejmladších dětí (24.–28. gestační týden) byla NEC diagnostikována iniciálně již ve stadiu IIIa/b ve 39 % případů.
Incidence NEC v hmotnostní kategorii <1500 g byla v našem regionu 5,6 % (51 případů), v hmotnostní kategorii <1000 g 10,5 % (33 případů), u novorozenců s porodní hmotností pod 750 g 12,6 % (15 případů). Děti >2500 g tvořily jen 5,8 % souboru.
U všech pacientů byla zahájena konzervativní léčba, u 64 (74 %) pacientů byla pro progresi onemocnění rozšířena o léčbu chirurgickou. Padesát pět (86 % z chirurgicky léčených) pacientů z našeho souboru bylo ošetřeno resekcí postiženého úseku střeva a vyvedením terminální stomie s ponecháním slepě uzavřeného aborálního úseku střeva. Šest (9 %) pacientů bylo ošetřeno vyvedením odlehčovací stomie bez nutnosti resekce postiženého úseku. Tři (5 %) pacienti podstoupili diagnostickou laparotomii bez resekce vzhledem k postižení celé délky tenkého a tlustého střeva (infaustní nález). Lokalizace postižení GIT ilustruje graf 1.
Graph 1. Lokalizace postižení/nekrózy pacientů s NEC. 
Z celého soboru 86 pacientů zemřelo 20 dětí. Letalita novorozenců s porodní hmotností <750 dosahovala 53 % (8 pacientů), ve skupině pacientů s porodní hmotností <1000 g 33 % (11 pacientů), u novorozenců s hmotností <1500 g 24,5 % (12 pacientů) a v celém souboru činila 23 %. Letalita podle gestačního stáří byla ve skupině novorozenců narozených mezi 24.–28. týdnem 33,3 % (12 pacientů), u novorozenců narozených mezi 29.–32. gestačním týdnem 22,7 % (5 pacientů) a ve skupině novorozenců narozených po 33. týdnu těhotenství 10,7 % (3 pacienti). U přeživších pacientů byla následně s odstupem 2–3 měsíců provedena druhá operace s obnovením kontinuity GIT. Mezi chirurgicky léčenými pacienty byla souhrnná letalita 30 %, mezi konzervativně léčenými pacienty byla souhrnná letalita 4,5 %. Průměrná délka hospitalizace u konzervativně léčených pacientů byla 49 dní (10–101 den), u pacientů léčených chirurgicky 84 dní (2–357 dní).
DISKUSE
Nekrotizující enterokolitida zůstává přes dramatické zlepšení výsledků porodnické a neonatologické péče extrémně závažným onemocněním s letalitou přesahující 25 %. Kromě toho má řada přeživších pacientů dlouhodobé následky, ať už ve smyslu postižení GIT (syndrom krátkého střeva) nebo neurovývojového opoždění, kognitivních a zrakových poruch [6, 7, 16, 17]. Onemocnění je rovněž typické i tím, že přichází v období po zvládnutí respiračních a oběhových problémů v prvních dnech života, kdy se již může zdát, že obavy o život předčasně narozeného dítěte jsou zažehnány. Při incidenci 10 % v kategorii dětí <1000 g dosahují v USA každoročně náklady na akutní péči o takto nemocné děti 1 miliardy USD [5, 13, 18]. Nejen to je samozřejmě důvodem, proč je nekrotizující enterokolitida jedním z hlavních témat výzkumu v neonatologii vůbec. Přesto je situace našeho poznání tohoto onemocnění vysloveně skličující a z pohledu klinika lze uvést, že se péče o děti s nekrotizující enterokolitidou od roku 1978 nezměnila vůbec. Tím nejkomplikovanějším bodem v situaci kolem nekrotizující enterokolitidy je naše zásadní neschopnost přesně definovat a přesně diagnostikovat nekrotizující enterokolitidu. Je totiž možné, že klinický, rentgenologický i patologický obraz v sobě sdružuje několik onemocnění aktivovaných celou řadou možných spouštěčů navenek se manifestujících „syndromem nekrotizující enterokolitidy“ [19].
Je obecně akceptovanou skutečností, že NEC je multifaktoriálně podmíněným zánětlivým procesem, přičemž specifická příčina onemocnění je neznámá. Hlavním rizikovým faktorem je závažnost vlastní nezralosti a nízká porodní hmotnost. V kategorii dětí <1000 g, a zvláště dětí <750 g, je incidence NEC nejvyšší; rovněž je v této kategorii nejvyšší frekvence potřeby chirurgického řešení onemocnění (60–70 %) s nejvyšší letalitou (40–52 %) [3]. Data z našeho sledování jsou s citovanou prací ve shodě. Ve sledovaném období 8 let byl v našem regionu výskyt NEC v kategorii dětí <1500 g 5,6 %. I tento údaj dobře koreluje s literárními daty.
Velmi zajímavou skutečností je fakt, že incidence nekrotizující enterokolitidy značně kolísá mezi jednotlivými rozvinutými státy světa. Battersbyová v recentní systematické souhrnné práci uvádí, že rozdíl v incidenci NEC v kategorii dětí <1000 g je až pětinásobný [4]. Absolutně nejnižší frekvence onemocnění je známa z Japonska, kde i u dětí narozených před 28. gestačním týdnem dosahuje jen 2 %. V této kategorii jsou data východočeského regionu obdobná incidenci známé z Austrálie a Nového Zélandu, Kanady, USA a Španělska. Nižší incidence NEC je kromě Japonska známa ze Švýcarska, Švédska a Německa, byť v citované práci byla použita odlišná diagnostická kritéria. Na druhé straně, vyšší incidence v kategorii dětí <1500 g je známa z USA, Kanady, Jižní Koreje nebo Polska [3, 4]. S ohledem na výše uvedené se nabízí otázka, zdali jsou uvedené rozdíly způsobeny modifikovatelnými faktory a existuje-li případný prostor pro klinické lékaře i výzkumníky, které by mohly vést ke snížení incidence NEC.
Kromě nezralosti a nízké porodní hmotnosti bylo na základě observačních i randomizovaných kontrolovaných studií vysloveno podezření na desítky dalších rizikových faktorů i několik možných protektivních vlivů. Řada těchto prací přinesla protichůdné názory, přičemž je opět možné, že tato rozporuplnost byla spojena s nejednoznačností v diagnostice. V současnosti spíše nezpochybňované rizikové a protektivní faktory jsou shrnuty v tabulce 3 [20].
Table 3. Rizikové a protektivní faktory NEC, upraveno dle Rose AT. [20]. ![Rizikové a protektivní faktory NEC, upraveno dle Rose AT. [20].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/43723af3480dbbd3bfba490906c56dee.png)
PPROM – předčasný prolongovaný odtok plodové vody; IUGR – intrauterinní růstová restrikce; VVV – vrozená vývojová vada; GIT – gastrointestinální trakt; ATB – antibiotika; SpO2 – saturace kyslíku I když v čase dochází ke zlepšování péče o nedonošené novorozence, zůstávají výsledky péče o děti s NEC velmi špatné, zvláště v kategorii dětí narozených s hmotností <750 g. Onemocnění u těchto dětí má často perakutní průběh a rozvoj multiorgánového selhání (MODS) je v řadě případů otázkou několika desítek minut. V našem pozorování byla diagnóza onemocnění stanovena v téměř 40 % případů ve stupni IIIa/IIIb modifikovaných Bellových kritérií – tedy ve fázi chirurgické NEC. Smrtnost přesahující 50 % je bohužel opět obdobná výsledkům rozsáhlé práce ze sítě pracovišť zahrnutých do Vermont Oxford Network (VON) hodnotící výsledky péče u více než 17 000 novorozenců léčených pro NEC [3]. Úmrtí na nekrotizující enterokolitidu není bohužel zcela vyloučeno ani u podstatně větších a gestačně starších dětí, a to přes velmi aktivní přístup našeho pracoviště.
Přes „archaičnost“ Bellových kritérií jde i dnes o nástroj použitelný pro rozhodování o léčebném přístupu. NEC ve stadiu IIa je léčena konzervativně, ve stadiu IIb/IIIa konzervativně i chirurgicky a ve stadiu IIIb chirurgicky. V kontrastu s literárními daty byla v našem souboru operována většina dětí s NEC. Tato skutečnost může vypovídat o 1) velmi aktivním přístupu celého operačního týmu, 2) velké kohortě velmi závažně nemocných dětí či 3) časné nebo dokonce předčasné indikaci operace u dětí, jejichž onemocnění teoreticky mohlo být zvládnuto konzervativně. Asi nejsme schopni příliš dobře posoudit, zdali v našem souboru byly děti se závažněji probíhající NEC; na druhé straně 39 % z chirurgicky léčených pacientů bylo indikováno k neodkladné revizi pro pneumoperitoneum. Všichni ostatní pacienti byli indikováni k operaci pro progresi onemocnění vzdor komplexní konzervativní léčbě. Načasování operace je velmi složité. Je maximální snahou našeho pracoviště indikovat pacienty k operaci ve fázi chirurgického, konzervativně nezvládnutelného onemocnění, nicméně pokud možno ještě před perforací střeva a rozvojem těžkého stavu s MODS. Názor o možné předčasnosti takového přístupu je jistě legitimní. I proto jsme se rozhodli prezentovat klinická data pacientů (tab. 4), u nichž se chirurg v průběhu operace nerozhodl provést resekci střeva (v okamžiku operace nedokončená nekróza) a pouze vyvedl enterostomii k jeho dekompresi. Letalita konzervativně léčených dětí v našem souboru byla extrémně nízká v porovnání s již citovanou prací databáze VON [3] i dalšími. Rovněž tento údaj nasvědčuje ne zcela všeobecně samozřejmé snaze poskytnout všem dětem možnost chirurgického ošetření, bez ohledu na závažnost vlastní prematurity či rozvoj MODS [13]. Jediný neoperovaný a zemřelý pacient našeho souboru se na operační sál nedostal pro rozvoj šokového stavu s nezvládnutelným cirkulačním kolapsem. Pitevní vyšetření následně prokázalo asi 10cm nekrózu tlustého střeva bez perforace.
Table 4. Klinické a operační nálezy u operovaných pacientů bez resekce, u všech pacientů vyvedena enterostomie k dekompresi GIT. Pacient Indikace 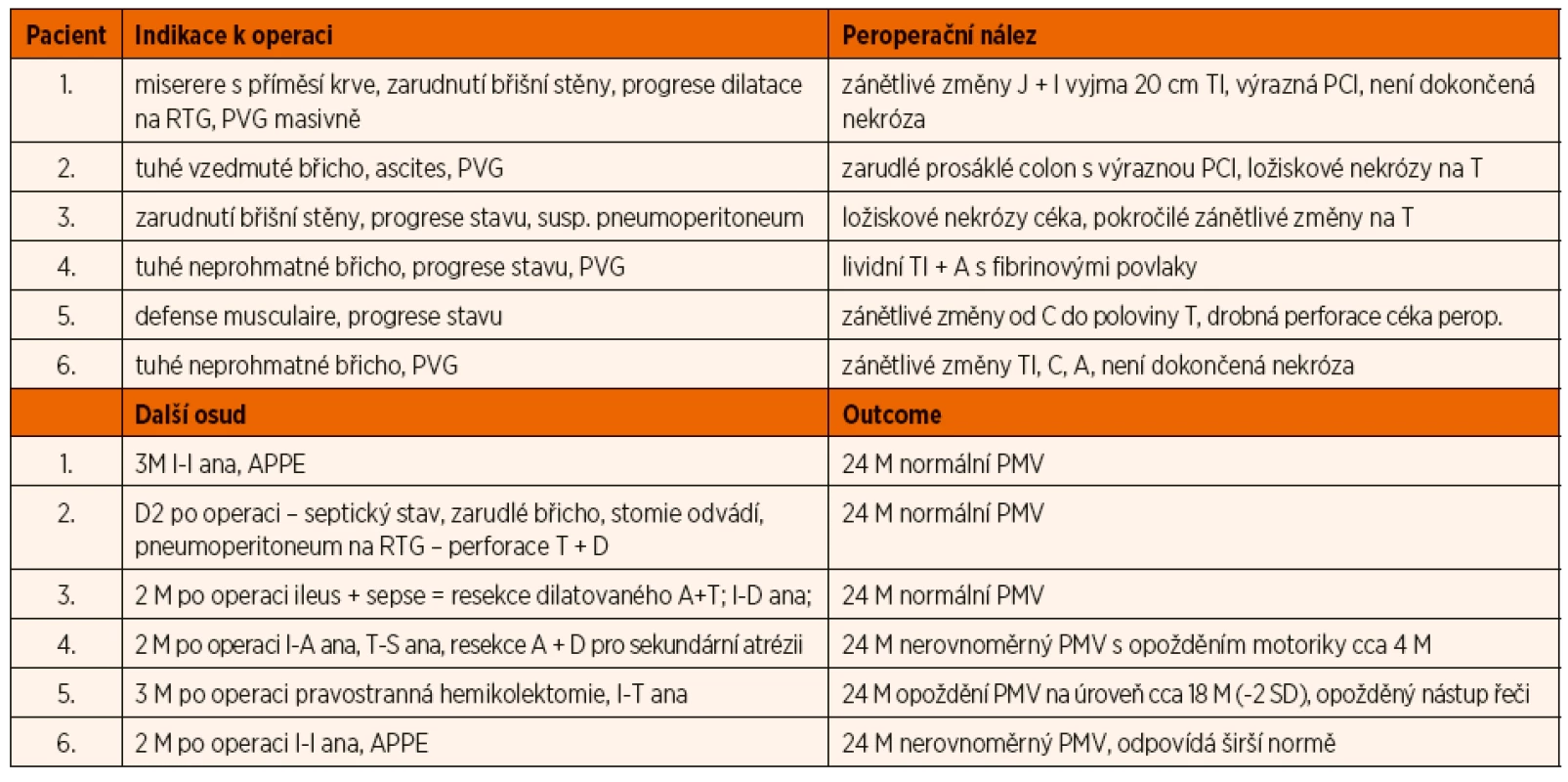
PVG – plyn ve větvích v. portae; PCI – pneumatosis cystoieis intestini; J – jejunum; I – ileum; TI – term. ileum; C – cékum; A – ascendens; T – transversum; D – descendes; M – měsíc; D – den; PMV – psychomotorický vývoj; M – měsíc; D – den; I-I/I-T/I-D ana – ileo-ileo/ileo-transverso/ ileo-descendentní anastomóza; APPE – apendektomie Chirurgická léčba nastupuje v případě neúspěchu konzervativní léčby nebo při fulminantně probíhající formě nekrotizující enterokolitidy. Timing operačního výkonu zůstává nejsložitějším bodem vlastní chirurgické léčby. Absolutní indikací k operační léčbě je pneumoperitoneum při RTG vyšetření. Tento nález ale nicméně ve většině případů znamená již velmi pokročilou formu onemocnění, která zvyšuje další perioperační rizika. Otázkou tedy zůstává, jestli operovat novorozence s NEC až při přítomnosti pneumoperitonea.
Podle našich zkušeností a některých literárních odkazů je vhodné operovat pacienta v relativně stabilizovaném stavu, ideálně ve fázi demarkované nekrózy [16, 21] (obr. 2). I proto je nutná úzká spolupráce neonatologa s dětským chirurgem, jejichž konsenzuální stanovisko by mělo vést k indikaci operace, např. v situaci progrese stavu navzdory maximální konzervativní léčbě. Rovněž tak považujeme za vhodné indikovat k operaci pacienta s ileem a obrazem fixované střevní kličky při sériovém RTG vyšetření. Varovným znamením svědčícím pro progredující NEC bývá zarudnutí břišní stěny, případně přítomnost hmatné fixované rezistence. Na druhou stranu si je nutné uvědomit, že transport na operační sál, vlastní anestezie i operační výkon je velkou zátěží pro nedonošeného novorozence s možnými komplikacemi a negativním dopadem na jeho další vývoj.
Image 2. Peroperační nález střevní nekrózy u NEC.
Fig. 2. Intestinal necrosis in surgically treated patient.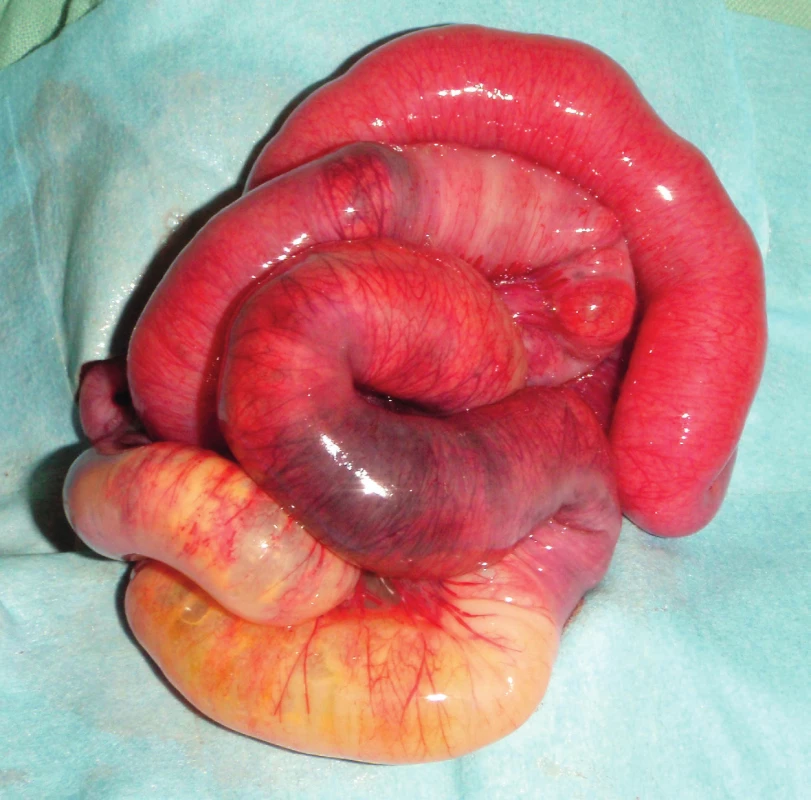
Chirurgická léčba spočívá v operační revizi dutiny břišní. Podle peroperačního nálezu je následována resekcí nekrózou postiženého úseku trávicí trubice. Tento výkon následovaný dekompresí GIT formou terminální stomie na nepostiženém úseku orálně od nekrózy je nejběžnějším výkonem prezentovaným v našem souboru. Výhodou tohoto postupu je krátký operační čas, který snižuje perioperační zátěž pro pacienta v akutní fázi onemocnění. Dřívější úvahy o možnosti včasnější enterální výživy a ústupu pooperačního ileu při tomto typu operace nebyly potvrzeny [22, 23]. Zřejmou nevýhodou tohoto přístupu je potřeba druhého operačního výkonu s obnovením kontinuity GIT. Tato operace je prováděna v závislosti na stavu pacienta a jeho výživy, na našem pracovišti nejčastěji 2–3 měsíce po první operaci. O načasování této operace opět není jednoznačná shoda. Banerjee et al. v recentní studii publikovali vyšší výskyt komplikací a potřeby umělé plicní ventilace u pacientů operovaných dříve než 10 týdnů od první operace [24]. Téměř současně publikovaná metaanalýza Zani et al. nicméně uvádí, že není rozdíl ve výskytu komplikací mezi časným a pozdním zrušením stomie a obnovením kontinuity GIT [23].
Alternativou uvedeného postupu je provedení anastomózy zdravých konců trávicí trubice v rámci jedné operace. Studie prokazují, že navzdory delšímu operačnímu času a vyššímu riziku komplikací po provedení anastomózy v terénu peritonitidy je riziko mortality stejné, nebo dokonce nižší než při provedení enterostomie [21, 22]. Bohužel, je nutné připomenout, že mortalita je velmi hrubým faktorem málo vypovídajícím o dalších výsledcích, především ve smyslu dlouhodobé morbidity pacientů s NEC, a proto je nutné vyčkat výsledků precizněji zpracovaných studií k definitivnímu rozhodnutí o preferenci jednoho či druhého přístupu. Rozhodně však považujeme za vhodné zvážit provedení primární anastomózy u pacientů s postižením proximálních úseků tenkého střeva nebo v terénu jasně demarkovaného postižení tenkého střeva.
Samostatnou a do určité míry kontroverzní otázkou zůstává použití peritoneální drenáže jako jediného výkonu při NEC IIIb s perforací GIT. Na našem pracovišti se tento postup neužívá. Použití drénu bývá vyhrazeno pro případy nemožnosti definitivního operačního výkonu buď z důvodu těžké nestability novorozence, nebo dočasné nedostupnosti erudovaného operačního týmu. Přes literárně doloženou obdobnou nebo vyšší mortalitu při použití peritoneálního drénu a vyšší morbiditu u přeživších je tento přístup nadále využíván, zvláště v kategorii nejmenších dětí [3, 13].
ZÁVĚR
Ve sledovaném období 2010–2018 byla ve východočeském regionu zaznamenána incidence nekrotizující enterokolitidy 5,6 % v kategorii dětí s velmi nízkou porodní hmotností (<1500 gramů) s letalitou 24,5 %. Přes aktivní chirurgický přístup k dětem všech váhových kategorií dosahuje letalita onemocnění 50 % u pacientů s porodní hmotností <750 gramů a 30 % u chirurgicky léčených pacientů. I nadále tak NEC patří k zásadním faktorům ovlivňujícím mortalitu i dlouhodobou morbiditu předčasně narozených novorozenců. Optimální načasování operačního výkonu zůstává skutečným ars medici v neonatologii. Přes intenzivní výzkum a vývoj poznání v dané oblasti nedochází k významnějšímu zlepšení výsledků péče.
Přednáška byla zařazena do programu XI. Východočeských perinatologických dnů v Deštném v Orlických horách a 64. kongresu českých a slovenských dětských chirurgů v Peci pod Sněžkou.
Korespondující autor:
MUDr. Jan Malý, Ph.D.
Dětská klinika LF UK a FN
Sokolská 581
580 00 Hradec Králové
e-mail: malyj@lfhk.cuni.cz
Sources
1. Obladen M. Necrotizing enterokolitis – 150 years of fruitless search for the cause. Neonatology 2009; 96 : 203–210.
2. Holman RC, Stoll BJ, Curns AT, et al. Necrotising enterocolitis hospitalisations among neonates in the United States. Paediatr Perinat Epidemiol 2006; 20 : 498–506.
3. Hull MA, Fisher JG, Gutierrez IM, et al. Mortality and management of surgical necrotizing enterocolitis in very low birth weight neonates: a prospective cohort study. J Am Coll Surg 2014; 218 : 1148–1155.
4. Battersby C, Santhalingam T, Costeloe K, Modi N. Incidence of neonatal necrotising enterocolitis in high-income countries: a systematic review. Arch Dis Child Fetal Neonatal Ed 2018; 103: F182-F189.
5. Neu J, Walker WA. Necrotizing enterocolitis. N Engl J Med 2011; 364 : 255–264.
6. Rees CM, Pierro A, Eaton S. Neurodevelopmental outcomes of neonates with medically and surgically treated necrotizing enterocolitis. Arch Dis Child Fetal Neonatal Ed 2007; 92: F193–F198.
7. Fullerton BS, Hong CR, Velazco CS, et al. Severe neurodevelopmental disability and healthcare needs among survivors of medical and surgical necrotizing enterocolitis: A prospective cohort study. J Pediatr Surg 2017. Oct 12. pii: S0022-3468(17)30651-6. doi: 10.1016/j.jpedsurg.2017.10.029.
8. Duggan CP, Jaksic T. Pediatric intestinal failure. N Engl J Med 2017; 377 : 666–675.
9. Patel RM, Denning PW. Intestinal microbiota and its relationship with necrotizing enterocolitis. Pediatr Res 2015; 78 : 232–238.
10. Bell MJ, Ternberg JL, Feigin RD, et al. Neonatal necrotizing enterocolitis. Therapeutic decisions based upon clinical staging. Ann Surg 1978; 187 : 1–7.
11. Walsh MC, Kliegman RM. Necrotizing enterocolitis: treatment based on staging criteria. Pediatr Clin North Am 1986; 33 : 179–201.
12. Faingold R, Daneman A, Tomlinson G, et al. Necrotizing enterocolitis: assessment of bowel viability with color doppler US. Radiology 2005; 235 : 587–594.
13. Stey A, Barnert ES, Tseng CH, et al. Outcomes and costs of surgical treatments of necrotizing enterocolitis. Pediatrics 2015; 135: e1190–e1197.
14. Rygl M, Čunát V, Pýcha K, et al. Nekrotizující enterokolitida u extrémně nezralých novorozenců - možnosti chirurgické léčby. Rozhl Chir 2004; 83 : 629–634.
15. Malý J, Melek J, Bréšková P, et al. Variabilita klinické manifestace norovirové infekce u novorozence – od perakutní nekrotizující enterokolitidy po asymptomatický průběh. Čes-slov Pediat 2012; 67 : 178–186.
16. Kalousová J, Fryč R. Nekrotizující enterokolitida. In: Šnajdauf J, Škába R (eds). Dětská chirurgie. Praha: Galén, 2005.
17. Hong CR, Fullerton BS, Mercier CE, et al. Growth morbidity in extremely low birth weight survivors of necrotizing enterocolitis at discharge and two-year follow-up. J Pediatr Surg 2018; 53 : 1197–1202.
18. Mowitz ME, Dukhovny D, Zupancic JAF. The cost of necrotizing enterocolitis in premature infants. Semin Fetal Neonatal Med 2018; 23 : 416–419.
19. Neu J, Modi N, Caplan M. Necrotizing enterocolitis comes in different forms: Historical perspectives and defining the disease. Semin Fetal Neonatal Med 2018; 23 : 370–373.
20. Rose AT, Patel RM. A critical analysis of risk factors for necrotizing enterocolitis. Semin Fetal Neonatal Med 2018; 23 : 374–379.
21. Thakkar HS, Lakhoo K. The surgical management of necrotising enterocolitis (NEC). Early Hum Dev 2016; 97 : 25–28.
22. Haricharan RN, Gallimore JP, Nasr A. Primary anastomosis or ostomy in necrotizing enterocolitis? Pediatr Surg Int 2017; 33 : 1139–1145.
23. Zani A, Lauriti G, Li Q, Pierro A. The timing of stoma closure in infants with necrotizing enterocolitis: A systematic review and meta-analysis. Eur J Pediatr Surg 2017; 27 : 7–11.
24. Banerjee DB, Vithana H, Sharma S, Tsang TTM. Outcome of stoma closure in babies with necrotising enterocolitis: early vs late closure. Pediatr Surg Int 2017; 33 : 783–786.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2018 Issue 8-
All articles in this issue
- Fokální nodulární hyperplazie u dětí – diagnostika a léčba
- Remodelace – základní předpoklad léčby zlomenin předloktí rostoucího skeletu
- Laparoskopia v detskom veku – apendektómia, záchovná resekcia sleziny, hepatobiliárne operácie
- Nekrotizující enterokolitida v Perinatologickém centru FN Hradec Králové 2010–2017
- Family Eating and Activity Habits Questionnaire – český překlad a ověření srozumitelnosti dotazníku
- Aktuální výskyt rizikových faktorů ischemické choroby srdeční u dětí v ČR v roce 2016
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Fokální nodulární hyperplazie u dětí – diagnostika a léčba
- Nekrotizující enterokolitida v Perinatologickém centru FN Hradec Králové 2010–2017
- Remodelace – základní předpoklad léčby zlomenin předloktí rostoucího skeletu
- Aktuální výskyt rizikových faktorů ischemické choroby srdeční u dětí v ČR v roce 2016
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

