-
Medical journals
- Career
Antiradikálová aktivita látek s potenciálním účinkem na kardiovaskulární systém
Authors: R. Opatřilová; Z. Kupková; J. Csöllei
Authors‘ workplace: Veterinární a farmaceutická univerzita Brno, Farmaceutická fakulta, Ústav chemických léčiv
Published in: Čes. slov. Farm., 2008; 57, 177-180
Category: Excerpt
Overview
Po objevení antioxidační ochrany biologických systémů se volné radikály a jejich účinky staly předmětem intenzivního výzkumu v procesu různých typů onemocnění. Práce je zaměřena na studium antiradikálové aktivity látek ze skupiny heteroarylethanolaminů. Místem působení těchto látek je kardiovaskulární systém, kde mohou vznikat endotelové dysfunkce, probíhá oxidace cholesterolu aj. Vysoce reaktivním volným radikálem je oxid dusnatý (NO.), vznikající endogenně působením enzymu NO-syntasy (NOS). Hlavním rozkladným produktem vodného roztoku oxidu dusnatého jsou dusitany, které se v přítomnosti hemoproteinů oxidují až na dusičnany. Základní metodou detekce oxidačních produktů oxidu dusnatého je Griessova metoda založená na spektrofotometrickém stanovení dusitanů po diazotaci sulfanilamidu a kopulaci s N-(1-naftyl)-etylendiaminem s detekcí v oblasti při 540 nm. Antioxidanty, látky, které organismus využívá k neutralizaci některých volných radikálů, reagují na principu oxidace – redukce. Pro průkaz antioxidační aktivity byla zvolena metoda bromometrie. V bromometrii po reakci bromidu a bromičnanu vzniká elementární brom, který je vlastním oxidačním činidlem. Tento vzniklý brom se může, v našich laboratorních podmínkách, považovat za „volný radikál“ schopný oxidovat další systémy. Na tomto modelu lze stanovit, jak velkou antioxidační kapacitu má sledovaná látka. Obě metody byly porovnány s metodou pro hodnocení antiradikálové aktivity pomocí stabilního radikálu 2,2 - difenyl-1-pikrylhydrazylu (DPPH).
Klíčová slova:
antioxidační aktivita – Griess – DPPH – bromometrieÚvod
Volné radikály, jejich účinky a antioxidační ochrana biologických systémů se staly předmětem intenzivního výzkumu v procesu různých typů onemocnění nejenom kardiovaskulárního systému, vzniku aterosklerotických plaků, ale i diabetes mellitus a mnoha dalších. Oxidační stres může být vyvolán nedostatečnou funkcí buněčného ochranného systému, ischémií (nedostatkem kyslíku), UV zářením, metabolickým stresem, zánětem, otravou, věkem nebo kouřením. Tyto změny následně vedou například ke zvýšenému ukládání cholesterolu do cévní stěny a k rozvoji druhotných onemocnění – např. hypertenze 1).
Práce je zaměřena na studium antioxidační a antiradikálové aktivity látek potenciálně vhodných pro použití v terapii hypertenze, ischemické choroby srdeční a infarktu myokardu ze skupin aryloxyaminopropanolů, heteroarylethanolaminů a heteroarylethanonaminů s potenciálním antiadrenergním a antidysrytmickým účinkem. Místem působení těchto látek je kardiovaskuární systém, kde mohou vznikat endotelové dysfunkce vlivem porušení rovnováhy mezi vznikem a odstraňováním volných radikálů.
Oxid dusnatý (NO.) je vysoce reaktivním volným radikálem, vzniká endogenně působením enzymu NO-syntasy (NOS) spolu s L-citrullinem z L-argininu. Účastní se regulace hemodynamiky, působí při neurotransmisi, v modulaci zánětu aj. Hlavním rozkladným produktem vodného roztoku oxidu dusnatého jsou dusitany, které se v přítomnosti hemoproteinů oxidují až na dusičnany. Látky reagující s NO, kompeticí s kyslíkem, snižují produkci dusitanů 2).
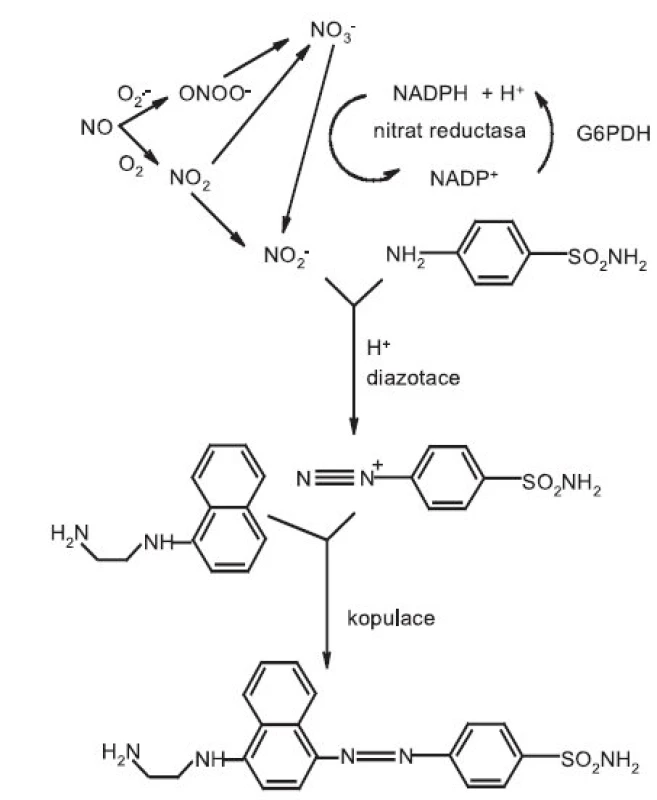
Griessova reakce je základní metodou detekce oxidačních produktů oxidu dusnatého. Je založena na spektrofotometrickém stanovení dusitanů po diazotaci sulfanilamidu a kopulaci s N-(1-naftyl)ethylendiaminem s detekcí v oblasti při vlnové délce 540 nm 3).
Významné je postupné přidávání obou složek Griessova činidla pro dosažení maximální citlivosti testu. Pokud reaguje postupně kyselý roztok sulfanilamidu a pak teprve sůl N-(1-naftyl)ethylendiaminu je reakce téměř třikrát citlivější, než v případě, kdy se obě složky smíchají před přidáním do reakční směsi 4).
Antioxidanty, látky, které organismus využívá k neutralizaci některých volných radikálů, mohou reagovat na principu oxidace – redukce. Pro průkaz antioxidační aktivity byla zvolena modifikovaná analytická oxidačně-redukční metoda bromometrie, kdy reakčním činidlem je brom ve stavu zrodu, vznikající v kyselém prostředí bromičnanu draselného za přítomnosti bromidu draselného jako urychlovače reakce. Touto reakcí vzniká elementární brom, z toho název bromometrie, který je vlastním oxidačním činidlem a může se, v našich laboratorních podmínkách, považovat za „volný radikál“ schopný oxidovat další systémy. Na tomto modelu lze stanovit, jak velkou antioxidační kapacitu má sledovaná látka 5).
Obě metody byly porovnány s metodou pro hodnocení antiradikálové aktivity pomocí stabilního radikálu 2,2 difenyl-1-pikrylhydrazylu (DPPH) 6).
Studované látky s pracovními názvy 4/1M až 4/6M a 4E/1 až 4E/6 byly syntetizovány dr. Kurfürstem 7) jako potenciální antagonisté β-adrenergních receptorů. Jsou to deriváty ze skupiny heteroarylaminoethanolu. Aromatickou částí je 3-alkylbenzofuran, bázickou pak arylpiperazin. Oba fragmenty spojuje ethanolový můstek. Na tyto látky lze pohlížet jako na analogy aryloxyaminopropanolu, u kterého se oxymethylenová část spojovacího řetězce stala součástí furanového kruhu kondenzovaného s benzenem. Struktura studovaných látek a jejich sumární vzorec a molekulová hmotnost jsou uvedeny v tabulce 1.
Table 1. 2-[4-(4-aryl)piperazin-1-yl]-1-(3-alkylbenzofuran –2-yl) ethan-1-oly ve formě hydrochloridů ![2-[4-(4-aryl)piperazin-1-yl]-1-(3-alkylbenzofuran –2-yl) ethan-1-oly ve formě hydrochloridů](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/b29eeb3e7d7398a622dd46f07627d8bb.png)
POKUSNÁ část
Griessova reakce (obr. 1) – oxid dusnatý byl vyroben reakcí 3 mol.l-1 roztoku kyseliny sírové s dusitanem sodným v inertní atmosféře (argon). Vzniklé vyšší oxidy dusíku zachyceny v koncentrovaném roztoku hydroxidu sodného a po vysušení koncentrovanou kyselinou sírovou získán čistý oxid dusnatý, kterým je sycena odplyněná voda. Vodný roztok oxidu dusnatého (0,5 ml) a stejné množství vodného roztoku zkoumané látky o koncentraci 1 mmol.l-1 je inkubováno při 30 °C po dobu 45 min. Po ukončení inkubace jsou do roztoku přidána Griessova činidla – 0,5 ml roztoku 2% sulfanilamidu rozpuštěného v 4% kyselině fosforečné a 0,5 ml vodného 0,2% roztoku N-(1-naftyl)etylendiaminu. Po 10 minutách ve tmě je měřena absorbance při 540 nm na přístroji spektrofotometr HP 8453. Koncentrace NO jako nitritu je počítána z kalibrační křivky dusitanu sodného (y = 485,64x - 0,0001; R2 = 0,9999).
Brom – reakcí bromičnanu draselného s bromidem draselným v kyselém prostředí kyseliny sírové 0,8 mol.l 1 vzniká ekvivalentní množství bromu. V přítomnosti studované látky může reagovat vznikající brom radikálově, substitučně anebo adičně. Průběh reakce – množství nespotřebovaného bromu v čase je zjišťováno z kalibrační křivky A = f (c) spektrofotometricky při 360 nm, kde y = 19131x - 0,0923; R2 = 0,9879.
DPPH – stabilní radikál 2,2-difenyl-1-pikrylhydrazyl byl připraven v koncentraci 1.10-4 mol.l-1 rozpuštěním v methanolu. Pro sledování antiradikálové aktivity byla opět použita spektrofotometrie ve viditelné oblasti (γ = 517 nm), kde byl úbytek radikálu sledován po přidání roztoku studované látky ve stejné koncentraci. Výsledky byly korigovány slepým pokusem. Rovnice přímky y = 12650x + 0,005; R2 = 0,9997.
Výsledky a diskuze
Pomocí tří metod se spektrofotometrickou detekcí byla hodnocena antiradikálová a antioxidační aktivita série dvanácti derivátů 2-(4-arylpiperazin-1-yl)-1-(3--alkylbenzofuran-2-yl)ethanolu, připravených v Ústavu chemických léčiv ve formě soli (hydrochloridu) 7).
Griessovou reakcí (hodnocení aktivity látek vychytáváním oxidu dusnatého), bromometricky (brom ve stavu zrodu) a metodou pomocí stabilního radikálu DPPH, vykazovala nejvyšší aktivitu, látka s pracovním označením 4/1E, dále silnou antiradikálovou aktivitu vykazovaly i látky pracovně označené jako 4/2E a 4/6M. Pro účinek je patrně více důležitá substituce na arylpiperazinu než na benzofuranovém jádře, kde je navázána v poloze 3 methyl - nebo ethyl - skupina.
Na arylu v poloze 4 - na piperazin je u 4/1 a 4/1E v poloze vázán fluor. Pokud je v poloze 2 - (4/3M; 4/3E), aktivita výrazně klesá. V případě substituce methoxylem do polohy 2 - (4/2M a 4/2E) je účinek vyšší, než pokud je zde navázán pouhý methyl (4/4, 4/4E). Látky 4/6 a 4/6E nemají na arylu substituent a jejich antiradikálový efekt patří k nejvýraznějším. Deriváty substituované v poloze 3-trifluormethylem mají účinnost nejnižší (obr. 2).
Image 2. Srovnání účinnosti zhášení radikálů 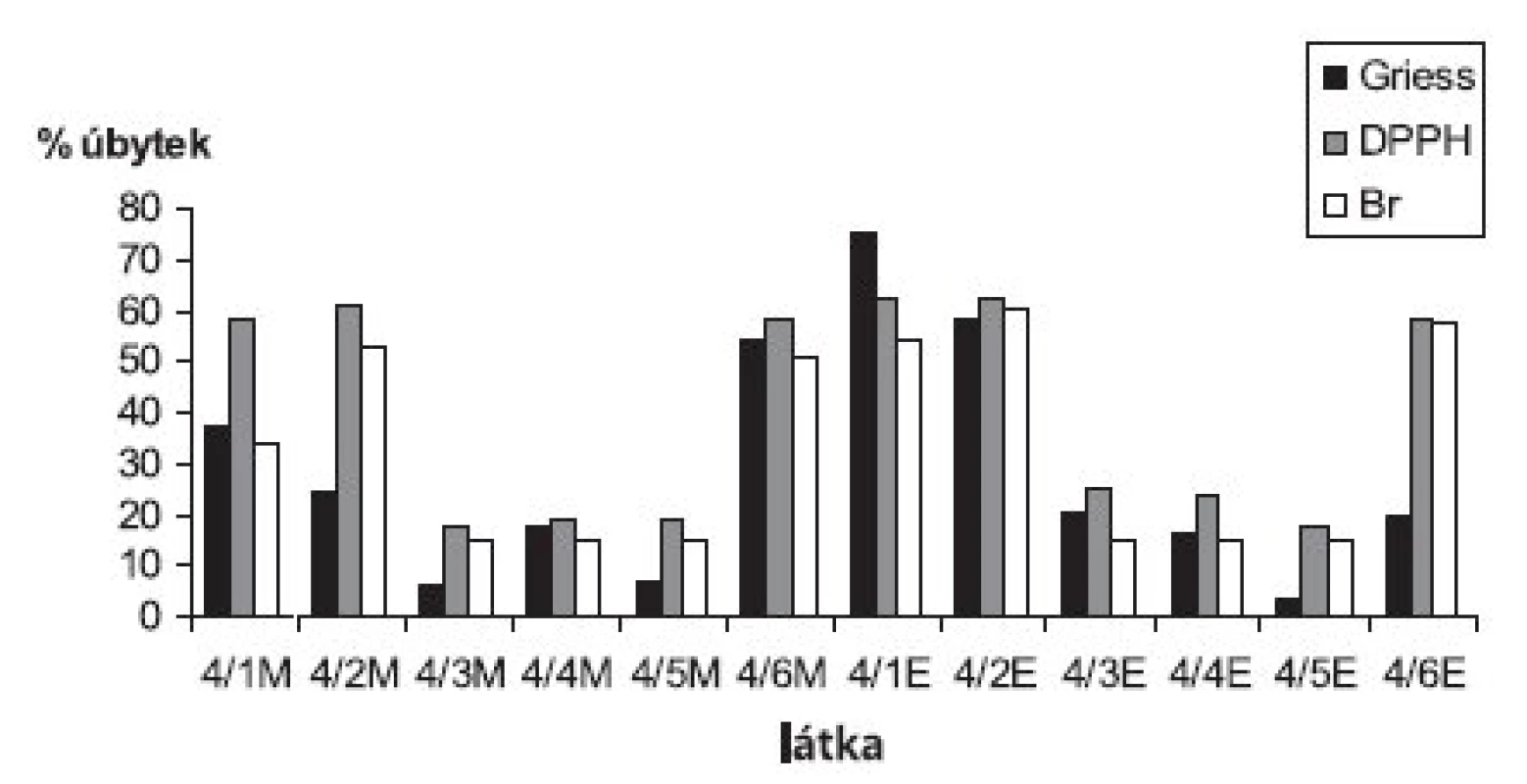
Pravděpodobně z hlediska strukturálních vztahů a účinku sehrává příznivou roli kladný mezomerní efekt elektronegativních substituentů navázaných na aromatickém jádře. Pro maximální účinek je tedy důležitá volná hydroxylová skupina a nesubstituovaný arylpiperazinový zbytek nebo substituce arylu fluorem navázaným v poloze 4, případně methoxyskupinou v poloze 2.
Látky nerozpustné ve vodě byly rozpuštěny v methanolu, který ale vykazoval vlastní vysokou antioxidační aktivitu v Griessově reakci. Proto bylo prováděno měření u kontrolního roztoku obsahujícího pouze methanol a byla zjištěna antioxidační aktivita (Amethanolu) a zjištěný účinek pak byl odečten od aktivity získané při stanovení v něm rozpuštěných látek (Acelková). Rozdílem je vlastní aktivita stanovované látky (Acelková – Amethanolu) = Atestované látky.
Při bromometrickém stanovení nebyl zaznamenána žádná výrazná změna aktivity látek při použití vody nebo methanolu jako rozpouštědla.
Hodnocení pomocí DPPH je již v základu ovlivněno methanolem – DPPH je prakticky nerozpustný ve vodě. Žádný z kontrolních vzorků nevykazoval výraznou aktivitu, která by prokazovala vychytávání DPPH methanolem.
Pro objasnění mechanismu nitridace (Griess) byl průběh reakce s oxidem dusnatým a látkou 4/1E změřen pomocí LC-MS spektroskopie (Agilent Technologies HP 1100 LC-MSD VL Trap spektrometr). Na hmotnostním spektru nejsou vidět molekuly s hmotností menší jak 80, proto nebyl NO detegovatelný. Při nitrosaci docházelo k rozštěpení molekuly na 1-(3-alkylbenzofuran-2--yl)ethanol a příslušný derivát 4-arylpiperazinu.
Při bromometrickém stanovení vznikaly mono-, di-, tribrom deriváty látek a proběhla i adice na dvojnou vazbu benzofuranu.
Pro metodu DPPH nebyla LC-MS provedena, ale předpokládáme různé radikálové reakce, štěpení a spojování molekul aj.
Závěr
Procentuální srovnání úbytku radikálu – účinnosti potenciálního lapače radikálu všech tří metod (obr. 2) ukazuje až na malé výjimky, že látky vykazují nevýznamný rozdíl v aktivitě při použitých metodách. Tato série testovaných látek má srovnatelnou aktivitu pro tři typy radikálů, což je pravděpodobně ovlivněno jejich podobnou chemickou strukturou. Předpokládáme, že tyto metody by bylo možné využít nejen pro testování nově připravovaných látek i látek různých chemických struktur, již v klinické praxi využívaných.
Došlo: 24. června 2008 / Přijato: 1. července 2008
Adresa pro korespondenci:
Ing. PharmDr. Radka Opatřilová, Ph.D.
Ústav chemických léčiv FaF VFU
Palackého 1–3, 612 42 Brno
e-mail: opatrilovar@vfu.cz
Sources
1. Štípek, S.: Antioxidanty a volné radikály ve zdraví a v nemoci. Praha, Grada, 2000.
2. Rapisarda, P., Tomaino, A. Cascio, R.: J Agric Food Chem., 1999; 77, 4748.
3. Green, L. C., Wagner, A., Glogowski, J.: Anal. Biochem., 1982; 126, 131.
4. Crkovská, J., Štípek, S.: Klin. Biochem. Metab., 1998; 6, 82.
5. López-Cueto, G., Ostra, M., Ubide, C.: Anal. Chim. Acta, 2001, 445, 117.
6. Dovolil, J., Beneš, L.: Čes. Slov. Farm., 2001; 50, 203.
7. Kurfürst, P., Marek, J., Vančo, J., Csöllei, J.: Acta Cryst., 2004; C60, 494.
Labels
Pharmacy Clinical pharmacology
Article was published inCzech and Slovak Pharmacy

2008 Issue 4-
All articles in this issue
- Aktuální acidita prostředí a účinnost pomocných látek používaných k protimikrobní stabilizaci léčivých přípravků připravovaných v lékárnách
- Antiradikálová aktivita látek s potenciálním účinkem na kardiovaskulární systém
- Zhodnocení farmakoterapie u geriatrických pacientů ve vybraných domovech důchodců v regionu Brno
- Syntéza, identifikácia a fyzikálno-chemické vlastnosti nových potenciálnych ultrakrátkopôsobiacich beta-adrenergných blokátorov
- Charakterizace mikrokrystalických celulos parametry trojexponenciální rovnice lisování
- Studium vlastností tablet ze dvou typů přímo lisovatelného xylitolu
- Czech and Slovak Pharmacy
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Aktuální acidita prostředí a účinnost pomocných látek používaných k protimikrobní stabilizaci léčivých přípravků připravovaných v lékárnách
- Zhodnocení farmakoterapie u geriatrických pacientů ve vybraných domovech důchodců v regionu Brno
- Antiradikálová aktivita látek s potenciálním účinkem na kardiovaskulární systém
- Studium vlastností tablet ze dvou typů přímo lisovatelného xylitolu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career