-
Medical journals
- Career
Farmakoterapie erektilní dysfunkce – kde jsme a kam směřujeme
Authors: J. Bultas 1; D. Karetová 2
Authors‘ workplace: Farmakologický ústav, 3. LF UK, Praha 1; II. interní klinika – klinika kardiologie a angiologie 1. LF UK a VFN v Praze 2
Published in: Kardiol Rev Int Med 2014, 16(4): 281-287
Category: Cardiology Review
Overview
Přehledový článek shrnuje současné poznatky o mechanizmu navození erekce, ukazuje možnosti farmakologického ovlivnění erektilní dysfunkce. V další části shrnuje obecně vlastnosti fosfodiesteráz a význam jejich inhibice s důrazem na izoenzym fosfodiesterázy 5. Následně jsou detailně probírány vlastnosti jednotlivých představitelů inhibitorů izoenzymu fosfodiesterázy 5 – sildenafilu, vardenafilu, tadalafilu a avanafilu z pohledu účinnosti a bezpečnosti i z pohledu lékových interakcí. Poslední část shrnuje naše znalosti o vlivu řady kardiovaskulárních léků na vlastní erektilní funkci.
Klíčová slova:
farmakoterapie – erektilní dysfunkce – inhibitory fosfodiestarázy 5 – sildenafil – vardenafil – tadalafil – avanafilErektilní dysfunkce bohužel často stojí na okraji zájmu kardiologů, angiologů, diabetologů či praktických lékařů. Přitom jsou to zejména tito odborníci, kteří o symptomatického nemocného pečují často řadu let, než vyhledá sexuologa či urologa. S tímto problémem se setkáváme stále častěji a příčin je více. Předně, téma erektilní dysfunkce přestalo být tabu a nemocní se s potížemi svěřují a žádají pomoc, stoupají nároky na plnou kvalitu života i v pokročilejším věku. Navíc řada léčiv může erektilní dysfunkci zhoršit či ji odmaskovat. Vzpomeňme jen některá antihypertenziva, antidepresiva typu pomalých inhibitorů reabsorpce serotoninu (SSRI), antiandrogeny z řady inhibitorů 5α ‑ reduktázy užívané k léčbě benigní hypertrofie prostaty (zejm. finasterid a dutasterid) či vysoké dávky statinů, které mohou inhibovat syntézu testosteronu. Možnosti léčby by měly zajímat zejména kardiologa a angiologa, neboť nemocní s aterotrombotickými chorobami jsou na prvním místě ve výskytu dysfunkce. Erektilní dysfunkce je často prvním signálem přítomnosti choroby na bázi aterotrombózy. Její odhalení pak může vést k včasné léčbě a zlepšení prognózy nemocného. Výskyt erektilní dysfunkce zpravidla předchází koronární příhodě řadu let. Nemocní s tímto postižením mají též zvýšené riziko infarktu myokardu (o 60 %) či jakékoli kardiovaskulární příhody (o 40 – 50 %) [1].
Problém erektilní dysfunkce není problémem novým, zřejmě provází lidstvo po celé věky. Řečeno slovy klasika, Lva Nikolajeviče Tolstého: „Muž přežije zemětřesení, trápení vleklé nemoci, veškeré soužení psychických muk,…ale největší tragédií je, a zůstane po věky věků, selhání v ložnici“. Proto možnosti účinné léčby, zejména zavedení inhibitorů fosfodiesterázy 5 (PDE5-I), byly přivítány nejen odbornou veřejností. Dokonce papež Jan Pavel II. zavedení sildenafilu k léčbě erektilní dysfunkce nezatratil, ale hodnotil jej slovy „…nechť přinese štěstí do rodin“.
Patofyziologie erekce a možnosti farmakologického zásahu
Zpravidla platí, že čím komplikovanější je mechanizmus určitého procesu, tím větší je riziko jeho poruchy. U erekce to platí dvojnásob. Příčin erektilní dysfunkce je více, vedle organických a psychogenních to mohou být funkční poruchy na řadě etáží. Více faktorů regulujících souhru vazodilatace a vazokonstrikce arteriol kavernózních těles však na straně druhé nabízí též rozmanité možnosti farmakologického zásahu.
Tumescence je řízena vegetativním nervovým systémem, noncholinergními, nonadrenergními nervovými vlákny (NANC) a celou řadou vazoaktivních systémů. Na prvním místě je nutno uvést význam gasotransmiteru oxidu dusnatého – NO. Dále je významná správná souhra vazodilatačních a vazokonstrikčních systémů: prostaglandinů, adenozinu, endotelinu, angiotenzinu II a angiotenzinu 1 – 7, vazoaktivního interstinálního polypeptidu (VIP) a dalších (obr. 1).
Image 1. Aktivace vazodilatace arteriol kavernózních těles působením NO, vazodilatačních prostaglandinů a adenozinu. Bližší popis, stejně jako vysvětlivky zkratek, v textu. 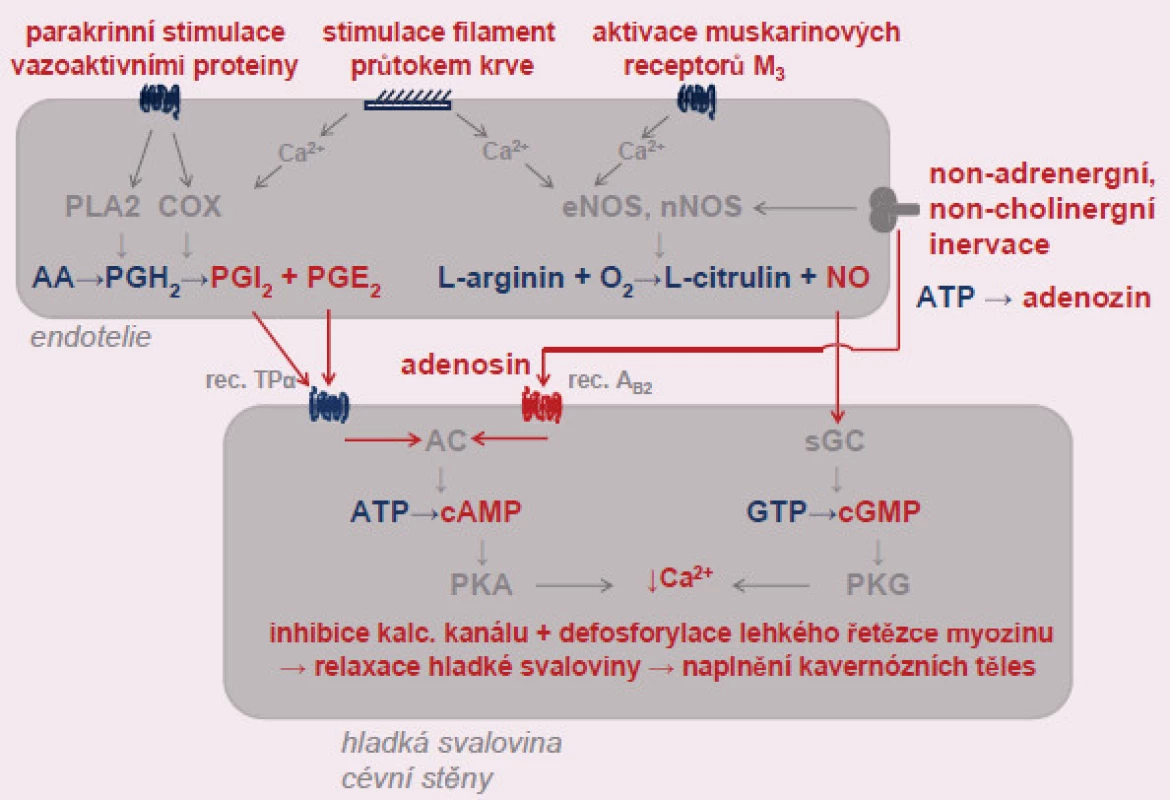
Vlastní erekce je závislá na dobrém cévním zásobení, tedy plnění kavernózních těles, neboť podstatou je zvýšení přítoku a snížení odtoku krve. Vlastní děj je zahájen erektilními podněty (zpravidla taktilními vjemy), které aktivují limbický systém a další podkorová centra a cestou vagových vláken a NANC vycházejících ze sakrální oblasti aktivují endotelie arteriol kavernózních těles. Aktivací endoteliální a neurogenní NO syntázy (eNOS a nNOS) se zvýší lokální nabídka transmiteru NO. Oxid dusnatý aktivuje solubilní guanylát ‑ cyklázu (sGC), která katalyzuje přeměnu guanozin‑trifosfátu (GTP) na cyklický guanozin‑monofosfát (cGMP) v buňkách hladké svaloviny cévní stěny. Tento druhý posel aktivuje další enzym kontrolující fosforylaci – proteinkinázu G (PKG) a defosforylací kaliového kanálu a lehkého řetězce myosinu dochází k relaxaci hladké svaloviny.
Paralelně uvolnění vazoaktivních polypeptidů (VIP aj.) aktivuje fosfolipázu A2 uvolňující kyselinu arachidonovou (AA) a cyklo ‑ oxygenázu (COX) se zvýšením nabídky vazodilatačních prostaglandinů – prostacyklinu (PGI2) a prostaglandinu E2 (PGE2). Stimulace tromboxan ‑ prostaglandinového receptoru α (TPα) aktivuje adenylát ‑ cyklázu (AC) a dějem zcela obdobným jako při působení NO dochází k relaxaci. Jediným rozdílem je zapojení jiné signální molekuly – cyklického adenozin‑monofosfátu (cAMP). Vedle aktivace receptoru TPa je adenylát ‑ cykláza stimulována též adenozinovým receptorem B2 (AB2R), zvýšení nabídky adenozinu je stimulováno neurogenně – vlákny typu NANC.
Jak je zřejmé, v relaxaci arteriol kavernózních těles hraje zásadní úlohu nabídka obou signálních molekul – cGMP a cAMP. Jejich syntéza je stimulována cyklázami (AC a GC), naopak degradace fosfodiesterázami (PDE). V případě kavernózních těles izoenzymem – fosfodiesterázou 5 (PDE ‑ 5). Stimulace adenylát či guanylát ‑ cyklázy či blokáda fosfodiesterázy 5 zvyšuje nabídku cGMP a cAMP a výrazně potencuje vazodilataci a schopnost i kvalitu erekce.
Vedle gasotransmiterů, prostanoidů a adenozinu je erekce ovlivněna též endotelinem a systémem renin‑angiotenzin‑aldosteron (RAAS). Stimulace endotelinových receptorů ETA vede k vazokonstrikci, naopak ETB1 k vazodilataci [2]. Selektivní blokátory ET receptorů jsou testovány v léčbě priapismu.
Další vazokonstrikčně‑vazodilatační systém – renin‑angiotenzin‑aldosteron – se rovněž podílí na indukci erekce. Stimulace receptorů AT1 pro angiotenzin II snižuje schopnost erekce, naopak aktivace vazodilatačních MAS receptorů pro angiotenzin 1 – 7 tumescenci podporuje [3].
Ochabnutí erekce je naopak pod taktovkou adrenergní stimulace. Vlastní ejakulace je stimulována vyplavením katecholaminů a aktivací adrenergních receptorů. Následná stimulace receptorů α1 a α2 vede k vazokonstrikci. Snížení přítoku krve do kavernózních těles je sledováno detumescencí.
Možnosti farmakologického zásahu v léčbě erektilní dysfunkce
Jak bylo řečeno, klíčovými působky indukujícími erekci a udržujícími její kvalitu jsou oxid dusnatý a vazodilatační prostanoidy (obr. 2). Oba zvyšují nabídku cyklických nukleotidů – cGMP a cAMP. V prvé etáži je možno stimulovat přirozené aktivátory či aplikovat jejich analoga. Selektivní zvýšení nabídky NO na úrovni corpora cavernosa není schůdné, efekt prekurzoru NO – L ‑ argininu – je iluzorní. Kontrolované studie nedoložily rozdíl proti podávání placeba [4]. V prostaglandinové a adenozinové větvi vazodilatace je situace lepší. Dlouhodobě je úspěšně užívána intrakavernózní či intrauretrální aplikace analog prostaglandinů, konkrétně prostaglandinu E1 (alprostadilu), ve fázi preklinického hodnocení jsou agonisté adenozinových receptorů A2BR [5].
Image 2. Mechanizmus účinku farmakologických postupů k léčbě erektilní dysfunkce postavené na zvýšení nabídky cyklických nukleotidů – cGMP a cAMP. Bližší popis, stejně jako vysvětlivky zkratek, v textu. 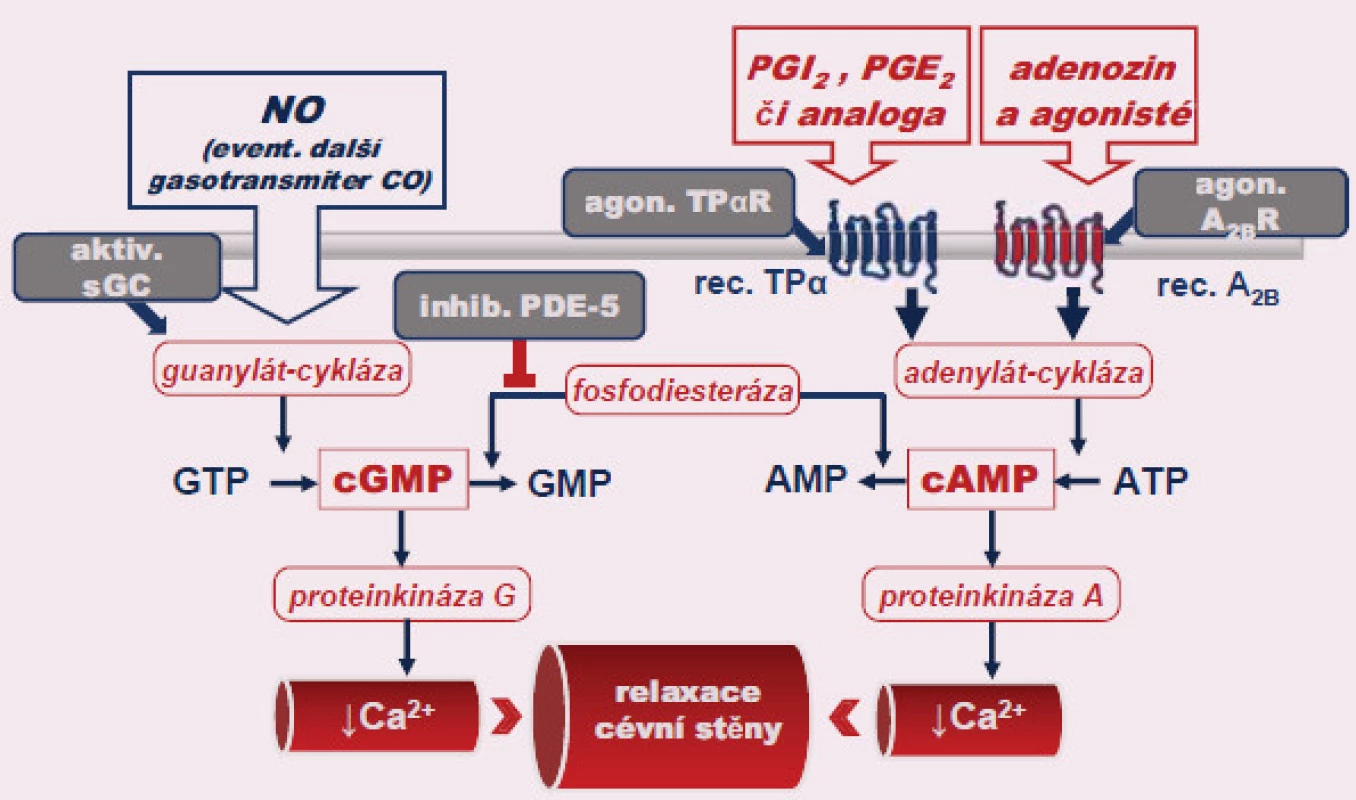
V druhé etáži je možno stimulovat solubilní guanylát cyklázu. Aktivátory zvyšující fyziologickou odpověď sGC na stimulaci NO (např. BAY 41 – 8543) jsou již ve fázi klinického hodnocení v léčbě erektilní dysfunkce [6].
Nejvýznamnějším farmakologickým postupem léčby erektilní dysfunkce je zvýšení nabídky cAMP a cGMP snížením jejich degradace – podáváním inhibitorů fosfodiesterázy 5. Léčba inhibitory PDE ‑ 5 bude z různých aspektů diskutována dále.
Ve fázi preklinického hodnocení je stimulace vazodilatačních receptorů MAS analogy angiotenzinu 1 – 7 [7]. Preklinická data jsou velmi slibná. Obdobně jsou zajímavé postupy cílené přímo na myozinové řetězce v cévní stěně. Relaxace arteriol kavernózních těles selektivním inhibitorem myozinu II blebbistainem vedla k řadě studií nejen v léčbě erektilní dysfunkce [8].
Naopak řada dalších postupů, zpravidla vyžadujících intrakavernózní aplikaci (papaverin, thymoxamin aj.), byla opuštěna. Yohimbin působící centrálně na úrovni podkorových paraventrukulárních jader stimulací adrenergních receptorů α2 je užíván minimálně.
Shrneme‑li, pak z perorálně účinných léčebných postupů dominují inhibitory PDE ‑ 5, ostatní léčebné postupy mají handicap intrakavernózní aplikace, absence účinku či jsou ještě ve fázi klinického hodnocení. Další orientace přehledu bude proto směřována na inhibitory PDE ‑ 5.
Úloha fosfodiesteráz a farmakologické možnosti jejich inhibice
Fosfodiesterázy (PDE), konkrétně soubor 12 izoenzymů PDE ‑ 1 až PDE ‑ 12, jsou důležitými regulátory nabídky „druhých poslů“ – cyklického adenozin‑monofosfátu či cyklického guanozin ‑ monofosfátu. Mechanizmem účinku fosfodiesteráz je degradace cAMP a cGMP hydrolýzou. Výsledkem inhibice PDE je zvýšení nabídky obou cyklických nukleotidů. V hladké svalovině cévní stěny vede vzestup koncentrace cGMP k vazodilataci. Obdobně zvýšení nabídky cAMP v trombocytu stabilizuje destičku a tlumí primární hemostázu. Obdobné schéma funguje na úrovni hladké svaloviny dutých orgánů (vývodných cest močových, dělohy, střeva či žlučových cest), v myokardu, v enterocytech, v řadě žláz, v centrálním nervovém systému či např. v sítnici oka. Zásah na tomto místě je výhodný, neboť se zpravidla jedná o poslední krok sdružující odpověď na různé podněty.
Plošně či cíleně umíme tlumit aktivitu všech fosfodiesteráz. Naším terapeutickým cílem však je zpravidla jen inhibice některých izoenzymů. Jejich užití je klíčovým farmakoterapeutickým postupem v řadě oborů – v sexuologii, kardiologii, angiologii, gastroenterologii, psychiatrii, urologii či pneumologii (tab. 1).
Table 1. Význam izoenzymů PDE v kontrole fyziologických funkcí, možnosti jejich inhibice. 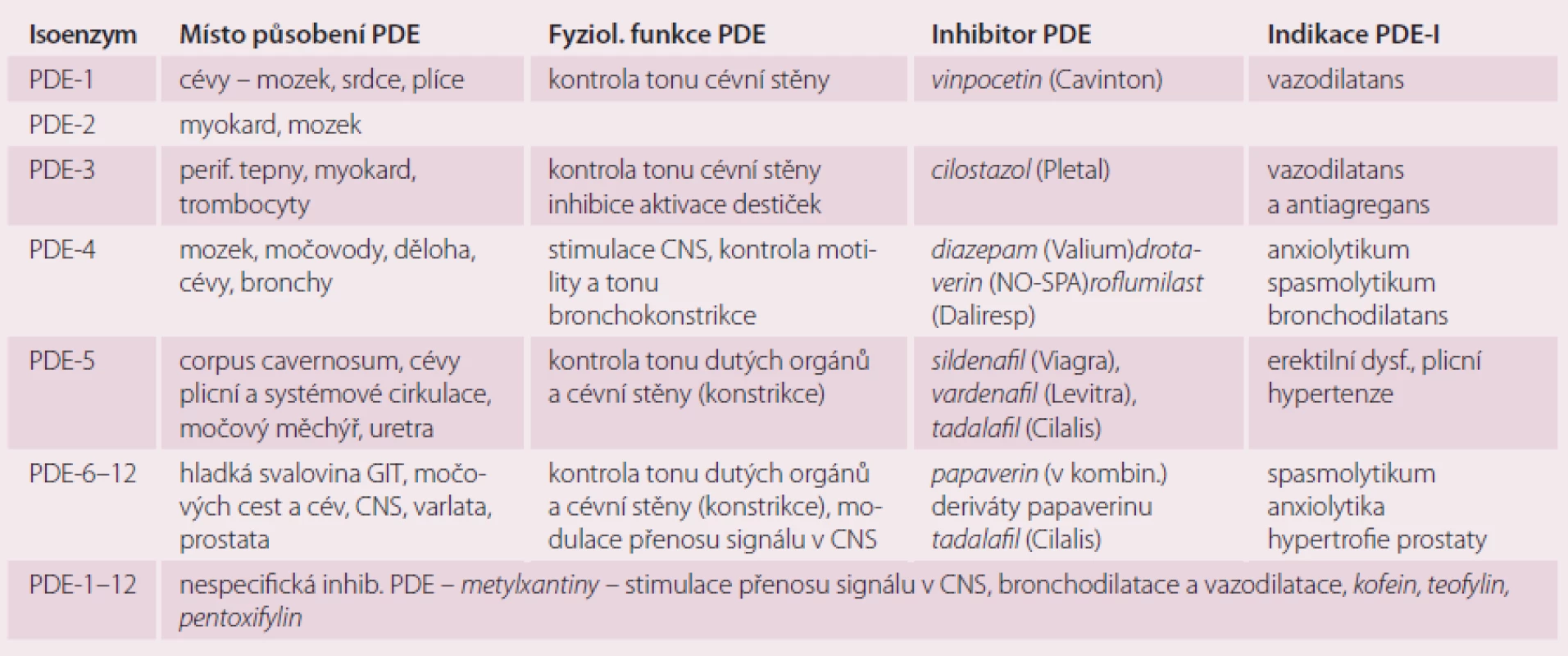
Nespecifické inhibitory PDE užívá každý z nás ve formě metylxantinů. Kofein, teofylin či teobromin jsou významnými součástmi řady nápojů, jejich deriváty (aminofylin či pentoxifylin) jsou široce užívanými léky. Inhibice PDE metylxantiny je nespecifická, tlumena je aktivita řady izoenzymů. Navíc metylxantiny zasahují i do jiných systémů, zejména však inhibují adenozinové receptory. Kombinací obou účinků je vysvětlen efekt na stimulaci CNS (např. navození nespavosti či aktivaci dechového centra, bronchodilatační a vazodilatační působení či zrychlení srdeční frekvence).
Selektivní inhibice fosfodiesterázy 5
Specifická inhibice PDE ‑ 5 omezuje farmakodynamické cílení léčby na corpus cavernosum, cévy plicní a systémové cirkulace, močový měchýř, prostatu a uretru. Z toho vyplývají hlavní indikace PDE5 - I – erektilní dysfunkce, plicní hypertenze a symptomatické zlepšení mikce u benigní hyperplazie prostaty. Zvýšení nabídky cGMP zpomalením jeho degradace vede k poklesu tonu arteriol corpora cavernosa penisu s usnadněním navození i kvality erekce, ke snížení rezistence plicních arteriol s poklesem plicní hypertenze a k relaxaci dolních cest močových se snížením tonu hrdla močového měchýře, prostaty (efekt na stroma i pouzdro) a močové trubice s následným usnadněním mikce.
V současné době máme k užití v indikaci léčby erektilní dysfunkce, resp. zkvalitnění erekce, k dispozici čtyři inhibitory PDE ‑ 5: sildenafil (Viagra aj.), vardenafil (Levitra), (Cialis) a avanafil (Spedra). Řada dalších inhibitorů (lodenafil, mirodenafil, udenafil aj.) je ve fázi klinického hodnocení nebo mají jen regionální registraci.
Rozdíly mezi inhibitory PDE ‑ 5 ve farmakokinetických vlastnostech a v indikacích
Mezi jednotlivými inhibitory PDE ‑ 5 nejsou zásadní rozdíly v mechanizmu účinku a ve farmakodynamickém efektu. Významné odlišnosti jsou však ve farmakokinetických vlastnostech, tj. konkrétně v rychlosti nástupu účinku a v délce působení. Dále se jednotlivé inhibitory liší v rozsahu schválených indikací. Tab. 2 porovnává jednotlivé inhibitory PDE ‑ 5.
Table 2. Srovnání vlastností a indikací jednotlivých inhibitorů PDE-5 (podle platných SPC). 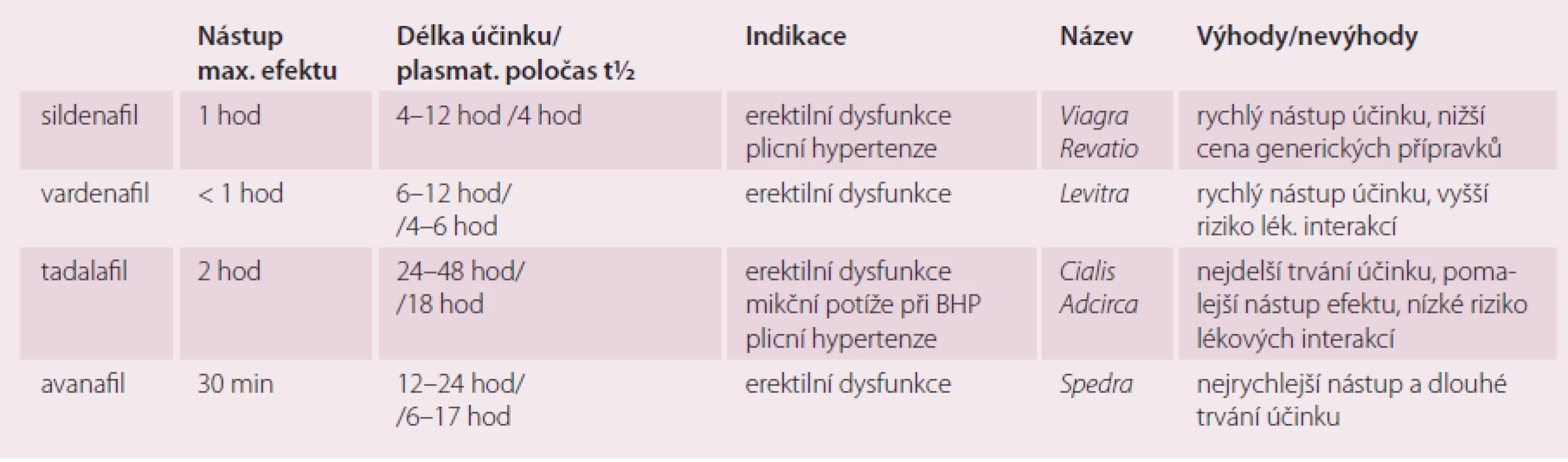
Porovnáme‑li klinický účinek v hlavní indikaci, tj. dosažení a udržení erekce, pak máme porovnání jednotlivých molekul s placebem u různých subpopulací (např. u diabetiků, u seniorů apod.). Obecně lze říci, že úspěšnost pohlavního styku (hodnoceném dosažením a udržením erekce) byla závislá na dávce inhibitoru PDE ‑ 5 a pohybovala se kolem 50 – 80 %. Naopak při aplikaci placeba tento ukazatel nepřesáhl zpravidla 30 %. Při nepřímém porovnání nebyl zřetelný rozdíl mezi jednotlivými léčivy při aplikaci srovnatelných dávek a respektování cílových populací [9]. Studie s jednotlivými inhibitory PDE ‑ 5 dokumentovaly široké terapeutické okno, u většiny nemocných bylo dosaženo dobrého efektu již základní dávkou, zvyšování pak jen mírně potencovalo efekt, výskyt nežádoucích účinků se významně nezvyšoval. Například i při dlouhodobější aplikaci vyšších dávek sildenafilu výskyt všech nežádoucích účinků nepřesáhl 0,5 % a byl méně než dvojnásobný v porovnání s podáváním placeba, přitom jejich výskyt celkově nepřesáhl 0,5 %; závažných nežádoucích účinků bylo stejně [9]. Zvýšení frekvence závažných nežádoucích účinků se vzrůstající dávkou bylo minimální, pouze nežádoucí účinky vyplývající z vazodilatace (návaly a bolesti hlavy) se zvýšením dávky stoupaly.
Hlavním rozdílem, který má praktický dopad, je tak rychlost nástupu účinku a délka působení (graf 1). Při podání avanafilu je možno očekávat efekt během desítek minut, při aplikaci vardenafilu a sildenafilu po 30 – 60 min a u tadalafilu po 1 – 2 hod. Na druhé straně účinek tadalafilu přetrvává zpravidla 48 hod, termín „víkendová pilulka“ je tak zcela namístě. Vzhledem k tomu, že velká část indikací této skupiny léčiv není přímo z důvodu neschopnosti dosažení a udržení erekce, ale ke zkvalitnění a prodloužení erekce při „rekreačním“ sexu, je tato vlastnost tadalafilu často preferována. Přesah účinku na několik dnů je vítán.
Graph 1. Porovnání základních farmakokinetických ukazatelů inhibitorů PDE-5. 
V ostatních indikacích – v léčbě plicní hypertenze – je schválen ke klinickému užití sildenafil a tadalafil. Tato indikace je specifická a vybočuje z tématu přehledu. Naopak druhá indikace, tj. mikční potíže při benigní hypertrofii prostaty (BHP), může při výběru konkrétního léčiva mít význam. Obě poruchy (erektilní dysfunkce a prostatické potíže) se často sdružují. Efekt tadalafilu na pokles symptomů (úpravu mikce) a zlepšení kvality života je srovnatelný s alfablokátory. Při léčbě BHP alfablokátory jsou ostatní inhibitory PDE ‑ 5 kontraindikovány, tadalafil je možno podat i při léčbě tamsulosinem (Omnic aj.).
Další diskutovanou oblastí je „off ‑ label“ indikace inhibitorů PDE ‑ 5 u ejaculatio precox. Dokladů o skutečném účinku této skupiny v této indikaci je minimum, objektivní zhodnocení není možné [10].
Srovnání účinku v hlavní indikaci, tj. v léčbě erektilní dysfunkce
Recentně (v roce 2013) byla zveřejněna rozsáhlá metaanalýza vzájemného porovnání jednotlivých inhibitorů PDE ‑ 5 či síťového porovnání efektu inhibitorů vůči placebu. Analýza téměř 120 studií s více než 30 tisíci pacientů nepozorovala zásadní rozdíly v efektu [11]. Autoři uzavírali, že tadalafil byl mírně účinnější, jednalo se však jen o trend bez většího klinického dopadu. Rovněž preference nemocných svědčila ve prospěch tadalafilu. Tolerance a bezpečnost byla u všech testovaných léků srovnatelná. Studie porovnávaly též efekt nově vyvíjených inhibitorů PDE ‑ 5 (avanafilu, udenafilu, mirodenafilu a lodenafilu). Klasická trojice – sildenafil, vardenafil a tadalafil – byla zpravidla srovnatelně účinná, často však dokonce účinnější.
Snášenlivost inhibitorů PDE ‑ 5
Oblastí, která je při indikaci inhibitorů PDE ‑ 5 přeceňována a zbytečně démonizována, je snášenlivost a bezpečnost. Řada lékařů kardiakům odpírá tyto léky z obavy ze závažných nežádoucích příhod. Vlastní nežádoucí účinky pramení ze dvou farmakodynamických vlastností – z inhibice PDE ‑ 5 navozující vazodilataci a z nedostatečné selektivity inhibice PDE, tj. působení též na PDE ‑ 6, projevem čehož je ovlivnění přenosu fotosignálu v sítnici.
První typ nežádoucích účinků pramení z vlastní inhibice fosfodiesterázy 5, tedy zejména z vazodilatace. Ta je přítomna nejen v topořivých tělesech a v plicní cirkulaci, ale v menší míře také v systémové cirkulaci, jmenovitě v kůži a v mozku. Ač je mezi lékaři tradován výskyt priapismu, ve 160 klinických studiích s tisícovkou dlouhodobě léčených nemocných se priapismus vyžadující ošetření nevyskytl ani jedenkrát. V jiné metaanalýze se priapismus vyskytl asi u 2 % nemocných [12]. Jednalo se však o priapismus referovaný nemocnými, který nevyžadoval léčbu a nebyl hodnocen jako závažná příhoda. V postregistračních hlášeních nežádoucích účinků je výskyt priapismu ojedinělý (méně než jeden případ na milion podaných dávek).
Výsledkem systémové vazodilatace mohou být návaly (objevující se v závislosti na dávce až do výše 12 %) či bolesti hlavy (s obdobnou frekvencí, opět závislou na dávce). Návaly a bolesti hlavy se vyskytují u senzitivních osob současně. Jiným projevem vazodilatace je kongesce nosní sliznice (graf 2).
Graph 2. Výskyt nežádoucích účinků vázaných na inhibici PDE-5 v %. Metaanalýza 69 studií s 53 tisíci nemocných, sledovaných měsíce až roky. Jen 2,1 % příhod bylo závažných. NAION (nonarteritic anterior ischaemic optic neuropathy) nezachycena ani jedenkrát [12]. ![Výskyt nežádoucích účinků vázaných na inhibici PDE-5 v %. Metaanalýza 69 studií s 53 tisíci nemocných, sledovaných měsíce až roky. Jen 2,1 % příhod bylo závažných. NAION (nonarteritic anterior ischaemic optic neuropathy) nezachycena ani jedenkrát [12].](https://pl-master.mdcdn.cz/media/image/29c2f70dc92a178010c6a644c2388f64.jpg?version=1537793169)
V druhém typu nežádoucích účinků jsou určité rozdíly mezi jednotlivými léky. Pramení z variabilní selektivity inhibice PDE ‑ 5, resp. působení i na ostatní izoenzymy. Inhibice PDE ‑ 5 sildenafilem a vardenafilem je o 3 – 4 řády selektivnější než inhibice PDE ‑ 3, kontraktilita a dráždivost myokardu tak není snížena, stejně tak je o dva řády selektivnější než inhibice PDE ‑ 1, PDE ‑ 2, PDE ‑ 4, PDE ‑ 7 až PDE-11 a není ani ovlivněna motilita zažívacího traktu či funkce CNS.
Rozdílný však je efekt na fosfodiesterázu 6. Ta se účastní přenosu fotosignálu v sítnici (fototransdukce). Inhibice tohoto izoenzymu však je pouze o jeden řád menší. Podávání sildenafilu či vardenafilu tak může být spojeno s reverzibilní poruchou barevného vidění. Inhibice PDE ‑ 5 tadalafilem a avanafilem je selektivnější, výskyt nežádoucích účinků na této úrovni je minimální [13]. Vzhledem k malé závažnosti a k vzácnosti poruchy vízu (kolem 3 % nemocných při léčbě sildenafilem) nejsou tyto rozdíly klinicky příliš významné [9]. Porovnání nejčastěji se vyskytujících nežádoucích účinků inhibitorů PDE ‑ 5 s placebem je zobrazeno v grafu 3. Výskyt vychází z metaanalýzy 69 studií s 53 tisíci nemocných sledovaných měsíce až roky [8]. Je patrné, že jen 2,1 % příhod byly příhody závažné, kritické se prakticky nevyskytly.
Graph 3. Výskyt koronárních či cerebrovaskulárních příhod při léčbě inhibitory PDE-5 ve srovnání s placebem v %. Metaanalýza 69 studií s 53 tisíci nemocných, sledovaných měsíce až roky [12]. AKS – akutní koronární příhody celkem, AMI – akutní infarkt myokardu, CMP – cévní příhody mozkové ![Výskyt koronárních či cerebrovaskulárních příhod při léčbě inhibitory PDE-5 ve srovnání s placebem v %. Metaanalýza 69 studií s 53 tisíci nemocných, sledovaných měsíce až roky [12].
AKS – akutní koronární příhody celkem, AMI – akutní infarkt myokardu, CMP – cévní příhody mozkové](https://pl-master.mdcdn.cz/media/image/e6f4f2621775bd1533e19a18d150c633.jpg?version=1537797398)
Napříč spektrem PDE5 - I se objevují mírné dyspepsie, jejich frekvence se pohybuje kolem 5 %. Jaká je jejich příčina, není jasné. Uvažuje se o přímém ovlivnění traktu vazodilatací či nespecifickou inhibicí některého izoenzymu fosfodiesteráz. Relaxace sfinkterů vývodných cest močových při inhibici PDE ‑ 5 není provázena nežádoucími účinky.
Posledním nežádoucím účinkem, zřejmě specifickým pro tadalafil a vardenafil, jsou myalgie či bolesti v zádech, mírné potíže jsou popisovány až u desetiny léčených.
Bezpečnost inhibitorů PDE ‑ 5
Výskyt všech nežádoucích účinků, včetně závažných, byl srovnatelný mezi jednotlivými molekulami a při metaanalýze nebyl doložen statistický rozdíl. Nutnost vysazení léčby z důvodu intolerance se pohybovala kolem 1 % při aplikaci vyšších dávek léčiva.
Mýtem je obava z nárůstu cerebro ‑ a kardiovaskulárních příhod při léčbě inhibitory PDE ‑ 5. Asi nejkvalitnější přehled o výskytu závažných cévních příhod dává nedávná metaanalýza více než dvou set studií s různými inhibitory PDE ‑ 5, která byla založena na sledování desítek tisíc léčených nemocných po dobu několika měsíců až let [9]. Bezpečnost inhibitorů PDE ‑ 5 byla porovnávána s placebem. Výskyt kardiovaskulárních příhod byl mírně vyšší (v řádu desetin procent) při léčbě sildenafilem; při léčbě vardenafilem či tadalafilem nebyl pozorován rozdíl proti placebu. Výskyt všech závažných nežádoucích příhod se pohyboval kolem 2 %, nelišil se při aktivní léčbě ve srovnání s placebem, nelišil se ani mezi jednotlivými inhibitory PDE ‑ 5 navzájem. V přehledu 67 studií se sildenafilem (i při vysokých dávkách sildenafilu – 100 mg) se závažné nežádoucí účinky objevily v 2,8 % a při léčbě placebem v 2,6 %; kritické příhody – s možnou vazbou na léčbu – byly napříč dávkami stejně časté jako ve větvích placebových, shodně se vyskytly v 0,1 % [12]. Nezdá se tedy, že by podání inhibitorů PDE ‑ 5 bylo zatíženo vyšším výskytem závažných či dokonce kritických nežádoucích účinků.
Poslední komplikací související s vazodilatací a s poklesem tlaku je ischemická neuropatie optiku (NAION – nonarteritic anterior ischaemic optic neuropathy). Tato extrémně vzácná, bohužel ireverzibilní příhoda je pravděpodobně vázána na protrahovanou hypotenzi. Ve velké studii u čtyř milionů mužů starších 50 let, z nichž asi 10 % užívalo inhibitory PDE ‑ 5 pravidelně, byl výskyt NAION zcela identický ve skupině užívajících a neužívajících PDE5 - I, vyskytl se u méně než pěti případů na 10 tisíc mužů/ rok. Je pravděpodobné, že ischemická neuropatie očního nervu není specifická pro léčbu inhibitory PDE ‑ 5, ale je spojena s protrahovanou hypotenzí, resp. se šokovým stavem. Pokud se vyvarujeme užití vysokých dávek či kombinaci inhibitorů PDE ‑ 5 s léky, které vazodilataci výrazně potencují (např. s nitráty), je její incidence raritní.
Lékové interakce inhibitorů PDE ‑ 5
Při léčbě inhibitory PDE ‑ 5 se setkáváme s interakcemi na bázi farmakodynamické i na bázi farmakokinetické. Klinicky významnou farmakodynamickou interakcí je potenciace vazodilatačního efektu. Významná je interakce s nitráty, jejich působení je odvislé od zvýšení nabídky cGMP. Inhibice degradace pak může vést k akcentaci vazodilatace až k hypotenzi. Nicméně toto riziko je zbytečně démonizováno. V dvojitě zaslepené studii byl probandům léčeným standardní dávkou nitrátu (ISDN či nitroglycerinu) přidán sildenafil (50 mg). Aplikace samotného nitrátu vedla k poklesu systolického tlaku asi o 10 mm Hg, přidání sildenafilu pokles potencovalo o dalších 10 – 20 mm Hg. Diastolický tlak poklesl méně významně [14]. Analýza postmarketingových studií u 40 000 nemocných léčených inhibitory PDE ‑ 5 ukázala, že asi 1 % užilo během léčby nitrát, u desetiny z nich se objevila symptomatická hypotenze. U těchto několika set nemocných, kteří současně užili obě vzájemně kontraindikované skupiny, však nebylo pozorováno žádné úmrtí ani kardiovaskulární příhoda [12]. Vedle nitrátů je kontraindikována kombinace inhibitorů PDE ‑ 5 s alfablokátory k léčbě mikčních potíží. Výjimkou je aplikace tamsulosinu, preferenčního inhibitoru adrenergních receptorů α1A v močových cestách, který má malý vazodilatační potenciál.
Inhibitory PDE ‑ 5 jsou substráty efluxní pumpy glykoproteinu P (P ‑ gp) a oxidázy CYP3A4. Z farmakokinetických interakcí se proto setkáváme se zvýšením jejich dostupnosti a zpomalením degradace při inhibici tohoto tandemu antimykotiky, virostatiky, makrolidovými antibiotiky, verapamilem, amiodaronem aj. Expozice u vardenafilu stoupá až padesátinásobně, u tadalafilu pouze trojnásobně. Rozdíly jsou dány nízkou biologickou dostupností vardenafilu (kolem 5 %). Obdobně se setkáme se snížením dostupnosti a zrychlením degradace při indukci P ‑ gp a CYP3A4 antikonvulzivy, rifampicinem, dexametazonem či např. třezalkou. Efekt v takovém případě selhává. Významná může být i interakce s potravou – tučné jídlo snižuje vrcholovou plazmatickou koncentraci sildenafilu, vardenafilu či avanafilu asi o třetinu, absorpce tadalafilu ovlivněna není.
Vzájemné porovnání dostupných inhibitorů PDE ‑ 5 v indikaci léčby erektilní dysfunkce
V současné době máme k užití čtveřici inhibitorů PDE ‑ 5. Nejdéle užívaný sildenafil má relativně rychlý, ale nejkratší účinek a střední riziko lékových interakcí se snížením efektu při užití po jídle. Dostupnost generických přípravků vedla k mírnému snížení nákladů. Nezanedbatelná je též psychická potenciace terapeutického účinku „synonymem“ pro skupinu inhibitorů PDE ‑ 5, tedy symbolem „ Viagra“. Vardenafil má rovněž rychlý nástup, ale relativně krátký účinek. V „urgentní situaci“ můžeme nástup ještě zrychlit sublingválním podáním léku. Nevýhodou je nejvyšší riziko lékových interakcí a zpomalení efektu při užití po jídle. Tadalafil má pomalejší nástup efektu, ale nejdelší účinek, bývá proto pacienty označován jako „víkendové potěšení“. Výhodou je možnost podání s předstihem a menší psychický tlak na léčeného z obavy před odezněním účinku. Předností je rovněž velmi nízké riziko lékových interakcí, užití po jídle nesnižuje ani nezpomaluje efekt. Je výhodný u mužů s benigní hypertrofií prostaty, jako jediný PDE5 - I lze kombinovat s alfablokátory (tamsulozinem). Navíc má vlastní příznivý účinek na úpravu mikce. Předností avanafilu je rychlý nástup a relativně dlouhá doba účinku. Daní by však mohl být poněkud menší efekt, jak již naznačila zmíněná metaanalýza porovnávající efekt inhibitorů PDE ‑ 5 s placebem. Head ‑ to ‑ head studii nemáme [11], rozdíly jsou i v dávkování (tab. 3).
Table 3. Srovnání dávkování jednotlivých inhibitorů PDE-5. Nízká dávka bývá doporučována na počátku léčby či při současném podávání léčiv zvyšujících dostupnost inhibitorů PDE-5. 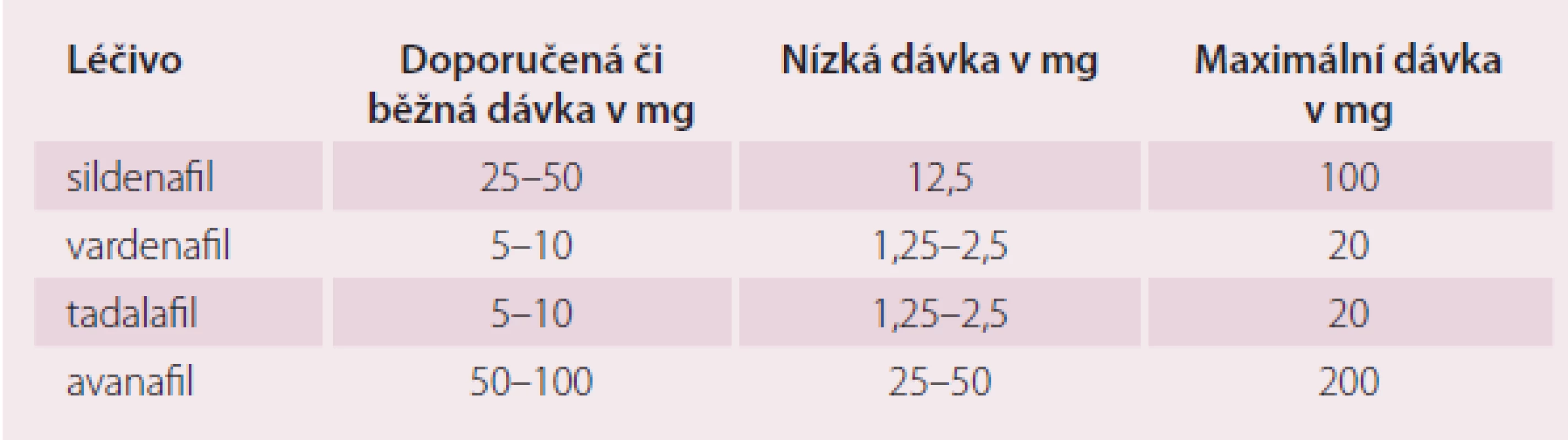
Které kardiovaskulární léky mohou ovlivnit, případně dokonce navodit erektilní dysfunkci?
Mluvíme‑li o farmakologických aspektech léčby erektilní dysfunkce, nelze se nezmínit o vlivu řady kardiovaskulárních léků. Jejich působení může být jak negativní, tak i pozitivní. Řada lékařů i pacientů se obává vlivu antihypertenziv na vznik erektilní dysfunkce.
Velká metaanalýza, která se zabývala tímto problémem, ukázala, že pouze thiazidová diuretika a starší, zejména neselektivní betablokátory, navodily poruchy erekce [15]. Novější selektivní betablokátory – konkrétně byl testován nebivolol či bisoprolol – dysfunkci nenavodily. Ve studii zabývající se efektem očekávané sexuální poruchy po nasazení betablokátoru bylo doloženo, že potíže nebyly vázány na lék, ale na informaci, kterou pacient dostal, navíc dysfunkci eliminovalo i placebo [16]. V řadě studií zabývajících se tímto problémem při léčbě inhibitory ACE, sartany či blokátory kalciového kanálu byl doložen neutrální či příznivý vliv. Studie sledující kombinaci antihypertenzní terapie doložila příznivý efekt kombinace sartanu a blokátoru kalciového kanálu, naopak kombinace sartanu s betablokátorem měla efekt neutrální [17]. Uzavřeme‑li toto téma, pak vztah antihypertenzní léčby k erektilní dysfunkci je přeceňován. Strategie léčby hypertenze postavená na užití vazodilatačně působících léků a léků vedoucích k regresi hypertrofie cévní stěny měla pozitivní efekt, β‑blokátory měly efekt neutrální (s výjimkou nebivololu s efektem příznivým) a pouze diuretika (užívaná ve studiích v dávkách vyšších, než je dnes doporučováno) ve významném procentu dysfunkci navodila. Důvodem, proč diuretika mají negativní vliv, je pravděpodobně pokles cirkulujícího objemu a změny v homeostáze, které aktivují RAAS. Bylo doloženo, že stimulace receptorů AT1 angiotenzinem II významně zhorší schopnost erekce [18].
Dyslipidemie je sama o sobě rizikovým faktorem erektilní dysfunkce. Léčba statiny vedla dlouhodobě ke zlepšení stavu, nicméně vysoké dávky statinů, které vedly ke snížení nabídky testosteronu, schopnost ztopoření naopak zhoršily [19]. Obdobně přítomnost diabetu dvoj ‑ až trojnásobně zvyšuje výskyt poruch erekce. Není však doložen vliv farmakoterapie (inzulinových senzibilizátorů či sekretagog) na vlastní poruchu.
Závěrem lze říci, že ve fázi klinického hodnocení je řada slibných léčebných postupů k farmakoterapii erektilní dysfunkce. Na jejich zavedení si však budeme muset ještě řadu let počkat. V současné době, z pohledu účinnosti i bezpečnosti, jsou inhibitory fosfodiesterázy 5 jednoznačně nejvýhodnější lékovou skupinou. Výběr konkrétního přípravku ze čtveřice sildenafil, vardenafil, tadalafil a avanafil záleží na požadavcích léčeného. Avanafil má nejrychlejší dobu nástupu, naopak tadalafil má efekt nejdelší. Účinnost, za podmínky užití farmakoekvivalentní dávky, je srovnatelná. Vysoká bezpečnost je přítomna též u kardiaků. Nízký výskyt lékových interakcí je společný celé skupině, nicméně u tadalafilu je riziko zvýšení expozice nejmenší.
Podpořeno PRVOUK ‑ P35/ LF3.
Doručeno do redakce: 22. 7. 2014
Přijato po recenzi: 14. 8. 2014
prof. MUDr. Jan Bultas, CSc.
www.vfn.cz
jbult@lf3.cuni.cz
Sources
1. Vlachopoulos C, Terentes ‑ Printzios D, Ioakeimidis N et al. Prediction of cardiovascular events and all‑cause mortality with erectile dysfunction: a systematic review and meta‑analysis of cohort studies. Circ Cardiovasc Qual Outcomes 2013; 6 : 99 – 109. doi: 10.1161/ CIRCOUTCOMES.112.966903.
2. Karakeci A, Firdolas F, Ozan T et al. Second pathways in the pathophysiology of ischemic priapism and treatment alternatives. Urology 2013; 82 : 625 – 629. doi: 10.1016/ j.urology.2013.06.029.
3. Fraga ‑ Silva RA, Montecucco F, Mach F et al. Pathophysiological role of the renin‑angiotensin system on erectile dysfunction. Eur J Clin Invest 2013; 43 : 978 – 985. doi: 10.1111/ eci.12117.
4. Klotz T, Mathers MJ, Braun M et al. Effectiveness of oral L ‑ arginine in first‑line treatment of erectile dysfunction in a controlled crossover study. Urol Int 1999; 63 : 220 – 223.
5. Baraldi PG, Tabrizi MA, Fruttarolo F et al. Recent improvements in the development of A(2B) adenosine receptor agonists. Purinergic Signalling 2008; 4 : 287 – 303. doi: 10.1007/ s11302 ‑ 008 ‑ 9097 ‑ z.
6. Lasker GF, Pankey EA, Kadowitz PJ. Modulation of soluble guanylate cyclase for the treatment of erectile dysfunction. Physiology (Bethesda) 2013; 28 : 262 – 269. doi: 10.1152/ physiol.00001.2013.
7. da Costa Gonçalves AC, Fraga ‑ Silva RA, Leite R et al. AVE 0991, a non‑peptide Mas ‑ receptor agonist, facilitates penile erection. Exp Physiol 2013; 98 : 850 – 855. doi: 10.1113/ expphysiol.2012.068551.
8. Zhang XH, Aydin M, Kuppam D et al. In vitro and in vivo relaxation of corpus cavernosum smooth muscle by the selective myosin II inhibitor, blebbistatin. J Sex Med 2009; 6 : 2661 – 2671. doi: 10.1111/ j.1743 ‑ 6109.2009.01424.x.
9. Tsertsvadze A, Fink HA, Yazdi F et al. Oral phosphodiesterase ‑ 5 inhibitors and hormonal treatments for erectile dysfunction: a systematic review and meta‑analysis. Ann Intern Med 2009; 151 : 650 – 661. doi: 10.7326/ 0003 ‑ 4819 ‑ 151 ‑ 9 ‑ 200911030 ‑ 00150.
10. Asimakopoulos AD, Miano R, Finazzi Agrò E et al. Does current scientific and clinical evidence support the use of phosphodiesterase type 5 inhibitors for the treatment of premature ejaculation? A systematic review and meta‑analysis. J Sex Med 2012; 9 : 2404 – 2416. doi: 10.1111/ j.1743 ‑ 6109.2011.02628.x.
11. Yuan J, Zhang R, Yang Z et al. Comparative effectiveness and safety of oral phosphodiesterase type 5 inhibitors for erectile dysfunction: a systematic review and network meta‑analysis. Eur Urol 2013; 63 : 902 – 912. doi: 10.1016/ j.eururo.2013.01.012.
12. Giuliano F, Jackson G, Montorsi F et al. Safety of sildenafil citrate: review of 67 double‑blind placebo ‑ controlled trials and the postmarketing safety database. Int J Clin Pract 2010; 64 : 240 – 255. doi: 10.1111/ j.1742 ‑ 1241.2009.02254.x.
13. Wang R, Burnett AL, Heller WH et al. Selectivity of avanafil, a PDE5 inhibitor for the treatment of erectile dysfunction: implications for clinical safety and improved tolerability. J Sex Med 2012; 9 : 2122 – 2129. doi: 10.1111/ j.1743 ‑ 6109.2012.02822.x.
14. Webb DJ, Muirhead GJ, Wulff M et al. Sildenafil citrate potentiates the hypotensive effects of nitric oxide donor drugs in male patients with stable angina. J Am Coll Cardiol 2000; 36 : 25 – 31.
15. Baumhäkel M, Schlimmer N, Kratz M et al. Cardiovascular risk, drugs and erectile function – a systematic analysis. Int J Clin Pract 2011; 65 : 289 – 298. doi: 10.1111/ j.1742 ‑ 1241.2010.02563.x.
16. Silvestri A, Galetta P, Cerquetani E et al. Report of erectile dysfunction after therapy with beta‑blockers is related to patient knowledge of side effects and is reversed by placebo. Eur Heart J 2003; 24 : 1928 – 1932.
17. Yang L, Yu J, Ma R et al. The effect of combined antihypertensive treatment (felodipine with either irbesartan or metoprolol. on erectile function: a randomized controlled trial. Cardiology 2013; 125 : 235 – 241. doi: 10.1159/ 000350955.
18. Fraga ‑ Silva RA, Montecucco F, Mach F et al. Pathophysiological role of the renin‑angiotensin system on erectile dysfunction. Eur J Clin Invest 2013; 43 : 978 – 985. doi: 10.1111/ eci.12117.
19. Miner M, Billups KL. Erectile dysfunction and dyslipidemia: relevance and role of phosphodiesterase type ‑ 5 inhibitors and statins. J Sex Med 2008; 5 : 1066 – 1067. doi: 10.1111/ j.1743 ‑ 6109.2008.00783.x.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2014 Issue 4-
All articles in this issue
- Endoteliální dysfunkce, erektilní dysfunkce a kardiovaskulární riziko
- Doporučení pro sexuální aktivitu nemocných s kardiovaskulárním onemocněním a jejich partnery – AHA, ESC GUIDELINES 2013
- Klinický význam parametru CAVI (Cardio‑ Ankle Vascular Index) v prevenci, diagnostice a terapii
- Farmakoterapie erektilní dysfunkce – kde jsme a kam směřujeme
- Terapie erektilní dysfunkce dle Guidelines Evropské urologické asociace
- Urologické příčiny erektilní dysfunkce
- Psychogenní erektilní dysfunkce
- Mužské sexuální dysfunkce jako párový problém
- Povrchová žilní trombóza – epidemiologie, diagnostika, léčba
- Chronické žilní onemocnění dolních končetin – diagnostika a konzervativní léčba
- Chronická žilní insuficience – invazivní terapie
- Syndrom pánevní kongesce
- Možnosti léčby hluboké žilní trombózy v roce 2014
- Sulodexid u angiologických pacientů
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Syndrom pánevní kongesce
- Povrchová žilní trombóza – epidemiologie, diagnostika, léčba
- Chronické žilní onemocnění dolních končetin – diagnostika a konzervativní léčba
- Psychogenní erektilní dysfunkce
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

