-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Vazospastická angina pectoris – patogeneza, diagnostika a léčba
Vasospastic angina pectoris – pathogenesis, diagnostics and treatment
In 1959 Prinzmetal described a syndrome of chest pains with typical ST segment elevation on ECG that is due to spasm of large epicardial or septal artery. Currently the term vasospastic angina (VSA) is used more often in literature. VSA can lead in acute myocardial infarction, it can be accompanied with serious cardiac arrhythmias and even sudden death is described in these patients. Pathogenesis of this syndrome is not completely clear. Effect of endothelial dysfunction, inflammatory factors, disorder of coagulation mechanisms, smoking and low level of magnesium belongs among suggested mechanisms of disease. ECG and Holter ECG monitoring is the basic examination of VSA, ergometry is not beneficial. Selective coronarography (SKG) with ventriculography performed during paroxysm proves focal spasm. SKG can be combined with spasm provocation (ergonovine, acetylcholine or hyperventilation). Provocative agent can be used also in combination with other imaging method, such as echocardiography or nuclear methods. The most widespread provocative agent in the world is ergonovine maleate, the test having sensitivity up to 100%. Nitrates and calcium antagonists are used in the treatment. Opinion on the use of beta-blockers and acetylsalicylic acid is not unified. Some authors recommend magnesium, estradiol supplement or vitamin E in the treatment.
Key words:
vasospastic angina – vasospastic angina pathogenesis – examination methods for vasospastic angina – vasospastic angina treatment
Autoři: E. Sovová; J. Lukl; Č. Číhalík
Působiště autorů: I. interní klinika Lékařské fakulty UP a FN Olomouc, přednosta prof. MUDr. Jan Lukl, CSc.
Vyšlo v časopise: Vnitř Lék 2005; 51(5): 548-554
Kategorie: Přehledné referáty
Souhrn
Prinzmetal popsal v roce 1959 syndrom bolesti na hrudi s typickými elevacemi ST úseku na EKG, které jsou způsobeny spazmem velké epikardiální nebo septální tepny. V současné době se v literatuře používá spíše termín vazospastická angina (VSA). VSA může vyústit do akutního infarktu myokardu, může být doprovázena závažnými srdečními arytmiemi a u těchto pacientů je popsána i náhlá smrt. Patogeneza tohoto syndromu není zcela jasná. Mezi předpokládané mechanizmy patří vliv endoteliální dysfunkce, zánětlivé faktory, porucha koagulačních mechanizmů, kouření, nízká hladina magnezia. Základním vyšetřením u VSA je EKG, Holterova monitorace EKG, ergometrie nebývá přínosná. Selektivní koronarografie (SKG) s ventrikulografií provedená při záchvatu prokáže fokální spazmus. SKG může být spojená s provokací spazmu (ergonovin, acetylcholin nebo hyperventilace). Provokační agens lze použít i v kombinaci s jinou zobrazovací metodou, jako je echokardiografie nebo nukleární metody. Ergonovin maleát je ve světě nejrozšířenější provokační agens, test má senzitivitu až 100 %. V léčbě se používají nitráty a kalcioví antagonisté. Na použití betablokátorů a kyseliny acetylsalicylové není jednotný názor. Někteří autoři doporučují v terapii magnezium, suplementaci estradiolu nebo vitamin E.
Klíčová slova:
vazospastická angina – patogeneza vazospastické anginy – vyšetřovací metody u vazospastické anginy – léčba vazospastické anginyÚvod
Prinzmetalova variantní angina byla popsána v roce 1959 Prinzmetalem a jeho kolegy jako syndrom bolesti na hrudi spojený s typickými elevacemi ST úseku na EKG (obr. 1). Tyto bolesti vznikají většinou v klidu. Variantní angina se vyskytuje u 2–3 % pacientů, kteří podstoupili invazivní kardiologické vyšetření. V současné době se v literatuře používá spíše termín vazospastická angina (VSA). Nejvyšší četnost výskytu VSA je udávána v Japonsku, výskyt v Evropě a Severní Americe je nižší [1].
Obr. 1. EKG obraz vazospaztické anginy. 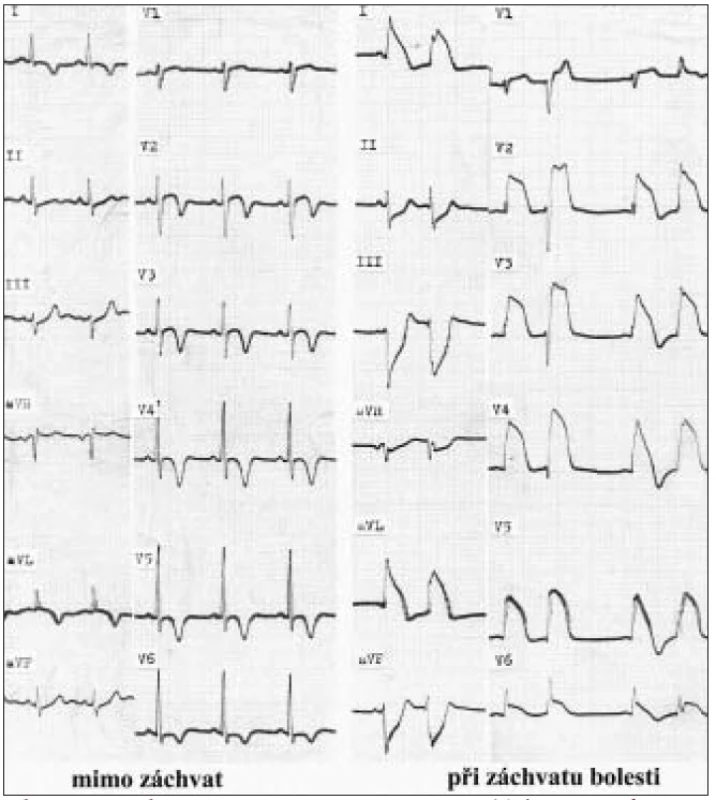
EKG v klidu a při záchvatu bolestí. Mechanizmem VSA je fokální koronární spazmus s následným přechodným zúžením koronární cévy s poruchou perfuze myokardu a s ischemií postižené oblasti. Tímto spazmem jsou nejčastěji postiženy velké epikardiální, případně velké septální koronární tepny. VSA může vyústit do akutního infarktu myokardu, může být doprovázena závažnými srdečními arytmiemi a u těchto pacientů je popsána i náhlá smrt [33]. Spazmus většinou ustoupí po aplikaci nitroglycerinu, někdy ve vysokých dávkách.
Spazmus může postihnout cévu postiženou aterosklerotickým procesem nebo i cévu, která je podle vyšetření selektivní koronarografí (SKG) normální.
U pacientů s VSA a normálním SKG nálezem je popisováno při vyšetření intravaskulárním ultrazvukem (intravaskulární monografie – IVUS) ztluštění intimy, které je proti kontrolní skupině statisticky významné [21].
Patogeneza
Patogeneza tohoto syndromu není zcela jasná [50].
Pacienti s VSA mají vyšší základní tonus koronárních arterií a vyšší odpověď na vazokonstrikční stimuly [4]. Jako mechanizmus vzniku spazmu jsou uváděny tyto možnosti:
1. Endoteliální dysfunkce
Endotel na jedné straně produkuje vazodilatační látky, jako je oxid dusný (NO), prostacyklin, bradykinin, a na druhé straně reguluje expresi vazokonstrikčních látek, jako jsou tromboxan A2, endotelin a angiotenzin II. Normální endotel tvoří ideální rovnováhu trombotických a fibrinolytických procesů. NO produkovaný endotelem inhibuje adhezi leukocytů pravděpodobně inaktivací superoxidového aniontu. Je prokázán vliv oxidačního stresu na vznik endoteliální dysfunkce.
Byly prováděny nejrůznější studie, které měly potvrdit vliv endoteliální dysfunkce na vnik VSA.
Kugiyama [13] zjistil sníženou tvorbu NO jako přirozeného vazodilatátoru u pacientů s VSA. Dále studoval vliv redukovaného glutathionu (GSH) (antioxidant, který preventivně působí proti inaktivaci endoteliálního NO) na vznik VSA [14]. Prokázal, že GSH podaný v infuzi potlačí u pacientů s VSA spazmus koronárních cév vyvolaný současným podáním acetylcholinu.
Příčinou spazmu může být porucha interakce mezi vazodilatačními účinky endoteliálního relaxačního faktoru a vazospastickými účinky neuropeptidu Y a tromboxanu B2 [34]. Autoři vyšetřovali hladinu neuropeptidu Y a tromboxanu u skupiny pacientů s VSA, u skupiny pacientů se stabilní anginou pectoris a kontrolní skupiny, a to v době před hyperventilačním testem, ihned po jeho dokončení a po 10 minutách klidu. Prokázali statisticky významný vzestup obou humorálních faktorů u skupiny s VSA po hyperventilaci ve srovnání s ostatními skupinami.
Halawa ve své práci popisuje zvýšení transmembranózního efluxu kalcia a zvýšení hladiny endotelinu u pacientů s VSA po hyperventilačním testu [5] a uvádí, že tyto dva faktory mohou být odpovědny zavznik arteriálního spazmu.
Vzhledem k úloze oxidačního stresu byl sledován vliv antioxidačních látek na vznik VSA. Byla popsána nízká hladina E vitaminu [20] u pacientů s VSA, dále pozitivní vliv léčby vitaminem E na vazodilataci cév u pacientů s VSA [25]. Pozitivním vlivem podání vitaminu C na snížení četnosti vzniku spazmu se zabývali japonští autoři [15].
2. Úloha zánětu při vzniku VSA
Zvýšené hladiny fosfolipázy A se nacházejí u nejrůznějších chronických zánětlivých onemocnění [1]. Kugiyama [12] u skupiny 57 pacientů s VSA prokázal zvýšené hladiny fosfolipázy A ve srovnání se skupinou pacientů se stabilní anginou (46 pacientů) a s kontrolní skupinou (53 pacientů). Zvýšení hladiny fosfolipázy A bylo podle statistické analýzy signifikantně rizikovým faktorem pro vznik koronárního spazmu a dá se předpokládat, že souvisí se zánětlivou aktivitou jako možným mechanizmem koronárního spazmu.
3. Sympatovagální dysbalance
Dysbalance autonomního nervstva může vyvolat VSA. U pacientů s VSA byla nalezena snížená vagová reaktivita, která byla potvrzena spektrální analýzou [16]. VSA může být i manifestací onemocnění, která se vyznačují generalizovanou poruchou reaktivity cév, jako je migréna a Raynaudův fenomén [28].
4. Magnezium
U pacientů s VSA byla nalezena nízká hladina intracelulárního magnezia [35]. Byl prokázán pozitivní vliv podání magnezia na vznik koronárního spazmu [46].
5. Hyperinzulinemie a inzulinová rezistence
U některých pacientů s VSA byla nalezena hyperinzulinemie a inzulinová rezistence [1], a inzulinová rezistence [32] bývá uváděna jako možný faktor vzniku VSA.
6. Úloha koagulačních faktorů
U pacientů s VSA byly nalezeny zvýšené hladiny plazmatického fibrinopeptidu A [31]. Misumi et al [19] se ve své práci zabývali hladinou antigenu inhibitoru tkáňového faktoru (TFPI). TFPI inhibuje začátek kaskády koagulace spuštěné tkáňovými faktory. Prokázali, že pacienti s VSA mají signifikantně vyšší cirkadiánní variaci tohoto antigenu, jeho hladina stoupá po ischemickém ataku a je nejvyšší v době od půlnoci do rána (doba nejčastějších projevů VSA).
7. Ostatní faktory
Mezi ostatní faktory, které mají vliv na vznik VSA, zařazujeme kouření [42], abúzus kokainu [1] a pozitivní vliv alkoholu [4].
8. Vztah VSA a aterosklerózy
Spazmus může akcelerovat proces aterosklerózy a vést k hyperplazii intimy [4], a zhoršuje tak endoteliální dysfunkci. Další zhoršení aterosklerotického procesu může být způsobeno i spazmem indukovanou aktivací koagulačního systému, která se děje buď aktivací krevních destiček nebo vyvolanou krevní stázou, která způsobuje konverzi fibrinogenu na fibrin.
9. Vztah VSA a kardiologického syndromu X
V současné době je zkoumán vztah mezi VSA a kardiologickým (koronárním) syndromem X. Syndrom X byl původně definován jako angina pectoris s negativním nálezem při selektivní koronarografii (SKG). Nyní je tento syndrom definován jako angina pectoris, negativní nález na SKG a průkaz myokardiální ischemie (většinou při zátěži – ergometrie, dobutaminové ECHO, SPECT) [45]. U části pacientů se syndromem X objevíme patologickou odpověď koronárního průtoku na vazodilatační podněty a snížení koronární rezervy. Tento syndrom nazýváme někdy mikrovaskulární angina. V jeho patogenezi je zdůrazněna úloha endoteliální dysfunkce.
Vztahem VSA a mikrovaskulární anginy (kardiologický syndrom X) se zabýval Sun [43]. V souboru 55 pacientů s prokázanou VSA pomocí koronarografie s provokací acetylcholinem popsal zároveň mikrovaskulární anginu u 25,5 % pacientů. Mikrovaskulární angina byla vyvolána submaximální dávkou acetylcholinu, byla provázena bolestí na hrudi, EKG změnami a vyšší produkcí laktátu. Ve skupině s přítomnou mikrovaskulární anginou bylo statisticky více žen a stenokardie trvaly delší dobu (30 minut a více).
Klinický obraz
V klinickém obrazu dominuje bolest na hrudi, která bývá popisována jako typická retrosternální a výrazná. Bolest se objevuje nejčastěji v klidu a hlavně v ranních nebo dopoledních hodinách. Pacienti obvykle dobře tolerují námahu, která nevyvolává bolesti. Často bývají postiženi mladší nemocní, ženy a silní kuřáci.
Bolest někdy bývá spojena se synkopou nebo arytmiemi (AV-blok, asystolie, komorové arytmie). VSA může být příčinou zvýšené hladiny troponinu I jako projevu nekrózy myokardu [48] u pacientů s akutním koronárním syndromem a negativní koronarografií.
Klinicky nelze prakticky rozlišit VSA s normálním koronarogramem a VSA s těžkým nálezem stenóz na koronárních cévách.
Spazmus může být v některých případech spojen s vývojem dilatační kardiomyopatie [30].
Prognóza
Co se týká prognózy pacientů s VSA, je většinou považována za velmi dobrou, 5leté přežívání je 89–97 % [4]. Byly ovšem popsány i případy náhlé smrti a výskyt život ohrožujících arytmií [27,33].
Diagnóza
Diagnóza VSA se stanovuje pomocí několika testů.
1. Základním vyšetřením je EKG
Při bolesti se často objevují na EKG elevace ST-úseku, někdy spojené s arytmiemi. V nízkém procentu případů se objevují i deprese ST-úseku spojené se změnami T-vlny, které ale nebývají spojené s arytmiemi. Alternans ST-úseku, T-vlny a nárůst R - vlny bývá spojen s výskytem potenciálně maligní komorové arytmie. U některých pacientů se vyskytuje i němá ischemie. U pacientů se nacházejí přechodné poruchy nitrosrdečního vedení a komorové extrasystoly.
Ke stanovení diagnózy je vhodné použít Holterovu monitoraci EKG nebo i transtelefonní přenos EKG.
Zátěžová ergometrie nebývá příliš přínosná, protože odpověď pacientů s VSA na zátěž je velmi rozdílná. U některých pacientů se objevují deprese nebo elevace ST při zátěži, u ostatních se neobjevují žádné změny.
2. Selektivní koronarografie
Základním vyšetřením pro diagnózu VSA je selektivní koronarografie (SKG) s ventrikulografií. Při SKG provedené při záchvatu bolesti bývá potvrzen spazmus velké cévy. Při SKG můžeme diagnostikovat i přítomné organické stenózy. Spazmus se objevuje nejčastěji na pravé koronární arterii, na druhém místě je ramus interventricularis anterior [4]. SKG lze doplnit provokačními testy.
3. Provokační testy
Provokační agens (ergonovin, acetylcholin, hyperventilaci) lze použít i v kombinaci s SKG nebo s jinou zobrazovací metodou, jako je echokardiografie nebo nukleární metody.
Ergonovin maleát
Ergonovin maleát je ve světě nejrozšířenější provokační agens [24], test má senzitivitu až 100 % [49]. Ergonovin maleát stimuluje alfa–adrenergní a serotoninové receptory a má tak přímý vazokonstrikční vliv na cévy. Dávka se pohybuje od 0,05–0,4 mg intravenózně. Jako komplikace podání je popisován prolongovaný spazmus, který může vést ke vzniku infarktu myokardu. Proto je doporučováno jeho podání u pacientů s normální nebo téměř normální SKG a při podání začít s malými dávkami. Při vzniku spazmu se doporučuje in trakoronární podání nitroglycerinu.
Podání vysokých dávek ergonovinu vede u pacientů s normálními koronárními cévami k difuzní redukci průsvitu koronárních cév (vazokonstrikční efekt). Tento fenomén se liší od typické VSA, která se vyznačuje fokálním spazmem. Výskyt tohoto fenoménu bývá připisován existujícím minimálním aterosklerotickým změnám cév.
Acetylcholin
Podání acetylcholinu intrakoronárně může indukovat spazmus u pacientů s VSA. Senzitivita tohoto testu je udávána 95 % a specificita 99 % [4].
Ostatní látky
Methacholin, histamin a dopamin mohou také indukovat spazmus u pacientů s VSA [4].
Hyperventilace
Hyperventilace u zdravého jedince vede k signifikantnímu zvýšení pulzové frekvence a krevního tlaku. Je to jednoduchá metoda k vyvolání koronárního spazmu [3], mechanizmus provokace je zatím nejasný. Je zvažována úloha respirační alkalózy vyvolané hyperventilací při vzniku spazmu. Tento test má 62% senzitivitu a 100% specificitu ve srovnání s koronarografií s provokací spazmu acetylcholinem [29]. Ve spojení s echokardiografií má tato metoda senzitivitu 84 % specificitu 100 % ve srovnání se koronarografií spojenou s provokací spazmu ergonovinem [23]. Tento test nerozliší spazmus při normálním nálezu při SKG a spazmus při současné stenóze koronární tepny.
Hyperventilace se dá kombinovat i se zátěží na běhátku [38], tato kombinace signifikantně zvyšuje provokaci bolestí na hrudi oproti samotné hyperventilaci nebo kombinaci hyperventilace a chladového testu.
Ve studii Suedy [39] u skupiny 58 pacientů při kombinaci hyperventilace a následné zátěže na běhátku byla potvrzena 100% specificita této kombinace pro diagnózu VSA. Senzitivita byla 63%.
Kombinace hyperventilace, chladového testu a echokardiografického vyšetření má ve srovnání s acetylcholinovým testem při koronarografii [6] senzitivitu 91 % a specificitu 90 %. Změny kinetiky se objevují dříve než změny na EKG a bolest na hrudi. Porucha kinetiky myokardu prokázaná na echokardiografii přitom odpovídala oblasti zásobované tepnou, na které byl acetylcholinem vyvolaný spazmus.
4. Nukleární metody
K zobrazení poruchy perfuze lze použít i nukleární metody v kombinaci s některým provokačním testem – s ergometrií, hyperventilací [9,17,18]. Hirano ve své práci srovnává zátěžový test (hyperventilaci spojenou s chladovým testem) v kombinaci s echokardiografickým vyšetřením anebo scintigrafií myokardu pomocí I-MIBG [7]. Specificita echokardiografie ve srovnání se scintigrafií je statisticky vyšší.
5. Ostatní metody
K diagnostice VSA lze použít i mentální stres [51] – například opakování naučených číslic a sčítání číslic. Miyata et al popsali i použití head up tilt testu v kombinaci s podáním isoproterenolu k provokaci VSA [22].
Léčba
Léčba pacientů s VSA je velmi složitá. Při výběru terapie záleží na tom, zda se jedná pouze o VSA nebo jde o pacienta s fixní koronární stenózou komplikovanou vznikem spazmu.
Zatím nebyly provedeny velké klinické studie, které by srovnávaly účinky jednotlivých medikamentů a jejich účinek proti placebu. Důvodem je pravděpodobně relativně nízký výskyt pacientů s VSA a také nejednotný mechanizmus vzniku VSA.
1. Nitráty
Nitráty se svým vazodilatačním účinkem jsou základem terapie u obou výše uvedených skupin. Můžeme použít jak sublingvální a intravenózní nitráty při akutním záchvatu, tak i dlouhodobě působící preparáty pro prevenci vzniku spazmu.
2. Beta−blokátory
Odpověď na beta-blokátor u pacientů s VSA je různá. Beta-blokátory mohou zhoršovat spazmus epikardiálních koronárních cév [11]. Na druhé straně je popsán pozitivní vliv betaxololu na zlepšení tolerance zátěže u pacientů s VSA [44].
3. Kalcioví antagonisté
Kalcioví antagonisté jsou v prevenci spazmu velmi efektivní. Tyto léky se mají podávat v maximální tolerované dávce.
Ovšem i tato terapie má své limitace, jak uvádí Sueda [40]. Pouze 38 % pacientů s VSA léčených dlouhodobě působícími kalciovými antagonisty bylo při medikaci bez potíží. Na medikaci lépe reagovaly ženy a ti pacienti, kteří měli obraz elevací ST-úseků při provokačních testech. Oproti tomu pacienti s delší anamnézou bolestí na hrudi a s prokázaným difuzním spazmem reagovalina terapii hůře.
4. Ostatní léky
Ostatní léky, jako je prazosin [47], troglitazon [26] a denopamin [36] se zatím nedočkaly většího rozšíření v terapii VSA.
V otázce medikace kyseliny acetylsalicylové není jednota. Někteří autoři její podání nedoporučují [4] vzhledem k jejímu negativnímu vlivu na tvorbu prostacyklinu.
V poslední době někteří autoři [10] popisují i efekt suplementace estradiolu u pacientek s VSA v menopauze. Použití estradiolu je doporučeno vzhledem k jeho účinku na zlepšení endoteliální dysfunkce, která se na vzniku spazmu může podílet.
Sueda [41] potvrdil, že intravenózně podané magnezium může zabránit vzniku spazmu vyvolaného zátěží u pacienta s VSA, nenašel ale korelaci u pacienta s deficitem magnezia. Intravenózně podané magnezium má pouze omezený účinek u pacientů s VSA.
Motoyama [25] popisuje zlepšení vazodilatace u pacientů s VSA při medikaci vitaminem E. Švýcarští autoři [2] popisují účinný vliv brachyterapie u pacientů s VSA.
5. Invazivní řešení
U pacientů s refrakterním klinickým obrazem VSA někteří autoři použili i aplikaci koronárního stentu do místa spazmu [8].
Vlastní zkušenosti
Na našem pracovišti se diagnostikou VSA zabýváme již delší dobu [37].
Provokaci spazmu pomocí ergonovin maleátu prakticky nepoužíváme. Důvodem byla jeho přechodná nedostupnost (dva roky nebyl dostupný na našem trhu) a dále organizace práce v katetrizační laboratoři. Na Echodnech ČKS v roce 2003 byla velká diskuse mezi pracovníky předních českých kardiologických pracovišť o užívání tohoto preparátu. Závěrem bylo shrnuto, že ergonovin maleát používá pouze minimum katetrizačních laboratoří, a to hlavně vzhledem k jeho vedlejším účinkům (osobní zkušenosti).
Acetylcholin v lékové formě vhodné pro provokaci spazmu není v současné době v ČR k dispozici, dá se objednat jako mimořádný dovoz, a to konkrétně na „rodné číslo“ pacienta. Tak se stává pro běžné použití nedostupný.
Na našem pracovišti používáme asi čtyři roky hyperventilační echokardiografický test. Tento test je jednoduchý, levný a zatím jsme neměli žádnou komplikaci. Podle výsledků upravujeme terapii a pacienty s VSA ještě rok sledujeme.
MUDr. Eliška Sovová, Ph.D.
www.fnol.cz
e-mail: eliska.sovova@fnol.cz
Doručeno do redakce: 13. 8. 2003
Přijato po recenzi: 25. 6. 2004
Zdroje
1. Armstrong PW. Stable ischemic syndromes. In: Topol E. Textbook of Cardiovascular Medicine. Philadelphia: Lippincott Raven Publishers 1998.
2. Chatterjee T, Juelke PD, Thum P et al. Successful brachytherapy of coronary vasospasm. Heart 2003; 89(9): 25.
3. Cheng TO. Clinical implication of the hyperventilation test in the diagnosis of coronary artery spasm. Am J Cardiol 1997; 80 : 1647.
4. Gersh BJ, Braunwald E, Bonow BO. Chronic coronary artery disease. In: Braunwald E. Heart Disease. A textbook of cardiovascular medicine. 6th ed. Philadelphia: WB Saunders 2001.
5. Halawa B, Salomon P. Activity of transmembrane calcium transport and levels of endothelin-1 in patients with variant angina. Pol Arch Med Wewn 2000; 104(2): 447–453.
6. Hirano Y, Ozasa Y, Yamamoto T et al. Hyperventilation and cold pressor stress echocardiography for noninvasive diagnosis of coronary artery spasm. J Am Soc Echocardiogr 2001; 14(6): 626–633.
7. Hirano Y, Ozasa Y, Yamamoto T et al. Diagnosis of vasospastic angina by hyperventilation and cold pressor stress echocardiography: comparison to I-MIBG myocardial scintigraphy. J Am Soc Echocardiogr
2002; 15(6): 617–623.
8. Jeong MH, Park JC, Rhew JY et al. Successful management of intractable coronary spasm with a coronary stent. Jpn Circ J 2000; 64(11): 897–900.
9. Katamura M, Matsumuro A, Tamagaki S et al. Clinical significance of diffuse vasoconstriction of coronary arteries – a study using hyperventilation thallium 201 myocardial imaging. Kaku Igaku 1995; 32(5): 479–486.
10. Kawano H, Motoyama T, Hirai N et al. Estradiol supplementation suppresses hyperventilation – induced attacks in postmenopausal women with variant angina. JACC 2001; 37(3): 735–740.
11. Kugiyama K, Yassue H, Horio Y et al. Effects of propranolol and nifedipine on exercise induced attack in patients with variant angina: assesment by exercise thallium 201 myocardial scintigraphy with quantitative rotational tomography. Circulation 1986; 74 : 374–380.
12. Kugiyama K, Ota Y, Kawano H et al. Increase in plasma levels of secretory type II phospholipase A(2) in patients with coronary spastic angina. Cardiovasc Res 2000; 47(1): 159–165.
13. Kugiyama K, Yassue H, Okumura K et al. Nitrid oxide activity is deficient in spasm arteries of patients with coronary spasm angina. Circulation 1996; 94 : 266–272.
14. Kugiyama K, Miyao Y, Sakamoto T et al. Glutathione attenuates coronary constriction to acetylcholine in patients with coronary spastic angina. Am J Physiol Heart Circ Physiol 2001; 280(1): 264–271.
15. Kugiyama K, Motoyama T, Hirashima O et al. Vitamin C attenuates abnormal vasomotor reactivity in spasm coronary arteries in patients with coronary spastic angina. J Am Coll Cardiol 1998; 32(1): 103–109.
16. Lanza GA, Pedrotti P, Pasceri V et al. Autonomic changes associated with spontaneous coronary spasm in patients with variant angina. J Am Coll Cardiol 1996; 28(5): 1249–1256.
17. Masuoka T, Ajisaka R, Watanabe S et al. Usefullness of hyperventilation thallium 201 single photon emission computed tomography for the diagnosis of vasospastic angina. Jpn Heart J 1995; 36 : 405–420.
18. Minoda K, Yasue H, Kugiyama K et al. Comparison of the distribution of myocardial blood flow between exercise induced and hyperventilation induced attacks of coronary spasm: a study with thallium 201 myocardial scintigraphy. Am Heart J 1994; 127(6): 1474–1480.
19. Misumi K, Ogawa H, Yasue H et al. Circadian variation in plasma levels offree–form tissue factor pathway inhibitor antigen in patients with coronary spastic angina. Jpn Circ J 1998; 62(6): 419–424.
20. Miwa K, Miyagi Y, Igawa A et al. Vitamin E deficiency in variant angina. Circulation 1996; 94 : 14–18.
21. Miyao Y, Kugiyama K, Kawano H et al. Diffuse intimal thickening of coronary arteries in patients with coronary spastic angina. J Am Coll Cardiol 2000; 36(2): 432–437.
22. Miyata S, Inoue H, Horimoto M et al. Head up tilt test with isoproterenol infusion provokes coronary vasospastic angina. Jpn Circ J 1998; 62(9): 670–674.
23. Morales MA, Reisenhofer DR, Rovai D et al. Hyperventilation-echocardiography test for the diagnosis of myocardial ischemia at rest. Eur Heart J 1993; 14 : 1088–1093.
24. Morales MA, Lombardi M, Distante A et al. Ergonovine echo test to assess the significance of chest pain at rest without ECG changes. Eur Heart J 1995; 16(10): 1361–1366.
25. Motoyama T, Kawano H, Kugiyama K et al. Vitamin E administration improves impairment of endothelium – dependent vasodilation in patients with spastic angina. J Am Coll Cardiol 1998; 32(6): 1672–1679.
26. Murakami T, Mizuno S, Ohsato K et al. Effects of troglitazone on frequency of coronary vasospastic induced angina pectoris in patients with diabetes mellitus. Am J Cardiol 1984; 92 : 1999.
27. Myerburg RJ, Kessler KM, Mallon SM et al. Life threatening ventricuclar arrhythmias in patients with silent myocardial ischemia due to coronary spasm. N Engl J Med 1992; 326 : 1451–1455.
28. Nakamura Y, Shinozaki N, Hirashawa M et al. Prevalence of migraine and Raynaud’s phenomenon in Japanese patients with vasospastic angina. Jpn Circ J 2000; 64 : 239–242.
29. Nakao K, Ohgushi M, Yoshimura M et al. Hyperventilation as a specific test for diagnosis of coronary artery spasm. Am J Cardiol 1997; 80 : 545–549.
30. Nishi I, Ilda K, Kawano S et al. Effects of anti–vasospastic agents in Japanese patients with dilated cardiomyopathy and coronary vasospasm. Jpn Heart J 2002; 43(4): 333–342.
31. Ogawa H, Yasue H, Oshima S et al. Circadian variation of plasma fibrinopeptide A level in patients with variant angina. Circulation 1989; 80 : 1617–1626.
32. Reaven GM. Role of insulin resistance in human disease: Banting Lecture 1988 Diabetes 1988; 37 : 1595–1607.
33. Roberts WC, Curry RC, Isner JM et al. Sudden death in Prinzmetals angina with coronary spasm documented by angiography: analysis of three necropsy patients. Am J Cardiol 1982; 50 : 203–210.
34. Salomon P, Halawa B. Levels of neuropeptid Y and tromboxane B2 in patients with variant angina. Pol Arch Med Wewn 1998; 100(4): 313–320.
35. Satake K, Lee JD, Shimizu H et al. Relation between severity of magnesium deficiency and frequency of anginal attacks in men with variant angina. J Am Coll Cardiol 1996; 28 : 897–902.
36. Shimizu H, Lee JD, Ogawa K et al. Efficacy of denopamine in preventing anginal attacks due to coronary spasm. Cardioangiology 1991; 29 : 418–421.
37. Sovová E, Marek D, Škvařilová M et al. Echokardiografický hyperventilační test u pacientů s negativní koronarografií. Vnitř Lék 2001 : 47(3): 156–160.
38. Sueda S, Saeki H, Otani T et al. Investigation of the most effective provocation test for patients with coronary spastic angina: usefulness of accelerated exercise following hyperventilation. Jpn Circ J 1999; 63(2): 85–90.
39. Sueda S, Hashimoto H, Ochi N et al. New protocol to detect coronary spastic angina without fixed stenosis. Jpn Heart J 2002; 43(4): 307–317.
40. Sueda S, Kohno H, Fukuda H et al. Limitations of medical therapy in patients with pure coronary spastic angina. Chest 2003; 123(2): 380–386.
41. Sueda S, Saeki H, Otani T et al. Limited efficacy of magnesium for the treatment of variant angina. J Cardiol 1999; 34(3): 139–147.
42. Sugiishi M, Takatsu F. Cigarette smoking is a major risk factor for coronary spasm. Circulation 1993; 87 : 76–79.
43. Sun H, Mohri M, Shimokawa H et al. Coronary microvascular spasm causes myocardial ischemia in patients with vasospastic angina. J Am Coll Cardiol 2002; 39 : 847–821.
44. Suzuki J, Watanabe K, Tsuruoka T et al. Beneficial effects of betaxolol, a selective antagonist of beta-1 adrenoceptors, on exercise-induced myocardial ischemia in patients with coronary vasospasm. Int J Cardiol 2003; 91(2–3): 227–232.
45. Štejfa M. Kardiologický syndrom X: fact or fancy? Kardiologická revue 2002 : 4: 195–196.
46. Teragawa H, Kato M, Yamagata T et al. The preventive effect of magnesium on coronary spasm in patients with vasospastic angina. Chest 2000; 118(6): 1690–1695.
47. Tzivoni D, Keren A, Benhorin J et al. Prazosin therapy for refractory variant angina. Am Heart J 1983; 105 : 262–266.
48. Wang CH, Kuo LT, Hung MJ et al. Coronary vasospasm as a possible cause of elevated cardiac troponin I in patients with acute coronary syndrome and insignificant coronary artery disease. Am Heart J 2002; 144(2): 275–281.
49. Waters DD, Szlachic J, Bonan R et al. Comparative senzitivity of exercise, cold pressor and ergonovine testing in provoking attacks of variant angina in patients with active disease. Circulation 1983; 67:
310–315.
50. Yasue H, Kugiyama K. Coronary spasm: clinical features and pathogenesis. Intern Med 1997; 36(11): 760–765.
51. Yoshida K, Utsunomiya T, Morooka T et al. Mental stress test is an effective inducer of vasospastic angina pectoris: comparison with cold pressor, hyperventilation and master two step exercise test. Int J Card 1999; 70(2): 155–163.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2005 Číslo 5- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
- S prof. Vladimírem Paličkou o racionální suplementaci kalcia a vitaminu D v každodenní praxi
-
Všechny články tohoto čísla
- Katetrová ablace atrioventrikulární nodální reentry tachykardie
- Prodloužené podávání nízkomolekulárních heparinů
- Genetické testy v predikci toxicity chemoterapie – první krok nové éry onkoterapie
- Normoglykemie – terapeutický cíl pro diabetiky (i nediabetiky) v kritickém stavu
- Obezita, spánková apnoe a erektilní dysfunkce: tři vrcholy jednoho trojúhelníku?
- Naše zkušenosti s léčbou membranózní nefropatie cyklosporinem
- Akútna myokarditída, výskyt, diagnostika a liečba v spádovej nemocnici
- Prevence žilní trombózy a plicní embolie na interním oddělení
- Příčina klinických projevů chronické žilní nedostatečnosti u pacientů s nadváhou a obezitou
- Urgentní endoskopická papilosfinkterotomie u osob starších 70 let
- Prietok cez portálnu vénu a kongestívne poškodenie pečene u chorých s pokročilým srdcovým zlyhávaním
- Katetrová ablace atrioventrikulární nodální reentry tachykardie (neinvazivní možnosti diagnostiky, okamžité a jednoroční výsledky sledování skupiny 40 nemocných s provedenou radiofrekvenční ablací v roce 2002)
- Vazospastická angina pectoris – patogeneza, diagnostika a léčba
- Prodloužené podávání nízkomolekulárních heparinů v prevenci pooperační trombózy
- Genetické testy v predikcii účinnosti a toxicity chemoterapie u onkologických pacientov
- Pneumologická problematika pacientů s diabetes mellitus
- Obstrukční spánková apnoe, hypertenze a erektilní dysfunkce
- Lokalizace zdroje recidivujícího krvácení v tenkém střevě u hemoragické hereditární teleangiektazie pomocí scintigrafie s in vivo označenými erytrocyty pomocí 99mTc−pertechnetátu
- Systémová AL−amyloidóza s dominující klinickou manifestací v trávicím traktu
- Primář MUDr. Petr Svačina jubilující
- XXIV. dny mladých internistů, Olomouc 26.–27. 5. 2005 – gastroenterologie
- XXIV. dny mladých internistů, Olomouc 26.–27. 5. 2005 – hematologie
- XXIV. dny mladých internistů, Olomouc 26.–27. 5. 2005 – kardiologie
- XXIV. dny mladých internistů, Olomouc 26.–27. 5. 2005 – nefrologie
- XXIV. dny mladých internistů, Olomouc 26.–27. 5. 2005 – poruchy metabolizmu, endokrinologie, diabetes mellitus
- XXIV. dny mladých internistů, Olomouc 26.–27. 5. 2005 – revmatologie
- XXIV. dny mladých internistů, Olomouc 26.–27. 5. 2005 – varia
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Akútna myokarditída, výskyt, diagnostika a liečba v spádovej nemocnici
- Vazospastická angina pectoris – patogeneza, diagnostika a léčba
- Naše zkušenosti s léčbou membranózní nefropatie cyklosporinem
- Pneumologická problematika pacientů s diabetes mellitus
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



