-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaMutace asociované s rezistencí u pacientů s chronickou lymfocytární leukemií léčených ibrutinibem, idelalisibem a venetoklaxem
Resistance-associated mutations in chronic lymphocytic leukaemia patients treated with ibrutinib, idelalisib and venetoclax
Targeted BCR signalling pathway inhibitors (ibrutinib, idelalisib) and BCL2 inhibitors (venetoclax) appear promising in patients with chronic lymphocytic leukaemia (CLL), as they have shown significant clinical efficacy in relapsed/refractory high-risk patients with deletion 17p and/or TP53 mutation, as well as in first-line treatment. Nevertheless, there is a growing body of evidence regarding the emergence of mutations leading to clinical resistance during treatment. So far, most information has been reported in patients treated with ibrutinib (an irreversible inhibitor of Bruton’s tyrosine kinase, BTK), where resistance-associated mutations have been found in the BTK and PLCG2 genes. For idelalisib (an inhibitor of the δ isoform of phosphatidylinositol 3-kinase, PI3K), no resistance-associated mutation and/or aberrant signalling pathway have been reported, but a number of various genetic aberrations associated with CLL have been found in relapsing patients. Recently, mutations in the BCL2 gene have been reported in resistant patients treated with venetoclax (BCL2 inhibitor). In most patients who progressed on novel agents, the mutations associated with resistance occurred at low allelic frequencies between the second and fourth years of therapy. Frequently, several subclones are present which can be detected several months prior to clinical relapse. In this review, we report state-of-the-art data about known gene variants associated with resistance to ibrutinib, idelalisib and venetoclax, and the latest findings of their clinical impact. Nevertheless, recent findings suggest that there are also alternative mechanisms of acquired resistance to treatment with these inhibitors, which will certainly become the subject of further studies. We also discuss recent findings in the development of next-generation pathway inhibitors for the treatment of CLL patients who have acquired resistant mutations to current inhibitors.
Keywords:
chronic lymphocytic leukaemia – targeted therapy – signalling pathway inhibitors – mutations associated with resistance – resistance to treatment
Autoři: L. Sedlaříková 1; T. Papajík 2; A. Petráčková 1; P. Turcsányi 2; E. Kriegová 1
Působiště autorů: Ústav imunologie, Lékařská fakulta Univerzity Palackého a Fakultní nemocnice, Olomouc 1; Hemato-onkologická klinika, Lékařská fakulta Univerzity Palackého a Fakultní nemocnice, Olomouc 2
Vyšlo v časopise: Transfuze Hematol. dnes,26, 2020, No. 1, p. 46-54.
Kategorie: Souhrnné/edukační práce
Souhrn
Cílené inhibitory BCR signální dráhy (ibrutinib a idelalisib) a BCL2 inhibitor (venetoklax) představují velkou naději pro pacienty s chronickou lymfocytární leukemií (CLL), neboť prokázaly významnou účinnost u relabujících/refrakterních vysoce rizikových pacientů s delecí 17p a/nebo mutací TP53 pacientů i u pacientů v první linii léčby. V současné době se však objevují první zmínky o somatických mutacích u pacientů léčených těmito léky, které vedou k rezistenci na tuto léčbu. Nejvíce informací o mutacích asociovaných s rezistencí je v současnosti popsáno u pacientů léčených ibrutinibem (ireverzibilní inhibitor Brutonovy tyrosinkinázy – BTK), kde byly rezistentní mutace nalezeny v genech BTK a PLCG2. U idelalisibu (inhibitor δ izoformy fosfatidylinositol 3kinázy – PI3K) zatím žádná specifická mutace ani aberantní signální dráha asociovaná s rezistencí nalezena nebyla, ale často nacházíme u těchto pacientů heterogenní genetické aberace asociované s CLL. U pacientů rezistentních na léčbu venetoklaxem (inhibitor BCL2) byly nedávno popsány mutace v genu BCL2. U většiny pacientů, kteří progredují na uvedené léčbě, se detekovaly rezistentní mutace ve velmi nízkých alelických frekvencích během druhého až čtvrtého roku léčby. Často bývá přítomno několik subklonů s nízkou alelickou frekvencí, které lze detekovat několik měsíců před projevem klinického relapsu. V tomto článku podáváme přehled známých mutací asociovaných s rezistencí u pacientů léčených ibrutinibem, idelalisibem a venetoklaxem a nejnovější poznatky o jejich klinickém dopadu. Současné výzkumy však naznačují, že existují i jiné mechanismy vzniku rezistence u pacientů léčených těmito inhibitory, které budou určitě předmětem dalších studií. Diskutujeme také novinky ve vývoji dalších generací inhibitorů pro léčbu CLL pacientů rezistentních na ibrutinib, idelalisib a venetoklax.
Klíčová slova:
chronická lymfatická leukemie – cílená léčba – inhibitory buněčných drah – rezistentní mutace – rezistence na léčbu
ÚVOD
V posledních letech došlo ke klíčové změně terapeutického paradigmatu u chronické lymfocytární leukemie (CLL), a to zavedením dvou perorálních inhibitorů BCR signální dráhy (ibrutinibu a idelalisibu) a antagonisty BCL2 (venetoklaxu). Tyto inhibitory prokázaly významnou klinickou účinnost u relabujících/refrakterních CLL vysoce rizikových pacientů s delecí 17p a/nebo mutací TP53 a komplexním karyotypem, i v první linii léčby CLL pacientů. Přestože léčba inhibitory signálních drah navozuje dlouhodobou remisi u většiny pacientů, včetně těch s rizikovými genetickými aberacemi, dochází u části pacientů k relapsu onemocnění a/nebo selhání léčby. Vzhledem k dlouhodobému podávání těchto preparátů a stále širší skupině pacientů indikovaných k této léčbě se dá očekávat, že se počty pacientů, u kterých k rozvoji rezistence dojde, budou v budoucnosti zvyšovat. Proto je nezbytné porozumět mechanismům vzniku rezistence a identifikovat mutace a signální dráhy, které se na rozvoji rezistence podílí. Jen tak bude možné navrhnout nové cílené terapie a kombinaci léků, které zabrání vzniku rezistence nebo prokážou účinnost u rezistentních pacientů. V této přehledové práci shrnujeme současný stav znalostí o mutacích asociovaných s rezistencí a známých mechanismech vzniku rezistencí u pacientů léčených ibrutinibem, idelalisibem a venetoklaxem, včetně směrů výzkumu, jak tyto rezistence překonat.
REZISTENTNÍ MUTACE U LÉČBY IBRUTINIBEM
Nejvíce informací o výskytu rezistentních mutací je popsáno u pacientů léčených ibrutinibem, perorálním inhibitorem BCR signalizace, který se ireverzibilně váže na Brutonovu tyrozinkinázu (BTK). Tento preparát s proapoptotickým a antiproliferativním účinkem prokázal vysokou účinnost nejen u relabujících/refrakterních vysoce rizikových pacientů s delecí 17p a/nebo mutací TP53 a komplexním karyotypem [1, 2], ale také u neléčených pacientů v první linii s/bez rizikových genetických aberací [3, 4].
V roce 2014 byla popsána první mutace asociovaná s rezistencí u 5/6 vysoce rizikových CLL pacientů s del(17p) léčených ibrutinibem, u kterých došlo k relapsu onemocnění [5]. Jednalo se o mutaci (C481S) v genu BTK ve vazebném místě pro ibrutinib, která snižuje afinitu ibrutinibu k BTK [6, 7]. Řada studií přítomnost této mutace u pacientů relabujících na ibrutinibu potvrdila a prokázala, že tato mutace nebyla přítomna v době před podáním léku [8–10]. V dalších pracích pak byly nalezeny jiné sekvenční varianty v genu BTK ve vazebném místě pro ibrutinib (C481R, C481F a C481Y), ale také méně časté varianty na jiných pozicích (T316A, T474I/S a L528W) (obr. 1, tab. 1) [8, 11, 12, 13]. Funkční charakterizace mutací ve vazebném místě pro ibrutinib prokázala, že zvýšení dávky ibrutinibu nestačí k překonání vlivu těchto mutací [7]. Recentní práce u 30 CLL pacientů se zbytkovou lymfocytózou léčených 3 roky ibrutinibem potvrdila výskyt mutací v BTK u 57 % pacientů a jejich výskyt byl asociován s následným relapsem onemocnění [14].
Obr. 1. Schéma výskytu nejčastějších mutací asociovaných s rezistencí v genech A) BTK, B) PLCG2, C) BCL2 PH – Pleckstrin homologní doména, SH2/3 – Src homologní doména 2/3 (autoinhibiční doména), TH – Tec homologní doména, C-2 – motiv vázající vápník, X – katalytická doména, Y – katalytická doména, BH1–4 – BCL2 homologní doména 1–4 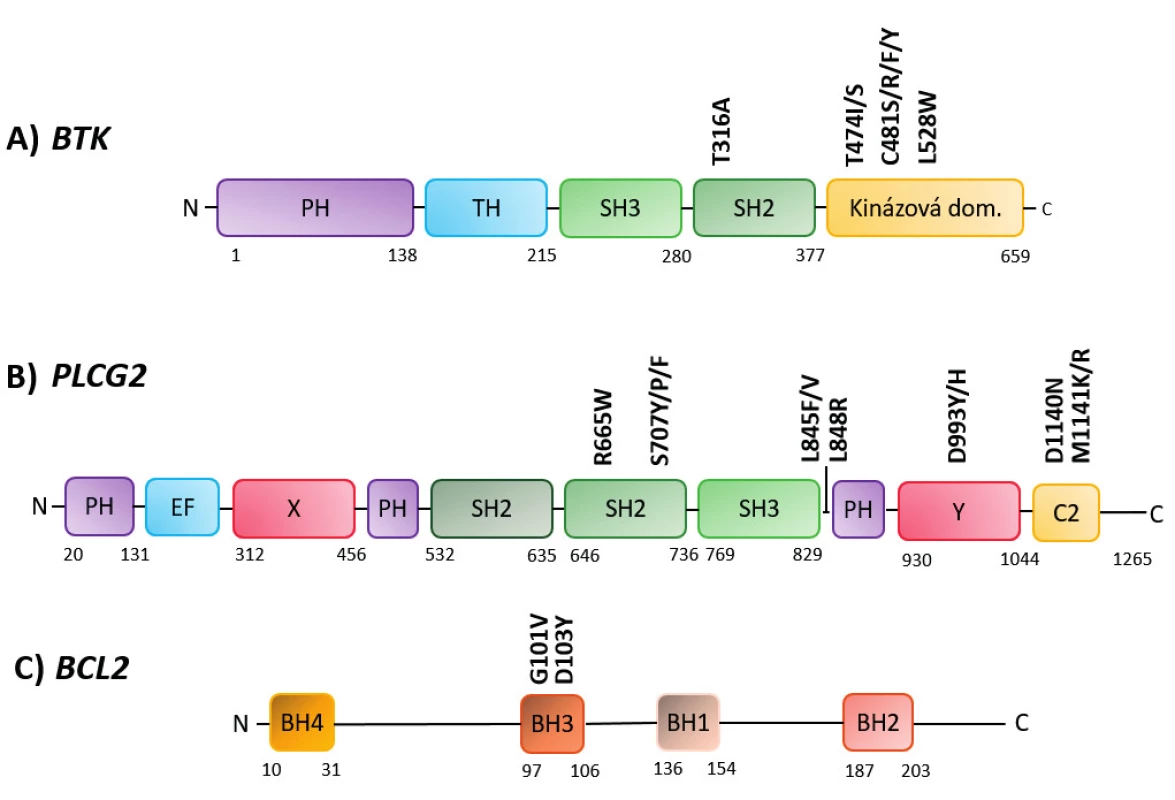
Tab. 1. Přehled vybraných studií popisujících výskyt mutací asociovaných s rezistencí u CLL pacientů léčených ibrutinibem 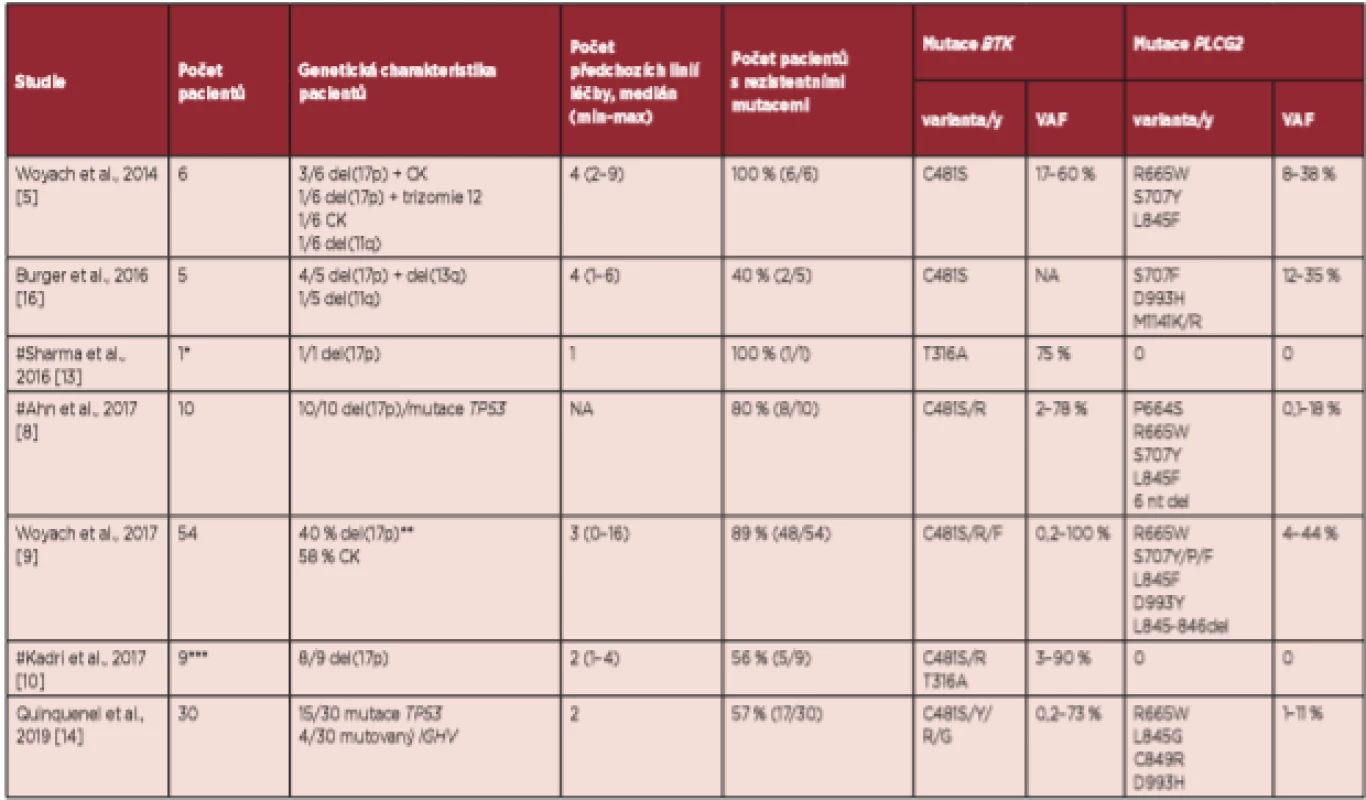
NA – není dostupné/neuvedeno, CK – komplexní karyotyp, VAF – frekvence variantní alely *Mutace asociovaná s rezistencí byla nalezena v periferní krvi, nikoliv v lymfatických uzlinách. ** Charakteristika pacientů ve studii Woyach et al. 2017 pro kompletní soubor 308 pacientů. *** Zařazeno 6/9 pacientů s Richterovou transformací. # vybrané studie popisující rezistentní mutace u Richterovy transformace CLL Dalším genem, jehož mutace jsou asociovány s rezistencí u CLL pacientů léčených ibrutinibem, je PLCG2. Většina mutací v PLCG2 vede k aktivaci fosfolipázy Cγ2 (PLCG2) v BCR signální dráze, což vede ke spuštění signální kaskády nezávisle na BTK [5, 15]. Mutace se nachází v několika doménách genu PLCG2 a často se vyskytují současně s BTK mutacemi. Většinou bývá přítomno několik subklonů s různými PLCG2 mutacemi s nízkou alelickou frekvencí (obr. 1) [8, 9, 11]. Recentní práce na 30 pacientech léčených 3 roky ibrutinibem se zbytkovou lymfocytózou uvádí výskyt mutace v PLCG2 u 13 % CLL pacientů [14]. Přesný mechanismus vlivu PLCG2 mutací na rezistenci zatím není zcela objasněn [15].
Přestože se mutace v BTK a PLCG2 genech vyskytují u přibližně 80 % CLL pacientů, kteří progredují na léčbě ibrutinibem [5, 8, 9], u zbývajících 20 % pacientů dosud neznáme příčinu vzniku rezistence [9, 10, 16]. Z toho vyplývá, že musí existovat alternativní mechanismy vzniku rezistence, které jsou stále předmětem zkoumání. Doposud bylo popsáno několik kandidátních lokusů/mutací, které mohou k rezistenci přispívat. Jedná se o del(8p) a mutace v genech SF3B1, PCLO, EP300, MLL2 a EIF2A [5, 10, 16]. Mezi další kandidátní genetické faktory asociované s rezistencí u pacientů léčených ibrutinibem řadíme přestavby BCL6, abnormality genu MYC, del(17p), del(18p), komplexní karyotyp a epigenetické změny [1, 10, 12]. Také změny mikroprostředí mohou přispívat k rezistenci [17]. Stále však není jasné, zda tyto genetické změny přispívají kauzálně ke vzniku rezistence.
Klonální výskyt mutací v BTK A PLCG2
S rezistencí asociované mutace v genech BTK i PLCG2 vznikají nejčastěji po více než roce léčby ibrutinibem (BTK: medián 34,3 měsíce, rozmezí 14–76,8 měsíce; PLCG2: medián 35,1 měsíce, rozmezí 17,4–64,6 měsíce) [11]. U téměř poloviny pacientů nacházíme subklony rezistentních mutací s velmi nízkou frekvencí variantní alely (VAF) pod 10 % [8, 9], u některých pacientů jsou detekovány varianty s > 80 % VAF [18]. U pacientů léčených ibrutinibem je také často pozorován klonální vývoj a subklonální heterogenita rezistentních mutací, tj. detekce více nezávislých subklonů nesoucích různé rezistentní mutace s různou rychlostí růstu [8, 16]. Ukazuje se, že zejména mutace v genu PLCG2 se často vyskytují ve formě více klonů s nižší VAF. Doposud však nebylo objasněno, jakým mechanismem malé subklony s mutacemi asociovanými s rezistencí vedou ke vzniku klinické rezistence na léčbu.
Z tkáňových biopsií bylo zjištěno, že se mohou rezistentní subklony i vlastní progrese onemocnění vyskytovat pouze v některých kompartmentech [9, 10]. Ve studii Woyach et al. (2017) byla u některých pacientů přítomnost rezistentních mutací popsána pouze v lymfatických uzlinách, kde také došlo k lokální progresi onemocnění, ale mutace nebyly prokázány současně v periferní krvi [9]. Proto je nutné volit správný odběrový materiál pro detekci rezistentních mutací a i negativní výsledek z periferní krve nemusí znamenat, že pacient nemá rezistentní mutace v jiné lokalitě [18].
Výskyt rezistentních mutací je většinou asociován s následným relapsem onemocnění [8, 9, 14]. V práci Woyach et al. (2017) byly detekovány rezistentní mutace už 9,3 měsíce před projevem klinického relapsu [9]. Také v práci Ahn et al. (2017) byly detekovány rezistentní mutace již 15 měsíců před projevem klinického relapsu [8]. S rezistencí asociované mutace BTK byly popsány rovněž u CLL pacientů léčených ibrutinibem, u kterých došlo k Richterově transformaci. U Richterovy trasformace jsou však tyto mutace přítomny v menším procentu pacientů (~ 40 %) a vznikají většinou do 15 měsíců po nasazení ibrutinibu, což je odlišuje od pacientů s rezistencí [9, 10] (obr. 2).
Obr. 2. Časová osa vývoje mutací asociovaných s rezistencí u CLL pacientů léčených ibrutinibem. U pacientů progredujících na léčbě ibrutinibem dochází nejčastěji k výskytu mutací v genech BTK a PLCG2 asociovaných s rezistencí mezi 2.–4. rokem léčby. Často bývá detekováno několik klonů s nízkou alelickou frekvencí, které lze detekovat několik měsíců před projevem klinického relapsu. K rozvoji Richterovy transformace dochází nejčastěji během prvních 15 měsíců léčby. Upraveno podle [8]. ![Časová osa vývoje mutací asociovaných s rezistencí u CLL pacientů léčených ibrutinibem. U pacientů progredujících na léčbě ibrutinibem dochází nejčastěji k výskytu mutací v genech BTK a PLCG2 asociovaných s rezistencí mezi 2.–4. rokem léčby. Často bývá detekováno několik klonů s nízkou alelickou frekvencí, které lze detekovat několik měsíců před projevem klinického relapsu. K rozvoji Richterovy transformace dochází nejčastěji během prvních 15 měsíců léčby. Upraveno podle [8].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/cdb890729878fbf1bcef73a9312ce598.jpeg)
REZISTENTNÍ MUTACE K IDELALISIBU
Idelalisib (inhibitor δ izoformy fosfatidylinositol 3-kinázy, PI3K) je další preparát pro léčbu CLL ze skupiny BCR inhibitorů, který nejen inhibuje PI3K signalizaci, ale současně selektivně indukuje apoptózu u CLL buněk [19]. V současné době jsou největší zkušenosti s léčbou idelalisibem v kombinaci s rituximabem především u skupiny relabujících/refrakterních CLL pacientů a vysoce rizikových pacientů s disrupcí TP53 [20, 21].
I přes intenzivní výzkum nebyl dosud nalezen gen nebo signální dráha asociovaná s rezistencí u pacientů léčených idelalisibem [22, 23]. Také biologický mechanismus progrese na tomto inhibitoru je dosud neznámý. Malá studie zaměřená na celoexomové sekvenování u 13 vzorků CLL pacientů, kteří progredovali na idelalisibu v rámci tří klinických studií, nenalezla žádné mutace v místě, kde se váže inhibitor ani jinde v PI3K nebo jiné signální dráze [24]. Výsledky naznačují, že pravděpodobně neexistuje jednotná dráha ani specifická mutace asociovaná s rezistencí na idelalisib [24].
Scheffold et al. (2019) provedli in vivo modelování rezistence k PI3K inhibitoru u myšího modelu a prokázal asociaci rezistence s deregulací genů zapojených v komplexu interginových receptorů, které se podílí na regulaci buněčné adheze, migrace, invaze a buněčného přežívání [23]. Skutečnost, že rezistence k idelalisibu stále nejsou asociovány s rekurentními mutacemi, ale pravděpodobně s deregulací signálních drah asociovaných s přežíváním a funkcí integrinových receptorů, bude určitě předmětem dalších studií.
REZISTENTNÍ MUTACE U LÉČBY VENETOKLAXEM
Dalším velmi nadějným preparátem pro léčbu CLL je perorální BH3 mimetikum venetoklax, který je selektivním inhibitorem antiapoptotického proteinu BCL2, schopným obnovit apoptózu nádorových buněk. V současné době jsou především zkušenosti s léčbou venetoklaxem u pacientů s CLL s disrupcí TP53 a těch, kteří jsou ibrutinib-rezistentní nebo nejsou vhodní pro léčbu inhibitory BCR signalizace [25, 26]. Venetoklax je vysoce účinný i u předléčených rizikových pacientů s CLL a pacientů refrakterních na imunochemoterapii [25, 27].
Teprve nedávná studie odhalila první mutaci asociovanou s rezistencí u pacientů, kteří selhali na venetoklaxu. Jedná se o bodovou mutaci (G101V) v genu BCL2, která byla detekována u 7 z 15 (47 %) CLL pacientů, kteří byli rezistentní k této léčbě [28]. Tato mutace byla prokázána po 19–42 měsících od zahájení léčby venetoklaxem a u párového vzorku z období před zahájením léčby prokázána nebyla. U pacientů byla evidentní velká variabilita v zastoupení klonu nesoucího (G101V) mutaci, a to v rozpětí 1,4–70 % [28]. Mutace byla prokázána 25 měsíců před klinickým relapsem a přetrvávala u většiny (5/7) pacientů více než 6 měsíců po ukončení terapie venetoklaxem na léčbě BTK inhibitory. Funkční studie prokázala, že samotná mutace (G101V) stačí k vyvolání rezistence na venetoklax, neboť 180krát snižuje afinitu léčiva k antiapoptotickému proteinu BCL2 [28]. Přítomnost vysoké subklonality (G101V) a skutečnost, že více než polovina rezistentních/relabujících pacientů tuto mutaci nenese, naznačují, že se na rezistenci k venetoklaxu mohou podílet alternativní dosud nepopsané mechanismy.
Také další recentní studie potvrdila výskyt mutace (G101V) u 3 ze 4 CLL pacientů s del(17p), u kterých vznikla rezistence k venetoklaxu v rámci klinické studie [29]. Zajímavý byl nález nové mutace v genu BCL2 (D103Y), která rovněž ovlivňuje vazbu venetoklaxu k proteinu BCL2, u jednoho z pacientů. Tato mutace se objevila 39 měsíců po zahájení léčby venetoklaxem s nízkou alelickou frekvencí (7 %) a nárůstem na 18 % během dalších 5 měsíců léčby. V pozdějším odběru byla u téhož pacienta nalezena současně i mutace BCL2 (G101V) s 14 % VAF. NGS analýza prokázala, že se jedná o dva různé nezávislé subklony s různou dynamikou růstu. V kontrolní skupině 546 pacientů s CLL neléčených venetoklaxem nebyly tyto mutace detekovány.
Jiná studie 8 CLL pacientů s del(17p), u kterých byla prokázána rezistence k venetoklaxu, popsala další kandidátní genetické aberace [30]. U 3 pacientů byla nalezena homozygotní delece CDKN2A/B, která má za následek ztrátu kontroly buněčného cyklu, a u 2 pacientů byly detekovány mutace v genu BTG1, který za normálních okolností působí proti buněčné proliferaci [30]. Analýzy párových vzorků z doby před zahájením léčby venetoklaxem prokázaly, že se tyto aberace vyvinuly až v průběhu léčby. Ve většině pacientských vzorků byly také detekovány mutace v genech BRAF, CD274, NOTCH1, RB1, SF3B1 a TP53. Přestože mutace BTG1, BRAF, homozygotní delece CDKN2A/B a amplifikace CD274 představují kandidátní aberace potenciálně asociované s rezistencí, jejich příspěvek k rezistenci na venetoklax není zatím objasněn [30].
ROLE SEKVENOVÁNÍ NOVÉ GENERACE (NGS) V DETEKCI REZISTENTNÍCH MUTACÍ
V detekci rezistentních mutací, které se často vyskytují v subklonech s nízkou frekvencí variantní alely, hraje klíčovou roli velmi citlivá technika NGS. Ukazuje se však, že pro detekci diagnostických vzorků s nízkou VAF je nezbytné nastavit parametry diagnostického NGS včetně zohlednění chybovosti přípravy knihovny i vlastního sekvenování s cílem minimalizovat falešně negativní a falešně pozitivní výsledky [31–34].
Výskyt rezistentních mutací s nízkou frekvencí VAF byl potvrzen i na naší kohortě 23 rizikových CLL pacientů léčených ibrutinibem. U dvou pacientů s mutací TP53, kteří selhávali na léčbě ibrutinibem, jsme prokázali v periferní krvi rezistentní mutace v BTK a PLCG2, které u předcházejícího párového vzorku z období před léčbou přítomny nebyly. U jednoho pacienta (P1) byla nalezena hotspot mutace BTK (C481S) s 4 % VAF v odběru z doby 35 měsíců po zahájení léčby ibrutinibem, přičemž předchozí odběr z období 28 měsíců po zahájení terapie byl negativní. Klon s mutací v genu TP53 (C277F, 17 % VAF), který byl přítomen před zahájením léčby ibrutinibem, v době detekce rezistentní mutace detekován nebyl. U dalšího pacienta s progresí na ibrutinibu (P2) byla přítomna mutace v genu PLCG2 (S707F) se zastoupením 8 % VAF v odběru z doby 7 měsíců po zahájení léčby ibrutinibem. Odběr z doby před zahájením léčby byl negativní (obr. 3). U tohoto pacienta přetrvával klon s mutací v genu TP53 (R110P), který byl přítomen před zahájením léčby ibrutinibem.
Obr. 3. Výsledek NGS analýzy mutací v PLCG2 genu asociovaných s rezistencí u CLL pacienta léčeného ibritinibem. (A) Schematické znázornění sekvenované oblasti a pokrytí genu PLCG2: hotspot oblasti v exonech 19, 20, 24, 27 a 30. (B) Negativní odběr z doby před zahájením léčby. (C) Pozitivní odběr z doby 7 měsíců po zahájení léčby ibrutinibem. 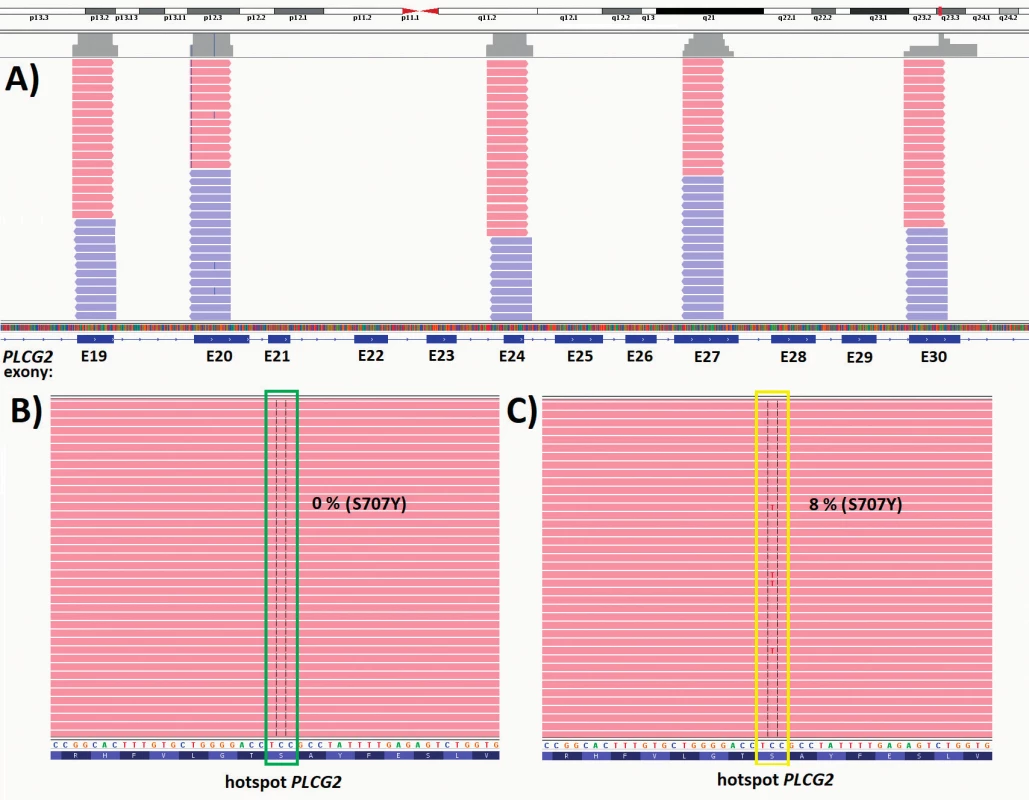
U všech pacientů léčených ibrutinibem byla detekována řada genetických aberací asociovaných s onemocněním CLL: u 14 pacientů patogenní mutace v TP53 genu, 11 pacientů del(17p) (z toho 64 % pacientů mělo současně del(17p)/TP53 mutaci), u 4 pacientů ATM mutace, 2 pacientů XPO1 mutace, 2 pacientů BIRC3 mutace, 2 SF3B1 mutace, 2 BRAF mutace, jeden pacient byl nositelem mutace v genu POT1. Jak již bylo popsáno dříve, stále není mnoho známo o příspěvku těchto genetických aberací na vznik rezistence.
MOŽNÉ CESTY PŘEKONÁNÍ REZISTENCE K NOVÝM INHIBITORŮM
V současné době slouží detekce rezistentních mutací BTK, PLCG2, BCL2 především jako biomarker blížící se progrese a selhání léčby [28, 35]. Proto by měl být výskyt těchto mutací u pacientů dlouhodobě léčených BCR a BCL2 inhibitory pravidelně testován pomocí vysoce citlivých laboratorních metod. U pozitivních pacientů by se neměla léčba těmito léky přerušit, ale měly by se navrhnout jiné vhodné inhibitory nebo alternativní kombinační terapie [36].
Poznání mechanismu vzniku rezistence je však klíčové také k návrhu nových přístupů, které by pomohly rezistenci překonat, případně zamezily jejímu vzniku. V současné době se hledají cesty, jak překonat rezistenci. Jednou z nich je cílení na jiné molekuly, případně jiné signální dráhy (obr. 4). Další možností je kombinace jednotlivých inhibitorů [36]. Velmi perspektivní se jeví nejen kombinace ibrutinibu s anti-CD20 protilátkami [21], ale především s venetoklaxem, neboť CLL buňky pacientů léčených BCR inhibitory vykazují zvýšenou závislost na expresi BCL2 [37, 38]. Zatím není známo, jak kombinační terapie nebo krátkodobé podávání BCR a BCL2 inhibitorů ovlivní výskyt mutací asociovaných s rezistencí, což prokážou další studie.
Obr. 4. Mechanismy rezistence vůči ibrutinibu a strategie jejího potenciálního překonání. Upraveno podle [45]. ![Mechanismy rezistence vůči ibrutinibu a strategie jejího potenciálního překonání. Upraveno podle [45].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/d8b9a771963e5c02054071dd0f828efe.jpeg)
V současnosti dochází k vývoji nových BTK inhibitorů, jako je acalabrutinib (ACP-196), tirabrutinib (ONO/GS-4059) a zanubrutinib (BGB-3111), které mají vyšší selektivitu vůči BTK [39–41]. Nicméně tyto inhibitory se na BTK váží kovalentně, stejně jako ibrutinib, a proto nejsou vhodné pro pacienty s rezistentní hotspot mutací BTK (C481S). Nově se testují inhibitory BTK druhé generace, které se k BTK váží nekovalentně a pro svůj účinek nevyžadují vazbu k C481 reziduu. Jedná se o vecabrutinib (SNS-062) a fenebrutinib (GDC-0853) [41, 42]. Výsledky prvních klinických studií s fenebrutinibem ukazují, že nekovalentní selektivní inhibice BTK může být účinná u rezistentních CLL pacientů léčených ibrutinibem [43]. Přesto bylo prokázáno in vitro mutagenezí v genu BTK, že mutace v kinázové doméně (L512M, E513G, F517L, L547P) snižují účinek těchto nových nekovalentních inhibitorů BTK [44]. V budoucnosti bude proto klíčové hledání dalších přístupů a možností, jak pokračovat v léčbě při vzniku rezistentních mutací.
ZÁVĚR
S rostoucími zkušenostmi s léčbou BCR a BCL2 inhibitory se ukazuje, jak nesmírně důležité je (1) detekovat genetické aberace asociované s rezistencí a progresí a (2) pochopit mechanismy vzniku rezistence a progrese onemocnění u pacientů léčených těmito preparáty. Mutace mohou také sloužit jako časný biomarker rezistence/progrese onemocnění, který je možno detekovat dlouho před klinickým relapsem, a umožnit tak včas terapeuticky zásahnout jinými inhibitory nebo různou kombinační terapií. Navíc pochopení mechanismu vzniku rezistence může pomoci hledat cesty, jak zamezit jejich vzniku, nebo jak je překonávat. Vzhledem k úspěšnosti léčby inhibitory buněčných drah můžeme v blízké budoucnosti očekávat nárůst počtu CLL pacientů, kteří budou indikováni k léčbě inhibitory, a také těch, kteří budou dlouhodobě léčeni těmito preparáty. Tato skutečnost se určitě odrazí v narůstajícím počtu pacientů rezistentních na léčbu, ale současně také v nových léčebných doporučeních s kombinacemi stávajících nebo nových cílených preparátů, které v klinických studiích prokazují svou klinickou účinnost. Je před námi dlouhá cesta a bude nutné se naučit zvládat rezistentní onemocnění, se kterým se budeme v éře léčby inhibitory buněčných drah stále častěji setkávat.
Podíl autorů na přípravě rukopisu
LS, EK: příprava rukopisu
AP, PT, TP, EK: revize, korekce rukopisu
Poděkování
Grantová podpora: MZ ČR VES16-32339A, IGA UP_2020_016, MH CZ-DRO (FNOL, 00098892)
Čestné prohlášení
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Do redakce doručeno dne 19. 12. 2019.
Přijato po recenzi dne 7. 1. 2020.
doc. Dr. Eva Kriegová
Ústav imunologie, Lékařská fakulta Univerzity Palackého a Fakultní nemocnice Olomouc
Hněvotínská 3
775 15 Olomouc
e-mail: eva.kriegova@email.cz
Zdroje
- Byrd JC, Furman RR, Coutre SE, et al. Targeting BTK with ibrutinib in relapsed chronic lymphocytic leukemia. N Engl J Med. 2013;369 : 32–42.
- Byrd JC, Hillmen P, O‘Brien S, et al. Long-term follow-up of the RESONATE phase 3 trial of ibrutinib vs ofatumumab. Blood. 2019;133(19):2031–2042.
- Burger JA, Tedeschi A, Barr PM, et al. Ibrutinib as initial therapy for patients with chronic lymphocytic leukemia. N Engl J Med. 2015;373(25):2425–2437.
- Barr PM, Robak T, Owen C, et al. Sustained efficacy and detailed clinical follow-up of first-line ibrutinib treatment in older patients with chronic lymphocytic leukemia: extended phase 3 results from RESONATE-2. Haematologica. 2018;103(9):1502–1510.
- Woyach JA, Furman RR, Liu TM, et al. Resistance mechanisms for the Bruton‘s tyrosine kinase inhibitor ibrutinib. N Engl J Med. 2014;370(24):2286–2294.
- Cheng S, Guo A, Lu P, Ma J, Coleman M, Wang YL. Functional characterization of BTK(C481S) mutation that confers ibrutinib resistance: exploration of alternative kinase inhibitors. Leukemia. 2015;29(4):895–900.
- Hamasy A, Wang Q, Blomberg KE, et al. Substitution scanning identifies a novel, catalytically active ibrutinib-resistant BTK cysteine 481 to threonine (C481T) variant. Leukemia. 2017;31(1):177–185.
- Ahn IE, Underbayev C, Albitar A et al. Clonal evolution leading to ibrutinib resistance in chronic lymphocytic leukemia. Blood. 2017;129(11):1469–1479.
- Woyach JA, Ruppert AS, Guinn D, et al. BTKC481S-mediated resistance to ibrutinib in chronic lymphocytic leukemia. J Clin Oncol. 2017;35(13):1437–1443.
- Kadri S, Lee J, Fitzpatrick C, et al. Clonal evolution underlying leukemia progression and Richter transformation in patients with ibrutinib-relapsed CLL. Blood Adv. 2017;1(12):715–727.
- Jones D, Woyach JA, Zhao W, et al. PLCG2 C2 domain mutations co-occur with BTK and PLCG2 resistance mutations in chronic lymphocytic leukemia undergoing ibrutinib treatment. Leukemia. 2017;31(7):1645–1647.
- Maddocks KJ, Ruppert AS, Lozanski G, et al. Etiology of ibrutinib therapy discontinuation and outcomes in patients with chronic lymphocytic leukemia. JAMA Oncol. 2015;1(1):80–87.
- Sharma S, Galanina N, Guo A, et al. Identification of a structurally novel BTK mutation that drives ibrutinib resistance in CLL. Oncotarget. 2016;7(42):68833–68841.
- Quinquenel A, Fornecker LM, Letestu R, et al. Prevalence of BTK and PLCG2 mutations in a real-life CLL cohort still on ibrutinib after 3 years: a FILO group study. Blood. 2019;134(7):641–644.
- Liu TM, Woyach JA, Zhong Y, et al. Hypermorphic mutation of phospholipase Cγ2 acquired in ibrutinib-resistant CLL confers BTK independency upon B-cell receptor activation. Blood. 2015;126(1):61–68.
- Burger JA, Landau DA, Taylor-Weiner A, et al. Clonal evolution in patients with chronic lymphocytic leukaemia developing resistance to BTK inhibition. Nat Commun. 2016;7 : 11589.
- Maffei R, Fiorcari S, Martinelli S, et al. Targeting neoplastic B cells and harnessing microenvironment: the „double face“ of ibrutinib and idelalisib. J Hematol Oncol. 2015;8 : 60.
- Lampson BL, Brown JR. Are BTK and PLCG2 mutations necessary and sufficient for ibrutinib resistance in chronic lymphocytic leukemia? Expert Rev Hematol. 2018;11(3):185–194.
- Hoellenriegel J, Meadows SA, Sivina M, et al. The phosphoinositide 3‘-kinase delta inhibitor, CAL-101, inhibits B-cell receptor signaling and chemokine networks in chronic lymphocytic leukemia. Blood. 2011;118(13):3603–3612.
- Brown JR, Byrd JC, Coutre SE, et al. Idelalisib, an inhibitor of phosphatidylinositol 3-kinase p110δ, for relapsed/refractory chronic lymphocytic leukemia. Blood. 2014;123(22):3390–3397.
- Burger JA, Wiestner A. Targeting B cell receptor signalling in cancer: preclinical and clinical advances. Nat Rev Cancer. 2018;18(3):148–167.
- Arnason JE, Brown JR. Targeting B cell signaling in chronic lymphocytic leukemia. Curr Oncol Rep. 2017;19(9):61.
- Scheffold A, Jebaraj BMC, Tausch E, et al. IGF1R as druggable target mediating PI3K-δ inhibitor resistance in a murine model of chronic lymphocytic leukemia. Blood. 2019; 134(6):534–547.
- Ghia P, Ljungström V, Tausch E, et al. Whole-exome sequencing revealed no recurrent mutations within the PI3K pathway in relapsed chronic lymphocytic leukemia patients progressing under idelalisib treatment. Blood. 2016;128 : 2770.
- Stilgenbauer S, Eichhorst B, Schetelig J, et al. Venetoclax in relapsed or refractory chronic lymphocytic leukaemia with 17p deletion: a multicentre, open-label, phase 2 study. Lancet Oncol. 2016;17 : 768–778.
- Jones JA, Mato AR, Wierda WG, et al. Venetoclax for chronic lymphocytic leukaemia progressing after ibrutinib: an interim analysis of a multicentre, open-label, phase 2 trial. Lancet Oncol. 2018; 19(1):65–75.
- Roberts AW, Davids MS, Pagel JM, et al. Targeting BCL2 with venetoclax in relapsed chronic lymphocytic leukemia. N Engl J Med. 2016;374 : 311–322.
- Blombery P, Anderson MA, Gong JN, et al. Acquisition of the recurrent Gly101Val mutation in BCL2 confers resistance to venetoclax in patients with progressive chronic lymphocytic leukemia. Cancer Discov. 2019;9(3):342–353.
- Tausch E, Close W, Dolnik A, et al. Venetoclax resistance and acquired BCL2 mutations in chronic lymphocytic leukemia. Haematologica. 2019;104(9):e434–e437.
- Herling CD, Abedpour N, Weiss J, et al. Clonal dynamics towards the development of venetoclax resistance in chronic lymphocytic leukemia. Nat Commun. 2018;9(1):727.
- Jennings LJ, Arcila ME, Corless C, et al. Guidelines for validation of next-generation sequencing-based oncology panels: a joint consensus recommendation of the Association for Molecular Pathology and College of American Pathologists. J Mol Diagn. 2017;19(3):341–365.
- Bacher U, Shumilov E, Flach J, et al. Challenges in the introduction of next-generation sequencing (NGS) for diagnostics of myeloid malignancies into clinical routine use. Blood Cancer J. 2018;8 : 113.
- Merker JD, Devereaux K, Iafrate AJ, et al. Proficiency testing of standardized samples shows very high interlaboratory agreement for clinical nextgeneration sequencing-based oncology assays Arch Pathol Lab Med. 2019;143 : 463–471.
- Petrackova A, Vasinek M, Sedlarikova L, et al. Standardisation of sequencing coverage depth in NGS: recommendation for detection of clonal and subclonal mutations in cancer diagnostics. Front Oncol. 2019;9 : 851.
- Sutton LA. Mechanisms of resistance to targeted therapies in chronic lymphocytic leukemia. HemaSphere. 2019;3(S2):p40–p43.
- Fürstenau M, Hallek M, Eichhorst B. Sequential and combination treatments with novel agents in chronic lymphocytic leukemia. Haematologica. 2019;104(11):2144–2154.
- Deng J, Isik E, Fernandes SM, et al. Bruton‘s tyrosine kinase inhibition increases BCL-2 dependence and enhances sensitivity to venetoclax in chronic lymphocytic leukemia. Leukemia. 2017;31(10):2075–2084.
- Bose P, Gandhi V. Recent therapeutic advances in chronic lymphocytic leukemia. F1000Res. 2017;6 : 1924.
- Byrd JC, Harrington B, O‘Brien S, et al. Acalabrutinib (ACP-196) in relapsed chronic lymphocytic leukemia. N Engl J Med. 2016;374(4):323–332.
- Walter HS, Rule SA, Dyer MJ, et al. A phase 1 clinical trial of the selective BTK inhibitor ONO/GS-4059 in relapsed and refractory mature B-cell malignancies. Blood. 2016;127(4):411–419.
- Thompson PA, Burger JA. Bruton‘s tyrosine kinase inhibitors: first and second generation agents for patients with Chronic Lymphocytic Leukemia (CLL). Expert Opin Investig Drugs. 2018;27(1):31–42.
- Crawford JJ, Johnson AR, Misner DL, et al. Discovery of GDC-0853: a potent, selective, and noncovalent bruton‘s tyrosine kinase inhibitor in early clinical development. J Med Chem. 2018;61(6):2227–2245.
- Reiff SD, Muhowski EM, Guinn D, et al. Noncovalent inhibition of C481S Bruton tyrosine kinase by GDC-0853: a new treatment strategy for ibrutinib-resistant CLL. Blood. 2018;132(10):1039–1049.
- Wang S, Mondal S, Zhao C, et al. Noncovalent inhibitors reveal BTK gatekeeper and auto-inhibitory residues that control its transforming activity. JCI Insight. 2019;4(12):pii:127566.
- Woyach JA. Patterns of resistance to B cell-receptor pathway antagonists in chronic lymphocytic leukemia and strategies for management. Hematology Am Soc Hematol Educ Program. 2015;2015 : 355–360.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2020 Číslo 1- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Antikoagulační léčba u pacientů před operačními výkony
-
Všechny články tohoto čísla
- Chromozomové změny u chronické lymfocytární leukemie, jejich prognostický a prediktivní význam
- Chromozomové aberace a jejich role v transformaci chronické lymfocytární leukemie v éře léčby inhibitory BCR signalizace
- Molekulárně genetické změny u Richterovy transformace chronické lymfocytární leukemie
- Mutace asociované s rezistencí u pacientů s chronickou lymfocytární leukemií léčených ibrutinibem, idelalisibem a venetoklaxem
- Rozvoj Richterovy transformace u nemocného s refrakterní chronickou lymfocytární leukemií na léčbě ibrutinibem
- Transformace chronické lymfocytární leukemie do Hodgkinovy varianty Richterova syndromu
- Vzdělávací workshop – uplatnění nových technologií v precizní medicíně CML a ALL
- Novinky z redakce
- Prof. MUDr. Ladislav Jebavý, CSc., slaví 70 let
- Životní jubileum MUDr. Věry Vozobulové
- Editorial
- Richterova transformace chronické lymfocytární leukemie v éře léčby inhibitory buněčných drah
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Chromozomové změny u chronické lymfocytární leukemie, jejich prognostický a prediktivní význam
- Molekulárně genetické změny u Richterovy transformace chronické lymfocytární leukemie
- Richterova transformace chronické lymfocytární leukemie v éře léčby inhibitory buněčných drah
- Transformace chronické lymfocytární leukemie do Hodgkinovy varianty Richterova syndromu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



