-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Synchronní, do jater metastazující karcinom rekta a možnosti simultánní resekce
Synchronous liver metastases of rectal cancer and the possibility of simultaneous resection
Treatment of metastatic rectal cancer and liver metastases continues to pose a major challenge. Synchronous liver metastases are present in up to one fifth of patients diagnosed with rectal carcinoma. Multidisciplinary cooperation is essential for determination of the consequent diagnostic and therapeutic plan. Only tight collaboration of experts from different medical fields allows for optimal timing of various medical procedures leading to a maximal benefit for the patient. Given the complexity of the problem, different specific methods and combinations thereof are applied in the course of the therapy, making the design of straightforward guidelines impossible. Since open surgery is complicated by the vastly distant locations of the rectum and liver, minimally invasive approach brings more perspectives in simultaneous surgery. A novel possibility of robotic and/or laparoscopic surgery performed by two teams is currently being developed. Despite the progress in surgical technology, optimal strategy has not yet been established.
Keywords:
rectal cancer – synchronous metastases – simultaneous resection
Autoři: M. Zatloukal 1; V. Procházka 1
; L. Ostřížková 2
; V. Válek 3; Z. Kala 1
; I. Penka 1
Působiště autorů: Chirurgická klinika Fakultní nemocnice Brno a Lékařské fakulty Masarykovy univerzity 1; Interní a hematoonkologická klinika Fakultní nemocnice Brno a Lékařské fakulty Masarykovy univerzity 2; Klinika radiologie a nukleární medicíny Fakultní nemocnice Brno a Lékařské fakulty Masarykovy univerzity 3
Vyšlo v časopise: Rozhl. Chir., 2019, roč. 98, č. 10, s. 394-398.
Kategorie: Souhrnné sdělení
Souhrn
Léčba metastazujícího karcinomu rekta a jaterních metastáz představuje stále vysoce aktuální problém. Synchronní metastázy jater jsou diagnostikovány až u pětiny pacientů s nově zachyceným karcinomem rekta. Je třeba, aby další strategie diagnosticko-terapeutického postupu probíhala od počátku za těsné mezioborové spolupráce s komisionálním hodnocením. Jen tímto způsobem lze zajistit optimální načasování jednotlivých léčebných modalit a maximální benefit pro pacienta. Složitost problematiky vede v průběhu léčby k uplatnění různých specifických metod a jejich vzájemných kombinací, které není možné v současné době vřadit do jednoduchých a jednoznačných schémat. V samotné chirurgii navíc situaci komplikuje zcela odlišná anatomická lokalizace jater a rekta, a tedy zásadně rozdílný operační přístup v otevřené chirurgii. Velkou perspektivu nyní přináší standardizace laparoskopických resekcí a roboticky asistovaných operací v obou lokalitách. Otevírají se tak možnosti dvoutýmových simultánních výkonů laparoskopickou/robotickou technikou či kombinovaným přístupem. I přes veškerý pokrok v chirurgických technikách však optimální postup není jednoznačně stanoven.
Klíčová slova:
karcinom rekta – synchronní metastázy – simultánní resekce
Úvod
Asi 20 % pacientů s diagnostikovaným karcinomem rekta je postiženo synchronními jaterními metastázami [1], což z této problematiky činí vysoce aktuální problematiku chirurgickou i onkologickou. Donedávna nebyla definice synchronicity plně jednotná; dnes se takto konsenzuálně označují ty metastázy, které jsou zjištěny v době diagnózy origa nebo před ní. Oproti pozdním metachronním metastázám – diagnostikovaným po 12 měsících – vykazují synchronní metastázy agresivnější biologickou povahu a pochopitelně i horší prognózu [2]. Problematika léčby metastazujícího karcinomu je složitá. Současná medicína disponuje různými terapeutickými modalitami, které lze kombinovat k dosažení co nejlepšího výsledku stran přežití a udržení kvality života. V rámci precizace medicíny se uplatňuje multidisciplinární přístup zahrnující pohled chirurga, klinického onkologa, radioonkologa, radiologa, gastroenterologa, patologa a dalších odborností, které volí strategii léčby a mohou přispět ke změně původně plánovaného postupu [3]. Z hlediska dlouhodobého přežití však hraje chirurgie kruciální úlohu, resekce primárního tumoru a metastáz zůstává jediným potenciálně kurativním způsobem léčby [4,5].
Metody
Terapeutická rozvaha
Léčebný plán závisí na kvalitním stagingu, v němž hrají hlavní úlohu zobrazovací vyšetření. U tumorů rekta dnes standardně využíváme zobrazení magnetickou rezonancí (MR) malé pánve, které podrobně zhodnotí velikost ložiska a jeho vztah k okolním strukturám, zejména k mezorektální fascii a svěračům. Dosahuje až 92% specificity při předpovědi negativního cirkumferenčního okraje [6]. Transrektální ultrasonografie (TRUS) je přínosná zejména k posouzení časných stadií nádoru rekta, kdy může přispět k indikaci lokální excize tumoru; u lokálně pokročilé formy onemocnění se její informační hodnota snižuje [7]. Zlatým standardem k diagnostice disseminace onemocnění je thorakoabdominální počítačová tomografie (CT). Výhodou MR oproti CT vyšetření je absence radiační zátěže, větší senzitivita u lézí menších než 1 cm a podle některých autorů lepší vyhodnocení ložisek po neoadjuvantní chemoterapii. Vyšetření pozitronovou emisní tomografií (PET), ve spojení s CT či magnetickou rezonancí, získává v souvislosti s lepší dostupností tohoto vyšetření větší prostor v diagnostice tumorů rekta. Jeho indikace však není rutinní, uplatňuje se při podezření na vzdálené metastázy, a to ve spojení s průkazem významné extramurální vaskulární invaze (EMVI), vysoké hladiny karcinoembryonálního antigenu (CEA) či suspektních lézí na CT či MR s dubiózním onkologickým potenciálem [8,9]. Zásadní význam má PET-CT v hodnocení rekurentních jaterních metastáz, kdy dosahuje senzitivity a specificity vysoko přes 90 % [10], a v posouzení léčebné odpovědi na předoperační onkologickou léčbu.
Hlavním sledovaným nádorovým markerem je CEA, vedlejším CA 19-9. Neslouží jako screeningové markery a není doporučeno je užívat v rámci preventivních vyšetření. V případě prokázaného tumoru se ale zvýšená hladina CEA považuje za nepříznivý prognostický faktor, v pooperačním období může být zvýšení jeho hladiny známkou relapsu onemocnění, proto je doporučeno pravidelně jeho hodnoty kontrolovat [8]. Izolované hodnocení jeho hladiny však není dostatečné a slouží pouze jako podpůrný prostředek [11].
Optimální postup k léčbě těchto pacientů není jednoznačně stanoven. Zcela nezbytné je projednat strategii léčby komisionálně a stanovit terapeutický plán multidisciplinárním konsenzem u jednotlivých pacientů individuálně. Vzhledem k pokročilosti onemocnění se však ve většině případů synchronního postižení doporučuje neoadjuvantní terapie [8], zahrnující chemoterapii, biologickou léčbu a radioterapii, zejména při nízkém karcinomu rekta. Této skutečnosti je rovněž podřízena strategie výkonu u symptomatických tumorů. Obstrukce trávicího traktu ohrožující jeho průchodnost si může vynutit akutní řešení formou derivační stomie; v případě, kdy neočekáváme provedení resekčního výkonu, lze užít samoexpandibilní stent. Krvácení z primárního tumoru způsobující anemii nebývá považováno za důvod k upřednostnění primární resekce origa. Většinou se daří zvládnout krevními převody a v průběhu podávané chemoterapie zpravidla ustává [2]. V případě neresekabilních jaterních metastáz je při systémové onkologické léčbě předpoklad zmenšení jejich velikosti, nepřímo pak lze odvodit senzitivitu tumoru na indukční léčbu [2]. Otázkou zůstává předřazení systémové léčby u resekabilních metastáz, kdy poměr přínosu léčby a vedlejších účinků na zdravý jaterní parenchym nemusí být výhodný pro další operativu v hepatální oblasti [2,12]. Základním požadavkem na chirurga je kompletní odstranění jaterních metastáz s bezpečným lemem zdravé tkáně při zachování dostatečného objemu funkčního jaterního parenchymu (FLR). V současné době je resekční okraj 1 mm zdravé tkáně považován za dostatečný [13,14]. Literární minimum 20 až 25 % ponechaného plně funkčního parenchymu u mladých pacientů se s věkem a zejména aplikovanou chemoterapií navyšuje na 40 i více procent ponechané jaterní tkáně, což může být pro chirurgický výkon výrazně limitující [15]. U menších metastatických ložisek uložených v hloubi parenchymu proto s výhodou užíváme možnosti kombinace s radiofrekvenční ablací (RFA).
Chirurgické postupy
V případě dosažené resekability, jejíž nutnou podmínkou je onkologická radikalita, je standardem léčby etapové chirurgické řešení karcinomu rekta a jaterních metastáz. V otázce načasování chirurgické resekce primárního tumoru či synchronních jaterních metastáz rozlišujeme v současné době tři základní postupy. Volba některého z nich závisí na stupni pokročilosti nálezu na rektu či játrech; obecně má přednost ten orgán, který je více postižen.
Dle toho pak uplatňujeme primary first approach, který je historicky starší, maximálně z něj benefitují symptomatičtí pacienti a dochází k resekci zdroje metastáz [16]. Někteří autoři popisují i přímý benefit resekce primárního tumoru při neresekabilních jaterních metastázách [17]. Chirurgický výkon na játrech pak následuje s odstupem 2−3 měsíců s vhodnou aplikací chemoterapie mezi operacemi [2]. U pacientů s možností rizikové anastomózy se využívá založení protektivní stomie [18,19]. Původní výhrady etapového postupu směřovaly k obavám z progrese nádorového onemocnění v mezidobí. Dnes se zdá, že tato progrese selektuje pacienty s velmi agresivním nádorovým onemocněním a je pravděpodobné, že by profit pro pacienty v těchto případech neznamenala ani simultánní resekce jaterních ložisek.
V případě inverzního, tzv. liver first přístupu je v první době provedena resekce jaterních metastáz. Ty mohou být resekabilní již zpočátku, či je u nich dosaženo resekability po aplikaci systémové terapie. Tyto metastázy jsou, v případě odložení jejich resekce, rizikové z hlediska další progrese a tedy jejich možné budoucí inoperability. Výhodou tohoto přístupu je umožnění včasného zahájení systémové terapie vzhledem k vyloučení možných septických komplikací souvisejících s resekčním výkonem na střevě. Dále je přístup vhodný pro extenzivní jaterní postižení u asymptomatického primárního tumoru rekta a rovněž v případě metastáz, u kterých bylo neoadjuvantní léčbou dosaženo resekability z původní inoperability [2]. Jestliže není před jaterní resekcí neoadjuvantní složka, označujeme tento postup jako up front hepatectomy; hlavním důvodem tohoto postupu volby je prevence chemoterapií indukovaného postižení jater [12].
Simultánní resekce
Koncept simultánní resekce byl u kolorektálního karcinomu představen Vogtem v roce 1991 [20]. Jde o chirurgicky přitažlivé pojetí resekce metastáz a primárního tumoru během jedné anestezie, které může vést ke zkrácení intervalu mezi chirurgickou a případnou adjuvantní léčbou, snížit počet potřebných hospitalizací a zmenšit jejich negativní vliv na pacienta.
Možnosti simultánního řešení karcinomu rekta byly v éře otevřené operativy většinou pouze ve sporadických případech. Specifika a náročnost operativy v malé pánvi spolu s nutností odlišné přístupové cesty obou anatomicky vzdálených orgánů umožňovala pouze řešení indikačně omezená především na oblast tumorů orálního rekta a dobře přístupných povrchových metastáz v segmentech II–VI jater. Výkony byly zatíženy vysokou perioperační morbiditou [21,22].
S rozvojem minimálně invazivní chirurgie, laparoskopických resekcí rekta a roboticky asistovaných operací a případné kombinace těchto modalit s otevřeným přístupem se možnosti simultánních resekcí zvýšily. Došlo k posunu problematiky i do méně přístupných jaterních segmentů a patologií středního a distálního rekta. Limitací širšího uplatnění tohoto přístupu bylo signifikantní prodloužení operačního času a peroperačních ztrát krve – hlavních příčin komplikací, zejména netěsnosti anastomózy střeva [23]. Technologická zlepšení v oblasti endoskopické techniky umožnila snížit tyto negativní faktory a umožnit rozšíření tohoto chirurgického řešení. V posledních letech bylo provedeno několik studií a analýz, které shledaly simultánní resekce s resekcí jater ekvivalentní etapovým postupům v krátkodobém měřítku [4,5,24–28]. Dlouhodobých výsledků bylo doposud publikováno méně, nicméně prezentované výsledky neukazují signifikantní rozdíl mezi uvedenými postupy, což přináší do budoucna slibná očekávání [29–31]. Ačkoliv někteří autoři popisují s příznivými výsledky i simultánní resekce zahrnující velké jaterní zákroky [32], je doporučeno provádět menší jaterní resekce, tj. do tří jaterních segmentů.
Jako perspektivní se jeví možnost kombinovat laparoskopické resekce jater s možnostmi potenciálně kurativního minimálně invazivního neoperačního řešení – k nimž patří zejména perkutánní radiofrekvenční ablace (RFA). RFA využívá proudu s vysokou frekvencí, který se převádí v místě ablace na teplo, čímž dochází k destrukci buněk. S výhodou je užíváme u malých metastáz v hloubi jaterního parenchymu, jež by vyžadovaly odstranění objemné porce zdravé tkáně. Dalším benefitem je zkrácení doby rekonvalescence, a tedy i intervalu bez systémové léčby, která je podstatným předpokladem úspěšné léčby. Z hlediska provedení lze tuto modalitu využít buď perkutánně s CT navigací, a to před operací, nebo po ní, či peroperačně. Limitací kvalitního ošetření s kurativním potenciálem je velikost metastázy do 3 cm [33].
Naše zkušenosti
Níže uvádíme dvě recentní kazuistiky z našeho pracoviště u pacientů s karcinomem rekta, u nichž byly prokázány vícečetné jaterní metastázy. Oba pacienti prodělali neoadjuvantní terapii, poté byli indikováni k resekčnímu výkonu pro příznivý nález při restagingu. Oba pacienti prodělali laparoskopickou resekci rekta současně s resekcí jaterních metastáz. U pacientů s vícečetnými metastázami jsme se zaměřili na odstranění povrchových metastáz; k destrukci intraparenchymatózních sekundárních nádorů byla multidisciplinárním týmem zvolena destrukce pomocí RFA.
Kazuistika 1
V době stanovení diagnózy 47letý pacient se zjištěným tumorem rekta v 10 cm, histologicky verifikován jako tubulární adenokarcinom G2. Dle provedeného MR pánve s podezřením na propagaci do perirektální tukové tkáně, CT břicha s obrazem metastáz bilobárně; největší v segmentu S2 (40x38 mm), další v segmentu S5, drobná ložiska susp. z metastáz v segmentech S6, S7/8, dále přítomny vícečetné nespecifické nodularity jater.
Pacient prošel multioborovou komisí s doporučením systémové chemoterapie a biologické léčby při pozitivní mutaci RAS. Po devíti cyklech chemoterapie a biol. léčby byla doplněna radioterapie na oblast rekta. Při restagingovém PET-MR byl primární tumor stacionární velikosti s lehkou regresí aktivity, nicméně došlo k metabolické a částečně velikostní progresi tří ložisek v S3, S4, S5 jater (21 mm, 14 mm, 8 mm respektive). Byla indikována operační revize zahrnující resekci tumoru a dostupných povrchových metastáz. Zbylá ložiska určena k ošetření radiofrekvenční ablací ve druhé době (Obr. 1).
Obr. 1. Vícečetné metastázy karcinomu rekta v játrech
Fig. 1: Multiple liver metastases of rectal cancer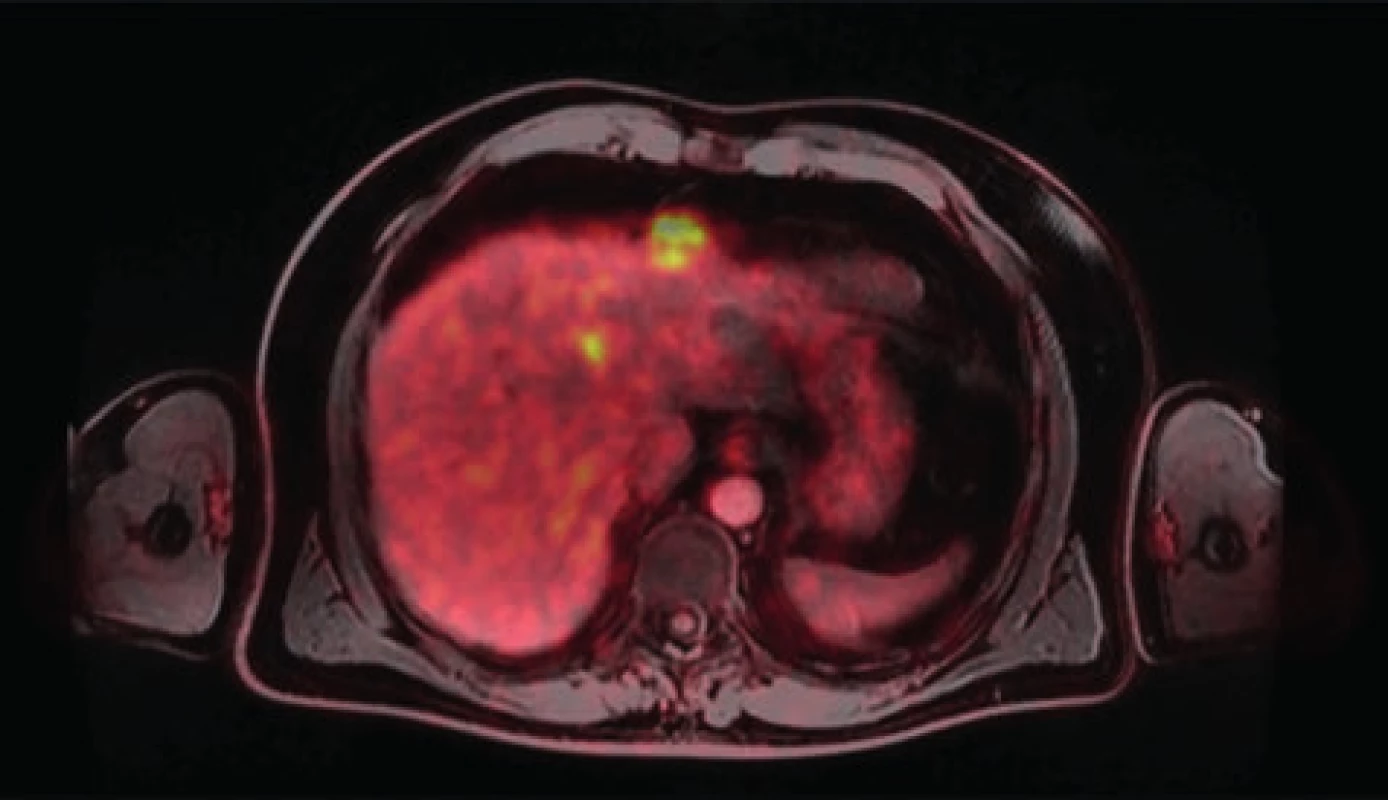
Deset měsíců od stanovení diagnózy byl proveden výkon v rozsahu atypické resekce metastázy v segmentu S3 jater. Výkon na játrech byl bez významného krvácení, bez oběhové nestability pacienta, bylo tedy možné následně provést laparoskopickou resekci rekta s TME (totální mezorektální excizí). Celkově trvala operace 6 hodin, bez významných ztrát krve. Pooperační průběh byl u pacienta komplikován protrahovaným nástupem peristaltiky, po obnovení pasáže a stabilizaci pacient dimitován. S odstupem 28 dnů od operace byl pacient opětovně přijat k RFA zbylých ložisek v játrech. Další den byla provedena ablace ložiska čtvrtého a pátého segmentu jater.
Histologicky byla v resekátu jater verifikována metastáza karcinomu intestinálního typu s bezpečným okrajem zdravé tkáně. V resekátu rekta byl potvrzen středně diferencovaný adenokarcinom infiltrující mezorektální tuk, s mírnou regresí po neoadjuvanci. Přítomných 5 pozitivních uzlin z 15 (typ T3, typ N2 a typ M1), resekční okraje bez přítomnosti malignity (vzdálenost od CRM 3 mm, od DRM 15 mm), kvalita TME 1. Po operaci a RFA přistoupeno k adjuvantní terapii kapecitabinem se zahájením 76 dnů od operace, nyní probíhá její 3. cyklus.
Kazuistika 2
64letý pacient s tumorem rekta ve 12 cm neprůchodným pro endoskop, způsobujícím poruchu pasáže. Dle stagingového PET-MR přítomna infiltrace mezorektální fascie vpravo, lymfadenopatie okolních lymfatických uzlin, 4 metastatická ložiska v jaterních segmentech − S8, dvě v S4b a S6. Po projednání multioborovou komisí doporučena systémová terapie se zajištěním průchodnosti trávicího traktu ileostomií.
Po 6 cyklech chemoterapie s biol. léčbou zjištěna přechodná regrese aktivity a velikosti metastáz v játrech, po doplněné radioterapii na oblast rekta však byla pozorována obnova původních jaterních lézí velikostně i metabolicky. Vzhledem k tomuto vývoji byla naplánována resekce rekta s resekcí povrchových metastáz; RFA zbylých ložisek k doplnění ve druhé době (Obr. 2).
Obr. 2. PET-MR obraz metastáz v segmentu S4
Fig. 2: PET-MR scan with two metastases in S4 segment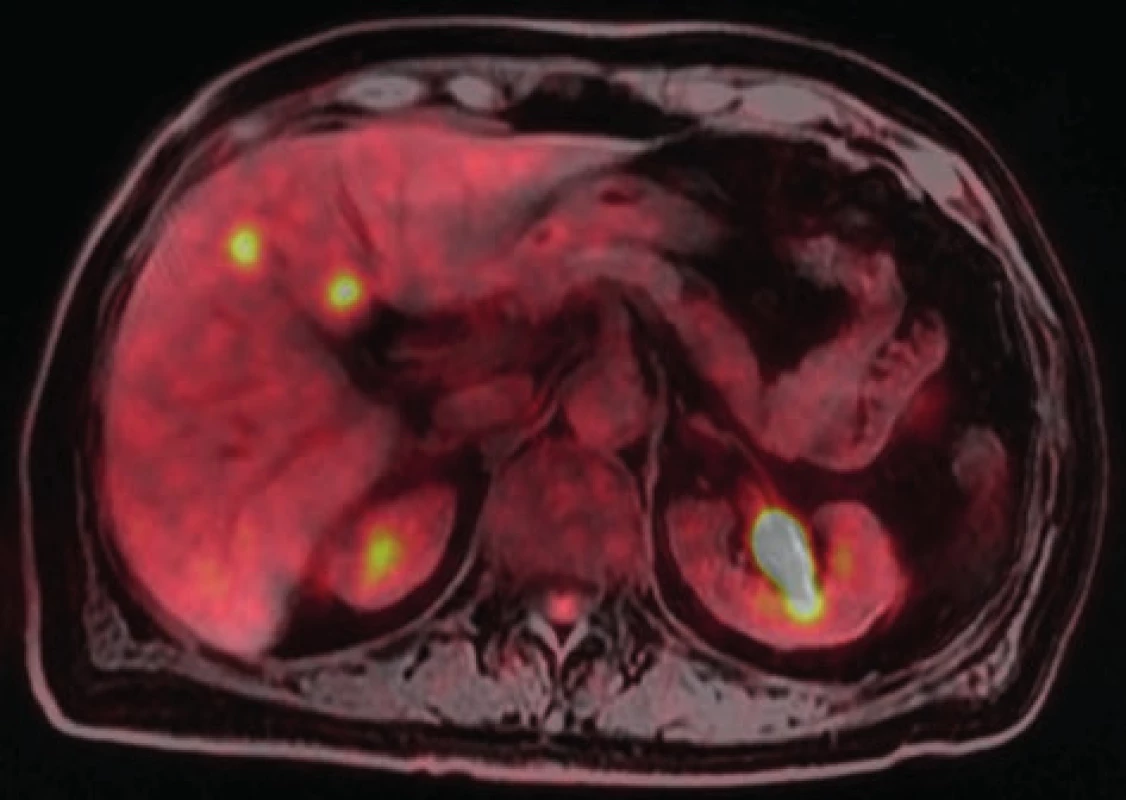
Během operačního výkonu byla provedena atypická resekce metastázy v S4b, které předcházela nutná cholecystektomie. Jaterní část výkonu proběhla bez komplikací, následně byla provedena resekce rekta. Výkon v délce 4 hodin proběhl s minimálními krevními ztrátami. Pooperační průběh byl bez komplikací, vzhledem k příznivému stavu pacienta konsenzuálně domluvena RFA zbývajících ložisek za téže hospitalizace. 9. pooperační den pak ablována zbývající tři metastatická ložiska. Pacient v dobrém stavu dimitován 19. pooperační den. Po operaci byl indikován k adjuvantní terapii, která nyní probíhá.
Histologicky byla potvrzena jaterní metastáza kolorekt. origa, v resekátu rekta klasifikován adenokarcinom typ T3 se střední regresí po neoadjuvanci, zastiženy 4 pozitivní lymfatické uzliny z 21 (typ N2). Resekční linie byly bez průkazu tumoru (vzdálenost tumoru od DRM 20 mm, od CRM 3 mm). Kvalita TME 1.
Závěr
Simultánní resekce synchronních jaterních metastáz a karcinomu rekta jsou diskutovanou variantou chirurgického postupu u čtvrtého stadia onemocnění. V době otevřené chirurgie sporadická a indikačně omezená možnost chirurgické intervence se při rozvoji minimálně invazivní chirurgie a rozšíření sofistikované technologie stala variantou s velkou perspektivou a obdobnými výsledky, jako mají etapové výkony; s výhodami plynoucími ze zkrácení doby hospitalizace a rychlejší chirurgické léčby. S výhodou lze využít kombinaci chirurgických resekcí s intervenčními metodami – RFA a metodami moderní radioterapie, které mohou rozšířit radikalitu výkonu se současným šetřením jaterního parenchymu. Přes všechny výhody a rozvoj tohoto přístupu zůstává simultánní resekce, vzhledem k její vysoké zátěži pro pacienta, vyhrazena citlivě a pečlivě vybraným jedincům s přihlédnutím k jejich celkovému zdravotnímu stavu. Postup léčby by měl vycházet ze shody v rámci mezioborové spolupráce.
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise.
doc. MUDr. Igor Penka, CSc.
FN Brno
Jihlavská 340/20
Brno 625 00
e-mail: penka.igor@fnbrno.cz
Zdroje
1. Národní onkologický registr (NOR) | ÚZIS ČR. Available from: https://www.uzis.cz/registry-nzis/nor (accessed 14 Jun 2019).
2. Adam R, de Gramont A, Figueras J, et al. Managing synchronous liver metastases from colorectal cancer: a multidisciplinary international consensus. Cancer Treat Rev. 2015;41 : 729–41. doi:10.1016/j.ctrv.2015.06.006.
3. Oxenberg J, Papenfuss W, Esemuede I, et al. Multidisciplinary cancer conferences for gastrointestinal malignancies result in measureable treatment changes: a prospective study of 149 consecutive patients. Ann Surg Oncol. 2015;22 : 1533–9. doi:10.1245/s10434-014-4163-y.
4. Ejaz A, Semenov E, Spolverato G, et al. Synchronous primary colorectal and liver metastasis: impact of operative approach on clinical outcomes and hospital charges. HPB (Oxford) 2014;16 : 1117–26. doi:10.1111/hpb.12302.
5. van der Pool AE, de Wilt JH, Lalmahomed ZS, et al. Optimizing the outcome of surgery in patients with rectal cancer and synchronous liver metastases. Br J Surg. 2010;97 : 383–90. doi:10.1002/bjs.6947.
6. MERCURY Study Group. Diagnostic accuracy of preoperative magnetic resonance imaging in predicting curative resection of rectal cancer: prospective observational study. BMJ 2006;333 : 779. doi:10.1136/bmj.38937.646400.55.
7. Burdan F, Sudol-Szopinska I, Staroslawska E, et al. Magnetic resonance imaging and endorectal ultrasound for diagnosis of rectal lesions. Eur J Med Res. 2015;20 : 4. doi:10.1186/s40001-014-0078-0.
8. Glynne-Jones R, Wyrwicz L, Tiret E, et al. Rectal cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2018;29:iv263. doi:10.1093/annonc/mdy161.
9. Balyasnikova S, Brown G. Optimal imaging strategies for rectal cancer staging and ongoing management. Curr Treat Options Oncol. 2016;17 : 32. doi:10.1007/s11864-016-0403-7.
10. Huebner RH, Park KC, Shepherd JE, et al. A meta-analysis of the literature for whole-body FDG PET detection of recurrent colorectal cancer. J Nucl Med. 2000;41 : 1177–89.
11. Nicholson BD, Shinkins B, Pathiraja I, et al. Blood CEA levels for detecting recurrent colorectal cancer. Cochrane Database Syst Rev. 2015. doi:10.1002/14651858.CD011134.pub2.
12. Lehmann K, Rickenbacher A, Weber A, et al. Chemotherapy before liver resection of colorectal metastases: friend or foe? Ann Surg. 2012;255 : 237–47. doi:10.1097/SLA.0b013e3182356236.
13. Vandeweyer D, Neo EL, Chen JW, et al. Influence of resection margin on survival in hepatic resections for colorectal liver metastases. HPB (Oxford) 2009;11 : 499. doi:10.1111/j.1477-2574.2009.00092.x
14. Are C, Gonen M, Zazzali K, et al. The impact of margins on outcome after hepatic resection for colorectal metastasis. Ann Surg. 2007;246 : 295–300. doi:10.1097/SLA.0b013e31811ea962.
15. Belghiti J, Ogata S. Assessment of hepatic reserve for the indication of hepatic resection. J Hepatobiliary Pancreat Surg. 2005;12 : 1–3. doi:10.1007/s00534-004-0951-2.
16. Lambert LA, Colacchio TA, Barth RJ. Interval hepatic resection of colorectal metastases improves patient selection. Arch Surg. 2000;135 : 473–9; discussion 479−80.
17. Clancy C, O’Leary DP, Burke JP, et al. A meta-analysis to determine the oncological implications of conversion in laparoscopic colorectal cancer surgery. Colorectal Dis. 2015;17 : 482–90. doi:10.1111/codi.12875.
18. Montedori A, Cirocchi R, Farinella E, et al. Covering ileo - or colostomy in anterior resection for rectal carcinoma. Cochrane Database Syst Rev. 2010. doi:10.1002/14651858.CD006878.pub2
19. Meleagros L, Varty PP, Delrio P, et al. Influence of temporary faecal diversion on long-term survival after curative surgery for colorectal cancer. Br J Surg. 1995;82 : 21–5. doi:10.1002/bjs.1800820108
20. Vogt P, Raab R, Ringe B, et al. Resection of synchronous liver metastases from colorectal cancer. World J Surg. 1991;15 : 62–7.
21. Thelen A, Jonas S, Benckert C, et al. Simultaneous versus staged liver resection of synchronous liver metastases from colorectal cancer. Int J Colorectal Dis. 2007;22 : 1269–76. doi:10.1007/s00384-007-0286-.y.
22. Reddy SK, Pawlik TM, Zorzi D, et al. Simultaneous resections of colorectal cancer and synchronous liver metastases: a multi-institutional analysis. Ann Surg Oncol. 2007;14 : 3481–91. doi:10.1245/s10434-007-9522-5.
23. Nakajima K, Takahashi S, Saito N, et al. Predictive factors for anastomotic leakage after simultaneous resection of synchronous colorectal liver metastasis. J Gastrointest Surg. 2012;16 : 821–7. doi:10.1007/s11605-011-1782-5.
24. van der Poel MJ, Tanis PJ, Marsman HA, et al. Laparoscopic combined resection of liver metastases and colorectal cancer: a multicenter, case-matched study using propensity scores. Surg Endosc. 2019;33 : 1124–30. doi:10.1007/s00464-018-6371-1.
25. Ali SM, Pawlik TM, Rodriguez-Bigas MA, et al. Timing of surgical resection for curative colorectal cancer with liver metastasis. Ann Surg Oncol. 2018;25 : 32–7. doi:10.1245/s10434-016-5745-7.
26. Silberhumer GR, Paty PB, Temple LK, et al. Simultaneous resection for rectal cancer with synchronous liver metastasis is a safe procedure. Am J Surg. 2015;209 : 935–42. doi:10.1016/j.amjsurg.2014.09.024
27. Gavriilidis P, Sutcliffe RP, Hodson J, et al. Simultaneous versus delayed hepatectomy for synchronous colorectal liver metastases: a systematic review and meta-analysis. HPB (Oxford) 2018;20 : 11–9. doi:10.1016/j.hpb.2017.08.008.
28. Abelson JS, Michelassi F, Sun T, et al. Simultaneous resection for synchronous colorectal liver metastasis: The new standard of care? J Gastrointest Surg. 2017;21 : 975–82. doi:10.1007/s11605-017-3422-1.
29. Viganò L, Karoui M, Ferrero A, et al. Locally advanced mid/low rectal cancer with synchronous liver metastases. World J Surg. 2011;35 : 2788–95. doi:10.1007/s00268-011-1272-7.
30. Sabbagh C, Cosse C, Ravololoniaina T, et al. Oncological strategies for middle and low rectal cancer with synchronous liver metastases. Int J Surg. 2015;23 : 186–93. doi:10.1016/j.ijsu.2015.08.034.
31. Alexandrescu S, Diaconescu A, Ionel Z, et al. Comparative analysis between simultaneous resection and staged resection for synchronous colorectal liver metastases – a single center experience on 300 consecutive patients. Chirurgia (Bucur) 2017;112 : 278–88. doi:10.21614/chirurgia.112.3.278.
32. Muangkaew P, Cho JY, Han H-S, et al. Outcomes of simultaneous major liver resection and colorectal surgery for colorectal liver metastases. J Gastrointest Surg. 2016;20 : 554–63. doi:10.1007/s11605-015-2979-9.
33. Abitabile P, Hartl U, Lange J, et al. Radiofrequency ablation permits an effective treatment for colorectal liver metastasis. Eur J Surg Oncol. 2007;33 : 67–71. doi:10.1016/j.ejso.2006.10.040.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek Odcházení
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2019 Číslo 10- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Stillova choroba: vzácné a závažné systémové onemocnění
- Hojení análních fisur urychlí čípky a gel
-
Všechny články tohoto čísla
- Jaterní chirurgie 21. století
- Cesta k novým játrům: Decelularizace prasečích jater a jejich znovuosídlení buňkami
- Synchronní, do jater metastazující karcinom rekta a možnosti simultánní resekce
- Radiofrekvenční ablace jaterních metastáz kolorektálního karcinomu
- Léčba jaterních cyst – zkušenosti Chirurgické kliniky FN Plzeň 2009−2018
- Srovnání efektivity chirurgické intervence s terapií Cyberknife® v léčbě jaterních malignit
- Multidisciplinární tým v léčbě kolorektálního karcinomu – analýza vlastní sestavy nemocných za rok 2017
- Endovaskulárna liečba trombózy aorto-hepatického bypassu po transplantácii pečene
- Zemřel primář Otomar Rychnovský
- Odcházení
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Léčba jaterních cyst – zkušenosti Chirurgické kliniky FN Plzeň 2009−2018
- Srovnání efektivity chirurgické intervence s terapií Cyberknife® v léčbě jaterních malignit
- Radiofrekvenční ablace jaterních metastáz kolorektálního karcinomu
- Cesta k novým játrům: Decelularizace prasečích jater a jejich znovuosídlení buňkami
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



