-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Problematika diagnostiky nealkoholovej steatohepatitídy v klinicko-patologickej praxi
Diagnostic problems of non-alcoholic steatohepatitis in clinicopathological practice
Non-alcoholic fatty liver disease (NAFLD) has recently become one of the most frequent and most important hepatic disorders throughout the world. This complex clinicopathological condition includes a spectrum of several nosological entities with distinct prognosis. The mildest form is a simple steatosis that can progress to steatohepatitis, steatofibrosis and can ultimately lead to cirrhosis or hepatocellular carcinoma. Although simple fatty liver is a relatively benign condition, non-alcoholic steatohepatitis (NASH) is much more dangerous and may have a very poor or unpredictable outcome. Furthermore, NAFLD is commonly without clinical manifestation and often discovered through incidentally elevated hepatic enzyme levels. Because it is an exclusion diagnosis, establishing of NASH can be difficult in clinical practice. It depends in great part on the veracity of the patient and his statement denying significant alcohol consumption. Liver biopsy is considered to be a “gold standard” diagnostic process, because it is of unquestioned value in determining the presence of steatosis or steatohepatitis. Fatty changes in liver parenchyma can be also detected by noninvasive imaging methods, however, microscopical examination is the only relatively reliable one to assess the morphological severity of this disease, and thus estimate a further prognosis. None of the clinical examinations has sufficient sensitivity and specificity for histological grading and staging of NAFLD, and cannot distinguish between simple steatosis and NASH with or without fibrosis. In addition to establishing the severity, histology permits the monitoring of disease progression and the response to therapy, as aminotransaminase levels may decrease during the course of the disease regardless of whether fibrosis progresses or improves. Finally, further studies on the pathogenesis of NASH may improve our understanding of the mechanisms involved in NAFLD progression, but may also lead to potentially novel therapeutic strategies to treat this frequent condition.
Key words:
non-alcoholic fatty liver disease, non-alcoholic steatohepatitis.
Autoři: V. Bartoš 1; P. Slávik 2; D. Krkoška 3
Působiště autorů: Ústav histológie a embryológie JLF UK v Martine Vedúci: doc. MUDr. Adamkov M. CSc. ; Ústav patologickej anatómie JLF UK a MFN v Martine Vedúci: prof. MUDr. Plank L. CSc. 2; Klinika infektológie a cestovnej medicíny JLF UK a MFN v Martine Vedúci: prof. MUDr. Szilágyiová M. CSc. 3
Vyšlo v časopise: Prakt. Lék. 2008; 88(1): 14-17
Kategorie: Přehledy
Souhrn
Nealkoholová tuková choroba pečene (NAFLD) je v súčasnosti celosvetovo jedna z najčastejších a najvýznamnejších chorôb pečene. Tento komplexný klinicko-patologický stav zahrňuje spektrum niekoľkých nozologických jednotiek s rozdielnou prognózou. Najľahšia forma je jednoduchá steatóza, ktorá môže progredovať do steatohepatitídy, steatofibrózy a nakoniec prechádzať do cirhózy, prípadne až hepatocelulárneho karcinómu. Hoci jednoduché stukovatenie pečene predstavuje relatívne benígny stav, nealkoholová steatohepatitída (NASH) je omnoho závažnejšia s potenciálne nepriaznivým a nepredvídateľným priebehom. Navyše je NAFLD väčšinou klinicky asymptomatická a mnohokrát diagnostikovaná iba na základe náhodne zistených zvýšených hodnôt hepatálnych enzýmov. V dôsledku prevažne vylučovacej diagnostiky môže byť potvrdenie NASH v klinickej praxi veľmi obtiažne. Vo veľkej miere závisí od pravdivosti výpovede pacienta o množstve denne konzumovaného alkoholu. Biopsia pečene je považovaná za „zlatý štandard“ v diagnostickom procese, pretože má dominujúcu úlohu pri dôkaze steatózy alebo steatohepatitídy. Tukové zmeny v pečeňovom parenchýme môžu byť detegované aj neinvazívnymi zobrazovacími metodikami, ale mikroskopické vyšetrenie ako jediné dokáže pomerne spoľahlivo určiť morfologický stupeň ochorenia a tak predpovedať ďalšiu prognózu. Žiadne z klinických vyšetrení nemá postačujúcu senzitivitu ani špecificitu na určovanie histologického gradingu a stagingu NAFLD, ani nedokáže rozlíšiť jednoduchú steatózu od NASH s/alebo bez fibrózy. Okrem hodnotenia závažnosti choroby umožňuje histologické vyšetrenie monitorovať jej pokročilosť a odpoveď na terapiu, pretože hodnoty aminotransferáz môžu klesať v priebehu ochorenia bez ohľadu na to, či sa fibróza stupňuje, alebo naopak ustupuje. Ďalšie štúdie patogenézy NASH môžu zlepšiť naše vedomosti o mechanizmoch zahrnutých v progresii NAFLD a prípadne aj viesť k zavádzaniu nových terapeutických stratégií pri liečbe tohto častého ochorenia.
Kľúčové slová:
nealkoholová tuková choroba pečene, nealkoholová steatohepatitída.Úvod
Nealkoholová tuková choroba pečene (NAFLD – Non Alcoholic Fatty Liver Disease) predstavuje v dnešnej lekárskej praxi pomerne závažnú interdisciplinárnu problematiku. V porovnaní s minulosťou sa na ňu v súčasnosti nazerá z úplne nového pohľadu (14). V skutočnosti sa nejedná o striktne ohraničenú chorobnú jednotku, ale o širšie spektrum viacerých dynamicky sa rozvíjajúcich klinicko-patologických stavov. Na začiatku tohto spektra sa nachádza jednoduchá steatóza, ktorá môže prostredníctvom steatohepatitídy a steatofibrózy progredovať do konečného štádia – cirhózy pečene, prípadne až do hepatocelulárneho karcinómu (16).
Nealkoholová steatohepatitída (NASH – Non Alcoholic Steato-Hepatitis) predstavuje prognosticky najzávažnejšiu formu (4, 16). Prvýkrát bola opísaná v r. 1980 patológom Jürgenom Ludwigom a spolupracovníkmi u pacientov, u ktorých bioptické vyšetrenie pečene preukázalo histomorfologické nálezy podobné alkoholovej hepatitíde, ale bez signifikantnej konzumácie etanolu v anamnéze (7). Prevalencia NASH nie je presne známa, ale vo vyspelých krajinách sa jej výskyt uvádza v rozmedzí 2–9 % (16). V Slo-venskej republike postihuje NAFLD až 25 % obyvateľstva (16), pričom asi u 100 000 obyvateľov je ochorenie v štádiu NASH, približne u 25 000 pacientov choroba progreduje do cirhózy a takmer 10 000 ľudí umrie v dôsledku zlyhania pečene alebo hepatocelulárneho karcinómu (4).
V súčasnosti sa však stále množia údaje (10, 13) o tom, že mnoho diagnostikovaných kryptogénnych cirhóz (bez objasnenej etiológie) vlastne predstavuje tzv. “vyhorenú“ (burned-out) steatohepatitídu. U časti pacientov s nerozpoznanou a neliečenou NASH preto pravdepodobne dochádza k väzivovej prestavbe pečeňového parenchýmu aj bez klinickej symptomatológie ochorenia. Steatohepatitída preto predstavuje jedno z najväčších úskalí tak klinickej, ako aj histomorfologickej diagnostiky.
Nealkoholová steatohepatitídav bioptickom obraze
Podobne ako pri etylickom poškodení pečene, aj pri NAFLD sa histologické zmeny vyskytujú prevažne vo vnútri lalôčikov. Rozlišuje sa niekoľko charakteristických morfologických nálezov – stukovatenie, regresívne zmeny hepatocytov, intralobulárne zápalové zmeny a fibróza parenchýmu (3, 16).
Steatóza hepatocytov tvorí najčastejšiu abnormalitu a v typických prípadoch býva makrovakuolárna, len zriedkavejšie mikrovakuolárna. Závažnosť tukových zmien sa bežne hodnotí percentuálnym zastúpením hepatocytov obsahujúcich lipidy. Hoci veľmi mierny stupeň stukovatenia (cca do 5 %) ešte nemusí predstavovať skutočnú patologickú abnormalitu (3), v závere histologického vyšetrenia by sa mal dokumentovať akýkoľvek rozsah steatózy v pečeni. V bežnom farbení hematoxylínom a eozínom sa tuk javí ako opticky prázdne priestory v cytoplazme pečeňových buniek (obr. 1). Za účelom lepšej vizualizácie lipidov možno využiť aj špeciálne histochemické metodiky napr. farbenie sudanom, čo však z praktického hľadiska nemá v rutínnej diagnostike väčší význam.
Obr. 1. V bežnom farbení hematoxylínom a eozínom sa tuk javí ako opticky prázdne priestory v cytoplazme pečeňových buniek 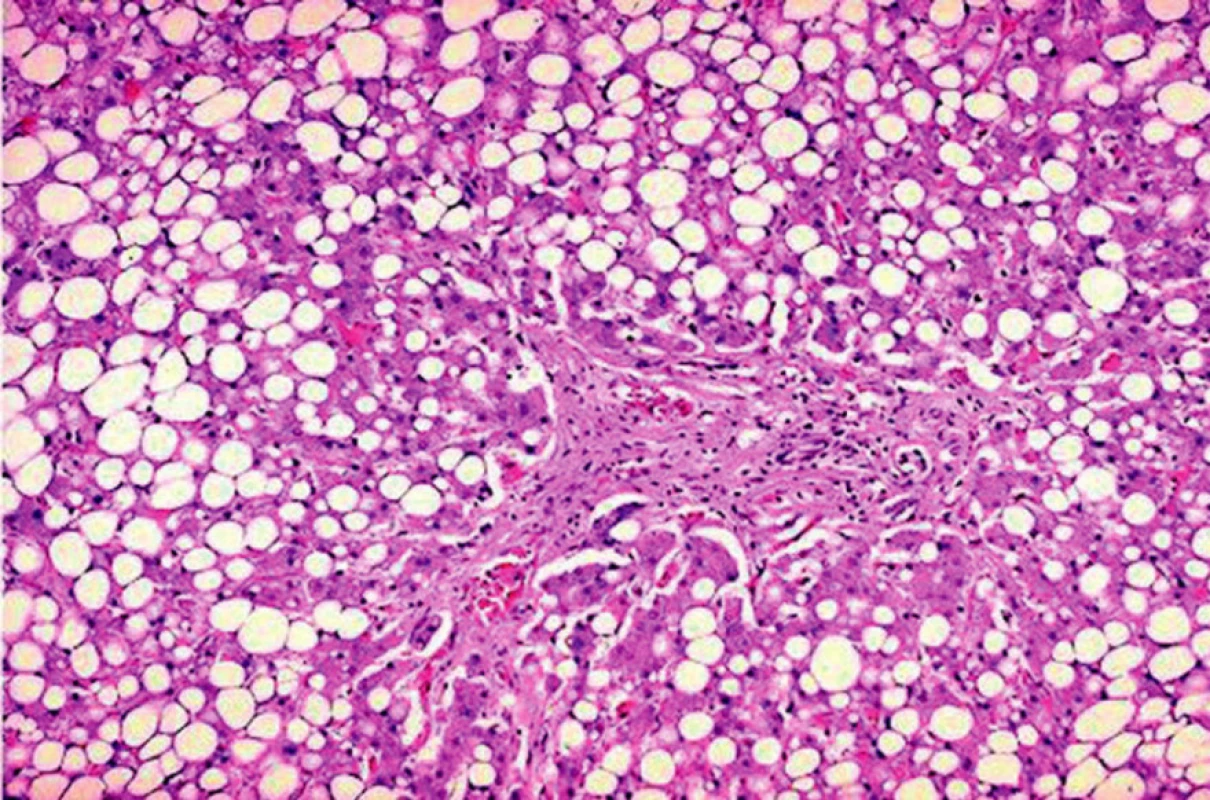
K typickým regresívnym zmenám parenchýmu patrí najmä hydropická dystrofia („balónovanie“) hepatocytov, ktorá je niekde považovaná za rozhodujúci nález z hľadiska histologickej diagnostiky NASH (3). V cytoplazme pečeňových buniek sa môžu vyskytovať hyalínové inklúzie charakteru Malloryho teliesok, ktoré sú však v porovnaní s alkoholovou hepatitídou menej výrazné. Len sporadicky možno pozorovať aj prítomnosť megamitochondrií alebo depozitov železa. Relatívne častým nálezom môžu byť aj ložiskové nekrózy či apoptotické zmeny hepatocytov.
Zápalová infiltrácia môže byť len minimálna, ale je podmienkou pre diagnózu NASH (16). Celulizácia býva väčšinou zmiešaná a pozostáva najmä z neutrofilov, menej T lymfocytov, aktivovaných makrofágov a Kupfferových buniek.
Intralobulárne sa pomerne často nachádza aj perisínusoidová a pericelulárna fibróza, ktorá je v typických prípadoch situovaná okolo centrálnej vény. Pozdĺž sínusových kapilár vytvára charakter jemného pletiva, v literatúre označovaného ako “chicken wire appearance”. Jej prítomnosť je prognosticky nepriaznivým ukazovateľom, pretože môže byť znakom budúceho vývoja ochorenia do pečeňovej cirhózy (16).
Portálne, respektive periportálne zmeny môžu byť relatívne často prítomné, ale typické bývajú skôr pre detskú populáciu (12). Reprezentované sú chronickou zápalovou infiltráciou a fibrózou v portobiliárnych priestoroch, nálezom “interface” hepatitídy, prípadne abnormalitami interlobulárnych žlčovodou.
Komplex uvedených mikroskopických nálezov je zahrnutý v recentne najviac používanom histologickom skórovacom systéme navrhnutom Kleinerom a spol. (5), ktorý numericky vyhodnocuje tieto samostatné parametre:
a) steatózu,
b) lobulárny zápal, a
c) hydropickú dystrofiu hepatocytov.
Pri klasifikovaní rozsahu stukovatenia využíva nasledovné “cut-off” hodnoty:
0 bodov (< 5 %),
1 bod (5–33 %),
2 body (33–66 %), a
3 body (> 66 %).
Intenzita intralobulárnej zápalovej infiltrácie je hodnota počtom ložísk tvorených zoskupením zápalových bunkových elementov v 1 zornom poli mikroskopu pri 200x zväčšení:
0 bodov (žiadne),
1 bod (< 2 prítomné ložiská),
2 body (2–4 prítomné ložiská), a
3 body (> 4 prítomné ložiská).
Podobne vyhodnocuje aj rozsah hydropických zmien pečeňových buniek:
0 bodov (žiadne),
1 bod (prítomných niekoľko „balónovaných“ hepatocytov),
2 body (prítomný veľký počet „balónovaných“ hepatocytov, respektive masívne hydropické zmeny).
Celková získaná hodnota – NAS (NAFLD Activity Score) varíruje od 0 do 8 bodov a na základe nej sa možno pomerne spoľahlivo vyjadriť k nálezu steatohepatitídy:
0 – 2 body → NASH neprítomná,
3–4 body → NASH neistá,
5–8 bodov → NASH pravdepodobná alebo istá.
Osobitný a taktiež veľmi významný parameter predstavuje rozsah perisínusoidovej aj periportálnej fibrózy (štádium 1 až 4).
V rámci diferenciálnej diagnostiky je však dôležité, že podobné mikroskopické nálezy sa vyskytujú aj pri iných chorobách sprevádzaných symptomatickým stukovatením pečene. U každého pacienta s predpokladanou steatózou alebo NASH sa preto musia vylúčiť aj iné príčiny ochorenia pečene, napr. vírusová genéza, autoimunitné poruchy, rôzne metabolicky podmienené stavy, účinky liekov či iných xenobiotík a rôznych faktorov vonkajšieho prostredia (16).
Nealkoholová steatohepatitída v klinicko-morfologických koreláciách
V rutínnej klinicko-patologickej praxi sa možno stretnúť s viacerými problematickými oblasťami, ktoré výrazne sťažujú diagnostiku tejto chorobnej jednotky. Základnou otázkou mnohokrát ostáva samotné rozlíšenie alkoholového od nealkoholového poškodenia pečene. Obidva typy ochorení majú takmer identický histologický obraz a konečná diagnóza môže byť urobená iba na základe spolupráce patológa s klinickými lekármi (3). Za všeobecne akceptované kritérium NAFLD sa považuje “pozitívny” morfologický nález u pacienta s maxi-málnym denným príjmom etanolu 20 g u žien a 40 g u mužov (9). Presné stanovenie či odhad množstva pravidelne konzumovaného alkoholu u chorého však nie je v lekárskej praxi väčšinou možné.
Hoci možno tukové zmeny v pečeni pomerne spoľahlivo diagnostikovať aj neinvazívnymi vyšetrovacími metodikami (počítačová tomografia, magnetická rezonancia, ultrasonografia), odlíšenie jednoduchej steatózy od steatohepatitídy, prípadne sprievodných fibrotických zmien môže poskytnúť iba histomorfologické vyšetrenie tkaniva (11, 16). Ani v súčasnej dobe nie sú k dispozícii jednoznačné laboratórne biochemické kritériá, pomocou ktorých by sa dala exaktne stanoviť diagnóza NASH. Príznaky ochorenia bývajú iba nevýrazné a nešpecifické, napr. únava, slabosť, tupá bolesť v pravom podrebrí alebo dyspeptické ťažkosti.
Zvýšená aktivita aminotransferáz je najčastejším patologickým nálezom, ktorý v prípade prítomných rizikových faktorov (mužský typ obezity, diabetes mellitus 2 typu, dyslipoproteinémia) nútia klinika myslieť na túto chorobu. Vyšetrením aktivity enzýmov však nemôžeme rozlíšiť jednoduché stukovatenie od NASH, pretože neexistuje jednoznačná korelácia medzi medzi klinickým, laboratórnym a histologickým nálezom (4, 16). Z toho dôvodu by bolo ideálne uskutočniť biopsiu u všetkých ľudí s podozrením na tukové zmeny v pečeni, najmä v prípadoch výraznejšej obezity.
Rozlíšenie jednoduchej steatózy od steatohepatitídy však môže byť náročné aj pri bioptickom vyšetrení, čo má vzhľadom na rozdielnu prognózu týchto 2 chorobných jednotiek veľký význam. V patológii preto zohráva dôležitú úlohu štandardizácia univerzálne akceptovaných minimálnych kritérií na stanovenie diagnózy NASH. V súčasnosti je zaužívaných niekoľko semikvantitatívnych histologických skórovacích systémov (1, 5, 9), ktoré rozlišujú grading (histologickú aktivitu) a staging (štádium fibrózy) choroby. Problémom pri všetkých uvedených histomorfologických systémoch však býva pomerne slabá reproducibilita a variabilita výsledkov. V rôznych komparatívnych štúdiách sa všeobecne preukázala najväčšia zhoda pri hodnotení stupňa steatózy, menšia pri rozsahu hydropickej dystrofie hepatocytov a najmenšia pri intenzite intralobulárnej zápalovej infiltrácie (5, 15).
Najvýraznejšia variabilita posledného parametra pravdepodobne súvisí s náročnosťou presného sčítania zápalových elementov v jednotlivých zorných poliach mikroskopu. Taktiež môže byť obtiažne rozlíšiť mierne hydropické zmeny hepatocytov od arteficiálnych zmien spôsobených pri spracovávaní vzorky. Nepresnosti pri hodnotení vznikajú často aj v dôsledku malého objemu získaného bioptického materiálu.
Výskyt NAFLD má v dôsledku stúpajúcej obezity detí a adolescentov rastúcu tendenciu aj v pediatrickej populácii (6). V praxi je dôležité, že u detí nemusí byť nález steatohepatitídy reprezentovaný histomorfologickými črtami typickými pre dospelú populáciu. U detí sa rozoznávajú 2 rozdielne formy NASH (12). Zriedkavejší 1. typ (17 %) je sprevádzaný steatózou, hydropickou degeneráciou pečeňových buniek a perisínusoidovou fibrózou – zmenami podobnými ako v dospelej populácii.
Častejší 2. typ (51 %) je charakteristický stukovatením a prítomným portálnym zápalom a periportálnou fibrózou. Približne v 16 % ide o prekrývanie sa obidvoch typov a v 16 % o jednoduchú steatózu.
Z hľadiska diferenciálnej diagnostiky je dôležité, že stukovatenie býva často sprevádzané rôznymi inými patomorfologickými nálezmi. Najmä u detí preto vyžaduje diagnóza NAFLD vylúčenie vrodených či metabolických príčin stukovatenia pečene (8), čo je v praxi mnohokrát bez biochemického rozboru vzorky veľmi obtiažne. Bez ohľadu na vek chorých býva ďalším diagnostickým problémom potenciálna koexistencia NAFLD s inými chronickými chorobami pečene. Pomerne často sa vyskytuje v kombinácii s chronickou hepatitídou C a B (2). V takýchto prípadoch je diskutabilné, do akej miery je hodnotenie histologických zápalových parametrov relevantné k jednej či druhej chorobnej jednotke. Bioptické vyšetrenie sa však ako jediné dokáže aspoň čiastočne vyjadriť k morfologicky predominujúcemu ochoreniu. Podobne môže sťažovať diagnostiku aj rozlíšenie nálezu nešpecifickej reaktívnej hepatitídy, ktorá bežne vzniká ako sekundárna reakcia na rôzne systémové ochorenia.
Záver
Hoci sa v minulosti považovalo stukovatenie pečene za pomerne nezávažný chorobný stav, v dnešnej dobe sa mu venuje mimoriadna pozornosť. Vzhľadom na nevýraznú symptomatológiu je v klinickej praxi potrebné myslieť na toto ochorenie pri prejavoch pečeňového poškodenia najmä v asociácii s obezitou a ostatnými rizikovými faktormi. V súčasnosti stále rastie potreba rozsiahlejších klinicko-patologických štúdií, ktoré by mohli poskytnúť dôležité informácie o prirodzenom priebehu NAFLD.
Nevyhnutné je aj objasnenie významu genetickej predispozície ovplyvňujúcej rozvoj ochorenia a jeho progresiu do závažnejších štádií pečeňového poškodenia. Len u malej časti rizikových pacientov totiž dochádza k rozvoju pokročilejších štádií, čo je pravdepodobne podmienené endogénne. Otázkou preto zostáva, ako by sa dalo predchádzať progresii jednoduchej steatózy do steatohepatitídy a tak zlepšiť prevenciu tohto častého ochorenia.
Táto práca bola podporená grantom UK/270/2006.
Poďakovanie
Ďakujeme všetkým lekárom a technickým pracovníkom, ktorí sa podieľali na diagnostickom procese prípadov súvisiacich s riešením uvedenej grantovej úlohy.
MUDr. Vladimír Bartoš
ul. P. Mudroňa 30/16
036 01 Martin
Slovenská republika
E-mail: vladimirbartos@post.sk, bartos@jfmed.uniba.sk
Zdroje
1. Brunt, E.M., Janney, C.G., Di Bisceglie, A.M. et al. Nonalcoholic steatohepatitis: a proposal for grading and staging the histological lesions. Am. J. Gastroenterol. 1999, 94, p. 2467-2474.
2. Gordon, A., McLean, C.A., Pedersen, J.S. et al. Hepatic steatosis in chronic hepatitis B and C: predictors, distribution and effect on fibrosis. J. Hepatol. 2005, 43, p. 38-44.
3. Hübscher, G.S. Histological assessment of non-alcoholic fatty liver disease. Histopathology 2006, 49, p. 450-465.
4. Jarčušková, M., Pobeha, J. Nealkoholová steatóza pečene a metabolický syndróm. Slovenský lekár 2006, 1-2, 16, (30), s. 4-6.
5. Kleiner, D.E., Brunt, E.M., Van Natta, M. et al. Design and validation of a histological scoring system for nonalcoholic fatty liver disease. Hepatology 2005, 41, p. 1313-1321.
6. Kuchta, M., Nováková, B., Gombošová, K., Petrášová, M. Steatóza a obezita detí a dospievajúcich. Pediatria 2007, 2 (1), s. 18-22.
7. Ludwig, J., Viggiano, T.R., McGill, D.B. et al. Nonalcoholic steatohepatitis. Mayo Clinic experiences with a hitherto unnamed disease. Mayo Clin. Proc. 1980, 55, p. 434-438.
8. Marion, A.W., Baker, A.J., Dhawan, A. Fatty liver disease in children. Arch. Dis. Child 2004, 89, p. 648-652.
9. Mendler, M.H. Kanel, G., Govindarajan, S. Proposal for a histological scoring and grading system for non-alcoholic fatty liver disease. Liver Int. 2005, 25, p. 294-304.
10. Poonawala, A.Q., Nair, A.P., Thuuluvath, P.J. Prevalence of obesity and diabetes in patients with cryptogenic cirrhosis. A case-control study. Hepatology 2000,; 32, p. 689-692.
11. Saadeh, S., Younossi, Z.M., Remer, E.M. et al. The utility of radiological imaging in nonalcoholic fatty liver disease. Gastroenterology 2002, 123 (3), p. 745-750.
12. Schwimmer, J.B., Behling, C., Newbury, R. et al. Histopathology of pediatric nonalcoholic fatty liver disease. Hepatology 2005, 42, p. 641-649.
13. Struben, V.M., Hespenheide, E.E., Caldwell, S.H. Nonalcoholic steatohepatitsi and cryptogenic cirrhosis within kindreds. Am. J. Med. 2000, 108 (1), p. 9-13.
14. Šochman, J. Nemoc tučných jater a statiny – kterému oboru patří tento problém? Čas. lék. čes. 2006, 145, s. 443-446.
15. Younossi, Z.M., Gramlich, T., Liu, Y.C. et al. Nonalcoholic fatty liver disease: assessment of variability in pathologic interpretations. Mod. Pathol. 1998, 11, p. 560-565.
16. Zima, M. Nealkoholová steatohepatitída. Gastroenterol. prax. 2006,; 5 (1), p. 7-13.
Štítky
Adiktologie Alergologie a imunologie Anesteziologie a resuscitace Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská dermatologie Dětská gastroenterologie Dětská gynekologie Dětská chirurgie Dětská kardiologie Dětská neurologie Dětská onkologie Dětská otorinolaryngologie Dětská pneumologie Dětská psychiatrie Dětská radiologie Dětská urologie Diabetologie Endokrinologie Farmacie Farmakologie Fyzioterapie Gastroenterologie a hepatologie Genetika Geriatrie a gerontologie Gynekologie a porodnictví Hematologie a transfuzní lékařství Hygiena a epidemiologie Hyperbarická medicína Chirurgie cévní Chirurgie hrudní Chirurgie plastická Infekční lékařství Intenzivní medicína Kardiochirurgie Logopedie Mikrobiologie Nefrologie Neonatologie Neurochirurgie Neurologie Nukleární medicína Nutriční terapeut Obezitologie Oftalmologie Ortodoncie Ortopedie Otorinolaryngologie Patologie Pediatrie Pneumologie a ftizeologie Popáleninová medicína Pracovní lékařství Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé Protetika Psychologie Radiodiagnostika Radioterapie Rehabilitační a fyzikální medicína Reprodukční medicína Sestra Sexuologie Soudní lékařství Stomatologie Tělovýchovné lékařství Toxikologie Urgentní medicína Urologie Laboratoř Domácí péče Foniatrie Zdravotnictví Dentální hygienistka Student medicíny
Článek RecenzeČlánek Konsiliární psychiatrie
Článek vyšel v časopisePraktický lékař
Nejčtenější tento týden
2008 Číslo 1- Psilocybin je v Česku od 1. ledna 2026 schválený. Co to znamená v praxi?
- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
-
Všechny články tohoto čísla
- Problematika diagnostiky nealkoholovej steatohepatitídy v klinicko-patologickej praxi
- Vztah klinického obrazu a neurobiologie vaskulárních demencí
- Vliv kouření a volných radikálů na antioxidační ochranu a na patogenezi některých nemocí
- Etické komise v České republice
- Importované tropické horečnaté infekce
- Záchranná léčba kombinací paclitaxel + gemcitabine pacientů s germinálními nádory (GCT – germ cell tumors)
- Kauzální metody léčby varixů dolních končetin
- Recenze
- Úloha praktického lékaře a odborníka pro nemoci z povolání při diagnostice profesního bronchiálního astmatu a profesní rinitidy
- Linka pro odvykání kouření – významná součást nabídky léčby závislosti na tabáku
- Dynamika onkomarkerů v rámci onkologické léčby testikulárních germinálních nádorů
- Psychotrauma a jeho problématika při poskytování zdravotní péče
- Miniportréty slavných českých lékařů Profesor MUDr. Ladislav Borovanský – představitel české anatomie v poválečné době
- Projekt CRAB, aneb Časnou diagnostikou k lepší kvalitě života
- Vyšetřování kůže vysokofrekvenčním ultrazvukem
- Mamma HELP a „umění žít naplno!“
- Projekt „Regionální centrum pro podporu výuky a výzkumu v oblasti medicínských obrazových a klinických dat
- Od základní péče po špičkovou specializaci
- Konsiliární psychiatrie
- Praktický lékař
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Vztah klinického obrazu a neurobiologie vaskulárních demencí
- Kauzální metody léčby varixů dolních končetin
- Dynamika onkomarkerů v rámci onkologické léčby testikulárních germinálních nádorů
- Vliv kouření a volných radikálů na antioxidační ochranu a na patogenezi některých nemocí
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



