-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Extraezofageální reflux up-to-date
Extraesophageal reflux up-to-date
Extraesophageal symptoms of gastroesophageal reflux disease (posterior laryngitis, vocal fold granuloma, globus pharyngeus, subglotis and tracheal stenosis, laryngopharyngeal carcinoma, poorly controlled asthma bronchiale, paroxysmal cough and others) have been studied more since the 1990‘s. It was long believed that extraesophageal reflux causes mucosal damage of the hypopharynx and larynx in the same way as gastroesophageal reflux in the oesophagus. However, this premise did not work in practice (only a few extraesophageal reflux episodes have been proven during pH-metry, poor correlation between symptoms and findings, limited effect of proton pump inhibitors) and this led to scepticism regarding the role of extraesophageal reflux in the pathogenesis of the diseases mentioned above. But research in the last few years has revealed much new information about the pathogenesis of extraesophageal reflux and has completely changed our understanding of this controversial issue. Acidity alone is no longer considered to be the main pathogenetic agent during extraesophageal reflux episodes, while pepsin, which maintains its stability and activity also in weakly acid refluxes, is considered to play an essential role. Furthermore, it has been revealed that mucosa of the hypopharynx, larynx and other parts of the airways is much more sensitive to refluxate than esophageal mucosa. Therefore, treatment is focused not only on cutting down the acidity, but also on reducing reflux episodes and minimizing the negative pepsin effect.
Key words:
extraesophageal reflux – esophageal impedance – weakly acid reflux – oropharyngeal pH-monitoring – pepsin
Autoři: Karol Zeleník 1
; P. Schwarz 1; O. Urban 2,3; J. Vydrová 4; Pavel Komínek 1
Působiště autorů: Otorinolaryngologická klinika FN Ostrava, 2Interní klinika FN Ostrava, 3Centrum péče o zažívací trakt, Vítkovická nemocnice a. s., Ostrava, 4Hlasové centrum Praha 1
Vyšlo v časopise: Gastroent Hepatol 2010; 64(6): 10-14
Kategorie: IBD: Aktuální přehled
Souhrn
Mimojícnové projevy refluxní choroby jícnu (zadní laryngitida, granulomy hlasivek, globus pharyngeus, těžce ovlivnitelné astma bronchiale, záchvatovitý kašel a další) jsou více zkoumány od devadesátých let 20. století. Dlouho existovala představa, že mechanizmus působení extraezofageálních refluxních epizod na sliznice hypofaryngu a horních cest dýchacích je stejný jako u působení refluxátu na sliznici jícnu. V praxi se však tento předpoklad neprokázal (pH-metrií zjištěno jen málo kyselých extraezofageálních refluxních epizod, malá korelace mezi nálezy a symptomy, slabá odpověď na inhibitory protonové pumpy), což vedlo ke skepticizmu ohledně úlohy extraezofageálního refluxu v patogenezi výše zmíněných nemocí. Až výzkum poslední let objasnil mnohé nové skutečnosti a zcela změnil pohled na extraezofageální reflux. Samotná „kyselost“ již není považována za nejdůležitější patogenetický faktor působící v průběhu extraezofageálních refluxních epizod a podstatnou úlohu hraje pepsin, který si zachovává svou stabilitu a aktivitu i v průběhu slabě kyselých refluxů, jejichž význam tak stoupá. Kromě toho bylo zjištěno, že sliznice hypofaryngu, hrtanu a dalších částí dýchacích cest je mnohem citlivější na složky refluxátu v porovnání se sliznicí jícnu. Z těchto důvodů se léčba zaměřuje nejenom na potlačení kyselosti, ale také na snížení počtu refluxních epizod a snížení negativního působení pepsinu.
Klíčová slova:
extraezofageální reflux – impedance jícnu – mírně kyselý reflux – orofaryngeální měření pH – pepsinÚvod
Extraezofageální reflux (EER) je stav, při kterém dochází k průniku (duodeno)gastrického refluxátu nad úroveň horního jícnového svěrače – do hltanu a horních cest dýchacích. Pokud EER nevyvolává žádné obtíže a/nebo slizniční změny, označuje se jako fyziologický, pokud způsobuje, označuje se jako patologický. V současnosti se patologický EER považuje za jeden z faktorů, který v menší či větší míře vyvolává, udržuje nebo zhoršuje zánětlivé procesy hltanu a horních cest dýchacích. Nejčastěji je dáván do souvislosti se zadní (syn. refluxní) laryngitidou, granulomy hlasivek (obr. 1), globus faryngeus, zahleněním, častým odkašláváním, těžko ovlivnitelným astma bronchiale a záchvatovitým kašlem [1].
Obr. 1. Granulom pravé hlasivky (označený šipkou) způsobený extraezofageálním refluxem. Fig. 1. Granuloma of the right vocal chord (arrow) caused by extraesophageal reflux. 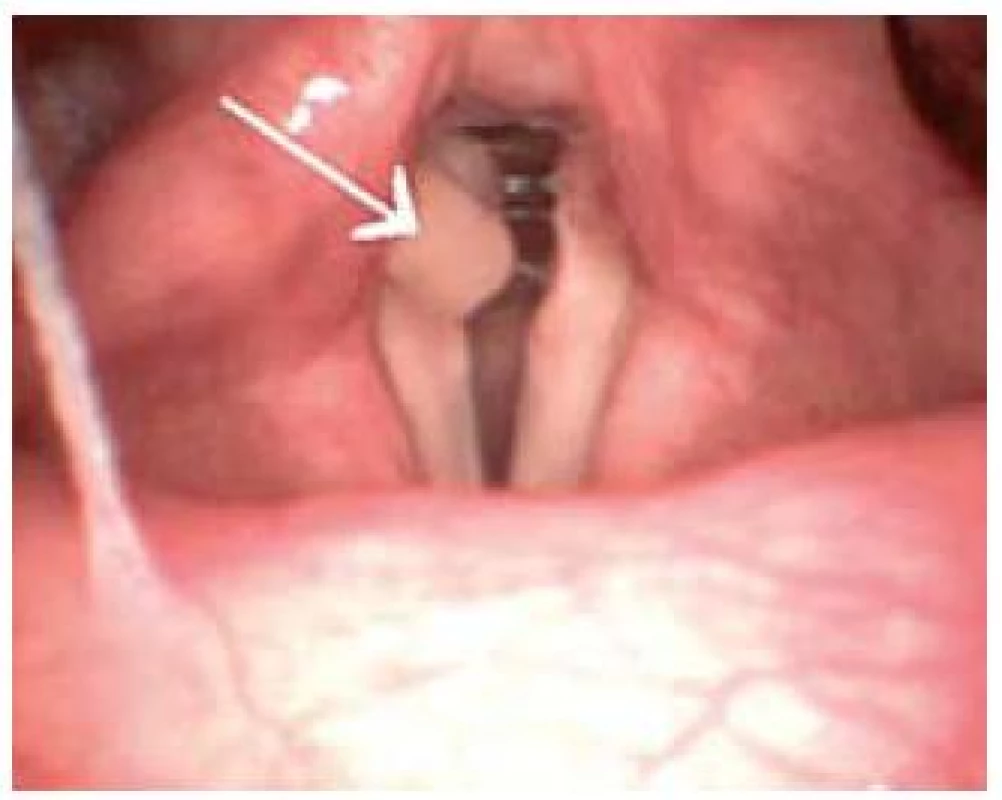
Mimojícnové projevy refluxní choroby jícnu (RCHJ) způsobené patologickým EER se začaly dostávat do popředí klinického zájmu v devadesátých letech 20. století. V té době byla popsána možná úloha EER v patogenezi mnoha nemocí hltanu, horních cest dýchacích a plic. Počáteční nadšení z toho, že byla konečně objevena „příčina skoro všech do té doby nevysvětlitelných symptomů a nemocí horních cest dýchacích a hltanu“ později vystřídal skepticizmus. Bylo to způsobeno tím, že jak otorinolaryngologové, tak gastroenterologové a pneumologové měli představu, že mechanizmus působení refluxátu na sliznice hltanu, horních cest dýchacích a plic při extraezofageální refluxní epizodě je stejný jako působení refluxátu na sliznici distálního jícnu při RCHJ. A protože se tato představa v praxi neprokázala, od konceptu škodlivosti EER mnozí upustili a na jeho úlohu v patogenezi mimojícnových projevů RCHJ přestali zcela věřit. Důvodů bylo hned několik:
- Do oblasti proximálního jícnu a nad úroveň horního jícnového svěrače se dostává jenom nepatrné množství refluxů. A i když se do oblasti proximálního jícnu nebo hypofaryngu či hrtanu reflux dostane, má většinou pH vyšší než 4,0 (hranice používaná pro definici kyselého refluxu v oblasti distálního jícnu). Proto není často pomocí pH-metrického vyšetření možné prokázat v proximálním jícnu, v oblasti horního jícnového svěrače a v hltanu kyselý reflux tak, jak je definovaný pro RCHJ.
- U patologického EER nejsou tak zřejmé slizniční změny, jako je erozivní ezofagitida u RCHJ. Změny v hrtanu jsou často nespecifické a jejich závažnost nekoreluje se závažností EER.
- Mezi extraezofageálními refluxními epizodami a symptomy není většinou přímá časová souvislost (nelze se v prokazování souvislosti opřít o symptomové skóre jako u RCHJ).
- Prospěch ze suprese žaludeční kyselosti pomocí inhibitorů protonové pumpy je u pacientů s patologickým EER menší než u pacientů s RCHJ. To bylo vykládáno tak, že reflux hraje malou nebo žádnou roli u pacientů s nemocemi hltanu, horních cest dýchacích a plic. Správná interpretace však zní: KYSELÝ reflux NEHRAJE v patogenezi zmíněných extraezofageálních nemocí HLAVNÍ roli!
Dalším faktorem, který diagnostiku a léčbu EER (stejně tak jako i RCHJ) komplikuje, je fakt, že sliznice horních cest dýchacích a polykacích je u různých pacientů rozdílně citlivá na složky refluxátu a vnímaní obtíží je u různých pacientů rozdílné (podobnost s rozdílným prahem bolesti). Z těchto důvodů se stává, že někdy minimální EER a malé změny na sliznici způsobují výrazné subjektivní obtíže a naopak někteří pacienti s výraznými změnami v hrtanu žádné problémy nemají.
Nové poznatky o extraezofageálním refluxu
Klíčovým patogenetickým faktorem jak u RCHJ, tak u patologického EER je délka a stupeň expozice jednotlivých orgánů (jícen, hrtan, hltan, trachea a další) refluxátu, což záleží na tom, do jaké míry agresivní faktory překonají obranné mechanizmy. Jak agresivní faktory, tak obranné mechanizmy jsou u RCHJ obecně známy a není cílem tohoto článku je diskutovat [2,3]. Je ale nutné připomenout, že z agresivních faktorů se v poslední době zdůrazňuje zejména negativní toxické působení kombinace kyseliny solné, pepsinu a žlučových kyselin – tzv. toxický synergizmus [2,3]. Z poruchy obranných mechanizmů je zejména důležitá hiátová hernie a spontánní relaxace dolního jícnového svěrače [2,3].
Patogeneze EER se od patogeneze RCHJ liší v mnoha ohledech, nejdůležitější nové poznatky o EER lze shrnout do několika oblastí (tab. 1):
Tab. 1. Nové poznatky o extraezofageálním refluxu (EER). Tab. 1. New knowledge about extraesophageal reflux (EER). 
1. Charakter refluxů: kyselost samotná nehraje hlavní roli v patogenezi nemocí způsobených EER. Jak kyselý reflux postupuje v jícnu proximálně, jeho kyselost se snižuje, což je způsobeno mechanizmy luminální očisty (hlen, bikarbonát, sliny). K EER epizodám tedy dochází, ale ve většině případů nemají pH nižší než 4, jsou jen slabě kyselé (pH 4,1–6,9), nebo i neutrální či dokonce zásadité [4].
2. Pepsin: je v současnosti považován za velmi důležitý patogenetický faktor působící poškození sliznic v průběhu EER epizody. Pepsin je hlavní proteolytický enzym gastrointestinálního traktu, je produkován v žaludečních mucinózních buňkách v neaktivní formě jako pepsinogen.
K aktivaci pepsinu dochází v kyselém prostředí – maximální enzymatická aktivita pepsinu je při pH 2,0 a je inaktivován při pH 6,5. Stabilní však zůstává až do pH 8,0 a v případě poklesu pH pod 6,5 může být opět reaktivován. Například při pH 7,0 a teplotě 37 °C zůstává pepsin stabilní po dobu 24 hod a po opětovné acidifikaci na pH 3,0 získává 79 % své původní aktivity [5,6]. Z výše uvedeného jasně vyplývá, že pepsin si ponechává část své aktivity i v slabě kyselém, nebo dokonce i mírně zásaditém prostředí.
Pepsin může poškodit buňky několika způsoby: zvyšuje tkáňovou permeabilitu, způsobuje buněčnou disrupci, snižuje hladinu karboanhydrázy III v buňkách (čímž omezuje produkci bikarbonátu, který zvyšuje pH) a snižuje produkci protektivních stresových proteinů Sep70 a Sep53 [7]. Kromě toho, že pepsin způsobuje poškození buněk svou proteolytickou aktivitou, bylo zjištěno, že do buněk se dostává také receptory zprostředkovanou endocytózou [4]. Z buněčných struktur pepsin nejvíce poškozuje mitochondrie a Golgiho systém [4]. Působení pepsinu na hypofaryngeální buňky vedlo i v neutrálním prostředí ke zvýšení exprese receptorů a cytokinů zánětlivé reakce (CCL20, CCL26, IL8, IL1F10 a další) [8].
3. Aerosolový reflux: pomocí nově vyvinutého vysoce citlivého zařízení Restech® byly detekovány v oblasti hltanu i tzv. „aerosolové refluxy“ [9,10]. Koncentrace škodlivin (zejména pepsinu) je v těchto aerosolových refluxech menší v porovnání s refluxem tekutého žaludečního obsahu, šíří se však jednodušeji a do mnohem vzdálenějších oblastí. Tímto konceptem „aerosolových refluxů“ lze vysvětlit přítomnost pepsinu a žlučových kyselin ve středouší, v paranazálních dutinách či ve vzorcích získaných z bronchoalveolární laváže. Koncepce aerosolových refluxů rovněž vysvětluje, proč bývá u pacientů s EER poškozená například přední komisura hlasivek a subglotická oblast, přičemž hlasivky samotné známky zánětu vykazovat nemusí (není přímý kontakt refluxátu a hlasivek) [9,10].
4. Porucha funkce horního jícnového svěrače: zatímco u pacientů s RCHJ je za nejdůležitější faktor jejího vzniku pokládána dysfunkce dolního jícnového svěrače, u pacientů s EER je to dysfunkce horního jícnového svěrače (HJS). Přesná příčina inkompetence HJS není zatím známa, zkoumají se hlavně následující faktory: relaxace HJS po podráždění sliznice proximálního jícnu refluxátem, trvalá hypotonie HJS, přechodné relaxace HJS (spontánní a vyvolané polykáním) a stres [11].
5. Zvýšená citlivost sliznic horních cest dýchacích: sliznice horních cest dýchacích je mnohem náchylnější k poškození složkami refluxátu v porovnání se sliznicí jícnu, který má poměrně sofistikované mechanizmy luminální očisty [1,12,13]. Je to podmíněno odlišným histologickým složením (dlaždicový epitel jícnu vs cylindrický řasinkový epitel hrtanu), molekulárně-biologickými vlastnostmi buněk (menší obsah a odlišná distribuce karboanhydrázy) a absencí některých obranných mechanizmů (slina, gravitace). V experimentu bylo prokázáno, že v hrtanu může i krátká doba expozice refluxátu (dokonce jenom 3 epizody za týden) způsobit její poškození [13].
6. Snížení prahu citlivosti – chronicita obtíží: poškození sliznice hypofaryngu a hrtanu vede ke snížení prahu citlivosti na škodlivé stimuly a trvá i několik týdnů až měsíců, než dojde k nastavení původního prahu citlivosti. V tomto období reaguje sliznice slabší obrannou reakcí. Tím lze vysvětlit, proč vymizení příznaků u pacientů s patologickým EER trvá i několik měsíců [14].
Nové metody v diagnostice extraezofageálního refluxu
Kombinace jícnové impedance a pH-metrie: v porovnání s pH-metrií je jejím přínosem diagnostika i slabě kyselých či zásaditých refluxů a také rozlišení charakteru refluxátu (tekutina, vzduch) [15,16].
Měření pH v oblasti orofaryngu – Restech® systém: Restech® systém je moderní zařízení k měření pH v oblasti hltanu. Senzor vysoce citlivé antimonové sondy je umístněný na špičce 1,5 mm tlustého katétru, který je zaveden do úrovně uvuly. Na ochranu proti vyschnutí mu postačuje kondenzace vydechovaného vzduchu. Vysoká citlivost zařízení umožňuje měřit pH nejen tekutiny, ale i drobných kapek aerosolu [9,10]. Data jsou přenášena bezdrátově do záznamového zařízení. Svítící konec katétru usnadňuje jeho přesné umístnění za uvulu. Protože katétr není zaveden do jícnu, vyšetření toleruje více pacientů v porovnání s tradiční pH-metrií jícnu. Byla již vypracována i normativní data u bezpříznakové skupiny a byly stanoveny patologické hodnoty, jejich korelaci s problémy pacientů bude nutné ověřit v dalších studiích [10].
Peptest (detekce pepsinu): pomocí Peptestu je možné detekovat pepsin v různých vzorcích (sliny, sputum, středoušní tekutina a jiné). Reakce pepsinu s vysoce specifickými monoklonálními protilátkami se projeví objevením „čárky“ na vyšetřovaném proužku podobně jako v těhotenském testu. Vyšetření je schopné detekovat 16 ng pepsinu v 1 ml a trvá asi 15–20 min. Autoři udávají 88% senzitivitu a 87% specificitu vyšetření [17].
Současná koncepce léčby extraezofageálního refluxu
Z výše uvedených zjištění lze vyvodit vhodné terapeutické kroky u pacientů s EER:
Režimová a dietní opatření: zůstávají podstatnou složkou léčby.
Snížení kyselosti pomocí inhibitorů protonové pumpy (IPP): z této léčby bude profitovat jenom část pacientů s převahou kyselých refluxních epizod. Léčba musí být pravidelná, dostatečně dlouhá (3–6 měsíců) a v dostatečné dávce (2× denně). Zásadní je správné užívaní IPP – nalačno, 30–60 min před jídlem.
Suspenze alginátu: bylo zjištěno, že alginát váže pepsin a žlučové kyseliny ze žaludečního sekretu, čímž se vysvětluje jeho pozitivní účinek u pacientů s EER [18]. Pilotní studie prokázaly signifikantní snížení symptomů EER u pacientů léčených alginátem v porovnání s placebem [19]. Přesný způsob podávání a vhodná dávka zatím nebyly stanoveny. Část autorů doporučuje přidat pacientům, kteří nemají po IPP dostatečnou úlevu, 10 ml suspenze alginátu před spaním. Jiní autoři doporučují (zejména u pacientů s mírnějšími příznaky) opačný postup, tj. začít léčbu suspenzí alginátu 3–4× denně a IPP přidat do kombinace při neúspěchu této léčby.
Prokinetika: jsou nejlogičtější léčbou RCHJ, protože zvyšují peristaltiku jícnu, zvyšují vyprazdňování žaludku a také zvyšují tonus dolního jícnového svěrače. Všemi těmito mechanizmy snižují počet a závažnost refluxů. Musejí však být podávána pravidelně a v dostatečné dávce.
Hlasová reedukace a kognitivně behaviorální léčba: jejichž cílem je snížit napětí a stres.
Protože nízká compliance je nejčastějším důvodem, proč je léčba EER „neúčinná“, je velmi důležité pacienta důkladně poučit o nutnosti pravidelného a správného užívání předepsané medikace! Nejčastější příčinou špatné compliance je to, že pacient nevěří, že jeho problémy jsou způsobeny EER (nepálí mě žáha, nemám reflux) a jsou v tom často utvrzováni i jinými lékaři, kteří mají o EER malé povědomí a směšují spolu navzájem RCHJ a EER. Vysvětlení rozdílů mezi EER a RCHJ je proto zcela zásadní. Při stanovení správné diagnózy, nasazení správné léčby v dostatečné dávce a dobré compliance lze EER úspěšně léčit kombinací diety, úpravy životosprávy a výše uvedených léků u 80 % pacientů. U pacientů s přetrvávajícími výraznými problémy lze zvážit fundoplikaci [20].
Budoucnost léčby extraezofageálního refluxu – ovlivnění pepsinu
Zjištění, že pepsin hraje v patogenezi EER podstatnou roli, vede výzkumná centra k hledání vhodného léku, který by jeho škodlivé působení snížil (stejně tak vedlo zjištění, že vředová choroba žaludku je způsobena negativním působením kyseliny solné k vývoji H2-blokátorů a později inhibitorů protonové pumpy). Bylo již zjištěno, že pepsin se do buněk dostává receptory zprostředkovanou endocytózou, v případě detekce tohoto receptoru by bylo možné vytvořit antagonistu tohoto receptoru, který by bránil vstupu pepsinu do buněk. Další možností by mohla být léčba pomocí inhibitorů pepsinu, jejichž vývoj také probíhá [4].
Závěr
Výzkum extraezofageálního refluxu v posledních letech objasnil mnohé nové skutečnosti a zjistil významné odlišnosti od refluxní choroby jícnu (tab. 2). Samotná „kyselost“ již není považována za nejdůležitější patogenetický faktor působící v průběhu extraezofageálních refluxních epizod a důležitá role je přisuzována pepsinu, který si zachovává svou stabilitu a aktivitu i v průběhu slabě kyselých refluxů.
Tab. 2. Rozdíly mezi refluxní chorobou jícnu (RCHJ ) a patologickým extraezofageálním refluxem (EER). Tab. 2. Differences between gastroesophageal reflux disease (GERD) and extraesophageal reflux (EER). 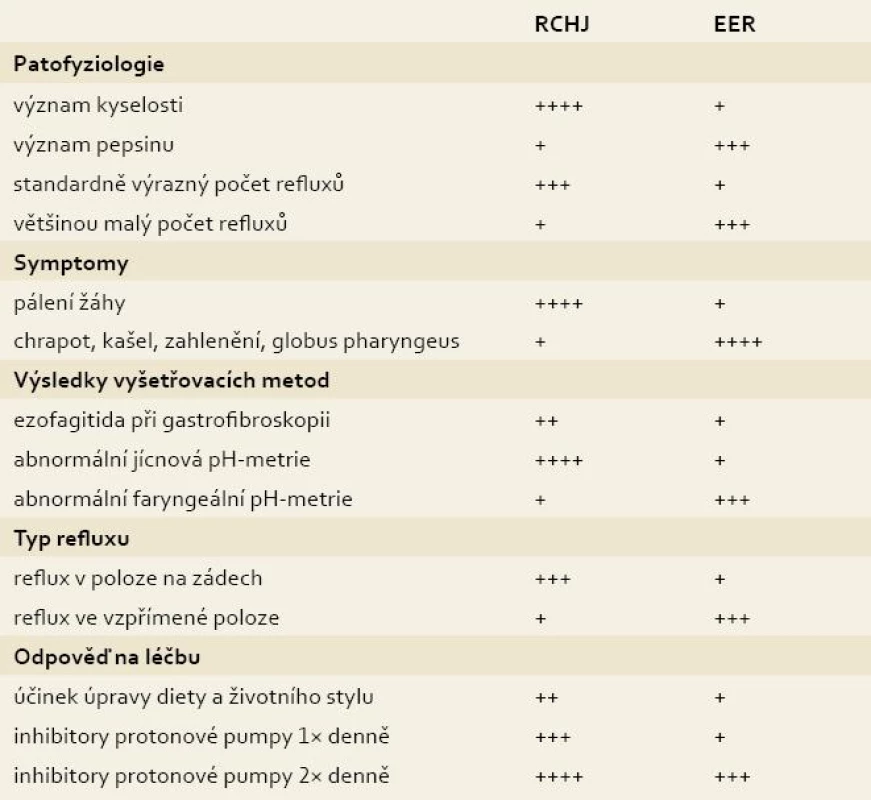
Bylo zjištěno, že sliznice hypofaryngu, hrtanu a dalších částí dýchacích cest je mnohem citlivější na složky refluxátu v porovnání se sliznicí jícnu.
Nové diagnostické metody (kombinace měření nitrojícnové impedance a pH-metrie, detekce pepsinu pomocí Peptestu, měření orofaryngeálního pH pomocí Restech® systému) umožňují lepší diagnostiku pacientů s patologickým extraezofageálním refluxem.
Léčbu je třeba zaměřit nejen na snížení kyselosti, ale také na snížení počtu refluxních epizod a snížení negativního působení pepsinu.
I přesto, že mnohé věci zůstávají zatím ne zcela objasněny, je pokrok v této oblasti potěšitelný a zcela jistě přispěje ke zlepšení kvality života mnohých pacientů s mimojícnovými projevy refluxní choroby jícnu.
Příprava článku byla podpořena grantem IGA MZ ČR 10612-3.
Doručeno do redakce: 23. 5. 2010
Přijato po recenzi: 11. 6. 2010MUDr. Karol Zeleník
ORL klinika Fakultní nemocnice Ostrava
17. listopadu 1790, 708 52 Ostrava-Poruba
karol.zelenik@fno.cz
Zdroje
1. Zeleník K, Komínek P, Stárek I et al. Extraezofageální reflux (1. část). Epidemiologie, patofyziologie a diagnostika. Otorinolaryngologie a Foniatrie 2008; 57 : 143–150.
2. Lukáš K et al. Refluxní choroba jícnu. Praha: Nakladatelství Karolinum 2003.
3. Lukáš K, Bureš J, Drahoňovský V et al. Refluxní choroba jícnu. Standardy České gastroenterologické společnosti – aktualizace 2009. Čes a Slov Gastroent a Hepatol 2009; 63 : 76–85.
4. Johnston N, Wells CW, Samuels TL et al. Pepsin in nonacidic refluxate can damage hypopharyngeal epithelial cells. Ann Otol Rhinol Laryngol 2009; 118(9): 677–685.
5. Johnston N, Dettmar PW, Bishwokarma B et al. Activity/stability of human pepsin: implications for reflux attributed laryngeal disease. Laryngoscope 2007; 117(6): 1036–1039.
6. Johnson N, Knight J, Dettmar PW et al. Pepsin and carbonic anhydrase isoenzyme III as diagnostic markers for laryngopharyngeal reflux disease. Laryngoscope 2004; 114(12): 2129–2134.
7. Johnston N, Dettmar PW, Lively MO et al. Effect of pepsin on laryngeal stress protein (Sep70, Sep53, and Hsp70) response: role in laryngopharyngeal reflux disease. Ann Otol Rhinol Laryngol 2006; 115(1): 47–58.
8. Samuels TL, Johnston N. Pepsin as a causal agent of inflamation during nonacidic reflux. Otolaryngol Head Neck Surg 2009; 141(5): 559–563.
9. Weiner GJ, Tsukashima R, Kelly C et al. Oropharyngeal pH monitoring for the detection of liquid and aerosolised supraesophageal gastric reflux. J Voice 2009; 23(4): 498–504.
10. Ayazi S, Lipham JC, Hagen JA et al. A new technique for measurement of pharyngeal pH: normal values and discriminating pH threshold. J Gastrointest Surg 2009; 13(8): 1422–1429.
11. Cook IJ. Clinical disorders of the upper esophageal sphincter. GI Motility online [online]. c2006, [cit. 2010-04-30]. Dostupné z <http://www.nature.com/gimo/contents/pt1/full/gimo37.html> .
12. Koufman JA. Laryngopharyngeal reflux is different from classic gastroesophageal reflux disease. Ear, Nose Throat J 2002; 81 (9 Suppl 2): 7–9.
13. Johnston N, Dettmar PW, Bishwokarma B et al. Activity/stability of human pepsin: implications for reflux attributed laryngeal disease. Laryngoscope 2007; 117(6): 1036–1039.
14. Bardhan KD. Reflux re-visited! Reflexctions and re-direction. Abstract book. Reflux and its consequences. Key opinions in laryngeal, pulmonary and oesophageal manifestations, Hull, United Kingdom, 21.–23. 4. 2010 : 36.
15. Dolina J, Kala Z, Prokešová J et al. Nové možnosti v diagnostice refluxní nemoci jícnu. Čes a Slov Gastroent a Hepatol 2009; 63 : 186–190.
16. Conchillo JM, Smout AJ. Review article: intra-oesophageal impedance monitoring for the assessment of bolus transit and gastro-oesophageal reflux. Aliment Pharmacol Ther 2008; 29 : 3–14.
17. Strugala V, Dettmar PW, Morice AH. Detection of the pepsin in sputum and exhaled breath condensate: could it be a useful marker for reflux-related respiratory disease? Gastroenterology 2009; 136 (5 Suppl 1): S1895.
18. Strugala V, Avis J, Jolliffe IG et al. The role af an alginate suspension on pepsin and bile acids – key aggressors in the gastric refluxate. Does this have implications for the treatment of gastro-oesophageal reflux disease? Journal of Pharmacy and Pharmacology 2009; 61 : 1021–1028.
19. McGlashan JA, Johnstone LM, Sykes J et al. the value of liquid alginate suspension (Gaviscon Advance) in the management of laryngopharyngeal reflux. Eur Arch Otorhinolaryngol 2009; 266(2): 243–251.
20. Drahoňovský V, Vrbenský L, Kmeť L et al. Laparoskopická antirefluxní operace u 100 operovaných po 2 a 5 letech ve srovnání s předoperačním stavem. Čes a Slov Gastroent a Hepatol 2006; 60 : 17–25.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2010 Číslo 6- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
-
Všechny články tohoto čísla
- Extraezofageální reflux up-to-date
- Nesteroidovými antireumatikami indukovaná kolopatia imitujúca Crohnovu chorobu
-
Klíčové otázky a odpovědi v léčbě Crohnovy nemoci
Závěry mezinárodního projektu IBD-AHEAD
- Fertilita, gravidita, dojčenie a nešpecifické črevné zápaly vo svetle záverov konsenzu ECCO 2010
- Použití biodegradabilního stentu u benigní stenózy žlučových cest
- Zamyšlení nad UEGW 2010
- Rejstřík 64. ročníku 2010
- Postavení a výtěžnost koloskopie v rámci screeningového programu založeného na testu na okultní krvácení (TOK) ve stolici
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Extraezofageální reflux up-to-date
- Použití biodegradabilního stentu u benigní stenózy žlučových cest
- Nesteroidovými antireumatikami indukovaná kolopatia imitujúca Crohnovu chorobu
- Fertilita, gravidita, dojčenie a nešpecifické črevné zápaly vo svetle záverov konsenzu ECCO 2010
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



