-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaTeória a zjednodušený matematický model viachladinovej umelej ventilácie pľúc
The theory and simplified mathematical model of multi-level intermittent positive pressure ventilation
Objective:
Considering the issues of intermittent positive pressure ventilation (IPPV) in non-homogenous pathological lung processes, the author built a mathematical model of tri-compartment non-homogenously injured lungs ventilated with a new mode of IPPV – multi-level ventilation. The author defines multi-level ventilation as a type (modification) of IPPV consisting of background ventilation using the CMV, PCV or PS (ASB) ventilation mode and an added level called “on-background ventilation“ consisting of multiple levels of PEEPh (PEEP high) with variable frequency and duration of transition between individual levels of PEEP.
The objective was to prove whether in cases of considerably non-homogenous gas distribution in acute pathological disorders of the lungs it is possible to improve gas distribution into slow broncho-alveolar compartments while only minimally or not at all increasing the volume load of the fast compartments by using the multi-level IPPV.Setting:
Department of Anaesthesiology and Intensive Care Unit.Materials and methods:
Multi-level ventilation on three pressure levels was carried out by a mathematical model as a combination of pressure-controlled ventilation (PCV) and two levels of PEEP: PEEP (constant) and PEEPh (PEEP high).Results:
Comparing single-level IPPV in the PCV mode with the tri-level ventilation (PCV+PEEPh/PEEP), the author found that the loading of the slow compartments in the model was considerably improved by as much as 50–60% in comparison to the baseline value. This difference, in absolute figures, reached as much as a 2–10 times increase in volume, or a 1.2–3 times increase in minute ventilation in compartments k4 and k5.Conclusions:
The mathematical model proves that the application of multi-level IPPV can achieve considerable changes in gas distribution in the lung parenchyma affected by a non-homogenous pathological process. The mathematical model requires further verification in the clinical setting to answer questions regarding its efficacy.Keywords:
IPPV – multi-level ALV – ARDS – ALI
Autoři: Török Pavol
Působiště autorů: OAIM, Vranovská nemocnica n. o., Vranov nad Topľou, Slovenská republika
Vyšlo v časopise: Anest. intenziv. Med., 19, 2008, č. 2, s. 96-104
Kategorie: Intenzivní medicína - Původní práce
Souhrn
Cieľ práce:
Dokázať, že pri výrazne nehomogénnej distribúcii plynov v ťažko patologicky postihnutých pľúcach je možné viachladinovou UVP zlepšiť distribúciu plynov do pomalých bronchoalveolárnych kompartmentov bez rizikovej zmeny objemového zaťaženia rýchlych kompartmentov. Autor realizoval softvérový matematický model viackompartmentných nehomogénne postihnutých pľúc, ktoré „ventiloval“ novým spôsobom UVP – tzv. trojhladinovou ventiláciou. Viachladinovú ventiláciu definuje ako spôsob (modifikáciu) UVP, pričom základnú hladinu ventilácie tvorí ventilačný režim CMV, PCV, alebo PS (ASB) a nadstavbu, tzv. ventiláciu na pozadí tvorí hladina PEEPh (PEEP high) s meniteľnou frekvenciou a trvaním prechodu medzi jednotlivými hladinami PEEPh/PEEP.Názov a sídlo pracoviska:
Oddelenie anestéziológie a intenzívnej medicíny.Materiál a metodika:
Viachladinová ventilácia na 3 tlakových úrovniach realizovaná matematickým modelom ako kombinácia tlakovo kontrolovanej ventilácie (PCV) a dvoch úrovní PEEP a (PEEPh).Výsledky:
Pri porovnávaní jednohladinovej UVP v režime PC s tzv. trojhladinovou ventiláciou ako kombináciou PC+PEEPh/PEEP autor zistil, že plnenie pomalých kompartmentov sa na modeli výrazne zlepšilo, a to rádove o 50–60 % oproti východzej hodnote. Tento rozdiel v absolútnom vyjadrení u obštrukčných kompartmentov dosahuje 2 až 10-násobok objemu, respektive 1,2–3-násobné zvýšenie MV v kompartmentoch k4 a k5.Záver:
Matematickým modelom sa dá preukázať, že aplikácia tzv. trojhladinovej UVP môže viesť k výrazným zmenám v distribúcii plynov v nehomogénne patologickým procesom postihnutom pľúcnom parenchýme. Matematický model si vyžiada klinické overenie, aby boli zodpovedané otázky účinnosti tejto modifikácie UVP.Kľúčové slová :
UVP – viachladinová UVP – ARDS – ALIÚvod
Jedným z vážnych a ťažko riešiteľných problémov umelej ventilácie pľúc (UVP) je ventilácia pacienta s difúznym patologickým procesom v pľúcnom parenchýme, ktorý spôsobuje výraznú nehomogenitu distribúcie plynov.
Vychádzajúc zo základov matematického a fyzikálneho modelovania umelej ventilácie pľúc (UVP) je možné povedať, že UVP klasickým režimom ventilácie aj pri najlepšej frekvenčnej a tlakovej optimalizácii, nemôže viesť u pacienta s nehomogénnou distribúciou plynov v pľúcach k optimálnej distribúcii plynov do jednotlivých, ale rôzne postihnutých kompartmentov [1, 6].
Rozdiely v časových konštantách (τ) jednotlivých kompartmentov v pľúcach, (aj modelovo simulovaných), sú také veľké, že pri optimálnom nastavení parametrov UVP pre jeden či dva kompartmenty, je nastavenie parametrov (frekvencia, pomer dôb Ti :Te, prietoky plynov) pre ďalšie kompartmenty nevyhovujúci, alebo výrazne suboptimálny.
Dá sa povedať, že jeden jediný režim ventilácie s určitými parametrami: frekvencia ventilácie (f), čas inspíria a exspíria (Ti : Te), dychový objem (VT), pozitívny tlak na konci výdychu (PEEP), tlak ventilačnej podpory (Ppc) v tlakovom režime UVP a pod., nemôže byť u nehomogénnych pľúc nastavený optimálne pre každý jeden, rôzne postihnutý kompartment [2, 3, 4, 5].
Najjednoduchším teoretickým riešením by bolo aplikovať pre každý kompartment iné nastavenie parametrov ventilácie, ktoré by boli optimálne vzhľadom na mechanické vlastnosti zvoleného kompartmentu. Keďže kompartmenty nie sú uložené na jednom mieste a nie je možné oddeliť vstup do každého kompartmentu zvlášť, takéto podmienky nie je možné technicky splniť [3].
Príkladom pre vhodnosť tejto úvahy je selektívna bibronchiálna ventilácia pri jednostrannom pľúcnom poškodení (napr. kontúzia jedných pľúc), kedy zdravé pľúca ventilujeme jedným režimom a parametrami UVP a pľúca postihnuté patologickým procesom ventilujeme iným režimom s inými parametrami nastavenia. V tomto prípade je možné anatomicky oddeliť poškodené a nepoškodené kompartmenty a fyzikálne oddeliť prúd plynov tečúci do každého kompartmentu (v tomto prípade „zdravé“ a „choré pľúca“).
Pri anatomicky nehomogénnom poškodení pľúc (pneumónia, ARDS, bronchiolitis, edém pľúc, početná kontúzia pľúc a pod.) existuje množstvo rôzne postihnutých, ale biofyzikálne podobných kompartmentov, ktoré sú anatomicky uložené difúzne po celých pľúcach a nie je možné rozdeliť prietok plynov do každého kompartmentu zvlášť [1, 3].
Obr. 1. Schematické znázornenie difúzne nehomogénne poškodených pľúc 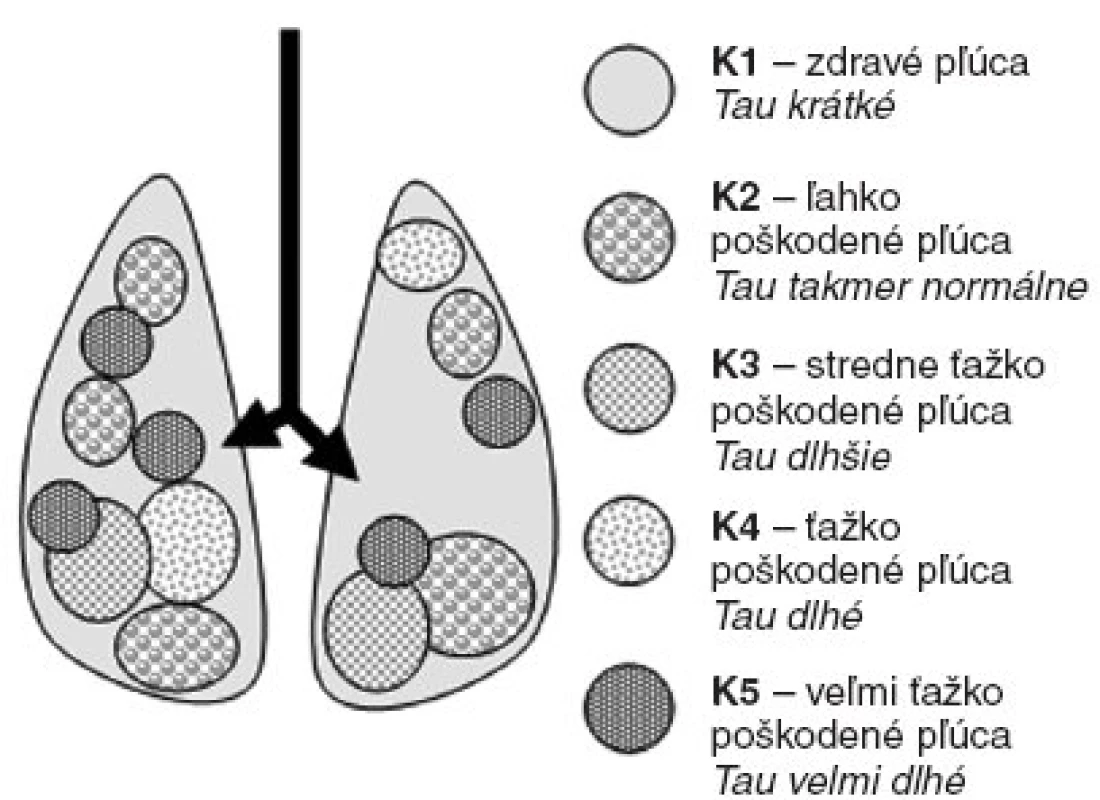
V týchto prípadoch bude ventilácia jednotlivých kompartmentov optimálna len v tých, pre ktoré je zvolené relatívne najoptimálnejšie nastavenie parametrov UVP. Ostatné kompartmenty budú ventilované viac či menej suboptimálne.
Pre diagnostiku mechanických vlastností dýchacích orgánov, ako aj pre aplikáciu dýchacích plynov je len jedna „signálová” aj „výkonová” cesta, a to trachea či endotracheálna (ET), respektive tracheostomická (TT) kanyla. Na konci tejto cesty môžeme merať základné parametre potrebné pre diagnostiku, a to fyzikálne parametre prietoku plynov. Tou istou cestou môžeme aplikovať aj UVP. Pritom priamo merať je možné len parametre prietoku (Q), tlaku (P) a času (t). Všetky ostatné parametre sú parametrami vypočítanými [3, 4].
Vyššie uvedené anatomické a fyzikálne obmedzenie spôsobuje problémy pri diagnostike, aj pri aplikácii optimálnych parametrov UVP pre jednotlivé, rôzne postihnuté a naviac anatomicky nehomogénne uložené kompartmenty.
Materiál a metodika
Teória viachladinovej UVP
Predpokladajme, že máme matematický multikompartmentný model nehomogénnych pľúc. Statická poddajnosť bola simulovaná ako lineárna, pre každý kompartment (k) Cst1–5= 100 ml . kPa-1 a odpory kompartmentov od 0,3 do 15 kPa . s . l-1. Časové konštanty (τ) /sek./ udávajúce „rýchlosť“ plnenia kompartmentu počas inspíria a rýchlosť vyprázdňovania kompartmentu počas exspíria v jednotlivých kompartmentoch sú v tabuľke 1.
Tab. 1. Časové konštanty multikompartmentného modelu 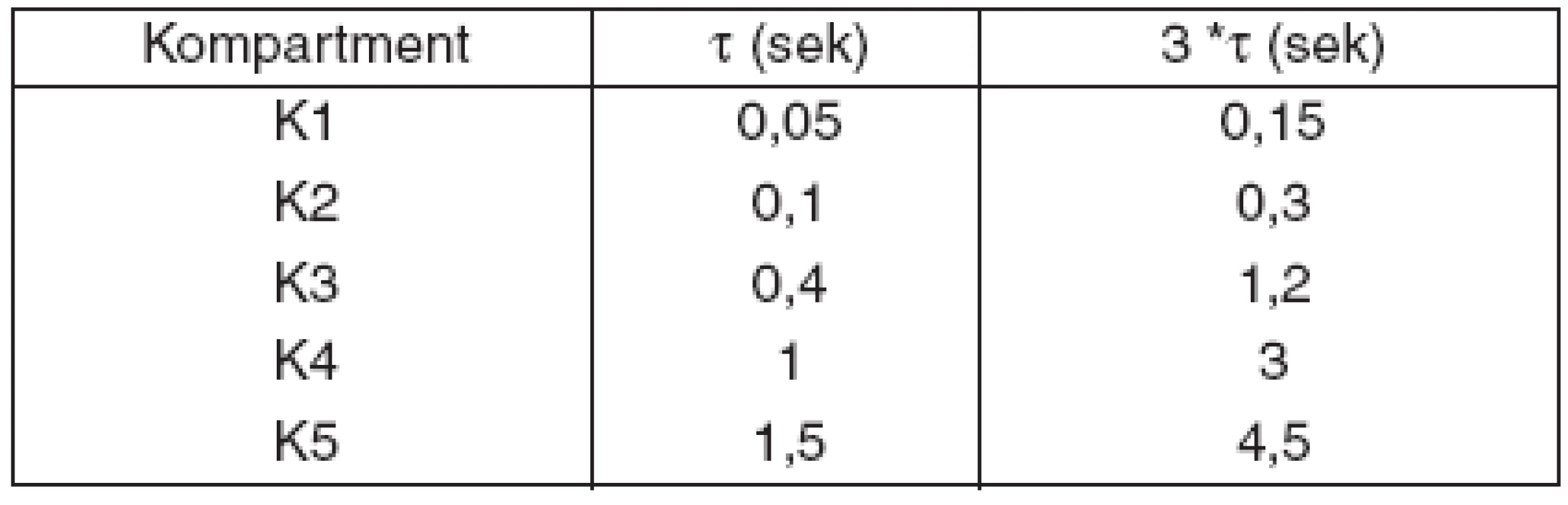
τ = R . C (0)
Predpokladajme, že aplikujeme UVP s pomerom Ti : Te = 1 : 1. Potom pre výmenu plynov v jednotlivých kompartmentoch za čas 3 . t sú „optimálne“ časy ventilačného cyklu (Tcy) a frekvencií ventilácie uvedené v tabuľke 2.
Tab. 2. Teoreticky optimálne frekvencie pre jednotlivé kompartmenty 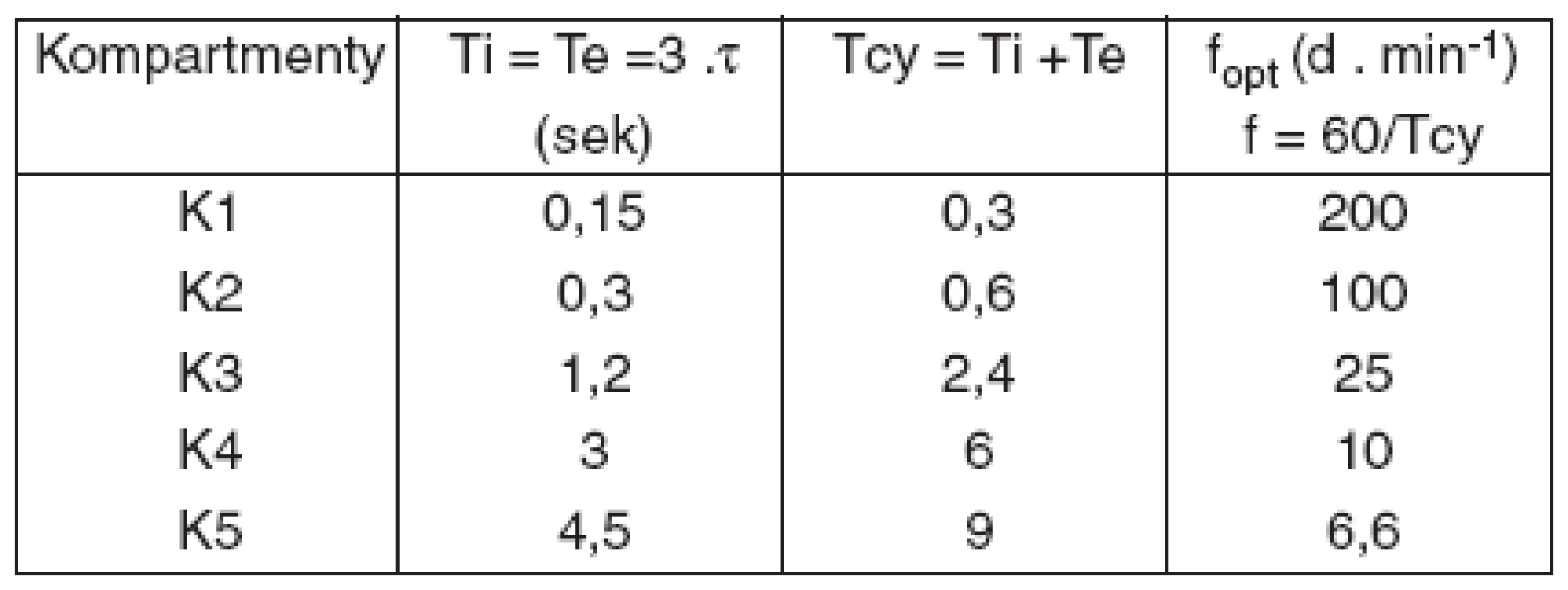
Ti = Te = 3 . τ (1)
Tcy = Ti + Te (2)
f = 60/Tcy (3)
Z tabuľky 2 vyplýva, že ak budeme pľúca ventilovať frekvenciou 200 d . min-1, bude optimálne ventilovaný len kompartment k1 a ostatné budú ventilované neoptimálne a v tomto prípade hypoventilované. Hypoventilácia bude tým výraznejšia, čím má kompartment dlhšie τ, teda čím sú kompartmenty „pomalšie“.
Naopak, ak budeme ventilovať frekvenciou 6–7 d . min-1, bude kompartment k5 ventilovaný optimálne, ale suboptimálne budú ventilované ostatné kompartmenty.
Suboptimálna ventilácia sa prejaví ako relatívna hyperventilácia/hypoventilácia a v prípade režimu UVP (volume control) VC (CMV) ventilácie výrazne stúpne špičkový alveolárny tlak (Pai) v kompartmentoch s kratším τ .
Ak úplne teoreticky zvážime vyššie povedané, potom môžeme dôjsť k záveru, že pre optimálnu výmenu plynov každého jedného kompartmentu si bude UVP vyžadovať simultánnu ventiláciu piatimi rôznymi frekvenciami, prípadne s rôznymi pomermi dôb TI : Te, dychovými objemami či tlakmi.
V skutočnosti pri UVP máme len jeden vstupný prvok, ktorým je trachea, respektíve endotracheálna či tracheostomická kanyla, cez ktorú musí inspirovaný i exspirovaný plyn pretiecť. Z toho vyplýva aj technické riešenie a filozofia umelej ventilácie pľúc viacerými tlakovými hladinami a frekvenciami ventilácie.
Režimy a nastavenie časových a tlakových parametrov jednotlivých hladín UVP musia byť kompatibilné vzájomne, prípadne aj so spontánnou dychovou aktivitou pacienta.
Vysvetlenie názvoslovia
Viachladinová ventilácia je riešením novým, preto je potrebné vysvetliť si jednotlivé pojmy, ktoré budeme používať v ďalšom texte.
Základná hladina UVP – tento pojem definuje ako ventilačný režim, vrátane parametrov nastavenia frekvencie, pomeru časov Ti : Te, objemu či tlaku, ktorý je aplikovaný u pacienta ako základný (napr. CMV, PCV, PS /ASB/). Túto hladinu ventilácie môžeme nazvať ventilácia na popredí.
Nadstavbové hladiny – tento pojem definuje modifikáciu ventilačného režimu, ktorý pracuje simultánne s ventiláciou na popredí, ale s inými nastavenými parametrami tlaku, časov dýchacieho cyklu. Takýchto hladín môže byť teoreticky väčší počet (multilevel), pričom ich nazývame nadstavbová hladina 1 ...až...n. Tieto hladiny môžeme nazvať – ventilácia na pozadí. Tieto hladiny sú akoby „skryté“ v základnej hladine. Frekvencia nadstavbových hladín, ako aj aplikovaný tlak, sú zvyčajne nižšie ako parametre základnej hladiny. Pre trojhladinovú ventiláciu sme použili názov PEEP high (PEEPh).
PEEP – nastavený ako statická veličina na ventilátore za účelom recruitmentu (alebo na udržanie geometrie alveolov) je konštantným tlakom v dýchacích cestách pôsobiacim v alveolárnom kompartmente.
Nastavenie tlakových parametrov v matematickom modeli bolo identické, ako je na obrázku 2.
Obr. 2. Schematické znázornenie tlakovej krivky pri aplikácii trojhladinovej ventilácie pľúc Základný ventilačný režim (PCV) s frekvenciou 30 d.min-1, a nadstavbová hladina ventilácie na pozadí s frekvenciou 10 d.min-1, tvorená tlakovou hladinou PEEPh / PEEP. 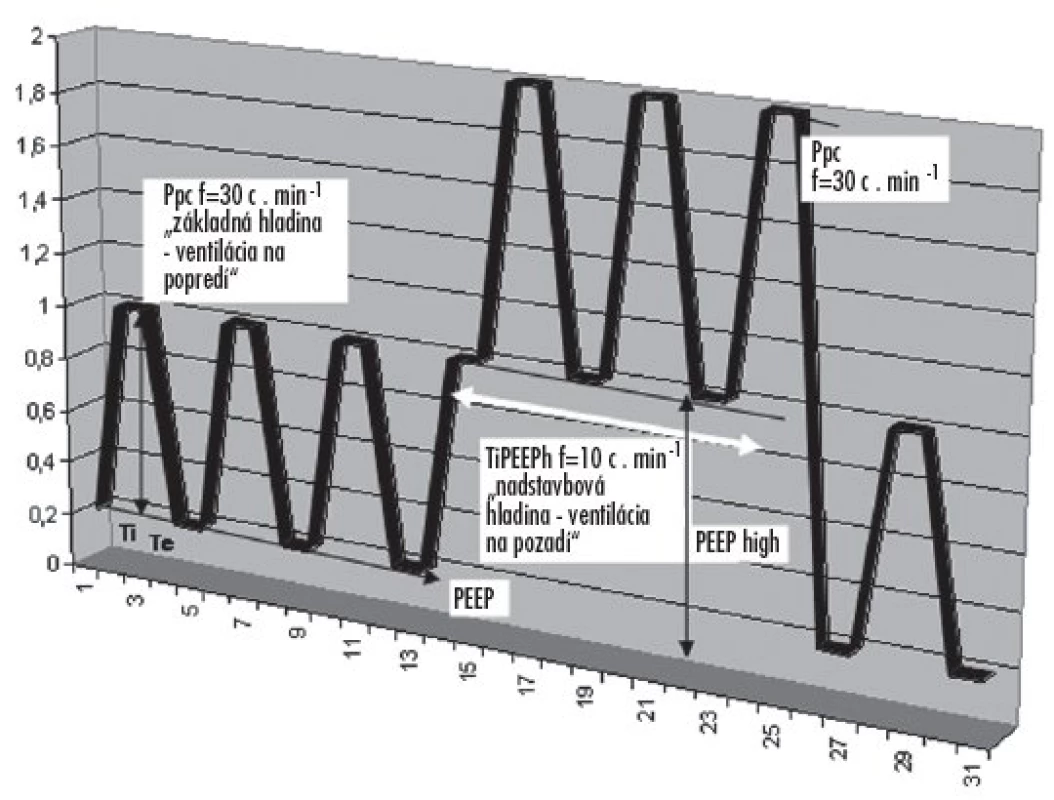
Je samozrejmé, že hodnoty Ppc a PEEPh, ako aj PEEP, môžeme pri prechode do trojhladinovej ventilácie nastaviť na zvolené hodnoty. Príklad je na obrázku 3.
Obr. 3. Základná fyzikálna schéma matematického 5-kompartmentného modelu, ktorý bol aplikovaný pri modelovaní výmeny plynov 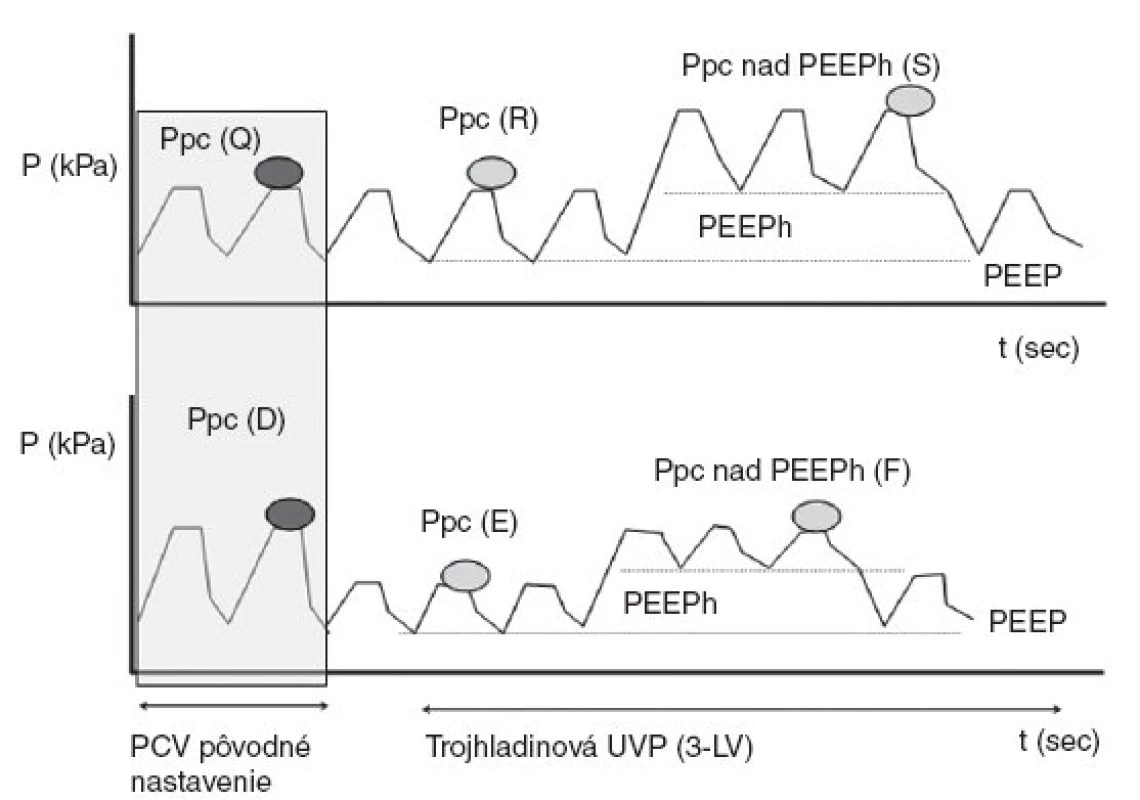
Na hornom grafe v obrázku 3 je znázornený prechod z ventilácie v režime PCV (pôvodné nastavenie) do trojhladinovej ventilácie. Ppc (bod Q a R) sme nemenili, a preto špičkový tlak Ppc nad PEEPh (bod S) stúpol o hodnotu PEEPh. Na dolnom grafe je znázornená iná možnosť nastavenia tlakových hodnôt. Ak pôvodne nastavený tlak v režime PCV – Ppc bol zvolený na hodnotu (bod D), pri nastavení trojhladinovej ventilácie sme parametre tlaku Ppc znížili na hodnotu (bod E), potom tlak Ppc nad PEEPh (bod F) dosahuje len pôvodnú hodnotu Ppc (bod D) použitú v pôvodnom režime PCV. Kombinácií a variant nastavenia je veľký počet a konkrétne nastavenie je závislé do veľkej miery od pľúcnej patológie a jej diagnostiky. Príklad na obrázku 3 je použitý ako didaktická pomôcka.
Základné vysvetlenie matematického modelu a fyzikálnych princípov trojhladinovej ventilácie a jej simulácia na nehomogénnom multikompartmentnom modeli pľúc
Predpokladajme, že pacient (model) s vyššie uvedenými mechanickými vlastnosťami je ventilovaný ventilačným režimom pressure control ventilation (PCV) zvolenými parametrami (pressure of pressure control) Ppc = 1 kPa, f = 30 d . min-1, Ti : Te = 1 : 1, PEEP = 0,2 kPa. Tento ventilačný režim teda považujeme za režim na popredí, respektive za základnú hladinu UVP.
Na pozadí tohoto ventilačného režimu aplikujeme striedavo hladinu PEEPh, s parametrami: PEEPh = 1 kPa nad PEEP, s frekvenciou fPEEPh = 1/3 z frekvencie PC, t. j. 10 d . min-1. Pomer Ti : Te nadstavbovej hladiny bol 1 : 1, t. j. (TiPEEPh) = Ti%h = 50%.
Tlakovo-časová krivka trojhladinovej ventilácie je schematicky znázornená na obrázku 2.
Teoreticky sa dá predpokladať, že kompartmenty s krátkou časovou konštantou na 5. kompartmentnom modeli pľúc budú ventilované lepšie vyššou frekvenciou, teda režimom PC, oproti kompartmentom patologickým, ktoré budú ventilované relatívne lepšie striedaním PEEPh /PEEP s frekvenciou 10 d . min-1.
Pre výpočet špičkového alveolárneho tlaku (Pai) a koncového alveolárneho tlaku (Pae), ako aj VT (dychového objemu) v jednotlivých kompartmentoch (k1–5) boli použité nasledujúce vzorce:
Model predpokladá lineárny priebeh Cst, idealizované exponenciálne priebehy prietoku a laminárne prúdenie cez jednotlivé komponenty. Generátor tlaku bol simulovaný ako generátor s nulovým vnútorným odporom (Rg = 0). Schematický princíp modelu je na obrázku 4.
Obr. 5. Schéma možného nastavenia tlakových hodnôt počas aplikácie trojhladinovej ventilácie v porovnaní s hodnotami pôvodne nastavených parametrov pri predošlej ventilácii PCV Vysvetlivky: C – poddajnosť, R – odpor, Pa – alveolárny tlak, VT – dychový objem, k – kompartmenty 1–5 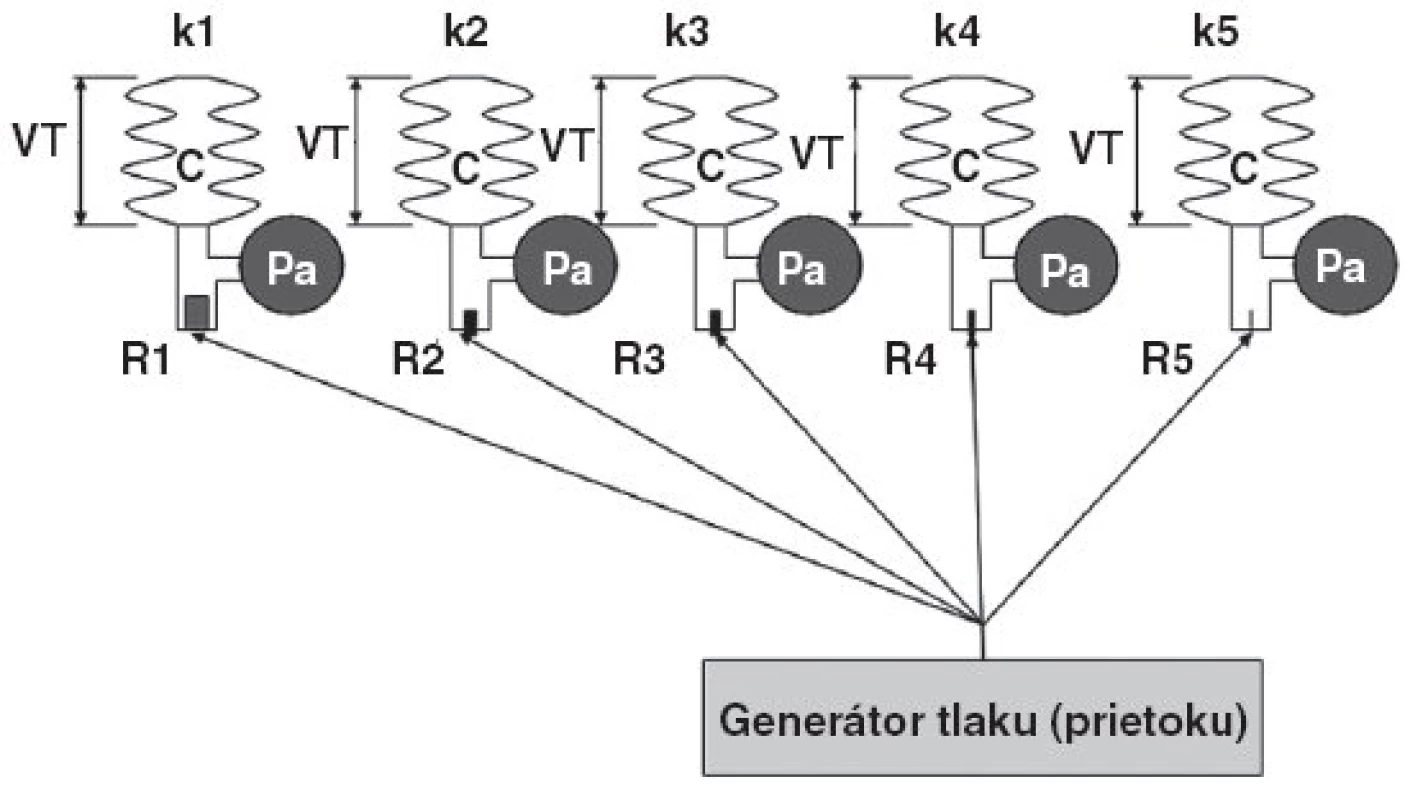
Schematické plnenie a vyprázdňovanie jednotlivých kompartmentov (k1–5) počas jednotlivých fáz trojhladinovej ventilácie je znázornené na obrázku 5.
Obr. 6. Schéma dynamického modelu vysvetľujúceho plnenie a vyprázdňovanie jednotlivých kompartmentov pľúc v rozhodujúcich fázach dýchacích cyklov pri trojhladinovej ventilácii 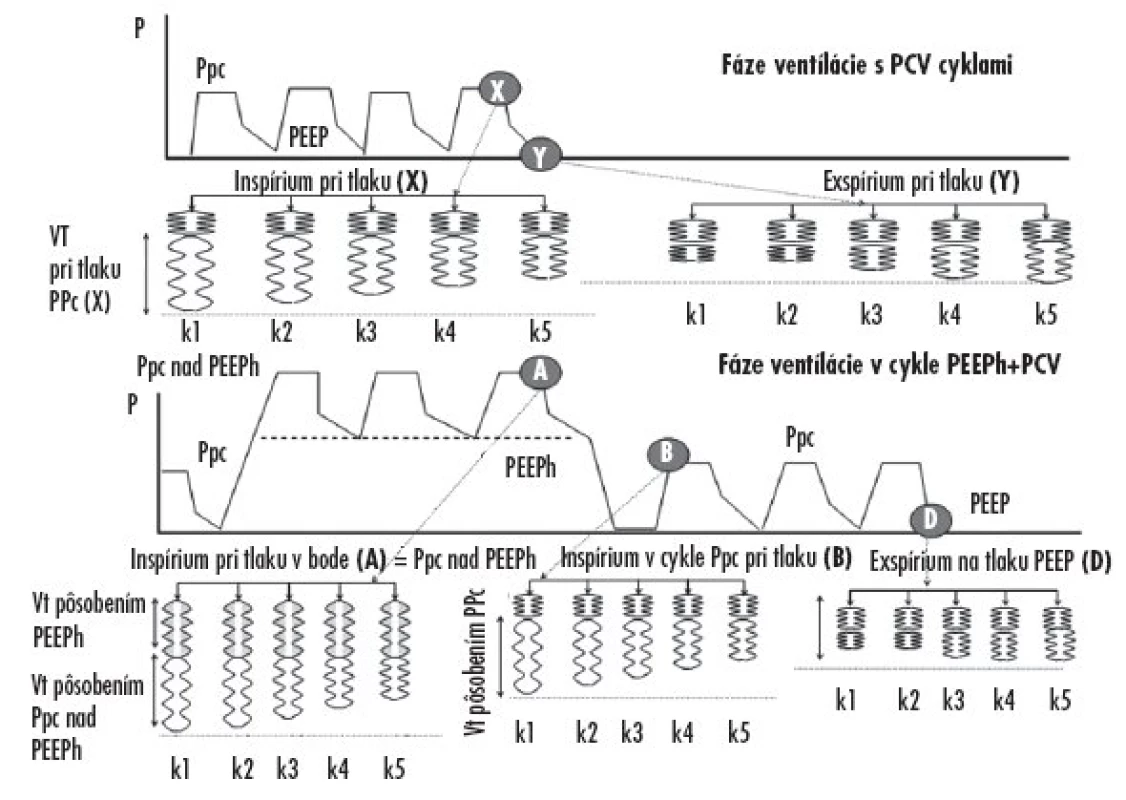
V hornej časti obrázku je znázornená prvá fáza ventilácie cyklami PCV a účinok tlaku Ppc na plnenie a vyprázdňovanie jednotlivých kompartmentov. Pri dosiahnutí tlakového bodu (X) na P/t krivke (koniec inspíria) dosiahne distribúcia plynov do jednotlivých kompartmentov naznačené objemy. Kompartmenty k1 a k2 sa naplnia maximálne, k3–k5 postupne menej. V exspíriu (tlakový bod označený Y – koniec exspíria), sa prvé dva kompartmenty vyprázdnia úplne, k3–k5 sa vyprázdňujú menej. V týchto kompartmentoch ostane uväznený určitý objem plynov (trap volume) a vznikne v nich auto (inadvertný) PEEPi. Nehomogenita distribúcie je spôsobená rozdielnymi časovými konštantami kompartmentov (τ).
V dolnej časti obrázku 5 je znázornená fáza dychového cyklu na tlakovej hodnote PEEPh + Ppc (bod A). Pretože vo vyššie uvedenom modeli trvá pri fPEEPh = 10 d . min-1, TiPEEPh = 3 sekundy, naplnia sa kompartmenty rýchle i pomalé vo fáze trvania PEEPh, a naviac sa naplnia kompartmenty pôsobením tlaku Ppc nad PEEPh. Po prechode PEEPh znovu do fázy PCV sa kompartmenty parciálne vyprázdnia a plnia nasledujúcim cyklom PCV tlakom Ppc, ako je naznačené pri tlakovej hodnote (bod B). Po ukončení cyklov PCV na tlaku PEEP (bod D) sa kompartmenty vyprázdnia na objemy, ako sú naznačené (v bode Y) na hornej časti obrázku. Potom sa cykly opakujú.
Výsledky
Zmeny špičkového alveolárneho tlaku (Pai), koncového alveolárneho tlaku (Pae) a objemového plnenia (VT) jednotlivých kompartmentov pri (jednohladinovej) PC ventilácii frekvenciou 30 c . min-1, Ti : Te = 1 : 1 a Ppc = 1 kPa pri PEEP = 0,2 kPa sú na grafe 1.
Graf 1. Distribúcia plynov (VT) počas inspíria a exspíria v modeli a tlaky (Pai a Pae) v alveolárnych kompartmentoch pri f = 30 d . min-1, Ti : Te = 1 : 1 a Ppc = 1 kPa. 
Zmeny špičkového alveolárneho tlaku (Pai), koncového alveolárneho tlaku (Pae) a objemového plnenia (VT) jednotlivých kompartmentov pri (jednohladinovej) PC ventilácii frekvenciou 10 c . min-1, Ti : Te = 1 : 1 a Ppc = 1 kPa pri PEEP = 0,2 kPa sú uvedené na grafe 2.
Graf 2. Distribúcia plynov (VT) počas inspíria a exspíria v modeli a tlaky (Pai a Pae) v alveolárnych kompartmentoch pri f = 10 d . min-1, Ti : Te = 1 : 1 a Ppc = 1 kPa. 
Z porovnania grafov 1 a 2 je zrejmé, že pri frekvencii f = 30 d . min-1 bude v pomalých kompartmentoch s dlhšou časovou konštantou (τ) stúpať Pae, pretože v nich bude stúpať PEEPi a znižovať sa delta Pai-Pae. Tento fakt má za následok zníženie objemového plnenia (VT) v pomalých kompartmentoch. Pri frekvencii f = 10 c . min-1 stúpne plnenie pomalých kompartmentov a vzostup Pae (spôsobený vznikom PEEPi) bude ďaleko menší. Kým pri frekvencii f = 30 c . min-1 bude sumárne VT za všetky kompartmenty nižšie, sumárna minútová ventilácia (MV) bude – napriek zhoršenej distribúcii plynov do pomalých kompartmentov – vyššia. Pri nižšej frekvencii bude napriek zlepšeniu distribúcie plynov do pomalých kompartmentov sumárny dychový objem VT vyšší, minútová ventilácia bude nižšia. Tieto zmeny sú závislé na ventilačnej frekvencii.
(MV = f . VT)
Ak si porovnáme distribúciu plynov (VT) do kompartmentov k3–k5, vidíme, že pri frekvencii f = 10 stúpne objemové plnenie týchto kompartmentov 2–10-násobne. Minútová ventilácia stúpla len o 1,2–3-násobok. V prípade, že aplikujeme trojhladinovú ventiláciu a budeme sledovať distribúciu plynov do jednotlivých kompartmentov, zistíme, že distribúcia plynov sa zlepší hlavne v kompartmentoch pomalých.
Na grafe 3 vidíme schematicky, že pri jednotlivých tlakových zmenách dochádza v pomalých kompartmentoch k integrácii objemu počas inspíria pomalšou frekvenciou (fpeeph) a zvyšovaniu celkového VT kompartmentu. Tým sa zlepší výmena plynov v pomalých pri f = 30 d . min-1 hypoventilovaných kompartmentoch. V závislosti nastavenia pracovných tlakov Ppc a PEEPh sa bude meniť aj plnenie kompartmentov rýchlych s krátkou časovou konštantou. Na prezentovanom modeli stúpla celková MV o cca 50 %. Veľký podiel na celkovom zvýšení MV je v zlepšenej distribúcii plynov do pomalých kompartmentov k4 a k5, u ktorých bola MV pri f = 30 d . min-1 = 0,6 l . min-1 a 1,3 l . min-1 pri f = 10 d . min-1, čo predstavuje dvojnásobné zvýšenie MV v kompartmentoch k4 a k5.
Graf 3. Priebeh tlakovej krivky a plnenie kompartmentu k1, kompartmentu k5 a priemerná hodnota kompartmentov k1–5, plynom (VT) pri 3-hladinovej ventilácii – schematicky Z grafu je zrejmé, že objemové plnenie kompartmenu k5 sa postupne zvyšuje počas fázy PEEPh + Ppc, podobne aj v priemernom plnení kompartmentov k1–5. fPpc = 30 d . min-1, fPEEPh = 10 d . min-1, Ti : Te = 1 : 1 
Diskusia
Modelovanie viachladinovej ventilácie malo za úlohu dokázať, že je možné zmeniť objemové plnenie (distribúciu plynov) hlavne kompartmentov simulujúcich patologickým procesom (pomalé kompartmenty) postihnuté pľúca (k4, k5). V kompartmentoch postihnutých patologickým procesom (obštrukcia) nie je možné jednohladinovou ventiláciou (PCV, PS, CMV) dospieť k ich optimálnemu, alebo aspoň lepšiemu plneniu bez kritického poklesu MV znížením ventilačnej frekvencie. Naproti tomu pri viachladinovej ventilácii je možné dosiahnuť redistribúciu plynov smerom do patologických „pomalých“ kompartmentov. Vyššie uvedený model nebol tlakovo optimalizovaný a mal len ukázať, že k želateľným zmenám dochádza. Čím ťažšie je postihnutie patologických kompartmentov v zmysle obštrukcie, tým relatívne väčšie zlepšenie ich plnenia dostaneme pri viachladinovej ventilácii [2, 3, 4].
Pre klinickú aplikáciu výsledkov vyššie uvedených modelov je možné povedať len toľko, že ak pri jednohladinovej ventilácii difúzne patologicky postihnutých dýchacích orgánov dochádza k zvyšovaniu pľúcneho shuntu aj z titulu nerovnomernej distribúcie plynov v pľúcach, potom ani optimalizácia takejto ventilácie nebude viesť k výraznému zníženiu shuntu [1, 2].
Pri viachladinovej UVP, ktorá bude navyše optimalizovaná, je predpoklad, že distribúcia plynov do jednotlivých, ale rôzne postihnutých kompartmentov, sa parciálne vyrovná, alebo prinajmenšom zlepší natoľko, aby sa znížili pľúcne skraty a zlepšila výmena plynov v pľúcach. Ďalšími modelmi sa dá dokázať, že vzhľadom na typ UVP sa špičkové tlaky v dýchacích orgánoch smerom do rizikových hodnôt zvyšujú len málo a minútová ventilácia sa nemení o viac ako +10–20 % pri porovnaní s klasickou jednohladinovou PC ventiláciou [5].
Pri difúznom multikompartmentnom poškodení pľúc patologickým procesom má každý kompartment iné mechanické vlastnosti a pre každý z nich je optimálna iná frekvencia ventilácie a pomer dôb Ti : Te [4, 5]. Jednohladinovou ventiláciou sa teda už len na základe tejto úvahy nedá dosiahnuť optimálna distribúcia plynov.
Záver
Viachladinová, v tomto prípade trojhladinová ventilácia simulovaná matematickým modelom ukazuje, že v teoretickej rovine je možné, iste nie ideálne, ale v podstatnej miere zlepšiť distribúciu plynov a tým aj ventiláciu patologickým procesom postihnutých (pomalých) kompartmentov pri súčasnom miernom zvýšení priemerného objemového plnenia (rýchlych) kompartmentov „zdravých“, pravdaže v závislosti na použitých tlakoch (Ppc a PEEPh). Je teda možné predpokladať, že u difúzneho nehomogénneho poškodenia pľúcneho parenchýmu povedie k zlepšenej distribúcii plynov do „pomalých“ kompartmentov a zásadne nezvýši riziko barotraumy v kompartmentoch „rýchlych“, čo by bolo veľmi nápomocné pre realizáciu „netraumatizujúcej ventilácie“, hlavne v ťažko poškodenom pľúcnom parenchýme. Táto matematická simulácia si vyžiada reálne klinické skúšanie, ktoré odpovie na doposiaľ nejasné otázky.
Došlo 20. 3. 2007.
Přijato 6. 10. 2007.
Adresa pro korespondenci:
h. Doc. MUDr. Pavol Török, CSc.
E. Urxa 14
093 01 Vranov n/Topľou
Slovensko
e-mail: torokp@t-zones.sk
Zdroje
1. Gattinoni, L. et al. Lung structure and function in different stages of severe ARDS. J. Am. Med. Assoc., 1994, 271, p. 1772–1779.
2. Májek, M., Krajčiová, K., Török, P. Akútne ventilačné a respiračné zlyhávanie. Lekársky obzor, 1997, 46, č. 9, s. 219–223.
3. Török, P. et al. Optimalizácia UVP počas anestézie. In Priebežná správa o riešení výskumnej úlohy MZ SR č. 49/97 za r. 1998. 68 s.
4. Török, P., Májek, M., Kolník, J. Je časová konštanta Tau (τ) pri umelej ventilácii pľúc konštantou? Teoretický a fyzikálny model. Anest. neodklad. Péče, 2001, 12, č. 6, s. 291–297.
5. Török, P. Multilevel ventilation. In Zborník z konferencie Ruskej akadémie vied – Akútne zlyhanie pľúc. Piešťany-Moskva, 30. 9.–3. 10. 2006, 187 s.
6. West, J. B. Bioengineering Aspects of the Lung. Marcel Dekker, inc. : New York 1977, 585 s.
Štítky
Anesteziologie a resuscitace Intenzivní medicína
Článek Zprávy ČSARIMČlánek Poznámka k pětiletému výročí
Článek vyšel v časopiseAnesteziologie a intenzivní medicína
Nejčtenější tento týden
2008 Číslo 2- Jak souvisí postcovidový syndrom s poškozením mozku?
- Perorální antivirotika jako vysoce efektivní nástroj prevence hospitalizací kvůli COVID-19 − otázky a odpovědi pro praxi
- Neodolpasse je bezpečný přípravek v krátkodobé léčbě bolesti
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
- Metamizol a jeho pozice v léčbě bolesti
-
Všechny články tohoto čísla
- Trojhladinová ventilácia pľúc (3LV® – 3 level ventilation) – prvé klinické skúsenosti
- Epidemiologie invazivní kandidózy a kandidémie – stále aktuální problém
- Zprávy ČSARIM
- Report of the meeting of the Section and Board of Anaesthesiology (SBA) Istanbul, Saturday 17th November 2007
- Minimal Monitoring Standards in the Perioperative Period
- Poznámka k pětiletému výročí
- Nozokomiální versus komunitní infekce na JIP
- Laryngeální maska LMA-ProSeal™ – bezpečná možnost zajištění dýchacích cest pro laparoskopické cholecystektomie
- Použití intramuskulárního podání dexmedetomidinu u popálených – předběžné výsledky
- Intravenózní sedace kombinací dexmedetomidinu a ketaminu u operací v místní anestezii
- Klasifikace infekcí v intenzivní péči, srovnání inkubační doby a nosičství
- Teória a zjednodušený matematický model viachladinovej umelej ventilácie pľúc
- Anesteziologie a intenzivní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Nozokomiální versus komunitní infekce na JIP
- Epidemiologie invazivní kandidózy a kandidémie – stále aktuální problém
- Laryngeální maska LMA-ProSeal™ – bezpečná možnost zajištění dýchacích cest pro laparoskopické cholecystektomie
- Trojhladinová ventilácia pľúc (3LV® – 3 level ventilation) – prvé klinické skúsenosti
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




