-
Medical journals
- Career
Celulózové materiály v ošetřování ran
: Tomáš Sopuch 1; Radomíra Drahovzalová 1; Josef Rýdl 1; Ivo Bureš 2; Miloslav Milichovský 3; Jarmila Vytřasová 4; Petra Moťková 4; Václav Švorčík 5; Jiří Podlaha 6,7; Marie Horáková 7; Ruta Masteiková 8; Lenka Vinklárková 8; Pavel Suchý 9
: Holzbecher, spol. s r. o., barevna a bělidlo Zlíč 1; Geriatrická klinika, Pardubická krajská nemocnice, a. s. 2; Oddělení dřeva, celulózy a papíru, Univerzita Pardubice 3; Katedra biologických a biochemických věd, Univerzita Pardubice 4; Ústav inženýrství pevných látek, VŠCHT Praha 5; Chirurgická klinika, LF MU a FN Brno 6; Chirurgická a cévní ambulance, Brno-Šlapanice 7; Ústav technologie léků, Veterinární a farmaceutická univerzita, Brno 8; Ústav humánní farmakologie a toxikologie, Veterinární a farmaceutická univerzita, Brno 9
: Hojení ran 7, č. 2: 14-20, 2013
:
Celulózové materiály nebo jejich deriváty nabízejí pro hojení ran řadu cenných vlastností. Karboxylované celulózy zastupuje především karboxymethylovaná celulóza a oxidovaná celulóza. Hcel HT (karboxymethylovaná celulóza) je nový typ celulózového krytí s kyselým povrchovým pH.
Klíčová slova:
hojení ran, celulózové materiály, karboxymethylcelulóza, oxidovaná celulózaTypy celulózových materiálů v ošetřování ran
Celulóza je nejrozšířenější přírodní polysacharid. V ošetřování ran se používá přírodní celulóza (bavlna), regenerovaná celulóza (viskóza) nebo nanocelulóza (mikrobiální celulóza nebo nanostruktury celulózy). Chemickou modifikací celulózy, např. karboxymethylací vznikají deriváty celulózy, které získávají další vlastnosti (např. rozpustnost ve vodě na koloidní systémy nebo vytvářejí ve vodě vláknitou hmotu připomínající konzistentní gel – hydrokoloidní vlákna). Usušením koloidních roztoků lze připravit filmy, chemickým zesíťováním pak kompaktní hydrogely. Selektivní oxidace a degradace celulózy vede ke vzniku vstřebatelné (resorbovatelné) oxidované celulózy. Celulózové materiály tak nabízejí řadu cenných vlastností, které je možno využít v ošetřování ran (Gupta et al. 2010; Woodings 2001; Sopuch et al. 2013).
Karboxylované celulózové materiály
V ošetřování ran a chirurgii se prosadily zejména dva anionaktivní deriváty celulózy obsahující funkční karboxylovou skupinu. Je to oxidovaná celulóza (6-karboxycelulóza, oxycelulóza) (Stilwell et al. 1997; Cullen et al. 2002) obsahující karboxylovou skupinu (-COOH) a karboxymethylcelulóza (Sannino et al. 2009) obsahující karboxymethylovou skupinu (-CH2COOH). Pro podobnost chemických názvů byly tyto dvě karboxylované celulózy občas i zaměňovány.
Karboxymethylcelulóza (CMC) je éter celulózy připravovaný např. karboxymethylací alkalizované celulózy kyselinou chloroctovou (viz obr. 1). K substituci může docházet na 2., 3. a 6. uhlíku základní jednotky celulózy (glukopyranózy). Teoreticky tak karboxymethylcelulóza může dosáhnout maximální hodnoty tzv. stupně substituce (DS) až 3,0.
1. Karboxymethylace celulózy – zjednodušené schéma reakce na C6 uhlíku 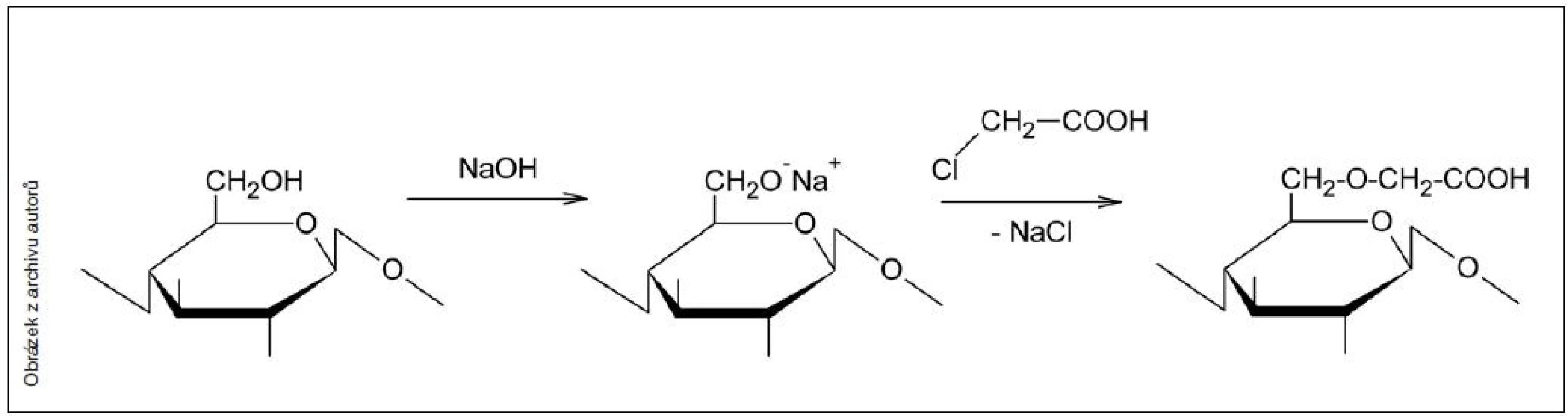
2. Oxidace celulózy – zjednodušené schéma oxidace glukopyranózové jednotky celulózy (předpokládající selektivní oxidaci C6 uhlíku) 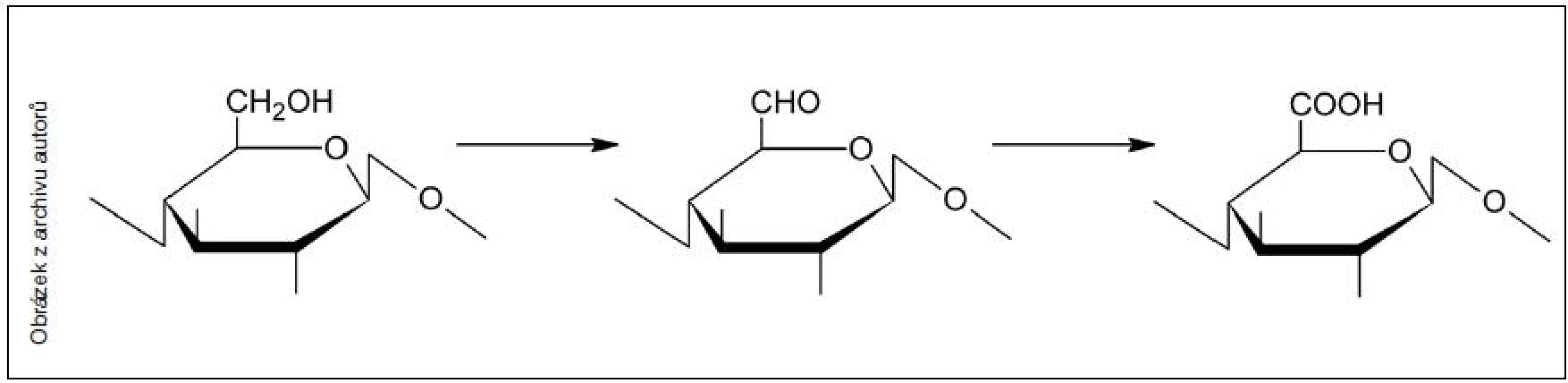
Proces přípravy karboxymethylcelulózy byl přihlášen k patentové ochraně poprvé v roce 1921 (Donohue 1922). Ve vodě rozpustnou CMC zavedla do výroby pro přípravu adheziv a detergentů poprvé německá společnost Henkel (www.henkel.com) a v roce 1946 americká firma Hercules prosadila CMC jako potravinářskou přísadu, např. zahušťovadlo (www.ashland.com). Sodnou sůl karboxymethylcelulózy lze v závislosti na molekulové hmotnosti a míře substituce připravit jako práškovitý produkt poskytující viskózní roztoky s tixotropním chováním nebo pseudoplastické roztoky z CMC s vyšší mírou substituce. Étery celulózy získávají široké uplatnění jako fyzikální vlastnosti modifikující činidlo ve farmacii, kosmetice, potravinářství, ale i v technických oblastech. Rozpustné formy CMC a dalších éterů celulózy dnes vyrábí v kapacitách nad 10 000 t/rok řada firem po celém světě.
Od padesátých let minulého století byl prováděn řadou společností (Kimberly Clark, DuPont, Asahi Chemicals, Kao Corp. aj.) výzkum použití karboxymethylované celulózy pro superabsorbenty (např. Burgeni et al. 1965) s předpokladem využití v hygienických materiálech (vložky). Prosadily se však levnější polyakryláty, které jsou dnes rovněž používané pro výrobu vysoce absorpčních krytí nebo hydrogelů pro hojení ran. Kyselá forma karboxymethylované celulózy jako poměrně málo známý produkt (Dieckman et al. 1953) se používá jako sorbent pro chromatografické kolony (www.whatman.com).
Oxidovaná celulóza byla poprvé připravena a začala se zkoumat ke konci třicátých let minulého století (Yackel et al. 1941; Wu et al. 2012). Podle amerického lékopisu (USP) obsahuje oxidovaná celulóza 16–24 % karboxylových (-COOH) skupin. Ve skutečnosti je složení a struktura oxidované celulózy složitější. Při oxidaci dochází k řadě vedlejších oxidačních reakcí a depolymerizaci celulózy (Newell and Zeronian 1985). Připravit oxidovanou celulózu jako materiál s nižší mírou degradace vhodný např. pro superabsorbenty se dosud nepodařilo.
Oxidovaná celulóza jako chirurgický hemostat a krytí pro ošetřování ran
Zásluhu na objevení oxidované celulózy pro medicínu má prof. V. K. Frantz (Frantz et al. 1944; Frantz et Lattes 1945), která v roce 1942 získala grant na vývoj hemostatických materiálů pro vojenské účely. Zjistila, že oxidací a hydrolýzou poškozená oxidovaná celulóza je při implantaci v tkáních živočichů vstřebatelná a navrhla aplikace, které se významnou měrou používají v chirurgii dodnes. Příčinou biodegradability a vstřebatelnosti oxidované celulózy není pouze snížení její molekulové hmotnosti hydrolýzou v průběhu oxidačního procesu, ale i oxidační poškození řetězce celulózy, tj. zejména přítomnost keto skupin (C=O) (obr. 3). Ty způsobují labilitu glukopyranózových jednotek oxidované celulózy v mírně alkalickém fyziologickém prostředí a její depolymerizaci na fragmenty o nižší hmotnosti reakčním mechanismem, tzv. beta-eliminací (Stephens et al. 2009; Dimitrijevich et al. 1990). Mechanismus biodegradace oxidované celulózy je tudíž založen na následujících stupních: I) solubilizace (gelovatění oxycelulózy); II) poměrně rychlá depolymerizace (beta-eliminace); III) enzymatické procesy (fagocytóza) likvidující zbytky celulózových fragmentů (Dimitrijevich et al. 1990). Při implantaci ve tkáních je oxycelulóza vstřebatelná během 1–3 týdnů, při aplikaci jako krytí ran se oxycelulóza vstřebává během 1–4 dnů.
3. Vedlejší produkty oxidace celulózy – keto skupiny, které jsou významnou příčinou nestability oxidované celulózy ve fyziologickém prostředí 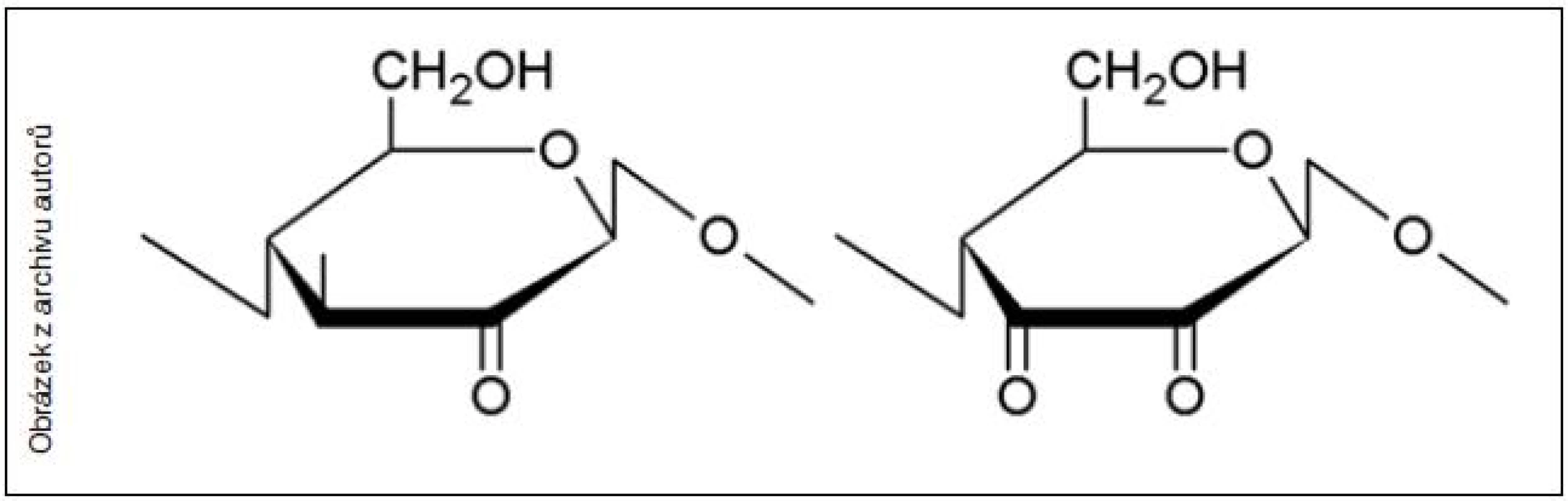
První komerční produkt – chirurgický vstřebatelný hemostat na bázi oxidované bavlny byl po válce Oxycel vyráběný firmou Eastman Kodak (později Eastman Chemical). Oxycel byl komercionalizován nejprve společností Parke, Davis & Co. a později Becton, Dickinson & Co. V padesátých a šedesátých letech minulého století prováděla firma Johnson & Johnson výzkum materiálů využitelných pro absorbovatelná hemostatika a implantáty. Karboxymethylovaná celulóza byla jedním z testovaných materiálů (Masci et Ashton 1959). Preferována byla tehdy nakonec oxidovaná celulóza. Technologie oxidace regenerované celulózy (viskózy) v organickém rozpouštědle (Stilwell et al. 1997) zajistila hebkost, stabilitu a homogenitu produktů Surgicel (Ethicon a) nebo Interceed (Ethicon b) a tím i dominantní postavení firmy Ethicon (Johnson & Johnson) na tomto trhu.
O vývoj oxidované celulózy se v průběhu let snažilo mnoho pracovišť na celém světě (např. Rusko, Francie, Itálie, Německo, Čína, Korea). Řada výrobců však svou činnost ukončila, takže po náhlém zastavení výroby Oxycelu okolo roku 2000 se společnost Johnson & Johnson stala nakrátko téměř monopolním výrobcem oxidované celulózy (zejména Surgicelu) s podílem na trhu více než 95 % a v hodnotě až 150 milionů USD/rok. V Evropě přežila česká firma Bioster s práškovými vápenatými solemi oxycelulózy řady Traumacel (www.traumacel.cz) a Borimed (www.borimed.com) s farmaceutickými přípravky a přípravky na hojení ran (Cysplacel, Linkocel, Ferancel).
4. Snímky z elektronového mikroskopu: oxidovaná regenerovaná celulóza připravená oxidací plynným N<sub>2</sub>O<sub>4</sub> v rozpouštědle (Surgicel) (vlevo) a oxidovaná bavlna připravená oxidací v kyselině dusičné a sírové (vpravo). U bavlny oxidované tradičním procesem v kyselinách je patrná degradace povrchových vrstev celulózy. 
České aktivity v oblasti oxidované celulózy byly tehdy limitovány nepříznivě dvěma faktory: „železnou oponou“ a dále i zvolenou koncepcí preferující práškové produkty (na rozdíl od textilních forem firmy Johnson & Johnson). Po roce 1986 byla vyvinuta pro ošetřování ran tzv. mikrodisperzní forma oxidované celulózy, m-doc (www.hemcon.com), která již neměla vláknitou strukturu celulózy. Nakonec se i v ČR prosadila koncepce plošných textilních materiálů využívajících to cenné, co celulóza od přírody má, tj. vláknitou strukturu celulózového polymeru. Shodou okolností se stalo, že v České republice je dnes největší koncentrace výrobců oxidované celulózy na světě (Bioster, Synthesia, Life Line a pro úplnost i Alltracel, který vznikl odchodem zaměstnanců z firmy Bioster (Alltracel je dnes součástí Hemcon Inc. – výrobce chitosanových hemostatik a krytí). Za pozornost v české historii oxycelulózy stojí práce prof. L. Bařinky – využití Traumacelu při chirurgické léčbě lymfedému (Bařinka 1984) ukázalo možnosti širšího uplatnění oxidované celulózy v hojení komplikovaných chirurgických ran.
O prosazení oxidované celulózy do segmentu ošetřování chronických ran se zasloužila opět firma Johnson & Johnson po roce 2002 výrobky řady Promogran (Systagenix a; Cullen et al. 2002). Jedná se o vstřebatelnou houbu připravenou lyofylizací kolagenu a oxidované regenerované celulózy. Bioaktivní krytí je charakterizováno jako proteázy modulující matrix (Systagenix b) pomáhající při kyselém pH snížit aktivitu proteolytických enzymů, jejichž nadbytek v chronické ráně je jedním z důvodů zpomalení hojení. Dalším produktem tohoto typu byly i produkty řady Traumacel Biodress na bázi částečně neutralizované hydrogenvápennaté soli oxidované celulózy. Ke konci roku 2008 firma Johnson & Johnson (Ethicon) překvapivě prodala segment ošetřování ran investiční společnosti One Equity Partners a vznikla společnost Systagenix (http://www.systagenix.com; http://www.jnj.com/connect/news/all/20081201_170000).
Karboxymethylovaná celulóza v ošetřování ran
V roce 1962 byl objeven princip vlhkého hojení ran (Winter 1962). První produkty na trhu byly v roce 1982 hydrokoloidy (hydrokoloidní krytí) (Queen 2010), konkrétně Granuflex nebo Duoderm (ConvaTec) a následně Comfeel (Coloplast). Hydrokoloidní krytí obsahují jako hlavní složku polymery tvořící ve vodě koloidní roztoky, tj. hydrokoloidy. To je obvykle karboxymethylcelulóza, pektin nebo želatina nebo další polymery. Krytí se často připravují i s podpůrnou fólií, např. z polyuretanu. Prosazování vlhkého hojení oproti tradičním obvazovým materiálům trvalo poměrně dlouhou dobu. Hydrokoloidy ale následně otevřely cestu dalším materiálům do revolučního oboru vlhkého hojení ran. Dnes se hydrokoloidy používají především pro slabě až středně exsudující rány bez infekce (obr. 5).
5. Použití hydrokoloidu na ráně 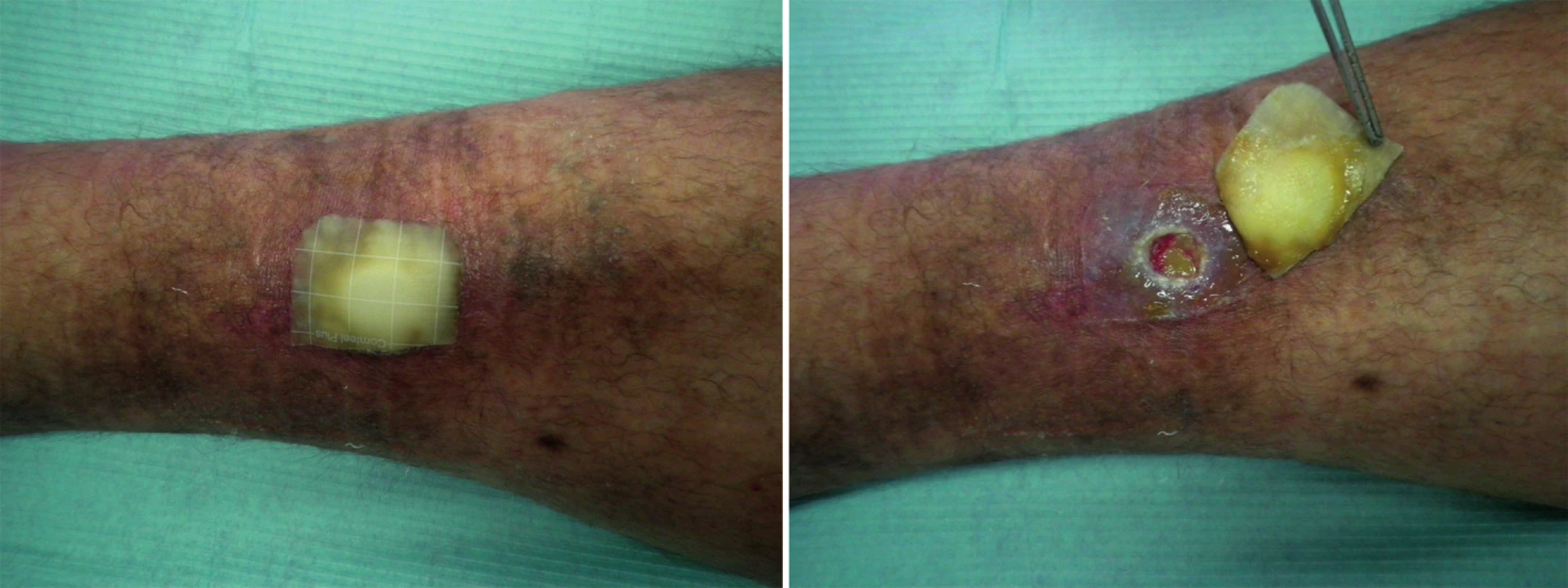
Další zlepšení CMC přinesla modifikovaná karboxymethylovaná celulózová vlákna, např. Super AB (Woodings 2001) a zejména Aquacel Hydrofibre od firmy ConvaTec (Walker et Parsons 2010; Queen 2010) (obr. 6). Hydrokoloidní vlákna jsou bobtnající až gelující celulózová vlákna, která jsou ve vlhkém stavu transparentní a mají gelovitou soudružnost. Nižší stupeň modifikace nenarušuje tolik významně vazebné interakce mezi celulózovými řetězci jako u roztoků CMC používaných pro výrobu hydrokoloidních krytí. Novým produktem na trhu je Durafiber od firmy Smith & Nephew (www.smith-nephew.com) (obr. 7), tvořící v kontaktu s exsudátem transparentní gel, který se nesráží. Durafiber zastupuje skupinu tzv. sulfonovaných derivátů celulózy. Je to netkaná textilie připravená ze směsi celulózy a ethylsulfonátu celulózy. Stejně jako Aquacel se Durafiber vyrábí i v podobě antimikrobiálního krytí se stříbrem.
6. Aquacel: (a) tvorba transparentního gelu v tlumivém roztoku fyziologickém, (b, c) vzhled krytí po sejmutí z rány 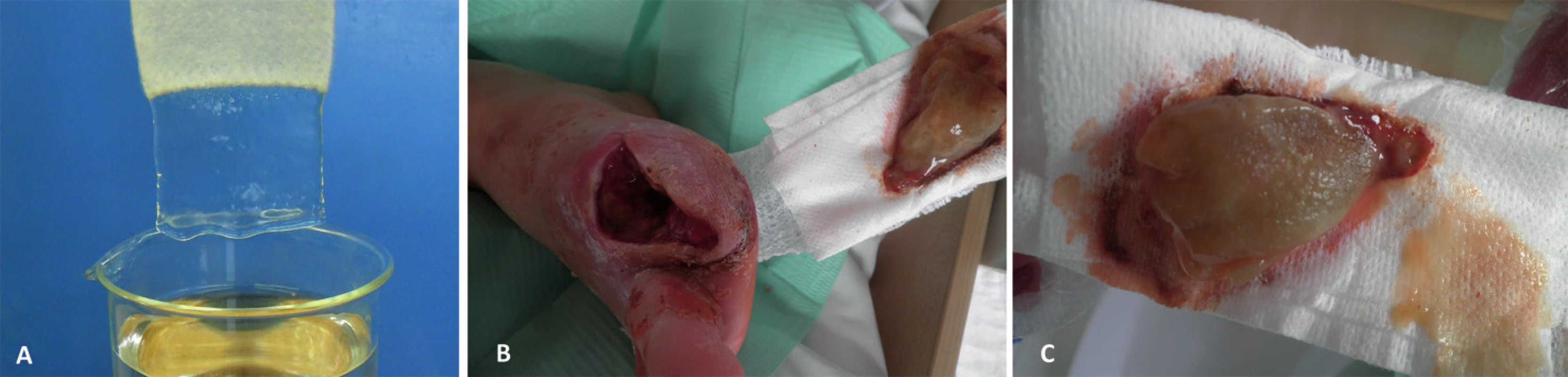
Hydrokoloidní vlákna nabízejí oproti tradičním hydrokoloidům následující výhody (Walker et Parsons 2010; Queen 2010):
- absorpční a retenční schopnost (sací mohutnost až 15–25 g/g);
- tvoří „hebký, hydrofilní gel“;
- propustnost pro plyny, ale bariéru vůči bakteriím;
- sequestrace a vázání bakterií (pasivní antimikrobiální účinek);
- zlepšené fyzikální vlastnosti (soudružnost) a snadnější odnímání krytí;
- vertikální nasávání a retence a snížení macerace okolí rány.
Hydrokoloidní krytí obsahující CMC i hydrokoloidní vlákna jsou nevstřebatelná. Později se i karboxymethylovaná celulóza uplatnila zásluhou čínských a následně amerických subjektů (www.actcel.com; McBee et Koerner 2005) v segmentu vstřebatelných hemostatik. Jedná se o produkty s vyšším stupněm modifikace, některé tyto produkty jsou částečně naoxidovanou karboxymethylcelulózou, což narušilo stabilitu celulózového řetězce (www.actcel.com; McBee et Koerner 2005). Tzv. biorozpustná hemostatika lze po aplikaci spláchnout vodou, což se využívá např. při ošetřování povrchových zranění.
Karboxymethylcelulóza si našla na rozdíl od oxidované celulózy rozsáhlé uplatnění jako pomocná látka ve farmacii a složka implantabilních materiálů pro chirurgii (Kamel et al. 2008; www.seprafilm.com; www.fziomed.com). Oxycelulóza se ve farmaceutických přípravcích prakticky neprosadila. Důvodem je podstatně užší rozsah možností derivatizace oxidované celulózy a omezení vyplývající z její stability a homogenity. Návrh společného využití obou látek na principu vláken oxidované celulózy zakomponované do hydrokoloidní matrice karboxymethylcelulózy je předmětem patentu (Silcock and Delbono 2007). Další materiály s vysokou absorpční a retenční schopností nabízejí kombinace CMC a alginátu obvykle se stříbrem (Beele et al. 2010; www.reliamedproducts.com).
Celulózové krytí Hcel
Do skupiny krytí karboxymethylovaných celulózových vláken s absorpčními vlastnostmi a schopností retence exsudátu patří i nové krytí na trhu Hcel (Podlaha et al. 2013; www.holzbecher.net), které vyrábí Holzbecher, spol. s r.o. barevna a bělidlo Zlíč (divize Holzbecher Medical) specializující se na výzkum a vývoj biokompatibilních materiálů, zejména na bázi karboxymethylace celulózy.
Krytí Hcel HT
Krytí spadá do vlhké terapie ran a rozšiřuje spektrum prostředků použitelných pro lokální ošetřování. Od jiných krytí z hydrokoloidních vláken se Hcel HT odlišuje tím, že bobtná postupně (24 hodin až 3 dny) a má hodnoty pH v kyselé oblasti, která je zachována po celou dobu aplikace (obr. 8).
8. Vlastnosti Hcel HT, Hcel NaT a bavlny při zkoumání in vitro 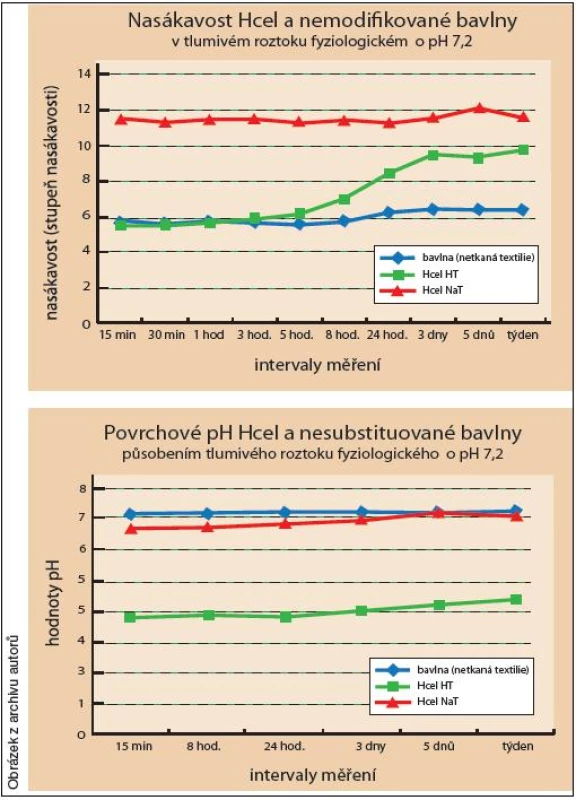
Krytí Hcel HT působí zmenšení ztrát bílkovin a eliminuje projevy infekce vybranými bakteriemi (P. aeruginosa, E. coli, S. aureus a K. pneumoniae s výjimkou kvasinky C. albicans). Je vhodné pro hojení povrchových akutních i chronických ran. Použití je možné u infikovaných ran, vředové choroby dolních končetin, chirurgických ran, traumatických ran, ran se sklonem ke krvácení a ran se sklonem k lymfatické sekreci (obr. 9). Unikátní vlastností krytí Hcel HT je, že je nedráždivé a proto je i dlouhodobě velmi dobře snášené. Během dosavadních klinických experimentů nedošlo k alergické reakci. Došlo ke zklidnění stavu a zvýšení komfortu v subjektivních pocitech u pacientů. Toto krytí zlepšuje a urychluje hojení. Po umístění krytí Hcel HT na plochu rány dochází k zástavě drobného krvácení a urychluje se hojení rány per secundam. Eliminací infekce je odstraněn zápach z ran. Krytí se dá použít i pro slabě secernující rány v kombinaci s navlhčením fyziologickým roztokem a to pouze nad oblastí rány.
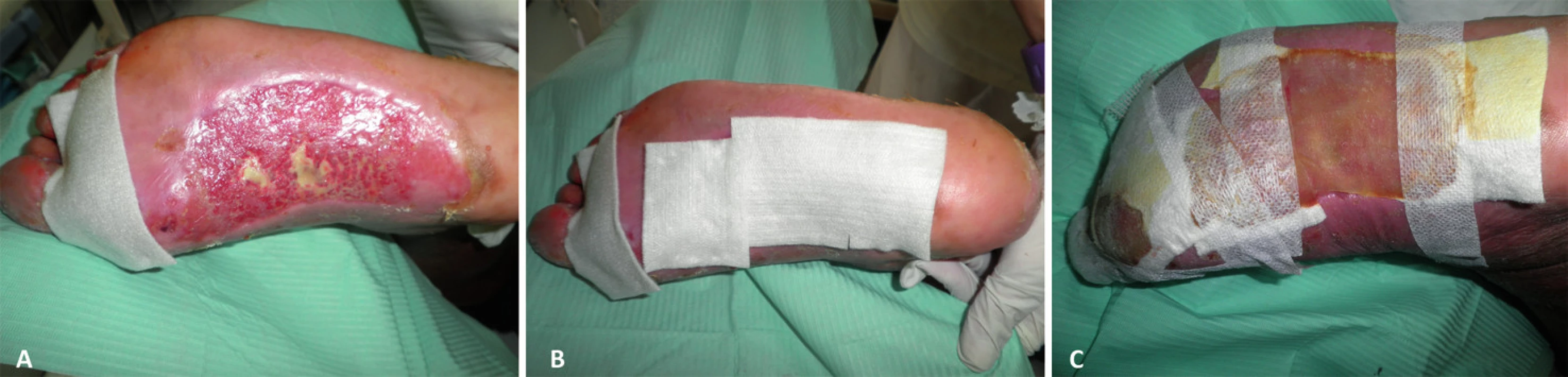
9. Komplikovaná postoperační rána léčená s použitím Hcel HT: (a) po vyčištění, (b) po dvou dnech před výměnou krytí, (c) po dvou dnech nové krytí, (d) vyhojený defekt 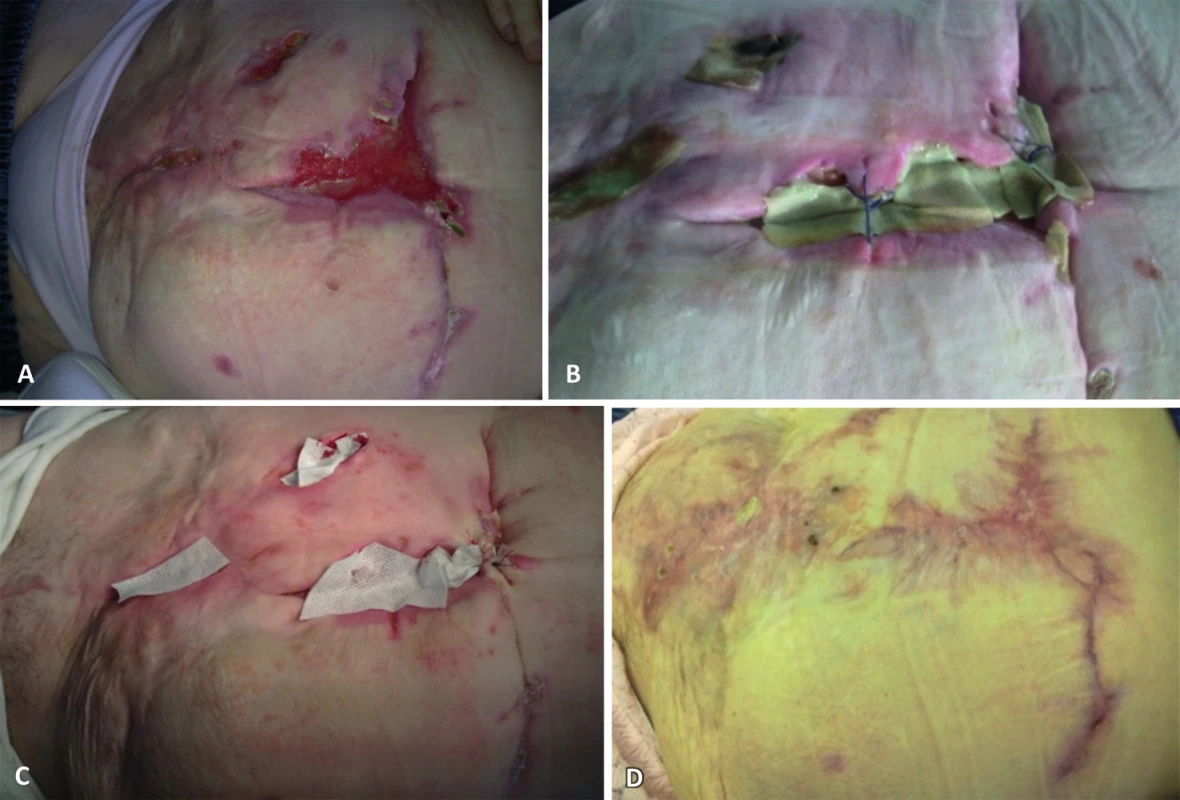
Krytí Hcel NaT
Jedná se o krytí s rychlou absorpcí exsudátu (obr. 8) vhodné pro více secernující rány a neinfikované rány (obr. 10). Od ostatních obdobných krytí se liší nižší sací mohutností (pod 15 g/g) a zlepšenou pevností materiálu.
10. Použití Hcel NaT na ráně: (a) rána před aplikací krytí, (b) krytí na ráně, (c) krytí po nasáknutí exsudátu, (d) vzhled stejné rány po 4 dnech aplikace Hcel NaT 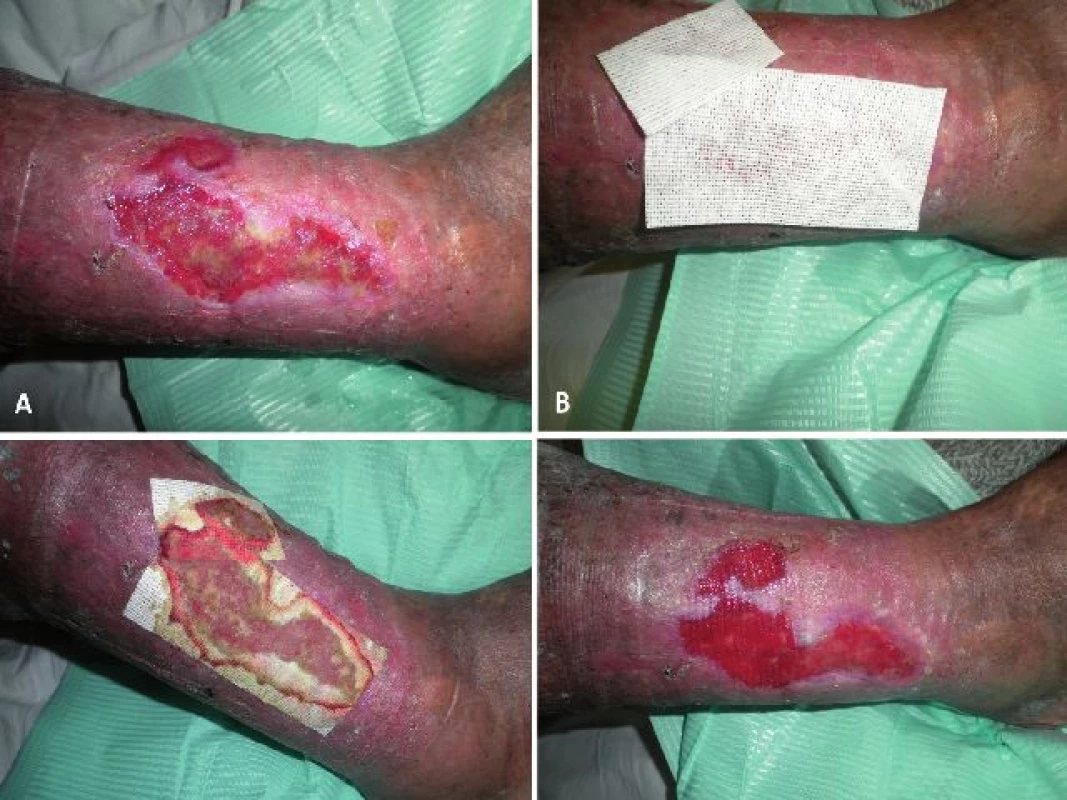
Oxidovaná celulóza a karboxymethylcelulóza (podobné a/nebo rozdílné mechanismy hojení ran)
Hojení ran (zejména chronických) představuje složitý proces, kde úkolem krytí je vytvoření optimálního prostředí pro léčení rány, tj. udržení vlhkého, teplého prostředí a optimálního pH, odstranění toxinů a mrtvé tkáně, absorpce bakterií a zajištění bariérové ochrany. I nepatrné rozdíly mezi jednotlivými chemicky totožnými materiály (např. u celulózy) mohou mít za následek vytvoření odlišného prostředí a tím i rozdílný účinek v hojení ran.
Oxidovaná celulóza se liší od karboxymethylcelulózy charakterem modifikace (oxidace vs. etherifikace) a molekulovou hmotností. Kyselá forma obou těchto derivátů celulózy je obvykle nerozpustná ve vodě. Sodná sůl oxidované celulózy, která ve vodě rozpustná je, nemá významné viskozitní vlastnosti. Prášková karboxymethylcelulóza naopak poskytuje viskózní roztoky ve vodě již při koncentraci 1–2 %. Oba polymery lze připravit jako biodegradabilní a vstřebatelné materiály. Karboxymethylcelulóza však potřebuje k dosažení vstřebatelnosti vyšší míru substituce (nad 0,6) a biodegradace probíhá odlišným mechanismem než u oxidované celulózy. Konečným metabolitem karboxymethylcelulózy v organismu živočichů je glukóza, u oxidované celulózy jsou to glukóza a kyselina glukuronová.
Oxidovaná celulóza má v důsledku nízkého pH (3,5) širokou antimikrobiální účinnost a je částečně cytotoxická. Naopak je dobře známo, že sodná sůl karboxymethylované celulózy (např. Aquacel) je inertní látka a působí především jako vlhké hojení (Stryja 2010; Sweeney et al. 2012). Antimikrobiální aktivitu vykazuje produkt se stříbrem (Aquacel Ag). Oxidovaná celulóza (Traumacel Biodress, Promogran) se charakterizuje jako bioaktivní krytí. Poněvadž se oxycelulóza poměrně rychle (1–4 dny) v ráně vstřebává, je nutné použít sekundární neadherentní vysoce absorpční krytí.
U Hcel HT (pH vodního výluhu cca 4,5) lze předpokládat uplatnění dvou principů podpory hojení: regulace aktivity proteolytických enzymů (obr. 11) a rovněž vytvoření vlhkého prostředí v ráně po celou dobu aplikace. Zajímavé je, že výsledná antimikrobiální aktivita Hcel HT a oxidované celulózy (Surgicel) vychází při klinickém testování srovnatelná (Touati et al. 2013), ačkoli by teoreticky (na základě srovnání testů in vitro) kyselejší oxidovaná celulóza (pH 3,5) měla dosahovat výrazně lepších výsledků. To naznačuje, že v klinické aplikaci se uplatňují různé mechanismy antimikrobiálního působení obou látek (v případě Hcel HT aktivní inhibiční i pasivní fyzikální – sorpční efekt). Tyto vlastnosti naznačují potenciál kyselých modifikovaných celulóz v prevenci infekcí při chirurgických infekcích (Touati et al. 2013) nebo prevenci post-operativních infekcí. Traumacel se může použít zejména u stagnujících ran k obnovení procesu hojení rány. Hcel HT navíc zajišťuje rovnoměrnou absorpci exsudátu a snižování pH chronické rány (obr. 12: Použití Traumacel nebo Hcel HT na ráně).
11. Vliv pH na aktivitu proteáz přítomných v chronické ráně (rozsah hodnot pH Hcel HT byl zjištěn při zkoumání in vitro na modelu rány) 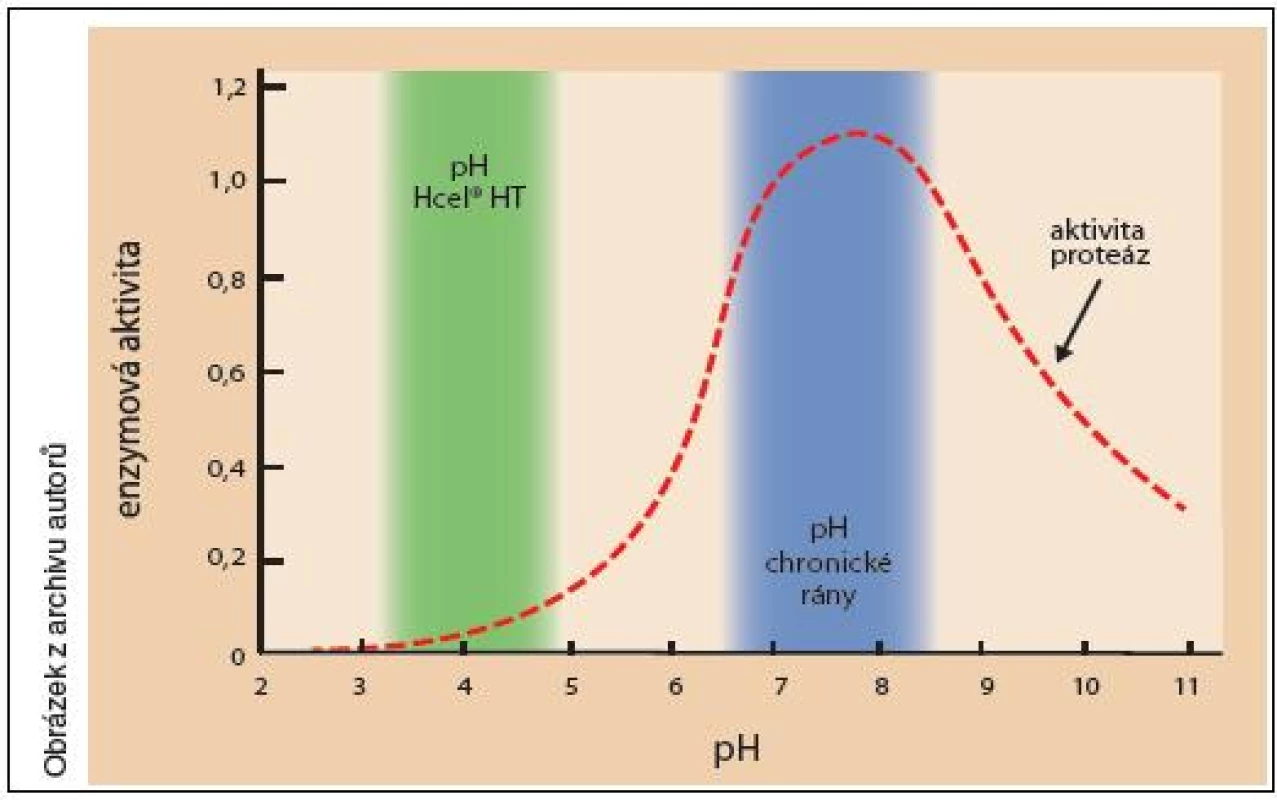
12. Oxycelulóza (Traumacel Biodress) (a) a Hcel HT (b – označeno šipkou) po 2 dnech na ráně. Krytí vedle Hcel HT je biokeramické krytí WoundEx (Batist Medical). 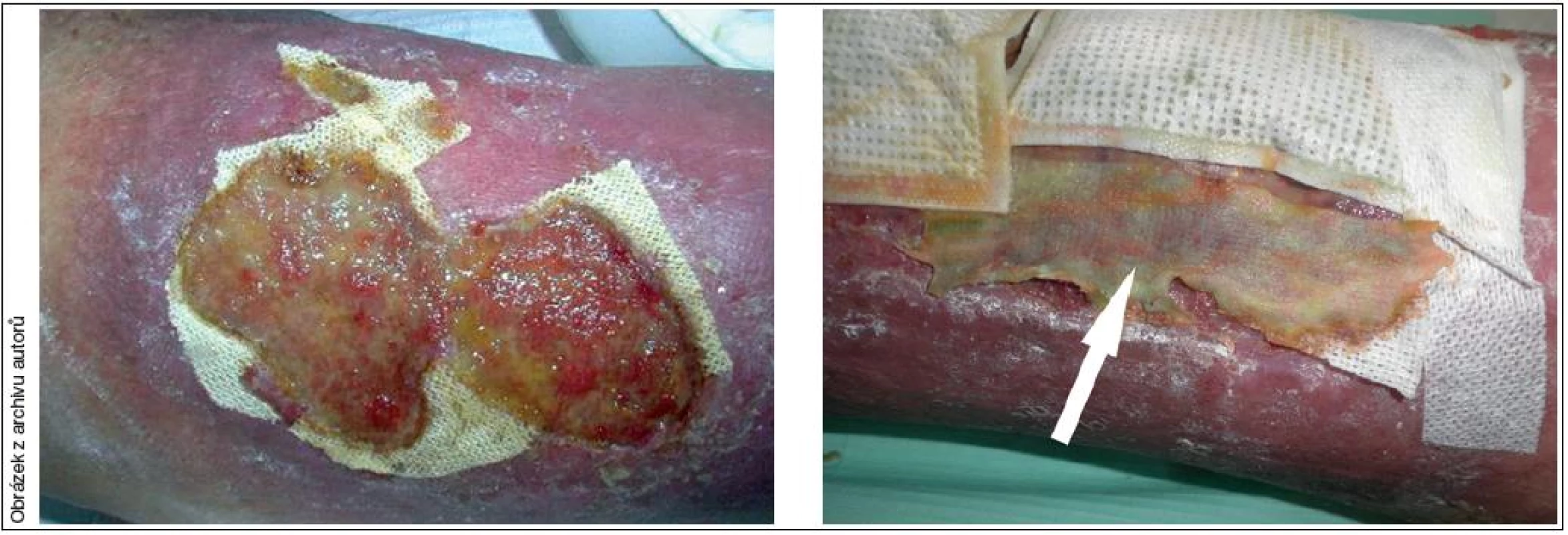
Závěr
Je nepochybné, že jak oxidovaná celulóza (např. Traumacel Biodress nebo Promogran), tak kyselá forma oxidované celulózy (Hcel HT) jsou „výjimečné“ látky. Ve své historii oxidovaná celulóza a karboxymethylcelulóza neustále umožňovaly a umožňují nové aplikace pro chirurgii a ošetřování ran. Studium vlastností obou látek jistě přinese řadu zajímavých poznatků z průběhu hojení zejména chronických ran a praktické využití těchto produktů. Jak se ukázalo v poslední době, pro aplikace celulózy a jejích derivátů je vhodné modifikovat především jejich povrchové vlastnosti (Mikulíková et al. 2008; Kolářová et al. 2013). Lze předpokládat, že tímto směrem by se mohl orientovat v příštím období základní i aplikovaný výzkum.
Autoři děkují za finanční příspěvek pro svoji práci TA ČR v rámci řešení projektu programu ALFA č. TA01010244 a GAČR v projektu P108/12/1168.
Tomáš Sopuch
Holzbecher, spol. s r.o.barevna a bělidlo Zlíč
552 03 Česká Skalice – Zlíč
e-mail: tomas.sopuch@holzbecher.net
Sources
Bařinka, L. Surgical treatment of lymphedema of the extremities. Acta Facultatis medicae Universitatis Brunensis 85 : 143–147, 1984.
Beele, H., Meuleneire, F., Nahuys, M., Percival, S. L. A prospective randomised open label study to evaluate the potential of a new silver alginate/carboxymethylcellulose antimicrobial wound dressing to promote wound healing. Int Wound J 7, 4 : 262–270, 2010.
Burgeni, A. A., Hills, S., Simkevich, J. C. Surgical absorbent pad having ion exchange properties. US 3187747, 1965.
Cullen, B., Smith, R., McCulloch, E. et al. Mechanism of action of PROMOGRAM, a protease modulating matrix, for treatment of diabetic foot ulcers. Wound Rep Regen 10, 1 : 16–25, 2002.
Dieckman, S. F., Jarrell, J. G., Voris, R. S. Carboxymethylcellulose in the free acid form. Ind Eng Chem 45 : 2287–2290, 1953.
Dimitrijevich, S. D., Tatarko, M., Gracy, R. W. et al. In vivo degradation of oxidized, regenerated cellulose. Carbohydr Res 198, 2 : 331–341, 1990.
Donohue, J. M. Process of making cellulose ethers. US 1415023, 1922.
Frantz, V. K., Clarke, H. T., Lattes, R. Hemostasis with absorbable gauze (oxidized cellulose). Ann Surg 120, 2 : 181–198, 1944.
Frantz, V. K., Lattes, R. Oxidized cellulose – absorbable gauze (cellulosic acid). J Amer Med Ass 129 : 798–801, 1945.
Gupta, B., Agarwal, R., Alam, M. S. Textile-based smart wound dressings. Ind J Fibre Textil Res 35 : 174–187, 2010.
Kamel, S., Ali, N., Jahangir, K. et al. Pharmaceutical significance of cellulose: A review. Express Polym Lett 2, 11 : 758–778, 2008.
Kolářová, K., Vosmanská, J., Rimpelová, S., Švorčík V. Effect of plasma treatment on cellulose fiber. Cellulose 20, 2 : 953–962, 2013.
Masci, J. N., Ashton, W. H. Absorbable carboxymethyl cellulose products. CA 586635, 1959.
McBee, W. L., Koerner, K. R. Review of hemostatic agents used in dentistry. Dent Today 24, 3 : 62–5, 2005.
Mikulíková, R., Švorčík, V., Náhlík, J., Sopuch, T., Havelka, P. Cytocompatibility of surface ground PE doped with calcium salt of 6-carboxycellulose. Cellulose 15, 3 : 473–481, 2008.
Newell, T. P., Zeronian, S. H. (eds.). Cellulose chemistry and its applications. New York: Halsted Press, John Wiley, 1985.
Podlaha, J., Horáková, M., Vytřasová, J., Moťková, P., Masteiková, R., Vinklárková, L., Sopuch, T. Hcel HT – nový typ celulózového krytí na ošetřování ran. Abstrakt z: Mezinárodní spolupráce při léčbě ran a kožních defektů. 24.–25.1.2013. Hojení ran 7, 1 : 26, 2013.
Queen, D. Technology update: Understanding Hydrofiber® Technology. Wounds Intern 1, 5 : 2010.
Sannino, A., Demitri, C., Madaghiele, M. Biodegradable cellulose-based hydrogels: Design and Applications. Materials 2, 2 : 353–373, 2009.
Silcock, D .W., Delbono, M. Hydrocolloid materials for use in wound healing. US 2007/0020318 A1.
Sopuch, T., Bureš, I., Milichovský, M., Švorčík, V. Celulózové materiály v ošetřování ran. Abstrakt z: Mezinárodní spolupráce při léčbě ran a kožních defektů. 24.–25.1.2013. Hojení ran 7, 1 : 24, 2013.
Stephens, C. H., Whitmore, P. M., Morris, H. R., Smith, T. Assessing the risks of alkaline damage during deacidification treatmentsof oxidized paper. J Am Inst Conserv 48, 3 : 235–249, 2009.
Stilwell, R. L., Marks, M. G., Saferstein, I., Wiseman, D. M. Oxidized cellulose: Chemistry, processing and medical applications. In: Domb, A. J., Kost, J., Wiseman, D. M. (eds.). Handbook of Biodegradable Polymers. Amsterdam: Harwood Academic Publishers, 1997.
Stryja, J. Porovnání efektivity léčby nehojících se ran krytím Aquacel a Traumacel Biodress: Závěrečná zpráva řešitele projektu. Hojení ran 4, 3 : 55–60, 2010.
Sweeney, I. R., Miraftab, M., Collyer, G. A critical review of modern and emerging absorbent dressings used to treat exuding wounds. Int Wound J 9, 6 : 601–612, 2012.
Touati, G., Barry, M., Cauet, H. et al. Antibacterial effect of modified cellulose: in vitro and clinical study potential applications in the prevention of surgical site infection. Abstrakta z: Mezinárodní spolupráce při léčbě ran a kožních defektů. 24.–25.1.2013. Hojení ran 7, 1 : 25–26, 2013.
Walker, M., Parsons, D. Hydrofiber® Technology: its role in exudate management. Wounds UK 6, 2 : 31–38, 2010.
Winter, G. D. Formation of the scab and the rate of epithelisation of superficial wounds in the skin of the young domestic pig. Nature 193 : 293–294, 1962.
Woodings, C. Regenerated cellulose fibres. Boca Raton: CRC Press, 2001.
Wu, Y., He, J., Cheng, W. et al. Oxidized regenerated cellulose-based hemostat with microscopically structure. Carbohydr Polym 88, 3 : 1023–1032, 2012.
Yackel, E. C., Kenyon, W. O. The oxidation of cellulose by nitrogen dioxide. J Am Chem Soc 64, 1 : 121–127, 1941.
Internetové zdroje
http://www.actcel.com/
http://www.ashland.com/Ashland/Static/Documents/AAFI/PRO-250-10H_Aqualon_CMC.pdf
http://www.borimed.com/
http://www.ethicon360.com/products/surgicel-family-absorbable-hemostats (Ethicon a)
http://www.ethicon360.com/products/gynecare-interceed-absorbable-adhesion-barrier (Ethicon b)
http://www.fziomed.com/core-science/
http://www.hemcon.com/Products/mdocproducts.aspx
http://www.henkel.com/about-henkel/company-history-11789.htm
http://www.holzbecher.net/
http://www.jnj.com/connect/news/all/20081201_170000
http://www.reliamedproducts.com/sellsheets/reliamed_silveralginate.pdf
http://www.seprafilm.com
http://www.smith-nephew.com/key-products/advanced-wound-management/durafiber/
http://www.systagenix.com/our-products/lets-promote/promogran-35 (Systagenix a)
http://www.systagenix.com/media/originals/20120402-125145-0028.pdf (Systagenix b)
http://www.traumacel.cz/
http://www.whatman.com/CationExchangeCelluloses.aspx
Labels
Surgery Nurse Home nurse
Article was published inWound Healing

2013 Issue 2-
All articles in this issue
- Antimicrobial prophylaxis in general surgery – results after one year using of standart
- Cellulose materials in the wound healing
- The complex regional pain syndrome in a wound treatment
- The use of plasma rich in thrombocytes in the wound healing – some new information and the first experience
- Perinatal traumatism
- The curiosities from the history of health care transportation I.
- A wound treatment in the intensive care from a physiotherapist’s point of view
- The importance of antimicrobial prophylaxis on urgent appendectomy
- Wound Healing
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- The complex regional pain syndrome in a wound treatment
- Perinatal traumatism
- Antimicrobial prophylaxis in general surgery – results after one year using of standart
- Cellulose materials in the wound healing
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career