-
Medical journals
- Career
Je potřeba stanovit frekvenci urodynamického vyšetření u pacientů postižených dysfunkcí dolních močových cest v důsledku roztroušené sklerózy?
Authors: G. Varga 1; D. Pacík 1; R. Wasserbauer 1; T. Pavlík 2; E. Janoušová 2; P. Praksová 3
Authors‘ workplace: Urologická klinika LF MU a FN Brno 1; Institut biostatistiky a analýz, LF a PřF MU, Brno 2; Neurologická klinika LF MU a FN Brno 3
Published in: Urol List 2014; 12(3): 21-31
Overview
Příznaky dolních močových cest v důsledku neurogenní dysfunkce dolních cest močových (NDMC) patří mezi symptomy, které nejvíce obtěžují pacienty s roztroušenou sklerózou (RS). Pokud nejsou léčeny správně, mohou způsobit ireverzibilní změny dolních i horních močových cest. NDMC mohou také zhoršit průběh samotné RS a tím i celkového zdravotního postižení. Současné doporučení vytvořené ICS a EAU pro sledování pacientů s NDMC je koncipováno pouze obecně pro pacienty postižené jakýmkoli neurologickým postižením, ne však pro pacienty s RS. Naše klinické pozorování naznačovalo zhoršování NDMC u pacientů s RS v návaznosti na dynamickou progresi demyelinizačního onemocnění. Cílem prospektivní kontrolované studie bylo zhodnotit parametry urodynamického vyšetření u pacientů s RS v časové ose a vytvořit případně doporučení dispenzarizace pro klinickou praxi.
Klíčová slova:
urodynamické vyšetření, neurogenní dysfunkce dolních močových cest, roztroušená sklerózaÚvod
Roztroušená skleróza (RS) je chronické zánětlivé onemocnění centrálního nervového systému (CNS), které vede jak k demyelinizaci nervových vláken, tak k jejich přímé ztrátě. Toto záludné onemocnění je v naší zeměpisné šířce nejčastější (!) příčinou invalidity mladších věkových skupin z neurologických příčin. Na celém světě postihuje 2,5 milionu lidí. RS je dnes jednoznačně řazena mezi autoimunitní zánětlivé onemocnění, přičemž cílovými antigeny pro autoimunitní agresi jsou antigeny myelinové pochvy, která obaluje nervová vlákna CNS [1]. Onemocnění je charakterizováno vznikem mnohočetných zánětlivých ložisek v bíle hmotě CNS. Jedná se o složitý autoimunitní proces iniciovaný autoagresivními T lymfocyty proti myelinovým antigenům. Dochází tím k aktivaci celé kaskády imunitních dějů s multicelulární účastí a s produkcí mnoha cytokinů a chemokinů, které vedou k poškození myelinu [1].
Podle průběhu dělíme RS na typy [1]:
- Remitentní‑relabující (80 – 85 % pacientů): onemocnění probíhá v atakách a následných remisích. Období remise může být bezpříznakové, pokud ataka nezanechala neurologický deficit. Polovina pacientů během prvních deseti let onemocnění přejde do sekundárně progresivního stadia.
- Sekundárně progresivní: dochází k pozvolnému nárůstů neurologického deficitu, většinou již trvalého charakteru s relapsy, nebo bez nich, které již nemají tak dramatický průběh jako u remitentního typu.
- Primárně progresivní (10 – 15 % pacientů): již od samého počátku je patrný pozvolný nárůst neurologického deficitu s dominující centrální (spastickou) paraparézou dolních končetin a častějším výskytem u mužů kolem 40. roku věku.
- Klinicky izolovaný syndrom (CIS): první ataka, která je na základě paraklinických vyšetření (magnetická rezonance, vyšetření likvoru) podezřelá z budoucího rozvoje RS.
I když se tzv. plaky demyelinizace mohou vyskytovat kdekoli v CNS, predilekční oblasti je cervikální segment míšní a hlavně laterální kortikospinální a retikulospinální trakty, které se podílejí na inervaci svaloviny močového měchýře a vnějšího svěrače uretry [2,3]. Poškozením těchto drah dochází u pacientů s RS k rozvoji neurogenně podmíněných dysfunkcí dolních močových cest (NDMC). Péče o pacienty s NDMC představuje jednu z nejobtížnějších oblastí urologické praxe [4]. Výsledný typ dysfunkce dolních močových cest poté závisí hlavně na lokalizaci a rozsahu neurologické leze v CNS. Cílem neurologické a urologické veřejnosti je proto snaha najít vhodnou strategii pro zhodnocení onemocnění, která by byla jakýmsi vodítkem plánování adekvátního postupu léčby a péče o pacienta s RS [3,5].
Cíle práce
Klinické pozorování naznačovalo zhoršování dysfunkce dolních močových cest (DMC) u pacientů s roztroušenou sklerózou (RS) v návaznosti na dynamickou progresi demyelinizačního onemocnění. Cílem šestileté prospektivní, kontrolované studie bylo zhodnotit výsledky urodynamického (UD) vyšetření u pacientů s RS v časové ose a vytvořit případné doporučení pro klinickou dispenzarizační péči.
Práce vycházela z nulových hypotéz:
- Parametry UD vyšetření u pacientů postižených RS nejsou odlišné od pacientů postižených jiným stabilizovaným neurologickým onemocněním.
- Parametry UD vyšetření nebo stanovená UD diagnóza u pacientů postižených RS, a to celkově i v závislosti na formě RS, se v čase nemění, a jsou tedy stabilní.
Pokud by se parametry nebo UD diagnóza signifikantně měnily v čase v důsledku progrese neurologického nálezu při RS, bylo by nutné stanovit doporučení pro klinickou praxi z hlediska dispenzarizace a frekvence UD měření u této skupiny pacientů s cílem včasné korekce léčby neurogenní dysfunkce DMC.
Metody
Od září 2007 do srpna 2013 bylo z původně zvažovaných 134 pacientů s roztroušenou sklerózou (RS) zahrnuto 74 pacientů (54 žen, 20 mužů, remitentní (R) forma 34 pacientů, sekundárně progresivní (SP) forma 34 pacientů, primárně progresivní (PP) forma 6 pacientů) s klinickými známkami dysfunkce DMC. Průměrný věk pacientů byl 51,5 let (tab. 1). Pacienti, kteří splňovali kritéria pro zařazení do studie, podstoupili po podepsání informovaného souhlasu urodynamické vyšetření (PQ studii nebo gynekologickou studii). V tab. 2 jsou uvedena vstupní i vylučovací kritéria pro zařazení pacientů s RS do studie.
Table 1. Sumarizace věkového složení pacientů s RS, kontrolních subjektů a pacientů dle typu roztroušené sklerózy (v letech). Věk byl vztažen ke dni prvního urodynamického vyšetření. 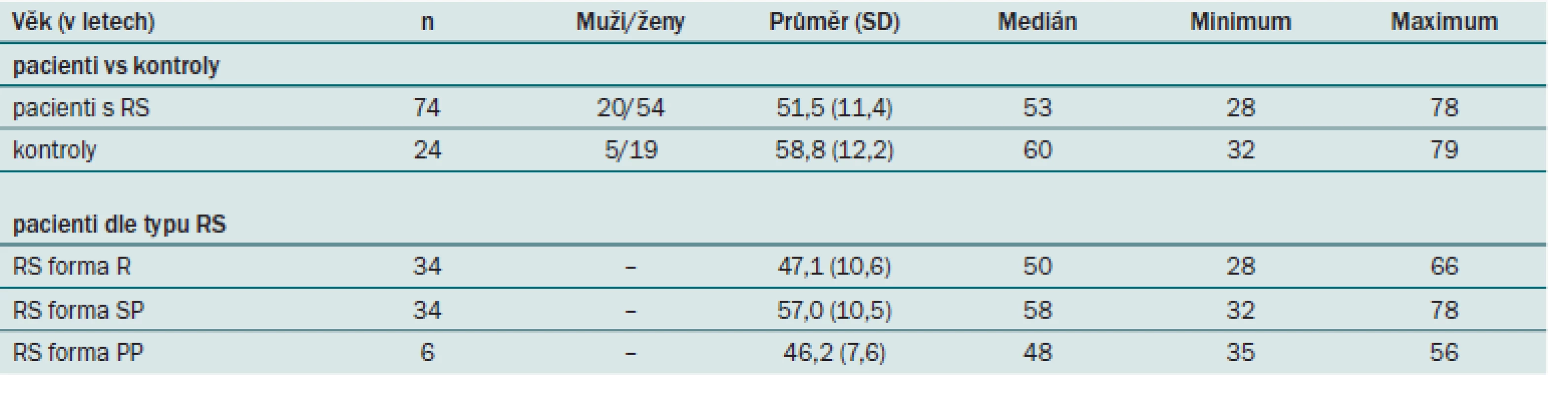
Table 2. Vstupní a vylučovací kritéria pro výzkumnou skupinu pacientů s RS. 
Kontrolní skupina 24 subjektů (19 žen, 5 mužů) byla tvořena pacienty, kteří měli mezi dvěma UD měřeními v průběhu ročního sledování stabilní neurologicky nález. Jednalo se o pacienty postižené jiným typem neurologického onemocnění než demyelinizační onemocnění typu RS. UD měření v tomto kontrolním souboru proběhlo v 0. měsíci (UD 1) a ve 12. měsíci (UD 4). Složení kontrolní skupiny je uvedeno v grafu 1. V tab. 3 jsou uvedena vstupní a vylučovací kritéria.
Table 3. Vstupní a vylučovací kritéria pro kontrolní skupinu pacientů. 
Graph 1. Složení kontrolní skupiny s neurogenní dysfunkcí DMC podle typu neurologického postižení. 
Materiál
UD vyšetření bylo prováděno pomocí urodynamického přístroje SOLAR® s využitím dvojcestného nebo trojcestného katetru T ‑ DOC pro měření Pves, Pabd a Pura. Každý pacient byl deset dnů před termínem měření telefonicky požádán o vysazení léků ovlivňujících funkci DMC. Tento fakt byl zohledněn i při preskripci léků tak, aby počet předepsaných tablet doužíval pacient minimálně deset dnů před dalším měřením.
Graph 2. Srovnání výskytu inkontinence u pacientů s RS a kontrolních subjektů v jednotlivých UD vyšetřeních: pomocí sloupcového grafu je zobrazen vývoj výskytu inkontinence u kontrolních subjektů v 0. a 12. měsíci (UD 1 a 4) a pa cientů s RS v 0., 4., 8. a 12. měsíci (UD 1–4). 
Metodika sběru dat
Pacienti s RS podstoupili UD měření v 0., 4., 8. a 12. měsíci (UD 1, UD 2, UD 3, UD 4), pacienti kontrolní skupiny v 0. a v 12. měsíci (UD 1, UD 4). Před každým vyšetřením proběhlo biochemické a mikroskopické vyšetření moči s cílem vyloučit infekci močových cest. Pacient byl před každým vyšetřením požádán o vyprázdnění měchýře. Postmikční reziduum bylo hodnoceno pomocí ultrazvukového vyšetření. Případná zbytková moč byla před každým vyšetřením vycévkována za aseptických kautel. Do rektální ampuly byl zaveden T ‑ DOC katetr pro měření intraabdominálního tlaku (Pabd). Transuretrálně byl do močového měchýře zaveden dvojcestný (v případě PQ studie) nebo trojcestný T ‑ DOC katetr (v případě gynekologické studie). Koncovky katetrů byly odpovídajícím způsobem napojeny na tlakové snímače UD přístroje SOLAR® a posléze všechny kanály byly kalibrovány tak, aby výchozí hodnota Pdet byla 0 cm H2O. Infuzní pumpa byla standardně nastavena na rychlost 50 ml/ min u všech pacientů a teplota infuzního roztoku (0,9% NaCl) byla standardně 37 °C. Vyšetření probíhalo u všech pacientů bez výjimky v poloze vleže. Mikce probíhala u žen vsedě, u mužů ve stoje do uroflowmetru. Průtokové parametry byly hodnoceny jako signifikantní jenom v případě, že mikční objem byl více než 125 ml. Výsledky UD vyšetření byly hodnoceny dvěma erudovanými lékaři, kteří stanovili i definitivní UD diagnózu.
Kvalita života pacientů s RS byla hodnocena pomocí validovaného dotazníku ICIQ ‑ SF (International consultation on incontinence questionnaire – short form), který je doporučován Mezinárodní urologickou společností pro vyšetřování pacientů s močovou inkontinencí [6]. Dotazník byl vyplněn před vstupním vyšetřením a poté před každým kontrolním vyšetřením ve 4., 8. a v 12. měsíci, přičemž výsledek odrážel stav kvality života při zavedené léčbě. Vyšší hodnota výsledného skóre ICIQ ‑ SF odráží horší kvalitu života v souvislosti s močovou inkontinencí, naopak hodnota 0 je odrazem ideálního stavu bez inkontinence.
Metodika statistického hodnocení
Předmětem výzkumu bylo zhodnocení kategoriálních a spojitých parametrů urodynamického vyšetření (tab. 4) u pacientů postižených RS a také u kontrolní skupiny pacientů postižených jiným neurologickým onemocněním. Z kategoriálních parametrů jsme v průběhu vyšetření UD 1–4 hodnotili přítomnost, resp. nepřítomnost hyperaktivity detruzoru, poruchy kontraktility v mikční fázi, výskyt močové inkontinence uváděný pacientem, typ urodynamické diagnózy (UD dg), případně výskyt evakuace měchýře pomocí čisté intermitentní katetrizace (ČIK).
Table 4. Kategoriální a spojité parametry UD vyšetření, které byly předmětem hodnocení. 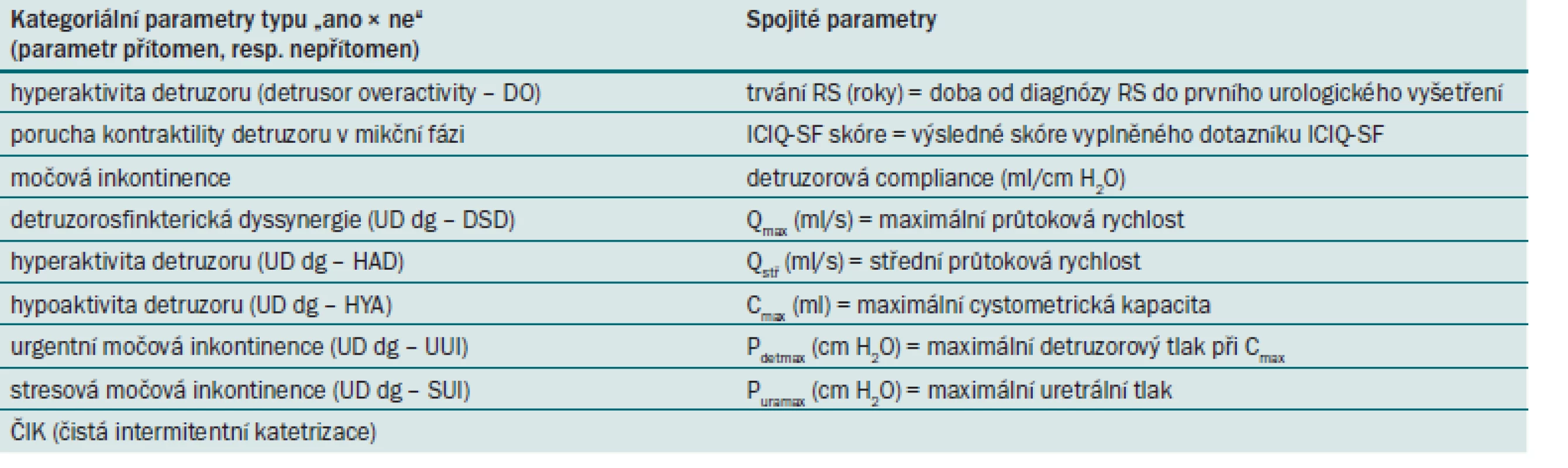
Pro sumarizaci sledovaných spojitých charakteristik (trvání RS, ICIQ ‑ SF skóre, detruzorová compliance, Qmax, Qstř, Cmax, Pdetmax, Puramax) byla použita popisná statistika, tedy průměr, medián, minimum a maximum. Kategoriální charakteristiky (detruzorová hyperaktivita, porucha kontraktility, ČIK, typ UD diagnózy, ne/ přítomnost inkontinence) byly popsány pomocí četnosti jednotlivých skupin a procentuálního zastoupení. Proměnná UD dg byla před zahájením analýzy převedena na pět proměnných typu „ano × ne“ (např. proměnná „UD dg – DSD“ ukazuje, zda byla, nebo nebyla přítomna diagnóza DSD).
Pro srovnání spojitých charakteristik v 0. a 12. měsíci a jejich změn u pacientů a kontrolních subjektů byl použit Mannův ‑ Whitneyho test. V případě srovnání spojitých charakteristik u pacientů s různou formou RS byl použit Kruskalův ‑ Wallisův test, a to pro všechna hodnocení, tedy v 0., 4., 8. i 12. měsíci. Protože pacientů s chronickou progresivní formou RS bylo pouze šest, bylo srovnání stejných charakteristik a jejich změn provedeno také s vyloučením této skupiny, tedy pouze mezi pacienty s remitentní a sekundárně progresivní formou RS, a to pomocí Mannova ‑ Whitneyho testu. Změny ve spojitých charakteristikách byly počítány jako rozdíl mezi hodnotami v 0. a 12. měsíci, kdy kladná hodnota změny odpovídá snížení hodnoty spojitého parametru po roce, záporná hodnota změny ukazuje zvýšení hodnoty daného parametru po roce od prvního vyšetření. Změny byly počítány a následně hodnoceny pouze pro ty kontrolní subjekty a pacienty, kteří měli vyplněné obě hodnoty v 0. a 12. měsíci bez ohledu na průběžné UD vyšetření. Dále bylo provedeno hodnocení změny spojitých charakteristik v čase (po roce) zvlášť pro všechny pacienty, pacienty s remitentní (R forma RS) a sekundárně progresivní formou RS (SP forma RS) a kontrolní subjekty pomocí Wilcoxonova párového testu. Srovnání kategoriálních charakteristik (typu „ano × ne“ i parametrů s více kategoriemi) bylo provedeno pomocí Fisherova exaktního testu mezi pacienty a kontrolními subjekty v 0. a 12. měsíci, mezi jednotlivými formami RS pak v 0., 4., 8. i 12. měsíci.
Pro grafické znázornění vývoje spojitých charakteristik v čase a srovnání mezi jednotlivými skupinami (kontrolní subjekty vs RS pacienti, R forma vs SP forma vs PP forma RS) byly použity krabicové grafy využívající tyto statistiky: medián, 25% a 75% percentil, minimum a maximum. Srovnání výskytu inkontinence (tedy kategoriální charakteristiky typu ano × ne) v jednotlivých UD vyšetřeních je graficky znázorněno pomocí sloupcových grafů, a to jak pro kontrolní subjekty a všechny pacienty, tak pro jednotlivé skupiny pacientů dle typu roztroušené sklerózy.
Hodnocení změn v kategoriálních charakteristikách typu „ano × ne“ (tzn. výskytu jednotlivých diagnóz) po roce od začátku studie bylo provedeno pomocí McNemarova testu zvlášť pro kontrolní subjekty, všechny pacienty a také pro pacienty s jednotlivými formami RS. Pracovali jsme s hladinou významnosti 5 %.
Výsledky
Srovnání vstupního vyšetření u pacientů s RS a kontrolních subjektů podle pohlaví
Protože naším záměrem nebyla evaluace fyziologických hodnot, ale naopak patologických hodnot u pacientů s RS, hodnotili jsme po splnění vstupních a vylučovacích kritérií muže i ženy jako jeden celek. Vstupní srovnání kategoriálních i spojitých charakteristik mezi muži i ženami s RS neprokázalo statisticky významný rozdíl (tab. 5 a 6), což znamená, že obě skupiny pacientů byly na vstupu srovnatelné, kromě výskytu detruzorosfinkterické dyssynergie (DSD). Tento byl podle Fisherova exaktního testu významně vyšší u mužů postižených RS (19 mužů (86,4 %) vs 29 žen (55,8 %); p = 0,016). Ani výsledky srovnání vstupních parametrů kontrolní skupiny neprokázaly, že by se ženy a muži patřící do kontrolní skupiny mezi sebou na vstupu v jednotlivých parametrech UD vyšetření statisticky významně odlišovali. Tento fakt však může být ovlivněn i nízkým počtem mužů zahrnutých do skupiny kontrolních jedinců.
Table 5. Srovnání spojitých parametrů při vstupním vyšetření v 0. měsíci u pacientů s roztroušenou sklerózou podle pohlaví. 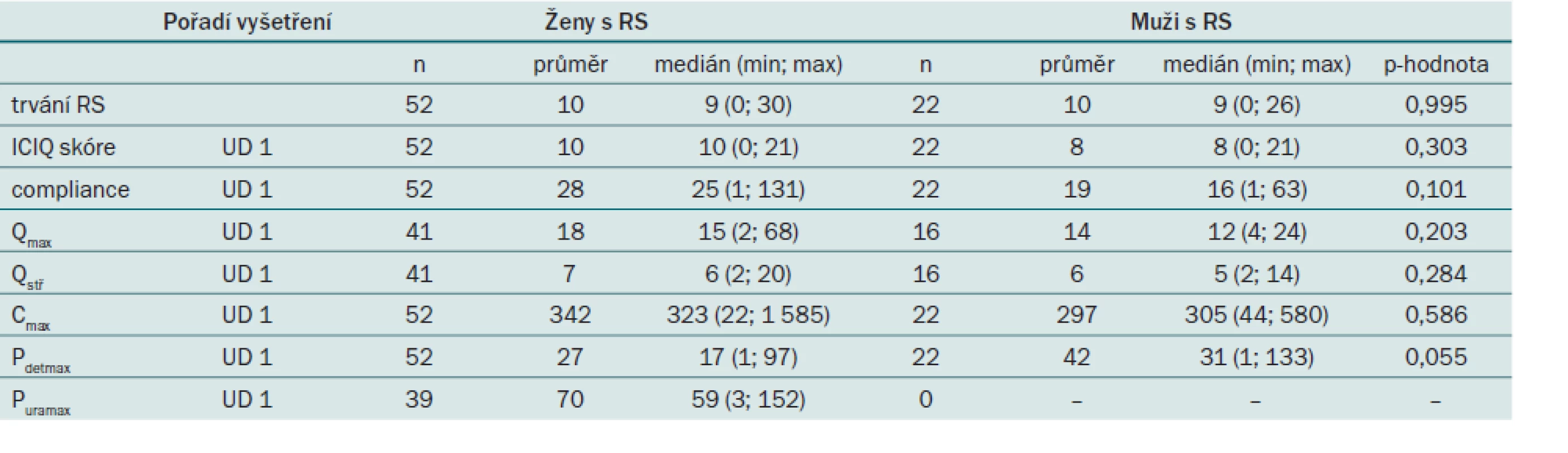
Table 6. Srovnání kategoriálních charakteristik typu „ano × ne“ u pacientů s RS podle pohlaví. 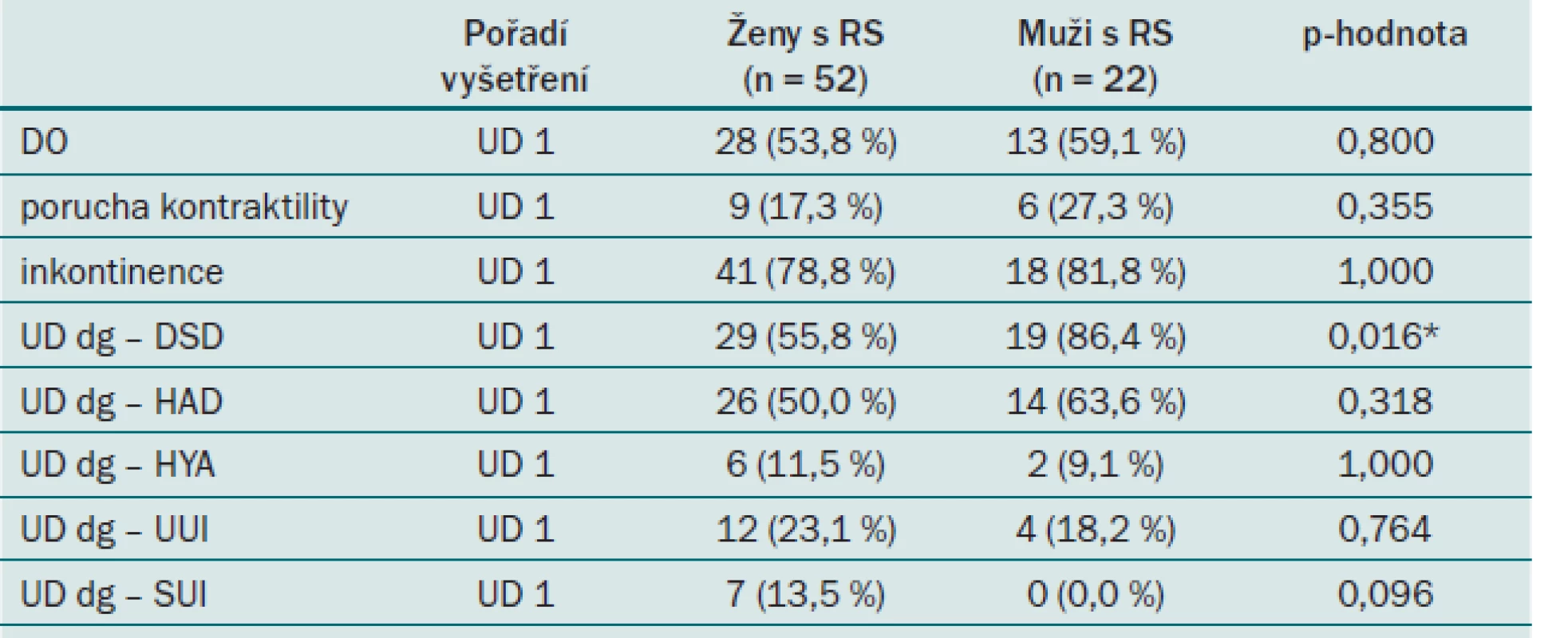
*Statisticky významný rozdíl na hladině významnosti 0,05. Ani výsledky srovnání vstupních parametrů kontrolní skupiny neprokázaly, že by se ženy a muži patřící do kontrolní skupiny mezi sebou na vstupu v jednotlivých parametrech UD vyšetření statisticky významně odlišovali. Tento fakt však může být ovlivněn i nízkým počtem mužů zahrnutých do skupiny kontrolních jedinců.
Popisná sumarizace sledovaných parametrů UD měření
Tab. 7 sumarizuje kategoriální charakteristiky typu „ano × ne“ pro přítomnost, resp. nepřítomnost daného parametru v průběhu UD vyšetření 1–4, tedy v 0., 4., 8. a 12. měsíci u obou sledovaných skupin pacientů (pacienti s RS i kontrolní skupina). V tabulce je u každé charakteristiky uveden počet a procentuální zastoupení subjektů s hodnotou „ano“, sumarizující fakt, že uvedený znak byl v průběhu vyšetření zaznamenán. Procentuální zastoupení pacientů s hyperaktivitou detruzoru (DO) zaznamenanou v průběhu UD vyšetření (resp. plnicí cystometrie) koreluje i s výskytem urodynamické diagnózy neurogenně podmíněné hyperaktivity detruzoru (UD dg HAD).
Table 7. Sumarizace kategoriálních charakteristik typu „ano × ne“. Např. první řádek tabulky ukazuje, že při prvním vyšetření mělo detruzorovou hyperaktivitu při plnící cystometrii zaznamenanou 15 z 24 kontrolních subjektů (tzn. 62,5 % kontrolních subjektů) a 41 ze 74 pacientů s RS (55,4 % pacientů). 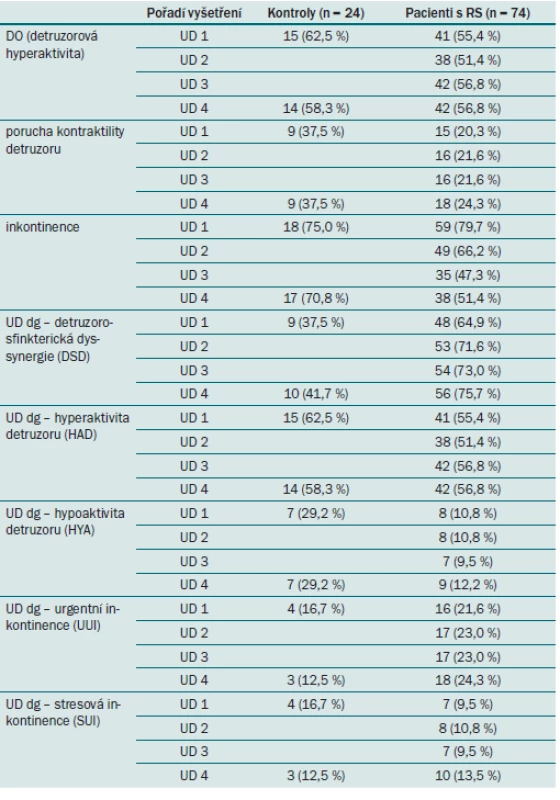
Sumarizace spojitých charakteristik UD vyšetření ve výzkumné skupině i u kontrol je uvedena v tab. 8. Průměrná doba trvání RS od stanovení diagnózy do prvního urologického vyšetření byla deset let, medián délky trvání byl devět let (rozsah 0,08 – 30 let). Vzhledem k zaokrouhlování na celé roky je minimum délky trvání RS v tabulce rovno 0. Průtokové parametry Qmax a Qstř byly hodnoceny jen u pacientů, kteří byli schopní mikce v rámci měření, tj. mikční objem dosahoval více než 125 ml. Puramax byl hodnocen pouze u žen v případě, že byla prováděna profilometrie uretry ke zhodnocení případné stresové inkontinence.
Table 8. Sumarizace spojitých parametrů UD vyšetření: skóre ICIQ-SF, detruzorová compliance, maximální a střední průtoková rychlost Q<sub>max</sub> a Q<sub>stř,</sub> maximální cystometrická kapacita měchýře C<sub>max</sub>, maximální detruzorový tlak P<sub>detmax</sub> dosažený na konci plnící fáze a maximální uretrální tlak P<sub>uramax</sub>. Popis jednotlivých parametrů je uvedený v tab. 4. 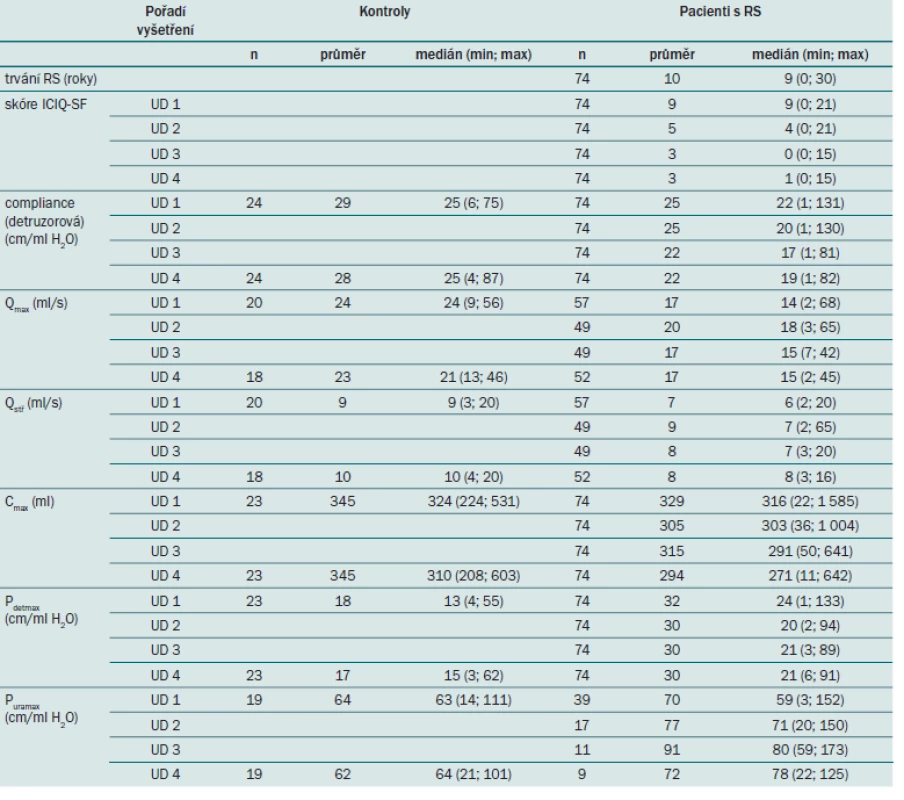
Výsledky statistického srovnání pacientů s RS a kontrolní skupiny
1. Srovnání spojitých parametrů UD 1 a UD 4 (v 0. a 12. měsíci)
Při srovnání parametrů UD vyšetření mezi výzkumnou a kontrolní skupinou pacientů jsme dospěli k závěru, že pacienti s RS mají oproti kontrolním subjektům statisticky významně nižší jak maximální průtokovou rychlost (Qmax), tak i střední průtokovou rychlost (Qstř), zatímco maximální detruzorový tlak (Pdetmax) dosažený při cystometrické kapacitě (Cmax) je u pacientů s RS vyšší (tab. 10). V uvedených charakteristikách byl zaznamenán statisticky významný rozdíl mezi pacienty a kontrolami jak při vstupním UD 1 v 0. měsíci, tak při UD 4 ve 12. měsíci.
Významně nižší průtokové parametry u pacientů s RS nelze vysvětlit sníženou kontraktilitou detruzoru v mikční fázi, protože procento jejího výskytu bylo naopak vyšší v kontrolní skupině v 0. i ve 12. měsíci (37,5% výskyt snížené kontraktility u kontrolních subjektů při UD 1 a UD 4 vs 20,3% a 24,3% výskyt u pacientů s RS; tab. 7). Byl však zaznamenán signifikantně vyšší výskyt DSD u pacientů s RS oproti kontrolní skupině při UD 1 i UD 4 na hladině významnosti p = 0,031 při UD 1, resp. 0,005 při UD 4 (blíže tab. 9). Právě tomuto faktu lze přičíst možný podíl na snížení (zhoršení) výtokových parametrů oproti kontrolní skupině, kde jsou výtokové parametry vyšší, ale výskyt DSD méně častý.
Table 9. Srovnání výskytu kategoriálních charakteristik typu „ano × ne“ mezi pacienty a kontrolními subjekty v 0. a 12. měsíci (UD 1 a UD 4). Popis jednotlivých parametrů je uvedený v tab. 4. 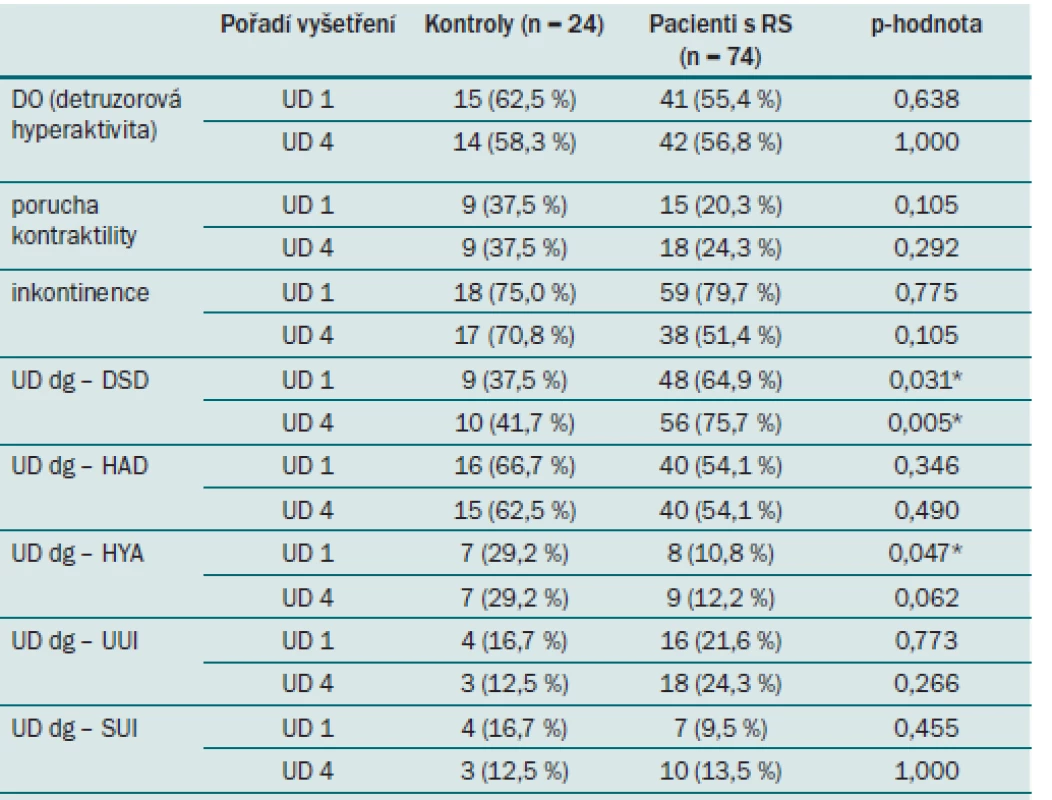
* Statisticky významný rozdíl na hladině významnosti 0,05. V ostatních spojitých charakteristikách byli pacienti s RS při UD 1 a UD 4 s kontrolními subjekty srovnatelní (tab. 10).
Table 10. Srovnání spojitých parametrů UD vyšetření v 0. a 12. měsíci (UD 1 a 4) mezi pacienty a kontrolními subjekty. Popis jednotlivých parametrů je uvedený v tab. 4. 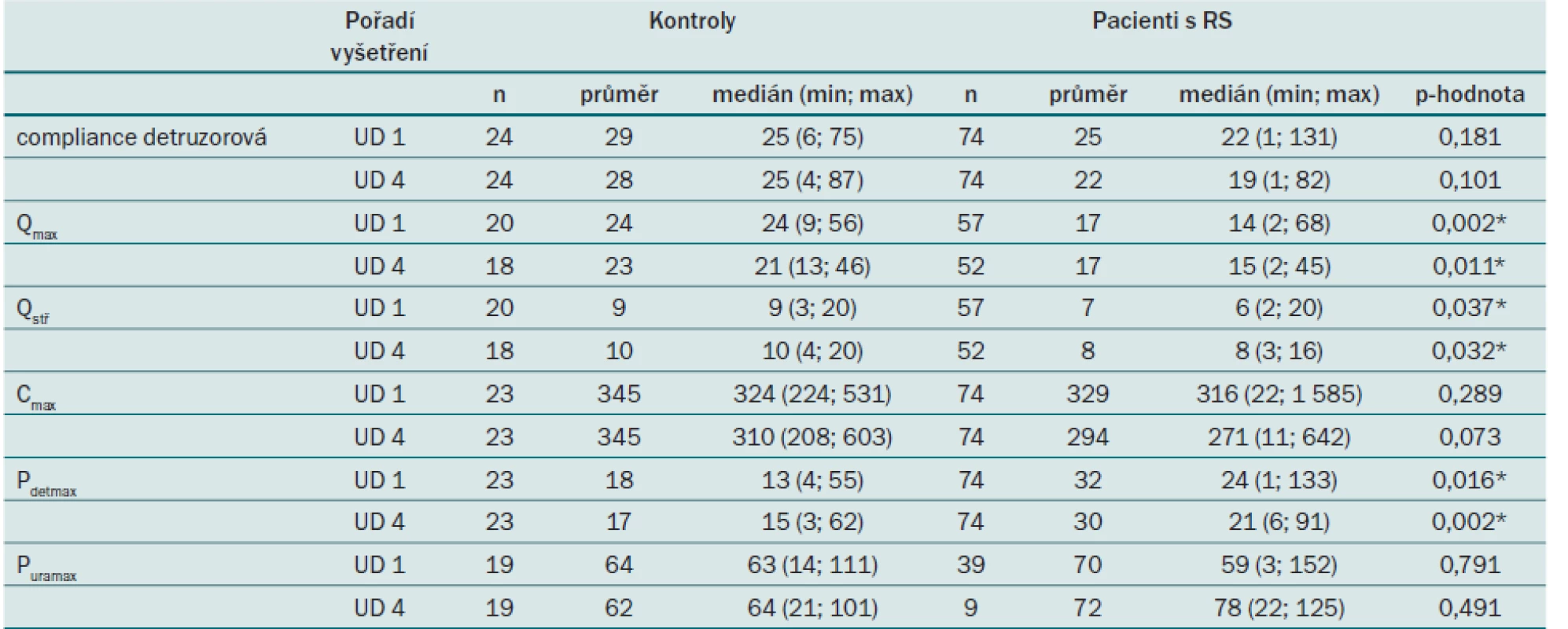
* Statisticky významný rozdíl na hladině významnosti 0,05. 2. Srovnání změn spojitých parametrů mezi UD 1 a UD 4 (v 0. a 12. měsíci)
Při srovnání změn sledovaných spojitých parametrů mezi pacienty s RS a kontrolními subjekty, ke kterým došlo po roce (tj. rozdíl mezi UD 1 a UD 4), se neprokázal mezi skupinami statisticky významný rozdíl (kromě skóre ICIQ ‑ SF). Jinými slovy, změny parametrů zaznamenané u kontrol a pacientů s RS mezi UD 1 a UD 4 nejsou statisticky významně rozdílné (tab. 11).
Table 11. Srovnání změn spojitých parametrů UD vyšetření po roce mezi pacienty a kontrolními subjekty. Do hodnocení jsou zařazeny pouze subjekty s vyšetřením v 0. i 12. měsíci (uvedené n). Interpretace změn je popsána v textu. Popis jednotlivých parametrů je uvedený v tab. 4. 
Grafické znázornění vývoje spojitých parametrů v čase u obou skupin je uvedeno na grafech 3 – 7 a sumarizace jednotlivých spojitých parametrů je také uvedena v tab. 8.
Graph 3. Vývoj detruzorové compliance (ml/cm H<sub>2</sub>O) v kontrolní skupině a ve skupině pacientů s RS v 0., 4., 8. a 12. měsíci (UD 1–4). 
Graph 4. Vývoj Q<sub>max</sub> (ml/s) v kontrolní skupině a ve skupině pacientů s RS v 0., 4., 8. a 12. měsíci, tj. UD 1, 2, 3, 4 (n<sub>1</sub>–n<sub>4</sub> = počet subjektů, kteří absolvovali vyšetření v rámci UD 1–4). 
Graph 5. Vývoj maximální cystometrické kapacity měchýře C<sub>max</sub> (ml) v kontrolní skupině a ve skupině pacientů s RS v 0., 4., 8. a 12. měsíci (UD 1, 2, 3, 4). 
Graph 6. Vývoj maximálního detruzorového tlaku P<sub>detmax</sub> (cm H<sub>2</sub>O) v kontrolní skupině a ve skupině pacientů s RS v 0., 4., 8. a 12. měsíci (UD 1–4). 
Graph 7. Vývoj skóre ICIQ-SF ve skupině pacientů s RS v 0., 4., 8. a 12. měsíci (UD 1–4). 
3. Hodnocení vývoje výskytu kategoriálních parametrů v čase
To, jak se v průběhu roku vyvíjely kategoriální proměnné typu „ano × ne“ od zahájení sledování u obou skupin, je uvedeno v tab. 12. Interpretace výskytu inkontinence u pacientů s RS je následující: 36 pacientů s RS ze 74 (48,6 %) trpělo inkontinencí v 0. i ve 12. měsíci, u 23 inkontinentních pacientů (31,1 %) inkontinence po roce odezněla, 13 (17,6 %) pacientů bylo kontinentních při UD 1 a i po roce zůstali bez známek inkontinence, zatímco dva pacienti s RS (2,7 %), kteří byli při prvním UD 1 vyšetření bez inkontinence, po roce při UD 4 již inkontinencí trpěli. Statisticky významná p ‑ hodnota testu naznačuje, že u pacientů s RS byl zaznamenán statisticky významný rozdíl ve výskytu inkontinence a diagnózy detruzorosfinkterické dyssynergie (UD dg – DSD) po roce od prvního vyšetření a to tak, že pacienti po roce výrazně méně trpěli inkontinencí (p < 0,001), ale častěji se u nich vyskytovala diagnóza DSD (p = 0,039). Pokles výskytu inkontinence je zřejmě výsledkem urologické cílené léčby.
Table 12. Vývoj kategoriálních charakteristik typu „ano × ne“ po roce a srovnání těchto změn zvlášť pro pacienty a zvlášť pro kontrolní subjekty. Popis jednotlivých parametrů je uvedený v tab. 4 (UD 1 – vyšetření v 0. měsíci, UD 4 – vyšetření ve 12. měsíci). 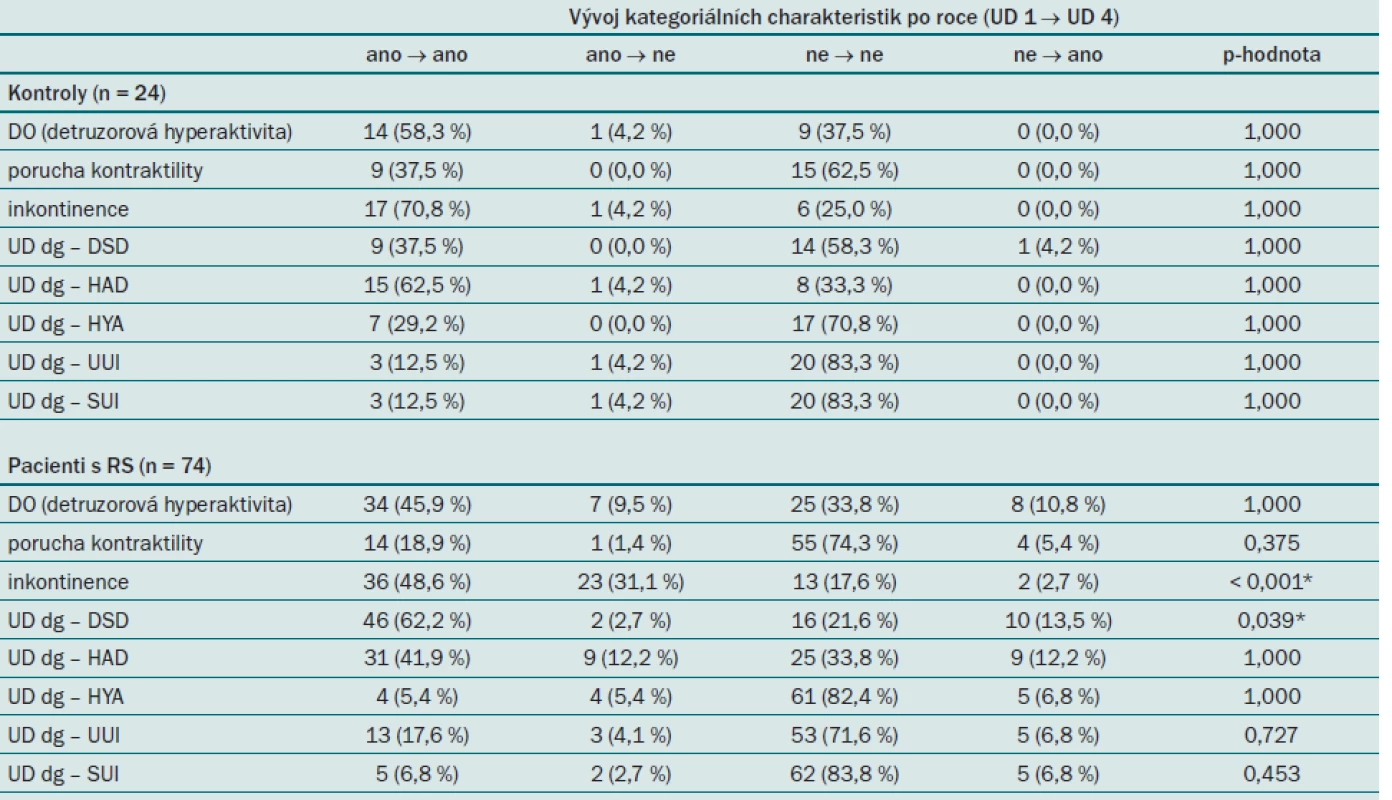
* Statisticky významná změna na hladině významnosti 0,05. Také při srovnání výskytu jednotlivých kategoriálních proměnných typu „ano × ne“ zvlášť v 0. a ve 12. měsíci mezi pacienty s RS a kontrolními subjekty se prokázal statisticky významný rozdíl pouze v přítomnosti diagnóz detruzorosfinkterické dyssynergie (UD dg – DSD) a hypoaktivity detruzoru (UD dg – HYA). Četnost výskytu diagnózy DSD je u pacientů s RS vyšší než u kontrolních subjektů, zatímco diagnóza HYA se častěji vyskytuje u kontrolních subjektů (tab. 9).
Podrobnější hodnocení vývoje kategoriálních charakteristik mezi jednotlivými UD vyšetřeními u pacientů s RS (mezi 0. a 4. měsícem, 0. a 8. měsícem, 4. a 8. měsícem a 8. a 12. měsícem) bylo provedeno u diagnóz, u kterých se po roce od prvního vyšetření prokázal významný rozdíl – tedy u DSD a inkontinence (tab. 13 a graf 8). Změna výskytu diagnózy DSD je pak významná až po roce (tedy mezi 1. a 4. UD měřením), mezi průběžnými vyšetřeními je vidět pouze pozvolný nárůst, avšak ne statisticky významný (tab. 7 a 13).
Table 13. Podrobné hodnocení vývoje výskytu inkontinence a diagnózy DSD u pacientů s RS mezi jednotlivými UD vyšetřeními. 
* Statisticky významná změna na hladině významnosti 0,05. Graph 8. Podíl pacientů s RS trpících inkontinencí a s diagnózou DSD v jednotlivých UD vyšetřeních. 
Souhrn závěrů
Závěr č. 1: U mužů z RS je zaznamenán signifikantně častější výskyt diagnózy DSD. Jinak jsou obě pohlaví jak ve skupině pacientů s RS, tak v kontrolní skupině z UD hlediska při vstupním vyšetření srovnatelná.
Závěr č. 2: Pacienti s dysfunkcemi DMC z důvodu RS jsou na vstupu signifikantně odlišní z hlediska UD parametrů od skupiny pacientů s jiným neurologickým postižením, a to ve výtokových parametrech Qmax, Qstř a Pdetmax. K ověření tohoto rozdílu by však bylo potřeba navýšit soubor pacientů v kontrolní skupině.
Závěr č. 3: Významné snížení skóre ICIQ ‑ SF a redukce inkontinence u pacientů s RS je pravděpodobně způsobeno cílenou léčbou neurogenních dysfunkcí DMC.
Závěr č. 4: U pacientů s RS lze v průběhu sledování zaznamenat vyšší výskyt DSD ve srovnání se skupinou pacientů s jiným neurologickým onemocněním, což může být projevem pozvolné progrese neurologického onemocnění bez zjevných klinických změn na neurologickém nálezu.
Shrnutí
Práce prokazuje, že pacienti s dysfunkcemi DMC z důvodu RS jsou na vstupu signifikantně odlišní z hlediska UD parametrů od skupiny pacientů s jiným neurologickým postižením, a to v Qmax, Qstř, a v Pdetmax. Riziko rozvoje inkontinence i při zavedené léčbě NDMC bylo 2,7 %. Riziko rozvoje DSD v RS skupině v průběhu roku bylo 13,5 %. Lze tedy konstatovat, že sumárně existuje 16,2% riziko zhoršení, resp. změny UD nálezu v průběhu ročního sledování, která si následně může vyžádat i úpravu nebo změnu terapie NDMC. Signifikantní zvýšení výskytu DSD v čase u pacientů s RS ve srovnání s kontrolní skupinou může být projevem dosud neodhalené neurologické progrese.
Současné doporučení EAU pro sledování pacientů s NDMC je koncipováno obecně pro pacienty postižené jakýmkoli neurologickým postižením. Skupina pacientů s RS je však z klinického hlediska odlišná, a to s ohledem na „dynamiku“ neurologického stavu odpovídajícímu průběhu RS. Současná medicína zatím nedokáže RS vyléčit, dokáže však průběh nemoci zpomalit a částečně i reparovat poškozené nervové dráhy. Tento činitel spolu s možnou progresí nemoci hrají důležitou roli ve výsledné funkci DMC u této skupiny pacientů. Pro výše uvedené by se mělo na pacienty s RS trpícími NDMC nahlížet jako na samostatnou skupinu neurogenních dysfunkcí vyžadující pravidelný ambulantní monitoring spočívající v klinickém vyšetření (anamnéza, mikční denník, UFM + PVR) minimálně každé čtyři měsíce a v UD měření minimálně jednou ročně nebo při klinické změně (zhoršení) charakteru močení v průběhu léčby.
MUDr. Gabriel Varga
Urologická klinika LF MU a FN Brno
Jihlavská 20, 625 00 Brno
gvarga@fnbrno.cz
Sources
1. Havrdová E. Roztroušená skleróza míšní. In: Neuroimunologie. Praha: Maxdorf 2001 : 231 – 269.
2. Khan F, Pallant JF, Pallant JI et al. A randomised controlled trial: outcomes of bladder rehabilitation in persons with multiple sclerosis. J Neurol Neurosurg Psychiatry 2010; 81(9): 1033 – 1038. doi: 10.1136/ jnnp.2010.206623.
3. Khan F, Pallant JF, Shea TL et al. Multiple sclerosis: prevalence and factors impacting bladder and bowel function in an Australian community cohort. Disabil Rehabil 2009; 31(19): 1567 – 1576.
4. Zachoval R, Záleský M, Lukeš M et al. Funkce dolních močových cest a jejich poruchy. Čes Fyziol 2000; 49(3): 134 – 144.
5. Borello ‑ France D, Dusi J, O‘Leary M et al. Test ‑ retest reliability of the urge ‑ urinary distress inventory and female sexual function index in women with multiple sclerosis. Urol Nurs 2008; 28(1): 30 – 35.
6. Thüroff J, Abrams P, Andersson KE et al. Guidelines EAU pro léčbu močové inkontinence. Urol List 2008; 6(1): 97 – 105.
Labels
Paediatric urologist Urology
Article was published inUrological Journal

2014 Issue 3-
All articles in this issue
- EAU – Léčba LUTS u mužů by měla být především kombinační
- Řešení infekcí močových cest souvisejících s katetrizací (založené na důkazech)
- Vývoj robotické technologie v urologické operativě
- Suspenze přední poševní stěny – popis techniky
- Je potřeba stanovit frekvenci urodynamického vyšetření u pacientů postižených dysfunkcí dolních močových cest v důsledku roztroušené sklerózy?
- Radikální operace a radioterapie – jaký smysl a výsledky mají tyto modality u pacientů s karcinomem prostaty vyšších stadií
- Priapizmus – čas jako limitující faktor
- Urological Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- EAU – Léčba LUTS u mužů by měla být především kombinační
- Řešení infekcí močových cest souvisejících s katetrizací (založené na důkazech)
- Suspenze přední poševní stěny – popis techniky
- Radikální operace a radioterapie – jaký smysl a výsledky mají tyto modality u pacientů s karcinomem prostaty vyšších stadií
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

