-
Medical journals
- Career
Vaporizace prostaty pomocí zeleného laseru (GreenLight laser) – zkušenost z jednoho centra po provedení více než 1 000 výkonů
Authors: M. Rieken; A. Bachmann
Published in: Urol List 2012; 10(4): 22-26
Overview
Klíčová slova:
GreenLight laser - PVPsymptomy dolních cest močových - BPHkomplikaceSymptomy dolních cest močových (LUTS) v důsledku benigního zvětšení prostaty (BPE) představují u mužské populace vysoce prevalentní onemocnění. Určitý stupeň klinické BPE se vyskytuje u 60 % všech mužů ve věku 60 let [1]. V případě, že selže medikamentózní terapie, je indikována operační léčba. Další indikace pro operační léčbu zahrnují recidivující infekci močových cest, recidivující hematurii, konkrementy v močovém měchýři a renální insuficienci v důsledku obstrukce [2].
U mužů s prostatou o velikosti 30–80 ml se za zlatý standard považuje transuretrální resekce prostaty (TURP) [2], zatímco u pacientů s větší prostatou je léčbou volby ve většině center otevřená prostatektomie (OP). Navzdory rozšířenému provádění může být TURP spojena se závažnými komplikacemi v podobě krvácení nebo absorpce irigační tekutiny (TUR syndrom), jež mohou mít závažné následky, jako např. otok mozku nebo průdušek [3–5]. Otevřená prostatektomie vede k dlouhodobému zlepšení mikčních parametrů a mikčních symptomů. Na druhou stranu je však spojena se značnou peroperační morbiditou, vyžaduje poměrně dlouhou hospitalizaci a není vhodná pro pacienty s vysokým rizikem [6–8]. Z tohoto důvodu byla vyvinuta laserová technika, jejímž cílem je zajištění stejných funkčních výsledků při současné eliminaci nedostatků TURP a OP.
Vizuální laserová ablace prostaty (VLAP) pomocí 1 064 nm neodymium: yttrium-aluminum-garnet (Nd:YAG) laseru byla poprvé uvedena na počátku 90. let minulého století [9]. Díky nízkému absorpčnímu koeficientu a hloubce penetrace 4–18 mm byla u většiny tkání pozorována hluboká koagulační nekróza [10]. Navzdory lepšímu pooperačnímu bezpečnostnímu profilu dosahuje tato technika horšího funkčního výsledku než TURP. Vzhledem k tomu, že VLAP vyžadovala navíc v mnoha případech opakování operace, bylo od této techniky ustoupeno [11,12]. Renezanci v laserové léčbě přineslo představení kalium - -titanyl-fosfátového laseru (KTP). Při průchodu Nd:YAG paprsku (1 046 nm) skrze KTP krystal dochází ke zdvojnásobení frekvence a zmenšení vlnové délky o polovinu, díky čemuž se generuje paprsek o vlnové délce 532 nm. Tato vlnová délka se nachází v rozmezí viditelného zeleného světla, jež propůjčilo tomuto typu laseru svůj název (GreenLight laser) (schéma 1a). Paprsek generovaný laserem GreenLight vykazuje naprosto odlišnou interakci s tkání než Nd:YAG laser. Vlnová délka není pohlcována ve vodném prostředí, je však významně pohlcována hemoglobinem, díky čemuž má tento laser posílené hemostatické vlastnosti. Hloubka absorpce ve vaskularizované tkáni, jakou je prostata, činí pouze 1–3 mm. Díky tomu je generována energie o vysoké hustotě, což způsobuje rychlou vaporizaci tkáně. Odtud také pochází název této techniky: fotoselektivní vaporizace prostaty (PVP) (schéma 1b) [13,14]. Zavedení 80W KTP laseru má na svědomí rozšíření této techniky. Od roku 2007 je na trhu k dispozici 120W vysoce účinný systém (HPS)-laser (American Medical Systems Inc., Minnetonka, MN, USA), který je vybaven lithium--triborátovým (LBO) krystalem a vláknem produkujícím soustředěnější paprsek. V roce 2010 byl na trh uveden 180W intenzivní systém (XPS)-laser (American Medical Systems Inc., Minnetonka, MN, USA). Díky 50% zvýšení výkonu (oproti 120W systému) je 180W laser vybaven vláknem chlazeným kapalinou, které je schopno vyzařovat větší množství energie. Ve srovnání se 120W laserem má 180W systém rovněž o 50 % větší paprsek, což umožňuje rychlejší vaporizaci. Autoři tohoto článku popisují své zkušenosti s PVP pomocí GreenLight laseru od zahájení této techniky v jejich centru v roce 2002.
Schéma 1a. Operace využívající GreenLight laser. 
Schéma 1b. Diagram zobrazující PVP. Povrchová tkáň prostaty je rychle zahřívána energií laserového paprsku, což vede k rychlé vaporizaci prostatické tkáně. 
MATERIÁL A METODY
Autoři analyzovali nashromážděné údaje týkající se techniky PVP. PVP s užitím 80W KTP laseru (American Medical Systems Inc., Minnetonka, MN, USA) byla poprvé provedena v září 2002. V období od června 2007 do července 2010 byly všechny výkony prováděny pomocí 120W HPS laseru (American Medical Systems Inc., Minnetonka, MN, USA). 180W XPS laser (American Medical Systems Inc., Minnetonka, MN, USA) užíváme na našem oddělení od července 2010. Indikace pro PVP jsou totožné jako indikace pro TURP na základě příslušných směrnic. Všichni pacienti před výkonem podepsali informovaný souhlas a byli poučeni o možných rizicích a vedlejších účincích PVP.
OPERAČNÍ TECHNIKA
Operační technika zahrnuje několik kroků. Ve stručnosti: vytvoříme anteriorní pracovní prostor, abychom zamezili kontaktu vlákna s tkání a abychom vytvořili spojení mezi močovým měchýřem a apexem. Po vytvoření pracovního kanálu vaporizujeme laterální laloky mezi hrdlem močového měchýře a apexem, přičemž vláknem kyvadlovým pohybem pohybujeme laterálně. Následně provádíme ablaci tkáně apexu a středního laloku a otevřeme hrdlo močového měchýře. Na konci operace je vytvořena dutina, podobně jako při TURP (schéma 2 b,c). Nakonec zkontrolujeme hemostázu a v případě nutnosti provedeme koagulaci.
Schéma 2. Prostatická fossa před (a), během (b) a po PVP (c). 
VÝSLEDKY
Peroperační údaje a bezpečnost techniky
Nejrůznější publikace prokázaly vysokou peroperační bezpečnost PVP. V analýze 500 po sobě jdoucích pacientů léčených pomocí PVP s užitím 80W KTP laseru činila průměrná délka operace 66,4 ± 26,8 min při léčbě prostaty o průměrné velikosti 56,1 ± 25,3 ml. V průměru bylo aplikováno 206 ± 94 kJ. Pacienti měli katétr zaveden průměrně po dobu 1,8 ± 1,2 dnů a byli hospitalizováni průměrně po 3,7 ± 2,9 dnů. Peroperační krvácení se vyskytlo u 3,6 % pacientů, perforace kapsuly u 0,2 % pacientů a u 5,2 % pacientů byla nutná konverze k TURP z důvodu krvácení, velikosti prostaty nebo defektu laserového vlákna. Nebyl zaznamenán jediný případ TUR syndromu a nebylo nutné provádět krevní transfuzi během výkonu [15]. Pomocí 180W XPS laserového systému bylo aplikováno průměrně 324 ± 187 kJ (na jednu prostatickou žlázu), což je významně více než při užití 80W laseru [16]. Pomocí 180W laserového systému bylo rovněž aplikováno významně (p < 0,05) více energie na objem prostaty (180 W: 5,3 ± 2,8 kJ/ml; 120 W: 3,0 ± 1,4 kJ/ml; 80 W: 3,9 ± ± 1,3 kJ/ml) i více energie na délku operace (180 W: 4,8 ± 1,8 kJ/min; 120 W: 3,0 ± 1,3 kJ/min; 80 W: 2,9 ± 0,7 kJ/ml) než pomocí starších laserových systémů (schéma 3) [17]. Nerandomizované srovnání peroperačních údajů posledních 200 pacientů, kteří podstoupili PVP s užitím 80W KTP laseru, a prvních 200 pacientů, kteří byli léčeni pomocí PVP s užitím 120W HPS laseru, prokázalo, že při užití 120W systému častěji dochází k horší viditelnosti v důsledku krvácení (21,2 vs 6,4 %; p < 0,001) [18]. Nedávno provedená multicentrická analýza prvních případů léčených pomocí 180W systému uvádí zhoršenou viditelnost v důsledku krvácení u 10 % případů a perforaci kapsuly u 3,5 % případů [16]. Byla zaznamenána významná korelace mezi předoperačním zavedením katétru a perforací kapsuly a výskytem peroperačního krvácení. Naopak velikost prostaty nesouvisela ani s krvácením ani s perforací kapsuly [16].
Schéma 3. Aplikace energie a typ laseru. 
Pooperační funkční výsledky a komplikace
Ke zlepšení mikčních symptomů a parametrů došlo po léčbě pomocí všech druhů GreenLight laseru. U 500 pacientů léčených pomocí 80W KTP laserové vaporizace prostaty přetrvalo okamžité i dlouhodobé zlepšení mikčních parametrů a symptomů po dobu až pěti let (schéma 4) [15]. Během 36 měsíců byla opakovaná operace nutná u 11 % (80 W) a 6 % (120 W, ns) pacientů. Příčiny zahrnovaly uretrální strikturu (1 vs 0 %, ns), strikturu hrdla močového měchýře (3 vs 1,5 %, ns) a recidivující nebo přetrvávající adenom (7 vs 4,5 %, ns) [18].
Schéma 4. Pooperační průběh (v délce trvání 60 měsíců) v hodnocení IPSS a Qmax po PVP s užitím 80W KTP laseru (nepublikované údaje). 
Analýza dlouhodobých výsledků po minimální době sledování 48 měsíců u 40 pacientů, kteří podstoupili laserovou vaporizaci prostaty s užitím 80W KTP laseru, prokázala zvýšení průměrného maximálního průtoku moči (Qmax) z 6,9 na 16,5 ml/s, pokles průměrného postmikčního rezidua (Vres) ze 118 na 41 ml, pokles průměrného IPSS skóre (International Prostate Symptom Score) z 18,2 na 7,2, pokles průměrného indexu Quality of Life (QoL) ze 4,0 na 1,2 po 48 měsících sledování ve srovnání s předoperačními hodnotami (p < 0,05). Tyto výsledky jasně prokazují trvanlivost účinku této techniky a přetrvávající významné zlepšení mikčních parametrů a symptomů [19].
Bezpečnost PVP již byla prokázána v několika našich předchozích publikacích. Co se týče časných pooperačních komplikací po PVP s užitím 80W KTP laseru: hematurie byla zaznamenána u 9,8 % pacientů, krevní transfuze byla nutná u 0,4 % pacientů, revize u 0,6 % pacientů, akutní renální selhání se vyskytlo u 0,6 % pacientů, urosepse u 0,4 % pacientů, dysurie u 14,8 % pacientů, přechodná urgentní inkontinence u 2,4 % pacientů a infekce močových cest u 6,8 % pacientů (z celkem 500 pacientů, u nichž jsou k dispozici všechny potřebné údaje) [15]. Co se týče výskytu pozdních komplikací: při analýze všech 500 pacientů bylo nutné léčbu opakovat z důvodu recidivujícího adenomu u 14,8 % pacientů, z důvodu přetrvávajícího adenomu u 6,8 % pacientů, v důsledku striktury hrdla močového měchýře u 3,6 % pacientů a z dů-vodu uretrální striktury u 4,4 % pacientů. Pouze 27 pacientů však mohlo podstoupit kontrolní vyšetření po pěti letech [15]. V selektivní analýze údajů skupiny 61 (po sobě jdoucích) pacientů, kteří byli sledováni déle než 48 měsíců (průměrná délka sledování: 58,1 měsíců), kteří podstoupili léčbu pomocí 80W KTP laseru, byla opakovaná léčba nutná u 47,6 % pacientů v důsledku recidivujícího adenomu, z důvodu přetrvávajícího adenomu u 29,5 % pacientů, v důsledku striktury hrdla močového měchýře u 6,6 % pacientů a z důvodu uretrální striktury u 11,5 % pacientů [20]. Je třeba si uvědomit, že tato analýza může být potenciálně ovlivněna předpojatou chybou v důsledku selekce pacientů a většího výskytu případů s nepříznivým pooperačním vývojem. Po průměrné době sledování 32,1 měsíců byl karcinom prostaty diagnostikován u 6,1 % pacientů léčených pomocí KTP-laserové vaporizace, což je výsledek srovnatelný s TURP a otevřenou operací (u pacientů odpovídajícího věku) [21].
Výsledky u pacientů užívajících perorální antikoagulační léčbu a pacientů s větší prostatou
Díky specifickým fyzikálním vlastnostem je PVP velmi vhodná i pro pacienty s vysokým rizikem krvácení. Dále na rozdíl od monopolární TURP není užívání PVP omezeno pouze na určitou velikost prostaty a lze ji využít i při léčbě větších prostat. Hodnotili jsme bezpečnost a dlouhodobý výsledek PVP u pacientů, kteří dlouhodobě užívají kumariny, klopidogrel nebo kyselinu acetylsalicylovou a u pacientů s prostatou > 80 ml. Z celkem 690 pacientů 42 % užívalo v době výkonu kumariny, klopidogrel nebo kyselinu acetylsalicylovou a 17 % pacientů mělo prostatu o objemu ≥ 80 ml. Peroperační krvácení způsobující horší viditelnost se vyskytovalo méně často u pacientů užívajících perorální antikoagulancia (6,6 vs 10,7 %; p < 0,05). Konverze k TURP (4,5 vs 8 %) a perforace kapsuly (2,1 vs 2,5 %) byla srovnatelná bez ohledu na to, zda pacienti užívali antikoagulancia, nebo nikoli. K peroperačnímu krvácení (18,4 vs 7,0 %; p < 0,005) a konverzi k TURP (17,6 vs 4,2 %; p < 0,0001) do-cházelo častěji u pacientů s prostatou o objemu ≥ 80 ml. Ve srovnání s předoperačními hodnotami došlo během 48měsíčního sledování k významnému zlepšení mikčních symptomů (IPSS, QoL) i mikčních parametrů (Qmax, Vres). Míra nutnosti opakovat operaci se významně nelišila mezi pacienty, kteří užívali antikoagulancia a kteří nikoli, ani u pacientů s prostatou o objemu ≥ 80 ml [22].
SROVNÁNÍ S TURP
Aktualizace naší komparativní nerandomizované studie ze dvou center srovnávající 80W KTP laserovou vaporizaci prostaty se standardní TURP prokázala, že PVP vyžaduje kratší dobu hospitalizace. Zlepšení mikčních parametrů i symptomů bylo u obou výkonů srovnatelné, zatímco po TURP došlo k významnějšímu poklesu hladiny PSA. Během 60měsíčního sledování bylo nutné výkon opakovat (jednou nebo vícekrát) u 21 % pacientů po PVP a u 7 % pacientů po TURP (p < 0,05) z důvodu sklerózy hrdla močového měchýře (4 vs 1 %), recidivujícího adenomu (14 vs 5 %) nebo uretrální striktury (8 vs 1 %) [23].
SROVNÁNÍ S VAPORIZACÍ S UŽITÍM DIODOVÉHO LASERU Z JEDNOHO CENTRA
S cílem dále hodnotit potenciál laserové vaporizace prostaty byl srovnáván 120W HPS laser a 200W 980nm diodový laser (Limmer Laser GmbH, Berlín, Německo). 62 pacientů bylo léčeno pomocí 120W HPS laserové vaporizace a 55 pacientů pomocí 980nm diodového laseru. Průměrná délka operace byla srovnatelná při užití obou technik, pomocí diodového laseru však bylo aplikováno výrazně větší množství energie – 313 vs 187 kJ (p < 0,001). U pacientů léčených pomocí 120W HPS laseru byla zaznamenána významně vyšší míra peroperačního krvácení (0 vs 12,9 %; p < 0,01) a perforace kapsuly (0 vs 4,8 %; p > 0,05) [24]. Nejnovější aktualizace po 36 měsících sledování prokázala 37,5% míru opakování operace po léčbě pomocí diodového laseru a 8,9% míru po léčbě pomocí 120W GreenLight laseru (p < 0,001), a to v důsledku obstrukční nekrotické prostatické tkáně (16,1 vs 0 %; p < 0,01), recidivujícího nebo přetrvávajícího adenomu (5,4 vs 7,1 %, ns) a sklerózy hrdla močového měchýře (16,1 vs 1,5 %; p < 0,05) [25].
DISKUZE
TURP a otevřená operace jsou považovány za zlatý standard léčby obstrukce výtoku z močového měchýře v důsledku BPH. I přes nesporně vynikající výsledky však vysoká míra výskytu peroperační a pooperační morbidity vedla k hledání dalších alternativ, jež budou dosahovat stejných funkčních výsledků při nižším celkovém výskytu komplikací. Jednou z těchto metod je právě GreenLight laserová vaporizace prostaty, kterou jsme poprvé v našem centru vyzkoušeli v roce 2002. V uplynulých deseti letech bylo pomocí této techniky léčeno více než 1 000 pacientů, což nám umožnilo nashromáždit značnou úroveň poznatků a zkušeností.
Co se týče peroperační bezpečnosti, jsou naše výsledky v souladu s výsledky ostatních skupin a prokazují (ve srovnání s TURP) benefit této techniky s ohledem na invazivitu [26]. Příznivý bezpečnostní profil a srovnatelné výsledky u pacientů s prostatou o objemu > 100 ml (srovnatelný s OP) prokázali i jiní autoři [27,28].
Při srovnání našich funkčních výsledků s údaji ostatních center lze říci, že PVP umožňuje dosáhnout trvalého funkčního zlepšení [29,30]. Nejrůznější prospektivní, randomizované studie prokázaly, že ve srovnání s TURP dosahují 80W KTP i 120W HPS laserová vaporizace prostaty srovnatelných funkčních výsledků po 12, 24, i 36 měsících sledování [31–36]. Studie zahrnující pacienty s prostatou o objemu > 70 ml prokázala po šesti měsících sledování u pacientů léčených TURP příznivější funkční výsledek [32,37] (tab. 1). V nedávné době provedená metaanalýza všech dostupných RCTs srovnávající PVP a TURP prokázala, že PVP je spojena s kratší dobou hospitalizace a katetrizace, ovšem delším trváním operace. Rovněž potřeba krevní transfuze a vznik retence v důsledku krevních sraženin byly významně méně časté při PVP, střednědobé výsledky jsou srovnatelné [38]. Vzhledem k tomu, že dlouhodobé údaje jsou zatím poměrně vzácné, máme pro přímé srovnání technik k dispozici pouze minimum publikací. 47,6% míra opakování operace (kterou uvádíme na základě selektivní analýzy pacientů, kteří byli sledováni po dobu delší než čtyři roky) je v ostrém kontrastu s údaji, jež uvádí Hai [30]. Hai uvádí, že ve skupině 246 pacientů, kteří byli sledováni po dobu pěti let, vyžadovalo opakovanou léčbu 8,9 % jedinců. Tento obrovský rozdíl lze vysvětlit skutečností, že vaporizaci pomocí GreenLight laseru provádí v našem centru různí operatéři s rozdílnou úrovní zkušeností a rovněž vlivem předpojaté chyby v podobě negativní selekce pacientů, neboť ne všichni pacienti byli sledováni.
Table 1. Randomizované kontrolované studie srovnávající PVP vs TURP nebo OP. 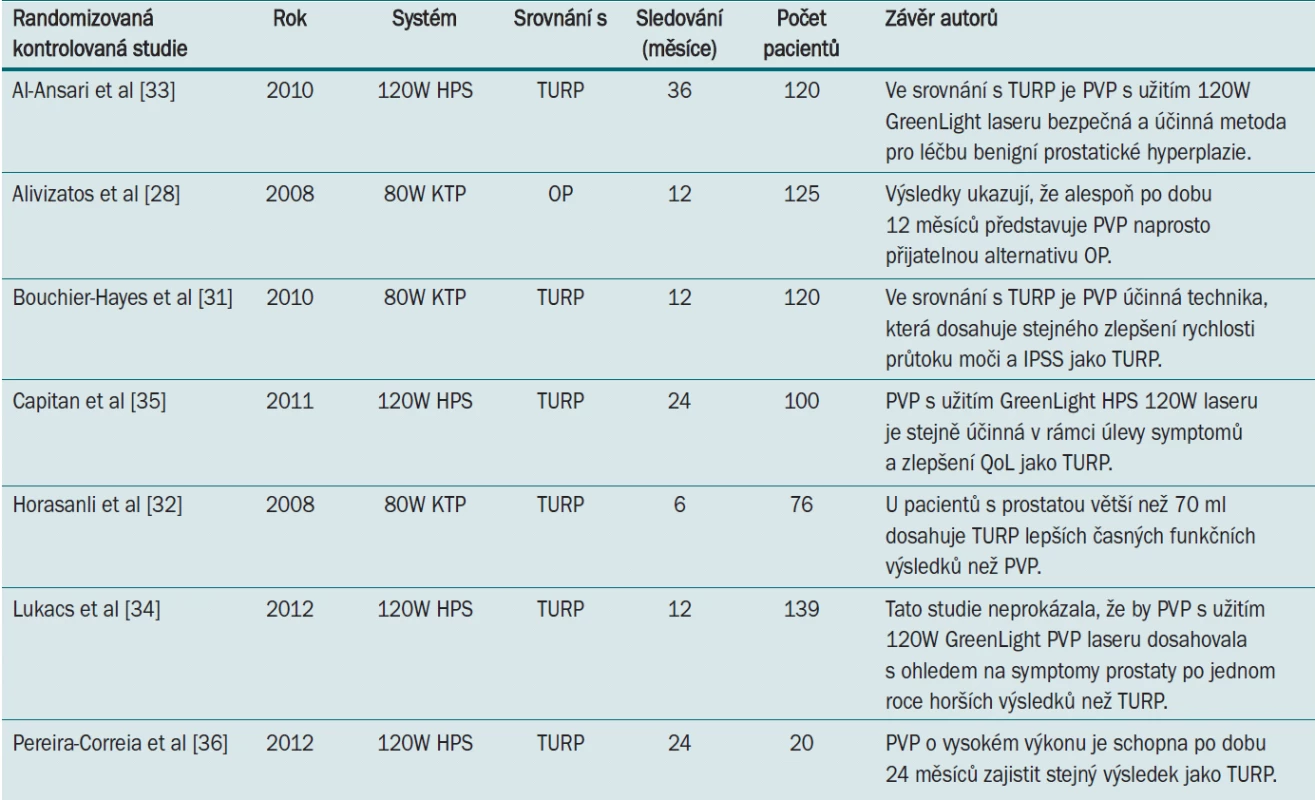
Neúčinná ablace tkáně, uváděná často jako hlavní nevýhoda PVP při užívání 80W systému, se již při užívání 180W systému nevyskytuje. Naše údaje jasně prokazují, že aplikace většího množství energie (což je benefit, který nabízejí nejnovější druhy laseru) umožňuje účinnější ablaci tkáně. V současné době očekáváme výsledky probíhající prospektivní randomizované studie srovnávající PVP s užitím 180W laserového systému vs TURP (GOLIATH-Study, hlavní investigátor: A. Bachmann), která snad rovněž potvrdí srovnatelnou účinnost PVP a TURP.
ZÁVĚR
Údaje prezentované v tomto článku představují souhrn našich dosavadních zkušeností s vaporizací prostaty pomocí GreenLight laseru. Naše analýzy prokazují, že tato technika dosahuje vynikající peroperační bezpečnosti a významné dlouhodobé účinnosti. Výhodou PVP oproti TURP a OP je možnost indikovat tuto techniku u pacientů s vysokým rizikem a u pacientů užívajících perorální antikoagulancia, nevýhodou je prozatím nedostatek dlouhodobých výsledků. Přesto jsme přesvědčeni, že PVP je pozitivním přínosem, který rozšíří možnosti operační léčby BPH, a lze ji považovat za adekvátní alternativu TURP a OP.
prof. Alexander Bachmann, MD
Department of Urology University Hospital Basel Switzerland
bachmana@uhbs.ch
Sources
1. Arrighi HM, Metter EJ, Guess HA et al. Natural history of benign prostatic hyperplasia and risk of prostatectomy. The Baltimore Longitudinal Study of Aging. Urology 1991; 38 (1 Suppl): 4–8.
2. Madersbacher S, Alivizatos G, Nordling J et al. EAU 2004 guidelines on assessment, therapy and follow--up of men with lower urinary tract symptoms suggestive of benign prostatic obstruction (BPH guidelines). Eur Urol 2004; 46(5): 547–554.
3. Rassweiler J, Teber D, Kuntz R et al. Complications of transurethral resection of the prostate (TURP)--incidence, management, and prevention. Eur Urol 2006; 50(5): 969–979.
4. Oelke M, Bachmann A, Descazeaud A et al. EAU 2012 Guidelines on the Management of Male Lower Urinary Tract Symptoms (LUTS), incl. Benign Prostatic Obstruction (BPO).
5. Ho HSS, Yip SKH, Lim KB et al. A prospective randomized study comparing monopolar and bipolar transurethral resection of prostate using transurethral resection in saline (TURIS) system. Eur Urol 2007; 52(2): 517–522.
6. Gratzke C, Schlenker B, Seitz M et al. Complications and early postoperative outcome after open prostatectomy in patients with benign prostatic enlargement: results of a prospective multicenter study. J Urol 2007; 177(4): 1419–1422.
7. Varkarakis I, Kyriakakis Z, Delis A et al. Long-term results of open transvesical prostatectomy from a contemporary series of patients. Urology 2004; 64(2): 306–310.
8. Tubaro A, Carter S, Hind A et al. A prospective study of the safety and efficacy of suprapubic transvesical prostatectomy in patients with benign prostatic hyperplasia. J Urol 2001; 166(1): 172–176.
9. Costello AJ, Johnson DE, Bolton DM. Nd:YAG laser ablation of the prostate as a treatment for benign prostatic hypertrophy. Lasers Surg Med 1992; 12(2): 121–124.
10. Kuntz RM. Current role of lasers in the treatment of benign prostatic hyperplasia (BPH). Eur Urol 2006; 49(6): 961–969.
11. Hoffman RM, MacDonald R, Slaton JW et al. Laser prostatectomy versus transurethral resection for treating benign prostatic obstruction: a systematic review. J Urol 2003; 169(1): 210–215.
12. Wilson LC, Gilling PJ. From coagulation to enucleation: the use of lasers in surgery for benign prostatic hyperplasia. Nat Clin Pract Urol 2005; 2(9): 443–448.
13. McAllister WJ, Gilling PJ. Vaporization of the prostate. Curr Opin Urol 2004; 14(1): 31–34.
14. Te AE. The development of laser prostatectomy. BJU Int 2004; 93(3): 262–265.
15. Ruszat R, Seitz M, Wyler SF et al. GreenLight laser vaporization of the prostate: single-center experience and long-term results after 500 procedures. Eur Urol 2008; 54(4): 893–901.
16. Bachmann A, Muir GH, Collins EJ et al. 180-W XPS GreenLight laser therapy for benign prostate hyperplasia: early safety, efficacy, and perioperative outcome after 201 procedures. Eur Urol 2012; 61(3): 600–607.
17. 29th World Congress of Endourology & SWL WCE 2011 Scientific Program & Abstracts. J Endourol 2011; 25 (Suppl 1): P1–A373.
18. Rieken M, Bonkat G, Mueller G et al. 2174 the influence of increased maximum power output on the outcome of photoselective vaporization of the prostate with the greenlight laser – three-year results of a comparison between the 80-w KTP and the 120-w HPS-laser. The J Urol 2012; 187: e877.
19. Rieken M, Wyler S, Rentsch C et al. Long-term results of transurethral KTP-laser vaporization of the prostate. The Journal of Urology 2009; 181 : 767.
20. Rieken M, Bonkat G, Rentsch C et al. MP-06.04: Long-Term Results of Laser Vaporization of the Prostate with the 80-W KTP-Laser. Urology 2009; 74: S69.
21. Rieken M, Bonkat G, Wyler S e tal. UP-3.061: Incidence of Adenocarcinoma of the Prostate and Feasibility of Laparoscopic Radical Prostatectomy after Photoselective Vaporization of the Prostate for Prostate Enlargement. Urology 2009; 74: S312–S313.
22. Rieken M, Bonkat G, Rentsch C et al. 891 long--term results of photoselective vaporization of the prostate in patients with ongoing anticoagulation, thrombocyte aggregation inhibition and large prostates. Eur Urol Supplements 2010; 9 : 281.
23. Rieken M, Bonkat G, Lehmann K et al. 2268 photoselective vaporization of the prostate with the 80-w KTP-laser versus transurethral resection of the prostate & endash; long-term results of a prospective bicenter trial. J Urol 2011; 185: e909.
24. Ruszat R, Seitz M, Wyler SF et al. Prospective single-centre comparison of 120-W diode-pumped solid-state high-intensity system laser vaporization of the prostate and 200-W high-intensive diode-laser ablation of the prostate for treating benign prostatic hyperplasia. BJU Int 2009; 104(6): 820–825.
25. Rieken M, Mueller G, Bonkat G et al. 2173 photoselective vaporization of the prostate with the 120-w HPS greenlight laser versus laser vaporization of the prostate with the 980 nm 200-w high intensity diode laser – 3-year results of a prospective non-randomized trial. J Urol 2012; 187: e876.
26. Bouchier-Hayes DM, Anderson P, Van Appledorn S et al. KTP laser versus transurethral resection: early results of a randomized trial. J Endourol 2006; 20(8): 580–585.
27. Rajbabu K, Chandrasekara SK, Barber NJ et al. Photoselective vaporization of the prostate with the potassium-titanyl-phosphate laser in men with prostates of >100 mL. BJU Int 2007; 100(3): 593–598.
28. Alivizatos G, Skolarikos A, Chalikopoulos D et al. Transurethral photoselective vaporization versus transvesical open enucleation for prostatic adenomas > 80 ml: 12-mo results of a randomized prospective study. Eur Urol 2008; 54(2): 427–437.
29. Te AE, Malloy TR, Stein BS et al. Impact of prostate-specific antigen level and prostate volume as predictors of efficacy in photoselective vaporization prostatectomy: analysis and results of an ongoing prospective multicentre study at 3 years. BJU Int 2006; 97(6): 1229–1233.
30. Hai MA. Photoselective vaporization of prostate: five-year outcomes of entire clinic patient population. Urology 2009; 73(4): 807–810.
31. Bouchier-Hayes DM, Van Appledorn S, Bugeja P et al. A randomized trial of photoselective vaporization of the prostate using the 80-W potassium-titanyl--phosphate laser vs transurethral prostatectomy, with a 1-year follow-up. BJU Int 2010; 105(7): 964–969.
32. Horasanli K, Silay MS, Altay B et al. Photoselective potassium titanyl phosphate (KTP) laser vaporization versus transurethral resection of the prostate for prostates larger than 70 mL: a short-term prospective randomized trial. Urology 2008; 71(2): 247–251.
33. Al-Ansari A, Younes N, Sampige VP et al. GreenLight HPS 120-W laser vaporization versus transurethral resection of the prostate for treatment of benign prostatic hyperplasia: a randomized clinical trial with midterm follow-up. Eur Urol 2010; 58(3): 349–355.
34. Lukacs B, Loeffler J, Bruyère F et al. Photoselective Vaporization of the Prostate with GreenLight 120-W Laser Compared with Monopolar Transurethral Resection of the Prostate: A Multicenter Randomized Controlled Trial. Eur Urol 2012; 61(6): 1165–1173.
35. Capitán C, Blázquez C, Martin MD et al. GreenLight HPS 120-W laser vaporization versus transurethral resection of the prostate for the treatment of lower urinary tract symptoms due to benign prostatic hyperplasia: a randomized clinical trial with 2-year follow-up. Eur Urol 2011; 60(4): 734–739.
36. Pereira-Correia JA, de Moraes Sousa KD, Santos JB et al. GreenLight HPSTM 120-W laser vaporization vs transurethral resection of the prostate (<60 mL): a 2-year randomized double-blind prospective urodynamic investigation. BJU Int 2012; 110(8): 1184–1189.
37. Bachmann A, Woo HH, Wyler S. Laser prostatectomy of lower urinary tract symptoms due to benign prostate enlargement: a critical review of evidence. Curr Opin Urol 2012; 22(1): 22–33.
38. Thangasamy IA, Chalasani V, Bachmann A et al. Photoselective Vaporisation of the Prostate Using 80-W and 120-W Laser Versus Transurethral Resection of the Prostate for Benign Prostatic Hyperplasia: A Systematic Review with Meta-Analysis from 2002 to 2012. Eur Urol 2012; 62(2): 315–323.
Labels
Paediatric urologist Urology
Article was published inUrological Journal

2012 Issue 4-
All articles in this issue
- Nádory penisu spojené s výskytem dalších novotvarů
- Vedlejší účinky hormonální substituční léčby testosteronem
- Vývoj chirurgického odběru spermií u mužů s azoospermií
- Adenomatoidní tumor varlete – diagnostika a doporučené operační postupy
- Vaporizace prostaty pomocí zeleného laseru (GreenLight laser) – zkušenost z jednoho centra po provedení více než 1 000 výkonů
- Syntetický miduretrální sling při léčbě močové inkontinence u žen: analýza 1 000 případů z jednoho centra
- Virulentný profil a rezistencia Escherichia coli izolovaných od imunokompromitovaných pacientov pri urosepse
- Sekvence léčby a sledování pacienta s metastatickým kastračně rezistentním karcinomem prostaty
- Urological Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Vedlejší účinky hormonální substituční léčby testosteronem
- Adenomatoidní tumor varlete – diagnostika a doporučené operační postupy
- Vaporizace prostaty pomocí zeleného laseru (GreenLight laser) – zkušenost z jednoho centra po provedení více než 1 000 výkonů
- Vývoj chirurgického odběru spermií u mužů s azoospermií
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

