-
Medical journals
- Career
Vývoj chirurgického odběru spermií u mužů s azoospermií
: V. Sobotka; J. Heráček
: Urol List 2012; 10(4): 15-18
Přehledový článek se zabývá vývojem chirurgického odběru spermií po zavedení techniky ICSI koncem 70. let minulého století. Tento způsob přímého vpichu spermie do vajíčka umožňuje oplození jednoho vajíčka jednou spermií. Metoda mimotělního oplodnění umožňuje počít geneticky vlastní děti i mužům, kteří trpí nejvážnějšími poruchami spermatogeneze, včetně mužů s neobstrukční azoospermií. Skupina těchto mužů byla do té doby vyloučena z možnosti reprodukce a možnost oplození byla pouze pomocí dárcovských spermií. ICSI je proto právem považována za jeden z milníků v asistované reprodukci. Pro urology se tím otevřela možnost týmové spolupráce s gynekology zabývajícími se reprodukční medicínou. Během čtvrtstoletí dospěl vývoj chirurgického odběru spermií k metodě microTESE. Metoda je nejefektivnější z pohledu ziskovosti spermií, je také nejšetrnější ke tkání a vaskularizaci varlete. Při provádění tohoto výkonu jsou minimalizovány časné (krvácení) i pozdní komplikace (poruchy vaskularizace, hypotrofie varlete a snížení produkce testosteronu). Článek popisuje jednotlivé techniky s hodnocením kladů a záporů jednotlivých postupů. V závěru autor seznamuje se svými zkušenostmi při získávání spermií za posledních 18 let.
Klíčová slova:
ICSI - neobstrukční azoospermie - metody chirurgického odběru spermií - TESEICSI
Koncem 80. let minulého století, po rutinním zavedení metody ICSI (obr. 1) do humánní medicíny [1], se snížil požadavek na množství spermií potřebné k mimotělnímu oplození minimálně o pět řádů. Ve zjednodušeném pohledu je k oplození jednoho vajíčka potřebná jediná spermie.
1. ICSI – vlevo „holding“ pipeta držící oocyt, vpravo mikropipeta s nasátou spermií připravena k injekci spermie do vajíčka. 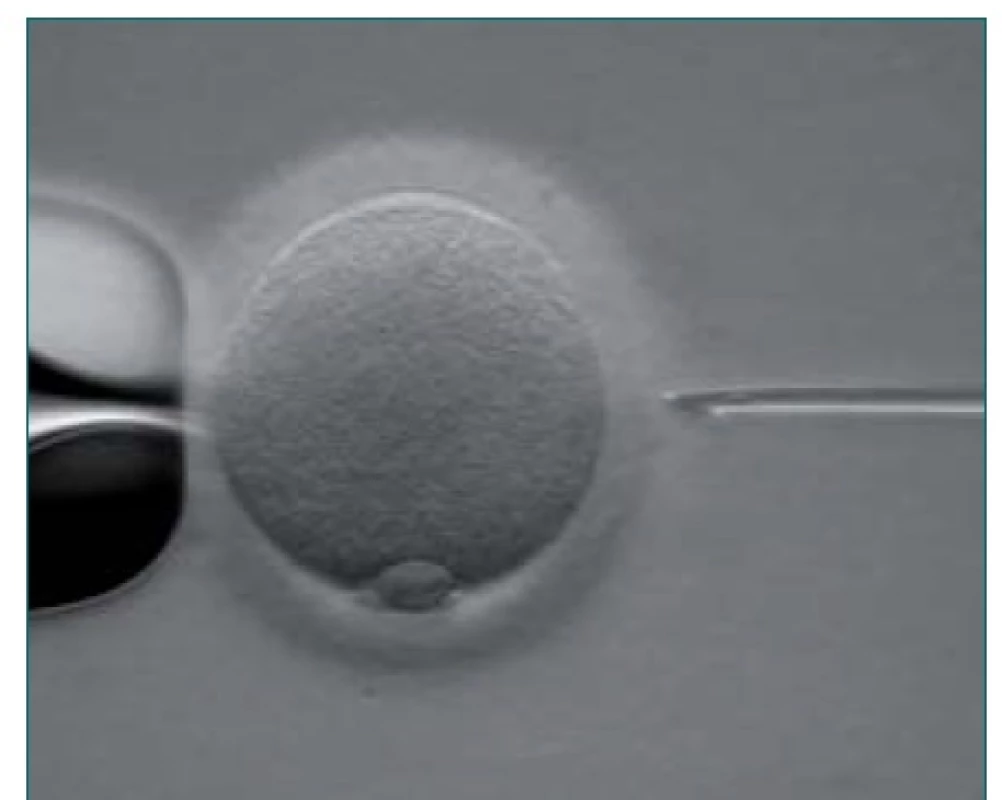
Pod tlakem nadějných výsledků fertilizace po ICSI [1–6] byly během velmi krátkého období zaváděny invazivní metody zisku spermií buď perkutánní (punkční), nebo otevřenou cestou.
PERKUTÁNNÍ TECHNIKY
U NOA je principem perkutánních metod proniknutí standardní punkční jehlou (PESA, RETA) nebo tenkou jehlou (FNA) přes kůži do varlete. Následným krokem je pak odsátí částí kanálků nebo jejich obsahu. V případě, že kanálky obsahují spermie, jsou tyto pak i obsaženy v punktátu [7–11,13].
Tyto přístupy jsou používány stále a jako jejich výhoda je zdůrazňována „nenáročnost“ na prostory, kde jsou odběry prováděny a na kvalifikaci a erudici provádějícího lékaře (nejedná se často o urology). Výkony jsou prováděny v místním znecitlivění, a není tedy nutná přítomnost anesteziologa se zázemím. Pacienty jsou tyto výkony často vnímány jako výkony ne operační, ale „pouze“ jako punkce nebo vpich. Požadavky na personální a přístrojové laboratorní vybavení jsou omezeny pouze na mikroskop a případně kryokonzervační zařízení.
Na druhou stranu jsou tyto metody zatíženy malou výtěžností, která je poplatná nemožností výběru lokality pro punkci. Jedná se o výkony „naslepo“ a šance na zisk je limitovaná množstvím kanálků, ze kterých je obsah získáván. Metody byly proto modifikovány tak, aby opakovanými manipulacemi jehlou mohlo být odsáto větší množství kanálků ve větším počtu lokalit. Zvýšenou pravděpodobností nálezu spermií však nemohou být vykoupeny možné časné komplikace ve formě krácení, které je navíc nepředvídatelné. Spolu s tím jsou ve vyšší míře indukovány i komplikace pozdní jako následek krvácení a poškození vaskularizace. Může se jednat o regresivní, degenerativní změny. Jako přímý důsledek těchto pozdních komplikací jsou popisovány atrofie s následným snížením hladiny testosteronu se všemi negativními dopady na organizmus muže [11].
TESE
Nejrozšířenější metodou zisku spermií při NOA je TESE (obr. 2). Jedná se o metodu „otevřenou“, „naslepo“, kdy jsou získávány kanálky varlete z několika incizí tuniky albuginey [9,11]. Získaná tkáň varlete je pak v laboratoři mechanicky zpracována a jsou vyhledávány spermie. Dle výsledku nálezu spermií je korigován další postup operatéra (opakované incize, výkon na druhostranném varleti).
2. TESE po natětí tuniky albuginey odběr kanálků z periferní části varlete. 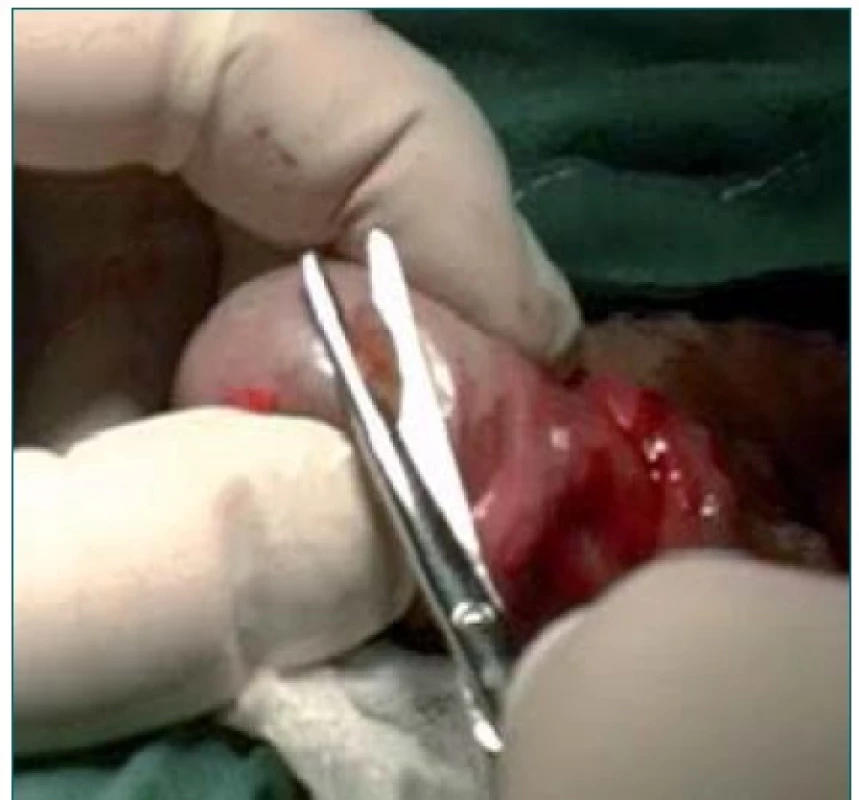
Výhodou této metody oproti punkčním technikám je možnost exaktního ošetření případného krvácení, a tím možnost minimalizace pozdních komplikací, dále je možnost zisku většího množství materiálu bez další traumatizace při nálezu spermií v dané lokalitě. Efektivnost metody je oproti perkutánním přístupům vyšší. Na druhé straně jsou popisovány možné negativní dopady vícečetných biopsií s možností odběru většího množství materiálu, ale i vyšší možností porušení vaskularizace [9].
Jako nevýhody jsou dále zdůrazňovány vyšší požadavky na prostorové a přístrojové vybavení (zákrokový sál, vybavená laboratoř). Personální požadavky jsou vyšší o nutnou přítomnost anesteziologa, urologa, pracovníků zákrokového sálu a laboratorního týmu. Standardně jsou výkony prováděny v celkovém znecitlivění, v lokální anestezii pouze z medicínské indikace nebo na přání pacienta. Výkony by měl provádět zkušený urolog a z toho vyplývá vyšší požadavek na erudici operatéra a tým zákrokového sálu. Nezbytností je personální obsazení laboratoře vyškoleným personálem. Jako nevýhoda je zdůrazňována vyšší cena, která odpovídá vyšším požadavkům na prováděný výkon. Stále zůstává zásadní nevýhodou výběr lokality „naslepo“, bez možnosti nalezení ložisek s předpokládanou zachovalou fokální spermatogenezí, a s tím je spojena nutnost odběru většího množství materiálu [9,11].
MICROTESE
V roce 1999 byla poprvé publikována metoda zisku spermií na otevřeném varleti pod optickou kontrolou se zvětšením 20–25× (obr. 3) [9]. Je zajímavé, že důvodem mikrochirurgického přístupu nebyl předpoklad vyšší ziskovosti spermií, ale snaha o cévy šetřící postup, který by zaručoval menší míru pozdních komplikací ve smyslu snižování produkce testosteronu po porušené vaskularizaci. Jako „vedlejší produkt“ hodnocení výsledků byl zjištěn signifikantně vyšší zisk spermií při microTESE oproti konvenční TESE [9]. Na ještě poměrně malých souborech v roce 1999 byl zisk spermií ze 45 % po standardní TESE zvýšen na 63 % při použití mikrodisekce. U 35 % mužů byla možnost získat spermie pouze díky metodě microTESE. Při první studii u 49 mužů byla také prokázána o 13 % vyšší míra fertilizace po použití spermií získaných mikrodisekční technikou [9].
3. MicroTESE na rozevřeném varleti po natětí tuniky albuginey tupě preparováno ložisko s dilatovanými kanálky, vlevo oplach fyziologickým roztokem. 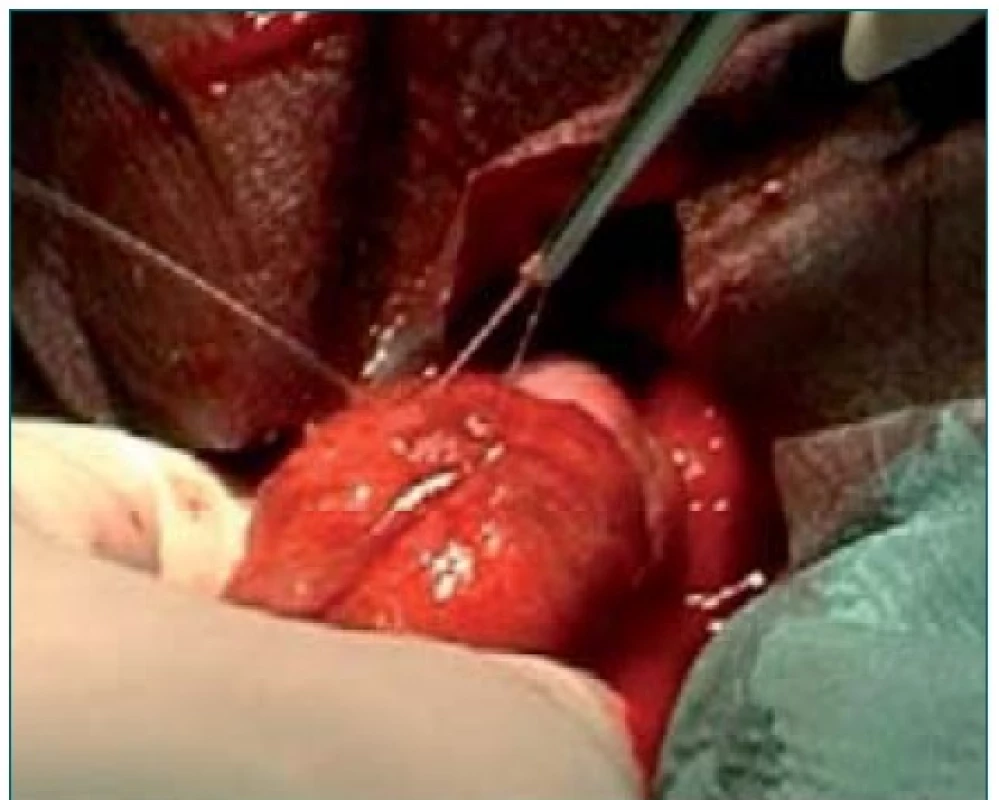
Princip metody popisuje Schlegel v možnosti rozlišení kanálků obsahujících pouze Sertoliho buňky oproti kanálkům s kompletním souborem buněk umožňujících spermatogenezi. Toto rozlišení je možné až při optickém zvětšení 20–25×. Tyto kanálky jsou v mikroskopickém obraze objemnější a méně průhledné (obr. 4) [9].
4. MicroTESE, ložisko dilatovaných mléčně zbarvených kanálků s nálezem motilních spermií muže s azoospermií, Klinefelterův syndrom. 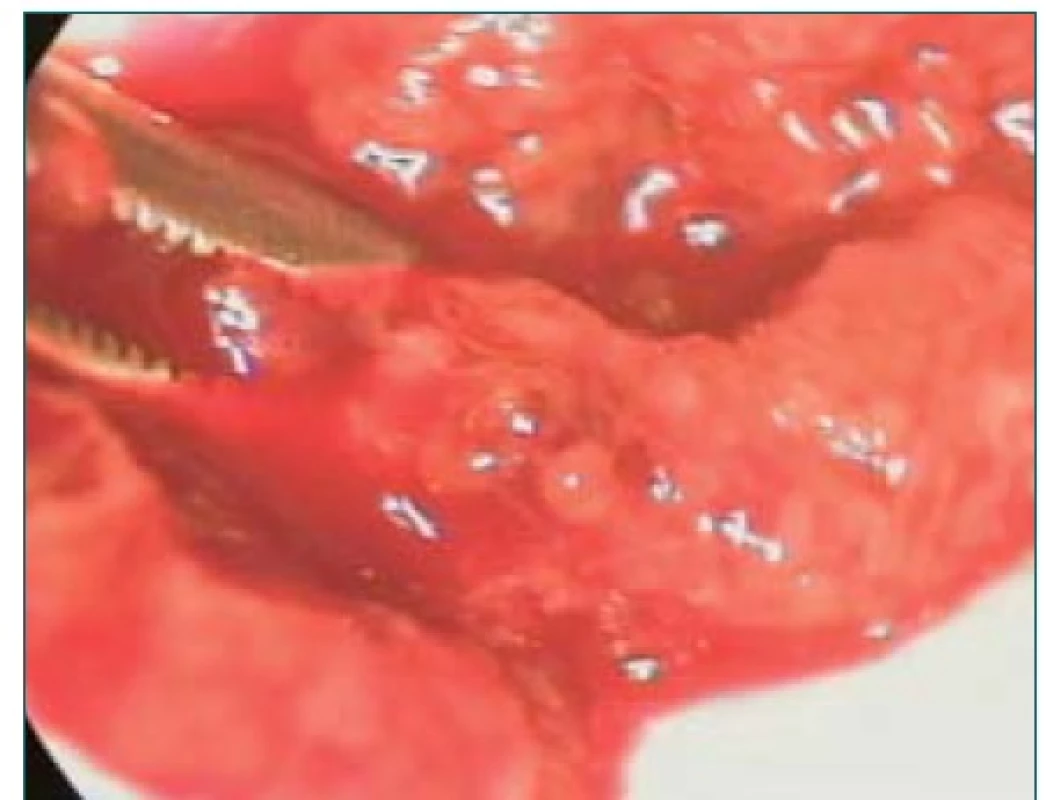
5. Výsledek fluorescenční in situ hydridizace jedné buňky embrya s označenými chromozomy X, Y, 13, 18, 21. Jedná se o embryo ženského pohlaví se správným počtem označených chromozomů. 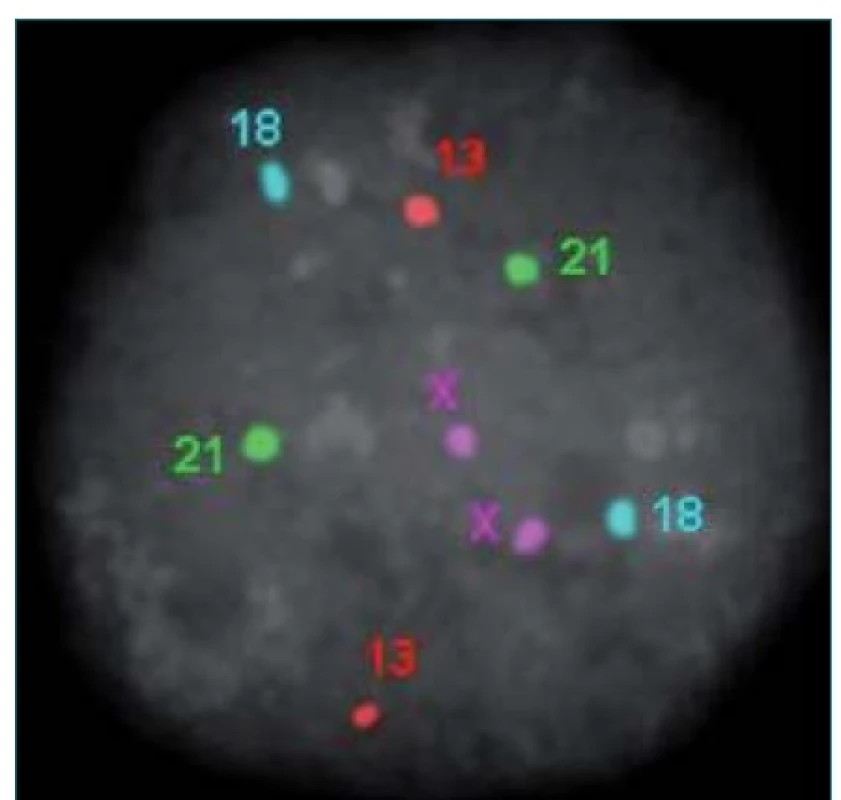
Efektivnost zisku spermií, která umožňuje odběr mnohonásobně menšího objemu tkáně nutné k zisku spermií, je mimořádně výhodná u pacientů s malými varlaty, zejména u Klinefelterova syndromu.
Již v závěrech této studie bylo uvedeno, že otevřené biopsie mají vyšší pravděpodobnost nálezu spermií než punkční techniky a mikrodisekční technika zvyšuje dále výtěžnost otevřených biopsií při minimalizaci poruch vaskularizace [9].
V roce 2009 publikoval Schlegel mikrodisekční techniku při otevřené biopsii varlete jako revoluční řešení na základě výsledků, kdy udává 60% úspěšnost zisku spermií u NOA a 70% zisk spermií u pacientů s Klinefelterovým syndromem. Tato metoda je prezentována jako nejbezpečnější postup při zisku spermií u NOA [11].
NOA se zpravidla vyznačuje snížením objemu varlat a elevací FSH. Udávaný výskyt je u 1 % mužů, přitom je však u 60 % mužů s tímto postižením spermatogeze zachována. Porušená spermatogeneze nepostihuje všechny lokality varlete stejně. Je prokázáno, že nejtěžší formy poruchy plodnosti u mužů provází reziduální fokální spermatogeneze, která je omezená pouze na určitou lokalitu bez komunikace s nadvarletem. Tento fakt vysvětluje příčinu absence spermií v ejakulátu [11].
Pokud je důvodem NOA varikokéla, je doporučována její korekce. Vzhledem k dynamice spematogeneze je doporučený odstup k hodnocení výsledku řešení varikokély alespoň šest měsíců. Je popsáno, že v méně než 10 % případů je obnovena spermatogeneze s nálezem spermií v ejakulátu [11].
Zajímavý soubor výsledků je ukázán na skupině 64 mužů po prodělané chemoterapii různých typů a pro různá onemocnění. Spermie byly získány ve více než polovině případů (53 %) s dosažením 40 % klinických těhotenství. Vyšší míra zisku spermií byla popsána u germinálních nádorů (73 %) oproti lymfomu (48 %) [11].
Zajímavé jsou výsledky microTESE po neúspěšné standardní TESE, kdy při předchozích 1–2 provedených výkonech TESE byl popsán zisk spermií u 50 %, po třech a více provedených biopsiích byla ziskovost stále ještě 22 %. Ukazuje to nevýhodu „naslepo“ prováděných výkonů, ale zvyšující se šanci při opakovaně provedených výkonech. Zcela jasně však potvrzují výsledky efektivnost metody microTESE při možnosti výběru tkáně pod optickou kontrolou operačního mikroskopu při 20–25násobném zvětšení.
Hladiny FSH, jako jednoho z predikčních faktorů, byly analyzovány ve studii Cornellovy univerzity ve vztahu k zisku spermií. Bylo popsáno, že hodnoty do 15 IU/l jsou předpokladem menšího zisku spermií (51 %), pravděpodobně pro konzistentnější zástavu spermatogeneze, často na podkladě genetických abnormalit. U skupiny s hladinou 15 UI/l a výše je míra zisku spermií popsána u 63 % mužů s NOA [11].
Jako limitující faktor k použití metody microTESE považuje Schlegel výsledek genetických vyšetření, kdy je testován rutinně Y chromozom na mikrodelece. Přítomnost delecí v lokusech a,b vylučuje prakticky nález spermií, ale u mikrodelecí v oblasti AZF c je standardní zisk spermií okolo 60 % [11].
ZÁVĚR
Na našem pracovišti byla zavedena metoda chirurgického zisku spermií konvenční TESE od roku 1996 (obr. 2) a od roku 2004 používáme při řešení NOA standardně techniku microTESE s použitím operačního mikroskopu ZEISS s optickým zvětšením do 25× (obr. 3). Do současnosti jsme provedli 280 výkonů microTESE. Naší snahou je maximální výtěžnost při chirurgickém zisku spermií spolu s minimalizací jak časných, tak pozdních komplikací. V současné době považujeme metodu microTESE za jedinou, která umožňuje vyhovět všem těmto požadavkům. Na našem pracovišti jsme nikdy nepoužívali punkční perkutánní techniky k zisku spermií s NOA.
V souladu s literaturou a názorem klinických genetiků považujeme za zásadní prognostický faktor hladinu FSH, výsledky urologických a genetických vyšetření.
U pacientů s NOA, kde je plánovaná microTESE, provádíme standardně vyšetření hormonálního souboru (testosteron, folikulostimulační hormon, luteinizační hormon, prolaktin) a genetické poradenství s genetickými vyšetřeními (karyotyp, vyšetření genu pro cystickou fibrózu a vyšetření Y chromozomu na mikrodelece v oblastech AZF a,b,c).
Tato vyšetření považujeme za zásadní a výsledek genetického vyšetření jako limitující pro použití spermií. Klinickým genetikem je doporučen předimplantační genetický screening nebo diagnostika embryí, která vznikla po oplození spermiemi chirurgicky získanými při neobstrukční azoospermii k vyloučení aneuploidií u sledovaných chromozomů (obr. 4) [12].
Podmínkou převzetí, zpracování a skladování spermií a tkání jsou předem provedená serologická vyšetření v rozsahu dle níže uvedeného zákona.
V České republice je zisk, skladování a propouštění spermií vázáno na vydání rozhodnutí SÚKL o schválení pracoviště jako tkáňového zařízení dle požadavků zákona 296/2008 Sb.
Tento zákon řeší v rámci tkáňové direktivy EU v jednotlivých státech vyšetření pacientů, jejichž tkáně jsou přijímány, zpracovávány, skladovány a propuštěny. Dále jsou předmětem auditů samotné prostory laboratoří, personální vybavení, zavedení pracovních postupů a postupy samotné a management používaného kritického materiálu (materiál, který přichází do přímého styku s tkáněmi a buňkami). Na základě osobních zkušeností a sdělení zahraničních kolegů je přístup k výkladu zákona SÚKL jeden z nejpřísnějších, domníváme se tedy, že v České republice lze vyloučit neprofesionální nakládání se spermiemi a tkáněmi, a tím je minimalizována možnost poškození pacientů a jejich vzorků.
Zkratky
ICSI intracytoplasmatic sperm injection
FNA fine needle aspiration
microTESE microdissectional testicular sperm extraction
NOA nonobstructive azoospermia
PGD preimplantation genetic diagnosis
PGS preimplantation genetic screening
RETA rete testis aspiration
TESA testicular sperm aspiration
TESE testicular sperm extraction
MUDr. Vladimír Sobotka
Pronatal s. r. o., oddělení reprodukční medicíny
Na Dlouhé mezi 4
147 00 Praha 4
sobotka@pronatal.cz
Sources
1. Lanzendorf SE, Maloney MK, Veeck LL et al. A preclinical evaluation of pronuclear formation by microinjection of human spermatozoa into huma oocytes. Fertil Steril 1988; 49(5): 835–842.
2. Palermo G, Joris H, Devroey P et al. Pregnancies after intracytoplasmic injection of a single sperrmatozoon into an oocyte. Lancet 1992; 230(8810): 17–18.
3. Palermo G, Joris H, Derde MP et al. Sperm characteristics and autosome of human assisted fertilization by subzonal insemination and intracytoplasmic sperm injection. Fertil Steril 1993; 59(4): 826–835.
4. Van Steirteghem AC, Liu J, Nagy Z et al. Use of assisted fertilization. Hum Reprod 1993; 8(11): 1784.
5. Van Steirteghem AC, Liu J, Joris H et al. Higher success rate by intracytoplasmatic sperm injection than by subzonal insemination. Report of a second series of 300 consecutive treatment cycles. Hum Reprod 1993; 8(7): 1055–1060.
6. Van Steirteghem AC, Nagy Z, Joris Het al. High fertilization and implantation rates after intracytoplasmatic sperm injection. Hum Reprod 1993; 8(7): 1061–1066.
7. Friedler S, Razier A, Strassburger D et al. Testicular sperm retrieval by percutaneaus fine needle sperm aspiration compared with testicular sperm extraction by open biopsy in men with non-obstructive azoospermia. Hum Reprod 1997; 12(7): 1488–1493.
8. Schlegel PN. Physiological consequenses of testicular sperm extraction. Hum Reprod 1996; 11(Abstr book 1): 74.
9. Schlegel PN. Testicular sperm extraction: microdissection improves sperm yield with minimal tissue excission. Hum Reprod 1999; 14(1): 131–135.
10. Tournaye H, Verheyen G, Nagy P et al. Are there any predictive factors for succeful surgical sperm recovery in azoospermic patients? Hum Reprod 1997; 12(1): 80–86.
11. Schlegel PN. Nonobstructive azoospermia: A Revolutionary Surgical Approach and Results. Semin Reprod Med 2009; 27(2): 165–170.
12. Verlinsky I, Kuliev A. Preimplantation Diagnosis of Genetic Diseases: a New Technique in Assisted Reproduction. New York: Wiley-Liss 1993.
13. Brindsen PR. Textbook of in vitro Fertilization and Assisted Reproduction. Third Edition 2007 : 45–52.
Labels
Paediatric urologist Urology
Article was published inUrological Journal

2012 Issue 4-
All articles in this issue
- Penile cancers associated with occurrence of other neoplasms
- Adverse events of hormone replacement testosterone therapy
- Development of surgical retrieval a men's sperm with azoospemia
- Testicular adenomatoid tumor – diagnosis and operating procedures
- Vaporizace prostaty pomocí zeleného laseru (GreenLight laser) – zkušenost z jednoho centra po provedení více než 1 000 výkonů
- Syntetický miduretrální sling při léčbě močové inkontinence u žen: analýza 1 000 případů z jednoho centra
- Virulent profile and resistance of Escherichia coli isolated in immunocompromised patients with urosepsis
- Sequencing of therapy and follow-up in patients with metastatic castrate resistant prostate cancer
- Urological Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Adverse events of hormone replacement testosterone therapy
- Testicular adenomatoid tumor – diagnosis and operating procedures
- Vaporizace prostaty pomocí zeleného laseru (GreenLight laser) – zkušenost z jednoho centra po provedení více než 1 000 výkonů
- Development of surgical retrieval a men's sperm with azoospemia
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

