-
Medical journals
- Career
Problematika urolitiázy u dětského pacienta: přinesla moderní doba nové možnosti?
Authors: MUDr. Květoslav Novák
Authors‘ workplace: Urologická klinika 1. LF UK a VFN, Praha
Published in: Urol List 2007; 5(1): 22-25
Overview
Urolitiáza v dětském věku není časté onemocnění, má však vysoký stupeň recidivity. Nejčastější příčinou vzniku jsou metabolické poruchy, často v kombinaci s jinými faktory (obstrukční uropatie, infekce). Dominantní léčbou je litotrypse extrakorporální rázovou vlnou, endoskopická léčba (ureteroskopie, perkutánní extrakce konkrementu) má díky vývoji endoskopů a možnostem intrakorporální litotrypse stále větší význam. Léčbu je nutné indikovat přísně individuálně s ohledem na možné komplikace. Zásadní je kompletní odstranění konkrementu a následné metabolické vyšetření.
Klíčová slova:
urolitiáza u dětí, extrakorporální litotrypse rázovou vlnou, ureteroskopie, perkutánní extrakce konkrementuÚVOD
Diagnostika i léčba urolitiázy v dětském věku má svá specifika, její výskyt je většinou spojen s nálezem metabolických abnormalit (až 90 %), obstrukčních uropatií (10–40 %) a infekce močových cest [1]. S tím souvisí vysoká recidivita onemocnění v průběhu celého života.
Naprosto dominantní metodou léčby je od konce 80. let minulého století litotrypse extrakorporální rázovou vlnou (ESWL - extracorporeal shock wave lithoripsy). V českém jazyce zdomácněla zkratka LERV - litotrypse extrakorporální rázovou vlnou. Společně s technickým pokrokem a miniaturizací nástrojů přibývá i endoskopické léčby - perkutánní extrakce konkrementu (PEK, v cizojazyčné literatuře PCNL - percutaneous nephrolithotomy), ureteroskopie (URS - - ureterorenoscopy). Vzhledem k povaze tohoto onemocnění závisí úspěch léčby nejen na odstranění urolitiázy, ale i na eradikaci infekce močových cest a korekci metabolických i anatomických abnormalit.
EPIDEMIOLOGIE A ETIOPATOGENEZE UROLITIÁZY U DĚTÍ
Urolitiáza není u dětí tak časté onemocnění jako mezi dospělými (prevalence 5–10 %) a tvoří asi 1–3 % urolitiázy v populaci. V české republice je incidence 5,8 nových pacientů na 100 000 dětí za rok [2]. Není tak zřetelná predominance výskytu u mužského pohlaví (M:F 1,5–2 : 1) jako je tomu u dospělých (M:F 3 : 1). Onemocnění se manifestuje nejčastěji ve věkové skupině nad 13 let (59 %), nejméně u mladších 3 let (4 %) [3].
Vznik urolitiázy je multifaktoriální. Nejčastější příčinou vzniku jsou metabolické poruchy (tab) - izolovaně nebo sdružené s jinými nemocemi či jejich léčbou (např. revmatoidní artritida, rachitida, novorozenecká nezralost, imobilizace z různých příčin), dalšími jsou lokální faktory (obstrukční uropatie, dřeňová cystóza, infekce močových cest), nízký objem moči, rodinný výskyt, geografické vlivy a vzájemná kombinace těchto rizikových faktorů. Specifickou skupinu tvoří pacienti po předchozích augmentačních a derivačních výkonech (neurogenní močový měchýř), u kterých je častá litiáza i v dolních močových cestách (cystolitiáza, uretrolitiáza).
KLINICKÝ OBRAZ A DIAGNOSTIKA
Klinická manifestace nebývá u pediatrických pacientů tak dramatická jako u dospělých. Ledvinná kolika je projevem jen u pětiny pacientů, většinou je nálezem mikroskopická hematurie (33–90 %) v kombinaci s bolestmi břicha, bederní krajiny nebo bolestmi v pánvi (50 %, často až v adolescenci), zřídka makrohematurie. Pacienti s vyjádřenými symptomy urolitiázy jsou starší a častěji mají pozitivní rodinnou anamnézu [4]. Kromě fyzikálního a laboratorních vyšetření jsou v průkazu urolitiázy dominantní zobrazovací vyšetření - ultrasonografie (USG), nativní nefrogram (NN), vylučovací urografie (IVU), nekontrastní (tzv. nativní) komputerová tomografie (NCCT). Každá z těchto metod má své výhody a nevýhody s ohledem na požadavek stanovení diagnózy urolitiázy (senzitivita a specificita metody) a plánování léčby (míra obstrukce, velikost konkrementu, lokalizace, přítomnost infekce atd). V době diagnózy se nachází 2/3 konkrementů v ledvině.
Nativní nefrogram zjistí jen kontrastní konkrementy velikosti nad 2 mm, u cystinu nad 3–4 mm, senzitivitu pro ureterolitiázu má jen v 52 %. IVU je hodnotná z hlediska stanovení morfologie močových cest, odhalení abnormalit, obstrukce, polohy konkrementu a odhadu renální funkce. Nevýhodou je nutnost jiného zobrazení při afunkci ledviny (CT, ascendentní ureteropyelografie - APG), potenciální toxicita a alergická reakce na kontrastní látku, časová náročnost.
Senzitivita metody při renální kolice je 64 %. Ultrazvukem prokážeme jen 70 % litiázy identifikovatelné na NN a senzitivita pro ureterolitiázu je pouze 19 %, nedeteguje 41 % symptomatické urolitiázy [4,5]. Výhodou NCCT je rychlé a bezpečné vyšetření, senzitivita až 100 %, specificita 98 %, dále možnost diagnostiky i neurologických příčin obtíží (apendicitida, ovariální cysta atd.). Zároveň je možno získat data v různých rovinách s možností 3D-rekonstrukce, podle denzity konkrementu lze odhadnout jeho složení a fragilitu a tak i plánovat vhodnou léčbu. Lze říci, že NCCT je nejlepší metodou pro zobrazení urolitiázy horních močových cest, je vhodné pro informaci o malých konkrementech v močovodu bez zjevné obstrukce. Pro pacienty vyžadující aktivní léčbu ale NCCT nestačí, nevede k identifikaci všech ovlivňujících faktorů - zde je komplexnější IVU i vzhledem k dynamické povaze vyšetření. Při abnormálních anatomických poměrech u větší litiázy a po selhání léčby je přínosem 3D-kontrastní CT. Rozhodování o indikaci je ovlivňováno i dalšími faktory, jako jsou např. sepse.
Table 1. Faktory vzniku urolitiázy. 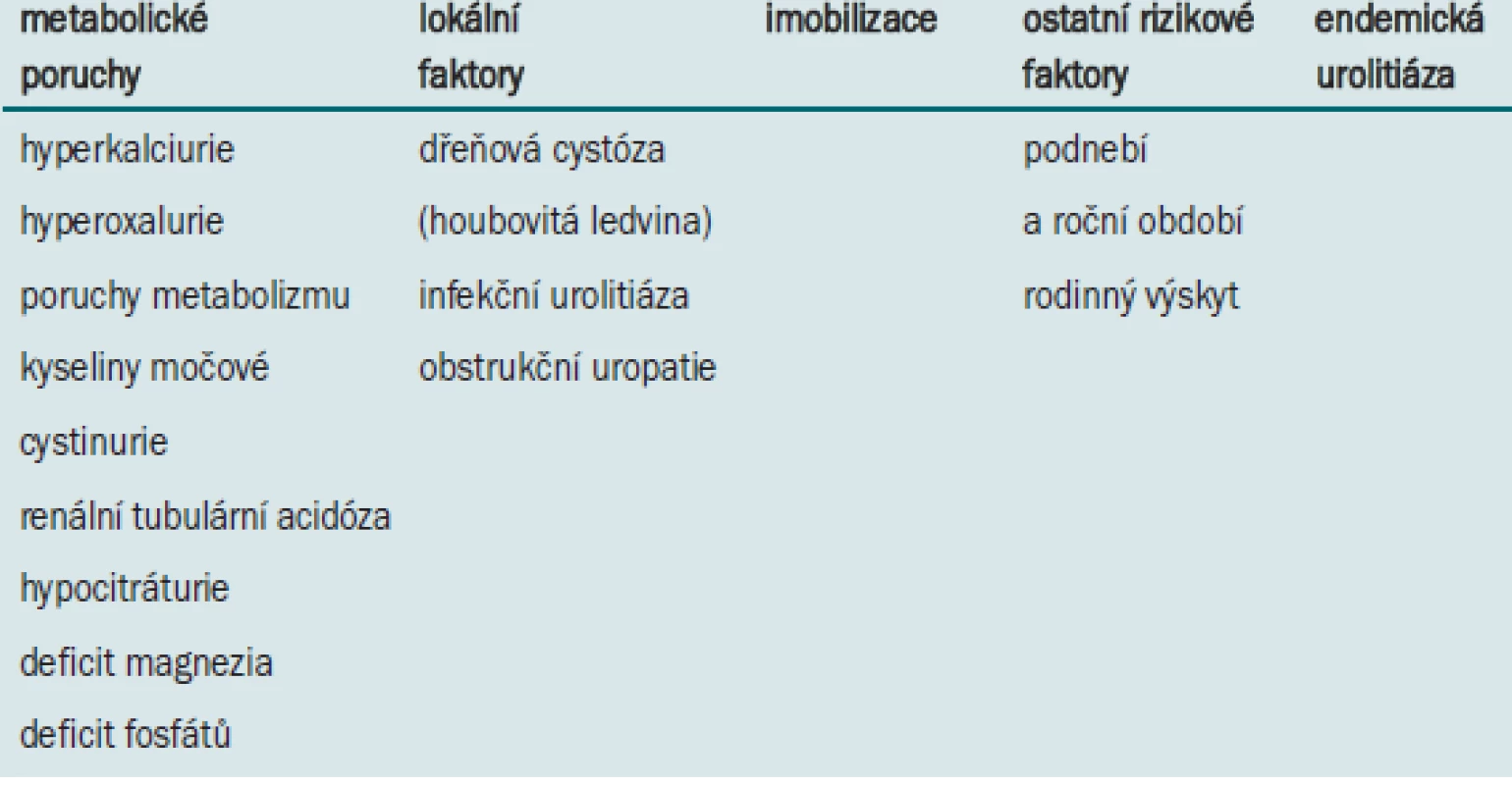
KONZERVATIVNÍ LÉČBA
Spontánní odchod konkrementu nastane asi v 50 %. U dětských pacientů vzhledem k rozdílným fyzickým parametrům lze jen těžko stanovit hranici velikosti litiázy, která by měla šanci ke spontánnímu odchodu. Obecně zde platí, že konkrement velký 4 mm bude zřejmě vyžadovat intervenci [1]. Konzervativní postup je indikován v případě, kdy předpokládáme spontánní odchod konkrementu, a v případě, kdy mají být zmírněny obtíže pacienta před dalším vyšetřením (např. IVU). K podpoře spontánního odchodu jsou kromě nesteroidních antirevmatik (ibuprofen, diklofenak), analgetik a spazmolytik recentně indikovány kombinace léků k redukci edému a inhibici spazmů ureteru indukovaných konkrementem - medikamentózní expulzivní terapie (kostikosteroid + tamsulozin - alfa-1-adrenergní antagonista) [6,7]. U dětských pacientů zatím nemáme s touto léčbou zkušenosti.
OPERAČNÍ LÉČBA
V případě symptomatické litiázy s febriliemi je nutné zajistit derivaci močových cest; definitivní řešení obstrukce močovodu indikujeme po derivaci, léčbě infekce a odeznění akutního stavu, až s odstupem několika dní.
Definitivní operační léčba je založena na neinvazivních či miniinvazivních endoskopických metodách. Indikace k jednotlivým výkonům je individuální, nejdůležitějšími rozhodujícími faktory jsou velikost, lokalizace a složení konkrementu, přítomnost anatomických abnormalit, obstrukce, infekce močových cest, fyzické parametry pacienta a v neposlední řadě též dostupnost metody či vhodného instrumentária a zkušenosti operatéra se zvolenou metodou.
EXTRAKORPORÁLNÍ LITOTRYPSE RÁZOVOU VLNOU
Většina urolitiázy u dětí je léčena neinvazivní ESWL. Úspěšné provedení ESWL u dítěte bylo publikováno již v roce 1986. Nyní je tento výkon metodou volby při řešení nefro - a ureterolitiázy u dětí. Není zde věkové omezení pro použití rázové vlny (nejmladší pacient ESWL ve 4 měsících věku), dosud nebyly zjištěny dlouhodobé nežádoucí účinky ESWL (hypertenze, alterace růstu ledviny či její funkce, alterace růstu z poškození růstové chrupavky) [8,9]. U velmi malých pacientů je zapotřebí vykrýt plíce tak, aby nedošlo k jejich kontuzi a hemoptýze [1]. V poslední dekádě je takto léčeno více než 80 % urolitiázy u dětí [1,10,11]. Kontraindikace se shodují s kontraindikacemi u dospělých pacientů, výkon se u menších dětí (obvykle pod 10 let) provádí v celkové anestezii, u větších v sedoanalgezii. Energie rázové vlny může být nižší vlivem nižšího napětí, mohou zde být ovšem rozdíly dané použitým přístrojem. Podle toho se liší i počet rázů.
U dětí odcházejí fragmenty konkrementu i při větší relativní velikosti lépe než u dospělých, většina nevyžaduje rutinní stenting močovodu. Vzhledem ke kratšímu trvání onemocnění dochází také k lepší fragmentaci, větší fragilitě konkrementu a nižší impedanci tkání vůči rázové vlně. Nesignifikantní fragmenty jsou u dětských pacientů pod 3 mm, fragmenty 4 mm a větší je obvykle nutno řešit. Zde však nelze definovat striktní hranici vzhledem ke značné věkové a fyzické variabilitě dětské populace léčené ESWL.
Výsledky u dětí jsou hodnoceny stejně jako v dospělé populaci, nejdůležitějšími parametry jsou procentuální úspěšnost v očištění ledviny či močovodu od fragmentů po 3měsíčním sledování (SFR - - stone free rate), efektivnostní kvocient (EQ) - počítaný parametr beroucí v úvahu i pomocné před - a pooperační výkony, opakování výkonu (RR - retreatment rate). Obecně jsou výsledky léčby výborné. Jediným signifikantním faktorem, který ovlivňuje úspěšnost léčby, je velikost konkrementu [1,10]. Podle různých studií je SFR 67–99 % při RR 10–30 %, u mladších pacientů se zdají být výsledky lepší (93,3 % u pacientů pod 5 let, 76,5 % u 11–14letých). Ve srovnání s dospělými lze u dětí dosáhnout u konkrementů nad 10 mm clearance rate (CR) až 95 % (versus 78,9 % u dospělých) [1,12]. Sami jsme prezentovali soubor 137 pacientů ve věku 3–18 let, úspěšnost byla u nefrolitiázy 88 % po první době litotrypse, v případě ureterolitiázy 95 %, dezintegrovány byly všechny druhy konkrementů včetně cystinu, steinstrasse jsme invazivně řešili jen u 4 pacientů [13]. Izolované výsledky léčby litiázy dolního kalichu se liší (SFR 56 %), za nejvýznamnější faktor ovlivňující SFR je považována délka dolního kalichu [1,12,14].
U odlitkových konkrementů monoterapie ESWL dosahuje SFR až 83 % (u dospělých 22–63 %) [1]. Nevýhodou je obvykle nutnost auxiliárních výkonů (stenting, řešení steinstrasse) - 7–33 % [12]. Zde je PCNL úspěšnější - SFR 67–92 %. U dětí je vyšší pravděpodobnost recidivy, přibližně třetina in situ stagnujících fragmentů narůstá během 24–48 měsíců a stejný počet pacientů se stává klinicky symptomatickým. Pacienti s rizikovými faktory jako jsou velký konkrement a anatomická abnormalita by tedy měli být léčeni spíše endoskopicky [1].
ESWL je dětskými pacienty dobře tolerována, morbidita je minimální. Kolika po výkonu není pravidlem, incidence hematurie (40 %) je nižší než u dospělých. Steinstrasse v močovodu je léčena podle pravidel vyplývajících z klinické situace stejně jako u dospělých.
K ESWL jsou nejčastěji indikovány konkrementy v horních močových cestách do 500 mm2 (cca 12 mm průměr), větší nefrolitiáza může vyžadovat více pomocných výkonů pro možné komplikace (steinstrasse, signifikantní reziduální fragmenty). Samostatnou kapitolou je léčba litiázy dolního kalichu, kde je nutné zohlednit morfologii této části dutého systému, při nepříznivých parametrech (dlouhý a úzký kalich, ostrý kalichopánvičkový úhel) je indikována PCNL. ESWL je suverénní metodou řešení ureterolitiázy v subrenálním a středním močovodu s výjimkou větších a zaklíněných konkrementů. V distálním močovodu má lepší výsledky metoda URS. Nejhůře fragilní je kalciumoxalát monohydrát (whewellit) a cystin, pro jehož dezintegraci je nutné 2–3krát větší celkové množství rázů než u jiných konkrementů. Vlastní zkušenost z našeho pracoviště ale potvrzuje dobrý léčebný efekt ESWL i u cystinu.
PERKUTÁNNÍ EXTRAKCE KONKREMENTU - PERKUTÁNNÍ NEFROLITOTOMIE
Léčba konkrementu perkutánní extrakcí (PCNL) byla u dětského pacienta poprvé popsána v roce 1985 (Woodside). Užívá se jako monoterapie nebo jako součást multimodálního přístupu u objemného konkrementu. Dříve se používalo instrumentárium pro dospělé, což způsobovalo větší krevní ztráty zejména u mladších pacientů (pod 7 let). Později se morbidita snížila díky redukci velikosti nástrojů, obvyklá šíře pracovního perkutánního kanálu je nyní 20–22 CH. Pro specifické účely jsou dostupné i nefroskopy 11–15 CH k miniperkutánním výkonům u velmi malých pacientů (tzv. miniperc). K získání přístupu do dutého systému se u dětí více využívá punkce pod ultrazvukovou kontrolou, nikoli pod skiaskopickou, aby se rentgenová expozice redukovala na co nejmenší míru [1]. K dezintegraci je v posledních letech nejvíce používán holmium:YAG laser, jehož pracovní vlákno (nejčastější velikost 365 mm) umožňuje použití i u nejmenších nástrojů, další jsou litoklast (elektrokinetický efekt) a ultrazvuková sonda. Holmium:YAG laser pracuje na principu fototermálního mechanizmu s průnikem energie na vzdálenost 0,5 mm, proto je vhodné u dětí volit co nejmenší účinnou energii k dezintegraci, aby nedošlo k poškození stěny dutého systému. Tento laser dezintegruje všechny druhy konkrementů.
Po PCNL nedochází k významnému úbytku parenchymu ledviny ani k jizvení, což bylo popsáno několika autory i přesto, že úspěšná léčba často vyžaduje založení více pracovních přístupů - až 61 % pacientů s odlitkovou litiázou [1,15]. Nejvýznamnějšími peroperačními komplikacemi je krvácení a hypotermie, oběma se dá předejít dobře zvládnutou technikou výkonu, tedy redukcí doby trvání operace, případně je užitečné výkon rozdělit do více dob - nejdříve zajistit přístup do dutého systému založením punkční nefrostomie a poté, s odstupem, řešit vlastní konkrement.
Indikace pro PCNL jsou u dětí podobné jako u dospělých - objemný konkrement, obstrukce, infekce a jejich vzájemná kombinace, dále selhání ESWL. Úspěšnost léčby (SFR) je u monoterapie odlitkové litiázy 90 %, v kombinaci s ESWL až 96 %, u menších konkrementů 1–2 cm velikosti i 100 % [15].
URETEROSKOPIE (URS)
Ureteroskopická léčba urolitiázy je u dětí preferována zejména v distálním močovodu, u větších a zaklíněných konkrementů i v proximální části. S vývojem designu ureteroskopů a jejich miniaturizací (semirigidní 4,5 CH, flexibilní 6,9 CH) a možností intrakorporální litotrypse (dominuje holmium: YAG laser) se endoskopická léčba dostává do popředí. Podle publikovaných údajů jsou ureteroskopicky léčeni pacienti již od 5 měsíců věku [16].
Při použití nástrojů menších než 8 CH není obvykle nutná dilatace ureteru nebo rutinní předoperační zavedení stentu. Po nekomplikované URS není nutné zavádět stent ani pooperačně [17].
Ve srovnání s ESWL je URS účinnější u větších či vícečetných konkrementů, má též kratší operační čas, kratší dobu expozice RTG záření a kratší interval dosažení SFR. Menší konkrementy pod 4 mm, které spontánně neodešly během 3 týdnů, jsou většinou hůře zaměřitelné a jsou indikovány k URS. Výhodou URS je též vysoká úspěšnost léčby v jednom sezení, výhodou ESWL je neinvazivita výkonu. SFR se liší podle velikosti konkrementu a ve srovnání s ESWL je vždy vyšší (nad 10 mm URS 93 %, ESWL 50 %, pod 10 mm URS 100 %, ESWL 80 %). Po URS není rutinně prováděn screening na vezikoureterální reflux, lze o něm uvažovat jen u symptomatických pacientů [1,15-20].
Dalšími možnostmi léčby jsou retrográdní intrarenální chirurgie (RIRS - retrograde intrarenal surgery). Jde o ureterorenoskopickou léčbu zejména dolní kalikolitiázy, provádí se flexibilním ureterorenoskopem. Konkrement je nejčastěji nejprve extrahován z dolního kalichu a poté denzintegrován při napřímeném průběhu flexibilního nástroje. U pediatrických pacientů jsou zkušenosti omezené, stejně tak je tomu v případě laparoskopické litotomie.
Otevřené chirurgické výkony pro urolitiázu jsou v současnosti raritní, téměř vždy jde o spojení korekce anatomické abnormality s odstraněním konkrementu.
Cystolitiáza má vysokou incidenci mezi pacienty po augmentaci močového měchýře a s kontinentní derivací moče - až 50 %. Konkrementy jsou většinou velké a tvrdé. Přístup k léčbě je transuretrální, ten však není šetrný k mužské močové trubici, nebo perkutánní suprapubický s litotrypsí. U větších konkrementů bývá efektivnější provést cystolitotomii [1].
Po každém výkonu pro urolitiázu u dítěte je vhodné snažit se získat fragment konkrementu a odeslat jej k analýze. Společně s následným metabolickým vyšetřením za 6–8 týdnů po odstranění konkrementu nám tato analýza umožní navrhnout specifická opatření (metafylaxe) k zabránění recidivy onemocnění, u augmentovaných měchýřů zavedení pravidelné irigace měchýře.
ZÁVĚR
Urolitiáza u dětí není časté onemocnění, ale vyžaduje specifický přístup. Vzhledem k větší tendenci k recidivám než u dospělých je maximální důraz kladen na kompletní odstranění konkrementu a ochranu funkcí ledvin. Nejčastější je léčba ESWL, ta však není jedinou možností léčby a díky vývoji technologií a designu nástrojů se rozšiřují indikace a možnosti o endoskopickou léčbu, která je bezpečná a efektivní. Indikace je nutno v dětském věku posuzovat zcela individuálně, s ohledem na možné komplikace, ale též s ohledem na možnosti technického vybavení daného pracoviště. Zcela zásadní je odhalení příčin vzniku urolitiázy a jejich kompenzace.
MUDr. Květoslav Novák
Urologická klinika 1. LF UK a VFN, Praha
Ke Karlovu 6, 128 08 Praha 2
e-mail: slavek.novak@seznam.cz
Sources
1. Desai M. Endoscopic management of stones in children. Curr Opin Urol 2005; 15 : 107-112.
2. Kočvara R. Urolitiáza. In: Dvořáček J et al. Urologie. 1. ed. Praha: ISV nakladatelství 1998 : 823-856.
3. Sternberg K, Greenfield SP, Williot P et al. Pediatric stone disease: an evolving experience. J Urol 2005; 174(4 Pt 2): 1711-1714.
4. Palmer JS, Donaher ER, O´Riordan MA et al. Diagnosis of pediatric urolithiasis: role of ultrasound and computerized tomography. J Urol 2005; 174(4 Pt 1): 1413-1416.
5. Bariol SV, Moussa SA, Tolley DA. Contemporary imaging for the management of urinary stones. EAU Update series 2005; 3 : 3-9.
6. Resim S, Ekebicer HC, Ciftci A. Role of tamsulosin in treatment of patients with steinstrasse developing after extracorporeal shock wave lithotripsy. Urology 2005; 66(5): 945-948.
7. Porpiglia F, Vaccino D, Billia M et al. Corticosteroids and tamsulosin in the medical expulsive therapy for symptomatic distal ureter stones:single drug or association? Eur Urol 2006; 50 : 339-344.
8. El-Assmy A, Hefez AT, Eraky I et al. Safety and outcome of rigid ureteroscopy for management of ureteral calculi in children. J Endourol 2006; 20(4): 252-255.
9. Lottmann HB, Archambaud F, Traxer O et al. The Efficacy and Parenchymal Consequences of Extracorporeal Shock Wave Lithotripsy in Infants. BJU Int 2000; 85 : 311-315.
10. Elsobky E, Sheir KZ, Madbouly K et al. Extracorporeal Shock Wave Lithotripsy in Children: Experience Using Two Second-Generation Lithotripters. BJU Int 2000; 86 : 851-856.
11. Al Busaidy SS, Prem AR, Medhat M et al. Paediatric Ureteric Calculi: Efficacy of Primary in Situ Extracorporeal Shock Wave Lithotripsy. BJU 1998; 82 : 90-96.
12. Tan AH, Al-Omar M, Watterson JD et al. Results of shockwave lithotripsy for pediatric urolithiasis. J Endourol 2004; 18 (6): 527-530.
13. Novák K, Vobořil V, Kočvara R. Extrakorporální litotrypse jeko metoda první volby řešení urolitiázy u dětí (Abstrakt). čes Urol 2000; 3 : 35.
14. Turna B, Nazli O, Simsir A et al. Impact of lower pole renal anatomy on stone clearance after shock wave lithotripsy in children (Abstrakt). Eur Urol 2006; 5(2): 187.
15. Desai MR, Kukreja RA, Petel SH et al. Percutaneous nehrolithotomy for complex pediatric renal calculus disease. J Endourol 2004; 18(1): 23-27.
16. Thomas JC, DeMarco RT, Donohoe JM et al. Pediatric ureteroscopic stone management. J Urol 2005; 174(3): 1072-1074.
17. Raza A, Smith G, Moussa S et al. Ureteroscopy in the management of pediatric urinary tract calculi. J Endourol 2005; 19(2): 151-158.
18. El-Assmy A, Hefez AT, Eraky I et al. Safety and outcome of rigid ureteroscopy for management of ureteral calculi in children. J Endourol 2006; 20(4): 252-255.
19. Minevich E, Defoor W, Reddy P et al. Ureteroscopy is safe and effective in prepubertal children. J Urol 2005; 174(1): 276-279.
20. Reddy PP. Pediatric ureteroscopy. Urol Clin N Am 2004; 31 : 145-156.
Labels
Paediatric urologist Urology
Article was published inUrological Journal

2007 Issue 1-
All articles in this issue
- Vezikoureterální reflux
- Poruchy sexuální diferenciace
- Obstrukční uropatie dětského věku
- Hypospadie: optimální možnosti řešení
- Problematika urolitiázy u dětského pacienta: přinesla moderní doba nové možnosti?
- Kryptorchizmus: kdy načasovat a jakou léčbu provést?
- Varikokéla: kdy načasovat a jakou léčbu provést?
- Fimóza v dětském věku
- Dysfunkce dolních močových cest u dětí
- Enuresis nocturna
- Urological Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Hypospadie: optimální možnosti řešení
- Varikokéla: kdy načasovat a jakou léčbu provést?
- Poruchy sexuální diferenciace
- Obstrukční uropatie dětského věku
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

