-
Medical journals
- Career
Lymfóm žalúdka ako príčina masívneho krvácania u pacienta s Castlemanovou chorobou
Authors: M. Smolár; L. Šutiak *; A. Mikolajčík *; Marek Vojtko *; L. Plank **
Authors‘ workplace: Chirurgická klinika JLF UKo a MFN v Martine, Slovenská republika, prednosta: doc. MUDr. D. Mištuna. Ph. D., mim. prof. ; Chirurgická klinika JLF UKo a MFN v Martine, Slovenská republika, prednosta: doc. MUDr. D. Mištuna. PhD., mim. prof. *; Ústav patologickej anatómie JLF UKo a MFN v Martine, Slovenská republika, prednosta: prof. MUDr. L. Plank, CSc. **
Published in: Rozhl. Chir., 2010, roč. 89, č. 5, s. 320-324.
Category: Monothematic special - Original
Overview
Primárne lymfómy žalúdka predstavujú zriedkavé malignity tráviaceho traktu. V ich etiológii sa často uplatňuje infekcia Helicobacter pylori. Menej častou príčinou vzniku týchto nádorov môžu byť aj systémové imunopatologické ochorenia spojené s imunodeficitom. Autori v článku referujú prípad pacienta s lymfómom žalúdka, u ktorého bola v predchorobí diagnostikovaná Castlemanova choroba bioptickým vyšetrením lymfatických uzlín. Pacient bol hospitalizovaný s masívnym krvácaním z ulcerácií žalúdka, ktoré si vyžiadalo urgentnú chirurgickú liečbu. Definitívnou histologickou diagnózou bol agresívny B-NHL žalúdka.
Kľúčové slova:
primárny lymfóm žalúdka – krvácanie – Castlemanova chorobaÚVOD
Krvácanie z tráviaceho traktu patrí medzi časté náhle príhody brušné a predstavuje závažný, často aj život ohrozujúci stav. Zvýšený výskyt krvácania v sezónnom období (jar, jeseň) už dnes neplatí a stále viac pacientov krváca počas celého roka [1]. Podľa rôznych štúdií je ročná incidencia krvácania do tráviaceho traktu 48–160/100 000 obyvateľov [2, 3]. Jeho mortalita sa udáva 6–10 % (8, 20) a v prípade vyššieho veku pacienta, alebo závažných pridružených ochorení až do 40 % [1]. Napriek mnohým pokrokom v konzervatívnej, endoskopickej, rádiologickej a chirurgickej liečbe sa mortalita pri krvácaní z horného tráviaceho traktu v priebehu posledných 30 rokov výraznejšie nezmenila [4, 5]. Približne 85–90 % predstavuje krvácanie z horného tráviaceho traktu, ktoré je často hemodynamicky závažné. Z toho asi 90 % krvácaní je nevarikózneho pôvodu.
Medzi najčastejšie zdroje krvácania z horného tráviaceho traktu patria vredová choroba žalúdka a duodéna, ezofageálne varixy a Malloryho-Weissov syndróm. Medzi zriedkavé príčiny (menej ako 1 %) patria angiómy, Dieulafoy lézia, hereditárna hemoragická telangiektázia, pseudoxanthoma elasticum, Ehlersov-Danlosov syndróm, Gastrointestinálne stromálne tumory (GISTy) a iné (Tab. 1). Medzi vzácnu príčinu krvácania patrí i malígny lymfóm žalúdka, ktorý tvorí približne 5 % všetkých primárnych nádorov žalúdka [6]. Okrem primárneho lymfómu môže ísť aj o sekundárne postihnutie žalúdka generalizovaným nádorovým procesom, najmä systémovou nádorovou lymfoproliferáciou.
Table 1. Zdroje krvácania z horného tráviaceho traktu [7] Tab. 1. Sources of bleeding in the upper gastrointestinal tract ![Zdroje krvácania z horného tráviaceho traktu [7]
Tab. 1. Sources of bleeding in the upper gastrointestinal tract](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/65da943ba9c7432ddf9753030804995e.jpeg)
V našej kazuistike predstavujeme pacienta s masívnym krvácaním z horného tráviaceho traktu. Zo spádovej nemocnice bol 5. 3. 2009 preložený na naše pracovisko pre hemodynamicky závažné krvácanie z exulcerovaných lézií v žalúdku (verifikované gastroskopicky), ktoré sa v spádovej nemocnici nedarilo zastaviť. V osobnej anamnéze pacienta bol údaj o cholecystektómii, choledocho-duodeno anastomóze a gastro-entero anastomóze (GEA) pre údajný benígny tumor v oblasti hlavy pankreasu v roku 1998. V roku 1999 bola urobená ľavostranná nefrektómia pre polycystickú obličku. Okrem toho má pacient chronickú renálnu insuficienciu a diabetes mellitus II. typu (DM II) liečený perorálnymi antidiabetikami (PAD). Od roku 2004 je liečený kortikoidmi hematológom pre multicentrickú formu Castlemanovej choroby – hyalínne-vaskulárny podtyp, ktorá bola verifikovaná bioptickým vyšetrením lymfatických uzlín inguiny a krku (Obr. 1).
Image 1. Biopsia LU Fig. 1. Lymph nodes biopsy 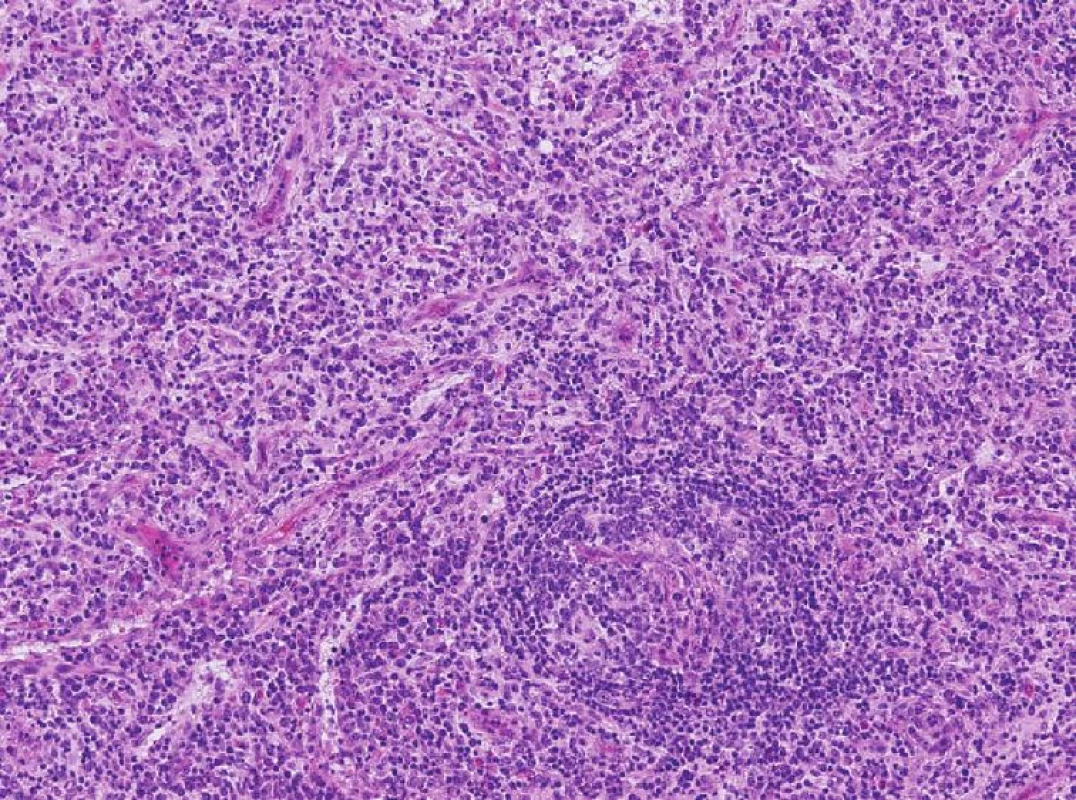
Pri príjme na jednotku intenzívnej starostlivosti bol pacient stabilizovaný. V hemograme bol obraz ťažkej anémie – hemoglobín 75 g/l. Ihneď sme indikovali hemostyptickú liečbu, vrátane terlipresínu 1 g/6 hod. a hemosubstitúciu erymasami a mrazenou plazmou. Vzhľadom na diagnostikovanú Castlemanovu chorobu bol konzultovaný hematológ, ktorý odporučil pokračovanie terapie kortikoidmi. Napriek tejto kortikoterapii, ktorá býva často príčinou krvácania zo žalúdočnej sliznice, aktívne krvácanie ďalej nepokračovalo. Dňa 6. 3. 2009 bolo urobené gastrofibroskopické vyšetrenie (GFS), kde gastroenterológ po odsatí krvi popísal v hĺbke 50 cm od predného zuboradia na prednej i zadnej stene žalúdka prominujúce infiltrácie steny s centrálnymi exulceráciami a nekrotickou spodinou s hematínom. Z troch lézií odobral bioptické vzorky sliznice. Krvácanie bolo podľa Forrestovej klasifikácie 2b - c.
V ďalšom priebehu pacient nekrvácal, hodnoty hemoglobínu boli doplnené na 104–117 g/l. Pacient začal prijímať tekutú stravu.
Dňa 12. 3. 2009 ráno došlo u pacienta k hemodynamicky závažnej recidíve krvácania a rozvoju šokového stavu (TK 60/35 mm Hg, tachykardia 124/min). Pacienta sme okamžite indikovali na operačný výkon. Indikáciu sme považovali za vitálnu. Po otvorení peritoneálnej dutiny a adheziolýze početných zrastov sme našli naplnený žalúdok. Urobili sme pozdĺžnu gastrotómiu. V žalúdku bolo množstvo koagúl a čerstvá krv. Po odsatí krvi sme našli v oblasti tela žalúdka 3 tumorózne infiltráty veľkosti 5x3 cm, jeden infiltrát rovnakej veľkosti bol subkardiálne smerujúci k veľkej kurvatúre (Obr. 2–4).
Image 2. Resekát žalúdka so zvyškom GEA Fig. 2. Gastric resecate with GEA (gastro-entero anastomosis) 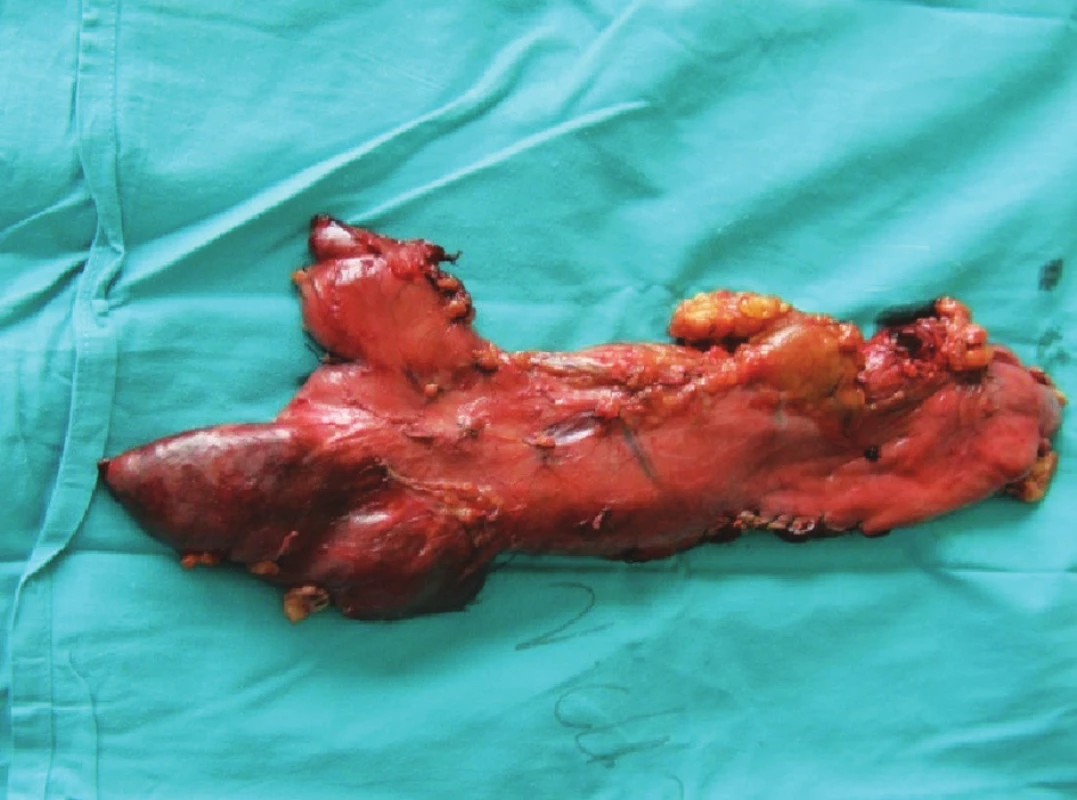
Image 3. Exulcerácie žalúdka – zdroj krvácania (pinzety v kardii a pylore) Fig. 3. Gastric exulcerations– sources of bleeding (pincers within the cardia and pylorus) 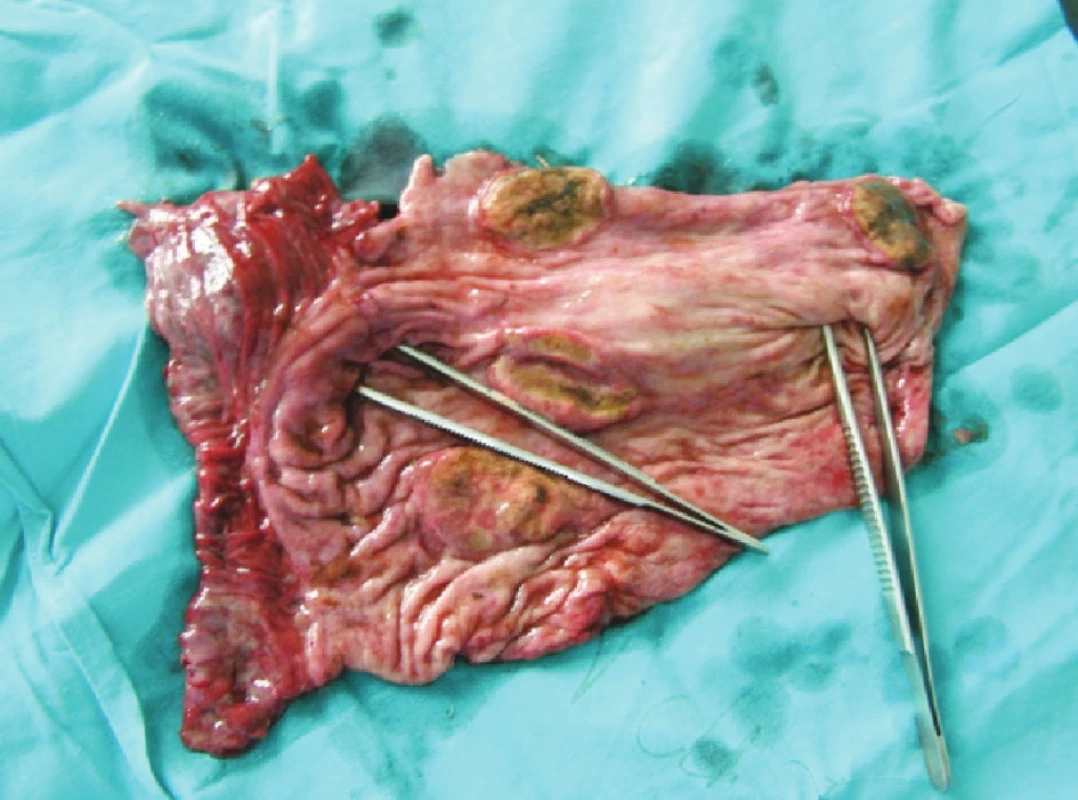
Image 4. Detail exulcerácii Fig. 4. Exulceration – a detail view 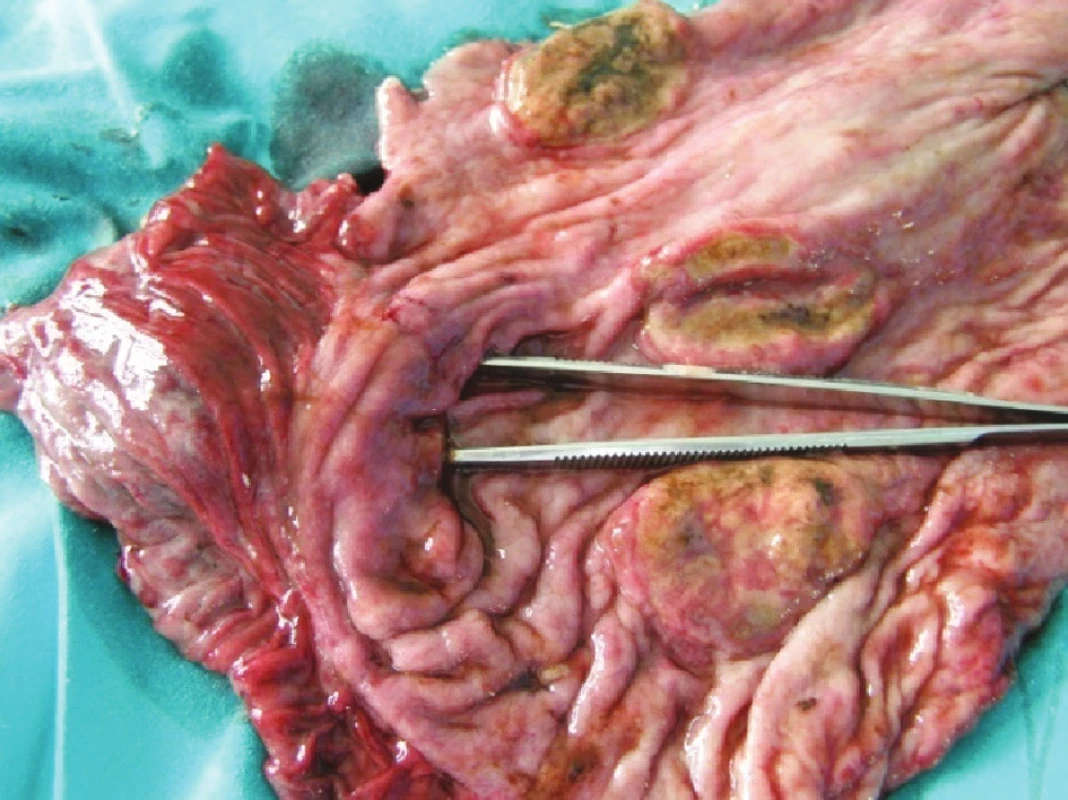
Po zhodnotení nálezu sme za jediné možné riešenie považovali totálnu gastrektómiu. Rekonštrukciu pasáže sme urobili na exkludovanej Roux Y kľučke tenkého čreva. Ešte pred uzatvorením brušnej dutiny sme v spolupráci s anesteziológom zaviedli nasoenterálnu sondu na včasnú enterálnu výživu, ktorej koniec siahal pod entero-entero anastomózu.
Pooperačné obdobie pacienta bolo komplikované výraznou hlienostázou v bronchoch, čo si vyžiadalo opakované terapeutické bronchoskopie. Pri fibrobronchoskopii bolo nájdené ústie horného lobárneho bronchu vpravo prakticky obturované tlakom zvonku. Bronchoskopické vyšetrenie korelovalo aj s RTG vyšetrením hrudníka, ktoré odhalilo rozsiahle zatienenie vpravo (Obr. 5). Opakovanými fibrobronchoskopiami, dychovou rehabilitáciou a pokračujúcou kortikoterapiou došlo k subjektívnemu i objektívnemu zlepšeniu stavu pacienta a ústie bronchov sa čiastočne spriechodnilo. Ako možná príčina obštrukcie prichádzalo do úvahy aj proliferované lymfatické tkanivo pri Castlemanovej chorobe, avšak pri absencii bioptického vyšetrenia tejto lokalizácie nemožno vylúčiť ani inú etiológiu tohto procesu (reaktívne zápalové zmeny, primárny nádor), vrátane možnej systémovej manifestácie agresívneho B-NHL, ktorý súčasne postihol oblasť žalúdka. Klinicky uvedené zlepšenie nálezu po kortikoterapii však podporuje skôr prvú možnosť.
Image 5. RTG nález tumoróznej masy v pravom hornom pľúcnom poli Fig. 5. RTG finding of a tumorous mass in the right upper lung region 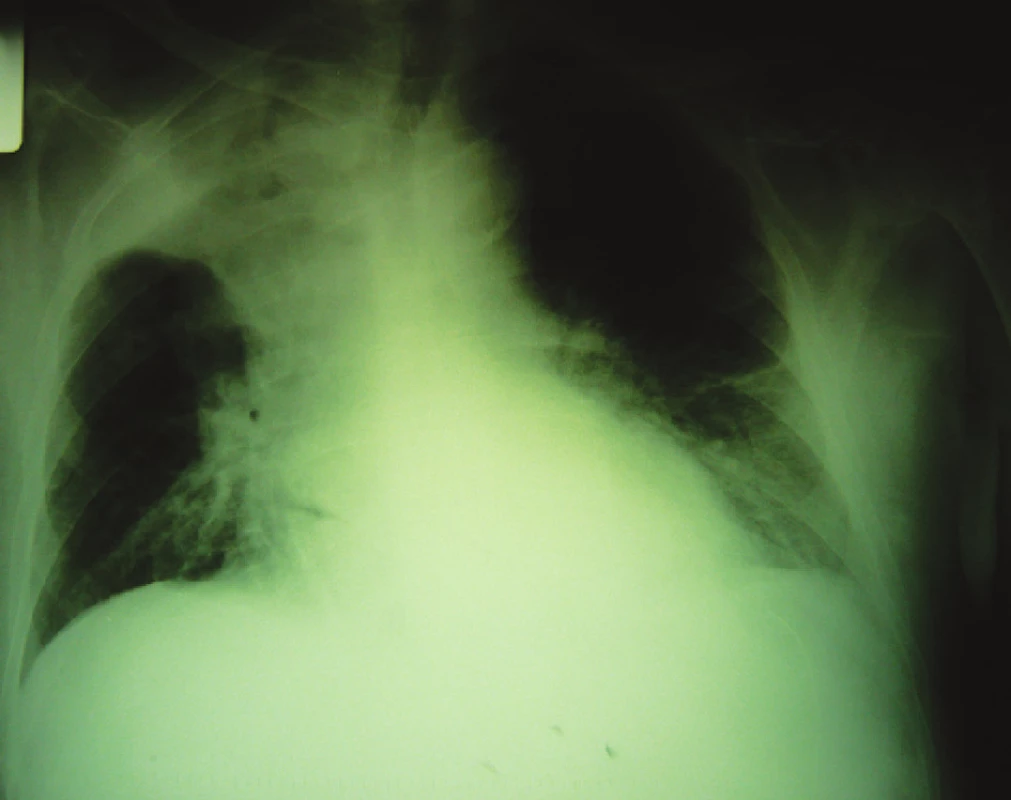
V pooperačnom období bol pacient bez prejavov krvácania, bez anemizácie. Od 1. pooperačného dňa začal prijímať definovanú stravu cez nasojejunálnu sondu, ktorú dobre toleroval. Dňa 19. 3. 2009 sme urobili pasáž vodnou kontrastnou látkou, ktorá voľne prechádzala cez anastomózu do tenkého čreva, bez úniku kontrastu mimo lúmen čreva. Na siedmy pooperačný deň začal pacient prijímať perorálne tekutú stravu s dobrou toleranciou.
Definitívna histológia žalúdka zo vzoriek odobratých pri GFS ako aj z resekátu žalúdka potvrdila vo všetkých makroskopicky opísaných ložiskách nádorovej infiltrácie obraz blastického malígneho nádoru s rozsiahlymi exulceráciami sliznice. Nádor zodpovedal agresívnemu B-NHL (non-Hodgkinov lymfóm) typu DLBCL (difúzny veľkobunkový B-bunkový lymfóm) v extranodálnej lokalizácii, morfologicky centroblastový variant, fenotypovo z tzv. „aktivovaných B-buniek“ (Obr. 6).
Image 6. Histologický obraz B-NHL v resekáte žalúdka Fig. 6. Histological finding of B-NHL in the gastric resecate 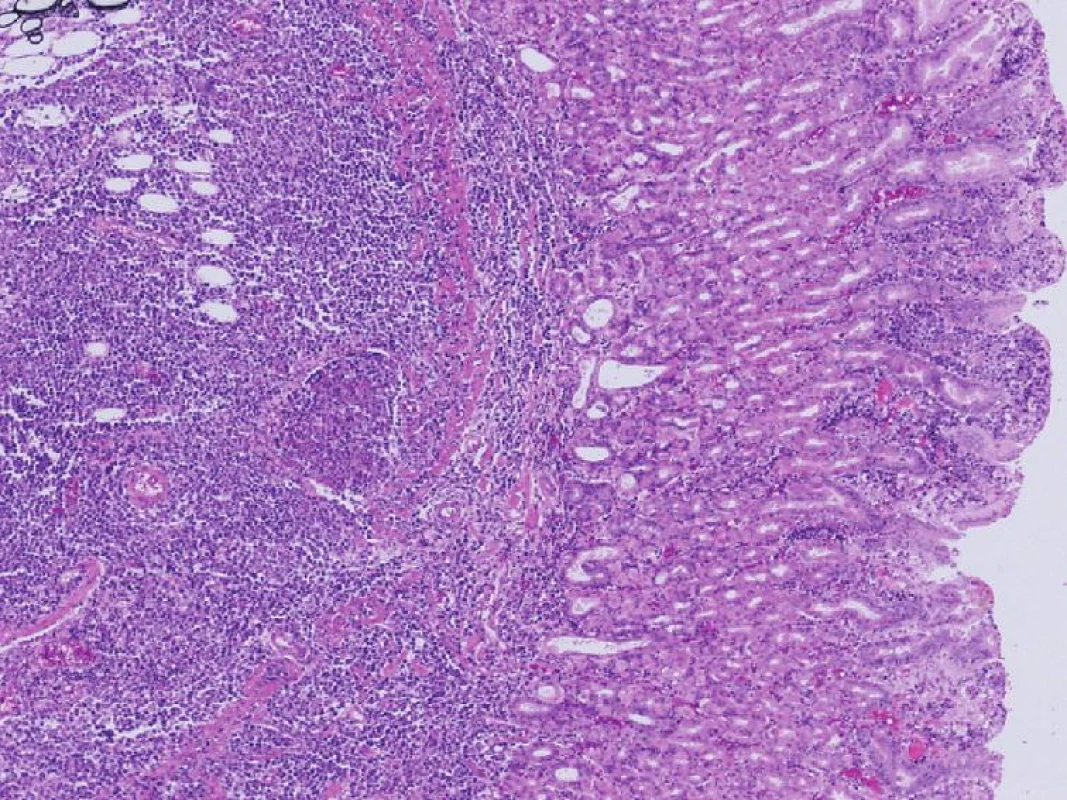
Dňa 26. 3. 2009, na 14. pooperačný deň, bol pacient preložený do spádovej nemocnice, kde pokračoval v hematologickej liečbe základného ochorenia. Pri preklade bol na perorálnom príjme, operačná rana bola zhojená per primam, v laboratórnom obraze bez anémie. Pacient je naďalej v dispenzárnej starostlivosti a liečbe onkohematológa. Ochorenie je v súčasnosti v remisii.
DISKUSIA
Napriek pomerne nízkej incidencii lymfómu žalúdka jeho výskyt v poslednom období stúpa. Ako možná príčina sa javí vysoká prevalencia baktérie Helicobacter pylori v populácii, ktorý pri neliečení spôsobuje chronické zápalové zmeny sliznice žalúdka. V takomto teréne sa môže z lymfatického tkaniva žalúdočnej sliznice rozvinúť primárny NHL, najčastejšie typu DLBCL, resp. B-bunkový lymfóm z buniek marginálnej zóny typu MALT (mucosa-associated lymphoid tissues) [8]. U nášho pacienta sa vzhľadom na generalizovanú lymfadenopatiu (krk, inguina) a postihnutie pľúc bližšie nedodiagnostikovaným procesom uplatnila v etiológii pravdepodobne systémová imunopatológia.
Medzi prvé symptómy lymfómu žalúdka patrí bolesť v epigastriu, ktorá často imituje vredovú chorobu žalúdka alebo duodéna, ochorenie žlčníka a pod. [9]. K nešpecifickým symtómom patrí strata hmotnosti, nauzea, vracanie, pocit plného žalúdka, poruchy trávenia. Menej časté je nočné potenie, žltačka, zvýšená telesná teplota a dysfágia [10]. Veľa pacientov vyhľadá lekára až pri prejave komplikácií [11]. Medzi najčastejšie z nich patrí krvácanie s hematemézou a melénou, ktoré sa vyskytuje u 20–30 % pacientov. Obštrukcia alebo perforácia žalúdka sa vyskytuje menej často [12].
Pre indikáciu správnej terapie je nevyhnutná klinická klasifikácia lymfómov žalúdka. Medzi najpoužívanejšie patrí klasifikácia podľa Musshoffových kritérií (Tab. 2).
Table 2. Klinická klasifikácia lymfómov žalúdka podľa Musshoffa (Za číslom štádia sa uvádza index písmenom: E = extranodal, S = splenic, A = asymptomatic, B = symptomatic) [8] Tab. 2. Clinical classification of gastric lymphomas according to Musshoff (stages are followed by letters: E = extranodal, S = splenic, A = asymptomatic, B = symptomatic) ![Klinická klasifikácia lymfómov žalúdka podľa Musshoffa (Za číslom štádia sa uvádza index písmenom: E = extranodal, S = splenic, A = asymptomatic, B = symptomatic) [8]
Tab. 2. Clinical classification of gastric lymphomas according to Musshoff (stages are followed by letters: E = extranodal, S = splenic, A = asymptomatic, B = symptomatic)](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/6f81c79fe057440c040e27f8547f83a1.jpeg)
U pacientov s nízkomalígnym lymfómom žalúdka a prítomnosťou H. pylori sa ukázala eradikačná liečba ako veľmi efektívna pri regresii lymfómu [13]. Pri lymfómoch, ktoré nereagujú regresiou na eradikačnú liečbu je metódou voľby chemoterapia a rádioterapia s viac ako 90% úspešnosťou v I. a II. štádiu [14].
Viac ako 60 % lymfómov žalúdka sú vysokomalígne lézie, ktoré vyžadujú chemoterapiu a rádioterapiu v závislosti od rozsahu ochorenia. Chirurgická liečba agresívnych typov je rezervovaná pre lokalizované rezistentné lézie po nechirurgickej terapii a pre zriedkavé prípady komplikácií ochorenia [15], akým bolo aj krvácanie u nášho pacienta.
Novou terapeutickou modalitou v liečbe B-NHL je použitie monoklonálnych anti-CD20 protilátok (rituximab). Výsledky randomizovaných štúdií ukázali, že použitie rituximabu zvyšuje prežívanie u pacientov nereagujúcich na chemoterapiu a rádioterapiu, resp. u pacientov s MALT-NHL bez prítomnosti H. pylori [14].
V minulosti bola chirurgická liečba lymfómov radikálna a často zahŕňala totálnu gastrektómiu. Výrazná pooperačná morbidita však postupne viedla k uprednostňovaniu rádioterapie, kombinovanej chemoterpie a použitiu monoklonálnych protilátok. Aviles et al. [16] porovnávali efekt samostatnej chirurgickej terapie (totálna gastrektómia), rádioterapie a kombinovanej chemoterapie u 241 pacientov s MALT lymfómom. U všetkých pacientov sa podarilo dosiahnuť celkovú remisiu. Dosiahnutie trvalej remisie bolo signifikantne nižšie u pacientov liečených len rádioterapiou (52 %) a len chirurgicky (52 %) v porovnaní so skupinou pacientov liečených kombinovanou chemoterapiou (87 %). Päťročné prežívanie pacientov liečených chemoterapiou bolo 87 %, po chirurgickej terapii 80 % a rádioterapii 75 %. Dané hodnoty nepredstavujú signifikantné rozdiely.
Ako najideálnejšia terapeutická modalita sa v súčasnosti javí eradikačná terapia H. pylori, ktorá môže navodiť trvalú remisiu. Konzervatívny prístup využívajúci chemoterapiu založenú na aplikácii antracyklínových prípravkov, samostatne, alebo v kombinácii s rádioterapiou, nahrádza gastrektómiu ako metódu voľby pri liečbe DLBCL. Úloha a účinnosť rituximabu v liečbe B-NHL žalúdka ešte nie je detailne preskúmaná a vyžaduje dlhodobejšie hodnotenie [14].
Zaujímavá bola u nášho pacienta i asociácia s Castlemanovou chorobou, ktorá bola prvý krát popísaná Benjaminom Castlemanom v roku 1954 a patrí medzi zriedkavé lymfoproliferatívne ochorenie [17]. Napriek tomu, že nepatrí medzi malignity, niektoré multicentrické formy tohto ochorenia svojim klinickým priebehom pripomínajú malígne lymfoproliferatívne ochorenia – malígne lymfómy. Taktiež sa pozorovala malígna transformácia tohto ochorenia a zvýšený výskyt lymfómov u týchto pacientov [18]. Práve tento fakt, napriek kortikoterapii, možno zohral rozhodujúcu úlohu pri vzniku malígneho lymfómu žalúdka nášho pacienta, u ktorého boli všetky vyšetrenia na prítomnosť H. pylori negatívne. Po stanovení diagnózy bioptizáciou by mal byť pacient dispenzarizovaný a pravidelne vyšetrovaný a kontrolovaný pre možný výskyt malígnych lymfoproliferatívnych ochorení asociovaných s Catlemanovou chorobou, resp. pre jej možnú malígnu transformáciu [19].
Náš pacient v čase prejavov krvácania zo žalúdka nemal ešte stanovenú histologickú diagnózu. Vzhľadom na rozsah ochorenia a hemodynamicky závažné krvácanie bola radikálna chirurgická liečba v danom prípade jediným možným riešením. Vzťah morfologicky verifikovanej Castlemanovej choroby k vysokomalígnemu lymfómu žalúdka je nejasný, ako aj samotný pôvod tohto lymfómu (primárny žalúdočný lymfóm versus systémový lymfóm s infiltráciou žalúdka). Je však zjavné, že imunodeficit spojený s Castlemanovou chorobou sa môže podieľať na vzniku rôznych malígnych tumorov, vrátane lymfómov.
ZÁVER
Lymfómy žalúdka nepatria medzi časté ochorenia, s ktorými prichádza chirurg do styku. Nezriedka sa stretáva až s komplikáciami, najmä krvácaním, ktoré vyžaduje urgentné riešenie. Interdisciplinárny prístup za účasti onkohematológa, patológa, chirurga a iných špecialistov môže včas odhaliť ochorenie a zabezpečiť adekvátnu konzervatívnu liečbu, ktorá zabráni vzniku závažných komplikácií, ktoré vyžadujú urgentnú chirurgickú liečbu.
Ešte zriedkavejší je súčasný alebo samostatný výskyt Castlemanovej choroby. Dlhodobé sledovanie týchto pacientov je nevyhnutné pre včasné odhalenie prípadného malígneho lymfoproliferatívneho ochorenia asociovaného s Castlemanovou chorobou. Manažérom liečby je onkohematológ.
MUDr. Marek Smolár
Š. Nahalku 533/83
059 40 Liptovská Teplička
Slovenská republika
e-mail: smoly2002@hotmail.com
Sources
1. Marko, Ľ., Molnár, P., Koreň, R. Praktický manažment pacienta s krvácaním do tráviaceho traktu. Miniinvazívna chirurgia a endoskopia, chirurgia súčasnosti, 9, ročník, 2005, č. 2, s. 41–46.
2. Almela, P., Benages, A., Peiró, S., Anón, R., Pérez, M. M., Peňa, A., Pascual, I., Mora, F. A risk score system for identification of patients with upper – GI bleeding suitable for outpatient management. Gastrointest. Endosc., 59, 2004, č. 7, s. 772–780.
3. Šimo, J., Matis, P., Vician, M., Žiak, M. Súčasná problematika krvácania z gastroduodena. Rozhl. Chir., 2000, roč. 79, č. 7, s. 272–274.
4. Dubaj, M., Bakoš, E., Birčák, J., Galko, J., Piesecká, Ľ. Algoritmus prístupu k pacientovi s krvácaním do gastrointestinálneho traktu. Slov. Lek., 14, 2004, č. 5–6, s. 135.
5. Zavoral, M. Endoskopická léčba krvácení do trávicího ústrojí – srovnání jednotlivých technik. In.: Zavoral, M., Dítě, P., Špičák, J., Bureš, J. a kol.: Nové trendy v digestivní endoskopické diagnostice a léčbě. Grada Publishing, spol. s.r.o., Praha, 2000, 313 s.
6. Al-Akwaa, A. M., Siddiqui, N., Al-Mofleh, I. A. Primary gastric lymphoma. World J. Gastroenterol., 2004; 10(1): 5–11.
7. Mooris, A. I. Upper gastrointestinal haemorrhage – endoscopic approaches to diagnosis and treatment. In : Gilmore, I. T. and Shields, R.: Gastrointestinal Emergencies. W. B. Saunders Company, London, 1992, 392 s.
8. Parsonnet, J., Hansen, S., Rodriguez, L., Gelb, A. B., Warnke, R. A., Jellum, E., Orentreich, N., Vogelman, J. H., Friedman, G. D. Helicobacter pylori infection and gastric lymphoma. N. Engl. J. Med., 1994; 330 : 1267–1271.
9. Kitamura, K., Yamaguchi, T., Okamoto, K., Ichikawa, D., Hoshima, M., Taniguchi, H., Takahashi, T. Early gastric lymphoma; a clinicopathologic study of ten patients, literature review, and compari-son with early gastric adenocarcinoma. Cancer, 1996; 77 : 850–857.
10. Chandran, R. R., Raj, E. H., Chaturvedi, H. K. Primary gastrointestinal lymphoma: 30 year experience at the cancer institute, Madras, India. J. Surg. Oncol., 1995; 60 : 41–49.
11. Al-Mofleh, I. A. Complications of primary upper gastrointestinal lymphoma. Ann. Saudi Med., 1992; 12 : 297–299.
12. Isaacson, P. G. Recent developments in our understanding of gastric lymphomas. Am. J. Surg. Pathol., 1996; 20(Suppl 1): S1–S7.
13. Wundisch, T., Mosch, C., Neubauer, A., Stolte, M. Helicobacter pylori eradication in gastric mucosa-associated lymphoid tissue lymphoma: results of a 196-patient series. Leuk. Lymphoma, 2006; 47 : 2110–2114.
14. Psyrri, A., et al. Primary extranodal lymphomas of stomach: clinical presentation, diagnostic pitfalls and management. Annals of Oncology, 19, No. 12, 2008, p. 1992–1999.
15. Yoon, S. S., et al. The diminishing role of surgery in the treatment of gastric lymphoma. Ann. Surg., 2004 Jul; 240(1): 28–37.
16. Aviles, A., Nambo, M. J., Neri, N. et al. Mucosa-associated lymphoid tissue (MALT) lymphoma of the stomach: results of a controlled clinical trial. Med. Oncol. 2005; 22 : 57–62.
17. Horger, M., Bares, R., Wiefels, J., Schober, W., Mussig, K. Radiologische Befunde bei Morbus Castleman. World J. Surg. Oncol., 2005; 3; 33.
18. Greiner, T. C., Gross, T. G. Atypical immune lymphoproliferations. In: Hematology: Basic Principles and Practice. 5th ed. Hoffman R, Benz Jr. E, Shattil SJ, Furie B, Silberstein LE, McGlave P, Heslop H, eds. Philadelphia, PA. Elsevier; 2009 : 1449–1459.
19. American Cancer Society: Castleman disease [on line]. [cit. 2010-1-16] Dostupné na WWW:
< http://documents.cancer.org/6636.00/6636.00.pdf.>
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2010 Issue 5-
All articles in this issue
- Kombinace dexmedetomidinu s ketaminem a opioidy významně potlačuje hemodynamické změny způsobené laparoskopickou cholecystektomií a prodlužuje trvání pooperační analgezie
- Komplikace hojení ran u kuřáků
- Přidružená poranění u zlomenin lopatky
- Úloha Hartmannovej operácie a možnosti jej rekonštrukcie v súčasnosti
- Buried bumper syndrom (BBS) jako komplikace perkutánní endoskopické gastrostomie
- Aneuryzma abdominální aorty – dlouhodobé výsledky léčby
- Současná strategie léčby neurogenního močového měchýře u pacientů s míšními dysrafismy
- Pneumochirurgie v řešení karcinomu kolorekta
- Perforace sigmatu vycestovalým duodenobilárním stentem
- Extragastrointestinální stromální tumor – diagnostická úskalí v kazuistice
- Lymfóm žalúdka ako príčina masívneho krvácania u pacienta s Castlemanovou chorobou
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Úloha Hartmannovej operácie a možnosti jej rekonštrukcie v súčasnosti
- Buried bumper syndrom (BBS) jako komplikace perkutánní endoskopické gastrostomie
- Komplikace hojení ran u kuřáků
- Současná strategie léčby neurogenního močového měchýře u pacientů s míšními dysrafismy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

