-
Medical journals
- Career
MELD-skóre v predikci časné mortality u nemocných s refrakterním ascitem léčených pomocí TIPS
Authors: T. Fejfar 1; V. Šafka 1; P. Hůlek 3; T. Vaňásek 1; A. Krajina 2; V. Jirkovský 1
Authors‘ workplace: II. interní klinika Lékařské fakulty UK a FN Hradec Králové, přednosta prof. MUDr. Jaroslav Malý, CSc. 1; Radiologická klinika Lékařské fakulty UK a FN Hradec Králové, přednosta prof. MUDr. Pavel Eliáš, CSc. 2; Katedra interních oborů Lékařské fakulty UK, Hradec Králové, vedoucí prof. MUDr. Jaroslav Malý, CSc. 3
Published in: Vnitř Lék 2006; 52(9): 771-776
Category: Original Contributions
Overview
Úvod:
Transjugulární intrahepatální portosystémová spojka (TIPS) je již dobře zavedenou možností terapie závažných komplikací symptomatické portální hypertenze, jako jsou krvácení do gastrointestinálního traktu, refrakterní ascites (RA) a Buddova-Chiariho syndromu. U některých nemocných v případě elektivních výkonů, zejména u nemocných s refrakterním ascitem, a to zejména u nemocných s hodnotami Childova-Pughova skóre C (kolem 12 bodů) je predikce dalšího přežití po výkonu obtížná a časná mortalita je u těchto nemocných poměrně vysoká. Přesto někteří nemocní i s pokročilým jaterním onemocněním mohou z výkonu dlouhodobě profitovat. Klasicky je k stratifikaci nemocných používáno Childovo-Pughovo skóre. Během posledního desetiletí byly zavedeny i další skórovací systémy s lepší výpovědní schopností. Jedním z nich je MELD-skóre (Model for End Stage Liver Disease), vycházející pouze z rychle dostupných laboratorních hodnot. Výsledky předchozích srovnávacích studií, porovnávajících oba skórovací systémy, byly poněkud rozporuplné, i když porovnání prediktivní síly vyznívalo spíše ve prospěch MELD-skóre.Cíl:
Naše práce měla retrospektivně zhodnotit význam MELD-skóre k předpovědi krátkodobé (v 1. a 3. měsíci) mortality u nemocných léčených pro refrakterní ascites pomocí TIPS a porovnat jej s výpovědní hodnotou Childova-Pughova skóre.Metodika:
Retrospektivně byla vyhodnocena data od 110 nemocných (průměrný věk 55 let) s jaterní cirhózou (61 % nemocných s jaterní cirhózou etylické etiologie) léčených TIPS na našem pracovišti v období od září roku 1992 do prosince roku 2003. Hodnoty MELD-skóre a Childova-Pughova skóre byly porovnávány ve skupinách nemocných zemřelých do 1, 3 a 12 měsíců, s těmi, kteří dle dostupných dat toto období prokazatelně přežívali. Ke statistickému hodnocení byla použita ROC (AUC) analýza a Studentův T-test.Výsledky:
Průměrná doba sledování byla 23 měsíců. Průměrné MELD-skóre v celé skupině bylo 16 <6; 31>, průměrné hodnoty MELD-skóre u nemocných zemřelých do 1, 3 a 12 měsíců byly 21, 20 a 18 bodů. Při porovnání výsledného MELD-skóre a Childova-Pughova skóre jednotlivých podskupin nemocných zemřelých a přežívajících dané časové období, na hladině významnosti p < 0,05, byl nalezen významný rozdíl u MELD-skóre pro 1měsíční, 3měsíční a 1roční období. U Childova-Pughova skóre byl rozdíl jen při hodnocení v období 3 a 12 měsíců. Při hodnocení dat ROC (AUC) analýzou byla prediktivní síla MELD-skóre v porovnání s Childovou-Pughovou klasifikací významně vyšší u1měsíční (0,73 vs 0,63) i 3měsíční (0,73 vs 0,67) mortality. Pro 12měsíční mortalitu byla výpovědního hodnota nízká u obou skóre (pod 0,7).Závěr:
MELD skóre je lepším nástrojem k určení rizika časné mortality u nemocných s refrakterním ascitem léčených pomocí TIPS než Childova-Pughova klasifikace. K určení dlouhodobé prognózy mají obě skóre u těchto nemocných nízkou výpovědní hodnotu.Klíčová slova :
TIPS - predikce mortality - MELDÚvod
Transjugulární intrahepatální portosystémová spojka (TIPS), jako neselektivní side to side portosystémová anastomóza konstituovaná nejčastěji mezi pravou větví porty a pravou jaterní žilou, zasahuje přímo do patofyziologického mechanizmu formace ascitické tekutiny při portální hypertenzi, jejíž nejčastější příčinou je u nás jaterní cirhóza. Po zavedení spojky nedochází pouze k poklesu vlastního intravaskulárního tlaku v portální žíle, ale též k modulaci mnoha působků endokrinního systému (ADH – antidiuretický hormon, RAAS - Renin-Angiotensin-Aldosteron-System) a sympatického nervového systému. Refrakterní ascites tedy spolu s krvácením do zažívacího traktu patří mezi hlavní indikace TIPS [2,3,9,11]. První transjugulární intrahepatální portosystémová spojka v klinické praxi byla provedena Richterem [17,18] v Německu v roce 1988. Byla uskutečněna u 49letého pacienta s jaterní cirhózou a nekontrolovatelným varikózním krvácením v klasifikační třídě Child-Pugh C, s těžkou jaterní encefalopatií, ascitem a rozvíjejícím se DIC (Disseminated Intravascular Coagulation) a respiračním selháním. Tento nemocný posléze 11. den po výkonu zemřel na jaterní selhání. V dnešní době by takový nemocný k výkonu indikován zřejmě nebyl. Do klinické praxe se TIPS dostal plně v 90. letech 20. století zejména zásluhou M. Röslleho a A. Ochse z Freiburgu.
V České republice byl TIPS poprvé v terapii užit v září roku 1992 v Hradci Králové [11].
Po zvládnutí prvotních technických potíží během předchozích let a zavedení nových potahovaných stentů, výrazně zlepšujících primární průchodnost zkratu, se do popředí zájmu dostává zejména otázka vhodného výběru nemocného k výkonu. To, co limituje nemocného vedle přidružených kardiovaskulárních onemocnění, je zejména pokročilost vlastní jaterní choroby. Po zavedení zkratu dochází ke změnám nitrojaterní cirkulace, která spolu s poklesem portálního tlaku vede u většiny pacientů sice k přechodnému, ale patrnému zhoršení jaterních funkcí s nebezpečím progrese do ireverzibilního jaterního selhání. Dosud nejčastěji užívaným prediktivním skórovacím systémem k posouzení rizikovosti nemocných je Childova-Pughova klasifikace. Toto hodnocení nemocných přináší poměrně přijatelnou informaci o pravděpodobnosti dlouhodobějšího přežívání i o operačním riziku u nemocných s jaterní cirhózou. Problematičtí jsou však nemocní spadající do funkční třídy C dle Childovy-Pughovy klasifikace. Dlouhodobé výsledky u nemocných s TIPS však ukazují, že i u nemocných ve funkční třídě B s bodovou hodnotou 8 - 9 může po zavedení portosystémového zkratu dojít k nezvladatelnému jaternímu selhání, a opačně jsou nemocní s Childovým-Pughovým skóre okolo 12, kteří ze zavedení zkratu dlouhodoběji profitují. Z potřeby přesnější stratifikace nemocných podstupujících TIPS k určení rizika, jak časné periprocedurální, tak dlouhodobé mortality, vznikaly nové skórovací systémy, mezi něž patří i MELD (Model for End stage Liver Disease) skóre. Je to skóre založené pouze na laboratorních hodnotách (bilirubin, kreatinin, INR) a vzniklo na podkladě statistického hodnocení prediktivní síly prospektivně shromážděných dat [10]. Nejvíce se následně rozšířilo v transplantační chirurgii.
Cílem naší práce bylo retrospektivně zhodnotit vhodnost použití MELD-skóre k predikci zejména časné mortality (1 - a 3měsíční) v porovnání s Childovým-Pughovým skóre u nemocných s refrakterním či tenzním ascitem léčených pomocí transjugulární intrahepatální portosystémové spojky.
Soubor nemocných
Od září roku 1992 do prosince roku 2003 byl TIPS pro tuto diagnózu proveden u 110 nemocných (průměrný věk 55 let). Většina nemocných měla jaterní postižení etylické etiologie (61 % etylické etiologie, 15 % posthepatické a 24 % ostatní; tab. 1). Zkrat se podařilo vytvořit u 99 % indikovaných pacientů bez vážnějších komplikací (1 nemocný byl pro abnormální konfiguraci portální žíly indikován k chirurgickému provedení spojky). Průměrná doba sledování v našem souboru byla 23 měsíců.
Table 1. Etiologie jaterního postižení (n = 110). 
AC – alkoholická cirhóza, AIH – autoimunitní hepatitida, PBC – primární biliární cirhóza, PSC – primární sklerózující cholangoitida Table 2. Childova-Pughova klasifikace [21]. ![Childova-Pughova klasifikace [21].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/2ded5aa1fcca2da583adc0619ac30943.jpg)
Metodika
U všech nemocných bylo dle protokolu OPTN (Organ Procurement Transplant Network) spočítáno MELD-skóre a stejně tak vyhodnoceno bodově skóre dle Childa a Pugha. Do hodnocení nebyli zařazeni žádní nemocní současně krvácející z jícnových varixů a indikování k výkonu akutně. Hodnocena byla postupně data nemocných zemřelých do 1 měsíce (30denní mortalita 10,9 %), 3 měsíců (23,6 % celého soboru) či 1 roku (46,4 % celého souboru) a byla porovnávána s nemocnými, kteří danou časovou hranici prokazatelně přežívali (zbylí nemocní souboru). Porovnání bylo provedeno vždy pro oba skórovací systémy. Pro hodnocení výsledného skóre v daných podskupinách byl použit nepárový T-test.
K porovnání prediktivní síly obou skóre pro 1měsíční, 3měsíční a 1roční mortalitu byla použita ROC-analýza (Receiving Operating Characteristic) s výpočtem plochy pod křivkou - AUC (Area Under the Curve).
Výpočty přinesly následující výsledky: průměrné MELD-skóre v celé skupině bylo 16 <6; 31> (tab. 3). Průměrné hodnoty MELD-skóre u nemocných zemřelých do 1, 3 a 12 měsíců (21, 20 a 18 bodů) byly vyšší na hladině významnosti p < 0,05 v porovnání se skupinou prokazatelně tuto časovou hranici přežívající (graf 2, tab. 3). Při hodnocení nemocných pomocí Childova-Pughova skóre rozdíl hodnot skóre mezi oběma skupinami dosáhl statistické významnosti až při hodnocení nemocných zemřelých do 3, resp. 12 měsíců, nikoliv v 1. měsíci (graf 3, tab. 4).
Table 3. Hodnoty MELD skóre v jednotlivých podskupinách s výsledky statistického hodnocení. 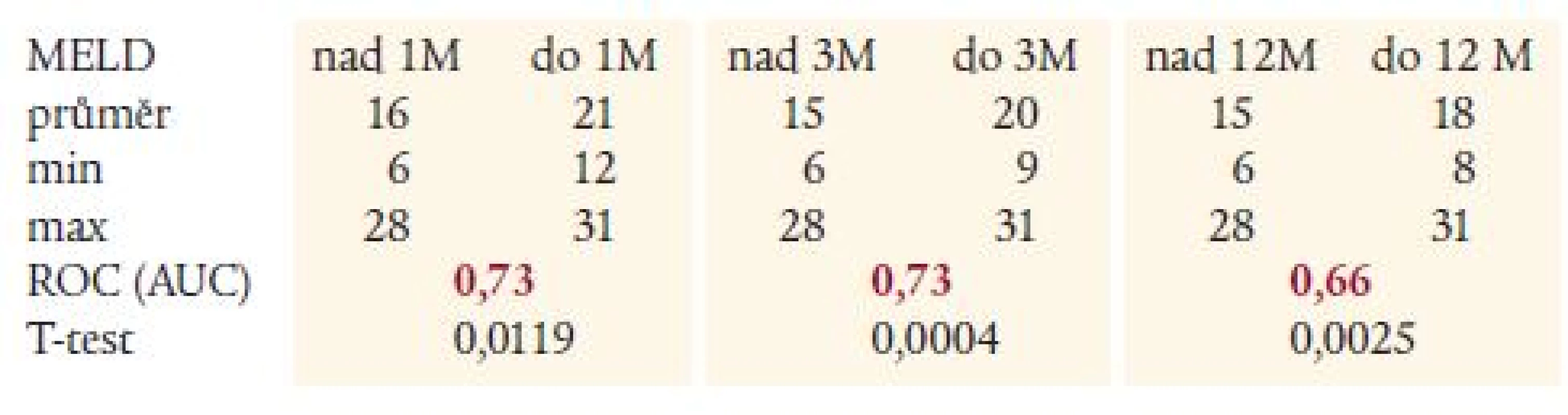
MELD – Model for End stage Liver Disease, M – měsíc Uspokojivá prediktivní síla MELD skóre k určení rizika úmrtí do 1 a 3 měsíců, již neuspokojivá hodnota do 12 měsíců – při hodnocení ROC. Table 4. Hodnoty Childova-Pughova skóre v jednotlivých podskupinách s výsledky statistického hodnocení. 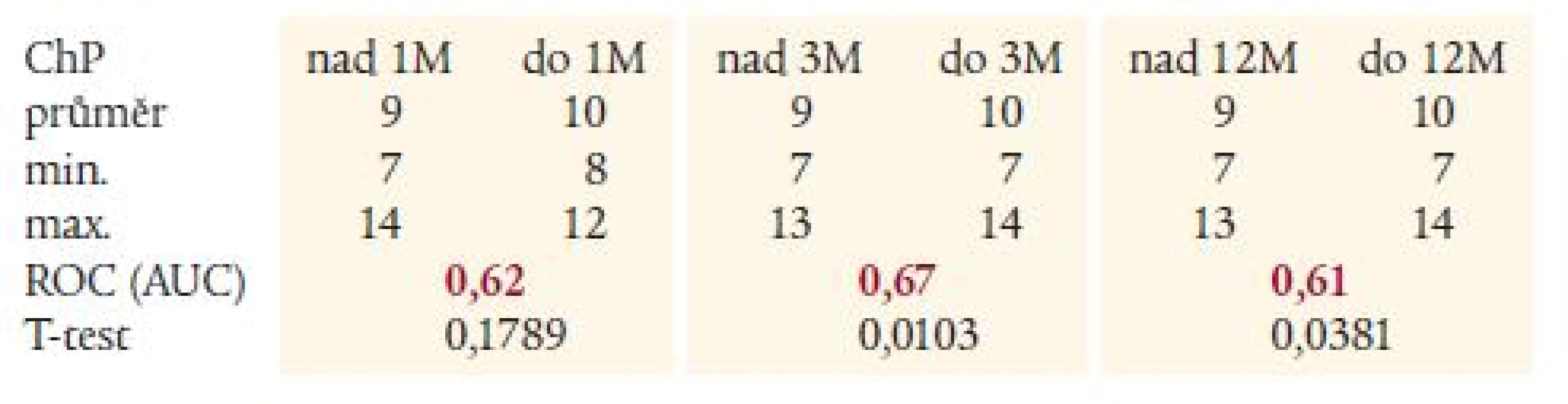
ChP – Childova-Pughova klasifikace, M – měsíc Neuspokojivá prediktivní síla MELD skóre k určení rizika úmrtí do 1, 3 i 12 měsíců – při hodnocení ROC. Graph 1. Porovnání MELD skóre u nemocných zemřelých do 1 měsíce a přežívajících 1 měsíc (zaznamenán významný rozdíl mezi skupinami). 
Graph 2. Porovnání Childova-Pugova skóre u nemocných zemřelých do 1 měsíce a přežívajících 1 měsíc (nezaznamenán významný rozdíl mezi skupinami). 
Graph 3. ROC-analýza MELD pro 1M (uspokojivá prediktivní síla skóre). 
Hodnocení pomocí ROC-analýzy (grafy 4 a 5, tab. 3 a 4) vyznělo v 1. i 3. měsíci pro MELD-skóre (AUC 0,73 pro 1 i 3 měsíce u MELD a 0,62 a 0,67 u Child-Pugh skóre). Pro 12měsíční mortalitu nebyl zaznamenán větší rozdíl a prediktivní hodnota obou skóre byla nízká (AUC 0,66 u MELD a 0,61 u Child-Pugova skóre).
Graph 4. ROC analýza Childova-Pugova skóre pro 1M (neuspokojivá prediktivní síla skóre). 
Diskuse
Poprvé bylo použití Childova skóre popsáno v roce 1964 [13] a následně bylo modifikováno Pughem v roce 1973 [15] (tab. 1). Původně sloužilo k určení míry rizika výkonu pro chirurgické obory u nemocných s jaterním onemocněním indikovaných k chirurgickému výkonu, zejména portokavální spojce. Od roku 1989 pak i k určení míry rizika u nemocných podstupujících TIPS [17]. Následně byl tento systém až do zavedení MELD-skóre [5,6,10,20,23] preferován i transplantační hepatologií. Nevýhodou tohoto skórování se časem ukázala zejména neschopnost dále diferencovat nemocné s hodnotou bilirubinemie nad 51 µmol/l. Dle Childovy-Pughovy klasifikace totiž přiřazujeme stejnou závažnost nemocnému s hodnotou bilirubinu 60 či 300 µmol/l, přičemž hladina celkového bilirubinu je významným prognostickým ukazatelem [16]. Někdy je tomuto systému vytýkáno i částečně subjektivní přiřazování hodnot pro jaterní encefalopatii nebo ascites. Stále je však nejpoužívanějším a časem prověřeným prediktivním skórovacím systémem. Obecně většina autorů považuje nemocné se skóre 12 a vyšším za vysoce rizikové pro TIPS [3,6,9,10,19]. Výše uvedené nevýhody vedly k hledání nových systémů založených spíše jen na laboratorních hodnotách. V poslední době se nejvíce uplatňuje již zmíněné MELD skóre, ale během času vznikly i mnohé další.
Pro urgentní TIPS byl například používán v intenzivní medicíně dobře známý APACHE II [19], nebo pak přímo pro nemocné s jaterním onemocněním vyvinuté, jako Bonn TIPS Early Mortality Score [4] , Emory score [9,22] nebo Prognostic Index, který vedle laboratorních hodnot (INR, kreatininu, trombocytů a leukocytů) pracuje i s údajem o ascitu a umělé plicní ventilaci.
U elektivních výkonů širšího uplatnění dosáhlo však jen MELD-skóre [9,20,22,23]. I toto skórování prošlo svým vývojem [10,14] až do současné podoby, v níž se již nezohledňuje etiologie jaterní cirhózy, a výpočet je postaven pouze na rychle dostupných laboratorních hodnotách - protokol OPTN (Organ Procurement and Transplantation Network). Vzorec k výpočtu je v současnosti dobře dostupný na několika internetových adresách, včetně demonstrací vzorového případu (http://www.optn.org nebo http://www.mayoclinic.org). Zadávání hodnot se většinou provádí v jednotkách běžných v anglosaských zemích. Výpočet je možno provést i dle následujícího vzorce:
MELD = 9,6 *ln(kreatinin mg/dl) + 3,8*ln(bilirubin v mg/dl) + 11,2*ln(INR) + 6,4.
Výsledek se zaokrouhluje na celá čísla a k přepočtu hodnot z µmol/l na mg/dl se hodnoty dělí 17 pro bilirubin a 89 pro kreatinin. Při hodnotách pod 1,0 se pro kreatinin či bilirubin do vzorce dosazuje 1. Pro hodnoty kreatininu nad 4 pak 4,0. Ve více studiích byla následně verifikována uspokojivá prediktivní hodnota jak pro krátkodobé, tak dlouhodobé přežívání nemocných [9].
Výsledky v našem souboru pak podporují spíše závěry práce Salerna [20] či Ferrala [8], kteří prokázali větší prediktivní sílu MELD-skóre v porovnání s Childovou-Pughovou klasifikací, než závěry práce Angermayra [1], v níž statisticky významný rozdíl nebyl pro krátkodobou mortalitu nalezen. Naopak v 6měsíčním horizontu byla u Angermayra lepší predikce přežití stanovena na podkladě Childova-Pughova skóre. U 12měsíční mortality se podle našich výsledků význam skórovacích systémů, a to jak MELD, tak Childovy Pughovy klasifikace snižuje. Může to být dáno poměrně selektovanou skupinou nemocných s refrakterním ascitem, u kterých je jaterní onemocnění již poměrně pokročilé a dekompenzované. Podle posledních prací je právě u těchto nemocných (konsenzuální konference Baveno IV) výpovědní hodnota obou skóre již velice nízká.
Otázkou stále zůstává stanovení určité hranice, nad kterou by nemocní k TIPS již indikováni být neměli. Z předchozích prací vyplývá, že velice rizikoví jsou nemocní s hodnotou MELD-skóre nad 25, u kterých přesahuje 1měsíční mortalita 40 % [9]. V našem souboru byla u těchto nemocných 1měsíční mortalita 33%. Senzitivita a specificita této hranice pro vyloučení nemocného z TIPS je však dle našich výsledků poměrně nízká. Na druhou stranu nemocný s hodnotou pod 25 má jen malou pravděpodobnost časného úmrtí. V našem souboru to bylo nemocných 9 % (senzitivita 95%, specificita 90%), proto nám MELD může přinést i opačnou informaci, kterého nemocného indikovat ještě můžeme. V opačném případě nemocného kontraindikovat k zavedení TIPS pouze na podkladě vysokého MELD-skóre by bylo zřejmě chybou. Vždy je nutno zohledňovat i další faktory, jako jsou věk nemocných, přidružená, zejména kardiovaskulární a plicní onemocnění (přítomnost plicní hypertenze), či etiologie jaterní cirhózy. Z našeho pohledu absence etiologie jaterní cirhózy, která byla dříve ve výpočtu zohledňována se může u nemocných s etylickou jaterní cirhózou jevit jako nevýhodná, jelikož v dlouhodobém sledování je přežívání nemocných, kteří abstinují lepší v porovnání s nemocnými s jinou etiologií jaterního postižení [7] a velká část z těchto nemocných není ani posléze k jaterní transplantaci indikována. Nezanedbatelná je i otázka přímé indikace nemocného k transplantačnímu řešení bez zavedení TIPS, k čemuž nám může pomoci i MELD-skóre (M > 15).
Závěr
MELD-skóre v porovnání s Childovou-Pughovou klasifikací je u nemocných s refrakterním ascitem léčených pomocí transjugulární intrahepatální portosystémové spojky (TIPS) citlivější metodou k posouzení rizika časného úmrtí (v 1 a 3 měsících).
Pro stanovení rizika úmrtí v horizontu dvanácti měsíců je prediktivní síla u obou skóre velice nízká.
Zpracováno s podporou VZ - MZ 000179906 a IGA MZČR NR8419-4.
MUDr. Tomáš Fejfar
II. interní klinika LF UK a FN Hradec Králové
Sokolská 850
500 05 Hradec Králové
e-mail: fejfar@fnhk.cz
Doručeno do redakce: 21. 2. 2006
Přijato po recenzi: 28. 3. 2006
Sources
1. Angermayr B, Cejna M, Karnel F et al. Child-Pugh versus MELD score in predicting survival in patients undergoing transjugular intrahepatic portosystemic shunt. Gut 2003; 52 : 879-885.
2. Azoulay D, Castaing D, Majno P et al. Salvage transjugular intrahepatic portosystemic shunt for uncontrolled variceal bleeding in patients with decopensated cirrhosis. J Hepatol 2001; 35 : 590-597.
3. Banares R, Casado M, Rodriguez-Laiz JM et al. Urgent transjugular intrahepatic portosystemic shunt for control of acute variceal bleeding. Am J Gastroenterol 1998; 93 : 75-79.
4. Brensing KA, Raab P, Textor J et al. Prospective evaluation of a clinical score for 60-day mortality after transjugular intrahepatic portosystemic stent-shunt: Bonn TIPSS early mortality analysis. Eur J Gastroenterol Hepatol 2002; 14 : 723-731.
5. Edwards EB, Harper AM Application of a continuous disease severity score to the OPTN liver waiting list. Clin Transpl 2001; 5 : 19-24.
6. Encarnacion CE, Palmaz JC, Rivera FJ et al Transjugular intrahepatic portosystemic shunt placement for variceal bleeding: predictor of mortality. J Vasc Interv Radiol 1995; 6 : 687-694.
7. Fejfar T, Hulek P, Stefankova J et al. TIPS in the treatment of alcoholic liver cirrhosis. Alcohol and Alcoholism 2003; 38: S04-S04.
8. Ferral H, Gamboa P, Postoak DW et al. Survival after elective transjugular intrahepatic portosystemic shunt creation: prediction with model for end stage liver disease score. Radiology 2004; 231 : 231-236.
9. Ferral H, Patel NH Selection Criteria for patients undergoing transjugular intrahepatic portosystemic shunt procedures: current status. J Vasc Interv Radiol 2005; 16 : 449-455.
10. Forman LM, Lucey MR Predicting the prognosis of chronic liver disease: An evolution from Child to MELD. Hepatology 2001; 33 : 473-475.
11. Hůlek P, Krajina A (eds). Current practice of TIPS, 1. ed. Hradec Králové: Olga Štambergová 2001.
12. Chalasani N, Clark WS, Martin LG et al. Determinants of mortality in patients with advanced cirrhosis after transjugular intrahepatic portosystemic shunting. Gastroenterology 2000; 118 : 138-144.
13. Child CG 3rd, Turcotte JG Surgery and portal hypertension. In: Child CG 3rd (ed). The Liver and Portal Hypertension. Philadelphia: WB Saunders 1964; 50.
14. Kamath PS, Wiesner RH, Malinchoc M et al A Model to Predict Survival in Patients With End Stage Liver disease. Hepatology 2001; 33 : 464-470.
15. Pugh RN, Murray-Lyon IM, Dawson JL et al. Transection of the oesophagus for bleeding oesophageal varices Br J Surg 1973; 60 : 646-649.
16. Rajan DK, Haskal ZJ, Clark TW. Serum bilirubin and early mortality after transjugular intrahepatic portosystemic shunts: results of multivariate analysis. J Vasc Interv Radiol 2002; 13 : 155-161.
17. Richter GM, Noeldge G, Palmaz JC et al. The transjugular intrahepatic portosystemic stent-shunt (TIPSS): result of a pilot study. Cardiovasc Intervent Radiol 1990; 13 : 200-207.
18. Richter GM, Noeldge G, Palmaz JC el al. Transjugular intrahepatic portocaval stent shunt: preliminary clinical results Radiology 1990; 1974 : 1027-1030.
19. Rubin RA, Haskal ZJ, O´Brien CB et al. Transjugular intrahepatic portosystemic shunting: decreased survival for patients with APACHE II scores. Am J Gastroenterol 1995; 90 : 556-563.
20. Salerno F, Merli M, Cazzaniga M et al. MELD score is better than Child-Pugh score in predicting 3-month survival of patients undergoing transjugular intrahepatic portosytemic shunt. J Hepatol 2002; 36 : 494-500.
21. Sherlock S, Dooley J (eds). Diseases of the Liver and Biliary System. 11th ed. Oxford: Blackwell Science 2002.
22. Schepke M, Roth F, Fimmers R et al. Comparison of MELD, Child Pugh and Emory model for prediction of survival in patients undergoing transjugular intrahepatic portosystemic shunting. Am J Gastroenterol 2003; 98 : 1167-1174.
23. Wiesner RH, McDiarmid SV, Kamath PS et al. MELD and PELD: application of survival models to liver allocation. Liver Transpl 2001; 7 : 256-580.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2006 Issue 9-
All articles in this issue
- MELD-skóre v predikci časné mortality u nemocných s refrakterním ascitem léčených pomocí TIPS
- Monitorování glykemie u kriticky nemocných pacientů: srovnání arteriálních a intersticiálních hladin glukózy měřených pomocí mikrodialýzy tukové tkáně
- Diuretika v terapii „diuretické rezistence“ u pacientů s městnavou srdeční slabostí
- Prevence vzniku diabetu 2. typu při léčbě antihypertenzivy ovlivňujícími systém renin-angiotenzin
- Nádorová angiogeneze
- Chronická autoimunitná tyreoiditída a systémové ochorenia spojiva
- Kontrastní látkou indukovaná nefropatie
- Trombendarterektomie plicnice u nemocného s klinickými známkami masivní embolie plicnice
- Traumatická trikuspidální regurgitace: kazuistika
- Kombinace imatinibu s anagrelidem v léčbě blastického zvratu chronické myeloidní leukemie
- Ateroskleróza a infekce?
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- MELD-skóre v predikci časné mortality u nemocných s refrakterním ascitem léčených pomocí TIPS
- Chronická autoimunitná tyreoiditída a systémové ochorenia spojiva
- Diuretika v terapii „diuretické rezistence“ u pacientů s městnavou srdeční slabostí
- Nádorová angiogeneze
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

