-
Medical journals
- Career
Sorafenib – nová naděje pro nemocné s pokročilým hepatocelulárním karcinomem
Authors: J. Abrahámová; M. Kupec
Authors‘ workplace: Fakultní Thomayerova nemocnice, Praha, Onkologické oddělení, Primářka: prof. MUDr. Jitka Abrahámová, DrSc.
Published in: Prakt. Lék. 2011; 91(12): 738-742
Category: Case Report
Overview
Autoři podávají stručný přehled léčby hepatocelulárního karcinomu (HCC) a zaměřují se zejména na léčbu pokročilého HCC sorafenibem. Výsledky studií s uvedeným léčivem prokazují prodloužení přežití u těchto nemocných. Zároveň probíhají klinické studie v adjuvanci či v kombinaci s jiným léčivem či jinou léčebnou metodou.
Povzbudivé výsledky léčby sorafenibem (Nexavar®) autoři dokládají vlastní kazuistikou nemocného s neobvykle dlouhodobým přežitím.Klíčová slova:
sorafenib, hepatocelulární karcinom, celkové přežití HCC, kurativní léčba HCC, paliativní léčba HCC.Úvod
Hepatocelulární karcinom (HCC) je šestým nejčastějším zhoubným nádorem na světě a třetí nejčastější příčinou smrti v důsledku zhoubného onemocnění. Jeho výskyt činí asi 500 tisíc nových případů za rok. Naprostá většina nemocných mu podléhá do jednoho roku od stanovení diagnózy (1).
Přibližně tři čtvrtiny případů (2) se vyskytují v asijských zemích, což koinciduje s vysokou prevalencí chronické infekce virem hepatitidy B (HBV). HCC představuje v Asii nepochybně velkou zdravotní zátěž. Největší výskyt je v Číně (asi polovina všech případů na světě), následuje
- Střední Afrika,
- Japonsko,
- Východní Afrika,
- Melanésie.
V zemích západní Evropy (Itálie 30/100 tisíc) a USA je udávaná incidence 4–5/100 tisíc, ale má narůstající tendenci.
Prevalence HCC jde paralelně nejen s výskytem virové hepatitidy typu B (HBV) ale i typu C (HCV). Chronická HBV infekce je hlavním rizikovým faktorem HCC v afrických a asijských zemích kromě Japonska. Infekce HCV je dominující v Evropských zemích (3, 4) a v Severní Americe a Japonsku.
Kromě virových infekcí je dalším faktorem podílejícím se na vzniku HCC jaterní cirhóza, která může vznikat jak na podkladě virovém, tak na podkladě poškození jater jinými noxami, zejména alkoholem či aflatoxiny. HCC je častější u mužů než u žen. Dalšími faktory podílejícími se na vzniku HCC je obezita, diabetes a hemochromatóza.
V České republice činila incidence v roce 2008 885 nových případů zhoubných novotvarů jater a intrahepatálních žlučových cest (C22), z toho 558 u mužů a 326 u žen (5). Předpokládá se, že hepatocelulární karcinom činí z tohoto počtu 90 % (5). Podle 7. vydání TNM klasifikace (6) se diagnóza C22 dělí na dvě skupiny, a to na
- C22.0 pro hepatocelulární karcinom, a
- C22.1 pro zhoubné nádory intrahepatálních žlučových cest.
TNM klasifikace je rovněž rozdílná.
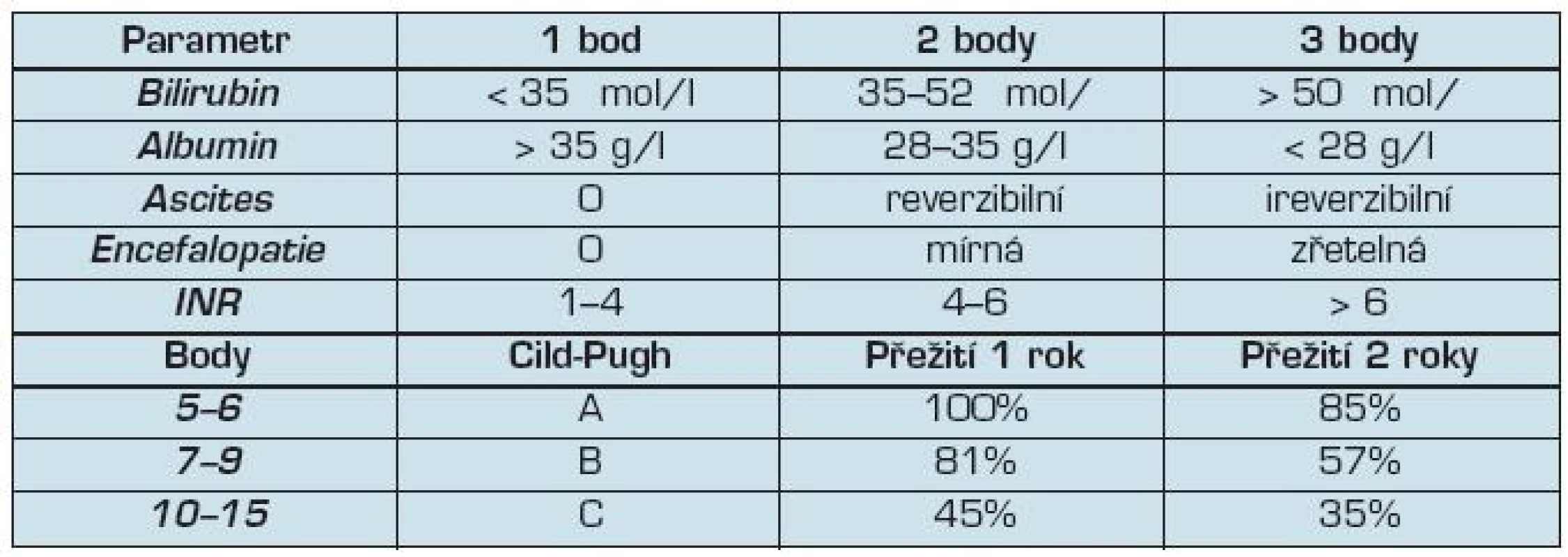
Pro posouzení možnosti léčby je nutné znát funkčnost jater. Běžně se používá skóre podle Childa a Pugha. Toto skóre hodnotí sérové hladiny
- bilirubinu a albuminu,
- výskyt ascitu,
- encefalopatie, a
- INR (tab. 1).
Důležité je též posouzení rozsahu onemocnění. Pro rozsah choroby se kromě TNM klasifikace všeobecně uplatnil systém barcelonský (BCLC systém – Barcelona Clinic Liver Cancer) (tab. 2).
Table 2. Skórovací systém BCLC (Barcelona Ckinic Liver Cancer) – rozhodující pro algoritmus terapie 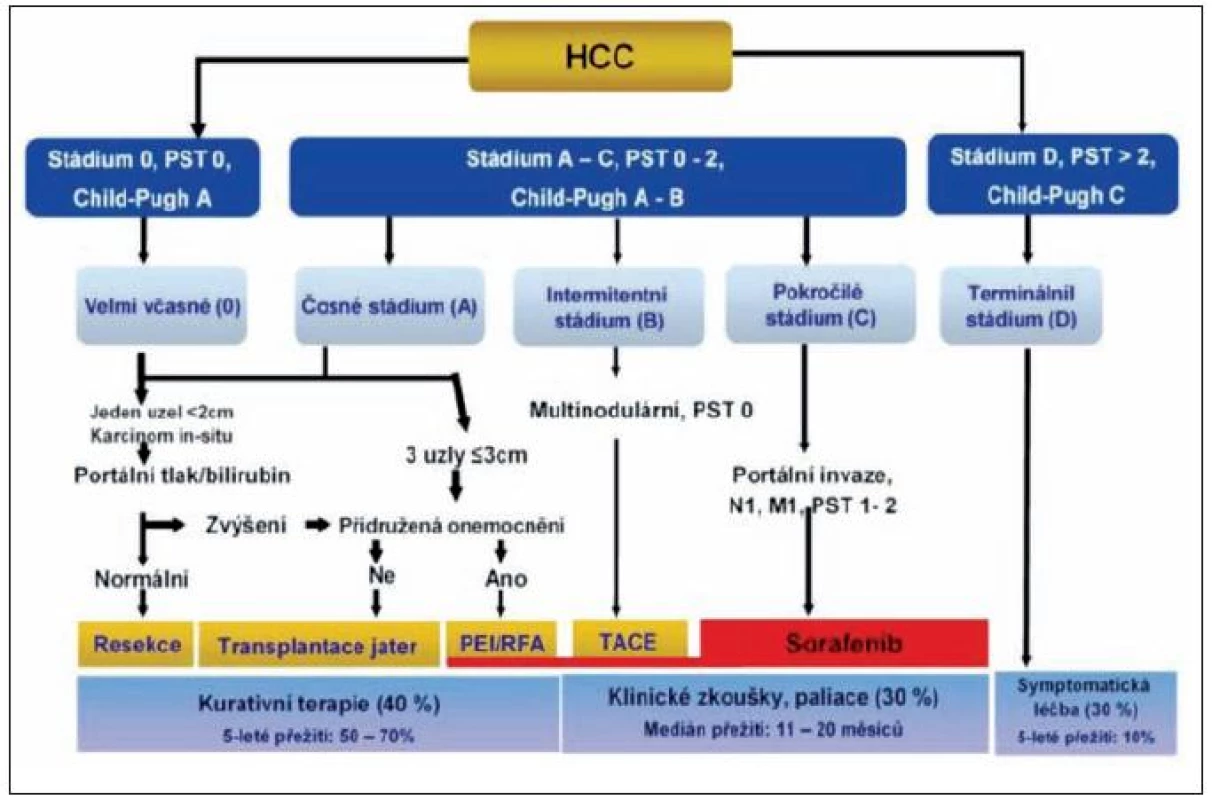
Vysvětlivky: PS – výkonnostní stav (performance status); PEI – perkutánní ethanolová injekce; RFA – radiofrekvenční ablace; TACE – transarteriální chemoembolizace; Léčba pokročilého HCC
V léčbě HCC je jednoznačně rozhodující včasná diagnóza a včas indikovaná kurativní chirurgická léčba. Za jediné potenciálně kurativní metody jsou dosud považovány
- chirurgická resekce, a
- transplantace jater.
Ostatní postupy jako je
- perkutánní etanolová injekce (PEI),
- radiofrekvenční ablace (RFA), či
-
transarteriální chemoembolizace (TACE)
jsou metodami paliativními.
Neléčené, pozdě rozpoznané nebo pokročilé onemocnění má velmi špatnou prognózu. Pětileté přežití u středně pokročilého onemocnění činí asi 16 %. U pokročilé choroby se nemocní dožívají 3 let v 8 %, pětileté přežití je 0 %.
Systémová chemoterapie, která byla v průběhu posledních 25 let uplatňována a v níž byla vyzkoušena řada cytostatik v monoterapii i v kombinaci, nepřinesla žádné přínosné výsledky. Objektivní odpověď se pohybovala mezi 0–25 %. Nikdy se neprokázalo prodloužení celkového přežití.
Hormonální léčba, která se opírala o průkaz estrogenních a androgenních receptorů u některých HCC, nepřinesla žádné pozitivní výsledky (7).
Teprve zavedení sorafenibu do léčebného schématu pokročilého HCC vedlo ke zlepšení přežití u těchto nemocných. Sorafenib je multifunkční inhibitor tyrozinkinázy, který inhibuje B-raf, receptor vaskulárního endoteliálního růstového faktoru (VEGFR), receptor destičkového růstového faktoru (PDGFR) a dále c-kit a RET (8). Má tedy antiproliferační a antiangiogenní účinky, jimiž lze vysvětlit jeho protinádorové působení.
Doporučení pro použití sorafenibu (Nexavar®) u HCC vycházejí ze studie SHARP (Sorafenib HCC Assessment Randomized Protocol), multicentrické, mezinárodní, randomizované studie kontrolované placebem (9, 10, 11). Výsledky studie byly zveřejněny Llovetem et al, (9, 10, 11) na zasedání ASCO v roce 2007.
Tato studie byla dvojjediná.
Vlastní studie SHARP byla uspořádána pro nemocné z Evropy a Severní Ameriky. Do této studie bylo zařazeno 602 nemocných – 299 v ramenu léčebném, 303 v ramenu s placebem.
Druhá studie byla uspořádána pro populaci asijsko-pacifickou, proto název „Asia-Pacific study“. Zařazeno do ní bylo 150 nemocných v ramenu se sorafenibem a 76 v ramenu s placebem.
Vstupní kriteria byla pro obě studie shodná, a to pokročilý HCC, který buď nebyl vhodný pro chirurgickou léčbu, nebo po ní progredoval, výkonnostní stav podle ECOG 0-2, bez předchozí systémové terapie. Použita byla Childova-Pughova klasifikace a systém BCLC. Dávkování bylo stejné v obou studiích, a to sorafenib 400 mg perorálně 2x denně.
Nemocní ve studii Asia-Pacific byli mladší (12), jejich onemocnění bylo pokročilejší, měli více extrahepatálních metastáz a měli horší PS. I přes tyto rozdíly byly konečné výsledky obou studií podobné (graf. 1, str. 741).
Graph 1. Sorafenib u HCC – fáze III 2 shodné studie! potvrzena shodná účinnost u >800 pacientů 
Procento celkového přežití bylo u nemocných léčených sorafenibem signifikantně vyšší oproti skupině s placebem, a to v obou studiích. Z analýzy podskupin vyplývá, že sorafenib prodlužuje přežití bez ohledu na věk nemocného, jeho předchozí kurativní chirurgickou léčbu či TACE, bez ohledu na předchozí rizikový faktor (HCV, alkohol), na výkonnostní stav, a dokonce i bez ohledu na přítomnost či nepřítomnost vaskulární invaze či extrahepatálního šíření. Sorafenib je velmi dobře snášen. Nejčastějšími vedlejšími účinky jsou
- průjem,
- slabost,
- hand-foot syndrom (HFSR),
-
rash, a
deskvamace kůže.V roce 2007 byl sorafenib (Nexavar) registrován EMEA pro léčbu pokročilého HCC. U nás byl Nexavar schválen v srpnu 2008. Patří mezi nákladnou léčbu, kterou je možné aplikovat v Komplexních onkologických centrech (KOC). Proto je nutné pacienty do příslušného KOC včas odeslat.
Sorafenib je v současnosti jedinou účinnou formou farmakoterapie u pokročilého HCC a je součástí odborných doporučení ČOS pro léčbu HCC (13).
Účinnost sorafenibu byla potvrzena metaanalýzou veškerých randomizovaných studií zveřejněných v databázích Medline Pubmed, Cochrane Library. U 828 nemocných se sledovalo
- celkové přežití (OS),
- doba do progrese,
- jakákoliv progrese, a
- výskyt nežádoucích účinků.
Bylo zjištěno signifikantní prodloužení OS u nemocných léčených sorafenibem a signifikantní snížení mortality u téže skupiny nemocných. Procento dosažených remisí bylo vyšší v léčebné skupině (14).
V současnosti probíhá mezinárodní multicentrická neintervenční prospektivní studie GIDEON (Global investigation of therapeutic decision in hepatocelluar carcinoma and of its treatment with sorafenib). Vstupní kriteria jsou pouze dvě, a to:
- neresekovatelný HCC, a
- lékařem plánovaná terapie sorafenibem.
Jsou tedy zařazováni nemocní, kteří běžně přicházejí k léčbě tak, jak je přináší život. Na posledním kongresu ASCO byla zveřejněna druhá interim analýza, ze které vyplynulo podobně jako v původní studii SHARP a v Asijsko-Pacifické studii, že u nemocných z asijsko-pacifické populace je HCC pokročilejší, nemocní jsou mladší, před vstupem do studie podstoupili více lokoregionálních výkonů a větší procento prodělalo infekci HBV (80 %). Vedlejší účinky byly únosné a nevykazovaly etnické ani geografické rozdíly. Incidence kožní toxicity se zdá být nižší u pacientů ve stadiu Child-Pugh B než u nemocných ve stadiu Child-Pugh A. Další analýza má proběhnout v příštím roce, kdy bude možné zveřejnit první výsledky (15,16).
U nás se začala léčba sorafenibem sledovat pomocí lékového registru, jehož zpracovatelským zázemím je Ústav biostatistiky a analýz Masarykovy univerzity v Brně.
Vzhledem k účinnosti sorafenibu v monoterapii je otázkou, zda nelze tuto účinnost zvýšit kombinací s jinými agens. Na toto se budou snažit odpovědět randomizované studie SPACE a studie SEARCH.
První ze studií sleduje kombinaci sorafenibu s TACE oproti TACE samotnému. Druhá studie zkoumá kombinaci sorafenibu s erlotinibem oproti sorafenibu samotnému.
Jestliže je sorafenib účinný u pokročilého onemocnění, z logiky věci vyplývá předpoklad jeho účinnosti v adjuvanci. Tento předpoklad ověřuje studie STORM, která u nemocných s HCC po kurativní chirurgické léčbě aplikuje sorafenib ve výzkumném rameni. V kontrolním rameni nemocní dostávají placebo. Všechny tři studie slibují zajímavé výsledky.
Sorafenib je první systémovou léčbou, která prokázala prodloužení přežití pacientů s pokročilým HCC. Je schválen ve více než 60 zemích a stal se tak referenčním standardem pro pokročilý HCC (14).
Vlastní pozorování
Kazuistika prezentuje výjimečně dlouhé trvání léčebného efektu sorafenibu (Nexavaru ®). Pacient R.P., narozen 1948, měl v anamnéze hepatitis B ve 35 letech. Dne 16. 6. 2007 byl na chirurgické klinice Fakultní Thomayerovy nemocnice akutně laparotomován pro hemoperitoneum, vzniklé bez jakýchkoli prodromů. Peroperačně byl v jaterním segmentu S5-6 nalezen tumor velikosti 5 cm a v segmentu S8 další krvácející tumor velikosti 3–4 cm. Krvácení bylo úspěšně stavěno koagulací. Pacient byl posléze podrobně vyšetřen.
CT prokázalo, že segmenty S5, 6 a 8 jsou prostoupeny nepravidelně neostře ohraničenými a zčásti splývajícími ložisky velikosti okolo 25 mm. Jedno z ložisek se propagovalo mírně extrahepatálně a tlačilo na portu před jejím větvením (obr. 1). Podle angio CT expanzivní ložisko infiltrovalo prakticky celý pravý lalok jaterní a vrůstalo do kmene v. portae (obr. 2).
Image 1. Červen 2007, červeně je vyznačen rozsah tumorózního postižení jaterního parenchymu a žlutě krvácející ložisko 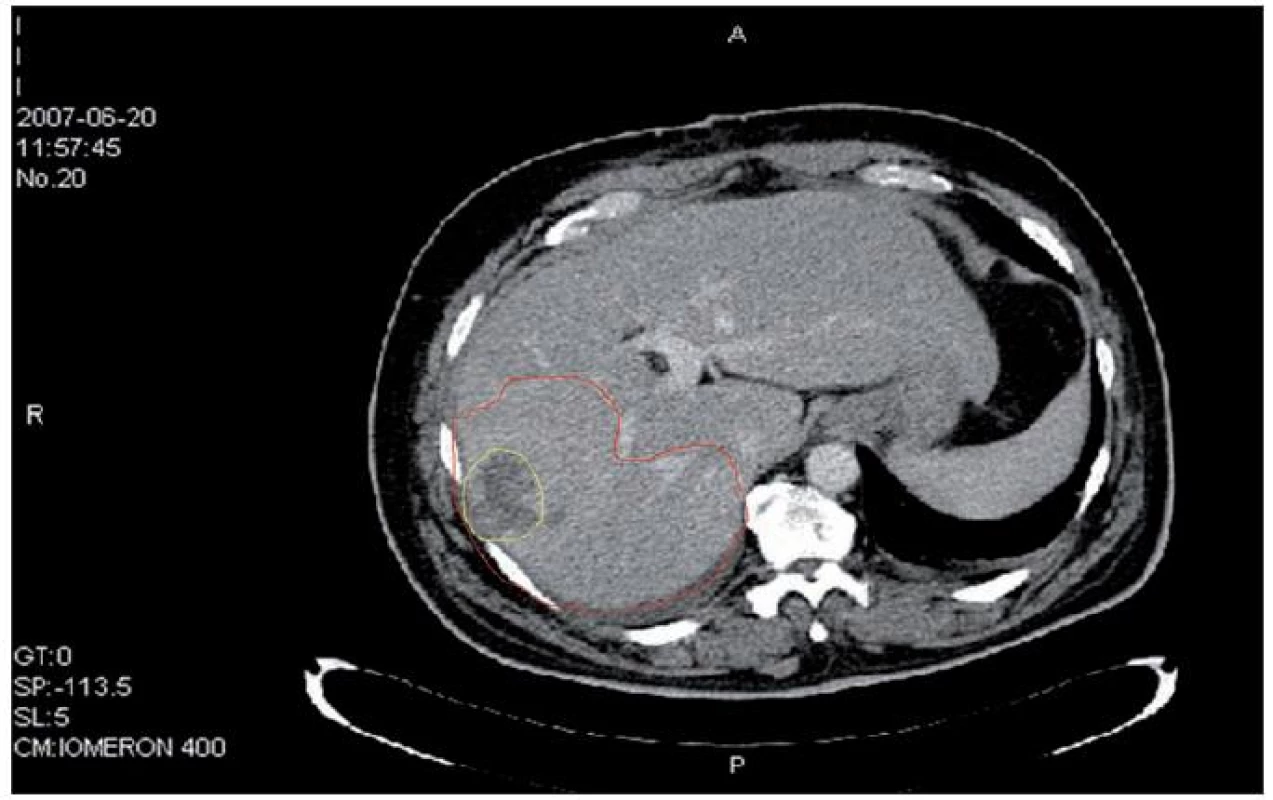
Image 2. Červen 2007, angio CT, červeně je vyznačena propagace tumoru do lumen portální žíly 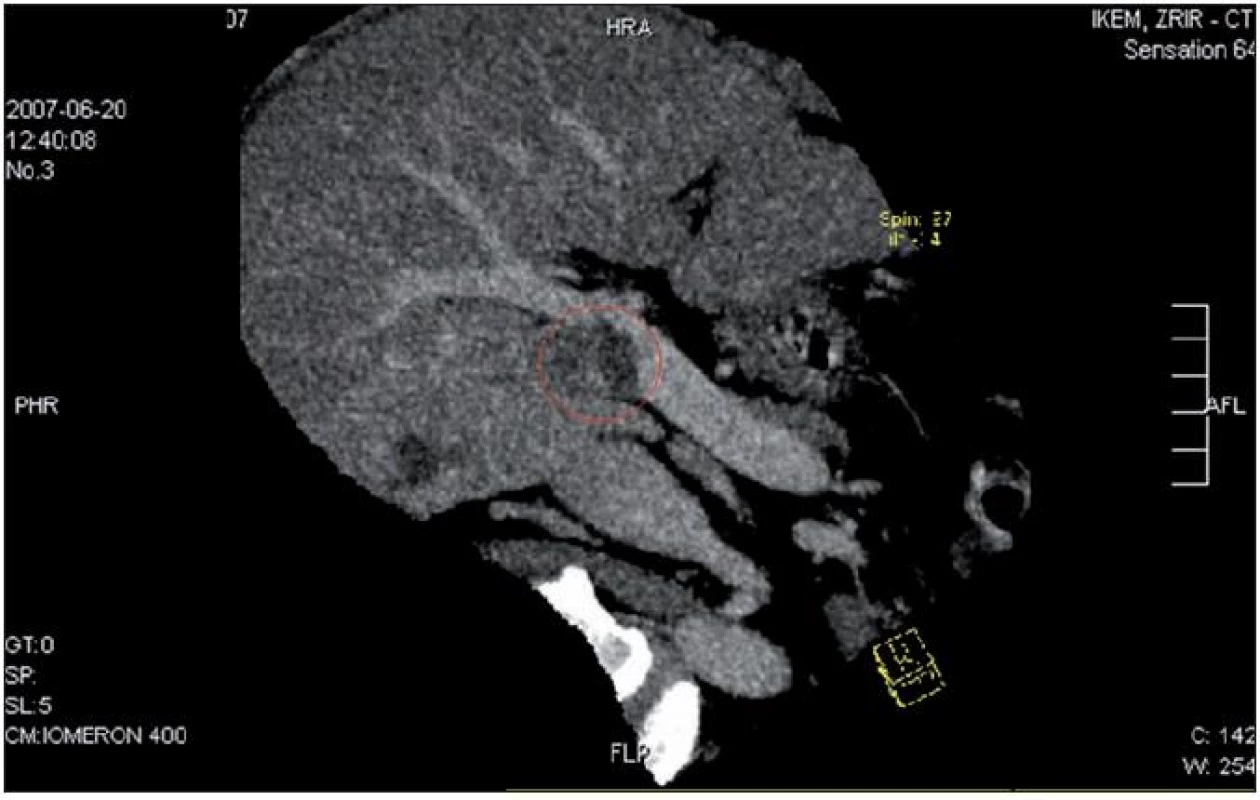
Dne 2. 8. 2007 byla elektivně provedena neanatomická resekce jaterního segmentu S8 spolu s cholecystektomií. Podle peroperačního ultrazvukového vyšetření byly postiženy i segmenty S1 a S5-8, kolem S5 byly přítomny satelity, peroperačně byla potvrzena infiltrace kmene v. portae, téměř obturující její lumen.
Pacientovi byly zavedeny 2 port-katétry, jeden zleva do povodí vv. portae cestou vv. gastroepiploicae (extrakce v říjnu 2007 pro flegmónu v jeho okolí) a zprava do a. hepatica cestou aa. gastroduodenalis (extrakce v srpnu 2008 pro chronickou zánětlivou píštěl nad portem).
Bioptické vyšetření resekátu prokázalo dobře diferencovaný hepatocelulární karcinom. Onemocnění bylo hodnoceno jako pT3 pNX M0 (Child-Pugh A).
Léčba byla zahájena v říjnu 2007 imunochemoterapií (Roferon ascendentně 3–9 MIU s.c. 3x týdně, 5-FU 75 mg/m2 týdně i.a.). Pro progredující elevaci markeru CA 19-9 v séru byla tato léčba jako neúčinná ukončena v březnu 2008. Alfa-fetoprotein nádor nesecernoval a jeho sérové hodnoty nebyly nikdy zvýšeny.
Cílenou léčbu Nexavarem jsme zahájili v dubnu 2008. Již za měsíc, v květnu 2008, byla na CT břicha patrná nekrotizace jaterních ložisek a (do té doby stoupající) sérová hodnota CA 19-9 od dubna 2008 do září 2009 rychle poklesla ze >180 na 65 kU/l.
Snášenlivost léčby byla po celou dobu velmi dobrá, její nežádoucí účinky byly omezeny pouze na průjem, hand-foot syndrom se neprojevil vůbec, běžné životní aktivity nebyly nikterak omezeny, PS (performance status) trvale 0–1.
Po 30 měsících terapie Nexavarem v říjnu 2010 začala hodnota CA 19-9 stoupat z historicky nejnižší hodnoty (52 kU/l) až na 70 kU/l. V červnu 2011 PET/CT prokázala (kromě stacionárního nálezu v játrech s útlakem pravé větve v. portae) nově osteolytické ložisko v příčném výběžku obratle Th5. Nemocného jsme po dohodě předali k další léčbě na kooperující pracoviště, kde byl zařazen do studie s ramucirumabem (obr. 3).
Image 3. Únor 2011; červeně je vyznačen rozsah tumorózního postižení 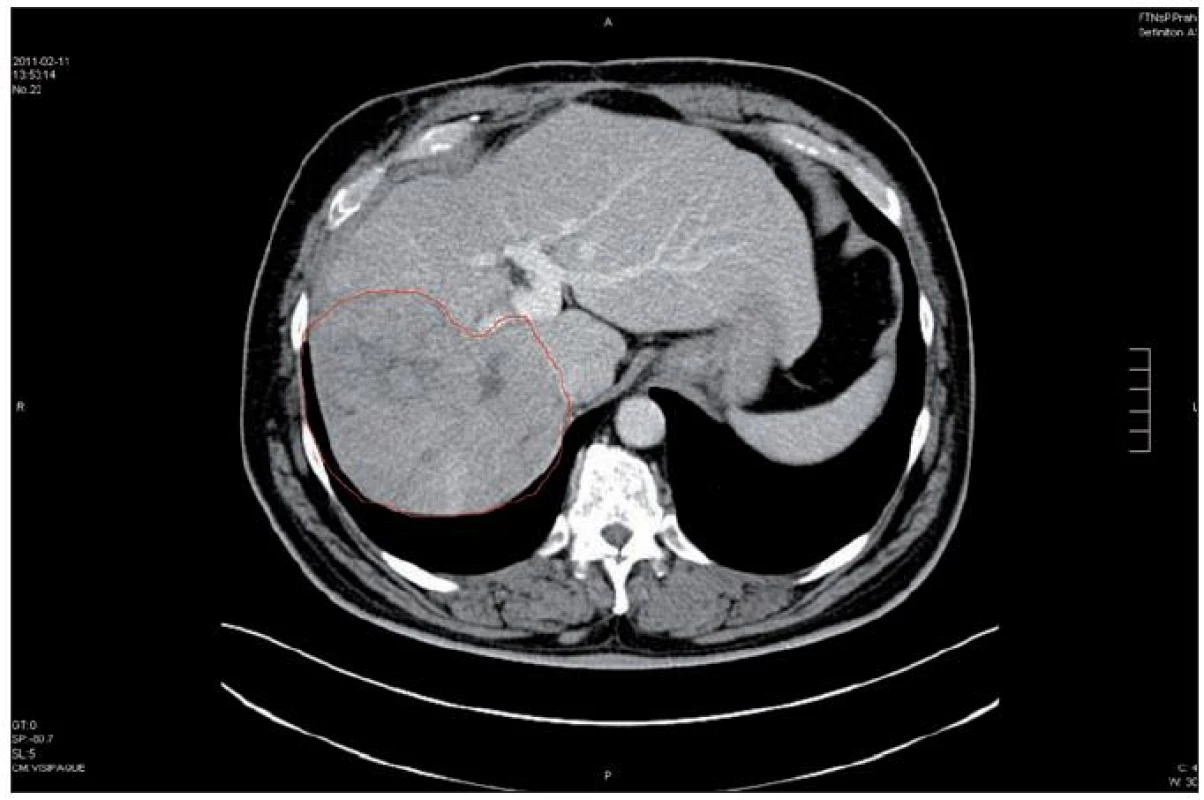
Diskuse a závěr
Metodou volby v léčbě hepatocelulárního karcinomu zůstává chirurgická resekce. Kurativní operaci je však možné provést pouze u malé části nemocných (cca 20 %). Nejčastějším důvodem inoperability je lokálně pokročilý tumor či chronické jaterní léze, které jsou spojené s významnou poruchou jaterní funkce. Nemocní s malým HCC v terénu jaterní cirhózy bez závažných komorbidit splňující striktní kriteria k zařazení, jsou indikováni k jaterní transplantaci.
Transarteriální chemoembolizace TACE se doporučuje u neresekabilního HCC bez známek extrahepatální progrese. U části nemocných s dobrou léčebnou odpovědí může TACE vést ke zmenšení nádoru, zlepšení operability a k chirurgické resekci v druhé době. Paliativní ablační metody jako
- kryodestrukce,
- radiofrekvenční ablace,
-
etanolizace a další
nemají vliv na prodloužení přežití nemocných s HCC.
Celkovou špatnou prognózu neoperabilního HCC neovlivnila ani léčba řadou chemických, hormonálních agens či interferonem.
Výsledky léčby HCC zůstávají neuspokojivé. Vedle zdokonalování primární a sekundární prevence je v současnosti v popředí reálného zájmu především vyhledávání a diagnostika časných stádií HCC u definovaných rizikových skupin nemocných. Nemocní s malým HCC bez známek angioinvaze, ošetření resekcí či transplantací jater mají největší naději na dlouhodobé přežívání.
Zavedení sorafenibu (Nexavar®) do léčby HCC však přináší i nemocným s pokročilými stádii onemocnění novou naději na výrazné prodloužení přežití. Příklad našeho pacienta (PFS – progress free survival – přežití bez progrese) 38 měsíců a OS (overall survival – celkové přežití) ke konci července 2011 již 48 měsíců) tuto naději posiluje.
Pro všechny lékaře u nás, kteří se s takovým onemocněním setkají, je prvořadým požadavkem poslat nemocného do příslušného Komplexního onkologického centra, které jediné je oprávněno sorafenibem léčit.
Podrobnosti o diagnostice a léčbě hepatocelulárního karcinomu jsou uvedeny ve speciální příloze časopisu Farmakoterapie z října 2011 (17-23).
Poděkování
Autoři děkují Radiodiagnostickému oddělení Fakultní Thomayerovy nemocnice (prim. MUDr. J. Urbanová) za možnost zveřejnění obrázku 2 a 4 a Základně radiodiagnostiky a intervenční radiologie (vedoucí – prof. MUDr. J. Peregrin, CSc.) za možnost zveřejnění obrázku 3.
Prof. MUDr. Jitka Abrahámová, DrSc.
Onkologické oddělení FTNsP
Vídeňská 800
140 00 Praha 4-Krč
E-mail: jitka.abrahamova@ftn.cz
Sources
1. Parkin, D.M., Whelan, S.L., Ferlay, J. et al. Cancer incidence in five continents, vol. VIII. Lyon: IARC Scientific; 2002. Publication No. 155.
2. Chen, C.J., Liang, K.Y., Chang, A.S. et al. Effects of hepatitis B virus, alcohol drinking, cigarette smoking and familial tendency on hepatocellular carcinoma. Hepatology 1991, 13, p. 398-406.
3. Fattovich, G., Ribero, M.L., Pantalena, M., et al. Hepatitis C virus genotypes: distribution and clinical significance in patients with cirrhosis type C seen at tertiary referral centres in Europe. J. Viral. Hepat. 2001, 8, p. 206-216.
4. Bruno, S., Silini, E., Crosignani, A. et al. Hepatitis C virus genotypes at risk of hepatocellular carcinoma in cirrhosis: a prospective study. Hepatology 1997, 25, p. 754-758.
5. ÚZIS ČR. Novotvary 2008. Praha: ÚZIS 2011.
6. Sobin, L.H., Gaspodraowicz, M.K., Wittekind, Ch. TNM classification of malignant tumours, 7. ed. London: Wiley-Blackwell, 2009 (české vydání 2011).
7. Thomas, M.B., Zhu, A.X. Hepatocellular carcinoma: The need for progress. J. Clin. Oncol. 2005, 23, p. 2898-2899.
8. Wilhelm, S., Carter, C., Lynch, M. et al. Discovery and development of sorafenib: a multikinase inhibitor for treating cancer. Nat. Rev. Drug. Discov. 2006, 5, p. 835-844.
9. Llovet, J.M., Bruix, J. Novel advancements in the management of hepatocellular carcinoma in 2008. J. Hepatol. 2008; 48 (Suppl 1), S20-S37.
10. Llovet, J.M., Bruix, J. Molecular targeted therapies in hepatocellular carcinoma. Hepatology 2008, 48, p. 1312-1327.
11. Llovet, J.M., Ricci, .S, Mazzaferro, V. et al. Sorafenib in advanced hepatocellular carcinoma. N. Engl. J. Med. 2008, 359, p. 378-390.
12. Cheng, A.L., Kang, Y.K., Chen, Z. et al. Efficacy and safety of sorafenib in patients in the Asia-Pacific region with advanced hepatocellular carcinoma: a phase III randomised, double-blind, placebo controlled trial. Lancet Oncol. 2009, 10, p. 25-34.
13. Česká onkologická společnost ČLS JEP. Zásady cytostatické léčby onkologických onemocnění 2011. Dostupné z http://www.linkos.cz/informace-pro-praxi/zasady-cytostaticke-lecby/.
14. Cinco, R.U.C., Ignacio, J.G., Domingo, F. Sorafenib in the treatment of advanced hepatocellular carcinoma: A meta-analysis of randomized trials. Hepatol. Int. 2011, 5, 3-558, PP29-07.
15. Yoon, S.K., Ye, S.L., Marrero, J. et al. GIDEON (Global Investigation of therapeutic Decision in Hepatocellular Carcinoma and Of its treatment with sorafeNib) interim results: regional subgroup analysis. Hepatol. Int. 2011, 5, 3-558, FC02-05.
16. Ye, S.L., Marrero, J., Lencioni, R. et al. GIDEON (Global Investigation of therapeutic Decision in Hepatocellular Carcinoma and Of its treatment with sorafeNib) interim results: Child-Pugh Status Subgroup Analysis. Hepatol Int, 2011, 5, 3-558, PP34-25.
17. Hlavová, K., Urbánek, P., Zavoral, M. Screening, diagnostika, klasifikace a terapie hepatocelulárního karcinomu. In: Farmakoterapie – Léčba hepatocelulárního karcinomu 2011. 2011; 7 (speciální příloha): 4–10.
18. Kala, Z., Kysela, P., Penka, I., et al. Hepatocelulární karcinom – možnosti radikální léčby. In: Farmakoterapie – Léčba hepatocelulárního karcinomu 2011. 2011; 7 (speciální příloha): 11–19.
19. Andrašina, T., Válek, V., Tomášek, J., et al. Radiologická léčba hepatocelulárního karcinomu. In: Farmakoterapie – Léčba hepatocelulárního karcinomu 2011. 2011; 7 (speciální příloha): 20–26.
20. Kiss, I., Halámková, J. Možnosti farmakoterapie hepatocelulárního karcinomu. In: Farmakoterapie – Léčba hepatocelulárního karcinomu 2011. 2011; 7 (speciální příloha): 27–31.
21. Abrahámová, J. Postavení sorafenibu v současné medikamentózní léčbě hepatocelulárního karcinomu. In: Farmakoterapie – Léčba hepatocelulárního karcinomu 2011. 2011; 7 (speciální příloha): 32–39.
22. Kupec, M., Büchler, T., Abrahámová, J. Dlouhodobé přežití pacienta s pokročilým hepatocelulárním karcinomem léčeného sorafenibem. In: Farmakoterapie – Léčba hepatocelulárního karcinomu 2011. 2011; 7 (speciální příloha): 40–41.
23. Priester, P., Kubala, E. Léčba hepatocelulárního karcinomu – kazuistika. In: Farmakoterapie – Léčba hepatocelulárního karcinomu 2011. 2011;7 (speciální příloha): 42–44.
Labels
General practitioner for children and adolescents General practitioner for adults
Article was published inGeneral Practitioner

2011 Issue 12-
All articles in this issue
-
Základy kognitivní, afektivní a sociální neurovědy
XII. Geny a kultura - Medicína dlouhodobé péče u nás i v zahraničí
- Jak rozdělit postupy, které mírní bažení (craving)
- Intersticiální plicní procesy v otázkách a odpovědích
- Ulcerogenita kortikoidů – přežívající mýtus mezi českými lékaři
- Standardizace nutriční péče v domově pro seniory
- Psychoterapeutický přístup v medicíně
- Srovnání metod DXA a BIA u obézních žen indikovaných ke sleeve gastrektomii – pilotní studie
-
Eutanázie a svědomí
Proč je etická diskuse tak obtížná? - Deficit objemu telových tekutín hodnotený sestrami podľa diagnostických znakov ošetrovateľskej diagnózy
- Telomery a vliv životního stylu na jejich délku
- Sorafenib – nová naděje pro nemocné s pokročilým hepatocelulárním karcinomem
- Vyšetření asymetrie páteře u předškolních dětí
-
Základy kognitivní, afektivní a sociální neurovědy
- General Practitioner
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Ulcerogenita kortikoidů – přežívající mýtus mezi českými lékaři
- Jak rozdělit postupy, které mírní bažení (craving)
- Deficit objemu telových tekutín hodnotený sestrami podľa diagnostických znakov ošetrovateľskej diagnózy
- Intersticiální plicní procesy v otázkách a odpovědích
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career