-
Medical journals
- Career
Zánětlivý pseudotumor močového měchýře jako projev aktivity u pacientky s granulomatózou s polyangiitidou (Wegenerovou granulomatózou) – méně obvyklá manifestace ANCA-asociované vaskulitidy
Authors: Jakub Řezáč 1; Zdenka Hrušková 1; Pavel Konopásek 1; Eva Honsová 2; Martin Mašek 3; Romana Ryšavá 1; Vladimír Tesař 1
Authors‘ workplace: Klinika nefrologie 1. LF UK a VFN, Praha 1; Pracoviště klinické a transplantační patologie IKEM, Praha 2; Radiodiagnostická klinika 1. LF UK a VFN, Praha 3
Published in: Ces Urol 2014; 18(3): 240-245
Category: Case report
Overview
Granulomatóza s polyangiitidou (GPA) je v České republice nejčastější z ANCA-aso-ciovaných vaskulitid, tj. vaskulitid (převážně) malých cév, které mohou postihovat kterýkoliv orgán v lidském těle. Postižení urogenitálního systému je poměrně vzácné a může být diagnosticky svízelné. My zde předkládáme kazuistiku pacientky s GPA, k jejímž iniciálním projevům patřila i tumorózní afekce močového měchýře. Diferenciálně diagnosticky byl zvažován i karcinom močového měchýře, odlišení od ložiskového zánětu v rámci aktivní vaskulitidy bylo pro další postup, který u GPA standardně zahrnuje potenciálně toxický cyklofosfamid, velmi důležité a bylo umožněno hodnocením biopsie patologem-specialistou. Jak dokumentujeme na opakovaných CT snímcích, po imunosupresivní terapii došlo k úplné regresi nálezu v močovém měchýři.
Závěr:
Projevy GPA jsou velmi pestré, správná dia-gnóza tohoto vzácného onemocnění může pacienta uchránit od zbytečného chirurgického výkonu či dokonce další cytostatické terapie.Klíčová slova:
ANCA, granulomatóza s polyangiitidou, močový měchýř, tumor, vaskulitida.ÚVOD
Wegenerova granulomatóza, dnes nazývána granulomatóza s polyangiitidou (GPA), je autoimunitní choroba řazená mezi vaskulitidy malých cév, které jsou charakterizovány nekrotizujícím zánětem stěny především drobných cév. Vaskulitidy malých cév se dnes podle revidované klasifikace z Chapel Hillu dělí na vaskulitidy imunokomplexové (např. IgA vaskulitida, dříve Henoch-Schöenleinova purpura) a ANCA-asociované, mezi něž řadíme kromě GPA i eozinofilní granulomatózu s polyangiitidou a mikroskopickou polyangiitidu. GPA je nejčastěji asociována s postižením horních a dolních cest dýchacích a ledvin. Postižen však může být kterýkoliv z orgánů lidského těla, především nervový systém (centrální i periferní), kůže, gastrointestinální trakt a srdce (1). Rovněž závažnost onemocnění může být různá – od lokalizovaných ORL forem po těžké, život ohrožující. Obvykle bývá GPA spojena s výskytem ANCA (Anti-Neutrophil Cytoplasmic Antibody) protilátek, konkrétně cANCA (se specifickým cytoplazmatickým obrazem při nepřímé imunofluorescenci), jejichž cílovým antigenem je obvykle proteináza 3 (PR3-ANCA). Protilátky cANCA jsou nalézány přibližně u 90 % pacientů s generalizovanou GPA (2, 3), u lokalizovaných forem může být výskyt nižší.
Z epidemiologického hlediska je GPA na vzestupu, částečně je to ale dáno také zlepšenou diagnostikou i prognózou tohoto potenciálně smrtelného onemocnění. Incidence se odhaduje na 4–12/milion, nejvyšší je okolo 60. roku života a mírně častěji jsou postiženi muži (1,3 : 1). Standardním léčebným postupem generalizované formy GPA je dodnes podávání kombinované imunosupresivní terapie kortikoidy a cyklofosfamidem, u závažných forem (renální selhání, plicní krvácení) i využití plazmaferézy (4, 5).
Urogenitální manifestace GPA je jednou z méně častých, většinou popisovanou ve formě kazuistik. Vaskulitida je příčinou nekrózy tkáně a je doprovázená intenzivní zánětlivou reakcí vytvářející ložiska, proto histologické nálezy z drobných bioptických vzorků nemusí být specifické, protože většinou zachytí pouze okrajový zánět a ne typickou cévní lézi (6). Rovněž může vaskulitida klinicky a na zobrazovacích metodách imitovat tumory, kde poté hrozí riziko zbytečně provedeného chirurgického zákroku až jiné agresivní terapie, a zároveň ohrožení funkce vitálně důležitých orgánů nerozpoznanou vaskulitidou.
Projevy GPA v močovém měchýři jsou velmi vzácné, ale naopak je známo, že při dlouhodobé léčbě cyklofosfamidem, trvající déle než 1 rok, se až u 10 % pacientů během následujících 16 let vytvořil papilokarcinom močového měchýře (7). Správné rozlišení etiologie ložiskové afekce u pacienta s GPA je tedy zásadní pro další léčebný postup. Uvádíme raritní případ afekce močového měchýře, která klinicky působila dojmem tumoru u pacientky se současně diagnostikovanou GPA.
Obr. 1A. Močový měchýř, vaskulitida žíly s fibrózním uzávěrem lumen a s destrukcí žilní stěny v pravé části snímku (šipky) Fig. 1A. Urinary bladder, vasculitis of the vein with fibrotic occlusion of the vessel lumen and segmental vasculitis with complete destruction of vessel wall in the right side of the picture (arrows) Obr. 1B. Ledvina, glomerulus s nekrózou hilové arterioly a současně s nekrózou trsu s epitelovým srpkem. Poškození glomerulu doprovází zánět v intersticiu. Fig. 1B. Glomerulus showing severe necrosis of the tuft surrounded by crescent formation and also fi brinoid necrosis of a hilar arteriole associated with prominent periglomerular granulomatous infl ammation 
Image 1. CT ložisko močového měchýře s kalcifikací – jeho regrese a vymizení Fig. 2. Pathologic CT finding in urinary bladder – its regression and complete disappearance 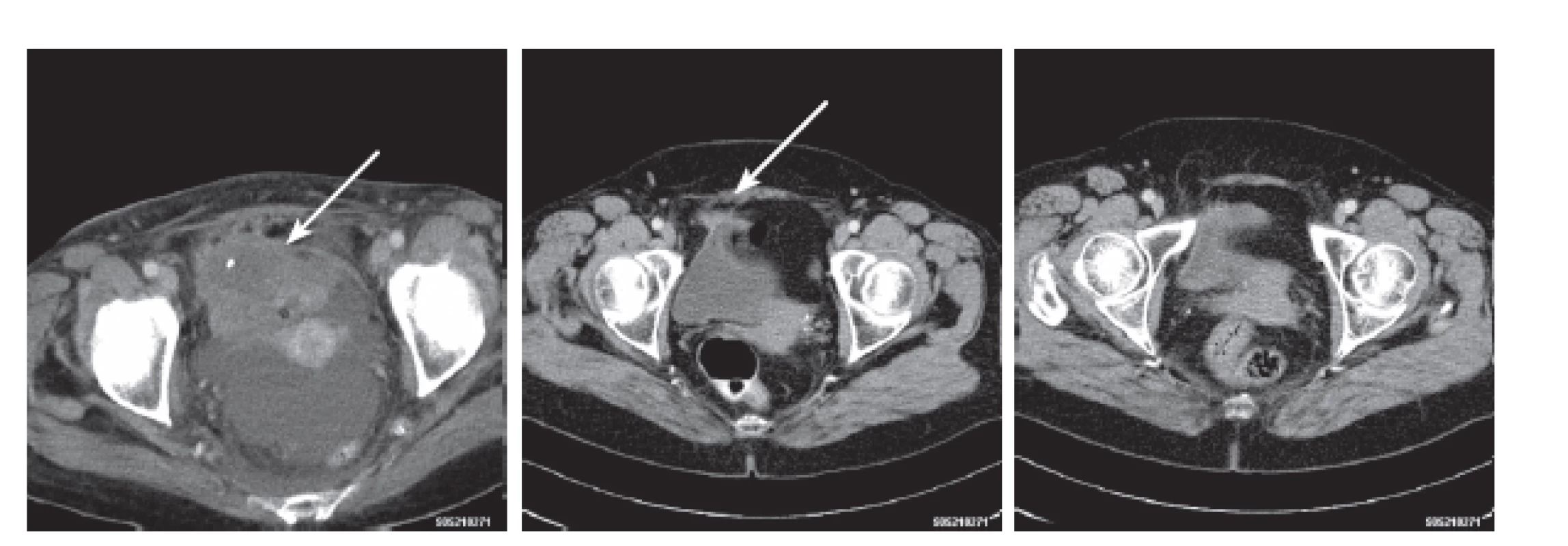
POPIS PŘÍPADU
Pacientka, 56 let, s negativní rodinnou anamnézou, kuřačka, byla léčena v LDN pro trofický defekt dolní končetiny. Tam byla zjištěna progrese renální insuficience. K nám byla přijata pro suspektní ANCA asociovanou vaskulitidu (ANCA antiPR3 pozitivita) a akutní renální selhání s nutností hemodialýzy.
V její osobní anamnéze se dále nacházela chronická obstrukční plicní nemoc a arte-riální hypertenze. Subjektivně se pacientka při překladu na naši kliniku cítila až na mírnou bolest hlavy dobře, popisovala oligurii a makroskopickou hematurii.
Ještě 2 měsíce před hospitalizací měla pacientka prokazatelně renální funkce v normě. Diagnóza ANCA asociované vaskulitidy byla potvrzena pozitivitou PR3-ANCA protilátek (nad 100 IU/ml, norma do 5) a renální biopsií s nálezem vysoce floridní, tzv. pauciimunní (tj. v cévách se zjistí jen malá nebo žádná depozita imunitních komplexů) glomerulonefritidy (s rozpadem glomerulů včetně pouzder) a vaskulitidou mimo glomeruly. Morfologie byla dobře kompatibilní s GPA. Dále dle CT hrudníku pacientka krvácela do plic, trofický defekt DK byl hodnocen jako vs. kožní postižení vaskulitidou.
Na CT břicha provedeném v místě bydliště byl popsán nejasný útvar sousedící s dělohou. Byla provedena sigmoideoskopie s normálním nálezem a dále cystoskopie, která rovněž diagnózu neobjasnila.
U nás bylo opakováno CT vyšetření břicha a popsána nehomogenně se sytící solidní expanze močového měchýře o velikosti 90 × 80 × 60 mm s kalcifikacemi.
Cystoskopicky byl na přední stěně měchýře patrný křehký bílý plošný tumor, který ve vertexu přecházel v tvrdý skirhus. V diferenciální diagnóze jsme uvažovali o papilokarcinomu či zánětlivém pseudotumoru nevaskulitické etiologie. Jako nejpravděpodobnější možnost se však zdálo, že se jedná o nekrotizující granulomatózní vaskulitidu s ložiskovými projevy, což bylo následně potvrzeno biopsií. Nález z biopsie byl popsán jako nekrotizující cystitida, ve druhém čtení patologem-specialistou byla afekce hodnocena jako nekrotizující granulomatózní vaskulitida s jizvením a s postižením žil různého stáří odpovídající projevům ANCA pozitivní vaskulitidy.
Pacientce byly podány pulsy kortikosteroidů a první puls cyklofosfamidu i.v. a vzhledem k selhání ledvin a krvácení do plic byla zahájena léčba plazmaferézou obden, celkem 10krát. Pro anasarku a renální selhání vstupně byla nutná denně hemodialýza s ultrafiltrací. Po 4 dnech nastal rozvoj diurézy. ANCA protilátky klesaly. Po 2 týdnech bylo možné ukončit dialyzační léčbu. Po 3 měsících a podání 6 pulsů cyklofosfamidu bylo provedeno kontrolní CT malé pánve, které prokázalo výraznou regresi „tumorózního“ ložiska, z původních 90 × 80 × 60 mm se patologická formace s kalcifikacemi zmenšila na 20 × 10 mm.
Po sedmém pulsu cyklofosfamidu (kumulativní dávka 5,025 g) byla pacientka převedena na udržovací terapii mykofenolát-mofetilem (který byl zvolen namísto běžně užívaného azathioprinu z důvodu známé hepatopatie). Klinický stav pacientky byl uspokojivý, renální funkce stabilní (kreatinin 130), močový nález negativní, zánětlivé parametry nízké, ANCA protilátky negativní, RTG nález nesvědčil pro aktivitu onemocnění v plicní oblasti. Při kontrolním CT vyšetření byl již i nález na močovém měchýři normální. Stav pacientky byl nadále uspokojivý i 2 roky od počátku léčby, ANCA protilátky negativní a renální funkce stabilizovány, léčba mykofenolát mofetilem (lék byl použit v off-label indikaci) mohla být ukončena. Bylo dosaženo dlouhodobé kompletní remise onemocnění.
DISKUSE
Jak již jsme uvedli v úvodu, urogenitální projevy GPA jsou jedny z méně častých a projevy v močovém měchýři jsou zcela vzácné. Mezi 125 pacienty s GPA pravidelně sledovanými na naší klinice, měli pouze dva diagnostikované urogenitální postižení, 1krát se jednalo o nekrotizující granulomatózní zánět nadvarlete. A zde uvádíme druhý případ – mapovité nekrózy s granulomatózními lemy při vaskulitidě v močovém měchýři. Například Hooda a Parsons v kazuistice z roku 2011 uvádějí, že byly popsány pouhé dva případy, kdy postižení močového měchýře předcházelo jiným projevům systémové vaskulitidy (8). Zároveň dodávají, že rozpoznání účasti močového měchýře při GPA je významné, neboť včasné rozpoznání a léčba umožní uchovat funkci močového měchýře a omezit potřebu chirurgického zásahu. To se podařilo i v našem případě, kdy tumorózní útvar byl pouze sledován a po imunosupresivní léčbě zcela regredoval.
Z hlediska diferenciální diagnostiky je u tumoru močového měchýře při GPA nutné uvážit i roli její léčby, konkrétně užití cyklofosfamidu. Existuje celá řada studií (9, 10) dokumentujících vznik karcinomu močového měchýře po terapii cyklofosfamidem, existují ale i doklady o tom, že riziko karcinomu močového měchýře je mírně (statisticky však nevýznamně) zvýšeno u pacientů s GPA ještě před podáním cyklofosfamidu. Přestože krátkodobé podávání cyklofosfamidu bylo nutné pro zvládnutí akutních projevů vaskulitidy, pokud by pacientka měla zároveň nádorové onemocnění, naše rozhodování o imunosupresivní léčbě by tímto jistě bylo ovlivněno. Imunosupresivní terapie by byla jednoznačně nutná, voleny by byly ale postupy co nejvíce vyhovující i uroonkologickému požadavku, rovněž by pacientka musela být zvýšeně sledována i pro riziko dalších malignit. Vzhledem k biopticky verifikované nenádorové etiologii ložiska byla pacientce podána běžná dávka imunosuprese. Je vhodné připomenout, že Hellmich a Kausch i EULAR doporučení dále vybízejí u pacientů po expozici cyklofosfamidem s perzistující hematurií provádět pravidelné urologické prohlídky za účelem včasného rozpoznání možného karcinomu měchýře.
K příznivému vývoji onemocnění u pa-cientky jistě přispělo i včasné odeslání pacientky do specializovaného centra. Pro diagnózu GPA je typická přítomnost PR3-ANCA protilátek a možnost statimového vyšetření těchto protilátek je pro včasné stanovení diagnózy, a tím i včasné zahájení terapie, zcela zásadní. Přes výrazné zlepšení prognózy pacientů s GPA se pětileté přežití stále pohybuje jen okolo 75–80 % a je spojeno s poměrně výraznou morbiditou danou jak samotným onemocněním, tak podanou léčbou.
GPA je relativně vzácné, ale život ohrožující onemocnění, na něž by mělo být pomýšleno v rámci diferenciální dg. nejasných nekrotizujících zánětlivých ložisek nacházejících se v kterémkoli orgánu a též v případech pacientů se zdánlivě nesouvisejícími stesky z různých orgánových systémů. V případě postižení urogenitálního traktu se jistě jedná o ojedinělou diagnózu, ale pokud bude na takovou diagnózu pomýšleno, může být pacient ušetřen chirurgického výkonu či dokonce onkologické terapie a po vhodné léčbě dojde k úplně remisi, jak jsme dokumentovali na našem případě.
Došlo: 4. 4. 2014.
Přijato: 29. 5. 2014.
Kontaktní adresa
Jakub Řezáč
Klinika nefrologie 1. LF UK a VFN
U Nemocnice 2, 128 08 Praha 2
e-mail: rezac.kuba@gmail.com
Střet zájmů: žádný.
Sources
1. Lynch JP, Tazelaar H. Wegener Granulomatosis (Granulomatosis With Polyangiitis). Semin Respir Crit Care Med 2011; 32(3): 274–297.
2. Habermann TM. Mayo Clinic internal medicine review, 2006–2007. 7. Ed. Mayo Clinic Scientific Press; 935.
3. Boomsma MM, Stegeman CA, van der Leij MJ, et al. Prediction of relapses in Wegener’s granulomatosis by measurement of antineutrophil cytoplasmic antibody levels: a prospective study. Arthritis Rheum 2000; 43(9): 2025–2033.
4. Lynch JP III, White E, Tazelaar H, Langford CA. Wegener’s granulomatosis: evolving concepts in treatment. Semin Respir Crit Care Med 2004; 25(5): 491–521.
5. Frausová D, Brejníková M, Šafránková H, Hrušková Z, Tesař V. Masivní gastrointestinální krvácení u pacientky s Wegenerovou granulomatózou – kazuistika. Čes. Revmatol. 2009; 17(4): 214–217.
6. Aasarød K, Bostad L, Hammerstrøm J, Jørstad S, Iversen BM. Renal histopathology and clinical course in 94 patients with Wegener’s granulomatosis. Nephrol Dial Transplant 2001; 16(5): 953–960.
7. Knight A, Askling J, Granath F, et al. Urinary bladder cancer in Wegener’s granulomatosis: risks and relation to cyclophosphamide. Ann Rheum Dis 2004; 63 : 1307–1311.
8. Hooda D, Parsons J, Hooda S, Nuss M, Layne R. Isolated bladder vasculitis: a rare presentation of Wegener’s granulomatosis. West Virginia Medical Journal 2011; 107(1): 24–25.
9. Hellmich B, Kausch I, Doehn C, Jocham D, Holl-Ulrich K, Gross WL. Urinary bladder cancer in Wegener’s granulomatosis: is it more than cyclophosphamide? Ann Rheum Dis 2004; 63 : 1183–1185.
10. Travis LB, Curtis RE, Glimelius B, et al. Bladder and Kidney Cancer Following Cyclophosphamide Therapy Non-Hodgkin’s Lymphoma. Journal of the National Cancer Institute 1995; 87(7): 524–531.
Labels
Paediatric urologist Nephrology Urology
Article was published inCzech Urology

2014 Issue 3-
All articles in this issue
- Varikokéla
- Penis šetřící metody léčby nižších T kategorií karcinomu penisu
- Aktivní sledování u karcinomu prostaty
- Zhodnocení věkově specifického PSA a PSA velocity na základě biopsií prostaty
- Komparace multiparametrické magnetické rezonance se silou magnetického pole 3 Tesla s transrektální sonografií naváděnou biopsií prostaty
- Litotrypse extrakorporální rázovou vlnou – čtyřleté zkušenosti s elektromagnetickým litotryptorem Urontech URO-EMX
- Zánětlivý pseudotumor močového měchýře jako projev aktivity u pacientky s granulomatózou s polyangiitidou (Wegenerovou granulomatózou) – méně obvyklá manifestace ANCA-asociované vaskulitidy
- Czech Urology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Varikokéla
- Zhodnocení věkově specifického PSA a PSA velocity na základě biopsií prostaty
- Aktivní sledování u karcinomu prostaty
- Penis šetřící metody léčby nižších T kategorií karcinomu penisu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

