-
Medical journals
- Career
Současné možnosti terapie juvenilní recidivující respirační papilomatózy
Authors: M. Formánek 1,2; H. Kučová 1; Karol Zeleník 1,2; Pavel Komínek 1,2
Authors‘ workplace: Otorinolaryngologická klinika FN Ostrava přednosta prof. MUDr. P. Komínek, Ph. D., MBA 1; Katedra kraniofaciálních oborů, Lékařská fakulta, Ostravská univerzita, Ostrava vedoucí prof. MUDr. P. Komínek, Ph. D., MBA 2
Published in: Čes-slov Pediat 2015; 70 (3): 174-178.
Category: Reviews
Overview
Juvenilní recidivující papilomatóza hrtanu (JRRP) představuje nejčastější dětské benigní nádorové onemocnění hrtanu a druhou nejčastější příčinu chrapotu u dětí. JRRP je způsobená lidskými papilomaviry (HPV), symptomy mají původ v obstrukci dýchacích cest a typicky se jedná o triádu příznaků – stridor, chrapot a dechová tíseň. Průběh onemocnění je variabilní a ve srovnání s dospělou formou je mnohem agresivnější a výrazněji ovlivňuje kvalitu života, má obecně větší tendenci recidivovat.
Standardní léčbou je chirurgické snesení, u pacientů s obtížně kontrolovatelným onemocněním je indikována adjuvantní léčba, do které je v současné době zahrnuto podání cidofoviru, interferonu, antirefuxní medikace, bevacizumabu a dalších látek. K dispozici je také profylaktická kvadrivalentní vakcína proti HPV 6, 11, 16 a 18.Klíčová slova:
juvenilní recidivující respirační papilomatóza, terapie, human papilloma virus, cidofovir, HPV vakcinace, bevacizumabÚVOD
Recidivující respirační papilomatóza (RRP) je benigní virové onemocnění charakterizované vznikem exofyticky rostoucích papilomů na sliznicích dýchacích cest, zvláště hrtanu (obr. 1). Je způsobeno lidskými papilomaviry (HPV). Jedná se o DNA viry, které byly v papilomech poprvé diagnostikovány Gismmanem a Mountsem v roce 1982 [1]. Do současnosti bylo popsáno více než 90 typů HPV, přičemž RRP je nejčastěji způsobena typem 11, méně typem 6, vzácně pak typy 16, 18, 31 a 33 [2]. Protože latentní viry lze nalézt u mnoha pacientů, kteří netrpí RPP, předpokládá se, že do patogeneze musí být zapojeny další faktory jako např. imunodeficience, abúzus nebo extraezofageální reflux [3, 4]. Je zvažována také genetická predispozice ke vzniku papilomatózy [5].
Obr. 1. Zvětšovací laryngoskopie – papilomatóza hrtanu postihující supraglottis a obě hlasivky. Fig. 1. Optically-enhanced laryngoscopy: laryngeal papillomatosis affecting supraglottis and true vocal chords bilaterally. 
V incidenci RRP jsou sledovány 2 vrcholy – v předškolním věku a během 3. decénia. Podle věku, ve kterém se onemocnění objeví, je rozlišována juvenilní a dospělá forma.
EPIDEMIOLOGIE
Juvenilní recidivující respirační papilomatóza (JRRP) je považována za nejčastější dětské benigní nádorové onemocnění hrtanu a druhou nejčastější příčinu chrapotu u dětí s prevalencí 4,3 na 100 000 dětí v USA [6, 7]. Je prokázáno že se jedná o sexuálně přenosné onemocnění a přenos HPV na dítě je nejčastěji uskutečněn při vaginálním porodu přenosem od matky [8]. HPV 6 a 11 jsou mimo jiné prokázanými původci genitálních bradavic ve více než 90 % případů [9]. Přibližně 3/4 pacientů s JRRP jsou zastoupeny prvorozenými dětmi velmi mladých matek (mladší 20 let), které se narodily vaginálním porodem – tyto skutečnosti jsou v současnosti považovány za rizikové faktory [8]. JRRP je sledována častěji u dětí pocházejících ze slabších socioekonomických poměrů. Nebyl sledován výraznější rozdíl v prevalenci mezi pohlavím [10].
SYMPTOMY A PRŮBĚH
Symptomy JRRP mají původ v obstrukci dýchacích cest a typicky se jedná o triádu příznaků – stridor, chrapot a dechová tíseň. Mezi další možné symptomy jsou řazeny perzistující kašel, recidivující pneumonie, neprospívání nebo dysfágie. Příznaky mohou být různě vyjádřeny a nezřídka dochází k nesprávné diagnostice, kdy jsou děti léčeny pro astma nebo chronickou bronchitidu, špatně odpovídají na terapii a JRRP se takto může vyvinout až v život ohrožující stav [11]. Nerozpoznaná a neléčená JRRP může mít u dětí za následek smrt udušením.
Průběh onemocnění je velmi variabilní a ve srovnání s dospělou formou je mnohem agresivnější a výrazněji ovlivňuje kvalitu života, má obecně větší tendenci recidivovat. Pacienti s prokázaným HPV typ 11 mají obecně horší průběh i prognózu oproti pacientům s jiným typem HPV [12]. Frekvence recidiv je vysoce individuální a pohybuje se od měsíce do několika let. JRRP může přecházet do dospělosti, nebo spontánně ustoupit. Věk, ve kterém k případné remisi dochází, je přitom zcela individuální [10]. I přesto, že se jedná o benigní onemocnění, bylo prokázáno riziko maligního zvratu papilomů, zvláště u HPV typ 11 [6, 13].
Pro potřeby stagingu choroby byl vytvořen skórovací systém dle Coltera/Derkay, který dělí aerodigestivní trakt na 25 oblastí a každá tato oblast je zvlášť ohodnocena podle přítomnosti a závažnosti papilomatózy 0–3 body (tab. 1) [14]. Systém bere v potaz i klinické symptomy. Výsledný bodový součet dává dobrou představu o tíži postižení a lepší možnost naplánování léčby.
TERAPIE
I přes objevy nových terapeutických látek v současnosti neexistuje léčebná modalita, u které by byla prokázaná schopnost kompletně eradikovat JRRP. Ačkoliv neexistuje jednoznačné schéma správné léčby, standardem terapie i dnes zůstává chirurgická léčba, která může být u obtížně kontrolovatelného onemocnění doplněná určitou formou adjuvantní terapie.
1. CHIRURGICKÁ LÉČBA
Cílem chirurgické léčby je odstranění všech papilomů při maximálním šetření okolních struktur tak, aby bylo dosaženo uvolnění lumina dýchacích cest a zlepšení kvality hlasu [15]. Je potřeba si uvědomit, že u papilomatózy se jedná o čistě slizniční patologii a tedy jakékoliv zásahy do hlubších vrstev hlasivky (podslizniční Reinkeho prostor, ligamentum vocale a další) jsou nežádoucí, prognózu nemoci nezlepší a vedou k zbytečnému jizvení hlasivek s následným zhoršením hlasu. Tento stav (jizvy hlasivek) nelze v současné době léčit a dysfonie vzniklá z tohoto důvodu je trvalá. Operace je prováděna v celkové anestezii při rigidní laryngoskopii pod endoskopickou nebo mikroskopickou kontrolou. K snesení papilomů jsou využívány studené nástroje, laser, nebo mikrodebridor (shaver).
Laser umožňuje přesnou vaporizaci slizničních lézí s minimálním krvácením. Nejčastěji je využíván CO2 laser v nejšetrnějších režimech s širším nastavením paprsku. Jako výhodu použití mikrodebridoru vidí někteří autoři nižší riziko peroperačních komplikací, šetrnější chování k okolním tkáním, kratší trvání výkonu a také nižší pořizovací cenu přístroje [16]. Holler et al. ve své studii prokázali lepší výsledky pooperačního objektivního hodnocení hlasu u pacientů operovaných mikrodebridorem v porovnání s použitím CO2 laseru [17].
U pacientů s JRRP je často nutné opakované chirurgické snášení papilomů. Podle údajů z literatury je během prvního roku diagnózy nutné u dětí provést 4,1–4,4 výkonů, průměrně podstoupí dítě s JRRP 19,7 operací, proto je maximální šetření okolní tkáně zvláště důležité [18]. V závažných případech JRRP může být také nutné provedení tracheotomie.
Ke komplikacím jakékoliv chirurgické léčby, zvláště opakované, patří jizvení sliznic hlasivek, vznik synechií, zhoršení hybnosti hlasivek a vznik stenóz. I v případě, že jsou všechny viditelné léze odstraněny, latentní virus v okolních tkáních perzistuje, proto je vhodné v případě zvýšeného rizika následného jizvení ponechat reziduální lézi [19].
2. ADJUVANTNÍ LÉČBA
Cílem adjuvantní terapie dnes stejně jako v minulosti zůstává snížit co možná nejvíce počet chirurgických výkonů. Pravě v této oblasti probíhá v současnosti nejintenzivnější výzkum. Neexistuje jasný standard, který by říkal, kdy adjuvantní terapii použít. Obecně je ale doporučováno zvážit tuto terapii v případě, že dítě potřebuje více než 4 operace ročně, pokud papilomy často způsobují poruchy dechu, nebo pokud se šíří distálně do průdušnice [19].
- Interferony
Jednu z prvních možností adjuvantní léčby papilomatózy hrtanu představovaly systémově podávané interferony (zvláště interferon α), používané u RRP od 80. let minulého století. Přesný mechanismus účinku není zcela znám. Je předpokládána inhibice virové proteosyntézy modulací hostitelské imunitní odpovědi. Při terapii JRRP je doporučena aplikace déle než 6 měsíců. Výsledky léčby jsou ale velmi obtížně předpověditelné a nemají delší efekt než 2 roky [19]. Pro vysoký výskyt nežádoucích účinků (např. leukopenie, trombocytopenie) a nepříjemné symptomy při léčbě, jako jsou horečka, nauzea, únava, bolesti kloubů a hlavy, je v současnosti užití interferonu u JRRP na ústupu.
- Cidofovir
Cidofovir je v současnosti ve světě nejpoužívanějším antivirotikem v léčbě JRRP. Jedná se o nukleosidový analog cytosinu, který má schopnost inkorporovat se do virové DNA a tak blokovat její replikaci. Působí tedy pouze proti DNA virům, u kterých spouští apoptózu. Cidofovir může být použit intralezionálně nebo podle posledních reportů také inhalačně. Výhodou intralezionálního podání je vyšší lokální koncentrace bez zvyšování potenciálně toxické koncentrace v plazmě [20]. Mezi popsané nežádoucí účinky po intralezionálním podání patří kožní vyrážka, bolesti hlavy, lokální zánětlivá reakce, jizvení hlasivek a otok. I přes potenciálně závažnější nežádoucí účinky je zvažována i intravenózní aplikace [21]. Při tomto podání je pacient vystaven riziku nefrotoxicity, iritidy, uveitidy nebo toxicity pro kostní dřeň. Na zvířecích modelech byla také popsána karcinogenita, embryotoxicita a teratogenita cidofoviru [22].
Navzdory těmto možným nežádoucím účinkům souhrnné studie popisují, že více než 80 % pacientů dobře zareagovalo na adjuvantní terapii cidofovirem ve smyslu prodloužení intervalu recidiv [23]. Na druhou stranu McMurray et al. ve své prospektivní, randomizované, dvojitě zaslepené studii neprokázali benefit podávání cidofoviru ve srovnání s kontrolní skupinou (fyziologický roztok) na průběh JRRP [24]. Panuje také veliká variabilita v použitém dávkování, počtu injekcí a intervalech mezi nimi. Použití cidofoviru v indikaci JRRP v České republice zůstává off label use, v současné době probíhá mezinárodní studie zabývající se sledováním vedlejších účinků místního užití cidofoviru u JRRP.
Table 1. Skórovací systém dle Coltera/Derkay – anatomické skóre. 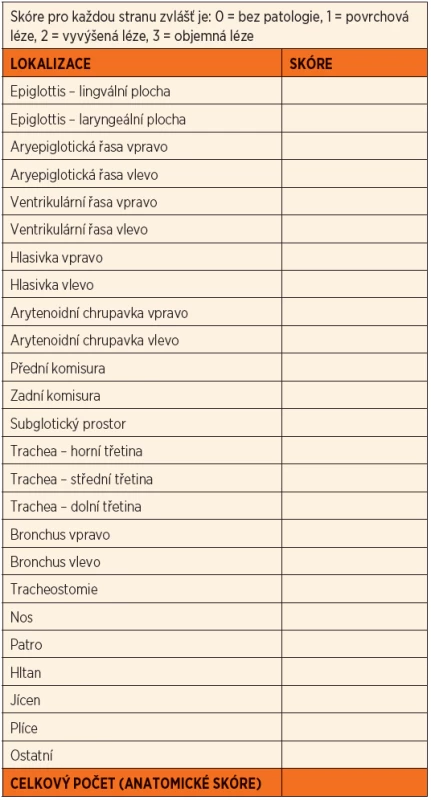
- Propranolol
Jedná se o neselektivní sympatolytický β-blokátor, který byl vyvinut jako jeden z prvních β-blokátorů. V současnosti je propranolol mimo jiné nově používán u dětí v léčbě hemangiomů s dobrým efektem a minimem nežádoucích účinků [25, 26]. Mechanismus účinku není zcela jasný, předpokládá se down-regulace tvorby vaskulárního endoteliálního růstového faktoru (VEGF) [25]. Rahbar et al. prokázali silnou expresi VEGF a receptorů pro VEGF u 12 pacientů s RRP [27]. Jinými autory byl prokázán vztah mezi HPV typ 16 a up-regulací VEGF [28]. Maturo et al. referovali o perorální léčbě propranololem 3 dětí s těžkou JRRP, kdy při 6měsíčním sledování 2 děti dobře odpověděly na terapii ve smyslu zvýšení intervalu chirurgických intervencí a zlepšení hlasu [29].
- Bevacizumab
Jedná se o lidskou monoklonální protilátku, která se váže na VEGF a tím jej neutralizuje. Byl vyvinut pro intravenózní podání při léčbě metastatického kolorektálního karcinomu. V současnosti jsou intraokulární injekce bevacizumabu používány očními lékaři k léčbě patologií sítnice (diabetická retinopatie, makulární degenerace). V případě RRP je aplikován intralezionálně ve stejné dávce, jaká by byla indikována při intraokulárním podání. O použití bevacizumabu k léčbě RRP u dospělých pacientů referovali v poslední době např. Zeitels et al. [30]. Maturo et al. použili tuto látku jako adjuvantní terapii u 3 dětí s těžší formou JRRP, kdy bylo u všech dětí zaznamenáno prodloužení času mezi operacemi a u 2 dětí navíc zlepšení objektivních hlasových parametrů a snížení rozsahu posti-žení (Coltera/Derkay skóre) [31]. Vhodnými pacienty pro aplikaci bevacizumabu by mohly být děti, které prodělaly alespoň 4 operace papilomatózy způsobující dechové obtíže a které dobře nezareagovaly alespoň na 3 intralezionální injektáže cidofoviru. Zůstává nejisté, zda je vhodná léčba 1 dávkou nebo opakovaná [31]. Mezi nežádoucí účinky intravenózního podání bevacizumabu jsou řazeny krvácení, krevní sraženiny, vysoký krevní tlak, hypotyreóza a další [32]. Při intraokulárním podání nebyly zaznamenány žádné nežádoucí účinky. V tomto případě je dávka cca 100–400x nižší než při podání intravenózním, přesto při testu na zvířatech byly po intraokulární aplikaci 1,25 mg bevacizumabu naměřeny jeho malé hodnoty také v plazmě [32, 33].
- Indol-3-karbinol
Indol-3-karbinol je potravinový doplněk, který se hojně vyskytuje v různých druzích zeleniny, jako je např. zelí, kapusta, květák nebo růžičková kapusta. Byl prokázán jeho vliv na metabolismus estrogenu ovlivněním P450 hydroxylace estronu, následkem toho vzniká více 2-hydroxyestronu na místo 16α-hydroxyestronu. Bylo zjištěno, že 16α-hydroxyestron působí genotoxicky a způsobuje hyperproliferaci epiteliálních buněk [34]. Bylo prokázáno, že 2-hydroxyestron navíc snižuje riziko vzniku hormon-dependentních tumorů [35]. Rosen et al. ve své prospektivní studii s absencí kontrolní skupiny prokázali dobrý efekt indol-3-karbinolu ve skupině 33 pacientů s RRP, kdy po léčbě 33 % pacientů setrvalo v kompletní remisi a u 30 % pacientů bylo sledováno zpomalení růstu papilomů, které rezultovalo v menší počet operací [36]. Do studie bylo zahrnuto také 9 pediatrických pacientů, ze kterých při dlouhodobém sledování 3 zůstávají v remisi onemocnění [36]. Nebyly zaznamenány nežádoucí účinky terapie.
- Další možnosti adjuvantní terapie
Popsáno bylo také použití jiných antivirotik – acykloviru a ribavirinu a dalších preparátů (retinová kyselina, zinek, fluorouracil) pro léčbu RRP. Další možnou alternativou se jeví i fotodynamická terapie, která ale může mít mnoho nežádoucích účinků [37]. Byla rovněž publikována data o použití lokální laryngeální aplikace vakcíny proti příušnicím. Mechanismus účinku je neznámý (příušnice jsou způsobeny RNA virem), Pashley nicméně ve své studii popisuje dlouhodobou remisi RRP v 76–82 % při lokálním použití této vakcíny [38]. Vzhledem k zvažované souvislosti RRP a extraezofageálního refluxu považují v současnosti někteří autoři antirefluxní léčbu za nedílnou součást terapie papilomatózy [3, 4].
3. Prevence – očkování
Jedinou prevencí vzniku RRP zůstává i dnes vakcinace. V roce 2006 byla uvedena na trh profylaktická kvadrivalentní vakcína, která je namířena proti HPV typ 6, 11, 16 a 18. Primárním účelem vzniku vakcíny bylo snížit incidenci rakoviny děložního čípku, která je způsobená vysoce rizikovými typy 16 a 18. Jedná se o rekombinantní vakcínu, připravenou z vysoce čištěných, viru podobných částic (virus-like particles) kapsidového proteinu L1. Klinické studie prokázaly, že vakcína je bezpečná a indukuje tvorbu specifických protilátek proti kapsidám obsažených virových typů. Má navíc prokazatelnou zkříženou účinnost proti dalším deseti typům HPV. Vakcínou indukované protilátky mají neutralizující aktivitu a vakcinací dosažené titry jsou mnohem vyšší v porovnání s titry dosaženými po přirozené infekci HPV virem [39]. Vakcinace je prováděna 3 dávkami s odstupem 2, resp. 4 měsíců.
Vakcína ale nemá terapeutické účinky u již existujících lézí. Protilátky proti L1 proteinu virové kapsidy neutralizují virus dříve, než způsobí infekci, neúčinkují však proti infekci již probíhající, protože buňky v dysplastickém stavu L1 protein neprodukují. V případě JRRP má tedy v prevenci vzniku onemocnění jen omezené využití, protože většina dětí s JRRP je virem nakažena již při porodu. V tomto případě by bylo řešením plošné očkování všech žen před prvním sexuálním stykem, efekt ve snížení incidence JRRP by nicméně nastal až za několik dekád. V poslední době je ale některými autory popisován příznivý efekt vakcinace také u již nakažených dětí ve smyslu zmírnění agresivity onemocnění [40]. Ve skupině pacientů, kteří byli HPV nakaženi až po narození, představuje profylaktická vakcinace možnou eventualitu.
ZÁVĚR
Současné možnosti terapie recidivující papilomatózy hrtanu jsou stále neuspokojivé. I přes objevy nových terapeutických látek neexistuje léčebná modalita, u které by byla jistě prokázaná schopnost kompletně eradikovat papilomy. Standardem terapie zůstává chirurgická léčba s cílem odstranění všech papilomů při maximálním šetření okolních struktur, tak, aby bylo dosaženo uvolnění lumina dýchacích cest a zlepšení kvality hlasu. Chirurgie může být u obtížně kontrolovatelného onemocnění doplněná určitou formou adjuvantní terapie.
Mezi nejčastěji používané a nejnadějnější adjuvantní terapeutika se řadí cidofovir a nověji bevacizumab. Zvažována je antirefluxní terapie. Objevují se také další alternativy. Jsou ale zapotřebí lépe strukturované studie k ověření efektu nových terapeutik. Možnosti prevence vzniku onemocnění jsou v případě dětí omezené.
Podpořeno institucionální podporou FN Ostrava FNOs/2014.
Došlo: 9. 12. 2014
Přijato: 13. 1. 2015
MUDr. Martin Formánek
Otorinolaryngologická klinika FN Ostrava
17. listopadu 1790
708 52 Ostrava
e-mail: martin.formanek@fno.cz
Sources
1. Gissmann L, Diehl V, Schultz-Coulon HJ, et al. Molecular cloning and characterization of human papilloma virus DNA derived from a laryngeal papilloma. J Virol 1982; 44 : 393–400.
2. Cogliano V, Baan R, Straif K, et al. Carcinogenicity of human papillomaviruses. Lancet Oncol 2005; 6 (4): 204.
3. Holland BW, Koufman JA, Postma GN, et al. Laryngopharyngeal reflux and laryngeal web formation in patients with pediatric recurrent respiratory papillomas. Laryngoscope 2002; 112 : 1926–1929.
4. McKenna M, Brodsky L. Extraesophageal acid reflux and recurrent respiratory papilloma in children. Int J Pediatr Otorhinolaryngol 2005; 69 : 597–605.
5. Buchinsky FJ, Derkay CS, Leal SM, et al. Multicenter initiative seeking critical genes in respiratory papillomatosis. Laryngoscope 2004; 114 : 349–357.
6. Derkay CS. Task force on recurrent respiratory papillomas. A preliminary report. Arch Otolaryngol Head Neck Surg 1995; 121 : 1386–1391.
7. Morgan AH, Zitch RP. Recurrent respiratory papillomatosis in children: a retrospective study of management and complications. Ear Nose Throat J 1986; 65 : 19–28.
8. Kashima HK, Shah F, Lyles A, et al. A comparison of risk factors in juvenile-onset and adult-onset recurrent respiratory papillomatosis. Laryngoscope 1992; 102 : 9–13.
9. Lacey CJ, Lowndes CM, Shah KV. Chapter 4: Burden and management of non-cancerous HPV-related conditions: HPV-6/11 disease. Vaccine 2006; 24 (3): 35–41.
10. Armstrong LR, Derkay CS, Reeves WC. Initial results from the national registry for juvenile-onset recurrent respiratory papillomatosis. RRP Task Force. Arch Otolaryngol Head Neck Surg 1999; 125 : 743–748.
11. Derkay CS. Recurrent respiratory papillomatosis. Laryngoscope 2001; 111 : 57–69.
12. Rabah R, Lancaster WD, Thomas R, et al. Human papillomavirus-11-associated recurrent respiratory papillomatosis is more aggressive than human papillomavirus-6-associated disease. Pediatr Dev Pathol 2001; 4 : 68–72.
13. Go C, Schwartz MR, Donovan DT. Molecular transformation of recurrent respiratory papillomatosis: viral typing and p53 overexpression. Ann Otol Rhinol Laryngol 2003; 112 : 298–302.
14. Derkay CS, Malis DJ, Zalzal G, et al. A staging system for assessing severity of disease and response to therapy in recurrent respiratory papillomatosis. Laryngoscope 1998; 108 (6): 935–937.
15. Kopřivová H, Zeleník K, Komínek P. Současné možnosti léčby recidivující papilomatózy hrtanu. Otorinolaryng a Foniat (Prague) 2010; 59 (4): 235–240.
16. Gallagher TQ, Derkay CS. Recurrent respiratory papillomatosis: update 2008. Curr Opin Otolaryngol Head Neck Surg 2008; 16 : 536–542.
17. Holler T, Allegro J, Chadha NK, et al. Voice outcomes following repeated surgical resection of laryngeal papillomata in children. Otolaryngol Head Neck Surg 2009; 141 : 522–526.
18. Armstrong LR, Derkay CS, Reeves WC. Initial results from the national registry for juvenile-onset recurrent respiratory papillomatosis. RRP Task Force. Arch Otolaryngol Head Neck Surg 1999; 125 (7):743–748.
19. Derkay CS, Wiatrak B. Recurrent respiratory papillomatosis: a review. Laryngoscope 2008, 118 : 1236–1247.
20. Naiman AN, Ceruse P, Coulombeau B, et al. Intralesional cidofovir and surgical excision for laryngeal papillomatosis. Laryngoscope 2003; 113 (12): 2174–2181.
21. Goon P, Sonnex C, Jani P, et al. Recurrent respiratory papillomatosis: an overview of current thinking and treatment. Eur Arch Otorhinolaryngol 2008; 265 (2): 147–151.
22. Wutzler P, Thust R. Genetic risks of antiviral nucleoside analogues – a survey. Antiviral Res 2001; 49 (2): 55–74.
23. Chadha NK, James AL. Antiviral agents for the treatment of recurrent respiratory papillomatosis: a systematic review of the English-language literature. Otolaryngol Head Neck Surg 2007; 136 (6): 863–869.
24. McMurray JS, Connor N, Ford CN. Cidofovir efficacy in recurrent respiratory papillomatosis: a randomized, double-blind, placebo-controlled study. Ann Otol Rhinol Laryngol 2008; 117 : 477–483.
25. Léauté-Labrèze C, Dumas de la Roque E, Hubiche T, et al. Propranolol for severe hemangiomas of infancy. N Engl J Med 2008; 358 : 2649–2651.
26. Buckmiller L, Dyanmenahalli U, Richter GT. Propranolol for airway hemangiomas: case report of novel treatment. Laryngoscope 2009; 119 : 2051–2054.
27. Rahbar R, Vargas SO, Folkman J, et al. Role of vascular endothelial growth factor-A in recurrent respiratory papillomatosis. Ann Otol Rhinol Laryngol 2005; 114 : 289–295.
28. López-Ocejo O, Viloria-Petit A, Bequet-Romero M, et al. Oncogenes and tumor angiogenesis: the HPV-16 E6 oncoprotein activates the vascular endothelial growth factor (VEGF) gene promoter in a p53-independent manner. Oncogene 2000; 19 : 4611–4620.
29. Maturo S, Tse SM, Kinane TB, et al. Initial experience using propranolol as an adjunctive treatment in children with aggressive recurrent respiratory papillomatosis. Ann Otol Rhinol Laryngol 2011; 120 (1): 17–20.
30. Zeitels SM, Lopez-Guerra G, Burns JA, et al. Microlaryngoscopic and office-based injection of bevacizumab (Avastin) to enhance 532-nm pulsed KTP laser treatment of glottal papillomatosis. Ann Otol Rhinol Laryngol 2009; 201 (Suppl): 1–13.
31. Maturo S, Hartnick CJ. Use of 532-nm pulsed potassium titanyl phosphate laser and adjuvant intralesional Bevacizumab for aggressive respiratory papillomatosis in children. Arch Otolaryngol Head Neck Surg 2010; 136 (6): 561–565.
32. Avery RL, Pearlman J, Pieramici DJ, et al. Intravitreal bevacizumab (Avastin) in the treatment of proliferative diabetic retinopathy. Ophthalmology 2006; 113 (10): 1695.e1–e15.
33. Bakri SJ, Snyder MR, Reid JM, et al. Pharmacokinetics of intravitreal bevacizumab (Avastin). Ophthalmology 2007; 114 (5): 855–859.
34. Michnovicz JJ, Bradlow HL. Altered estrogen metabolism and excretion in humans following consumption of indole-3-carbinol. Nutr Cancer 1991; 16 : 59–66.
35. Bradlow HL, Michnovicz JJ, Telang NT, et al. Effect of dietary indole-3-carbinol on estradiol metabolism and spontaneous mammary tumors in mice. Carcinogenesis 1991; 12 : 1571–1574.
36. Rosen CA, Bryson PC. Indole-3-carbinol for recurrent respiratory papillomatosis: long-term results. J Voice 2004; 18 (2): 248–253.
37. Shikowitz MJ, Abramson AL, Freeman K, et al. Efficacy of DHE photodynamic therapy for respiratory papillomatosis: immediate and long-term results. Laryngoscope 1998; 108 : 962–967.
38. Pashley NR. Can mumps vaccine induce remission in recurrent respiratory papilloma? Arch Otolaryngol Head Neck Surg 2002; 128 (7): 783–786.
39. Villa LL, Ault KA, Giuliano AR, et al. Imunologic response following administration of vaccine targeting human papillomavirus types 6, 11, 16 and 18. Vaccine 2006; 24 : 5571–5583.
40. Goldemund K, Máchalová M, Šlapák I, et al. Recidivující papilomatóza laryngu a změna průběhu onemocnění při vakcinaci proti humánnímu papillomaviru. Pediatr pro Praxi 2010; 11 (2): 115–117.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2015 Issue 3-
All articles in this issue
- Primárny imunodeficit v praxi pediatrického pneumológa
- Lehká mentální retardace v ambulanci dětského lékaře – poznáte ji?
- Pozdní záchyt syndromu kaudální regrese u dítěte s extrémně nízkou porodní hmotností
- Preventivní vyšetření sportovců se zaměřením na klidové EKG
- Krční uzlinový syndrom z pohledu otorinolaryngologa
- Současné možnosti terapie juvenilní recidivující respirační papilomatózy
- Jednofotonová emisní tomografie při diagnostice lingvální ektopie štítné žlázy. Užití u novorozence s kongenitální hypotyreózou
- Přínos sonografického vyšetření v diagnostice akutní apendicitidy
- Segmentální dilatace střeva – prezentace souboru novorozenců se segmentální dilatací tenkého střeva a přehled literatury
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Krční uzlinový syndrom z pohledu otorinolaryngologa
- Lehká mentální retardace v ambulanci dětského lékaře – poznáte ji?
- Segmentální dilatace střeva – prezentace souboru novorozenců se segmentální dilatací tenkého střeva a přehled literatury
- Preventivní vyšetření sportovců se zaměřením na klidové EKG
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

