-
Medical journals
- Career
Změny močových a sérových markerů poškození ledvin u dospělých pacientů po podání kontrastní látky při angiografii
: M. Fořtová 1; B. Sopko 1; D. Zemánek 2,3; M. Oravec 2; E. Klapková 1; R. Průša 1
: Ústav lékařské chemie a klinické biochemie 2. LF UK a FN Motol, Praha 1; Kardiologická klinika 2. LF UK a FN Motol, Praha 2; II. interní klinika kardiologie a angiologie 1. LF UK a VFN, Praha 3
: Klin. Biochem. Metab., 27, 2019, No. 2, p. 83-89
Cíl studie: Sledovat změny parametrů poškození ledvin po podání kontrastní látky (KL) u pacientů po angiografickém vyšetření v závislosti na vstupní odhadnuté glomerulární filtraci (estimated glomerular filtration, eGF).
Typ studie: Prospektivní studie.
Název a sídlo pracoviště: Ústav lékařské chemie a klinické biochemie 2. lékařské fakulty Univerzity Karlovy a Fakultní nemocnice Motol; Kardiologická klinika 2. lékařské fakulty Univerzity Karlovy a Fakultní nemocnice Motol; V Úvalu 84,150 06 Praha 5.
Materiál a metody: Do studie bylo zařazeno 40 pacientů, kteří podstoupili angiografický výkon. Podle vstupní hodnoty eGFCKD-EPI jsme soubor rozdělili na dva podsoubory: podsoubor s eGF ≥ 1 ml/s/1,73 m2 tvořilo 28 pacientů (19 M a 9 Ž, věk 61,5 ± 10,7 let) a podsoubor s eGF < 1 mL/s/1,73 m2 12 pacientů (5 M a 7 Ž, věk 74,6 ± 6,2 let). V časech 0, 4 a 24 h po podání KL byly odebírány vzorky séra k vyšetření kreatininu a cystatinu C a v časech 0, 4, 12 a 24 h po podání KL vzorky moči k vyšetření lipokalinu asociovaného s želatinázou neutrofilů (NGAL), N-acetyl-β-D-glukosaminidázy (NAG), α-1-mikroglobulinu, albuminu a kreatininu. Ke statistickému zpracování byly použity bootstrapované statistické metody.
Výsledky: V časech 12 a 24 h po podání KL došlo ke statisticky významnému vzestupu močových koncentrací NGAL, α-1-mikroglobulinu (p < 0,05) a NAG (p = 0,05 až v čase 24 h); v čase do 24 h po podání KL nedošlo ke statisticky významným změnám albuminurie, koncentrací sérového kreatininu a cystatinu C, ani GF z těchto markerů odvozených. Všechny sledované markery se v obou podsouborech vyvíjely mezi jednotlivými odběry obdobně.
Závěr: V naší studii u pacientů po podání KL předcházel vzestup koncentrací močových NGAL, α-1-mikroglobulinu a NAG vzestupu sérového kreatininu, cystatinu C a albuminurie.
Klíčová slova:
lipokalin asociovaný s želatinázou neutrofilů – α-1-mikroglobulin – N-acetyl-β-D-glukosaminidáza – albuminurie – kontrastní látkou indukovaná nefropatie
Úvod
Po podání kontrastní látky (KL) při angiografickém vyšetření hrozí rozvoj tzv. nefropatie způsobené podáním kontrastní látky. Je definována jako akutní poškození ledvin (acute kidney injury, AKI) po podání KL při vyloučení jiné příčiny tohoto stavu. Konkrétní definice této nefropatie je však nejednotná [1]: kontrastem indukované AKI (contrast induced AKI, CIAKI) bývá definováno jako relativní zvýšení sérového kreatininu alespoň o 50 % nebo jeho absolutní zvýšení alespoň o 26,5 µmol/L v průběhu 48 hodin po podání KL [2, 3 a podle Acute Kidney Injury Network], a kontrastem indukovaná nefropatie (contrast induced nephropathy, CIN) jako relativní zvýšení sérového kreatininu alespoň o 25 %, nebo v absolutních hodnotách alespoň o 44,2 µmol/L v průběhu 48 resp. 72 hodin po podání KL [3-5 a podle European Society of Urogenital Radiology). V riziku vzniku této nefropatie (v dalším textu bude užívána pro nefropatii způsobenou KL pouze zkratka CIN, nezávisle na výše uvedených zpřesňujících kritériích) jsou pacienti s chronickým onemocněním ledvin (chronic kidney disease, CKD). Míru rizika pak ovlivňují další faktory jako stav hydratace, věk, užívání nefrotoxických léků (např. ACE inhibitory, nesteroidní antiflogistika), diabetes mellitus s obezitou a přítomnost srdečního selhání [6].
Ačkoli se CIN obecně omezuje na přechodné snížení funkce ledvin, nejedná se o benigní komplikaci. Určitý stupeň zbytkového poškození ledvin byl zaznamenán u 30 % osob postižených CIN [7]. CIN představuje třetí nejčastější příčinu akutního selhání ledvin u hospitalizovaných pacientů (po ischemickém poškození a poškození nefrotoxickými léky) a 10 % všech příčin selhání ledvin vzniklých během hospitalizace [8]. Vzrůstající incidence je dána výrazným nárůstem prováděných diagnostických a intervenčních radiologických vyšetření s KL. U běžné populace se výskyt CIN udává do 2,5 %, u rizikových nemocných incidence stoupá na 20 až 38 % a u pacientů se vstupním kreatininem nad 440 μmol/L až na 50 % [9, 10].
Cílem naší studie bylo sledovat změny parametrů poškození ledvin, a to močových markerů: lipokalinu asociovaného s želatinázou neutrofilů (NGAL), N-acetyl-β-D-glukosaminidázy (NAG), α-1-mikroglobulinu, albuminu a sérových markerů: cystatinu C a kreatininu v závislosti na podání KL u pacientů po angiografickém vyšetření v kontextu různé vstupní odhadnuté glomerulární filtrace (estimated glomerular filtration, eGF).
Soubor pacientů a metody
Soubor tvořilo 40 pacientů (24 mužů a 16 žen) průměrného věku 66,2 ± 11,2 let (od 39 do 85 let, medián 67 let), kteří podstoupili angiografický výkon. 28 pa-cientů podstoupilo selektivní koronarografii (základní diagnóza byla u 25 pacientů chronická ischemická choroba srdeční, u 1 pacienta bolest na hrudi, u 1 pacienta angina pectoris a u 1 pacienta stenóza aortální chlopně). 12 pacientů podstoupilo digitální subtrakční angiografii pro aterosklerózu končetinových tepen. U většiny pacientů se jednalo o plánované nekomplikované výkony s propuštěním den následující po výkonu. Z tohoto důvodu jsme nemohli provést vyšetření za 48 resp. 72 hodin po podání kontrastní látky a hodnotit případný rozvoj kontrastem indukované nefropatie. Všichni pa-cienti podepsali informovaný souhlas se studií.
V časech 0, 4 a 24 hodin (T0, T4, T24) po podání KL byly odebírány vzorky séra k vyšetření kreatininu a cystatinu C a v časech 0, 4, 12 a 24 hodin (T0, T4, T12, T24) po podání KL vzorky moči k vyšetření NGAL, NAG, α-1-mikroglobulinu, albuminu a kreatininu. Tyto markery jsme hodnotili jednak v souboru všech pacientů a jednak po jeho následném rozdělení podle vstupní eGFCKD-EPI v podsouborech s eGF ≥ 1 ml/s/1,73 m2 a < 1 ml/s/1,73 m2.
Koncentrace sérového a močového kreatininu, sérového cystatinu C, močového NAG a močového α-1-mikroglobulinu byly stanoveny automatickým analyzátorem Advia 1800 (Siemens, USA). Kreatinin byl stanoven enzymovou kolorimetrickou metodou (Enzymatic Creatinine_2, Siemens, USA). Stanovení je navázáno na standardní referenční materiál NIST SRM 967 metodou LC-IDMS (liquid chromatography-isotope dilution mass spectrometry) a je založeno na enzymové reakci Fossatiho, Prencipa a Bertiho, měří se výsledná absorbance barevného produktu při 596/694 nm. Pro odhady GF ze sérových koncentrací kreatininu byla použita rovnice CKD-EPI z roku 2009. Sérový cystatin C byl stanoven imunoturbidimetricky (Dako Cytomation; metoda využívá králičí antisérum, vytvořený zákal měřen při 545 nm), k naměřenému výsledku byla automaticky vypočtena odhadovaná hodnota GF podle Grubbeho CAPA rovnice [11]. Močový NAG byl stanoven kolorimetrickou metodou (Diazyme), při které NAG hydrolyzuje v alkalickém prostředí substrát 2-methoxy-4-(2’nitrovinyl)-fenyl-2-acetamido-2-deoxy-β-D-glukopyranosid na 2-methoxy-4-(2’nitrovinyl)-fenol, koncentrace NAG je přímo úměrná změně absorbance při 505 nm. Močový α-1-mikroglobulin byl stanoven imunoturbidimetricky (Roche Diagnostics, Německo; reakce s ovčí polyklonální protilátkou, vytvořený zákal měřen při 340 nm).
Koncentrace močového NGAL byla stanovena chemiluminiscenční mikročásticovou imunoanalýzou (CMIA, automatický analyzátor Architect i4000, Abbott). Výrobcem byla definována hodnota cut-off pro AKI: 131,7 μg/L.
Albuminurie byla vyšetřována jednak imunoturbidimetrickou (IT) metodou využívající polyklonální ovčí protilátky proti lidskému albuminu (metoda Tina-quant Albumin 2. generace, Roche Diagnostics, Německo; vytvořený zákal měřen při 340 nm) automatickým analyzátorem Cobas Integra 400 (Roche Diagnostics, Německo) a jednak vysokoúčinnou kapalinovou chromatografií (HPLC, home-made metoda [12], HPLC sestava Agilent 1200, Agilent Technologies, Santa Clara, USA). Výsledky byly klasifikovány do kategorií A1, A2, A3 [13, 14].
Při statistickém zpracování jsme nejdříve testovali rozložení dat a zjistili jejich nenormální distribuci. Abychom předešli zkreslení díky tomuto typu rozložení dat, použili jsme bootstrapované statistické analýzy s 1000 opakováním [15] a R statistický program [16, 17]. Ke zjištění statistických rozdílů ve vývoji hodnot jednotlivých parametrů v čase, odlišnosti hodnot jednotlivých parametrů mezi podsoubory s eGFCKD-EPI ≥ 1 a < 1 ml/s/1,73 m2 a odlišnosti vývoje jednotlivých parametrů v čase mezi těmito podsoubory jsme použili bootstrapovanou dvoucestnou ANOVA analýzu, ke zjištění rozdílů mezi dvěma časy odběrů u jednotlivých parametrů jsme následně použili bootstrapovaný Tukeyho HSD Post-hoc test. Korelační závislosti mezi jednotlivými parametry byly hodnoceny stanovením Spearmanových korelačních koeficientů. Hodnoty p < 0,05 byly považovány za statisticky významné.
Výsledky
Rozdělení souboru pacientů
Podle vstupní hodnoty eGFCKD-EPI jsme soubor všech pacientů (N = 40) rozdělili na dva podsoubory: Podsoubor s eGF ≥ 1 ml/s/1,73 m2 („podsoubor s eGF ≥ 1“) tvořilo 28 pacientů, 19 mužů a 9 žen, průměrného věku 61,5 ± 10,7 let a podsoubor s eGF < 1 ml/s/1,73 m2 („podsoubor s eGF < 1“, nejnižší vstupní eGF podle CKD-EPI: 0,66 ml/s/1,73 m2) 12 pacientů, 5 mužů a 7 žen, průměrného věku 74,6 ± 6,2 let.
Biochemické nálezy
Výsledky vyšetření jednotlivých sérových a močových markerů v podsouborech pacientů s eGF < a ≥ 1 jsou uvedeny v Tabulce 1 až 4, výsledky bootstrapované ANOVA analýzy v Tabulce 5.
1. Serum biomarkers and eGF in the eGFCKD-EPI < 1 mL/s/1.73 m2 subgroup (N = 12) 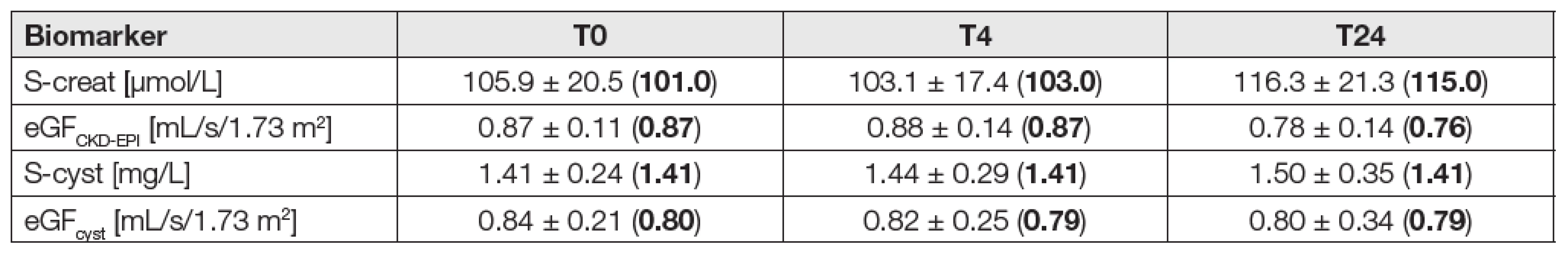
The results are expressed as means ± SD and medians (bold in brackets); T0, T4, T24: 0, 4, 24 hours after administration of the contrast medium; creat: creatinine, cyst: cystatin C. 2. Urinary biomarkers in the eGFCKD-EPI < 1 mL/s/1.73 m2 subgroup (N = 12) 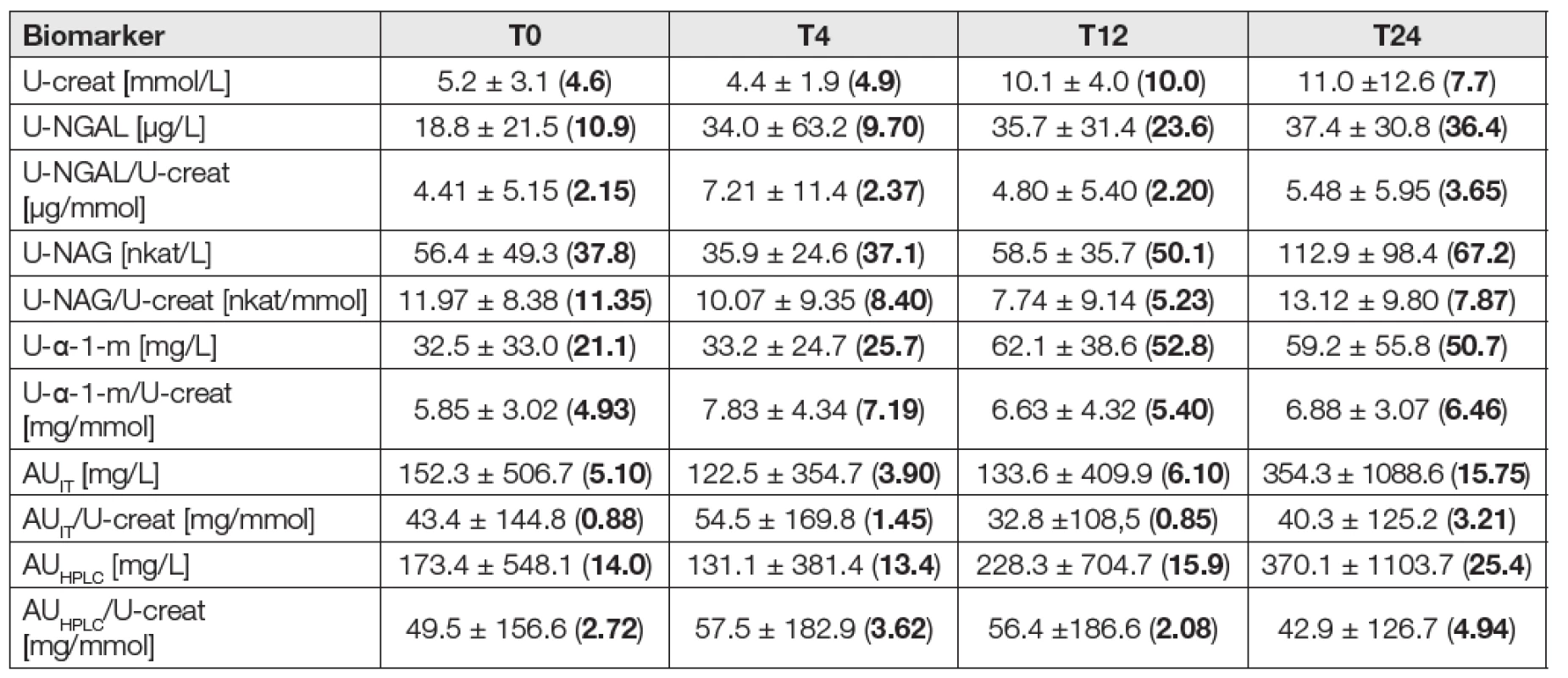
The results are expressed as means ± SD and medians (bold in brackets); T0, T4, T12, T24: 0, 4, 12, 24 hours after administration of the contrast medium; creat: creatinine, NGAL: neutrophil gelatinase-associated lipocalin, NAG: N-acetyl-β-D glucosaminidase, α-1-m: α-1-microglobulin, AU: albuminuria, IT: immunoturbidimetry, HPLC: high performance liquid chromatography. 3. Serum biomarkers and eGF in the eGFCKD-EPI ≥ 1 mL/s/1.73 m2 subgroup (N = 28) 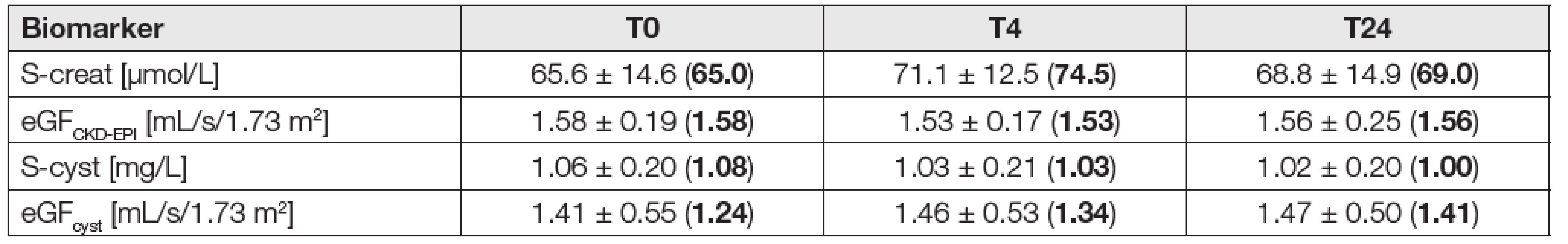
The explanation is the same as in Table 1. 4. Urinary biomarkers in the eGFCKD-EPI ≥ 1 mL/s/1.73 m2 subgroup (N = 28) 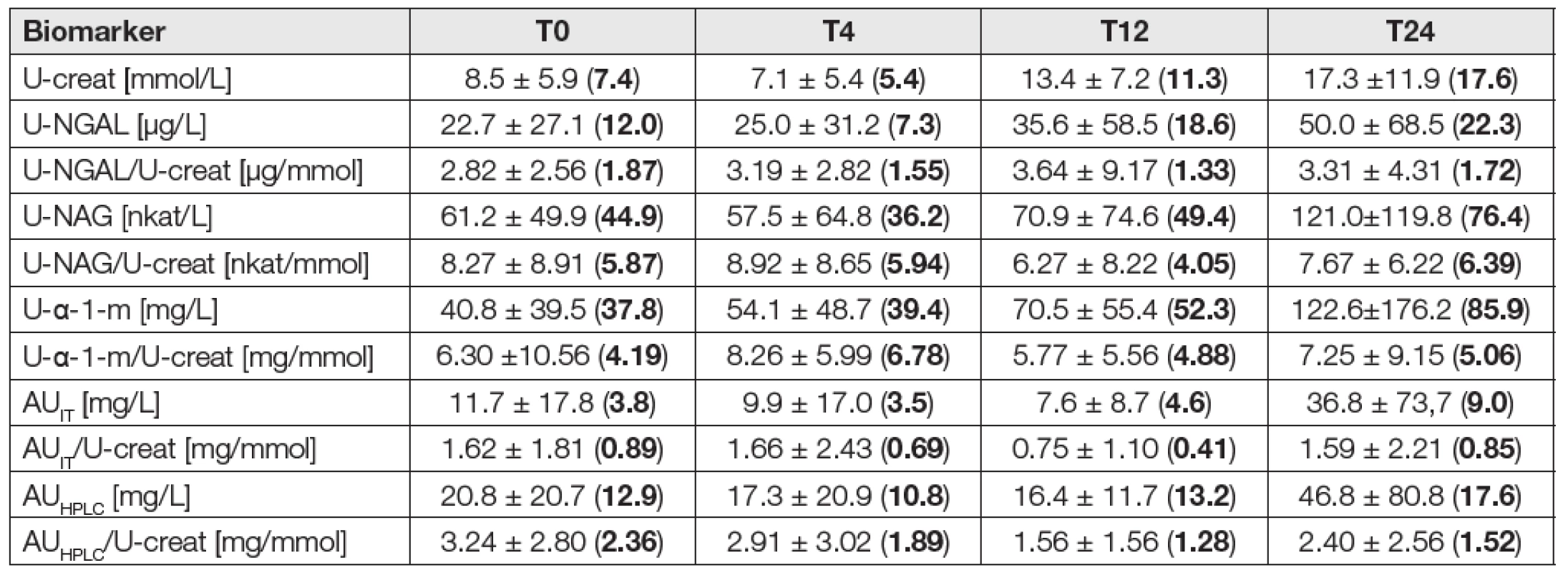
The explanation is the same as in Table 2. 5. Bootstrapped two-way ANOVA 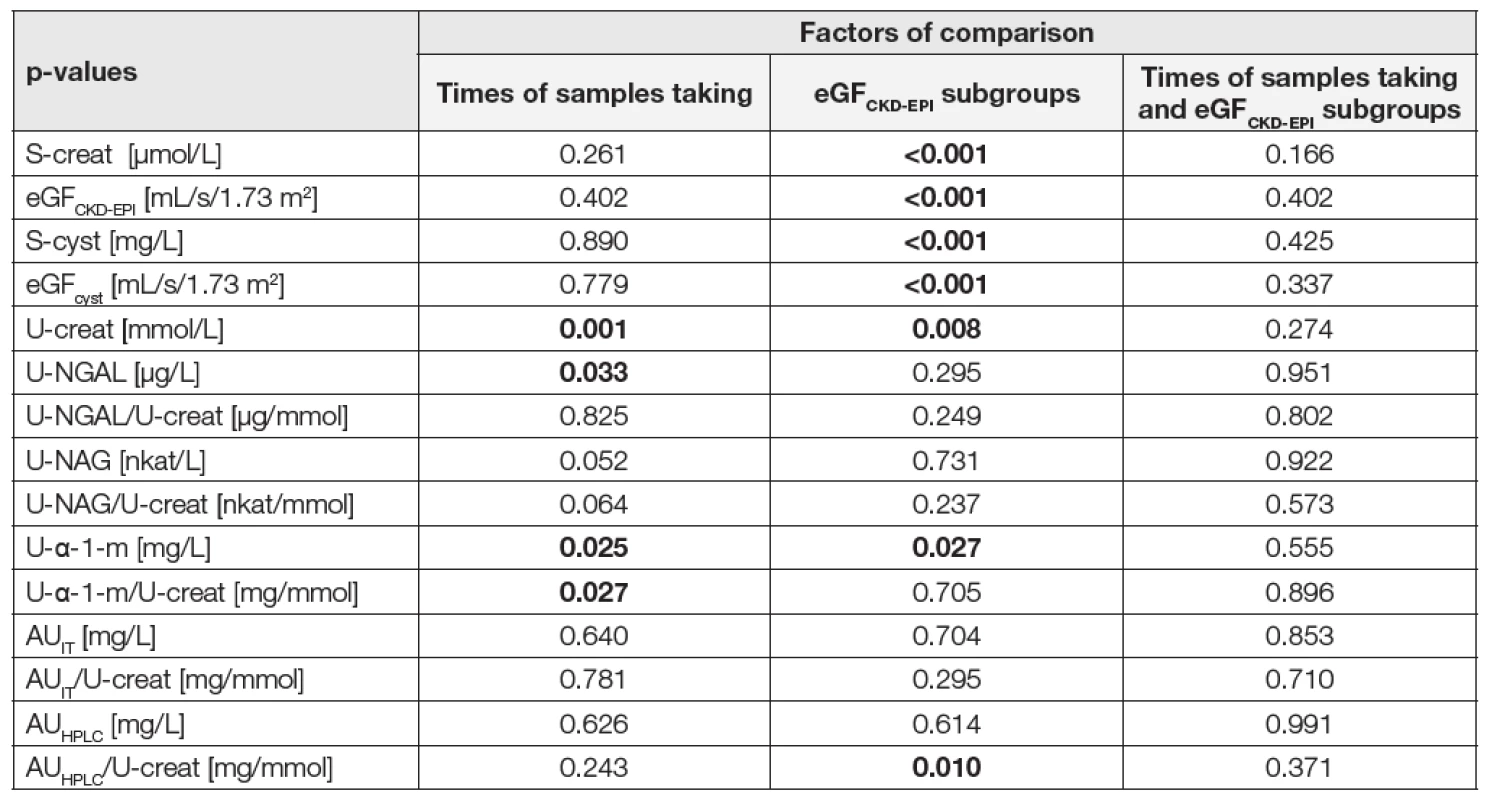
Factor “times of samples taking“: the significance of the change of the individual biomarkers over time in the all group of patients (N = 40). Factor “eGFCKD-EPI subgroups“: the significance of the differences of the individual biomarkers (regardless of the time factor) between the eGFCKD-EPI subgroups, it means between the subgroup with eGF ≥ 1 mL/s/1.73 m2 (N = 28) and with eGF < 1 mL/s/1.73 m2 (N = 12). Factor “times of samples taking and eGFCKD-EPI subgroups“: the significance of the different behavior of individual markers over time between the eGFCKD-EPI subgroups. The statistically significant p-values are shown in bold. Explanation of abbreviations of biomarkers is given in Table 1 and 2. V průběhu našeho sledování nedošlo ke statisticky významným změnám koncentrací sérového kreatininu a cystatinu C, ani GF z těchto markerů odvozených.
Došlo však ke změnám některých močových markerů. Statisticky významný vzestup močových NGAL a α-1-mikroglobulinu ve srovnání s výchozími hodnotami byl zjištěn v čase 12 hodin po podání KL (T12; p < 0,05), v čase 24 hodin (T24) bylo zvýšení ještě významnější (p < 0,01). Mezi korigovanými močovými koncentracemi NGAL nebyl zjištěn statisticky významný rozdíl v čase, v případě korigovaného močového α-1-mikroglobulinu statisticky významné změny v čase zjištěny byly (T0 vs. T4; p < 0,05). Močový α-1-mikroglobulin se významně lišil i mezi podsoubory podle eGF (p < 0,05; koncentrace byly s podivem vyšší v podsouboru s eGF ≥ 1), překvapující pro nás bylo také zjištění, že většina hodnot (94 %) byla nad referenčním rozmezím. V případě močového NAG byl zjištěn pouze statisticky hraniční vzestup jeho koncentrace v čase mezi odběry T0 a T24 (p = 0,05). Mezi močovými koncentracemi α-1-mikroglobulinu a NAG byla zjištěna významná korelace (r = 0,80; p < 0,05).
Albuminurie stanovená IT i HPLC, stejně tak jako jejich poměry na kreatinin, se v závislosti na podání KL s časem statisticky významně neměnily. Mezi těmito markery albuminurie IT vs. HPLC byly zjištěny významné korelační vztahy, a to v případě vstupních, postproceduálních i všech dat (r = 0,999; p < 0,001).
Močový kreatinin se významně měnil v čase, k významnému vzestupu oproti vstupní hodnotě T0 a hodnotě v čase T4 došlo v časech T12 a T24 (p < 0,01). Byl zjištěn významný rozdíl (p = 0,008) mezi CKD-EPI podsoubory: pacienti s eGF ≥ 1 vykazovali vyšší hodnoty ve všech odběrech. V časech T0 a T4 jsme nalezli vysoké procento (51 %) zastoupení koncentrací močového kreatininu pod dolní hranicí referenčního rozmezí, v časech T12 a T24 jsme nalezli naopak značné zastoupení (35 %) nad horní hranicí referenčního rozmezí.
Všechny sledované markery se chovaly v obou podsouborech obdobně mezi jednotlivými odběry (nebyly zjištěny statisticky významné diference v čase mezi podsoubory, viz poslední sloupec v Tabulce 5).
Diskuse
V naší studii jsme měli k dispozici vzorky pouze do 24 hodin po podání KL, proto jsme nemohli hodnotit rozvoj CIN, ale pouze vývojové trendy jednotlivých markerů po zátěži ledvin KL. I přesto je z našich výsledků patrné, že v časech 12 a 24 hodin po podání KL došlo k statisticky významnému vzestupu močových koncentrací NGAL, α-1-mikroglobulinu a NAG; a že v čase do 24 hodin po podání KL nedošlo k statisticky významným změnám albuminurie (stanovené jak IT, tak HPLC), sérového kreatininu a cystatinu C, ani GF z těchto markerů odvozených. I pokud by tedy u ně-kterých našich pacientů k rozvoji CIN došlo, vzestup močových NGAL, α-1-mikroglobulinu a NAG by velmi pravděpodobně předcházel vzestupu sérového kreatininu, cystatinu C a albuminurie.
Významný vzestup močového NGAL po podání KL bývá popisován u pacientů s normální funkcí ledvin i u pacientů s CKD. Některé studie uvádějí významný korelační vztah vstupního NGAL s věkem, sérovým kreatininem, glomerulární filtrací, stadiem CKD a někdy též se sérovým cystatinem C nebo s albuminurií [18-21]. Naše studie však při korelaci vstupních, postprocedurálních, ani všech dat těchto markerů žádné ze zmíněných korelací nezjistila, určité odlišnosti v podsouborech podle eGF však vysledovat lze. V případě podsouboru s eGF < 1 došlo k více než dvojnásobnému vzestupu mediánu NGAL v čase 12 hodin a k více než trojnásobnému v čase 24 hodin po podání KL, v čase 24 hodin došlo i k téměř dvojnásobnému vzestupu poměru močový NGAL/močový kreatinin. V podsouboru s eGF ≥ 1 bylo zvýšení mediánů méně výrazné (nedošlo ani ke dvojnásobnému vzestupu NGAL, korigovaný NGAL byl v průběhu celého sledování prakticky stejný). Subklinická CIN bývá v některých studiích definována více než dvojnásobným vzestupem koncentrací NGAL (bez vzestupu sérového kreatininu [21]). K němu došlo u 54 % pacientů s eGF < 1 a pouze u 35 % pacientů s eGF ≥ 1. Tento podrobnější rozbor naznačuje na vyšší náchylnost pacientů s CKD k rozvoji kontrastem indukované nefropatie. Jsme si však vědomi skutečnosti, že se statistická analýza rozdílnosti vývoje tohoto markeru v čase mezi podsoubory nepotvrdila a že jsme v obou podsouborech pozorovali ve většině případů poměrně nízké hladiny NGAL.
Změny koncentrací kreatininu byly sice statisticky nevýznamné, ale stojí za povšimnutí, že u pacientů z podsouboru s eGF ≥ 1 byl zjištěn v čase 4 hodiny po podání KL vzestup mediánu o 15 % a v čase 24 hodin došlo k jeho návratu téměř k hodnotě před výkonem, v případě pacientů z podsouboru s eGF < 1 ke vzestupu mediánu (o 14 %) došlo až v čase 24 hodin po podání KL.
Na výsledcích se mohla odrazit i skutečnost, že pacienti z podsouboru s eGF < 1 byly v průměru o 13 let starší (korelace žádného z vyšetřovaných markerů s věkem však nalezena nebyla).
Úloha NGAL při včasné diagnostice CIN byla zkoumána u dětských i dospělých pacientů v celé řadě studií, jež většinou poukazují na jeho velmi dobrý prediktivní potenciál. Jeho vzestup po podání KL byl zaznamenán v různých časech, např. studie u dětí popisuje zvýšení již za 2 hodiny [22], studie u dospělých za 4, 12 nebo dokonce až za 24 hodin [8, 23, 24]. V roce 2017 byly publikovány dvě studie, které význam vyšetření NGAL v predikci CIN zpochybňují [25, 26]. Tito autoři však močový NGAL vyšetřovali v časech 4 až 6 hodin po výkonu, v tomto časovém úseku nedošlo k jeho vzestupu ani v naší, ani v řadě dalších studií [8, 24]. Rozhodovací meze pro významné zvýšení NGAL po podání KL byly navíc poměrně přísné: buď vzestup koncentrace nad 150 µg/L v případě vstupních hodnot < 75 µg/L nebo zdvojnásobení koncentrací v případě vstupních hodnot ≥ 75 µg/L [25]. Podle těchto kritérií by v případě naší studie došlo k významnému zvýšení NGAL pouze u jednoho pacienta (s eGF < 1) v čase 4 hodiny, u jednoho pacienta (s eGF ≥ 1) v čase 12 hodin a u dvou pacientů (s eGF ≥ 1) v čase 24 hodin po podání KL.
Ve studii [26] došlo k rozvoji CIN u 16 % pacientů a v čase 4 hodiny po podání KL byl u nich zaznamenán významný vzestup cystatinu C. Na význam cystatinu C v čase 24 hodin po výkonu v predikci CIN upozorňuje i další studie [27]. V naší studii jsme však významné změny v čase nezaznamenali.
V případě α-1-mikroglobulinu a NAG některé studie nenacházejí koncentrační změny po podání KL [27], jiné ano [28, 29], podobně jako naše studie. U α-1-mikroglobulinu pro nás bylo překvapující, že 94 % všech výsledků překročilo referenční meze a dále to, že jeho hodnoty byly významně vyšší v podsouboru s eGF ≥ 1. Předmětem našeho dalšího zájmu bude tento marker sledovat u co největšího souboru pacientů různých věkových kategorií, jak bez poškození ledvin, tak s různým stupněm renální insuficience.
Albuminurie je sledovaná po podání KL výjimečně, v dostupné literatuře jsme našli pouze dvě studie [27, 28] a jejich výsledky korespondují s našimi (nebyly zjištěny významné změny). Mezi albuminurií stanovenou IT a HPLC jsme zjistili statisticky významný korelační vztah (a to jak v případě vstupních, posproceduálních, tak i všech dat), z čehož vyplývá, že po podání KL v ledvině pravděpodobně nevzniká další imunochemicky nereaktivní albumin.
Vyšetření močového kreatininu pro nás bylo důležité ze dvou důvodů: jednak jsme na jeho koncentraci vztahovali zmiňované močové markery, jednak nám sloužil jako marker hydratace pacientů a funkce ledvin. Pacienti z podsouboru s eGF < 1 vykazovali významně nižší hodnoty močového kreatininu ve všech odběrech, ve vstupním vyšetření a v čase 4 hodiny po podání KL jsme u nich nalezli 58 % zastoupení koncentrací kreatininu pod dolní hranicí referenčního rozmezí (v podsouboru s eGF ≥ 1 to bylo 48 %), ostatní hodnoty v těchto časech byly v rámci referenčního rozmezí. Tyto výsledky ukazují na dobrý stav hydratace (resp. až zvýšenou hydrataci) před výkonem v rámci přípravy před podáním KL, což je v souladu s doporučením [6]. V časech 12 a 24 hodin po podání KL jsme nalezli naopak značné zastoupení močového kreatininu nad referenčním rozmezím, a to především v podsouboru s eGF ≥ 1 (45 % případů vs. „pouze“ 15 % případů v podsouboru s eGF < 1). Výsledky nasvědčují tomu, že větší důraz na dostatečný stav hydratace byl kladen v rizikovém souboru pacientů s renální insuficiencí. Močový kreatinin v naší studii v některých případech zkorigoval močové markery tak, že jejich statisticky významný vzestup se stal po korekci nevýznamným. V souladu se závěry studie [30] doporučujeme i při hodnocení vzniku kontrastem indukované nefropatie vyšetřovat jak markery nekorigované, tak korigované na močový kreatinin.
Závěr
U dospělých pacientů po angiografii došlo v časech 12 a 24 hodin po podání KL ke statisticky významnému vzestupu močových koncentrací NGAL, α-1-mikro-globulinu a NAG; v čase do 24 hodin po podání KL nedošlo ke statisticky významným změnám albuminurie, koncentrací sérového kreatininu a cystatinu C, ani GF z těchto markerů odvozených. Při hodnocení vzniku kontrastem indukované nefropatie doporučujeme vyšetřovat močové markery jak nekorigované, tak korigované na močový kreatinin.
Střet zajmů: Autoři prohlašují, že nejsou ve střetu zajmů.
Do redakce došlo: 14. 3. 2019
Adresa pro korespondenci:
MUDr. Ing. Magdaléna Fořtová, Ph.D.
Ústav lékařské chemie a klinické biochemie 2. LF UK a FN Motol
V Úvalu 84, 150 06 Praha 5
Sources
1. Moura, E. L. B., Amorim, F. F., Huang, W., Maia, M. O. Contrast-induced acute kidney injury: the importance of diagnostic criteria for establishing prevalence and prognosis in the intensive care unit. Rev. Bras. Ter. Intensiva, 2017, 29 (3), p. 303–309.
2. Mehta, R. L., Kellum, J. A., Shah, S. V. et al. Acute Kidney Injury Network: report of an initiative to improve outcomes in acute kidney injury. Crit. Care, 2007, 11 (2), R31.
3. American College of Radiology. ACR Manual on Contrast Media. Version 9. 2013. Contrast-induced nephrotoxicity; p. 33–42. Available at:http://aegysgroup.com/wp-content/uploads/2014/03/170675431-2013-Contrast-Media-ACR-v-9.
4. Mehran, R., Nikolsky, E. Contrast-induced nephropathy: definition, epidemiology, and patients at risk. Kidney Int. Suppl., 2006, 100 (69), S11–S15.
5. Mohammed, N. M. A., Mahfouz, A., Achkar, K., Rafie, I. M., Hajar, R. Contrast-induced nephropathy. Heart Views, 2013, 14 (3), p. 106–116.
6. Vachek, J., Zakiyanov, O., Bandúr, Š., Tesař, V. Akutní poškození ledvin. Kardiol. Rev. Int. Med., 2014, 16 (1), p. 57–61.
7. Madyoon, H., Croushore, L., Weaver, D., Mathur, V. Use of fenoldopam to prevent radiocontrast nephropathy in high-risk patients. Catheter. Cardiovasc. Interv., 2001, 53 (3), p. 341–345.
8. Ling, W., Zhaohui, N., Ben, H. et al. Urinary IL-18 and NGAL as early predictive biomarkers in contrast-induced nephropathy after coronary angiography. Nephron Clin. Pract., 2008, 108 (3), p. 176–181.
9. Lautin, E. M., Freeman, N. J., Schoenfeld, A. H. et al. Radiocontrast-associated renal dysfunction: Incidence and risk factors. Am. J. Roentgenol., 1991, 157 (1), p. 49–58.
10. Svojanovský, J., Ševela, K., Souček, M. Kontrastní látkou indukovaná nefropatie. Interní Med., 2011, 13 (5), p. 205–208.
11. Grubb, A., Horio, M., Hansson, L. O. et al. Generation of a new cystatin C-based estimating equation for glomerular filtration rate by use of 7 assays standardized to the international calibrator. Clin. Chem., 2014, 60 (7), p. 974–986.
12. Fořtová, M., Klapková, E., Průša, R. Stanovení albuminurie – porovnání imunoturbidimetrické metody a vysokoúčinné kapalinové chromatografie. Klin. Biochem. Metab., 2012, 20 (41), p. 216–221.
13. Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2012 Clinical practice guideline for the evaluation and management of chronic kidney disease. Kidney Int., 2013, Suppl. 3, p. 1–150.
14. Zima, T., Racek, J., Tesař, V. et al. Doporučení
k diagnostice chronického onemocnění ledvin (odhad glomerulární filtrace a vyšetřování proteinurie) České
nefrologické společnosti ČLS JEP a České společnosti klinické biochemie ČLS JEP. Klin. Biochem. Metab., 2014, 22 (43), p. 138–152.15. White, I. R., Thompson, S. G. Choice of test for comparing two groups, with particular application to skewed outcomes. Stat. Med., 2003, 22 (8), p. 1205–1215.
16. R Core Team. R: A language and environment for statistical computing, 2014, R Foundation for Statistical Computing, Vienna, Austria. URL http://www.R-project.org/.
17. Canty, A., Ripley, B. D. Boot: Bootstrap R (S-Plus) Functions, R package version 1.3-18, 2016.
18. Bachorzewska-Gajewska, H., Malyszko, J., Sitniewska E., Malyszko, J. S., Dobrzycki, S. Neutrophil-gelatinase-associated lipocalin and renal function after percutaneous coronary interventions. Am. J. Nephrol., 2006, 26 (3), p. 287–292.
19. Weber, C. L., Bennett, M., Er, L., Bennett, M. T., Levin, A. Urinary NGAL levels before and after coronary angiography: a complex story. Nephrol. Dial. Transplant., 2011, 26 (10), p. 3207–3211.
20. McCullough, P. A., Williams, F. J., Stivers, D. N. et al. Neutrophil gelatinase-associated lipocalin: a novel marker of contrast nephropathy risk. Am. J. Nephrol., 2012, 35 (6), p. 509–514.
21. Akrawinthawong, K., Ricci, J., Cannon, L. et al. Subclinical and clinical contrast-induced acute kidney injury: data from a novel blood marker for determining the risk of developing contrast-induced nephropathy (ENCINO), a prospective study. Ren. Fail., 2015, 37 (2), p. 187–191.
22. Hirsch, R., Dent, C., Pfriem, H. et al. NGAL is an early predictive biomarker of contrast-induced nephropathy in children. Pediatr. Nephrol., 2007, 22 (12), p. 2089–2095.
23. Bachorzewska-Gajewska, H., Malyszko, J., Sitniewska, E. et al. Could neutrophil gelatinase-associated lipocalin (NGAL) and cystatin C predict the development of contrast-induced nephropathy after percutaneous coronary interventions in patients with stable angina and normal serum creatinine values? Kidney Blood Press. Res., 2007, 30 (6), p. 408–415.
24. Torregrosa, I., Montoliu, C., Urios, A. et al. Urinary KIM-1, NGAL and L-FABP for the diagnosis of AKI in patients with acute coronary syndrome or heart failure undergoing coronary angiography. Heart Vessels, 2015, 30 (6), p. 703–711.
25. Ribitsch, W., Schilcher, G., Quehenberger, F. et al. Neutrophil gelatinase-associated lipocalin (NGAL) fails as an early predictor of contrast induced nephropathy in chronic kidney disease (ANTI-CI-AKI study). Sci. Rep., 2017, 7, p. 41300.
26. Cecchi, E., Avveduto, G., D’Alfonso, M. G. et al. Cystatin C, but not urinary or serum NGAL, may be associated with contrast induced nephropathy after percutaneous coronary invasive procedures: A single center experience on a limited number of patients. Acta Med. Acad., 2017, 46 (1), p. 34–43.
27. Kato, K., Sato, N., Yamamoto, T., Iwasaki, Y. K., Tanaka, K., Mizuno, K. Valuable markers for contrast-induced nephropathy in patients undergoing cardiac catheterization. Circ. J., 2008, 72 (9), p. 1499–1505.
28. Carraro, M., Mancini, W., Artero, M. et al. Dose effect of nitrendipine on urinary enzymes and microproteins following non-ionic radiocontrast administration. Nephrol. Dial. Transplant., 1996, 11 (3), p. 444–448.
29. Niboshi, A., Nishida, M., Itoi, T., Shiraishi, I., Hamaoka, K. Renal function and cardiac angiography. Indian J. Pediatr., 2006, 73 (1), p. 49–53.
30. Helmersson-Karlqvist, J., Arnlöv, J., Larsson, A. Day-to-day variation of urinary NGAL and rational for creatinine correction. Clin. Biochem., 2013, 46 (1–2), p. 70–72.
Labels
Clinical biochemistry Nuclear medicine Nutritive therapist
Article was published inClinical Biochemistry and Metabolism

2019 Issue 2-
All articles in this issue
- Vysoce citlivé (hs) kardiální troponiny. Pomníček velkému úsilí, které tak hned neustane.
- Comparison of troponin I (Abbott, Beckman Coulter, Siemens) and troponin T (Roche) high-sensitivity measurement results
- Role of rs17817449 FTO gene polymorphism in patients with type 1. diabetes in terms of obesity and diabetes control
- Fatty acid elongases and their involvement in the pathogenesis of disease states
- POCT system for the fecal calprotectin detection in the tele-monitoring of patients with inflammatory bowel disease
- Changes in urinary and serum markers of renal injury in adult patients after angiographic contrast medium administration
- Rare pyrophosphate renal stone in 5 years old boy with congenital hypophosphatasia
- Pleural exudate positive for paraprotein and free light chains as a very first sign of multiple myeloma
- Clinical Biochemistry and Metabolism
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Comparison of troponin I (Abbott, Beckman Coulter, Siemens) and troponin T (Roche) high-sensitivity measurement results
- POCT system for the fecal calprotectin detection in the tele-monitoring of patients with inflammatory bowel disease
- Changes in urinary and serum markers of renal injury in adult patients after angiographic contrast medium administration
- Fatty acid elongases and their involvement in the pathogenesis of disease states
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

