-
Medical journals
- Career
Srdeční vrozené vady v dospělosti
: J. Rubáčková-Popelová
: Centrum pro dospělé s vrozenou srdeční vadou, Kardiochirurgické oddělení, Nemocnice Na Homolce, Praha
: Kardiol Rev Int Med 2015, 17(4): 315-321
: Cardiology Review
Dospělých pacientů s vrozenou srdeční vadou (VSV) rychle přibývá, jejich počet se odhaduje na 2 800–3 000 na milion obyvatel. Asi polovina z nich má složitější komplexní VSV, která vyžaduje nejen specializované sledování, ale i zvýšení základních znalostí o těchto vadách u spádových kardiologů, internistů i praktických lékařů. Řada dospělých s VSV řešenou v dětství vyžaduje další operaci nebo intervenci v dospělosti, a to často i v asymptomatickém období. Je-li pacient odeslán do specializovaného centra až s významnými symptomy, jsou jeho prognostické vyhlídky i dlouhodobé operační výsledky významně horší, než je-li odeslán včas. V Centru pro dospělé s VSV v Nemocnici Na Homolce v Praze bylo v posledních deseti letech operováno více než 840 dospělých s VSV s 30denní mortalitou 1,36 %. Komplexní a vzácné VSV tvořily 47 % operací. Reoperace po operaci v dětství tvořily 44 % výkonů. Na dobrých výsledcích se podílí dlouhodobé zkušenosti a týmová spolupráce kardiochirurgů dětského i dospělého věku, kardiologů a kardioanesteziologů se znalostí problematiky VSV u dospělých.
Klíčová slova:
vrozené srdeční vady v dospělosti – operace – reziduální nálezy
Vrozené srdeční vady (VSV) již dávno nejsou výlučnou náplní dětské kardiologie a kardiochirurgie, ale stávají se integrální součástí kardiologie dospělých. Možná si ani neuvědomujeme, že počet žijících dospělých s VSV je v současnosti 2–3× vyšší než počet dětí s VSV a toto číslo bude dále narůstat. Při současném přežívání cca 90 % všech dětí narozených se srdeční vadou přibývá v ČR asi 500–600 dospělých s VSV ročně. Jejich počet byl v ČR odhadován na 20–30 000 [1]. Tento odhad dobře koresponduje se závěry 32. konference v Bethesdě s odhadovaným počtem 2 800 žijících dospělých s VSV na jeden milion obyvatel [2]. K podobnému číslu dospěli i nizozemští autoři na podkladě systematické analýzy literatury s odhadovanou prevalencí 3 000 dospělých s VSV na jeden milion obyvatel s vyloučením bikuspidální chlopně aorty, prolapsu mitrálního chlopně, vrozených arytmií a spontánně uzavřených defektů [3]. Více než polovina VSV u dospělých je středně a více komplexních a vyžaduje systematické sledování a kvalifikovanou péči [2].
Kompletní přehled o VSV v dětství podávají monografie prof. Václava Chaloupeckého Dětská kardiologie, Echokardiografie prof. Jana Marka a Dětská kardiochirurgie prof. Bohumila Hučína [4–6]. Specifika dospělých s VSV jsou probrána v monografiích autorky tohoto článku a v kapitole věnované VSV v učebnici Klinické kardiologie [7–9]. Samozřejmě existuje i velké množství zahraničních monografií věnovaných stále aktuálnější problematice VSV v dospělosti [10–12]. Pro běžnou potřebu jsou vhodná poslední doporučení Evropské kardiologické společnosti (ESC) [13].
Z praktického hlediska lze rozdělit VSV v dospělosti na časté, se kterými se opakovaně setká každý kardiolog, a méně časté, k jejichž správnému posouzení jsou potřebné určité zkušenosti. Je také potřeba si uvědomit velký rozdíl v chirurgických postupech, ochraně myokardu a výskytu reziduálních nálezů mezi dospělými operovanými v 50.–70. letech 20. století a mezi mladšími dospělými operovanými před 20–30 lety. Velkou roli hraje i věk v době operace a typ provedené operace.
Časté VSV v dospělosti
Defekt septa síní typu II (atrial septal defect – ASD)
Je to nejčastější VSV dospělého věku, v dětství bývá často nepoznán. Není vzácností, že je objeven až po 50.–60. roce věku. Nemusí dlouho působit žádné obtíže, poslechový nález tichého systolického šelestu nad plicnicí a fixní rozštěp druhé ozvy je nenápadný. Podezření budí dilatace pravé komory a plicnice, v pokročilém stadiu supraventrikulární arytmie a námahová dušnost. Definitivní diagnóza je stanovena echokardiograficky, lépe jícnovou echokardiografií ke zhodnocení podrobností, vyloučení vícečetných defektů a jiných anomálií. Léčba spočívá v uzávěru defektu, který je indikován u hemodynamicky významného defektu i bez symptomů [13]. Věk není kontraindikací léčby, u starších pacientů je často nutné řešit přidružené vady (trikuspidální a mitrální regurgitaci). Současná plicní hypertenze vyžaduje podrobné vyšetření včetně katetrizace a vazodilatačního testování na pracovišti zabývajícím se VSV. Při plicní cévní rezistenci do 5 Wj není kontraindikace uzávěru. Těžší plicní hypertenze (PH) u defektu septa síní typu II (atrial septal defect – ASD) je řešena individuálně. Pacientů s Eisenmengerovým syndromem s těžkou ireverzibilní PH je u ASD málo. Katetrizační uzávěr je vhodný pouze pro defekty typu secundum (nikoli sinus venosus nebo primum), pouze do určité velikosti, s dostatečnými okraji pro oporu okluderu a bez přidružených vad. Chirurgický uzávěr defektu včetně výkonu na chlopních lze provést z minithorakotomie či roboticky.
Bikuspidální chlopeň aorty a vrozené aortální vady
Bikuspidální aortální chlopeň (bicuspid aortic valve – BAV) je častá vrozená odchylka přítomná asi u 1–2 % běžné populace. Vzácná je unikuspidální chlopeň aorty. U mladších dospělých mužů s BAV nacházíme poměrně často aortální regurgitaci (AR). BAV má tendenci časněji degenerovat a kalcifikovat se vznikem aortální stenózy (AS). U BAV vzniká degenerativní kalcifikovaná AS v mladším věku než u trojcípé aortální chlopně. Bikuspidální i unikuspidální aortální chlopeň bývá spojena s dilatací ascendentní aorty, většinou až nad sinotubulární junkcí. Vzhledem k tomu, že se porucha funkce často vyvine až v dospělosti, nebývají BAV většinou zahrnovány mezi VSV.
Je však potřeba odlišit vrozené aortální stenózy, které jsou přítomny již při narození nebo v dětství, ať již na vrozeně bikuspidální, unikuspidální nebo dysplastické trojcípé aortální chlopni. Fetálně vzniklá AS bývá kritickou vrozenou srdeční vadou s rizikem fibroelastózy endokardu a hypoplastické levé komory. Na některých pracovištích se vzácně provádí fetální aortální valvuloplastika u kritické AS již in utero. Jinak se však běžně provádí katetrizační balonková valvuloplastika nebo chirurgická valvulotomie po narození s načasováním podle klinického stavu novorozence.
Pro dospělého kardiologa je důležité, že naprostá většina pacientů po katetrizační nebo chirurgické valvulotomii vrozené AS v dětství má často reziduální AR nebo méně často aortální restenózu, kterou je třeba pečlivě sledovat a řešit. Vrozené AS bývají spojeny s úzkým až hypoplastickým aortálním anulem a úzkým výtokovým traktem levé komory, velmi těžkou hypertrofií myokardu levé komory způsobenou nejen hypertrofií myocytů, ale i jejich hyperplazií (zmnožením) v časném postnatálním období.
Při významné reziduální aortální vadě lze kromě mechanické náhrady mladým pacientům v některých případech nabídnout i Rossovu operaci, bioprotézu nebo plastiku aortální chlopně – vše bez nutnosti trvalé antikoagulační léčby (obr. 1). Při splnění kritérií dilatace aorty (tab. 1) je vhodná současná náhrada ascendentní aorty (případně její bandáž) nebo náhrada kořene aorty. Významně vyšší riziko disekce je u Marfanova syndromu (obr. 2) a k disekci může dojít i u nedilatované aorty u Loeys-Dietzova syndromu.
1. Indikace chirurgického výkonu na dilatované aortě. 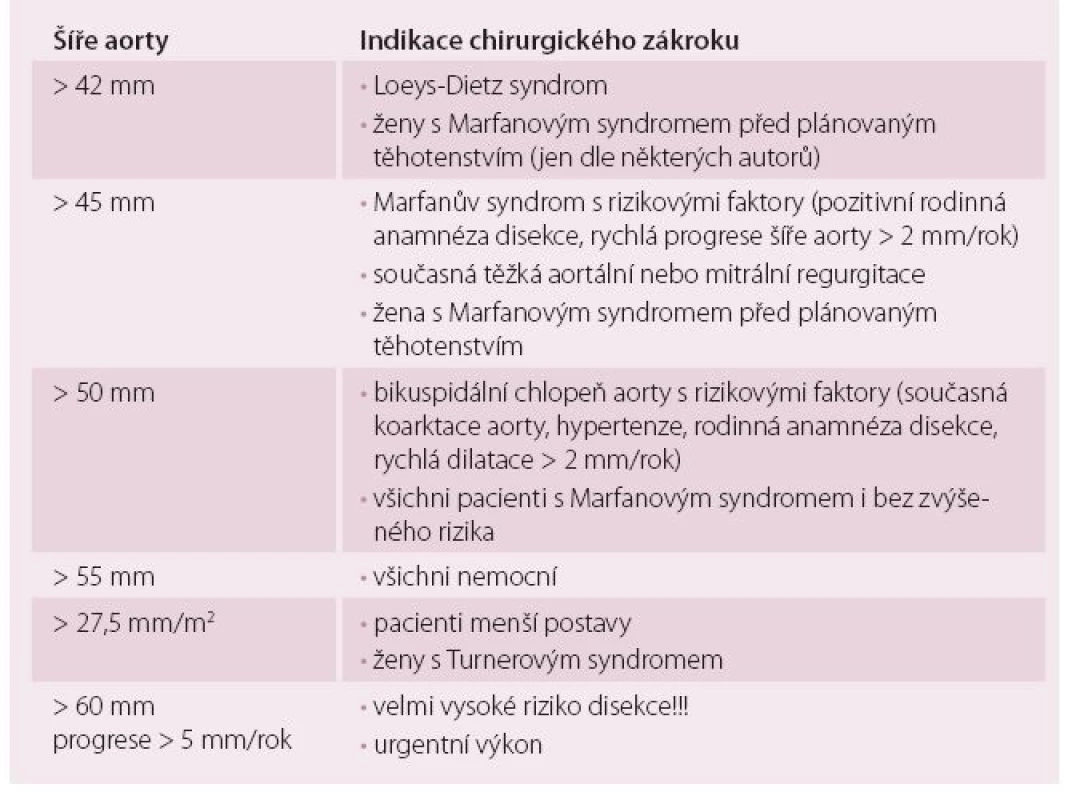
1. Chirurgické řešení Marfanova syndromu se zachováním vlastní aortální chlopně, která je implantována do cévní protézy 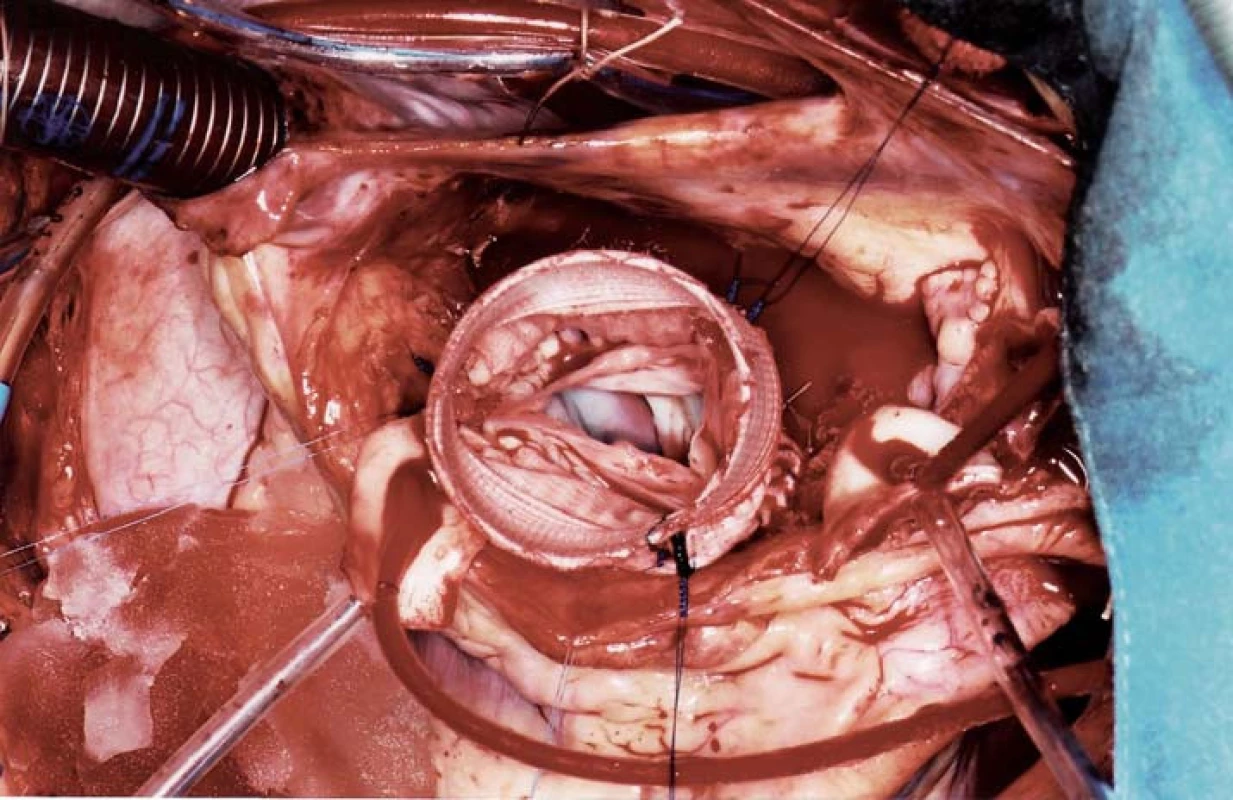
(obr. poskytl laskavě MUDr. Štěpán Černý, Kardiochirurgie Nemocnice Na Homolce). 2. Marfanův syndrom, operační nález: těžká dilatace aorty 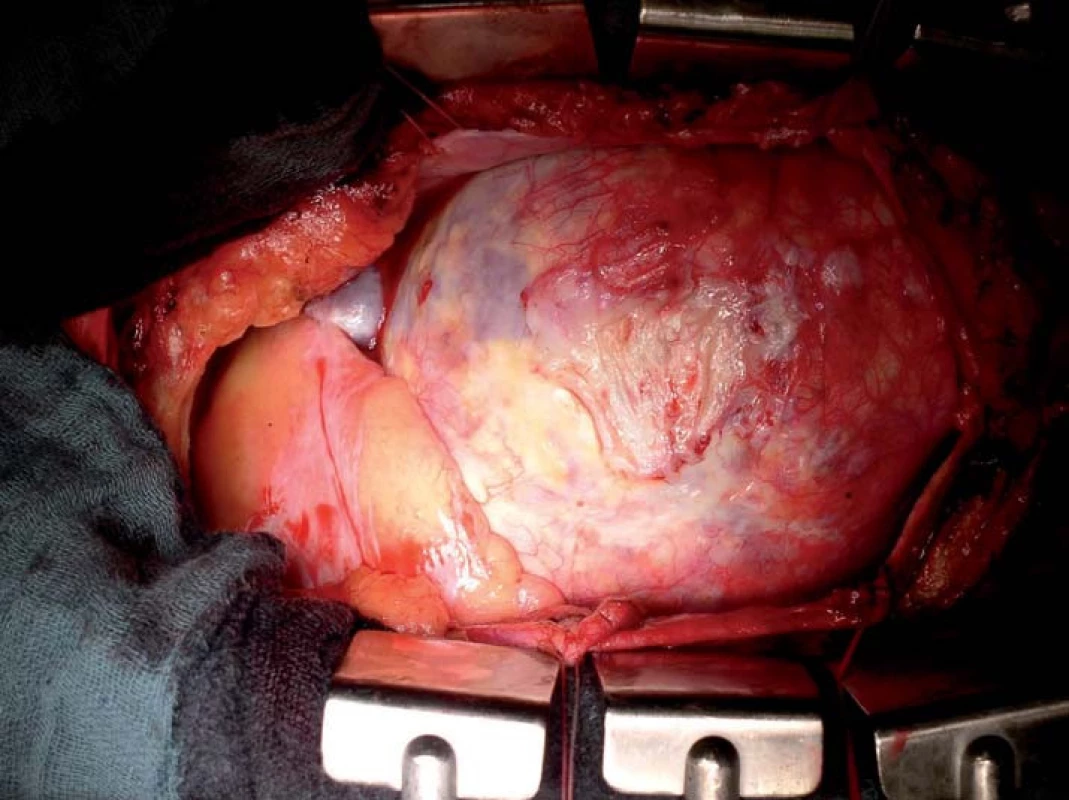
(obr. poskytl laskavě MUDr. Petr Pavel a MUDr. Štěpán Černý, Kardiochirurgie Nemocnice Na Homolce). Defekt komorového septa
Defekt komorového septa (ventricular septal defect – VSD) bývá většinou objeven a uzavřen v dětství, část defektů se uzavírá spontánně. Reziduální defekty nacházíme často u pacientů operovaných v počátcích kardiochirurgie. Defekt se projeví hlučným systolickým šelestem a při významném levo-pravém zkratu dilatací levé komory a levé síně, někdy i pravé komory. Hemodynamicky významný neoperovaný nebo reziduální defekt je indikován k uzávěru, většinou chirurgickému, i bez významných symptomů. Katetrizační uzávěr je vhodný jen u některých defektů. Chirurgický uzávěr může být obtížný při masivních kalcifikacích okraje defektu nebo kalcifikaci dehiscentní záplaty. Uzávěr je kontraindikován u Eisenmengerova syndromu (viz níže), ale není doporučen ani u malého defektu bez hemodynamické významnosti a bez anamnézy infekční endokarditidy.
Méně časté VSV v dospělosti
Fallotova tetralogie
Nejčastější cyanotická VSV je způsobena anterokraniální deviací výtokového septa, které způsobí subvalvární stenózu plicnice, nasedání aorty nad velký perimembranózní komorový defekt a sekundární hypertrofii pravé komory. Může být přítomna i valvární stenóza plicnice a periferní stenózy větví plicnice. Dříve se Fallotova tetralogie (tetralogy of Fallot – TOF) řešila dvoufázově, nejprve pomocí subclavio-pulmonální spojky (podle Blalocka-Taussigové), která zvýšila plicní průtok a snížila stupeň cyanózy s následnou radikální korekcí, která cyanózu odstranila zcela. V současnosti je upřednostněna většinou přímo radikální korekce.
I po úspěšné korekci je často přítomna řada reziduálních nálezů a pacienti mohou v dlouhodobém sledování ve 2–6 % umírat náhlou smrtí při maligních komorových arytmiích [14,15]. Nejčastějším reziduálním nálezem je pulmonální regurgitace. Méně časté jsou pulmonální stenóza, stenózy nebo uzávěry větví plicnice, reziduální defekty komorového nebo síňového septa, aortální regurgitace, sekundární trikuspidální regurgitace a další. I velmi těžká pulmonální regurgitace bývá dlouho dobře tolerována, avšak vede k dilataci a objemovému přetížení pravé komory se zvýšeným rizikem arytmií a srdečního selhání. Rizikovým faktorem úmrtí je šíře QRS při bloku pravého raménka Tawarova nad 180 ms [16]. Standardní léčbou je chirurgická implantace pulmonální bioprotézy. Pokud měl pacient v dětství implantován konduit (homograft), je v některých případech možná i katetrizační implantace pulmonální chlopně do tohoto konduitu. Současně je třeba korigovat ostatní reziduální nálezy. Všichni pacienti po operaci TOF by měli být vyšetřeni na specializovaném pracovišti, které rozhodne o dalším postupu.
Stenóza plicnice
Stenóza plicnice (pulmonary stenosis – PS) může vzácně zůstat nepoznána do dospělého věku a může být objevena až jako příčina pravostranné dekompenzace. PS vede k vysokému gradientu na trikuspidální regurgitaci, který nesmí být zaměněn s plicní hypertenzí. PS je operabilní vada. Většinou je PS řešena v dětství pomocí balonkové valvuloplastiky nebo chirurgické valvulotomie. V obou případech se po letech postupem času většinou vyvíjí střední nebo těžká pulmonální regurgitace. Ta zůstává někdy nepoznaná a podhodnocená. Měli bychom na ni myslet u všech PS řešených v dětství. Léčbou je chirurgická náhrada pulmonální chlopně, nejčastěji bioprotézou nebo homograftem.
Pulmonální atrezie
Pulmonální atrezie (pulmonary atresia – PA) s intaktním komorovým septem je těžká, kritická vada. Vzácně se provádí perforace pulmonální chlopně již u fétu. Chirurgické řešení je nutné brzy po narození, dříve než dojde k uzávěru otevřené tepenné dučeje. PA bývá spojena s hypoplazií pravé komory, trikuspidální chlopně a plicního řečiště, které je zásobeno mnohočetnými aorto-pulmonálními kolaterálami (MAPCAS). Dětští pacienti podstupují řadu korekčních operací, v některých případech je možná biventrikulární korekce, u jiných zůstane jednokomorová cirkulace (viz níže).
V dospělosti mají tito nemocní řadu reziduí, většinou vyžadují reoperaci do 20 let od primární korekce. Mohou mít stenózu nebo nedomykavost pulmonálního homograftu, významné stenózy větví plicnice, ale i plicní hypertenzi, reziduální aorto-pulmonální kolaterály i AR při dilatované aortě. Významnost stenózy pulmonálního homograftu může být při menší zkušenosti podhodnocena, zvláště při dysfunkční pravé komoře. Pacienti s PA musí být pravidelně sledováni ve specializovaném centru.
Atrio-ventrikulární septální defekt
Inkompletní atrio-ventrikulární septální defekt (atrio-ventricular septal defect – AVSD) je znám jako defekt septa síní typu primum. Kromě defektu v dolní části mezisíňového septa k němu patří i abnormální („kanálová“) mitrální chlopeň, která má kromě „rozštěpu“ předního cípu i další abnormality chlopně samotné i závěsného aparátu. Defekt bývá nejčastěji zjištěn a chirurgicky uzavřen v dětském věku, ale může zůstat nepoznán až do dospělosti. Lze uzavřít pouze chirurgicky, nikoli katetrizačně. I když byla mitrální chlopeň v dětství plastikována, je nejčastějším reziduálním nálezem mitrální regurgitace. Plastika či replastika této abnormální chlopně není jednoduchá a někdy je nutná náhrada. AVSD má vrozeně úzký výtokový trakt levé komory (LVOT), který může způsobit progredující subvalvární AS. K obstrukci mohou přispívat i abnormální šlašinky mitrální chlopně a mitrální protéza. Pacienti mohou mít reziduální defekt mezi síněmi, ale i zkrat mezi levou komorou a pravou síní, případně i mezi pravou komorou a levou síní. Operace a reoperace této vady patří na pracoviště, které má s operacemi AVSD zkušenosti.
Přechodná forma AVSD má kromě síňové složky i menší komorovou složku defektu.
Kompletní AVSD má velký defekt nejen mezi síněmi, ale i velký vtokový komorový defekt a společnou vícecípou atrio-ventrikulární chlopeň. Bývá většinou korigován v dětském věku. Není-li korigován v dětství a nemá-li současně významnou stenózu plicnice, je v dospělosti spojen s těžkou ireverzibilní plicní hypertenzí (Eisenmengerův syndrom, viz níže). Má-li současně významnou stenózu plicnice, není vyloučena operace ve specializovaném centru i v dospělosti.
Koarktace aorty
Koarktace aorty (coarctation of the aorta – COA) je považována v současnosti za generalizovanou arteriopatii, nejen lokalizované zúžení descendentní aorty v blízkosti odstupu levé podklíčkové tepny. V některých případech je přítomna dlouhá hypoplazie aortálního oblouku, případně jeho zalomení (gotický oblouk aorty). Až v 85 % je COA spojena s bikuspidální aortální chlopní, může být přítomna i současná dilatace ascendentní aorty. Neřešená COA vede k hypertenzi a předčasné ateroskleróze v prekoarktačním řečišti (koronární, mozkové tepny). Většina COA je operována v dětství, nejčastěji resekcí s anastomózou end-to-end. Někdy jsou nativní koarktace i rekoarktace řešeny angioplastikou a stentingem. Větší či menší stupeň rekoarktace/ reziduální koarktace je přítomen u mnoha pacientů po chirurgické i katetrizční léčbě. Klinicky významná COA/ rekoarktace je definována klidovým katetrizačním nebo klinickým gradientem mezi pravou horní a dolními končetinami nad 20 mm Hg a/ nebo více než 50% zúžením aorty oproti šíři aorty nad bránicí. Kromě arteriální hypertenze v horní části těla a hypertrofie levé komory srdeční vede u starších pacientů COA/ reCOA k těžké diastolické dysfunkci levé komory s dušností, někdy i plicní hypertenzí. COA může být spojena s aneuryzmaty mozkových tepen. Řešení významné COA/ reCOA je chirurgické či katetrizační na pracovišti se zkušenostmi s daným způsobem léčby. Chirurgické řešení může spočívat v resekci nebo v extra-anatomickém bypassu spojujícím ascendentní a descendentní aortu. Katetrizační řešení spočívá v dilataci a zavedení stentu. Vhodnou zobrazovaní metodou je CT angiografie (obr. 3a, 3b) a magnetická rezonance.
Obr. 3a. CT angiografie s 3D rekonstrukcí ukazuje těžkou neléčenou koarktaci aorty u 50leté ženy s dilatací ascendentní aorty. 
Obr. 3b. Chirurgické řešení pomocí extra-anatomického bypassu a náhrady dilatované ascendentní aorty cévní protézou. 
Ebsteinova anomálie trikuspidální chlopně
Pacienti s touto vzácnou VSV často přežívají bez operace do dospělosti. Jedná se o poruchu delaminace septálního a zadního cípu trikuspidální chlopně od endokardu pravé komory, přední cíp je elongován, může být perforován, je zde abnormální závěsný aparát i myokard pravé komory. Nejedná se tedy jen o prostou poruchu samotné trikuspidální chlopně. Trikuspidální ústí je posunuto apikálně a u těžších případů rotováno až do výtokového traktu pravé komory pod plicnici. Vzniká tak tzv. atrializovaná část pravé komory (ARV), což je dyskinetický, tenkostěnný oddíl mezi dislokovaným trikuspidálním ústím a původním anatomickým trikuspidálním anulem (obr. 4). V dospělosti bývá přítomna velmi těžká trikuspidální regurgitace s těžkou dilatací ARV a pravé síně. Často je přítomen defekt septa síní nebo PFO. Podle směru zkratu na úrovni síní Ebsteinova anomálie nemusí, ale může mít cyanózu. Asi u 25 % pacientů se vyskytuje jedna nebo více akcesorních atrio-ventrikulárních spojek (WPW syndrom), většinou řešených katetrizační intervencí, případně chirurgicky. Vlastní Ebsteinova anomálie je v současnosti korigována chirurgicky pomocí složité plastiky dle daSilvy (konoplastika), se kterou má zkušenosti a umí ji kvalitně provést jen velmi omezený počet kardiochirurgů, u kterých se nemocní s Ebsteinovou anomálií centralizují. Alternativou při nepohyblivé, fixované dysplastické chlopni je náhrada bioprotézou. U velmi rizikových nemocných lze doplnit bidirekční cavo-pulmonální spojku k odlehčení dysfunkční pravé komory. Pacienti s Ebsteinovou anomálií by měli být bez ohledu na symptomy vyšetřeni v centru, které se specializuje na operativu této vzácné vady.
3. Ebsteinova anomálie trikuspidální chlopně, echokardiografická čtyřdutinová apikální projekce s patrným apikálním posunem odstupu septálního cípu trikuspidální chlopně o 3 cm (= ARV, označeno křížky). Dilatace pravostranných oddílů, útlak malých levostranných oddílů. 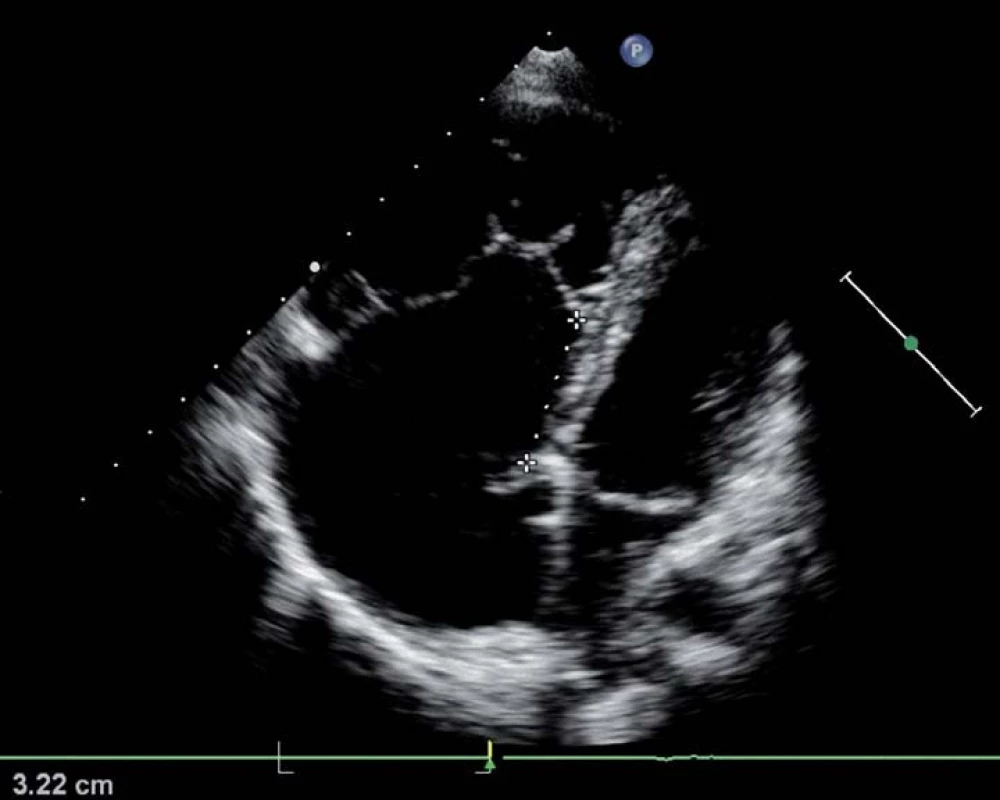
Otevřená tepenná dučej
Otevřená tepenná dučej (ductus arteriosus patens – DAP, patent ductus arteriosus – PDA) je dučej mezi aortou a plicnicí a představuje důležitou funkční strukturu ve fetálním životě. Zůstane-li otevřena dlouhodobě po narození, představuje při levo-pravém zkratu recirkulaci plicním řečištěm s objemovým přetížením levé síně a levé komory. Je-li dučej velká, může dojít ke vzniku těžké PH až Eisenmengerova syndromu (viz níže), zkrat se mění na pravo-levý a dochází k tlakovému přetížení pravé komory a k cyanóze v dolní polovině těla. Menší dučej se projeví typickým systolicko-diastolickým šelestem pod levým klíčkem. Při plicní hypertenzi může být přítomen jen krátký systolický šelest nebo jen akcentace druhé ozvy nad plicnicí. Pokud není přítomna těžká PH a dučej je hemodynamicky významná, je indikován katetrizační, vzácněji chirurgický uzávěr. Většina dučejí je uzavřena v dětství.
Transpozice velkých tepen
Jedna z nejčastějších cyanotických VSV. Jedná se o stav, kdy z pravé komory odstupuje aorta a z levé komory plicnice. Aorta odstupuje vpravo, proto se jedná o d-transpozici velkých tepen (transposition of the great arteries – TGA, d-TGA). Jedná se o dvě oddělené cirkulace, tedy stav neslučitelný se životem, pokud nedojde alespoň k částečnému mísení krve, např. velkým defektem komorového septa. Pacienti mají velmi těžkou cyanózu. Léčba TGA se vyvíjela se zdokonalováním chirurgické techniky. Paliativním výkonem po narození byla chirurgická a později katetrizační atriální septostomie, která umožnila mísení krve na úrovni síní. V 70.–80. letech 20. století se TGA řešila často pomocí tzv. atriální korekce podle Mustarda nebo Senninga. Obě operace měly stejný princip: zkřížení žilních návratů na úrovni síní. Tím se do pravé síně dostala okysličená krev z plicních žil, která pak přes trikuspidální chlopeň a pravou komoru tekla do aorty. Do levé síně se dostávala krev ze systémových žil, která se levou komorou dostávala do plicnice. Tento typ korekce odstranil cyanózu a umožnil dětem v zásadě normální život. K problémům po tomto typu operace dochází v časné dospělosti, kdy je pravá komora v systémové pozici často dysfunkční a selhává, systémová trikuspidální chlopeň regurgituje a někteří pacienti dospějí až k nutnosti mechanické srdeční podpory a srdeční transplantace. Od konce 80. let 20. století se v ČR používá výhodnější typ korekce, anatomická arteriální korekce dle Jateneho (poprvé popsána v roce 1976). Spočívá ve výměně obou velkých tepen nad chlopněmi s reimplantací koronárních tepen do neo-aorty. Provádí se časně po narození. U tohoto typu operace nejsou problémy se systémovou pravou komorou, ale mohou být jiné reziduální nálezy (obstrukce výtokového traktu pravé komory, regurgitace na neo-aortě, stenózy reimplantovaných koronárních tepen). Někteří pacienti s TGA, stenózou plicnice a defektem komorového septa podstoupili Rastelliho operaci s redirekcí aorty nad defekt a nad levou komoru záplatou a spojením pravé komory s plicnicí homograftem. Ten vyžaduje za 10–15 let výměnu pro degeneraci.
Všichni pacienti s TGA musí mít svého kardiologa podrobně obeznámeného s problematikou a typem jejich operace a s možnými reziduálními nálezy a kromě toho musí být pravidelně sledováni ve specializovaném centru.
Vrozeně korigovaná transpozice velkých tepen
Jedná se o vzácnou VSV a je to zcela jiná vada, než je výše uvedená TGA. Aorta odstupuje vlevo, proto l-TGA, ale spíše se užívá název vrozeně korigovaná transpozice velkých tepen (congenitally corrected transposition of the great arteries – CCTGA, l-TGA). U CCTGA jsou vrozeně jakoby vyměněné komory s příslušnými AV chlopněmi. Aorta tak sice odstupuje z morfologicky pravé komory, ta je však umístěna vlevo a přitéká do ní okysličená krev z levé síně a z plicních žil. Vada je tedy vrozeně korigovaná dvojí diskordancí (atrio-ventrikulární a ventrikulo-arteriální). Pokud je CCTGA izolovaná, tak je cirkulace fyziologická a vada je bez cyanózy. Problémy způsobuje až v dospělosti dysfunkční a selhávající morfologicky pravá komora v systémové pozici, regurgitující systémová trikuspidální chlopeň a také poruchy AV převodu při abnormálním převodním systému. Kompletní AV blok vyžadující trvalou stimulaci je u této vady častý, může být přítomen již při narození nebo se vyvinout v průběhu let. Izolovaná CCTGA může být objevena až v dospělosti. Pacienti jsou léčeni pro srdeční selhání, při těžké regurgitaci podstupují náhradu systémové trikuspidální chlopně a mají často trvalou (biventrikulární) kardiostimulaci. V dětství je většina CCTGA (80–90 %) spojena s přidruženou vadou, nejčastěji stenózou plicnice a defektem komorového septa, které mohou vést k většinou mírné cyanóze a bývají v dětství korigovány.
Funkčně společná komora, Fontanovská jednokomorová cirkulace
Některé komplexní VSV mají jen jedinou funkční komoru, druhá komora bývá hypoplastická, nefunkční. Patří sem např. trikuspidální atrezie, mitrální atrezie, dvojvtoková levá komora a další. Tyto i jiné vady (např. extrémní forma Ebsteinovy anomálie s velmi těžce hypoplastickou a dysfunkční pravou komorou) lze řešit chirurgicky tzv. jednokomorovou cirkulací. To znamená, že jediná/ společná komora funguje pouze pro systémovou cirkulaci. Komora může být morfologicky levá, pravá nebo neurčená. Systémové žíly jsou chirurgicky napojeny přímo na větve plicnice. Je tak zcela vyřazena funkce pravé komory. Původní operace podle Fontana spočívala v napojení pravé síně přímo na plicnici; pro závažné reziduální nálezy s extrémní dilatací pravé síně a s arytmiemi se však již delší dobu nepoužívá. V současnosti se provádí tzv. totální cavo-pulmonální spojení (total cavo-pulmonary connection – TCPC) s napojením horní duté žíly na pravou větev plicnice, případné perzistující levostranné horní duté žíly na levou větev plicnice a dolní dutá žíla je napojena intraatriálním nebo extraatriálním konduitem též na plicnici. Tato cirkulace vyžaduje trvale nízký tlak v plicnici a dobrou funkci jediné komory a jejích chlopní. Pacienti jsou zbaveni těžké cyanózy, lehká cyanóza se saturací nad 90 % často přetrvává. Jsou ohroženi mnoha riziky, zvláště tromboembolickými komplikacemi, arytmiemi, srdečním selháním. U mnoha dospělých pacientů s Fontanovskou cirkulací je vhodná trvalá antikoagulační léčba. Všichni nemocní s jednokomorovou cirkulací musí být pravidelně sledováni ve specializovaném centru, avšak i jejich ošetřující lékaři v místě bydliště musí být seznámeni s principem této operace a s jejími riziky.
Eisenmengerův syndrom, těžká plicní hypertenze
VSV s významným zkratem (zvláště defekty komorového septa, kompletní defekty atrioventrikulárního septa, otevřené tepenné dučeje a některé komplexní VSV), pokud nejsou uzavřeny do jednoho roku věku, mohou vést ke vzniku těžké ireverzibilní plicní arteriální hypertenze (PAH) s těžkou remodelací plicního cévního řečiště, tzv. Eisenmengerovu syndromu (ES) [17]. Tlak v plicnici je u ES blízký systémovému tlaku, plicní cévní rezistence je vysoká, obvykle nad 10–14 Wj a pokud přetrvává zkratová vada, je plicní průtok nízký (Qp/ Qs < 1,5 : 1). Těžká plicní arteriální hypertenze může přetrvat i po pozdním uzávěru defektu. Kromě ES však existují i defekty spojené s plicní hypertenzí, která nesplňuje kritéria ES a která může být alespoň zčásti reverzibilní. U těchto defektů lze v některých případech zvážit jejich uzávěr, na rozdíl od ES, kdy je uzávěr zkratové vady kontraindikován. Pacienti s ES při zkratové vadě mají těžkou cyanózu při pravo-levém zkratu, sekundární erytrocytózu (nesprávně „polyglobulii“) a mnoho rizik. Zvýšený počet erytrocytů a vyšší Hb a HTK je fyziologickým důsledkem pravo-levého zkratu. Pokud nemá pacient jasný hyperviskózní syndrom nebo hemoptýzy, nejsou indikovány venepunkce ani hemodiluce. Ty vedou k sideropenii, mikrocytóze a postupně k progresi symptomů dušnosti. Normální počet erytrocytů a normální Hb znamená pro cyanotického pacienta vlastně anémii. Pacient s ES nepatří na hematologii, ale ke kardiologovi znalému této problematiky. U symptomatických pacientů (NYHA III–IV) s ES nebo těžkou ireverzibilní PAH lze zavést specifickou plicní vazodilatační léčbu (inhibitory endotelinových receptorů, inhibitory fosfodiesterázy-5, prostanoidy). Před zahájením léčby je však nutné podrobné vyšetření v centru pro VSV, které odliší ES od jiných cyanotických VSV, které mohou být operabilní díky přítomné stenóze plicnice.
Závěr
U dospělých pacientů s VSV je třeba na specializovaném pracovišti podrobným vyšetřením stanovit přesnou diagnózu a přesný rozsah a význam reziduálních nálezů. Pacienty s nevýznamnými nálezy je třeba zbavit obav z normálních pohybových aktivit a sportu. Někteří pacienti vyžadují nácvik správného dýchání, rehabilitaci, účinnou léčbu nadváhy, psychoterapii, případně sociální poradenství. U žen ve fertilním věku je důležité probrat vhodné a nevhodné metody antikoncepce, možnost a riziko těhotenství, rozhodnout o léčbě v průběhu těhotenství a o způsobu vedení porodu, ale i o načasování případné reoperace s ohledem na plánované těhotenství. Závažné reziduální nálezy a závažné neoperované VSV je třeba řešit vhodným způsobem, vždy po podrobném vysvětlení a dohodě s pacientem. Řešení má být komplexní, s odstraněním i středně významných reziduálních nálezů, které by mohly progredovat. Antiarytmická léčba je řešena komplexně katetrizační intervencí, chirurgicky nebo kombinací obou metod.
- Při sledování dospělých s VSV se vyplatí:
- mít přesné informace o typu VSV a typu operace (operací) v dětství,
- nespoléhat se na to, že malé symptomy znamenají vždy příznivý nález, i prognosticky závažný reziduální nález může být zcela asymptomatický,
- nechat konsiliárně posoudit klinický stav a echokardiografický nález ve specializovaném centru, které rozhodne o dalším postupu,
- při podezření na infekční endokarditidu odebrat vždy hemokultury před zavedením antibiotické léčby,
- zachytit případné arytmie na EKG, které může být posouzeno při plánování antiarytmické intervence (katetrizační či chirurgické).
V Nemocnici Na Homolce bylo od roku 2005 operováno více než 840 dospělýchs VSV s 30denní mortalitou na úrovni 1,36 %. Komplexní a vzácné VSV tvořily 47 % operací. Reoperace po operaci v dětství tvořily 44 % výkonů [18]. Klademe důraz na záchovné operace, (pokud to nález dovoluje) a na méně invazivní chirurgické přístupy. U složitějších VSV je nutný kombinovaný tým složený z dětského a dospělého kardiochirurga a kardio-anesteziologa se zkušenostmi s hemodynamikou a pooperačním průběhem u komplexních VSV.
Podpořeno MZ ČR – RVO, Nemocnice Na Homolce –NNH-00023884, IG140201.
Doručeno do redakce: 20. 7. 2015
Přijato po recenzi: 30. 8. 2015
doc. MU Dr. Jana Rubáčková Popelová, CSc.
www.homolka.cz
jana.popelova@homolka.cz
Sources
1. Popelová J, Frídl P, Hučín B et al. Doporučení pro diagnostiku a léčbu vrozených srdečních vad v dospělosti a prevenci jejich komplikací. Cor Vasa 2002; 44: K165–K184.
2. Warnes CA, Liberthson R, Danielson GK et al. Task force 1: the changing profile of congenital heart disease in adult life. J Am Coll Cardiol 2001; 37 : 1170–1175.
3. van der Bom T, Bouma BJ, Meijboom FJ et al. The prevalence of adult congenital heart disease, results from a systematic review and evidence based calculation. Am Heart J 2012; 164 : 568–575. doi: 10.1016/ j.ahj.2012.07.023.
4. Chaloupecký V. Dětská kardiologie. Praha: Galén 2006.
5. Marek J. Pediatrická a prenatálni Echokardiografie. 2. díl. Praha: Triton 2003.
6. Hučín B. Dětská kardiochirurgie. 2. dopl. vyd. Praha: Grada Publishing 2012.
7. Popelová J. Vrozené srdeční vady v dospělosti. Praha: Grada Publishing 2003.
8. Popelová J, Oechslin E, Kaemmerrer H et al. Congenital heart disease in adults. London: Informa UK 2008.
9. Popelová J, Rubáček M, Mates M et al. Vrozená srdeční onemocnění. In: Vojáček J, Kettner J. Klinická kardiologie. 2. vyd. Hradec Králové: Nucleus 2012.
10. Perloff JK, Child JS, Aboulhosn J. Congenital heart disease in adults. 3rd ed. Philadelphia: Saunders Elsevier 2009.
11. Gatzoulis M, Webb G, Daubeney PE. Diagnosis and management of adult congenital heart disease. Edinburgh: Churchill Livingstone, Elsevier Limited 2003.
12. Moodie DS. Clinical management of congenital heart diseases from infancy to adulthood. Minneapolis, USA: Cardiotext Publishing LLC 2014.
13. Baumgartner H, Bonhoeffer P, De Groot NM et al.ESC Guidelines for the management of grown-up congenital heart disease (new version 2010). The Task Force on the Management of Grown-up Congenital Heart Disease of the European Society of Cardiology (ESC). Eur Heart J 2010; 31 : 2915–2957. doi: 10.1093/ eurheartj/ ehq249.
14. Nollert G, Fischlein T, Bouterwek S et al. Long-term results of total repair of tetralogy of Fallot in adulthood; 35 years follow-up in 104 patients corrected at the age of 18 or older. Thorac Cardiovasc Surg 1997; 45 : 178–181.
15. Silka MJ, Hardy BG, Menashe VD et al. A population-based prospective evaluation of risk of sudden cardiac death after operation for common congenital heart defects. J Am Coll Cardiol 1998; 32 : 245–251.
16. Gatzoulis MA, Till JA, Somerville J et al. Mechanoelectrical interaction in tetralogy of Fallot. QRS prolongation relates to right ventricular size and predicts malignant ventricular arrhytmias and sudden death. Circulation 1995; 92 : 231–237.
17. Jansa P, Popelová J, Al-Hiti H et al. Chronická plicní hypertenze. Doporučený diagnostický a léčebný postup České kardiologické společnosti 2010. Cor Vasa 2011; 53 : 169–182.
18. Rubáčková Popelová J, Gebauer R, Černý Š et al. Operations of adults with congenital heart disease – single center experience with 10 years results. Cor Vasa. In press 2016.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2015 Issue 4-
All articles in this issue
- Myocarditis and inflammatory cardiomyopathy
- Giant cell myocarditis and cardiac sarcoidosis – update 2015
- Pericarditis
- Venous vascular diseases – an urgent issue in clinical medicine
- Diagnosis, classification and principles of management of cerebrovascular atherosclerotic disease from perspective of angiology
- Evolocumab – antibody against PCSK9 with a profound lipid-lowering effect
- Infectious endocarditis – diagnostics and guidelines
- Adults with congenital heart diseases
- Clinical approach to patients with aortic stenosis
- Indication for intervention and the most appropriate treatment of mitral regurgitation
-
Vztah a klinický význam chronického onemocnění ledvin u pacientů s poruchami srdečního rytmu a/ nebo s implantabilními elektrickými přístroji
Zkrácená komentovaná verze oficiálního stanoviska Evropské společnosti pro srdeční rytmus -
Jak léčit dyslipidemii u pacientů s renální insuficiencí
Výběr z doporučení KDIGO s klinickým komentářem - Prescribing antibiotic treatment in patients on renal replacement therapy
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Pericarditis
- Myocarditis and inflammatory cardiomyopathy
- Adults with congenital heart diseases
- Infectious endocarditis – diagnostics and guidelines
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

