-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Výsledky konfirmačních HLA typizací dárců jako indikátor kvality HLA typizace dárců Českého národního registru dárců dřeně (ČNRDD)
Confirmatory HLA typing results as an indicator of quality of the HLA typing of the door pool: Czech national marrow doors registry (CNMDR) experience
Objective estimation of the HLA typing quality of the donor registry could be deduced from the analysis of confirmatory typing results. We tested this approach in the Czech National Marrow Donors Registry. CT results information has been continuously collected separately for HLA-AB (serology) and DRB1 (DNA) during period of 1998-2005. Altogether 758 results were analysed for HLA-A,B and 1107 for DRB1. Serological HLA-A,B phenotypes were confirmed in 704 (92.9 %) donors with the 2972/3032 (98 %) correctly serologically assigned HLA-A,B antigens. In 26/54 (48%) of incorrectly typed, the discrepancies were caused by serologically missed antigens. In this group the less frequent or rare antigens predominates (14/27 discrepancies in 26 donors). In the misassigned and overassigned antigen group a prevalence of CREG-type errors was reported (28/33 discrepancies in 31 donors), with a majority being wrongly assigned splits (19/28 CREG errors). In totally, 16/54 (30 %) of unconfirmed results were related to A19 group mistyping. The DRB1 accuracy was excellent; only 8/1107 (0.7%) donors were unconfirmed. Discrepancy rate was insignificantly higher for donors recruited during 1993-98 than for donors recruited later (59 vs. 41 %, p=0,21). The system represents a simple tool allowing determination of the quality of HLA-A, -B serological, as well as DRB1* DNA typing of a national registry, and complements classical QC programmes. The transition to DNA-based typing of Class I at recruitment will solve the problem of errors inherent in serology.
Key words:
confirmatory typing, HLA typing, quality control, serology, stem cell registry, typing discrepancies, DNA analysis
Autoři: P. Jindra 1,2; Z. Ambrůzová 3; F. Mrázek 3; H. Pittrová 1; J. Navrátilová 1; K. Steinerová 1,2; V. Koza 1,2
Působiště autorů: Český národní registr dárců dřeně, Plzeň, 2Hematologicko-onkologické oddělení, FN Plzeň, 3HLA laboratoř Ústav imunologie, FN Olomouc 1
Vyšlo v časopise: Transfuze Hematol. dnes,13, 2007, No. 3, p. 142-148.
Kategorie: Souhrnné práce, původní práce, kazuistiky
Souhrn
Kvalita HLA typizace v registrech dárců dřeně by mohla být objektivně posouzena na základě výsledků konfirmačních typizací. Tento přístup jsme použili v Českém národním registru dárců dřeně. Výsledky konfirmačních typizací za období 1998–2005 byly analyzovány zvlášť pro HLA-A,B lokusy (sérologie) a pro HLA-DRB1* lokus (DNA). Celkem bylo vyhodnoceno 758 výsledků pro HLA-A,B lokus a 1107 pro DRB1. Sérologické HLA-A,B fenotypy byly potvrzeny u 704 (92,9 %) dárců, což představovalo 2972/3032 (98 %) korektně sérologicky stanovených HLA-A,B antigenů. U 26/54 (48 %) z nesprávně typizovaných byla diskrepance způsobená antigenem nepoznaným sérologicky. V této skupině dominovaly málo časté či přímo vzácné specificity (14/27 diskrepancí u 26 dárců). U správně zaznamenaných, ale chybně určených, stejně jako u sérologicky falešně heterozygotních, naopak dominovaly chyby dané zkříženou reaktivitou sér (CREG, 28/33 diskrepancí u celkem 31 dárců), většinou šlo o chybně stanovené splity (19/28 CREG chyb). Celkem 16/54 (30 %) chyb bylo v souvislosti s chybnou typizací sérologické skupiny A19. Přesnost DRB1* typizace byla excelentní, pouze 8/1107 dárců (0,7 %) nebylo konfirmováno. Počet chyb u dárců typizovaných v letech 1993–1998 byl nesignifikantně vyšší než u dárců typizovaných později (59 % versus 41 %, p = 0,21). Prezentovaná studie představuje jednoduchý prostředek umožňující objektivně stanovit kvalitu HLA typizace registru dárců krvetvorných buněk jak pro sérologii (HLA-A,B), tak DNA (HLA-DRB1) a vhodně doplňuje standardní programy kontroly kvality. Definitivní vyřešení relativně vysokého podílu chyb daného vlastní podstatou sérologické metodiky však přinese pouze přechod na DNA typizaci i pro I. třídu HLA již při náboru.
Klíčová slova:
konfirmační typizace (CT), HLA typizace, kontrola kvality, sérologie, DNA analýza, registr dárců krvetvorných buněk, typizační diskrepanceÚvod
Nepříbuzenské transplantace krvetvorných buněk jsou již standardním léčebným postupem u vybraných pacientů s hematologickými malignitami (1) a šance na nalezení nepříbuzného, HLA shodného dárce, v současnosti výrazně vzrostly (2, 3). To je důsledkem trvalého růstu dobrovolných nepříbuzných dárců krvetvorných buněk, jejichž počet v roce 2005 již překročil 10 milionů (4).
Přesnost vyšetřených HLA znaků u nepříbuzných dárců je základní podmínkou efektivní činnosti každého registru nepříbuzných dárců. U typického registru je databáze dárců tvořena HLA daty, která jsou primárně získána typizací dárce při jeho náboru. Tato typizace je prováděna v HLA laboratořích jednotlivých dárcovských center a jejich výsledek je pak reportován do centrální databáze registru. Kontrola registru nad procesem získávání těchto HLA dat je pak logicky limitovaná. Navíc při vstupní typizaci dárců se pro I. třídu HLA nadále většinou používá sérologie, přičemž nepřesnost této typizační techniky byla opakovaně přesvědčivě dokumentována – podíl sérologicky chybných typizací se dle řady studií pohybuje mezi 5–25 % pro typizaci HLA I. třídy (5–7). Je tedy evidentní, že každý registr nepříbuzných dárců by měl mít zavedený systém externí kontroly kvality (EKK) HLA typizace dárců. Standardně používanou metodou je systematické a pravidelné zasílání „slepých“ vzorků do všech HLA laboratoří typizujících pro daný registr a následná analýza výsledků. Nicméně tyto vzorky jsou „slepé“, pouze pokud jde o jejich HLA fenotyp. „Kontrolní“ charakter těchto vzorků je totiž obvykle personálu znám a proto i přístup k jejich zpracování a typizaci nemusí přesně odrážet běžnou praxi laboratoře při rutinní typizaci nově rekrutovaných dárců. Objektivní informace o kvalitě HLA typizace poolu dárců registru však může být získána analýzou výsledků tzv. konfirmačních typizací (CT). Tyto typizace jsou ze své definice v podstatě HLA retypizacemi předběžně shodného potenciálního dárce prováděnými na žádost transplantačního centra (a většinou HLA laboratoří transplantačního centra). Dárci, u nichž je prováděno CT, jsou vybíráni náhodně transplantačním centrem na základě potenciální HLA shody s pacientem. Cílem této opakované typizace je (1) jednak potvrdit (konfirmovat), a (2) jednak upřesnit HLA fenotyp dárce, který byl získán vstupně při jeho náboru. Tyto CT dárců jsou tedy přirozeným a objektivním indikátorem kvality každodenní rutinní typizační praxe dané laboratoře, neboť jsou vybírány náhodně a nezávisle na laboratoři či registru a jsou typizovány jinou než původně typizující laboratoří. Systematický dlouhodobější sběr a analýza těchto výsledků CT mohou tedy dobře plnit úlohu externí „náhodné“ kontroly kvality HLA typizace dárců registru nepříbuzných dobrovolných dárců, neboť primární HLA data dárce z registru tak mohou být průběžně srovnávána s HLA daty získanými nezávislou laboratoří transplantačního centra při konfirmační typizaci.
V naší studii retrospektivně analyzujeme data získaná sběrem CT výsledků dárců Českého národního registru dárců dřeně (ČNRDD) během let 1998–2005, s cílem (1) stanovit celkový podíl chybně typizovaných dárců a (2) pokusit se definovat typický charakter a následně i příčinu nejčastěji se vyskytujících chyb.
Materiál a metodika
Organizace, struktura a základní charakteristiky registru
Český národní registr dárců dřeně (BMDW kód CS2) byl založen v roce 1991 a roku 1992 zahájil nábor dárců. V současnosti disponuje databází více než 30 000 dárců, více než 80 % z nich je současně DRB1* molekulárně-geneticky (DNA) typizováno (data z dubna 2007) (4). Dárci jsou náborováni sítí 9 dárcovských center (obvykle při transfuzních odděleních v krajských městech) a v těchto centrech jsou typizováni sérologicky na I. třídu HLA. Od roku 1996 jsou všichni nově zařazení dárci současně i DNA typizováni na DRB1* gen, výhradně v EFI akreditovaných HLA laboratořích (Plzeň a Olomouc). EKK HLA typizace v laboratořích ČNRDD byla ustanovena v roce 1998 a sestává ze 2 částí. První z klasické EKK tvořené pravidelným zasíláním slepých vzorků do laboratoří kontrahovaných dárcovských center, kterou pro sérologii organizuje HLA laboratoř ÚIA v Olomouci (pro DNA typizaci je organizovaná prof. Fischerem, Dpt. of Blood Group Serology, Vídeň). Druhou součástí systému kontroly kvality, která je předmětem naší práce, je právě kontinuální analýza CT výsledků, jež jsou systematicky shromažďovány od roku 1998.
Vstupní HLA typizace dárců ČNRDD
Vstupní sérologická typizace dárců byla prováděna standardní CDC (komplement-dependentní cytotoxický test) technikou, přičemž od roku 1998 byly používány uniformní komerční typizační plotny (Dilen s.r.o, ČR) standardizované pro českou populaci.
HLA-DRB1* typizace nízkým rozlišením (2-digits) byla prováděna DNA technikou (PCR-SSP či PCR-SSOP) za použití komerčních kitů (PCR-SSP: GenoVision, Vienna, Austria; PCR-SSOP: Dynal Biotech, Oslo, Norway). Stejnými kity byla prováděna i typizace vysokým rozlišením (4-digits), jakož i typizace ostatních HLA-genů.
Design studie
Jedná se o retrospektivní analýzu dat CT získaných kontinuálně během časového období 1998–2005 zvlášť pro sérologii (HLA I. třídy, jmenovitě A,B lokus) a zvlášť pro DNA typizaci (DRB1*). Konfirmační typizace pro I. třídu HLA byly prováděny různými metodikami a různým rozlišením podle zvyklosti retypizující laboratoře, nicméně více než 90 % CT výsledků bylo reportováno v DNA formátu. Pro DRB1* byla jako CT výsledek akceptována pouze DNA typizace. Část konfirmačních DNA retypizací HLA I. i II. třídy byla na základě požadavků transplantačních center prováděna i Centrální HLA laboratoří ČNRDD v Plzni (tzv. customized typing service), tyto výsledky retypizací byly do analýzy též zahrnuty. Výsledky typizací ze zahraničních laboratoří byly primárně referovány do koordinačního centra ČNRDD a odtud neprodleně distribuovány do Centrální HLA laboratoře. Zde byly všechny diskrepance s původním výsledkem HLA typizace dárce (tzv. nekonfirmovaný dárce) ověřovány (viz dále). Ze souboru dat výsledků CT dárců byl kalkulován podíl chybných typizací a současně byla provedena analýza typu těchto typizačních chyb. Vzhledem k zásadně odlišnému kvalitativnímu charakteru sérologické a DNA typizace, a tedy i nemožností analyzovat přesnost typizace těchto metodik současně, byla typizační data pro HLA-I. třídu (tj. sérologii) a HLA–DRB1 (DNA) analyzována separátně a takto jsou i prezentována.
Diskrepantní HLA typizace
Všechny CT výsledky, u kterých byla reportována diskrepance s původní HLA typizací dárce, byly verifikovány třetí DNA typizací za použití originálního vzorku DNA dárce a pokud bylo nezbytné, pak i z nového náběru dárce. Analýza byla prováděna ve spolupráci s dárcovským centrem, které typizovalo dárce při náboru. Pro hodnocení sérologických diskrepancí pro HLA-A,B lokus byly použity standardy a oficiální definice EFI (Evropská federace pro imunogenetiku, www.efiweb.org). Chyby (diskrepance) sérologických typizací byly tedy definovány takto:
- I. Nedetekovaná, ale přítomná alela, to jest alela sérologií nezaznamenaná, ale přítomná za použití DNA typizace (přičemž nejde o tzv. null alelu). Jde o falešnou homozygocii („missed“ antigen) – diskrepance typu I
- II. Chybně určená alela, to jest antigen versus antigen. Je správně určena přítomnost alely, ale chybně určen její typ („misassigned“ antigen) – diskrepance typu II
- III. Stanovená, ale nepřítomná alela, tedy antigen zaznamenaný sérologicky, ale DNA typizací neprokázaný. Jde o falešnou heterozygocii („over-assigned“ antigen) – diskrepance typu III
Za diskrepance nebyly považovány případy, kdy výsledek CT určil „split“ alelu v případě, že byla původně reportována pouze odpovídající “broad” specificita. HLA-Cw lokus nebyl hodnocen vzhledem k obtížné přímé komparaci sérologicky a molekulárně–geneticky definovaných specificit (pro řadu Cw alel neexistuje sérologický ekvivalent). Pro potřeby analýzy možné příčiny chyb byly chybné typizace (sérologické diskrepance) klasifikovány dle pravděpodobné základní vyvolávající příčiny do následujících 3 skupin:
- zkříženě reagující antigeny („cross-reactive groups“) = CREG skupina
- nedostatek monospecifických sér = skupina vzácných antigenů
- neklasifikovatelné
Diskrepance typu I (tj. falešné homozygocie, „missed“ antigeny) byly klasifikovány podle druhého (původně nedetekovaného) antigenu, zatímco diskrepance typu II („misassigned“ antigeny) byly klasifikovány podle původně nesprávně určené specificity.
Diskrepantní (chybné) typizace DNA technikou DRB1* genu byly na rozdíl od sérologie pouze zaznamenány a jednoduše spočítány.
Výsledky
HLA –A,B: sérologie
V analyzovaném časovém úseku 1998–2005 bylo v rámci CT retypizováno celkem 758 původně sérologicky HLA-A,B typizovaných dárců a tyto výsledky byly srovnány s výsledky typizace při náboru. Data jsou shrnuta v tabulce 1. HLA genotyp byl potvrzen u 702 dárců (92,6 %). Diskrepance s původním, vstupně registrovaným HLA fenotypem byla tedy zaznamenána u 56 dárců (7,4 %). U 2 dárců (0,3 % z retypizovaných a 3,6 % ze všech diskrepantních dárců) byla příčinou diskrepance administrativní chyba při zápisu do databáze ČNRDD, zatímco originální výsledek vydaný HLA laboratoří dárcovského centra byl v souladu s výsledkem CT. Tyto 2 dárci byly proto z následujících analýz a kalkulací HLA typizačních chyb vyloučeni. Celkový podíl nesprávně HLA-A,B sérotypizovaných dárců byl tedy 7,1 %. Nicméně mezi 175 HLA-A a /nebo HLA-B sérologicky homozygotními dárci (23 % z CT) jsme zaznamenali celkem 26 nekonfirmovaných, což činilo celkový podíl diskrepancí u homozygotů více než dvojnásobný – 15 %. Současně byl pozorován statisticky nesignifikantní trend (p = 0,21) k vyššímu podílu chybných typizací u dárců rekrutovaných, a tedy i vyšetřených během první poloviny období existence registru. Ze všech 54 chybně typizovaných dárců bylo celkem 32 (59 %) vyšetřeno v letech 1993–1998, zatímco pouze 22 chybně typizovaných v období 1999–2004.
Tab. 1. Souhrn 758 CT vzorků typizovaných původně sérologicky na HLA-A,-B. 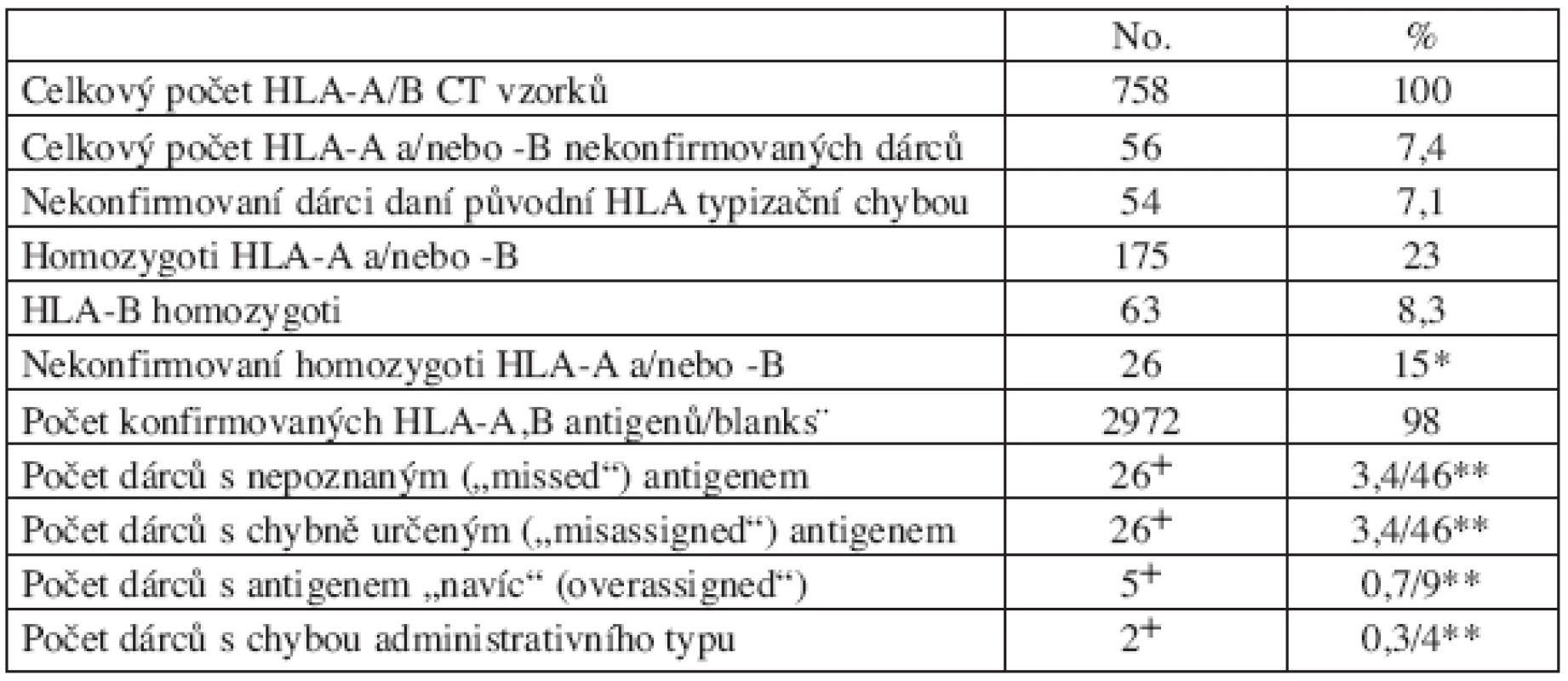
*Kalkulováno z homozygotních dárců + Někteří dárci měli více typů chyb **procento kalkulované ze všech CT/pouze z nekonfirmovaných
Z celkového počtu 3032 HLA-A a -B stanovených antigenů u 758 retypizovaných dárců jich bylo 2972 (98 %) potvrzeno CT vyšetřením.Většinu diskrepancí tvořily antigeny sérologií nedetekované (falešná homozygocie, diskrepance typu I) či chybně určené (diskrepance typu II). Oba typy diskrepancí byly zaznamenány vždy u 26 dárců, tj. 48 % ze všech nekonfirmovaných. Pouze u 5 dárců (9 % chybně typizovaných) byla zaznamenána diskrepance typu III. Souhrn všech diskrepancí podle typu a sérologických specificit je uveden v tabulkách 2–4. Správné sérologické fenotypy jsou v tabulkách pro jednodušší srovnání uvedené v sérologickém a nikoliv v DNA formátu (ve kterém byly obvykle po konfirmační typizaci reportovány). Jak je patrno, většina chyb se týkala sérologické skupiny A19, protože 12/26 (48 %) z chyb typu I a 4/26 (15 %) z chyb typu II se týkalo nepoznaných nebo chybně určených antigenů náležejících k sérologické skupině A19. Celkově byla chyba související s A19 sérologickou skupinou zaznamenána u 30 % z nekonfirmovaných dárců. V souvislosti s tím jsme poněkud překvapivě zaznamenali vyšší prevalenci chyb typu I („missed“ antigeny) u HLA-A lokusu než u HLA-B (19 versus 8 dárců, u jednoho dárce byly chyby v obou lokusech), přičemž největší frekvenci chybného stanovení měl antigen A33 (7/26). Mezi antigeny sérologicky nepoznanými nebyla DNA retypizací zaznamenána žádná „null“ alela, tedy alela s absencí exprese na povrchu buňky a tedy sérologicky nezachytitelná. Je zajímavé, že pro všechny typy chyb (tedy diskrepance I–III) bylo možné vysledovat specifický charakter a tedy i příčinu těchto chyb (viz tab. 2–4). U chyb I typu („missed“antigeny, tab. 2) jednoznačně dominovala jako příčina relativní vzácnost nepoznaných antigenů (nedostatek monospecifických sér, 14/27 diskrepancí u 26 dárců), zatímco zbytek chyb byl rovnoměrně rozložen mezi „neklasifikovatelné“ a zkříženě reagující antigeny (viz Materiál a metodika pro přesnou definici). Naproti tomu u diskrepancí typu II (chybně určené antigeny, tab. 3) měly jasnou převahu chyby způsobené zkříženě reagujícími antigeny (CREG) – 23/28 detekovaných chyb u 26 dárců. Většinou se jednalo o chybně určené „splity“ u „broad“ specificit. U chyb III typu se jednalo výlučně o chyby způsobené zkříženě reagujícími antigeny – CREG skupina (5/5).
Tab. 2. Seznam sérologických diskrepancí dle CT výsledků - sérologicky nepoznané, ale přítomné antigeny („missed“) – chyba typu I, 26 dárců. 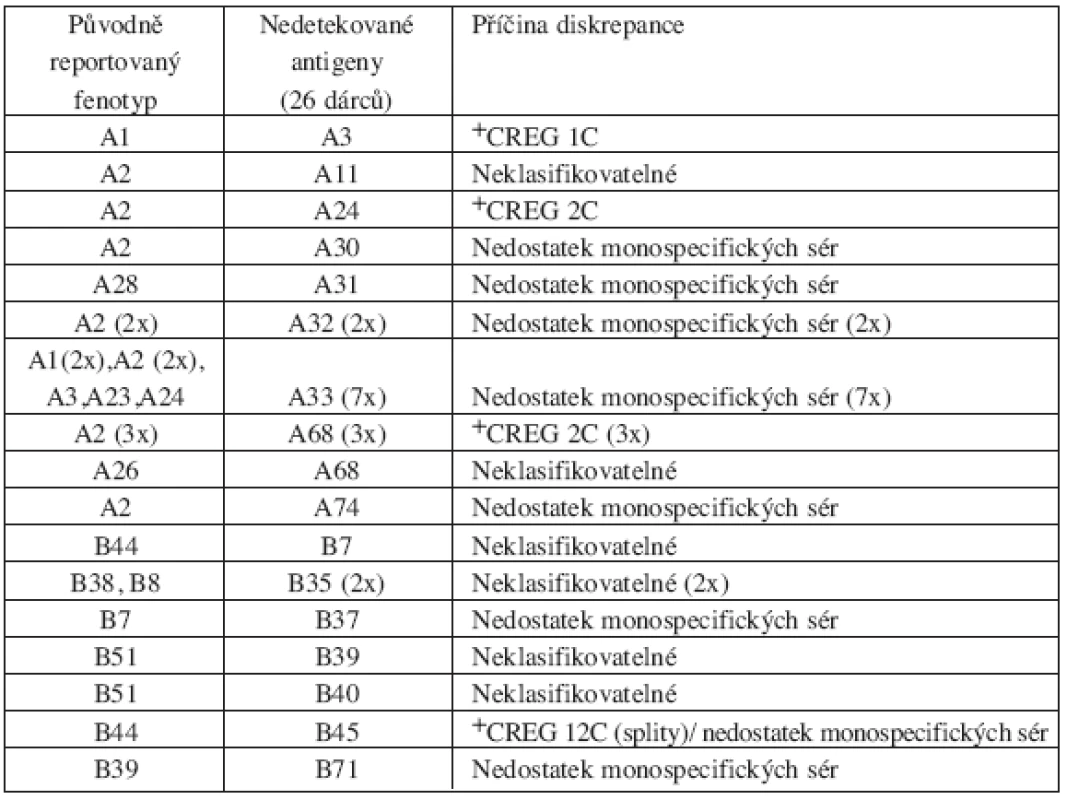
Pozn.: Jeden dárce měl současně nedetekované jak HLA-A, tak –B antigeny +CREG – skupina antigenů ze zkříženě reagující skupiny („cross-reactive groups) a označení skupiny dle WHO nomenklatury Tab. 3. Seznam sérologických diskrepancí dle CT výsledků – sérologicky chybně určené („misassigned“) antigeny – chyba typu II, 26 dárců. 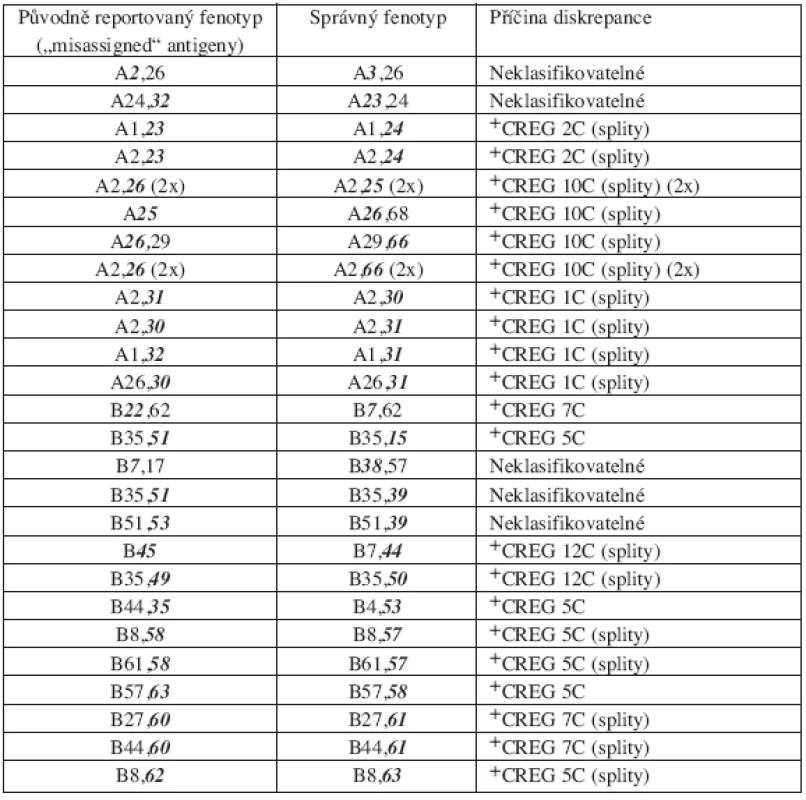
Pozn.: 2 dárci měli jak HLA-A, tak současně HLA–B chybně určené antigeny +CREG – skupina antigenů ze zkříženě reagující skupiny („cross-reactive groups) a označení skupiny dle WHO nomenklatury Tab. 4. Seznam sérologických diskrepancí dle CT výsledků – antigeny detekované sérologicky, ale nepřítomné („overassigned“ ) – chyba typu III, 5 dárců. 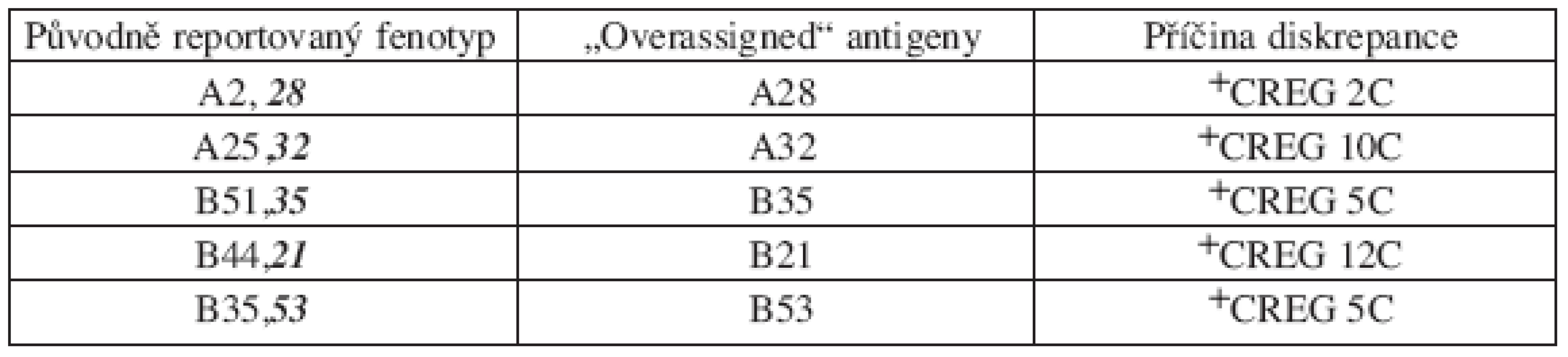
+CREG – skupina antigenů ze zkříženě reagující skupiny („cross-reactive groups) a označení skupiny dle WHO nomenklatury HLA-DRB1*: DNA
Ze všech dárců, kteří byli vstupně molekulárně geneticky (DNA) typizováni na II. třídu, bylo celkem 1107 retypizováno z důvodů konfirmační typizace. Přehled uvádí tabulka 5. Pouze 8 dárců nebylo konfirmováno (< 1 %). Vzhledem k takto nízkému počtu chybně typizovaných nemohla být identifikována žádná dominantní příčina chyb. Ve 3 případech nešlo o technické typizační chyby, ale o chyby administrativní (38 %). Polovina diskrepantních CT výsledků byla způsobena chybným určením alel skupiny DRB1* 03/11/13/14. V těchto případech šlo vždy o suboptimální provedení PCR s následným chybným určením alely. Všichni DRB1*1 nekonfirmovaní dárci byli původně typizováni před rokem 1999.
Tab. 5. Souhrn DRB1* diskrepancí (vstupně DNA typizování) dle CT výsledků. 
*kalkulováno pouze z nekonfirmovaných Diskuse
V naší práci prezentujeme jednoduchou analýzu kvality HLA typizace ČNRDD, která je založena na informacích získaných z výsledků konfirmačních typizací (CT). Hlavní sílou naší analýzy je to, že poskytuje reálnou informaci o celkové spolehlivosti HLA typů dárců zařazených do databáze v průběhu celého období činnosti registru. To je výhodné oproti klasickým schématům externí kontroly kvality, kde je spíše hodnocena kvalita typizační procedury pouze v čase kontroly kvality a vztažená k aktuálnímu kontrolnímu vzorku.
Námi pozorovaný, přibližně 7% podíl sérologicky diskrepantních typizací u 758 retypizovaných dárců ČNRDD, je v souladu s předchozími literárními údaji, kde se reportovaný podíl sérologických chyb po DNA retypizaci pohyboval v rozmezí 3–25 % (5–12). Podobně jako jiní autoři (5, 8, 12) jsme potvrdili 2–3krát vyšší podíl diskrepancí u sérologických homozygotů. Schaffer et al. (5) sice zaznamenala při podobné analýze dat registru u stejné, kavkazoidní populace, poněkud nižší 3 %) celkový podíl chyb než jsou naše výsledky, její zjištění 12–19% podílu chyb u sérologicky homozygotních dárců však dobře koresponduje s naším výsledkem 15 % chyb u této skupiny dárců. Dosud nejrozsáhlejší studie zabývající se přesností HLA typizace v registru nepříbuzných dárců krvetvorných buněk byla provedena v největším světovém registru v USA (NMDP) a DNA typizací paralelně analyzovala více než 40 000 sérologicky typizovaných dárců (9). Zjištěný podíl chyb u sérologie byl sice několikrát vyšší než výsledky ČNRDD – 24 % oproti našim 7 %, nicméně hodnocená populace pocházela primárně z non-kavkazoidních minorit, u kterých je sérologická typizace mnohem obtížnější. Podobný podíl chyb jako v naší studii byl zaznamenán analýzou výsledků kontrol kvality u laboratoří kontrahovaných NMDP (11) či analýzou Švýcarského registru dárců dřeně (8), kde byl publikován 20–25% podíl chyb pro sérohomozygoty a 4–5% celkový podíl chyb pro sérologii I. třídy HLA. Celosvětově zkoumá podíl tzv. nekonfirmovaných dárců „Discrepant Typing Project“ organizovaný WMDA (World Marrow Donor Association) a předběžná data ukazují, že minimálně 3–4 % výsledků CT jsou diskrepantní s výsledky, na jejichž základě byl dotyčný dárce původně považován za identického s pacientem. Při více než 11 milionech nepříbuzných dárců v registrech (4) to představuje téměř půl milionu chybně typizovaných dárců (McGregor M, Wales Registry, osobní komunikace).
V protikladu se sérologií jsou výsledky CT pro HLA II. třídu, typizovanou v ČNRDD již při náboru výhradně DNA technikami. Zde je > 99 % konkordance se vstupní typizací. Stejně vysoký podíl souhlasných, a tedy korektních typizací, jsme zaznamenali i v malé skupině dárců s I. třídou HLA typizovanou také DNA metodikou (data nejsou prezentována). Potvrzujeme tedy jednoznačně vyšší typizační spolehlivost a přesnost DNA typizačních technik, kterou publikovali i jiní autoři (5, 8, 9, 11).
Opět v souladu s ostatními autory, byla většina z našich diskrepantních CT způsobena rovnoměrně chybami jak ve smyslu nezaznamenaných specificit (diskrepance typu I, „missed“), tak chybně určených specificit (diskrepance typu II, „misassigned“). Tento druh chyb opětovně dokládá známý problém sérologie – zkříženou reaktivitu a nedostatek monospecifických sér pro některé vzácnější specificity. Z tohoto pohledu je nejproblematičtější sérologickou skupinou A19, která v naší studii byla spojena s 30 % nekonfirmovaných CT, především jako nepoznané (missed) antigeny. Nespolehlivost sérologie pro přesné stanovení A19 séroskupiny byla též již v minulosti publikována (5, 8, 9, 11). Tento problém lze bohužel obtížně eliminovat systematickou a cílenou retypizací původně sérologicky typizovaných dárců, protože většina chyb byla nepoznanými („missed“) A19 v kombinaci s jinak frekventní homozygocií A1,2 nebo A3.
Souhrn současných dat již dostatečně přesvědčivě ukazuje, že 4–10 % potenciálně shodných nepříbuzných dárců jsou ve skutečnosti neshodní v HLA molekulách I. třídy po retypizaci v rámci konfirmační typizace (hovoříme o neshodě na úrovni „low resolution, čili 2-digits!). To má 2 závažné konsekvence. Za prvé jsou domněle shodní potenciální dárci zbytečně obtěžováni opakovaným odběrem krve s nutností návštěvy často vzdáleného dárcovského centra. Druhým, mnohem závažnějším důsledkem, je časová prodleva při vyhledávání kompatibilního dárce, která u řady pacientů může být pro úspěch transplantace kritickou. Tato prodleva v podstatě přímo torpéduje základní misi každého registru, tj. poskytnout potřebnému nemocnému vhodného dárce v nejkratším možném čase. Proto je také standardizační a akreditační úsilí WMDA výrazně zaměřeno na přesnost HLA typizace v registrech (12, 14).
Systematická analýza výsledků CT může být s výhodou využita ke stanovení co nejefektivnější strategie DNA retypizace HLA-I. třídy. Umožní definovat kategorii sérologicky typizovaných dárců s největším rizikem chybné sérologie a tedy s potenciálně největším přínosem DNA retypizace.
Závěr
Závěrem lze konstatovat, že prezentovaný systém kontroly kvality prostřednictvím CT výsledků představuje velmi jednoduchý a efektivní prostředek posouzení kvality jak sérologické HLA-A,B, tak DRB1* DNA typizace registru a vhodně doplňuje klasická schémata kontroly kvality. Tento přístup by měl být implementován každým registrem a je v souladu s aktivitami i cíly WMDA, jak nakonec dokládá i nedávno touto organizací iniciovaný “Discrepant Typing Project&Survey&Report“. Zveřejněním těchto dat za každý registr by poskytlo cennou informaci transplantačním centrům zamýšlejícím žádat o CT vzorek potenciálně shodných dárců ve specifickém registru. Nicméně problém chyb nevyhnutelně daných podstatou sérologické metodiky bude definitivně eliminován až přechodem na kompletní – tedy I. i II. třídy HLA – DNA typizaci již při náboru.
Poděkování
Všechna výše uvedená data, jakož i samotná činnost ČNRDD, by nebyly možné bez vzorného vedení, udržování a rozšiřování databáze dárců a především bez včasné a bezchybné organizace zasílání vzorků ke konfirmačním typizacím. Za to všechno patří dík především veškerému personálu dárcovských center, jmenovitě MUDr. Heleně Banzetové (TO Nemocnice České Budějovice), MUDr. Janě Pavlíčkové (TO FN Plzeň), MUDr. Kláře Váchové a MUDr. Jiřímu Masopustovi (TO Masarykovy nemocnice Ústí nad Labem), MUDr. Elišce Vyskočilové a MUDr. Miloslavě Strašíkové (TO Nemocnice Most), RNDr. Aleně Bartoníčkové a RNDr. Líbě Janků (TO FN Brno), Mgr. Aleně Maluškové (Krevní centrum FN Ostrava), RNDr. Bohuslavě Jílkové a MUDr. Jitce Černohorské (TO FN Hradec Králové), MUDr. Jaroslavě Urbanové (ÚVN Střešovice, Praha) a prof. MUDr. Martinovi Petřekovi (Ústavu imunologie FN Olomouc).
Největší dík pak samozřejmě patří všem dobrovolným dárcům krvetvorných buněk ČNRDD.
MUDr. Pavel Jindra
Český Národní Registr Dárců Dřeně, Plzeň &
& Hematologicko-onkologické oddělení, FN Plzeňalej Svobody 80304 60 Plzeňe-mail: jindra@fnplzen.cz
Došlo do redakce: 18. 5. 2007
Přijato: 20. 7. 2007
Zdroje
1. Gratwohl A, Baldomero H, Fraunedorfer K, Urbano-Ispizua A and Niederwieser D, for the Joint Accrediation Committee of the ISCT and EBMT. Results of the EBMT activity survey 2005 on haematopoietic stemcell transplantation: focus on increasing use of unrelated donors. Bone Marrow Transplant 2007; 39 : 71–87.
2. Oudshoorn M, Cornelissen JJ, Fibbe WE, de Gareff-Meeder ER, Lie JL Schreuder GM, et al. Problems and possible solutions in findings an unrelated bone marrow donor. Results of consecutive searches for 240 Dutch patients. Bone Marrow Transplant 1997; 20 : 1011–1117.
3. Tiercy JM, Bujan-Lose M, Chapuis B, Gratwohl A, Gmur J, Seger RA, et al. Bone marrow transplantation with unrelated donors: what is the probability of identifying an HLA-A,/B/Cw/DRB1/B3/B5/DQB1-matched donor? Bone Marrow Transplant 2000; 26 : 437–441.
4. Bone Marrow Donors Worldwide. Available at URL: http://www.bmdw.org.
5. Schaffer M, Ollerup O. HLA-AB typing by polymerase-chain reaction with sequnce-specific primers: more accurate, less errors, and increased resolution compared to serological typing. Tissue Antigens 2001; 58 : 299–307.
6. Lorentzen DF, Iwanaga KK, Meuer KJ, Moritz TL, Watkins DI. A 25% error rate in serologic typing of HLA-B homozygotes. Tissue Antigens 1997; 50 : 359–365.
7. Yu N, Ohashi M, Alosco S, Granja C, Salazar M, Hegland J, et al. Accurate typing of HLA-A antigens and analysis of serologic deficiencies. Tissue Antigens 1997; 50 : 380–386.
8. Tiercy JM, Bujan-Lose M, Chapuis B, Gratwohl A, Schanz U, Seger RA, et al. Quality control of a national marrow donor registry: results of a pilot study and proposal for standardized approach. Bone Marrow Transplant 2003; 32 : 623–637.
9. Noreen HJ, You N, Setterholm M, Ohashi M, Baisch J, Endres R, et al. Validation of DNA-based HLA-A and HLA-B testing of volunteers for a bone marrow registry through parallel testing with serology. Tissue Antigens 2001; 57 : 221–229.
10. Mytilineos J, Lempert M, Middleton D, Wiliams F, Cullen C, Scherer S, et al. HLA class I DNA typing of 215 ‘HLA-A-B-DR zero mismatched’ kidney transplants. Tissue Antigens 1997; 50 : 355–8.
11. Gourley, IS, Kearns J, McKeen M, Birkos S, Brown M, Kamoun M. HLA Class I typing of volunteers for a bone marrow registry: QC analysis by DNA-based methodology identifies serological typing discrepancies in the assignment of HLA-A and B antigens. Tissue Antigens 2001; 59 : 211–215.
12. Hurley CK, Wade JA, Oudshoorn M. on behalf of QA and DRWG of the WMDA. A Special Report: Histocompatibility Testing Guidelines for Hematopoietic Stem Cell Transplantation Using Volunteer Donors. Human Immunology 1999; 60 : 347–360.
13. World Marrow Donor Associations. Available at URL: http://www.worldmarrow.org/fileadmin/workinggroups_Subcommittees/QAWG/HLA_discrepant/Discrepant_Typing_2004__Minneapolis.pdf
14. Hurley CK, Raffoux C. World Marrow Donor Association. Special Report: World Marrow Donor Association: International Staadards for unrelated hematopoietic stem cell registries. Bone Marrow Transplantation 2004; 34 : 103–110.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2007 Číslo 3- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
-
Všechny články tohoto čísla
- Chronická B-lymfocytární leukemie Část V. Transplantace krvetvorných buněk
- Co nám v každodenní praxi skutečně říkají tzv. moderní prognostické faktory u chronické lymfatické leukemie?
- Zprávy o knihách
- Klinický význam 18F-FDG-pozitronové emisní tomografie u folikulárního lymfomu
- Zprávy o knihách
- Režim CTD (cyklofosfamid, thalidomid, dexametazon) v léčbě relabujících a refrakterních forem mnohočetného myelomu
- Rezistence na imatinib a možnosti využití vyššího dávkování léku u pacientů s chronickou myeloidní leukemií
- Výsledky konfirmačních HLA typizací dárců jako indikátor kvality HLA typizace dárců Českého národního registru dárců dřeně (ČNRDD)
- Zprávy o knihách
- G-CSF u zdravých dárců. Bezpečný nebo škodlivý?
- Návrh populační registrace hematoonkologických diagnóz vycházející z WHO klasifikace nádorových chorob z roku 1999, z hodnocení základních léčebných přístupů a z požadavků Národního onkologického registru ČR
- Produkce a spotřeba transfuzních přípravků v České republice v roce 2006
- K šedesátinám prof. MUDr. Karla Indráka, DrSc.
- XXI. Olomoucké hematologické dny s mezinárodní účastí, Olomouc 16. 6. – 19. 6. 2007
- Autotransfuze v České republice v roce 2006
- Možnosti kryokonzervace erytrocytů - použití a postup zajištění u potřeby autologních odběrů a dovezených přípravků
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- G-CSF u zdravých dárců. Bezpečný nebo škodlivý?
- Režim CTD (cyklofosfamid, thalidomid, dexametazon) v léčbě relabujících a refrakterních forem mnohočetného myelomu
- Klinický význam 18F-FDG-pozitronové emisní tomografie u folikulárního lymfomu
- Produkce a spotřeba transfuzních přípravků v České republice v roce 2006
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



