-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Výskyt pooperační reziduální kurarizace na dospávacím pokoji po aplikaci rokuronia
The Incidence of Postoperative Residual Curarization in the Recovery Room after Rocuronium Administration
In 513 patients, we investigated residual curarization after general anaesthesia with rocuronium administered, without peroperative neuromuscular blockade monitoring. On admission to the recovery room, the ulnar nerve was stimulated submaximally (30 mA) and the evoked muscle response was quantified with accelerometry (TOF-Watch® SX, Organon). The postoperative residual curarization was defined as a TOF-ratio < 0.9 and could be demonstrated in 174 patients (34 %). Compared to the group with adequate recovery, these patients received larger rocuronium dose [45.4 (SD 13.2) mg vs. 40.4 (SD 14.3) mg, p < 0.01], less experienced anaesthesiologists conducted their case [p < 0.01], shorter time had elapsed since the last rocuronium dose [58.4 (20.9) min. vs. 64.9 (27.2) min., p < 0.05], their core temperature was lower [35.4 (0.6) °C vs. 35.8 (0.6) °C, p < 0.01] and on average, they received less neostigmine during anaesthesia [0.26 (0.47) mg vs. 0.57 (0.71) mg, p < 0.01]. We conclude that it is necessary to antagonize residual block after rocuronium, especially in the absence of perioperative neuromuscular monitoring.
Key words:
post-operative residual curarization – neuromuscular blocker – rocuronium – recovery room
Autoři: M. Adamus 1; J. Koutná 1; Č. Neoral 2
Působiště autorů: Klinika anesteziologie a resuscitace, Fakultní nemocnice a lékařská fakulta Univerzity Palackého, Olomouc, přednosta: MUDr. O. Marek 1; I. chirurgická klinika, Fakultní nemocnice a lékařská fakulta Univerzity Palackého, Olomouc, přednosta: doc. MUDr. Č. Neoral, CSc. 2
Vyšlo v časopise: Rozhl. Chir., 2007, roč. 86, č. 1, s. 11-16.
Kategorie: Monotematický speciál - Původní práce
Souhrn
Vyšetřovali jsme reziduální blok u 513 nemocných po celkové anestezii se svalovou relaxací rokuroniem bez peroperačního monitorování relaxace. Při příjezdu na dospávací pokoj jsme stimulovali loketní nerv v režimu TOF (train-of-four) proudem submaximální intenzity (30 mA), evokovanou svalovou odpověď jsme vyhodnocovali akcelerometricky přístrojem TOF-Watch® SX (Organon). Pooperační reziduální kurarizace byla definována jako TOF-ratio < 0,9. Prokázali jsme ji u 174 nemocných (34 %). Ve srovnání se skupinou pacientů s adekvátním zotavením tito nemocní dostali peroperačně vyšší dávku rokuronia [45,4 (SD 13,2) mg vs. 40,4 (SD 14,3) mg, p < 0,01], byli častěji anestezováni méně zkušeným anesteziologem (p < 0,01), mezi poslední aplikací rokuronia a předáním na dospávací pokoj u nich uplynul kratší čas [58,4 (20,9) min. vs. 64,9 (27,2) min., p < 0,05], po operaci byli víc podchlazení [35,4 (0,6) °C vs. 35,8 (0,6) °C, p < 0,01] a peroperačně dostali v průměru méně neostigminu [0,26 (0,47 mg vs. 0,57 (0,71) mg, p < 0,01]. Pokud relaxaci peroperačně nemonitorujeme, doporučujeme rutinní dekurarizaci neostigminem.
Klíčová slova:
pooperační reziduální kurarizace – kurarimimetikum – rokuronium – dospávací pokojÚVOD
Základní metodou moderní anesteziologické péče je doplňovaná anestezie (balanced anaesthesia). Během ní se využívá několika druhů farmak, která víceméně selektivně působí na svou cílovou oblast (vyřazení vědomí, analgezie a svalová relaxace). Ve srovnání s monoanestezií tak látky mohou být podány v nižší dávce, která ovlivní během celkové anestezie právě tu modalitu, která je v daném okamžiku nedostatečně zabezpečena. Popsaný postup, jakkoli logický a racionální, je však spojen i s určitými riziky. Příkladem může být nekorektní použití svalových relaxancií, které vede ke dvěma obávaným aneste-ziologickým komplikacím. První z nich je nedostatečné vyřazení vědomí během operačního výkonu při částečné nebo úplné svalové relaxaci, druhou je pooperační reziduální kurarizace.
Pojmem pooperační reziduální kurarizace (PORC) označujeme přetrvávání svalové relaxace po ukončení celkové anestezie, kdy se svalová síla neobnoví na předoperační úroveň. Nemocný si tento stav nemusí uvědomovat, při závažnějším stupni PORC však pociťuje dechovou nouzi, nemůže pohybovat končetinami a často má diplopii z obrny okohybných svalů. Výraznou PORC lze prokázat klinickými testy (zvednutí a udržení hlavy po 5 s, silný a stálý stisk ruky po dobu 5 s, zvednutí a udržení končetiny nad podložku po 5 s) [1]. Mělčí stupeň reziduálního bloku je však možné odhalit pouze přístrojově – pomocí periferního nervového stimulátoru. Ten vytvoří přesně definovaný sled elektrických impulzů, kterými je přes kožní elektrody drážděn motorický nerv. Univerzálním stimulačním vzorcem je TOF (train-of-four), sestávající ze 4 po sobě jdoucích impulzů stejné intenzity v odstupu 0,5 s. Vyhodnocení pak spočívá ve sledování a kvantifikaci evokované svalové odpovědi, která se snižuje s hloubkou relaxace. Parametrem vhodným k detekci PORC je index TOF-ratio. Ten srovnává velikost 4. a 1. svalové odpovědí v režimu TOF a jeho pokles pod 1,0 odráží závažnost PORC. Podle současných znalostí je známkou dostatečného zotavení z účinku kurarimimetika dosažení TOF-ratio nad 0,90 [2, 3].
Rokuronium (ROC, Esmeron®, Organon) je moderní aminosteroidní kurarimimetikum s intermediární délkou účinku. Ze všech v současnosti používaných nedepolarizujících látek má nejrychlejší nástup účinku (60 s) a po jednorázové dávce 0,6 mg.kg-1 trvá klinický efekt přibližně 30 minut [4]. Jeho zotavovací charakteristiky vykazují obecné vlastnosti intermediárních svalových relaxancií, včetně rizika PORC [5].
Ve studii jsme zjišťovali výskyt této potenciálně nebezpečné komplikace na anesteziologických pracovištích univerzitní nemocnice.
METODY
Po schválení Etickou komisí LF UP Olomouc a získání informovaného souhlasu jsme na dospávacím pokoji prospektivně vyšetřovali nervosvalový přenos a stupeň případné PORC u všech nemocných, kteří v průběhu tří měsíců roku 2005 podstoupili plánovaný operační výkon v celkové anestezii se svalovou relaxací. Volba anestezie, výběr i množství peroperačně podaných látek byly ponechány plně v kompetenci příslušného anesteziologa. Ten o probíhající studii úmyslně nebyl informován, aby neměnil svůj obvyklý způsob anestezie ani indikaci podávání farmakologické dekurarizace. Nemocní hospitalizovaní pooperačně na dospávacím pokoji byli ošetřováni podle zavedených pravidel, včetně způsobu analgetizace.
Bezprostředně po příjezdu na dospávací pokoj jsme u každého nemocného změřili digitálně tělesnou teplotu (tympanickou a kožní) a standardizovanou metodikou vyšetřili nervosvalový přenos [TOF-Watch SX® (Organon), submaximální stimulace loketního nervu, akcelerometrické vyhodnocení TOF-ratio na m. adductor pollicis]. Podle této vstupní hodnoty TOF-ratio byli nemocní rozděleni do 3 skupin, které se lišily způsobem léčby případné PORC i počtem dalších měření NMT:
U nemocných 1. skupiny (vstupní TOF-ratio > 0,90) nebyla léčba PORC nutná (dekurarizace z operačního sálu byla dostatečná) a další měření nervosvalového přenosu jsme u nich neprováděli.
U nemocných 2. skupiny (vstupní TOF-ratio mezi 0,70 až 0,89) jsme bezprostředně po zjištění nízké hodnoty TOF-ratio aplikovali intravenózně 0,5 mg atropinu (Atropin, Hoechst-Biotika) a 1,0 mg neostigminu (Syntostigmin, Hoechst-Biotika). Kontrolní měření NMT jsme uskutečnili po 5 minutách od aplikace neostigminu (1. kontrola). Pokud takto zjištěná hodnota TOF-ratio přesáhla 0,90, v dalším průběhu jsme postupovali jako u nemocných 1. skupiny (bez dalších měření, bez dalšího podání neostigminu). Pokud 1. kontrolní měření TOF-ratio nedosáhlo nejméně 0,90, podali jsme opět 0,5 mg atropinu a 1,0 mg neostigminu s následnou kontrolou NMT po 5 minutách (2. kontrola). Tento postup jsme opakovali do celkové dávky 3,0 mg neostigminu.
U nemocných 3. skupiny (vstupní TOF-ratio < 0,70) jsme ihned aplikovali intravenózně 1,0 mg atropinu a 2,5 mg neostigminu. Pokud 1. kontrolní měření po 5 minutách ukázalo TOF-ratio opět pod 0,70, zopakovali jsme intravenózní aplikaci atropinu a neostigminu (1,0, resp. 2,5 mg) s 2. kontrolou TOF-ratio po dalších 5 dalších minutách. Pokud nedošlo k jeho úpravě nad 0,70, zvažovali jsme intubaci a přechodnou umělou plicní ventilaci. Pokud 1. kontrolní měření TOF-ratio leželo v pásmu 0,70 až 0,89, podali jsme intravenózně atropin 0,5 mg a neostigmin 1.0 mg. Jestliže 2. kontrolní vyšetření prokázalo TOF-ratio nad 0,90, postupovali jsme dále jako u nemocných 1. skupiny (bez dalších měření, bez dalšího podání neostigminu). Pokud 2. kontrolní vyšetření leželo opět v rozmezí 0,70 až 0,89, podali jsme intravenózně opět atropin 0,5 mg a neostigmin 1.0 mg. Tento postup jsme opakovali do celkové dávky 3,0 mg neostigminu.
U každého nemocného jsme zaznamenali následující údaje:
- Z anesteziologického dotazníku jsme zjistili demografická data nemocných – pohlaví, věk, hmotnost, výšku, klasifikaci podle ASA a vypočítali BMI (body mass index, [6]) a BSA (tělesný povrch, [6]).
- Z anesteziologického záznamu jsme zaznamenali typ anestezie. Poznačili jsme, zda anestezii vedl lékař se specializací I. nebo II. stupně, popřípadě lékař bez atestace. Podrobně jsme zachytili údaje se vztahem ke svalové relaxaci – použité kurarimimetikum, velikost a načasování dávky pro intubaci, velikost a načasování případných doplňujících dávek, celkovou dávku kurarimimetika, množství kurarimimetika přepočtené na tělesnou hmotnost, frekvenci, množství a čas případné aplikace neostigminu. Sledované časové údaje zahrnovaly délku anestezie (minuty), interval od ukončení anestezie do iniciálního měření NMT a interval mezi poslední aplikací kurarimimetika a iniciálním měřením NMT.
- Měřené parametry obsahovaly hodnoty TOF-ratio získané při vstupním a případných kontrolních měřeních, teplotu bubínku a kůže v místě měření.
STATISTICKÁ PODPORA
Ke zpracování dat a prezentaci výsledků jsme použili statistické softwarové balíky SPSS for Windows v. 14.0 (SPSS, Inc., USA), SigmaStat for Windows v. 3.5 (Systat, Inc., USA) a SigmaPlot for Windows v. 9.01 (Systat, Inc., USA). Pro analýzu byli nemocní podle výchozí hodnoty TOF-ratio rozděleni do dvou souborů:
Soubor A (odpovídá 1. skupině, úvodní TOF-ratio > 0,90) tvořili nemocní předávaní na dospávací pokoj bez reziduální kurarizace s adekvátním zotavením z nervosvalového bloku.
Soubor NON-A (odpovídá 2. a 3. skupině, úvodní TOF-ratio < 0,90) zahrnoval nemocné opouštějící operační sál s určitým stupněm reziduální kurarizace a tedy s nedostatečným zotavením z účinku kurarimimetik.
Získaná data jsme nejprve analyzovali, zda respektují normální rozložení (Kolmogorov-Smirnov). Podle toho jsme použili k jejich srovnám buď parametrický (Studentův t-test) nebo neparametrický test (Mann-Whitney). Rovněž kategorické údaje jsme porovnali příslušným testem (Fisherův test, chí-kvadrát).
Výsledky jsou uvedeny ve formátu průměr (směrodatná odchylka) nebo jako počty oddělené lomítky. Za statisticky významnou jsme považovali hodnotu p < 0,05, resp. p < 0,01.
VÝSLEDKY
Během tří měsíců roku 2005 bylo na dospávacím pokoji hospitalizováno 518 nemocných, kteří podstoupili operační výkon v celkové anestezii se svalovou relaxací. Naprostá většina nemocných byla relaxována rokuroniem, pouze u tří nemocných bylo ke svalovému uvolnění použito cis-atrakurium (Nimbex™, GlaxoSmithKline) a u dvou pacientů atrakurium (Tracrium™, GlaxoSmithKline). Tito nemocní byli vzhledem k malému počtu ze souboru vyřazeni. Hodnocený soubor tak tvořilo 513 nemocných, jimž bylo peroperačně podáno rokuronium.
U všech nemocných byla použita doplňovaná anestezie: Na indukci propofolem, thiopentalem nebo etomidatem navazovalo vedení anestezie izofluranem nebo sevofluranem ve směsi s oxidem dusným nebo vzduchem, analgetická složka byla zajištěna podáním sufentanilu nebo alfentanilu, svalová relaxace výhradně rokuroniem (úvodní intubační dávka ± doplňující dávky) bez použití suxametonia.
Nervosvalový přenos nebyl u žádného nemocného během operace monitorován přístrojově, svalová relaxace byla posuzována pouze na základě klinických kriterií. Všichni nemocní byli extubováni na operačním sále v okamžiku, kdy příslušný anesteziolog považoval jejich dekurarizaci (spontánní nebo farmakologickou) za dostatečnou.
Skupiny A a NON-A se nelišily v demografických údajích nemocných (Tab. 1) kromě BMI, který byl vyšší ve skupině NON-A (p < 0,01).
Tab. 1. Demografické údaje nemocných s adekvátním (soubor A) vs. nedostatečným (soubor NON-A) zotavením z účinku rokuronia Tab. 1. Demographic data from patients with adequate (group A) and insufficient (group NON-A) recovery from rocuronium effects 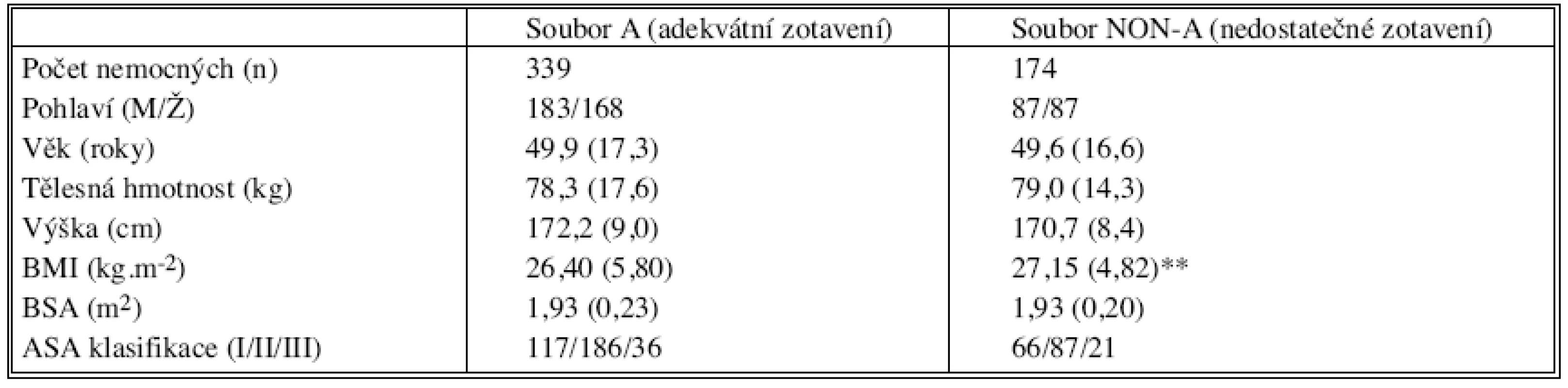
Data jsou ve formátu průměr (SD) nebo počty oddělené lomítkem, **p < 0,01 BMI (body mass index) [6] = hmotnost [kg]/ (výška [m])2 BSA (body surface area) [6] = hmotnost [kg]. výška [cm]/3600 Nedostatečné zotavení z účinku rokuronia (TOF-ratio < 0,90) jsme na dospávacím pokoji zjistili u 174 nemocných (34 % z celkového počtu) – viz tabulka 1. Méně závažný stupeň PORC (TOF-ratio mezi 0,70 a 0,89) jsme diagnostikovali u 135 pacientů (26 %) a výraznou PORC (TOF-ratio < 0,70) u 39 nemocných (8 %). Nemocní skupiny NON-A měli vyšší BMI (p < 0,01), byli častěji anestezováni méně zkušenými lékaři s nižší kvalifikací (p < 0,01), při příjezdu na dospávací pokoj měli nižší centrální teplotu (p < 0,01) a během operace dostali vyšší dávku rokuronia celkovou i v přepočtu na tělesnou hmotnost (p < 0,01). Interval mezi poslední aplikací rokuronia a příjezdem na dospávací pokoj (a tím i iniciálním měřením TOF-ratio) byl kratší ve skupině NON-A (p < 0,01). Nemocní skupiny A dostali na operačním sále více neostigminu (p < 0,01) (Tab. 2.)
Tab. 2. Klinické údaje nemocných s adekvátním (soubor A) vs nedostatečným (soubor NON-A) zotavením z účinku rokuronia Tab. 2. Clinical data from patients with adequate (group A) and insufficient (group NON-A) recovery from rocuronium effects 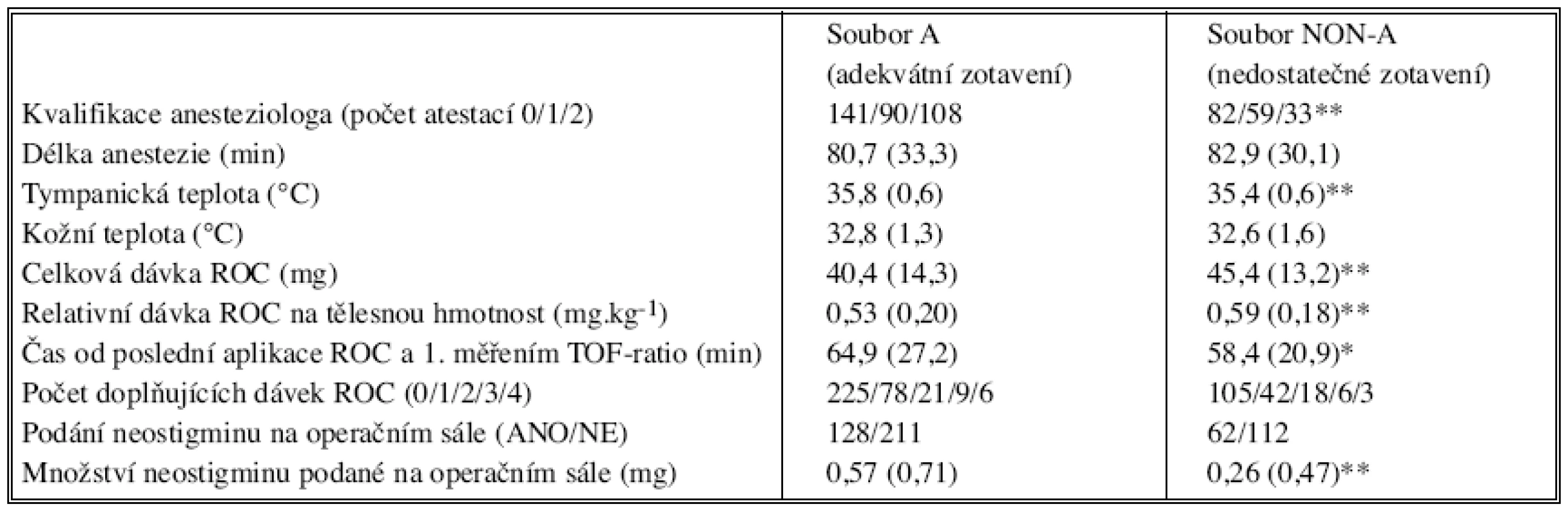
ROC rokuronium, BSA body surface area, BMI body mass index Data jsou ve formátu průměr (SD) nebo počty oddělené lomítkem, *p < 0,05, **p < 0,01 DISKUSE
Motivace
Téma pooperační reziduální kurarizace je v zahraniční anesteziologické literatuře častým námětem [např. 7–11]. Proč jsme se rozhodli ke zpracování této problematiky?
- Prvním impulzem bylo na našem pracovišti všeobecně rozšířené mínění, že se nás tento problém netýká a pokud se tato komplikace vyskytne, jde o jev zcela nezávažný bez vlivu na morbiditu operovaných nemocných.
- Druhým motivem pro zveřejnění našich zkušeností se stal názor většiny anesteziologů, kteří považují kurarimimetika s intermediální délkou účinku za látky bezpečné, u nichž se reziduální kurarizace nevyskytuje, a proto není nutno jejich efekt na konci operace antagonizovat neostigminem. Podle přesvědčení většiny anesteziologů potíže s reziduální kurarizací, tak časté při použití dlouhodobě účinných relaxancií, byly odstraněny právě zavedením moderních látek s intermediární délkou účinku.
- Poslední pohnutkou pro naše sdělení byl článek profesora Pafka „Chirurg jako vysokoškolský učitel a věda“ uveřejněný v Rozhledech v chirurgii [12]. Podle něho je z bibliometrického hlediska pro autora cennější publikace v zahraničním časopise, pokud možno impaktovaném. Praktický dopad pro naši lékařskou obec je však daleko mohutnější, pokud je práce zveřejněna česky a v České republice dobře dostupném a uznávaném lékařském periodiku. Tím „Rozhledy v chirurgii“ bezesporu jsou.
PORC v kontextu medicíny založené na důkazech (evidence-based medicíně) [1]
Varování před nesprávným používáním kurarimimetik následovalo brzy po jejich klinickém použití [13]. Zpřesnění informací o PORC a uvedení nových látek na trh změnilo i postoj k PORC. Před více než čtvrt stoletím Viby-Mogensen zveřejnil alarmující údaj z kodaňské univerzitní nemocnice [14]. Podle něho 42 % nemocných předávaných ze sálu na pooperační pokoj vykazovalo závažný stupeň PORC (TOF-ratio pod 0,70) a 24 % nebylo schopno udržet hlavu nad položkou po dobu 5 sec. Tyto údaje byly později provedenými studiemi v jiných zemích potvrzeny [7, 15, 16]. Zároveň však prokázaly, že na rozdíl od pankuronia (dlouhodobě účinná látka) použití kurarimimetik s intermediární délkou účinku (atrakurium, vekuronium) snížilo výskyt PORC pod 10 %. Tato skutečnost společně s pozdějším zjištěním, že reziduální blok představuje reálnou hrozbu pro nemocného [17], vedla k postupnému ústupu od používání dlouhodobě účinných kurarimimetik. Mnoho anesteziologů tím považovalo problém s PORC za vyřešený.
Není pochyb o tom, že četnost i závažnost PORC poklesla s širším používání intermediálních látek. Recentní studie [9, 10, 11, 18, 19] však dokumentují stále nepřijatelně vysoký výskyt PORC i přes aplikaci relaxancií s intermediární délkou účinku. Zajisté to souvisí i s faktem, že bylo zpřísněno kritérium dostatečné dekurarizace [2, 3, 20]. Podle něho by TOF-ratio na konci anestezie mělo přesáhnout 0,9. Při nižších hodnotách totiž dochází ke snížení reaktivity chemoreceptorů na hypoxii a dyskoordinaci svalů hltanu a horního jícnu s následnými mikroaspiracemi. Ty mají za následek zvýšení výskytu pooperačních plicních komplikací, a tím i nárůst morbidity operovaných nemocných [17].
Naše studie potvrzuje potřebu adekvátně antagonizovat účinek rokuronia i přesto, že je považováno za látku s intermediární délkou účinku [21]. Rovněž z ní vyplývá nutnost monitorovat nervosvalový přenos, pokud se chceme na konci anestezie vyhnout aplikaci neostigminu, např. u astmatiků nebo kardiálně limitovaných nemocných [22].
Standardní adekvátní dávka neostigminu je 0,04 mg.kg-1. V tomto množství nezvyšuje incidenci PONV (postoperative nausea and vomiting) [23], ani neohrožuje pevnost střevní anastomózy zvýšením motility. V dávkování i indikaci dekurarizace však existují značné rozdíly mezi evropskými státy. Nejvyšší dávky neostigminu podávají britští anesteziologové, kteří ho rovněž velmi často aplikují paušálně po každém podání nedepolarizujícího kurarimimetika. Naopak rezervovanější postoj k rutinní dekurarizaci je zřetelný v německé a francouzské anesteziologické praxi [24]. V České republice je situace v tomto ohledu někde mezi oběma názory [25] – neostigmin podává rutinně 16 % našich anesteziologických pracovišť, většina oddělení pak podle klinických známek na konci operace. Žádné české pracoviště nemonitoruje nervosvalový přenos jako součást standardní anesteziologické péče. Přicházíme tak o možnost snížit incidenci PORC i možnost aplikovat neostigmin výběrově pouze tam, kde je to nutné podle naměřených hodnot.
Intenzitu svalové relaxace ovlivňuje během anestezie mnoho faktorů. Dobře známé je jak prohloubení, tak i prodloužení bloku při poklesu tělesné teploty [26]. V naší studii pokles centrální teploty představoval významný rizikový faktor pro výskyt PORC.
Přístrojové monitorování nervosvalového přenosu je u nás výjimkou. Podle odpovědí přednostů českých anesteziologických oddělení, získaných dotazníkovou studií [25], jsou hlavní příčinou absence monitorování ekonomické důvody (62 %). Zřejmá je však i skutečnost, že 25 % našich primářů nepovažuje měření hloubky relaxace za potřebné. Tento údaj je ve shodě s údaji získanými v zahraničí. Podle dánských zkušeností [27] 91 % anesteziologů podceňuje výskyt PORC po aplikaci intermediárních kurarimimetik a 27 % se nesprávně domnívá, že PORC lze vždy odhalit klinickými testy. Pouze 45 % dánských anesteziologů vědělo, že pro vyloučení PORC musí TOF-ratio dosáhnout na konci anestezie 0,90. Přitom 91 % z nich má k dispozici periferní nervový stimulátor, u 85 % i s možností objektivního vyhodnocení evokované svalové odpovědi. Tato čísla dokazují, že i přes dostupnost přístrojového vybavení v Dánsku je hlavní příčina nedostatečného monitorování svalové relaxace jiná. Je jí nedostatek znalostí, spíše než omezené finanční zdroje pro nákup hardware [27].
Ve FN Olomouc jsou na dospávací pokoj krátkodobě přijímáni nemocní, kteří podstoupili méně závažný operační výkon. Po uplynutí přibližně 2 hodin jsou při stabilizovaném stavu předáváni na standardní oddělení příslušné kliniky. Použití svalových relaxancií je doménou anesteziologů. Jistě však není od věci, pokud chirurg ví, že i po méně závažném operačním výkonu může být morbidita operovaných nemocných v důsledku anestezie vyšší než jako následek vlastního chirurgického postupu.
ZÁVĚR
Podle vlastních zkušeností i dostupného písemnictví doporučujeme v našich podmínkách pro bezpečnou aplikaci kurarimimetik následující postup:
- Pokud je dostupný přístroj pro měření nervosvalového přenosu, použijeme ho vždy při aplikaci nedepolarizujícího kurarimimetika. Opomenutí měřit hloubku nervosvalového bloku (obzvláště máme-li k dispozici přístrojové vybavení) představuje v tomto případě substandardní péči a hraničí s postupem non lege artis [27].
- Pokud lze, preferujeme stimulátor s kvantitativním vyhodnocením svalové odpovědi před jednoduššími přístroji, které jsou schopny pouze generovat stimulační proud. U nich evokovaná svalová odpověď není měřena, ale pouze odhadována na základě subjektivního palpačního nebo vizuálního vjemu anesteziologa.
- Ke svalové relaxaci preferujeme moderní látky s intermediární délkou účinku (rokuronium, cis-atrakurium).
- Při anestezii je nutné podávat kurarimimetika uváženě. Při volbě jejich dávky a načasování musíme vždy zvážit poměr mezi prospěchem (zlepšením operačních podmínek) a rizikem (PORC). Kurarimimetikum by mělo učinit nemožné možným, ne obtížné snadným.
- Pokud nemáme přístroj pro vyhodnocení hloubky svalové relaxace, je vhodné zvážit na konci anestezie farmakologickou dekurarizaci podáním adekvátní dávky neostigminu i po aplikaci intermediárních látek. Standardní doporučené množství představuje atropin v dávce 1,0 mg (popř. glykopyrolát 0,2–0,4 mg) a neostigmin 2,5 mg.
- Při anestezii je nezbytné pečovat o tepelnou pohodu nemocného a pečlivě zvažovat velikost dávky zvláště u obézních nemocných. U nich je bezpečnější vztáhnout potřebné množství relaxancia ne na skutečnou, ale na libovou hmotnost.
Poděkování
Autoři děkují Prof. MUDr. Vladimíru Královi, CSc., emeritnímu přednostovi I. chirurgické kliniky FN a LF UP Olomouc, za cenné připomínky a pečlivou revizi textu.
Dík patří rovněž úsekové sestře dospávacího pokoje KAR FN Olomouc Dagmar Žáčkové za pomoc při realizaci studie.
MUDr. M. Adamus, Ph.D.
Kaštanová 11
772 00 Olomouc
e-mail: milan.adamus@seznam.cz
Zdroje
1. Viby-Mogensen, J. Postoperative residual curarization and evidence-based anaesthesia. British Journal of Anaesthesia, 2000, roč. 84, č. 3, s. 301–303.
2. Eriksson, L. I., Lennmarken, C., Wyon, N., Johnson, A. Attenuated ventilatory response to hypoxaemia at vecuronium-induced partial neuromuscular block. Acta Anaesthesiologica Scandinavica, 1992, roč. 36, č. 7, s. 710–715.
3. Eriksson, L. I., Sundman, E., Olsson, R. et al. Functional assessment of the pharynx at rest and during swallowing in partially paralyzed humans: simultaneous videomanometry and mechanomyography of awake human volunteers. Anesthesiology, 1997, roč. 87, č. 5, s. 1029–1031.
4. Adamus, M., Adamus, P., Bělohlávek, R., Vujčíková, M., Janásková, E. Vliv odlišných dávek rokuronia na jeho farmakodynamický profil: prospektivní studie. Anesteziologie a intenzivní medicína, 2004, roč. 15, č. 6, s. 269–275.
5. Cammu, G., De Baerdemaeker, L., Den Blauwen, N., De Mey, J. C., Struys, M., Mortier, E. Postoperative residual curarization with cisatracurium and rocuronium infusions. European Journal of Anaesthesiology, 2002, roč. 19, č. 2, s. 129–134.
6. References and formulas ušed by the Body Surface Area Calculator. Formula for Body Mass Index [on line] [citováno 12. července 2006] Dostupný z WWW <http://www.halls.md/body-surface-area/refs.htm>
7. Beemer, G. H., Rozental, P. Postoperative neuromuscular function. Anaesthesia and intensive care, 1986, roč. 14, č. 1, s. 41–45.
8. Cammu, G. Postoperative residual curarisation: complication or malpractice? Acta Anaesthesiologica Belgica, 2004, roč. 55, č. 3, s. 245–249.
9. Baillard, C., Clec, H. C., Catineau, J., Salhi, F., Gehan, G., Cupa, M., Samama, C. M. Postoperative residual neuromuscular block: a survey of management. British Journal of Anaesthesia, 2005, roč. 95, č. 5, s. 622–626.
10. Cammu, G., De Witte, J., De Veylder, J., Byttebier, G., van de Put, D., Foubert, L., van den Broucke, G., Deloof, T. Postoperative residual paralysis in outpatients versus inpatients. Anesthesia and Analgesia, 2006, roč. 102, č. 2, s. 426–429.
11. Murphy, G. S. Residual neuromuscular blockade: incidence, assessment, and relevance in the postoperative period. Minerva Anestesiologica, 2006, roč. 72, č. 3, s. 97–109.
12. Pafko, P. Chirurg jako vysokoškolský učitel a věda. Rozhledy v chirurgii, 2004, roč. 83, č. 12, s. 607–608.
13. Beecher, H. K., Todd, D. P. A study of the deaths associated with anesthesia and surgery: based on a study of 599, 548 anesthesias in ten institutions 1948–1952, inclusive. Annals of surgery, 1954, roč. 140, č. 1, s. 2–35.
14. Viby-Mogensen, J., Jorgensen, B. C., Ording, M. Residual curarization in the recovery room. Anesthesiology, 1979, roč. 50, č. 6, s. 539-541.
15. Andersen, B. N., Madsen, J. V., Schurizek, B. A., Juhl, B. Residual curarization: a comparative study of atracurium and pancuronium. Acta Anaesthesiologica Scandinavica, 1988, roč. 32, č. 2, s. 79–81.
16. Bevan, D. R., Smith, C. E., Donati, F. Postoperative neuromuscular blockade: a comparison between atracurium, vecuronium and pancuronium. Anestesiology, 1988, roč. 69, č. 2, s. 272–276.
17. Berg, H., Roed, J., Viby-Mogensen, J., Mortensen, C. R., Engbaek, J., Skovgaard, L. T., Krintel, J. J. Residual neuromuscular block is a risk factor for postoperative pulmonary complications. A prospective, randomised, and blinded study of postoperative pulmonary complications after atracurium, vecuronium and pancuronium. Acta Anaesthesiologica Scandinavica, 1997, roč. 41, č. 9, s. 1095–1103.
18. Baillard, C., Gehan, G., Reboul-Marty, J., Larmignat, P., Samama, C. M., Cupa, M. Residual curarization in the recovery room after vecuronium. British Journal of Anaesthesia, 2000, roč. 84, č. 3, s. 394–395.
19. McCaul, C., Tobin, E., Boylan, J. F., McShane, A. J. Atracurium is associated with postoperative residual curarization. British Journal of Anaesthesia, 2002, roč. 89, č. 5, s. 766–769.
20. Kopman, A. F., Yee, P. S., Neuman, G. G. Relationship of the train-of-four fade ratio to clinical signs and symptoms of residual paralysis in awake volunteers. Anesthesiology, 1997, roč. 86, č. 4, s. 765–771.
21. Bevan D. Reversal of neuromuscular block: the case FOR reversal. Acta Anaesthesiologica Scandinavica Suppl, 1997, roč. 41, č. 110, s. 102.
22. Mortensen, C. R., Berg, H., El-Mahdy, A., Viby-Mogensen, J. Perioperative monitoring of neuromuscular transmission using acceleromyography prevents residual neuromuscular block following pancuronium. Acta Anaesthesiologica Scandinavica, 1995, roč. 39, č. 6, s. 797–801.
23. Cheng, C. R., Sessler, D. I., Apfel, C. C. Does neostigmine administration produce a clinically important increase in postoperative nausea and vomiting? Anesthesia and analgesia, 2005, roč. 101, č. 5, s. 1349–1355.
24. Osmer, C., Vogele, C., Zickmann, B., Hempelmann, G. Comparative use of muscle relaxants and their reversal in three European countries: a survey in France, Germany and Great Britain. European Journal of Anaesthesiology, 1996, roč. 13, č. 4, s. 389–399.
25. Adamus, M., Marek, O. Monitorování účinku kurarimimetik během anestezie - současný stav v České republice. Anesteziologie a neodkladná péče, 2000, roč. 11, č. 6, s. 245–250.
26. Heier, T., Caldwell, J. E. Impact of hypothermia on the response to neuromuscular blocking drugs. Anesthesiology, 2006, roč. 104, č. 5, s. 1070–1080.
27. Sorgenfrei, I. F., Viby-Mogensen, J., Swiatek, F. A. Does evidence lead to a change in clinical practice? Danish anaesthetists‘ and nurse anesthetists‘ clinical practice and knowledge of postoperative residual curarization. Ugeskrift for laeger, 2005, roč. 167, č. 41, s. 3878–3882.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek Eutanazie
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2007 Číslo 1- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Jak souvisí postcovidový syndrom s poškozením mozku?
- Hojení análních fisur urychlí čípky a gel
-
Všechny články tohoto čísla
- Výskyt pooperační reziduální kurarizace na dospávacím pokoji po aplikaci rokuronia
- Insuficience anastomóz u resekcí sigmoidea a rekta. Retrospektivní studie na chirurgické klinice v Hradci Králové
- Peutz-Jeghersov syndróm – kazuistika
- Hemangiomy jater – strategie diagnostiky a léčby
- Jak si má chirurg udržet vedoucí postavení při mezioborové spolupráci v medicíně
- Vzpomínka na doc. MUDr. Milana Schücka, CSc.
- Laparoskopická korekce posttraumatického uterovaginálního sestupu s prolapsem rekta
- Mnohočetná divertikulóza tenkého a tlustého střeva. Kazuistika
- Role CT v indikaci laparotomie u tupých úrazů břicha: porovnání CT závěrů a operačních nálezů v souboru 101 pacientů
- Resekce subrenální aorty u disekcí hrudní aorty technikou aortální fenestrace
- Nepoznané zadní luxace ramenního kloubu. Předběžné sdělení
- Eutanazie
- Chirurg a informovaný souhlas
- Zápis z jednání schůze výboru ČCHS dne 14. 12. 2006.
- Zápis z Valné hromady České chirurgické společnosti ČLS JEP 15. 12. 2006, Aula, Ústřední vojenská nemocnice Praha
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Hemangiomy jater – strategie diagnostiky a léčby
- Nepoznané zadní luxace ramenního kloubu. Předběžné sdělení
- Mnohočetná divertikulóza tenkého a tlustého střeva. Kazuistika
- Insuficience anastomóz u resekcí sigmoidea a rekta. Retrospektivní studie na chirurgické klinice v Hradci Králové
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



