-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Waldenströmova makroglobulinemie
Waldenström macroglobulinemia
Background: Waldenström macroglobulinemia (WM) is a hematological malignancy; it is a monoclonal gammopathy, a disease characterized by presence of a monoclonal immunoglobulin in serum and/or urine. The median age at diagnosis is 71 years. WM is not an aggressive disease and patients with this diagnosis can live for several years. Infiltration of the bone marrow with lymphoplasmacytoid cells causes anemia, leading to various problems, mainly fatigue. Hepatomegaly, splenomegaly and lymphadenopathy can also occur. Hyperviscosity syndrome can appear and is caused by excessive production of immunoglobulin M. A mutation in MYD88 gene is detected in almost every WM patient, and in almost one third of them, a mutation in CXCR4 gene is detected. The detection of MYD88 mutation is important for a correct therapeutic strategy, since a Bruton’s tyrosine kinase inhibitor, ibrutinib, is most effective in patients with mutated MYD88 and wt CXCR4. The therapy is started when first symptoms occur. Purpose: The aim of this study is to summarize current knowledge about this disease, its diagnostics, molecular basis and treatment.
Keywords:
incidence – Mutation – Prognosis – mikroRNA – Waldenström macroglobulinemia
Autoři: K. Baďurová 1; J. Gregorová 1; M. Vlachová 1; M. Krejčí 2; S. Ševčíková 1
Působiště autorů: Babákova myelomová skupina, Ústav patologické fyziologie, LF MU Brno 1; Interní hematologická a onkologická klinika LF MU a FN Brno 2
Vyšlo v časopise: Klin Onkol 2021; 34(6): 428-433
Kategorie: Přehled
doi: https://doi.org/10.48095/ccko2021428Souhrn
Východiska: Waldenströmova makroglobulinemie (WM) je hematoonkologické onemocnění patřící mezi monoklonální gamapatie – onemocnění, která jsou charakterizovaná přítomností monoklonálního imunoglobulinu v séru a/nebo v moči. Medián věku při diagnóze je 71 let. WM není agresivní onemocnění a pacienti s touto diagnózou přežívají několik let. Infiltrace kostní dřeně lymfoplazmocytárními buňkami způsobuje různé obtíže vyplývající z anemického syndromu, zejména únavu. Dále se objevuje hepatomegalie, splenomegalie a lymfadenopatie. Může se vyskytovat hyperviskózní syndrom způsobený nadměrnou produkcí monoklonálního imunoglobulinu třídy M. U pacientů s WM je téměř vždy detekovatelná mutace v genu MYD88 a u přibližně třetiny pacientů mutace v genu pro CXCR4. Detekce mutace MYD88 je podstatná pro volbu vhodné terapeutické strategie, protože inhibitor Brutonovy tyrozinkinázy ibrutinib má největší účinek u pacientů s mutovaným MYD88 a wt CXCR4. Léčba je zahájena až při výskytu prvních příznaků. Cíl: Cílem práce je shrnout současné znalosti o tomto onemocnění, jeho diagnostiku, molekulární podstatu a léčbu.
Klíčová slova:
incidence – mutace – prognóza – mikroRNA – Waldenströmova makroglobulinémie
Úvod
Waldenströmova makroglobulinemie (WM) patří do vzácné podskupiny indolentních B buněčných lymfomů. Řadí se mezi monoklonální gamapatie, což je skupina onemocnění, při kterých je monoklonální imunoglobulin nebo jeho fragment produkován klonálními B lymfocyty. Vyznačuje se přítomností monoklonálních imunoglobulinů třídy M (IgM) v séru a alespoň 10 % monoklonálních lymfoplazmocytárních buněk v kostní dřeni [1,2]. U 4,3 % případů byl potvrzen výskyt lymfoplazmocytárního lymfomu nebo WM v rodině pacienta, zároveň je rodinný výskyt spojen s horší prognózou, na rozdíl od případů, kde se tato onemocnění v rodině nevyskytují [3].
Historie WM
Své jméno dostala WM podle prof. Waldenströma. Jan Gösta Waldenström (17. 4. 1906 – 1. 12. 1996) byl profesorem teoretické medicíny na univerzitě v Uppsale, profesorem praktické medicíny na univerzitě v Lundu a vedoucím lékařem ve Všeobecné nemocnici v Malmö. Během své dlouhé kariéry objasnil základy několika onemocnění, např. porfyrie, hemosiderózy, makroglobulinemie a monoklonální gamapatie. Poté, co získal lékařský titul na univerzitě v Uppsale, studoval organickou chemii v laboratoři Hanse Fishera v Technische Hochschule v Mnichově. Toto studium vedlo k monografii s názvem „Studien Über Porphyrie“. Po návratu na univerzitu v Uppsale studoval nemoci spojené se zvýšenou sedimentací erytrocytů [4]. V průběhu let se podílel na popsání dalších chorob – chronické aktivní hepatitidy, pulmonární hemosiderózy, Waldenströmovy benigní hypergamaglobulinemické purpury a dalších [4,5].
Jeho nejvýznačnějším přínosem je však bezesporu popis makroglobulinemie. Roku 1944 popsal dva pacienty s oronazálním krvácením, lymfadenopatií, normochromní anemií, zvýšenou sedimentací erytrocytů, trombocytopenií, hypoalbuminemií, nízkou hladinou fibrinogenu v séru a zvýšeným počtem lymfoidních buněk v kostní dřeni [6]. Také u nich pozoroval prodlouženou dobu krvácení po biopsii lymfatické uzliny a krvácení sítnice. Tento stav uváděl do kontrastu s mnohočetným myelomem, protože RTG vyšetření kostí bylo v normálu a nevyskytovala se ani bolest kostí. Hlavním poznatkem byl výskyt hyperglobulinemie, kdy pozoroval velké množství homogenního globulinu s vysokou molekulární hmotností. Dle jeho hypotézy nepřítomnost postižení kostí odlišuje makroglobulinemii od mnohočetného myelomu.
Další studie potvrdily Waldenströmovy poznatky o morfologii a bylo potvrzeno, že nádorové buňky u makroglobulinemie patří do vývojové řady plazmatických buněk, avšak ranějších stadií než u mnohočetného myelomu. Roku 1961 představil profesor Waldenström koncept monoklonálních a polyklonálních gamapatií. Pacienty patřící do těchto skupin dělil na ty s mnohočetným myelomem a s „esenciální hypergamaglobulinemií“ nebo s benigní monoklonální gamapatií – dnes známo jako monoklonální gamapatie nejasného významu (monoclonal gamapathy of undetermined significance – MGUS) [4].
Klinické příznaky Waldenströmovy makroglobulinemie
K nejčastějším obtížím u WM patří únava spojená s normocytární anemií [7]. Mezi poměrně časté projevy patří také hepatomegalie (20 % pacientů), splenomegalie (15 % pacientů) nebo i lymfadenopatie (15 % pacientů) [8]. Monoklonální IgM může způsobit hyperviskózní syndrom, periferní neuropatii nebo i hemolytickou anemii [9–11]. Ne každý pacient s diagnózou WM vyžaduje léčbu, pacienti jsou pouze sledováni, dokud se neprojeví symptomy. S léčbou se začíná při počátečních příznacích a u mladších jedinců je možná i transplantace kostní dřeně [12,13].
Diagnostika a epidemiologie
Ve většině případů je pacientům nejdříve diagnostikován IgM MGUS [14]. Samotná diagnóza IgM MGUS je nejvýznamnějším rizikovým faktorem vzniku WM s pravděpodobností progrese 1–2 % případů za rok [15]. WM tvoří 1–2 % hematoonkologických onemocnění a ročně postihuje 3,8/1 000 000 osob (USA) [1]. Incidence v ČR zatím není známa [16]. WM je onemocnění starších lidí, průměrný věk při diagnóze je 71 let. S vyšším věkem se zkracuje možná délka přežití pacienta [17,18]. Tito pacienti mají vyšší riziko vývoje dalšího maligního onemocnění oproti zdravým jedincům. Mezi časté malignity u pacientů s WM patří difuzní velkobuněčný B lymfom, myelodysplastický syndrom a mozkové nádory [12].
Pro diagnostiku WM je nutná detekce monoklonálního IgM v séru a přítomnost abnormální populace lymfoplazmocytárních buněk, která je zodpovědná za produkci onoho monoklonálního IgM. Pro diagnózu WM musí množství těchto lymfoplazmocytárních buněk překročit hranici 10 % [19]. U většiny pacientů s podezřením na WM je prováděno množství testů zahrnujících krevní diferenciál, stanovení funkce jater a ledvin, CT vyšetření, kvantitativní stanovení imunoglobulinů a detekci imunoglobulinu v moči. V současné době se provádí také detekce mutace MYD88 L265P, která je detekovatelná u > 90 % pacientů s WM [18–20].
Molekulární podstata Waldenströmovy makroglobulinemie
Mutace v genu MYD88
MYD88 (primární odpověď myeloidní diferenciace 88) je adaptorový protein, který interaguje s toll-like a interleukinovými (IL-1) receptory a po receptorové aktivaci dimerizuje. Dimerizace MYD88 poskytuje lešení pro přijímání dalších proteinů do myddozomového komplexu, který spouští signalizaci vedoucí k aktivaci jaderného faktoru-kB (nuclear factor-kB – NF-kB) [21]. Mezi součásti myddozomového komplexu spouštějící aktivaci NF-kB patří také kináza spojená s receptorem interleukinu 1 nebo 4 (interleukin 1 / interleukin-4 associated kinase – IRAK1/IRAK4) a Brutonova tyrozinkináza (BTK) [22]. Příjem a aktivace molekul IRAK a BTK může být blokována potlačením funkce nebo inhibicí MYD88, což vede k apoptóze MYD88 mutovaných WM buněk. Mutovaný MYD88 může také zapříčinit zvýšení transkripce tyrozinové proteinkinázy HCK (kináza rodiny SRC – nereceptorové tyrozinkinázy) a může aktivovat HCK přes IL-6. Aktivovaná HCK spouští signalizaci podporující přežití MYD88 mutovaných WM buněk přes BTK, fosfatidylinositol-3-kinázu / proteinkinázu B (0PI3K/AKT) a mitogenem aktivovanou proteinkinázu / extracelulárním signálem regulovanou kinázu (MAPK/ERK1/2) [23]. Tyrozinová proteinkináza SYK, součást dráhy B-buněčného receptoru (B-cell receptor – BCR), je přítomna ve své aktivní formě v myddozomu, jehož aktivace je spouštěna mutovaným MYD88. Takto aktivovaná SYK spouští převodník signálu a aktivátor transkripce 3 (STAT3) a AKT signalizaci podporující přežití, což značí možné využití inhibitorů SYK v léčbě WM [24]. Mutovaný MYD88 tedy může řídit několik kaskád podporujících přežití WM buňky, které vedou k aktivaci NF-kB, AKT, ERK a STAT3 [25] (obr. 1).
Obr. 1. Signální dráha podporující přežití buňky zprostředkovaná mutovaným MYD88. 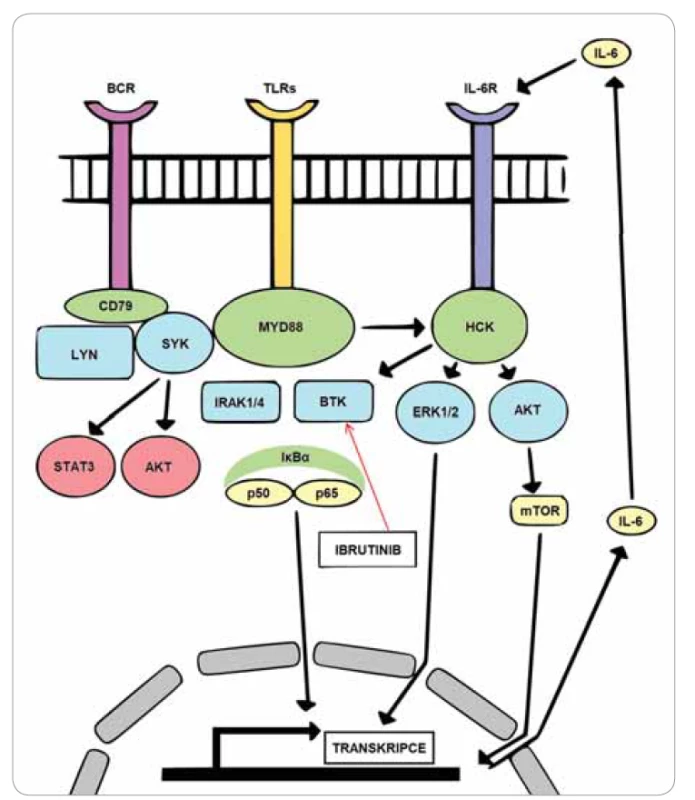
U 93–97 % pacientů s WM je detekována mutace MYD88 L265P jak ve vybraných B buňkách, tak i v plazmatických buňkách, které tvoří maligní klony při WM [26,27]. Také byly odhaleny non-L265P MYD88 mutace, avšak jejich exprese se vyskytuje u 1–2 % pacientů s WM. Mutace v MYD88 byla detekována u pacientů s IgM MGUS, nikoli však u pacientů s IgA nebo IgG MGUS, což poukazuje na časnou onkogenní roli MYD88 v patogenezi WM. Pacienti s IgM MGUS, u kterých je nalezena mutace MYD88, mají vyšší riziko progrese WM [23,26,27].
Mutace v genu CXCR4
C-X-C chemokinový receptor typu 4 (CXCR4) je G-proteinový párový receptor, který spolu se svým ligandem CXCL12/SDF-1 (faktor 1 odvozený ze stromálních buněk, chemokin 12) hraje důležitou roli v lymfopoéze [28]. Dráha SDF1/CXCR4 vyvolává aktivaci několika drah vč. RAS, AKT a NF-kB a interaguje s dráhou BCR [28–30]. Somatické mutace zahrnující C-terminální doménu CXCR4 jsou přítomny přibližně u 30–40 % pacientů s WM, z toho mutace CXCR4 C1013G je nejčastější a objevuje se u 7 % pacientů. Téměř vždy se vyskytují současně s mutacemi MYD88, avšak někteří pacienti s wt MYD88 mají také mutaci v CXCR4 [28,31]. Mutace v CXCR4 jsou přítomny převážně u WM, ačkoli objevily se i případy lymfomu z marginální zóny a difuzního velkobuněčného B lymfomu s mutací v tomto genu.
U WM bylo popsáno > 40 „nonsense“ mutací a mutací posouvajících čtecí rámec C-terminální domény CXCR4 [28,32]. Mutace v C-terminální doméně CXCR4 vedou ke ztrátě regulačních serinů a podporují nepřetržitou aktivaci drah AKT a ERK řízenou CXCL12, což se v in vivo pokusech na myších projevuje progresí a diseminací WM [23,33,34]. Navzdory autonomní signalizaci podporující přežití buňky spojené s mutací CXCR4 inhibice MYD88 způsobuje apoptózu WM buněk s wt CXCR4 i s mutovaným CXCR4, což odpovídá hypotéze, že mutace MYD88 má primární roli v signalizaci podporující přežití WM buněk [23]. Na rozdíl od mutace v MYD88 je mutace v CXCR4 subklonální povahy, i u jednoho pacienta je možné nalézt různé mutace v CXCR4 v jednotlivých klonálních buňkách WM. Tyto poznatky spolu s nízkým výskytem mutace CXCR4 u IgM MGUS naznačují, že k mutaci CXCR4 dochází až po mutaci MYD88 [35].
Exprese mikroRNA spojená s Waldenströmovou makroglobulinemií
MikroRNA (miRNA) jsou krátké (19–22 nukleotidů) endogenní nekódující molekuly RNA, které fungují jako negativní regulátory eukaryotické genové exprese [36]. K této regulaci dochází posttranskripčně prostřednictvím navázání miRNA na 3’ nepřepisované oblasti cílových transkriptů [37]. MiRNA má zásadní roli v kontrole důležitých biologických procesů, jako jsou proliferace, apoptóza, buněčná signalizace a metabolizmus [38,39]. Exprese specifických miRNA je spolu s vnějšími podněty z buněčného mikroprostředí a dalšími vnitřními podněty klíčová při diferenciaci hematopoetických buněk [39,40].
U WM byla zatím popsána dysregulace sedmi miRNA, kterými lze WM odlišit od zdravých jedinců. Těmito miRNA jsou miR-363, miR-206, miR-494, miR-155, miR-184 a miR-542-3p, jejichž exprese je zvýšená, a miR-9, jejíž exprese je naopak snížená. Expresi miRNA u WM může také ovlivnit léčba, jelikož byli pozorováni pacienti, u kterých se snížením infiltrace kostní dřeně došlo také k změně profilu exprese miRNA, který se podobal spíše zdravým buňkám [39,41].
MiRNA může být transportována z buněk pomocí exozomů. Exozomy jsou vezikuly o velikosti 50–140 nm, které jsou sekretovány buňkami různých typů vč. buněk nádorových. Zajišťují mezibuněčnou komunikaci prostřednictvím transportu lipidů, proteinů a nukleových kyselin do recipientních buněk [42]. MiRNA není náhodně rozdělována do exozomů, prekurzory miRNA se přemění na zralé miRNA uvnitř exozomů produkovaných nádorovými buňkami [43]. Exozomy se mohou šířit lidským organizmem pomocí tělních tekutin a mohou být izolovány z periferní krve [44]. Některé exozomální miRNA jsou slibnými markery pro zjištění diagnózy i prognózy, na čemž má podíl i fakt, že miRNA je chráněna před nukleázami membránou exozomu [45,46]. Pacienti s WM jsou odlišitelní od zdravých podle hladiny exprese miRNA v jejich exozomech. Pacienti s asymptomatickou WM vykazují hladinu miRNA v exozomech srovnatelnou s hladinou u neléčených pacientů se symptomatickou WM. Hladiny exprese miR-192-5p, miR-320b a miR-21-p se zvyšují s progresí WM, a naopak hladina miR-let-7d se snižuje. Z toho lze usoudit, že změny v obsahu miRNA v exozomech nastávají dříve, než onemocnění progreduje do symptomatické WM [46,47].
Léčebné postupy u Waldenströmovy makroglobulinemie
Primárním cílem terapie pacientů s WM je redukce symptomů souvisejících s infiltrací kostní dřeně a se zvýšenou hladinou monoklonálního IgM imunoglobulinu. V současné době se využívají různé terapeutické látky, jako inhibitory proteazomů, inhibitory BTK a kombinace rituximabu s alkylačními činidly nebo s purinovými analogy. Pro volbu terapie je také důležité, zda je pacient nositelem mutace v MYD88, příp. i v CXCR4 [48,49]. V roce 2019 bylo v ČR možné použít k léčbě WM rituximab, bortezomib, bendamustin a ibrutinib pouze po schválení revizním lékařem příslušné zdravotní pojišťovny. Pro léčbu WM se dále používají klasická cytostatika, kortikoidy a fludarabin [20].
Alkylační činidla
Počátky chemoterapie lze vystopovat k hořčičnému plynu používanému jako chemická zbraň během první světové války, kdy byla u vojáků pozorována aplazie kostní dřeně a zmenšení lymfatických uzlin spolu s pancytopenií několik dní po vystavení tomuto plynu. Tato pozorování vedla k prvním experimentům na myších s hořčičným plynem jako látkou, která by mohla být účinná proti maligním onemocněním [50,51]. Cytotoxický účinek těchto látek je dán především alkylací bází DNA, která může narušit nepostradatelné procesy, jako replikaci DNA nebo transkripci DNA. I když je v současné době klinické využití alkylačních činidel mnohem menší než využití nových cílených terapií, pořád mají své místo v léčbě specifických malignit [51]. Alkylační činidla jsou spojena se zvýšeným rizikem vzniku sekundárních malignit myeloidní řady [52].
Nukleosidová analoga
Při inkorporaci purinových nukleosidových analog do DNA rychle se dělících nádorových buněk je zastavena jejich reprodukce. Nejpoužívanějšími látkami v léčbě WM patřícími do této skupiny jsou fludarabin a kladribin. Při užívání těchto látek dochází k redukci počtu leukocytů (zejména neutrofilů a T lymfocytů) a k redukci hladiny IgA a IgG, což má za následek vyšší náchylnost k infekcím (infekce herpes zoster) [53]. Nukleosidová analoga a alkylační činidla jsou používána v kombinaci s anti-CD20 monoklonální protilátkou rituximabem. Vzhledem k poškození kmenových buněk a dalším toxickým účinkům jsou nukleosidová analoga při léčbě WM používána málo [54].
Monoklonální protilátky
Terapie založená na monoklonálních protilátkách je jednou z nejúspěšnějších léčebných strategií pro hematologické malignity i pro solidní tumory. Kromě léčby maligních onemocnění jsou monoklonální protilátky využívány i při transplantaci orgánů, léčbě autoimunitních onemocnění i některých infekcí [55,56]. Monoklonální protilátky imitují protilátky přirozeně produkované lidským organizmem. Po vazbě monoklonální protilátky na cílovou buňku dojde k reakci s imunitním systémem a následné destrukci nádorové buňky. Všechny monoklonální protilátky jsou typu IgG [57].
Rituximab
Jednou z nejvyužívanějších chimérických anti-CD20 monoklonálních protilátek v léčbě WM je rituximab [54]. CD20 je transmembránový fosfoprotein, který je bohatě exprimován na povrchu většiny maligních B lymfocytů, avšak ne na většině ostatních buněk lidského organizmu, proto je vhodným terapeutickým cílem u B-buněčných malignit a autoimunitních poruch. Také je exprimován nezralými prekurzory B lymfocytů a plazmatických buněk. CD20 je zásadní pro diferenciaci a proliferaci B lymfocytů [58,59]. Kromě cytotoxicity závislé na protilátkách a aktivace komplementové kaskády může navázání rituximabu na CD20 vést k influxu vápníku a apoptóze. Podávání rituximabu způsobuje úbytek normálních i maligních CD20-pozitivních B lymfocytů v krvi, kostní dřeni a lymfatických uzlinách. Rituximab neoslabuje humorální imunitu; i když způsobuje B-lymfopenii a snížení množství plazmatického IgM, incidence infekcí není zvýšená [58,60].
Inhibitory proteazomů
Proteazomy jsou objemné proteinové komplexy nacházející se uvnitř téměř všech buněk a jejich hlavní funkcí je enzymaticky rozkládat nepotřebné a poškozené proteiny na peptidy a aminokyseliny. Inhibitory proteazomu zapříčiňují hromadění poškozených a nepotřebných proteinů v buňce, což narušuje funkce buňky a může vést až k její smrti. Jelikož nádorové buňky akumulují proteiny rychleji než buňky zdravé, jsou více ovlivněny působením inhibitorů proteazomu [61]. Proteazom je nepostradatelný pro aktivaci NF-kB, jelikož katalyzuje vznik podjednotek NF-kB p50 z neaktivních prekurzorů p105 a také destrukci inhibitoru kB. NF-kB má antiapoptické vlastnosti, tudíž inhibitory proteazomu mohou učinit buňku citlivější k další léčbě [62].
Bortezomib
Bortezomib je reverzibilní inhibitor 26S proteazomu, který se nachází ve všech eukaryotických buňkách. Bortezomib je modifikovaný dipeptidyl kyseliny borité navržený tak, aby se přesně vázal na aktivní část proteazomu. Proteazom má tři typy katalytické aktivity – chymotrypsinovou, trypsinovou a kaspázovou. Skupina kyseliny borité vytváří komplex se skupinou threoninhydroxylovou v místě s chymotrypsinovou aktivitou a funguje jako reverzibilní inhibitor této aktivity proteazomu, což způsobuje inhibici proteolýzy [62].
Inhibitory BTK
BTK je důležitá pro funkci BCR, který je podstatný pro proliferaci a přežití B lymfocytů [63]. Inhibice aktivované BTK u WM buněk může zamezit nadměrné proliferaci [63,64]. Nepostradatelná role BTK v BCR signalizaci činí z BTK ideální cíl pro potlačení BCR signalizace. Inhibitory BTK, ať už kovalentně, nebo nekovalentně se vázající, se vážou na doménu BTK a blokují její katalytickou aktivitu. Množství kovalentních BTK inhibitorů, jako je ibrutinib, bylo vyvinuto cíleně pro terapii B-buněčných malignit. Tyto kovalentní inhibitory byly velmi úspěšné při léčbě WM, avšak není výjimkou vznik rezistence na tato léčiva. Používání nekovalentních inhibitorů BTK by mohlo zamezit vzniku rezistence [65].
Ibrutinib
Ibrutinib je selektivní a ireverzibilní inhibitor BTK, který blokuje signalizaci přes BCR v lidských B lymfocytech tím, že se kovalentně váže na nekatalytický cysteinový zbytek (Cys481) v BTK [66]. U pacientů s WM může dojít k částečné rezistenci na ibrutinib, kdy klonální subpopulace nese mutaci v BTK C481S, která snižuje afinitu ibrutinibu k vazebnému místu [67]. Velikost odpovědi na léčbu ibrutinibem je spjata s genetickým profilem pacientů s WM. Pacienti s WM s mutací v MYD88 L265P jako jedinou genetickou abnormalitou mívají větší a stabilnější odpověď na ibrutinib, a to snížení monoklonálního IgM alespoň o 50 % u 80 % pacientů. Avšak pacienti s mutacemi v MYD88 L265P i CXCR4 mají slabší celkovou odpověď i kratší dobu bez progrese. Pacienti bez mutace v MYD88 nebo CXCR4 nedosáhli léčbou ibrutinibem ani částečné odpovědi [68].
Závěr
WM je vzácné onemocnění starších lidí. Jedná se o nízce agresivní chorobu, u které není nutná okamžitá terapie, dokud nedojde k projevu symptomů omezujících běžný život. V současné době existuje široké spektrum různých terapií, zejména monoklonální protilátky (rituximab), jejich kombinace s dalšími terapeutickými látkami nebo inhibitor BTK ibrutinibu pro léčbu pacientů s WM, které významně zlepšily přežívání i kvalitu života.
Tato práce byla podpořena grantem AZV 17 - 29343A.
This work was supported by grant AZV 17 - 29343A.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE recommendation for biomedical papers.
doc. RNDr. Sabina Ševčíková, Ph.D.
Babákova myelomová skupina
Ústav patologické fyziologie LF MU Kamenice 5
625 00 Brno
e-mail: sevcik@med.muni.cz
Obdrženo/Submitted: 16. 5. 2021
Přijato/Accepted: 29. 8. 2021
Zdroje
1. Wang H, Chen Y, Li F et al. Temporal and geographic variations of Waldenstrom macroglobulinemia incidence: a large population-based study. Cancer 2012; 118 (15): 3793–3800. doi: 10.1002/cncr.26627.
2. Glavey SV, Leung N. Monoclonal gammopathy: the good, the bad and the ugly. Blood Rev 2016; 30 (3): 223–231. doi: 10.1016/j.blre.2015.12.001.
3. Steingrímsson V, Lund SH, Turesson I et al. Population-based study on the impact of the familial form of Waldenström macroglobulinemia on overall survival. Blood 2015; 125 (13): 2174–2175. doi: 10.1182/blood-2015-01-622068.
4. Kyle RA, Anderson KC. A tribute to Jan Gosta Waldenström. Blood 1997; 89 (12): 4245–4247.
5. Kyle RA, Gleich GJ, Bayrid ED et al. Benign hypergammaglobulinemic purpura of Waldenström. Medicine (Baltimore) 1971; 50 (2): 113–123.
6. Waldenström J. Incipient myelomatosis or eessentiala hyperglobulinemia with fibrinogenopenia – a new syndrome? J Int Med 1944; 117 : 3–4.
7. Björkholm M, Johansson E, Papamichael D et al. Patterns of clinical presentation, treatment, and outcome in patients with Waldenstrom’s macroglobulinemia: a two-institution study. Semin Oncol 2003; 30 (2): 226–230. doi: 10.1053/sonc.2003.50054.
8. Dimopoulos MA, Anagnostopoulos A. Waldenström’s macroglobulinemia. Best Pract Res Clin Haematol 2005; 18 (4): 747–765. doi: 10.1016/j.beha.2005.01.028.
9. Baehring JM, Hochberg EP, Raje N et al. Neurological manifestations of Waldenström macroglobulinemia. Nat Clin Pract Neurol 2008; 4 (10): 547–556. doi: 10.1038/ncpneuro0917.
10. Berentsen S. Cold agglutinin-mediated autoimmune hemolytic anemia in Waldenström’s macroglobulinemia. Clin Lymphoma Myeloma 2009; 9 (1): 110–112. doi: 10.3816/CLM.2009.n.030.
11. Stone M. Waldenström’s macroglobulinemia: hyperviscosity syndrome and cryoglobulinemia. Clin Lymphoma Myeloma 2009; 9 (1): 97–99. doi: 10.3816/CLM.2009.n.026.
12. Gertz MA. Waldenström macroglobulinemia: 2019 update on diagnosis, risk stratification, and management. Am J Hematol 2019; 94 (2): 266–276. doi: 10.1002/ajh.25292.
13. Adam Z, Pour L, Krejčí M et al. Změny v prognóze a v léčbě Waldenströmovy makroglobulinemie : přehled literatury a vlastní zkušenosti. Vnitr Lek 2016; 62 (1): 25–39.
14. Paiva B, Corchete LA, Vidriales MB et al. The cellular origin and malignant transformation of Waldenström macroglobulinemia. Blood 2015; 125 (15): 2370–2380. doi: 10.1182/blood-2014-09-602565.
15. Kyle RA, Therneau TM, Rajkumar SV et al. Long-term follow-up of IgM monoclonal gammopathy of undetermined significance. Blood 2003; 102 (10): 3759–3764. doi: 10.1182/blood-2003-03-0801.
16. Adam Z, Šmardová J, Ščudla V. Waldenströmova makroglobulinemie: klinické projevy a diferenciální diagnostika a prognóza nemoci. Vnitr Lek 2007; 53 (12): 1325–1337.
17. Castillo JJ, Olszewski AJ, Kanan S et al. Overall survival and competing risks of death in patients with Waldenström macroglobulinaemia: an analysis of the Surveillance, Epidemiology and End Results database. Br J Haematol 2015; 169 (1): 81–89. doi: 10.1111/bjh.13264.
18. Gertz MA. Waldenström macroglobulinemia: 2021 update on diagnosis, risk stratification, and management. Am J Hematol 2021; 96 (2): 258–269. doi: 10.1002/ajh.26082.
19. Gertz MA. How is Waldenström’s macroglobulinemia diagnosed? IWMF Torch 2008.
20. Kaščák M, Hájek R, Minařík J et al. Diagnostika a léčba Waldenströmovy makroglobulinemie. Transfuze Hematol Dnes 2019; 25 (Suppl. 1): 7–22.
21. Lin S-C, Lo Y-C, Wu H. Helical assembly in the MyD88-IRAK4-IRAK2 complex in TLR/IL-1R signalling. Nature 2010; 465 (7300): 885–890. doi: 10.1038/nature09121.
22. Yang G, Zhou Y, Liu X et al. A mutation in MYD88 (L265P) supports the survival of lymphoplasmacytic cells by activation of Bruton tyrosine kinase in Waldenström macroglobulinemia. Blood 2013; 122 (7): 1222–1232. doi: 10.1182/blood-2012-12-475111.
23. Treon SP, Xu L, Guerrera ML et al. Genomic landscape of Waldenström macroglobulinemia and its impact on treatment strategies. J Clin Oncol 2020; 38 (11): 1198–1208. doi: 10.1200/JCO.19.02314.
24. Munshi M, Liu X, Chen JG et al. SYK is activated by mutated MYD88 and drives pro-survival signaling in MYD88 driven B-cell lymphomas. Blood Cancer J 2020; 10 (1): 12. doi: 10.1038/s41408-020-0277-6.
25. Manček-Keber M, Lainšček D, Benčina M et al. Extracellular vesicle-mediated transfer of constitutively active MyD88 (L265P) engages MyD88 (wt) and activates signaling. Blood 2018; 131 (15): 1720–1729. doi: 10.1182/blood-2017-09-805499.
26. Poulain S, Roumier C, Decambron A et al. MYD88 L265P mutation in Waldenstrom macroglobulinemia. Blood 2013; 121 (22): 4504–4511. doi: 10.1182/blood-2012-06-436329.
27. Jiménez C, Sebastián E, Chillón MC et al. MYD88 L265P is a marker highly characteristic of, but not restricted to, Waldenström’s macroglobulinemia. Leukemia 2013; 27 (8): 1722–1728. doi: 10.1038/leu.2013.62.
28. Poulain S, Roumier C, Venet-Caillault A et al. Genomic landscape of CXCR4 mutations in Waldenström macroglobulinemia. Clin Cancer Res 2016; 22 (6): 1480–1488. doi: 10.1158/1078-0432.CCR-15-0646.
29. Nie Y, Waite J, Brewer F et al. The role of CXCR4 in maintaining peripheral B cell compartments and humoral immunity. J Exp Med 2004; 200 (9): 1145–1156. doi: 10.1084/jem.20041185.
30. Chatterjee S, Behnam Azad B, Nimmagadda S. The intricate role of CXCR4 in cancer. Adv Cancer Res 2014; 124 : 31–82. doi: 10.1016/B978-0-12-411638-2.00002-1.
31. Hunter ZR, Xu L, Yang G et al. The genomic landscape of Waldenstrom macroglobulinemia is characterized by highly recurring MYD88 and WHIM-like CXCR4 mutations, and small somatic deletions associated with B-cell lymphomagenesis. Blood 2014; 123 (11): 1637–1646. doi: 10.1182/blood-2013-09-525808.
32. Treon SP, Cao Y, Xu L et al. Somatic mutations in MYD88 and CXCR4 are determinants of clinical presentation and overall survival in Waldenstrom macroglobulinemia. Blood 2014; 123 (18): 2791–2796. doi: 10.1182/blood-2014-01-550905.
33. Roccaro AM, Sacco A, Jimenez C et al. C1013G/CXCR4 acts as a driver mutation of tumor progression and modulator of drug resistance in lymphoplasmacytic lymphoma. Blood 2014; 123 (26): 4120–4131. doi: 10.1182/blood-2014-03-564583.
34. Cao Y, Hunter ZR, Liu X et al. The WHIM-like CXCR4 (S338X) somatic mutation activates AKT and ERK, and promotes resistance to ibrutinib and other agents used in the treatment of Waldenstrom’s macroglobulinemia. Leukemia 2015; 29 (1): 169–176. doi: 10.1038/leu.2014.187.
35. Xu L, Hunter ZR, Tsakmaklis N et al. Clonal architecture of CXCR4 WHIM-like mutations in Waldenström macroglobulinaemia. Br J Haematol 2016; 172 (5): 735–744. doi: 10.1111/bjh.13897.
36. Iorio MV, Croce CM. MicroRNAs in cancer: small molecules with a huge impact. J Clin Oncol 2009; 27 (34): 5848–5856. doi: 10.1200/JCO.2009.24.0317.
37. Meister G, Tuschl T. Mechanisms of gene silencing by double-stranded RNA. Nature 2004; 431 (7006): 343–349. doi: 10.1038/nature02873.
38. Bartel DP. MicroRNAs: genomics, biogenesis, mechanism, and function. Cell 2004; 116 (2): 281–297. doi: 10.1016/s0092-8674 (04) 00045-5.
39. Hodge LS, Elsawa SF, Grote DM et al. MicroRNA expression in tumor cells from Waldenstrom’s macroglobulinemia reflects both their normal and malignant cell counterparts. Blood Cancer J 2011; 1 (6): e24. doi: 10.1038/bcj.2011.25.
40. Chen CZ, Li L, Lodish HF et al. MicroRNAs modulate hematopoietic lineage differentiation. Science 2004; 303 (5654): 83–86. doi: 10.1126/science.1091903.
41. Roccaro AM, Sacco A, Chen C et al. MicroRNA expression in the biology, prognosis, and therapy of Waldenström macroglobulinemia. Blood 2009; 113 (18): 4391–4402. doi: 10.1182/blood-2008-09-178228.
42. Théry C, Zitvogel L, Amigorena S. Exosomes: composition, biogenesis and function. Nat Rev Immunol 2002; 2 (8): 569–579. doi: 10.1038/nri855.
43. Melo SA, Sugimoto H, O’Connell JT et al. Cancer exosomes perform cell-independent microRNA biogenesis and promote tumorigenesis. Cancer Cell 2014; 26 (5): 707–721. doi: 10.1016/j.ccell.2014.09.005.
44. Zhang J, Li S, Li L et al. Exosome and exosomal microRNA: trafficking, sorting, and function. Genomics Proteomics Bioinformatics 2015; 13 (1): 17–24. doi: 10.1016/j.gpb.2015.02.001.
45. Taylor DD, Gercel-Taylor C. MicroRNA signatures of tumor-derived exosomes as diagnostic biomarkers of ovarian cancer. Gynecol Oncol 2008; 110 (1): 13–21. doi: 10.1016/j.ygyno.2008.04.033.
46. Bouyssou JM, Liu CJ, Bustoros M et al. Profiling of circulating exosomal miRNAs in patients with Waldenström Macroglobulinemia. PLoS One 2018; 13 (10): 1–16. doi: 10.1371/journal.pone.0204589.
47. Varettoni M, Arcaini L, Zibellini S et al. Prevalence and clinical significance of the MYD88 (L265P) somatic mutation in Waldenström’s macroglobulinemia and related lymphoid neoplasms. Blood 2013; 121 (13): 2522–2528. doi: 10.1182/blood-2012-09-457101.
48. Grimont CN, Castillo Almeida NE, Gertz MA. Current and emerging treatments for Waldenström macroglobulinemia. Acta Haematol 2020; 144 (2): 146–157.
doi: 10.1159/000509286.
49. Abeykoon JP, Yanamandra U, Kapoor P. New developments in the management of Waldenström macroglobulinemia. Cancer Manag Res 2017; 9 : 73–83. doi: 10.2147/CMAR.S94059.
50. DeVita VT, Chu E. A history of cancer chemotherapy. Cancer Res 2008; 68 (21): 8643–8653. doi: 10.1158/0008-5472.CAN-07-6611.
51. Puyo S, Montaudon D, Pourquier P. From old alkylating agents to new minor groove binders. Crit Rev Oncol Hematol 2014; 89 (1): 43–61. doi: 10.1016/j.critrevonc.2013.07.006.
52. Martin P, Chen Z, Cheson BD et al. Long-term outcomes, secondary malignancies and stem cell collection following bendamustine in patients with previously treated non-Hodgkin lymphoma. Br J Haematol 2017; 178 (2): 250–256. doi: 10.1111/bjh.14667.
53. International Waldenstrom’s Macroglobulinemia Foundation. Waldenstrom’s macroglobulinemia a guide to treatment options: chemotherapy – alkylating agents and nucleoside analogs. [online]. Dostupné z URL: https: //iwmf.com/media-library/download-iwmf-publications.
54. Olszewski AJ, Treon SP, Castillo JJ. Evolution of management and outcomes in Waldenström macroglobulinemia: a population-based analysis. Oncologist 2016; 21 (11): 1377–1386. doi: 10.1634/theoncologist.2016-0126.
55. Scott AM, Allison JP, Wolchok JD. Monoclonal antibodies in cancer therapy. Cancer Immun 2012; 12 : 14.
56. Singh S, Kumar NK, Dwiwedi P et al. Monoclonal antibodies: a review. Curr Clin Pharmacol 2018; 13 (2): 85–99. doi: 10.2174/1574884712666170809124728.
57. International Waldenstrom’s Macroglobulinemia Foundation. Waldenstrom’s macroglobulinemia a guide to treatment options: monoclonal antibodies. [online]. Dostupné z URL: https: //iwmf.com/media-library/download-iwmf-publications.
58. Stern M, Herrmann R. Overview of monoclonal antibodies in cancer therapy: present and promise. Crit Rev Oncol Hematol 2005; 54 (1): 11–29. doi: 10.1016/j.critrevonc.2004.10.011.
59. Rougé L, Chiang N, Steffek M et al. Structure of CD20 in complex with the therapeutic monoclonal antibody rituximab. Science 2020; 367 (6483): 1224–1230. doi: 10.1126/science.aaz9356.
60. Bergantini L, d’Alessandro M, Cameli P et al. Effects of rituximab therapy on B cell differentiation and depletion. Clin Rheumatol 2020; 39 (5): 1415–1421. doi: 10.1007/s10067-020-04996-7.
61. International Waldenstrom’s Macroglobulinemia Foundation. Waldenstrom’s macroglobulinemia a guide to treatment options: proteasome inhibitors. [online]. Dostupné z URL: https: //iwmf.com/media-library/download-iwmf-publications.
62. Paramore A, Frantz S. Bortezomib. Nat Rev Drug Discov 2003; 2 (8): 611–612. doi: 10.1038/nrd1159.
63. Herman SEM, Gordon AL, Hertlein E et al. Bruton tyrosine kinase represents a promising therapeutic target for treatment of chronic lymphocytic leukemia and is effectively targeted by PCI-32765. Blood 2011; 117 (23): 6287–6296. doi: 10.1182/blood-2011-01-328484.
64. Wang ML, Rule S, Martin P et al. Targeting BTK with ibrutinib in relapsed or refractory mantle-cell lymphoma. N Engl J Med 2013; 369 (6): 507–516. doi: 10.1056/ NEJMoa1306220.
65. Gu D, Tang H, Wu J et al. Targeting Bruton tyrosine kinase using non-covalent inhibitors in B cell malignancies. J Hematol Oncol 2021; 14 (1): 40. doi: 10.1186/s13045-021-01049-7.
66. Zanwar S, Abeykoon JP, Kapoor P. Novel treatment strategies in the management of Waldenström macroglobulinemia. Curr Hematol Malig Rep 2020; 15 (1): 31–43. doi: 10.1007/s11899-020-00559-4.
67. Despina F, Meletios Athanasios D, Efstathios K. Emerging drugs for the treatment of Waldenström macroglobulinemia. Expert Opin Emerg Drugs 2020; 25 (4): 433–444. doi: 10.1080/14728214.2020.1822816.
68. Dimopoulos MA, Trotman J, Tedeschi A et al. Ibrutinib for patients with rituximab-refractory Waldenström’s macroglobulinaemia (iNNOVATE): an open-label substudy of an international, multicentre, phase 3 trial. Lancet Oncol 2017; 18 (2): 241–250. doi: 10.1016/S1470-2045 (16) 30632-5.
Štítky
Dětská onkologie Chirurgie všeobecná Onkologie
Článek vyšel v časopiseKlinická onkologie
Nejčtenější tento týden
2021 Číslo 6- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Editorial
- Waldenströmova makroglobulinemie
- Erdheimova-Chesterova choroba
- Pozdní endokrinologické komplikace onkologické léčby
- Pokročilá stadia klasického Hodgkinova lymfomu – možnosti první linie léčby
- Klinická aplikace principů časového faktoru v radioterapii při kompenzaci přerušení ozařovací série
- Polymorfismy rs4673 a rs28714259 v predikci antracyklinem zprostředkované kardiotoxicity u pacientek s karcinomem prsu
- Incidence, mortalita a přežití novotvarů močového měchýře v České republice v letech 1977–2017: analýza časových trendů
- Primární lymfom prsu – kazuistika
- Doporučení pro preventivní a léčebnou péči o kůži pacientů podstupujících radioterapii
- Anotace knihy
- Aktuality z odborného tisku
- Účinnost a bezpečnost entrektinibu při léčbě nádorů s genovou fúzí NTRK
- Klinická onkologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Waldenströmova makroglobulinemie
- Erdheimova-Chesterova choroba
- Doporučení pro preventivní a léčebnou péči o kůži pacientů podstupujících radioterapii
- Pokročilá stadia klasického Hodgkinova lymfomu – možnosti první linie léčby
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



