-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Adjuvatní radioterapie karcinomu prsu s využitím Active breathing control – moderate inspiration breath-hold – kazuistika
Breast Cancer Adjuvant Radiotherapy Using Active Breathing Control-Moderate Inspiration Breath-Hold – a Case Report
Background:
Chest movements during the breathing cycle represent a significant problem during radiotherapy of target volumes in the chest. There are several methods how to solve this problem.Case:
We have used Active breathing control-moderate inspiration breath-hold device in the case of adjuvant treatment of breast cancer.Results:
Comparing the DVH (dose-volume histograms) without ABC the heart dose is V25 = 6,95% = 34 cm3, V30 = 5,36%, V45 = 1,71%, D mean 6,2 Gy, however in the case of using ABC device V25 = 1,96% = 8,77 cm3, V30 = 1,26%, V45 = 0%, D mean = 2,58 Gy. The dose delivered to left lung was in the first case V20 = 31,2%, D mean = 15,9 Gy and with ABC device V20 = 26,99% a D mean 13,6 Gy. Doses deliver to right lung, cord and target volume coverage were similar in both situations.Conclusion:
According to our experience ABC device represents simple technique how to solve problems with chest movements during radiotherapy.Key words:
radiotherapy – adjuvant therapy – active breathing control – breast cancer – radiotherapy reproducibility
Autoři: D. Vrána 1,2; K. Cwiertka 1; L. Lukešová 1
Působiště autorů: Onkologická klinika LF UP v Olomouci, Olomouc 1; Oddělení toxikogenomiky, Centrum toxikologie a zdravotní bezpečnosti, Státní zdravotní ústav, Praha 2
Vyšlo v časopise: Klin Onkol 2013; 26(2): 143-146
Kategorie: Kazuistika
Souhrn
Východiska:
Dýchací pohyby během dechového cyklu představují signifikantní problém v průběhu radioterapie v oblasti hrudníku. Existuje několik možných metod, jak tuto situaci vyřešit.Případ:
Použili jsme metodu aktivní kontroly dýchání se zadržením dechu ve středně hlubokém nádechu v případě adjuvantní radioterapie pacientky s karcinomem prsu.Výsledky:
Při srovnání DVH (dose-volume histogram) bez použití ABC zařízení byla dávka na srdce V25 = 6,95 % = 34 cm3, V30 = 5,36 %, V45 = 1,71 %, D mean 6,2 Gy, avšak v případě použití ABC zařízení V25 = 1,96 % = 8,77 cm3, V30 = 1,26 %, V45 = 0 %, D mean = 2,58 Gy. Dávka na levou plíci byla v prvním případě V20 = 31,2 %, D mean = 15,9 Gy a s ABC zařízením V20 = 26,99 % a D mean 13,6 Gy. Dávka na pravou plíci, míchu a pokrytí cílového objemu byla v obou případech srovnatelná.Závěr:
Dle našich zkušeností ABC zařízení představuje jednoduchou metodu, jak vyřešit problém s dýchacími pohyby v průběhu radioterapie.Klíčová slova:
radioterapie – adjuvantní léčba – active breathing control – karcinom prsu – reprodukovatelnost zářeníÚvod
Adjuvantní radioterapie karcinomu prsu po prs záchovném výkonu hraje spolu s adekvátním chirurgickým výkonem zásadní roli v lokální kontrole časného karcinomu prsu. Značným problémem pro plánování radioterapie jsou dýchací pohyby hrudníku, které snižují inter-frakcionační a intra-frakcionační reprodukovatelnost radioterapie. Řada studií poukazuje na zvýšenou kardiální morbiditu při radioterapii levostranného prsu. Aktivní kontrola dýchání (active breathing control – ABC) s použitím zadržení dechu ve středně hlubokém nádechu (moderate inspiration breath-hold) představuje jednu z možností, jak redukovat ozáření zdravých tkání (organs at risk – OAR) během radioterapie cílových orgánů (target volume – TV) v oblasti hrudníku a současně zlepšit reprodukovatelnost radioterapie [1]. Zařízení pro ABC umožňuje dočasné znehybnění hrudníku, a tím omezení dýchacích pohybů, což dovoluje redukci velikosti cílového objemu (planning target volume – PTV), a tím i redukci dávky na OAR za současného dodržení a eventuální eskalace dávky na cílové struktury.
Popis případu
V naší kazuistice jde o 41letou pacientku s invazivním duktálním karcinomem prsu s mutací BRCA1, GII, triple-negativním, Ki67 90 %, bez závažných interních komorbidit po neoadjuvantní chemoterapiii 4krát AC v třítýdenním podání + 12krát Paclitaxel + CBDCA v týdenním režimu, po prs záchovném výkonu s exenterací axily s pooperačním stagingem ypT0ypN0cM0. Následovat měla v souladu s běžným standardem [2] radioterapie 50 Gy s boostem na oblast lůžka tumoru do 66 Gy, s denní frakcionací 2 Gy. Lůžko tumoru bylo lokalizováno na základě peroperačně umístěných klipů. Technika dosycení formou zevní radioterapie byla provedena na základě přání pacientky, která nesouhlasila s nabízenou brachyterapií. Po provedení obvyklého plánovacího CT po 5 mm a spočtení plánu jsme konstatovali neakceptovatelnou dávku na srdce (a to zejména levou komoru), proto jsme se rozhodli pro použití přístroje ABC. Po nacvičení procedury s pacientkou jsme opakovali plánovací CT. Pro plánování byla použita technika 7 polí s dalšími 2 poli k dosycení lůžka tumoru (Energie mix 6 MeV + 18 MeV), lineární urychlovač Elekta Synergy, plánovací systém XiO. Dávka byla normalizovaná tak, aby 95 % PTV bylo pokryto 95–107 % předepsané dávky. Pacientka byla před procedurou důsledně poučena o významu a mechanizmu použití ABC přístroje. Byla instruována, aby klidně dýchala a aby zadržela dech v momentě, kdy je přístrojem omezen proud vzduchu (80 % objemu maximálního nádechu). V tomto momentě byla zahájena radioterapie po dobu 25–30 s. Následně byla radioterapie přerušena a pacientce bylo umožněno volně dýchat. Celý postup se opakoval až do aplikace plné frakce radioterapie. Pro aplikaci jedné frakce radioterapie (2 Gy) je nutno 15–20krát zadržet dech, tedy 1–2krát na každé ozařované pole. Tento postup je s pacientem edukační sestrou opakovaně nacvičen. Radioterapie tedy probíhá vždy pouze ve stejné fázi dechového cyklu. Kazuistika pacientky s karcinomem prsu, kdy první plánovací CT bylo pořízeno bez použití ABC přístroje, následující CT bylo provedeno s použitím ABC zařízení. I z běžného pohledu na CT byl zřejmý rozdíl ve vzdálenosti srdce (a to zejména levé komory) od hrudní stěny v prvním a druhém případě (obr. 1, 2), což umožnilo zásadně redukovat dávku na rizikové orgány za současného dodržení dávky na cílové struktury. Rozdíl byl dále ještě markantnější při pohledu na DVH (dose-volume histogramy), viz obr. 3, 4. V prvním případě byla dávka na srdce V25 = 6,95 % = 34 cm3, V30 = 5,36 %, V45 = 1,71 %, D mean 6,2 Gy, kdežto v případě použití ABC byla V25 = 1,96 % = 8,77 cm3, V30 = 1,26 %, V45 = 0 %, D mean = 2,58 Gy. Dávka na levou plíci byla v prvním případě V20 = 31,2 %, D mean = 15,9 Gy a při použití ABC přístroje V20 = 26,99 % a D mean 13,6 Gy. Dávka na pravou plíci, míchu a pokrytí cílových struktur byla v obou případech srovnatelná. Stejně tak je možno očekávat zlepšení inter-frakcionační a intra-frakcionační reprodukovatelnosti radioterapie.
Obr. 1. Plán bez použití ABC zařízení. 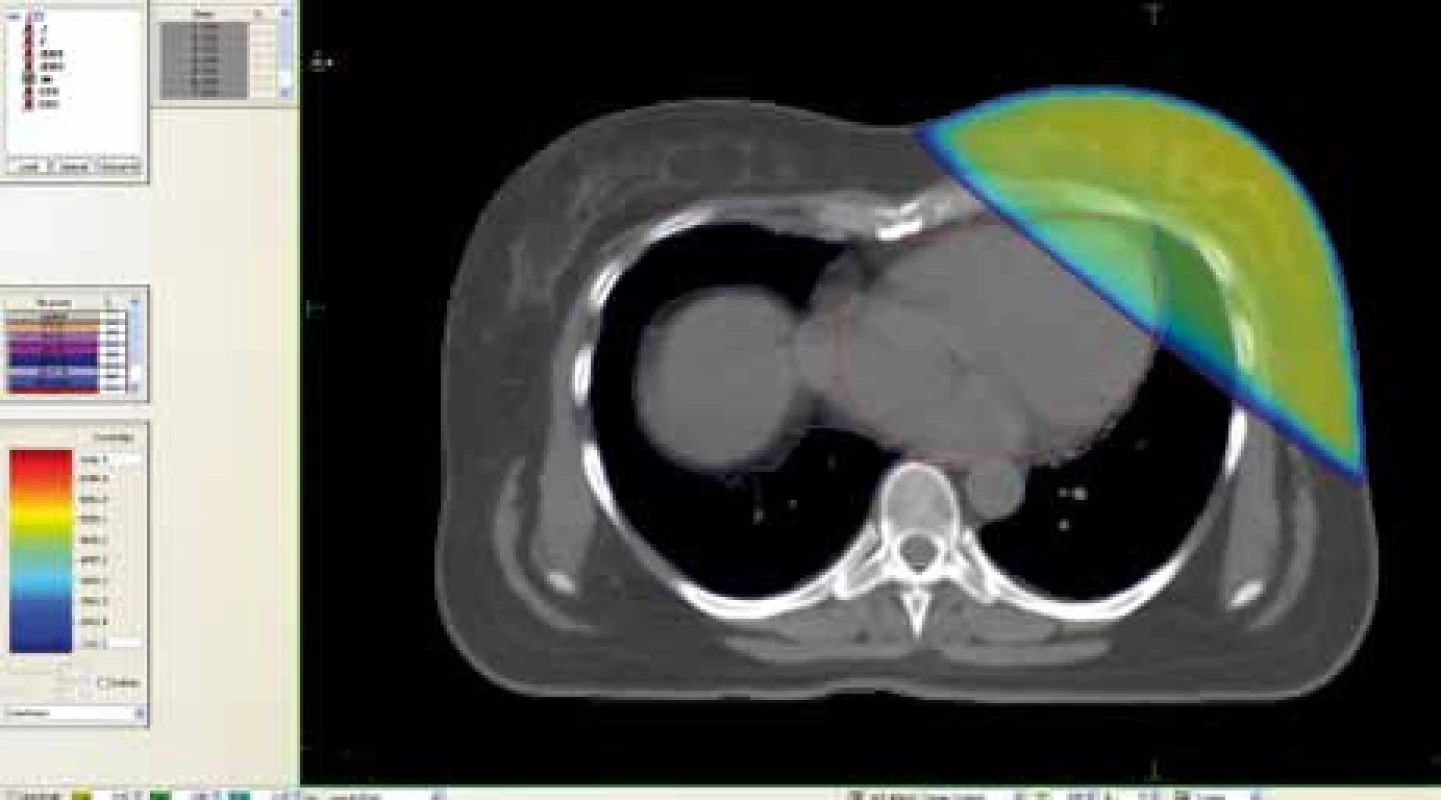
Obr. 2. Plán s použitím ABC zařízení. 
Obr. 3. Dose-volume histogram bez použití ABC zařízení. 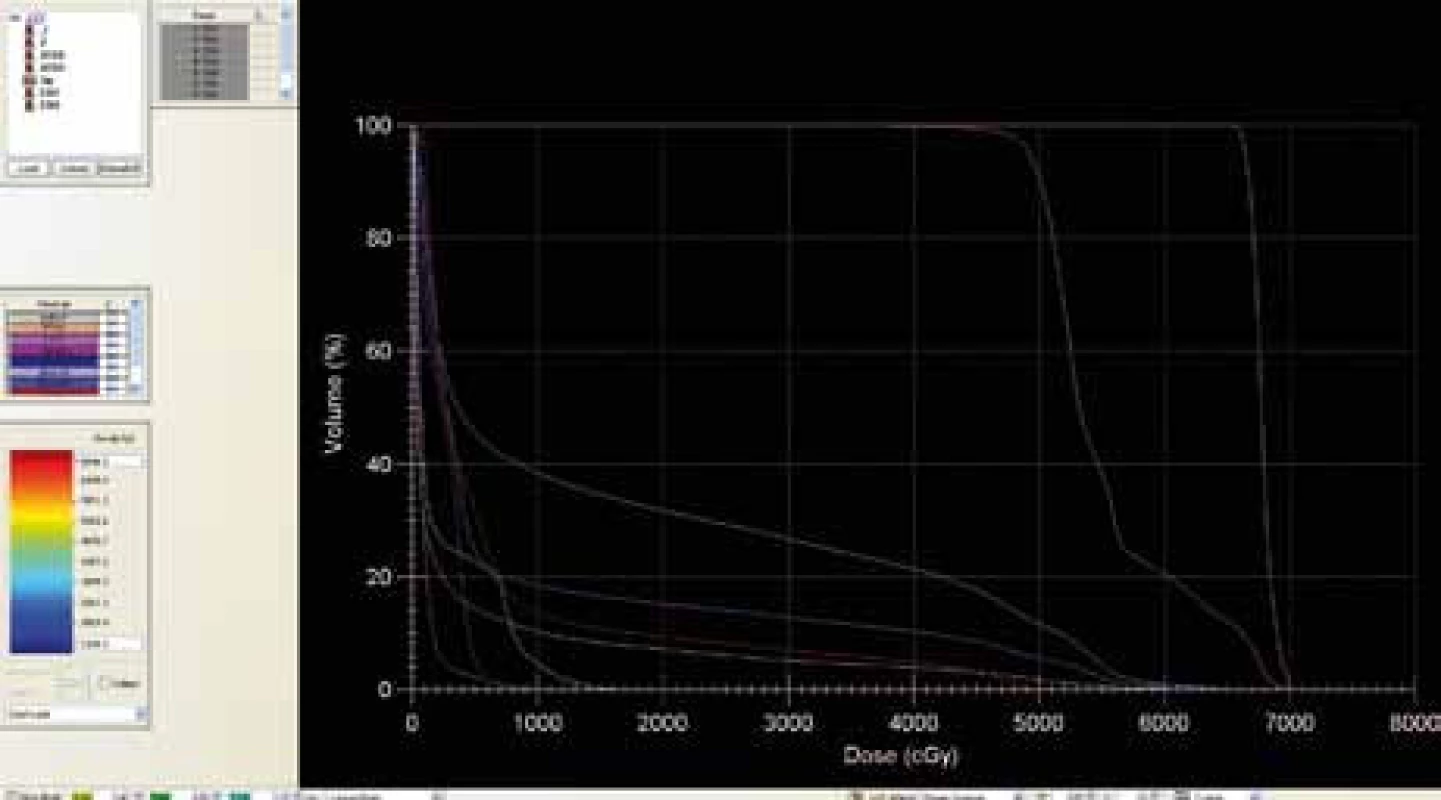
Obr. 4. Dose-volume histogram s použitím ABC zařízení. 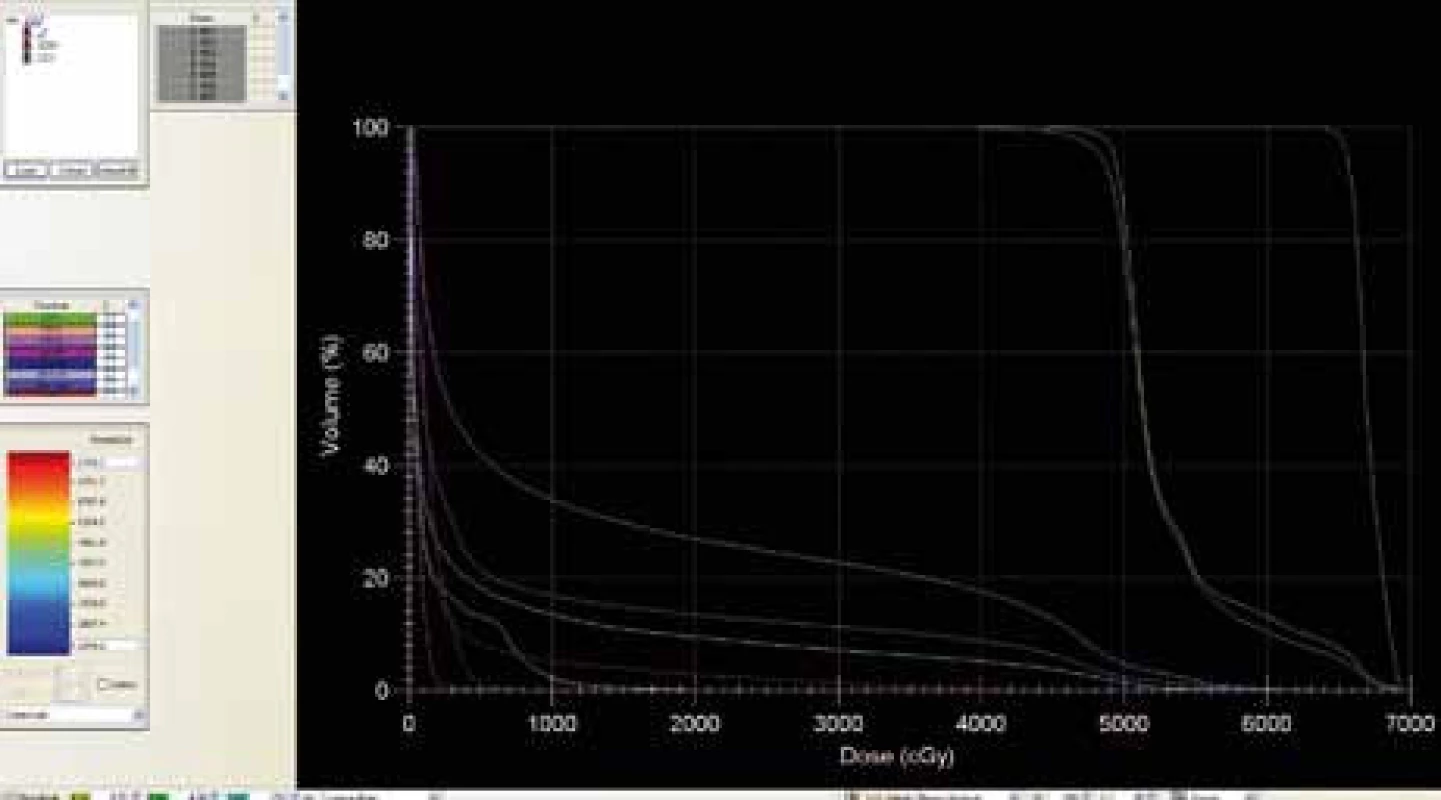
Diskuze
Adjuvantní radioterapie prsu do 50 Gy s dosycením lůžka tumoru, a to formou zevní radioterapie, eventuálně formou brachyterapie do 10–20 Gy dle stavu resekčního okraje tumoru, představuje obvyklý postup po prs záchovném výkonu [3]. Značným problémem při radioterapii v oblasti hrudníku jsou dýchací pohyby hrudníku, které snižují inter-frakcionační a intra-frakcionační reprodukovatelnost radioterapie a nutí nás k adekvátnímu zvětšení lemu PTV ke korekci těchto nepřesností. Při zvětšování objemu PTV se ovšem nevyhneme obtížím při dodržení optimální distribuce dávky na cílové struktury a současně dodržení limitu dávky na rizikové orgány (v případě karcinomu prsu: srdce, druhostranný prs, plíce, mícha, brachiální plexus). Ještě markantnější je tento problém v případě nutnosti ozáření vnitřních mamárních uzlin, i když jejich ozáření samotné v nepřítomnosti klinických známek postižení je dalším často diskutovaným problémem [4–6]. Řada studií poukazuje na zvýšenou kardiální morbiditu při radioterapii levostranného prsu, která zahrnuje ischemickou chorobu srdeční [7], myokarditidu, dilatační kardiomyopatii, perikarditidu a snad i snížené přežívání u levostranných karcinomů prsů ve srovnání s pravostrannými [8,9]. Jednou z možností, jak částečně vyřešit tento problém, je ABC (active breathing control), která využívá jednoduchého přístroje k omezení dýchacích pohybů hrudníku. Tento postup byl ověřen na nádorech plic [10–12], prsu [13–15], jater [16], Hodgkinově chorobě [17] a dalších. Existují studie, které poukazují na skutečnost, že ABC může dále zvýšit lokální kontrolu onemocnění z důvodu možnosti eskalace dávky radioterapie [18]. Jinými možnostmi jsou povrchní dýchání (shallow breathing), respiratory gating nebo respiratory tracking. Dalším důvodem pro snahu o omezení dávky na rizikové orgány je fakt, že naše znalosti o pozdních nežádoucích účincích radioterapie jsou omezené a dnes platné dávkové limity budou v budoucnu zřejmě dále revidovány. S postupně rostoucím přežíváním pacientek po adjuvantní léčbě karcinomu prsu a současně prodlužující se střední délkou života související s rostoucími možnostmi léčby interních chorob bude stále důležitější nejen kontrola vlastního onkologického onemocnění, ale také pozdních nežádoucích účinků radioterapie, zejména na kardiovaskulární systém, které se projevují zpravidla s odstupem 10–15 let po ukončené radioterapii [19]. Nevýhodou ABC přístroje je nutnost zadržení dechu po dobu radioterapie, což může představovat značný problém zejména pro pacienty s karcinomem plic.
Závěr
Aktivní kontrola dýchání se zadržením dechu ve středně hlubokém nádechu s využitím zařízení ABC představuje velmi jednoduchou a efektivní metodu, jak omezit pohyby hrudníku v průběhu dýchacího cyklu s možností redukce dávky na rizikové orgány za současného zlepšení inter-frakcionační a intra-frakcionační reprodukovatelnosti radioterapie. Z našich zkušeností jde o poměrně jednoduchý postup, jenž je možné snadno s pacientem natrénovat a který bude zřejmě stále častěji využíván na našem pracovišti.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do bi omedicínských časopisů.
MUDr. David Vrána, Ph.D.
Onkologická klinika LF UP v Olomouci
I. P. Pavlova 6
775 20 Olomouc
e-mail: davvrana@gmail.com
Obdrženo: 24. 1. 2013
Přijato: 13. 2. 2013
Zdroje
1. McNair HA, Brock J, Symonds-Tayler JR et al. Feasibility of the use of the Active Breathing Co ordinator (ABC) in patients receiving radical radiotherapy for non-small cell lung cancer (NSCLC). Radiother Oncol 2009; 93(3): 424–429. Epub 2009 Oct 23.
2. Kubecová M. Radioterapie karcinomu prsu. Onkologie 2009 : 3(1): 28–31.
3. Clarke M, Collins R, Darby S et al. Early Breast Cancer Trialists’ Collaborative Group (EBCTCG). Effects of radiotherapy and of differences in the extent of surgery for early breast cancer on local recurrence and 15-year survival: an overview of the randomized trials. Lancet 2005; 366(9503): 2087–106.
4. Stranzl H, Zurl B, Langsenlehner Tet al. Wide tangential fields including the internal mammary lymph nodes in patients with left-sided breast cancer influence of respiratory-controlled radiotherapy (4D-CT) on cardiac exposure. Strahlenther Onkol 2009; 185(3): 155–160. doi: 10.1007/s00066-009-1939-2. Epub 2009 Mar 28.
5. Ragaz J, Olivotto IA, Spinelli JJ et al. Locoregional radiotherapy in patients with high-risk breast cancer receiving adjuvant chemotherapy: 20-year results of the British Columbia randomized trial. J Natl Cancer Inst 2005; 97(2): 116–126.
6. Freedmann GM, Fowble BL, Nicolaou N et al. Should internal mammary lymph nodes in breast cancer be a target for the radiation oncologist? Int J Radiat Oncol Biol Phys 2000; 46(4): 805–814.
7. Nilsson G, Holmberg L, Garmo H et al. Distribution of coronary artery stenosis after radiation for breast cancer. J Clin Oncol 2012; 30(4): 380–386. doi: 10.1200/JCO.2011.34.5900. Epub 2011 Dec 27.
8. Paszat LF, Vallis KA, Benk VM et al. A population-based case-cohort study of the risk of myocardial infarction following radiation therapy for breast cancer. Radiother Oncol 2007; 82(3): 294–300.
9. Paszat LF, Vallis KA, Benk VM et al. A population-based case-cohort study of the risk of myocardial infarction following radiation therapy for breast cancer. Radiother Oncol 2007; 82(3): 294–300.
10. Sager O, Beyzadeoglu M, Dincoglan F et al. Evaluation of active breathing control-moderate deep inspiration breath-hold in definitive non-small cell lung cancer radiotherapy. Neoplasma 2012; 59(3): 333–340.
11. Panakis N, McNair HA, Christian JA et al. Defining the margins in the radical radiotherapy of non-small cell lung cancer (NSCLC) with active breathing control (ABC) and the effect on physical lung parameters. Radiother Oncol 2008; 87(1): 65–73.
12. Yan J, Yu JM, Li BS et al. Application of active breathing control system to precise radiotherapy for non-small cell lung cancer. Ai Zheng 2006; 25(10): 1311–1314.
13. Zhang QS, Li JB, Xu M et al. Comparison of overlap ratios of the target volume in different respiratory states with active breathing control for external-beam partial breast irradiation. Zhonghua Zhong Liu Za Zhi 2010; 32(12): 927–931.
14. Moran JM, Balter JM, Ben-David MA et al. Short-term displacement and reproducibility of the breast and nodal targets under active breathing control. Int J Radiat Oncol Biol Phys 2007; 68(2): 541–546.
15. Krauss DJ, Kestin LL, Raff G et al. MRI-based volumetric assessment of cardiac anatomy and dose reduction via active breathing control during irradiation for left-sided breast cancer. Int J Radiat Oncol Biol Phys 2005; 61(4): 1243–1250.
16. Zhong R, Wang J, Jiang X et al. Hypofraction radiotherapy of liver tumor using cone beam computed tomography guidance combined with active breath control by long breath-holding. Radiother Oncol 2012; 104(3): 379–385.
17. Claude L, Malet C, Pommier P et al. Active breathing control for Hodgkin’s disease in childhood and adolescence: feasibility, advantages, and limits. Int J Radiat Oncol Biol Phys 2007; 67(5): 1470–1475. Epub 2007 Jan 8.
18. Partridge M, Tree A, Brock J et al. Improvement in tumour control probability with active breathing control and dose escalation: a modelling study. Radiother Oncol 2009; 91(3): 325–329.
19. Umlauf J, Petrakova K, Drbal J. Radioterapie a myokard. Klin Onkol 1997; 10(3): 77–79.
Štítky
Dětská onkologie Chirurgie všeobecná Onkologie
Článek vyšel v časopiseKlinická onkologie
Nejčtenější tento týden
2013 Číslo 2- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Nejasný stín na plicích – kazuistika
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Adjuvant! Online: Pozor na rozdíly!
- Epidemiologická a klinicko-patologická charakteristika pacientů s renálním karcinomem: analýza 544 případů z jednoho centra
- Castlemanova choroba: retrospektivní studie léčebných výsledků u 10 pacientů z jednoho centra
- Kazuistika: Výskyt grade IV neutropenie a febrilní neutropenie u pacientky s generalizovaným karcinomem prsu léčené paliativní chemoterapií cyklofosfamid/Myocet
- Erratum
- Spontánní remise akutní myeloidní leukemie – klinické případy jednoho centra
- Adjuvatní radioterapie karcinomu prsu s využitím Active breathing control – moderate inspiration breath-hold – kazuistika
- Informace z České onkologické společnosti
- Životní jubileum paní profesorky MUDr. Jitky Abrahámové, DrSc.
- Kam kráčí genetické testování v onkologii?
- Prognostické faktory karcinomu děložního hrdla
- Antiangiogenní bioterapie a chemoterapie v terapii karcinomu prsu: přehled literatury a kazuistika
- Postavení radioterapie v léčbě maligních lymfomů – doporučení Kooperativní lymfomové skupiny
- Klinická onkologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Prognostické faktory karcinomu děložního hrdla
- Spontánní remise akutní myeloidní leukemie – klinické případy jednoho centra
- Kazuistika: Výskyt grade IV neutropenie a febrilní neutropenie u pacientky s generalizovaným karcinomem prsu léčené paliativní chemoterapií cyklofosfamid/Myocet
- Postavení radioterapie v léčbě maligních lymfomů – doporučení Kooperativní lymfomové skupiny
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



