-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Pseudotumory varlete a adnexálních testikulárních struktur
Pseudotumors of the testis and testicular adnexa
A review article dealing with the most common pseudotumors of the testicular region. Nodules of immature tubules, pseudotumors in adrenogenital syndrome, fibromatous periorchitis, pseudosarcomatous myofibroblastic proliferation, posstraumatic mesothelial glandular inclusions and vasitis nodosa are described in detail, including morphologic and immunohistochemical features, altogether with a differential diagnostic approach.
Key words:
testis – testicular adnexa – nodules of immature tubules – pseudotumors in adrenogenital syndrome – fibromatous periorchitis – pseudosarcomatous myofibroblastic proliferation – posstraumatic mesothelial glandular inclusions – vasitis nodosa
Autoři: O. Hes; M. Michal
Působiště autorů: Oddělení speciální diagnostiky ŠPAÚ, Lékařská fakulta a Fakultní nemocnice Plzeň
Vyšlo v časopise: Čes.-slov. Patol., 48, 2012, No. 3, p. 146-149
Kategorie: Přehledový článek
Souhrn
Přehledný článek zabývající se nejčastějšími pseudotumory testikulární oblasti.
Detailně jsou popsány jednotky noduly nezralých tubulů, testikulární „tumor“ u adrenogenitálního syndromu, fibromatózní periorchitis, pseudosarkomatózní myofibroblastická proliferace, posttraumatické glandulární mezoteliální inkluze a vasitis nodosa, včetně vlastností imunohistochemických a včetně základních diferenciálně diagnostických kroků při stanovení diagnózy.Klíčová slova:
testis – testikulární adnexa-noduly nezralých tubulů – testikulární „tumor“ u adrenogenitálního syndromu – fibromatózní periorchitis – pseudosarkomatózní myofibroblastická proliferace – posttraumatické glandulární mezoteliální inkluze – vasitis nodosaPseudotumory v oblasti varlete a nadvarlete jsou léze poměrně vzácné. V tomto přehledném článku se zaměříme pouze na ty pseudotumory, které se vyskytují v rutinní diagnostické praxi nejčastěji. Prakticky vždy jde o zcela benigní afekce, maligní zvrat je naprosto výjimečný a bude u jednotlivých lézí zmíněn.
NODULY NEZRALÝCH TUBULŮ
(synonyma: Pickův adenom, noduly ze Sertoliho buněk, adenom ze Sertoliho buněk, tubulární adenom)
Jedná se o drobné shluky Sertoliho buněk, které se nacházejí obvykle jako vedlejší nález při vyšetřování parenchymu varlete z jiného důvodu (například při resekci atrofického kryptorchického varlete, apod.). Obvykle jsou nacházeny právě v kryptorchických varlatech, v sestouplých varlatech jde o nález neobvyklý. Podle současných názorů se nejedná o skutečný nádor (1,2). Makroskopicky obvykle nejsou při rutinním popisu noduly nalezeny. Pokud je možné noduly nezralých tubulů makroskopicky vůbec odhalit, jedná se o miniaturní bělavé či žlutavé uzlíky (3,4).
Histologicky jde o ohraničené, neopouzdřené shluky tubulů tvořených nezralými Sertoliho buňkami, které jsou obkrouženy hyalinním materiálem (obr. 1).
Obr. 1. Noduly nezralých tubulů tvoří nevelké, poměrně dobře ohraničené útvary v parenchymu varlete. HE, 100x 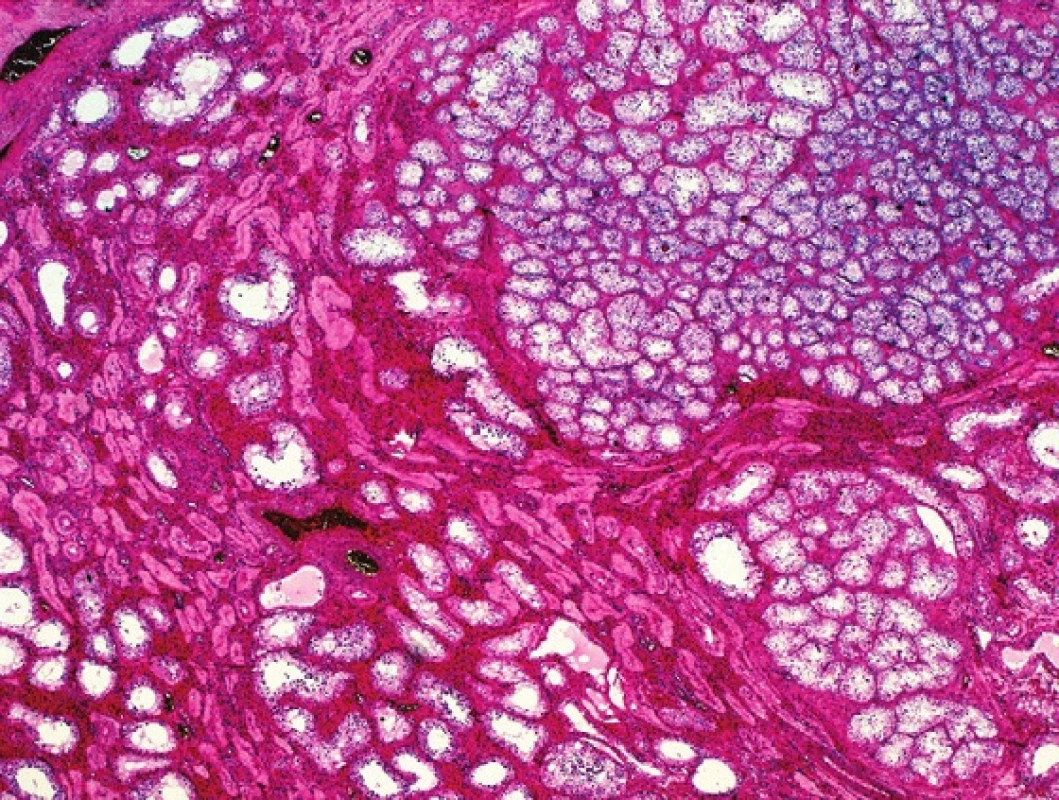
Hyalinní materiál v centru tubulů může být kalcifikován. Zbytnělé membrány kolem tubulů reagují pozitivně s protilátkou proti kolagenu IV a jsou negativní při reakci s fibronektinem, což dokazuje, že se jedná o materiál bazálních membrán (5). V Sertoliho buňkách uvnitř tubulů lze najít imunohistochemickou pozitivitu s protilátkami proti cytokeratinům a inhibinu.
Diferenciální diagnostika. Morfologicky tumor nejvíce připomíná vzácný ovariální tzv. „sex cord tumor s anulárními tubuly“. Pokud se vyskytují ve varleti, kde je současně přítomen germinální tumor, což v kryptorchickém varleti nemusí být nutně vzácné, mohou být noduly nezralých tubulů infiltrovány buď invazivním germinálním tumorem či in situ lézí.
Dále je nutné odlišit gonadoblastom. Gonadoblastom se v převážné většině vyskytuje u pacientů s gonadální dysgenezou či u pacientů s ženským fenotypem. Navíc noduly nezralých tubulů jsou miniaturní léze, které postrádají jasnou komponentu germinálního tumoru, což lze u sporných nálezů snadno ověřit imunohistochemicky, negativní reakcí s OCT 3/4, nanog, SALL 4 či LIN28.
TESTIKULÁRNÍ „TUMOR“ u adrenogenitálního syndromu
Afekce se vyskytuje u jedinců mužského pohlaví, kteří trpí adrenogenitálním syndromem, a kteří jsou neadekvátně léčeni, popřípadě nejsou léčeni vůbec. Odběr tohoto „tumoru“ k bioptickému vyšetření je pak prakticky vždy chybou klinického lékaře, jelikož léze má natolik jasnou symptomatologii a biochemický obraz, že k bioptickému vyšetření by nemělo být přistoupeno. Morfologicky velmi podobné tumory jsou nacházeny při Nelsonově syndromu a mohou být lokalizovány intratestikulárně nebo paratestikulárně, či u žen v širokých vazech děložních nebo tubárních fimbriích (6–10).
Je znám jediný případ s maligním zvratem této jinak zcela benigní nenádorové afekce (11).
Typicky jde o hrbolaté, hnědě zbarvené lobulární útvary, s výraznými fibrózními septy na řezu. Lobuly je možné znázornit i ultrasonograficky. Velikost může dosahovat až 10 cm v průměru. Tumory bývají typicky mnohotné, bilaterální. Histologicky jsou léze tvořené solidně uspořádanými nápadnými lobuly objemných eozinofilních buněk, popřípadě rostou difúzně. Lobuly jsou odděleny silnými fibrózními septy (obr. 2). Mezi „nádorovými“ buňkami mohou být zavzaty semenotvorné kanálky, popřípadě je možné kanálky nalézt ve fibrózním stromatu. Vlastní „nádorové“ buňky jsou objemné, mají granulární eozinofilní cytoplazmu s velkým množstvím hnědého lipochromu. Mitózy jsou vzácné, ale byl popsán i případ s atypickými mitózami (11). V okolí lobulů bývají reaktivní uzle Leydigových buněk. Pozitivní imunohistochemickou reakci lze nalézt s protilátkami proti testosteronu a cortisolu, negativní reaktivita je obvykle s S-100 proteinem.
Obr. 2. Na snímku je patrné, že „tumor“ u adrenogenitálního syndromu je lobulárně uspořádán a obsahuje nápadné fibrózní pruhy. HE, 200x 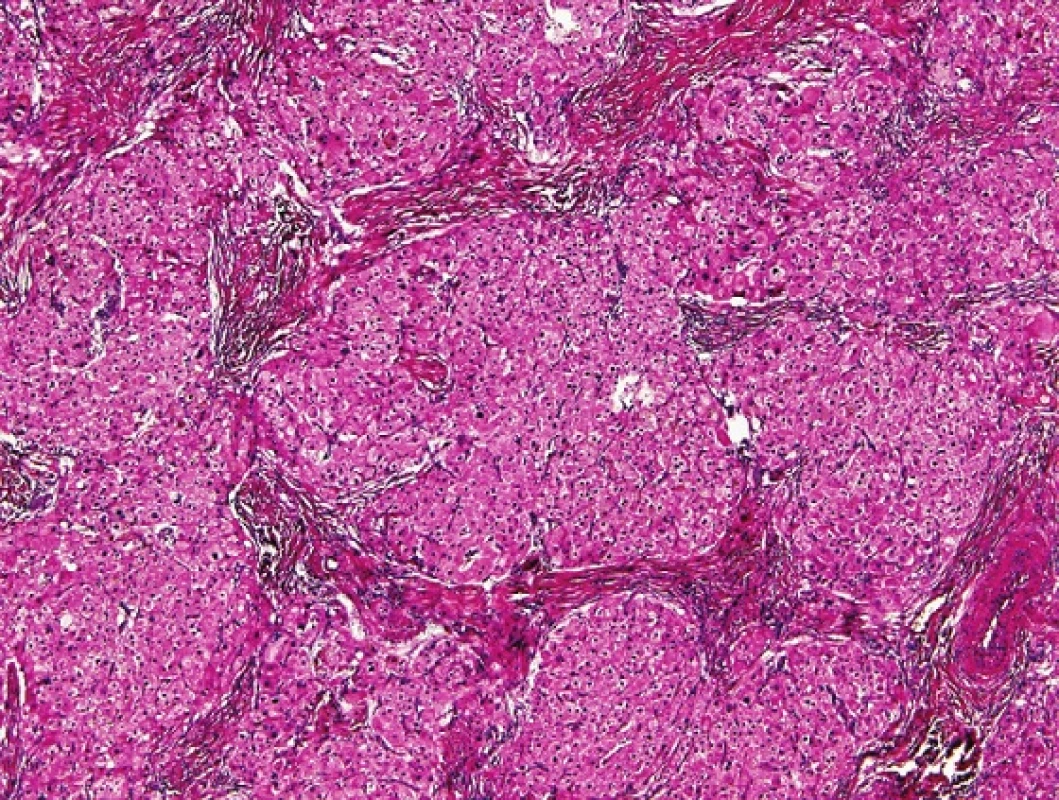
Základní diferenciálně diagnostická otázka je odlišení této léze od nádoru z Leydigových buněk (12,13). Nádory z Leydigových buněk jsou téměř vždy solitární. Postrádají laboratorní a klinické nálezy typické pro „tumor“ u adrenogenitálního syndromu. Histologicky jsou nádory z Leydigových buněk tvořeny menšími buňkami, neobsahují tolik pigmentu v cytoplazmě. Nádory z Leydigových buněk mají často v cytoplazmě tzv. Reinkeho krystaly. Chybí typické silné fibrózní pruhy, které rozdělují masu do lobulů. Ektopickou tkáň nadledvinek je snadné odlišit lokalizací od „tumoru“ při adrenogenitálním syndromu. Ektopická tkáň nadledvinek je typicky lokalizována v blízkosti epididymis nebo ve spermatickém provazci, vzácně v hilu či tunica albuginea. Samozřejmě histologicky se významně liší od velkých eosinofilních granulárních buněk diskutované léze.
FIBROMATÓZNÍ PERIORCHITIS
(synonyma: fibrózní pseudotumor, nodulární periorchitis,kalcifikující fibrózní pseudotumor)
Jde o afekci vyskytující se v jakémkoliv věku. Často bývá anamnesticky spojena s infekcí, traumatem či s hydrokélou (14,15). Je velmi pravděpodobné, že fibromatózní periorchitis je jen pozdním fibrózním stadiem pseudosarkomatózní myofibroblastické proliferace. Popisovány jsou případy fibromatózní periorchitis u pacienta s retroperitoneální fibrózou či ve spojení s Gorlinovým – Goltzovým syndromem („nevoid - basal cell carcinoma syndrom“) (2,16,17,18). Obvykle má charakter masy či ztluštění v oblasti varlete, nadvarlete, méně často ve funikulu. Na řezu jde o bělavou tuhou hmotu. Histologicky je léze charakteristická denzní kolagenní tkání, někdy s ložisky rozsáhlých kalcifikací (obr. 3). Většinou se jedná o buněčně velmi chudou lézi, pouze vzácně se zastihnou i mírně buněčnější partie se zánětlivým infiltrátem.
Obr. 3. Histologicky je léze charakteristická denzní kolagenní tkání, někdy s ložisky rozsáhlých kalcifikací. HE, 200x 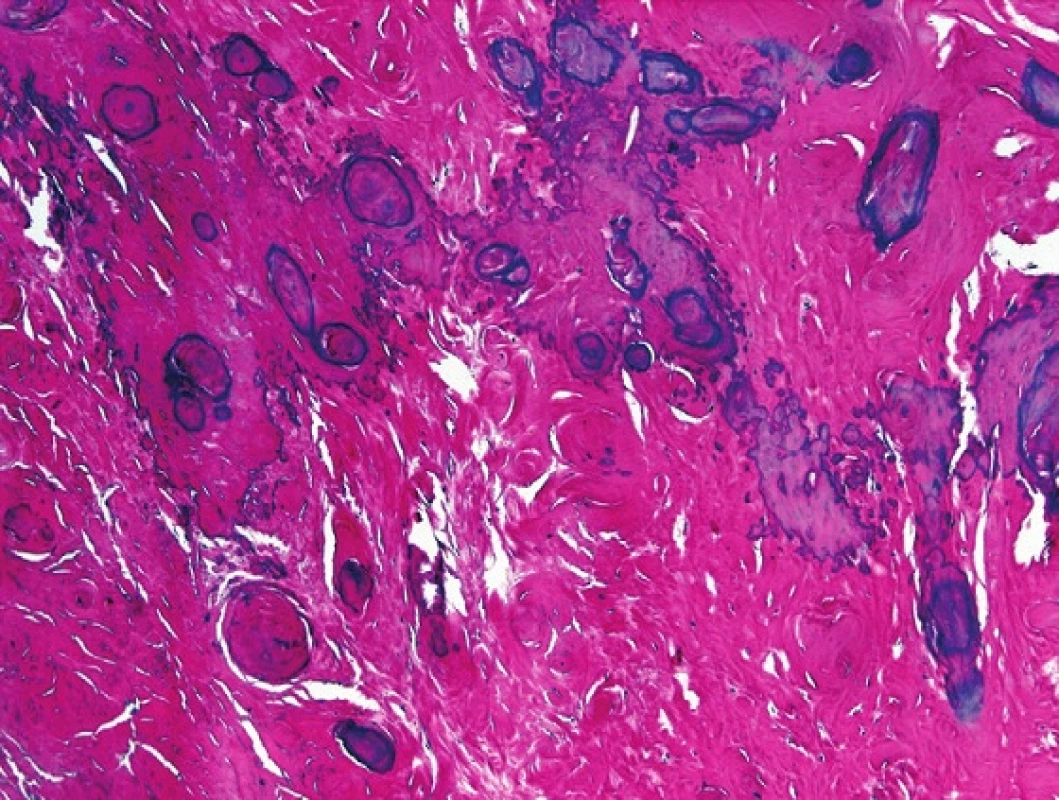
V diferenciální diagnostice je nutné odlišit zejména skutečné nádory měkkých tkání, které se v oblasti varlete mohou vyskytnout. Dále, pokud afekce zasahuje do parenchymu nebo jeho těsné blízkosti, je nutné vyloučit nádory ze skupiny fibromu/thekomu. Oproti těmto nádorům je fibromatózní periorchitis spíše lokalizovaná v obalech varlete či postihuje adnexální struktury. Histologicky je oproti fibromům/thekomům výrazně hypocelulární, eventuálně s kalcifikacemi.
PSEUDOSARKOMATÓZNÍ MYOFIBROBLASTICKÁ PROLIFERACE
(synonyma: proliferativní funikulitis, pseudosarkomatoidní fibromyxoidní tumor, inflamatorní pseudotumor, atypický myofibroblastický tumor, inflamatorní myofibroblastický tumor, atypický fibromyxoidní tumor, plazmocytární granulom či nodulární fasciitis)
Pseudosarkomatózní myofibroblastická proliferace se v rámci struktur varlete téměř vždy vyskytuje v oblasti semenného provazce. Vykazuje některé společné znaky s postoperačním vřetenobuněčným nodulem vznikajícím v genitourinární oblasti po traumatizaci tkáně (19,20). Typicky se vyskytuje u dětí či mladých dospělých. Pokud není pseudosarkomatózní myofibroblastická proliferace radikálně odstraněná, může recidivovat, avšak nikdy nemetastazuje.
Makroskopicky se jedná o nepřesně ohraničenou lézi nodulárního tvaru. Konzistence je buď tuhá nebo gelatinózní, někdy prokrvácená či cystická. Velikost zřídla přesahuje 3 cm (2). Pseudosarkomatózní myofibroblastická proliferace je typicky složena z nepravidelně uspořádaných vřetenobuněčných elementů, bez nápadnějších buněčných atypií. Často bývá nápadná smíšená chronická zánětlivá infiltrace. Někdy mohou být přítomné obrovskobuněčné elementy. Stroma může být nenápadné nebo naopak objemné, hyalinizované s kalcifikacemi. Morfologie je identická s tzv. celulárními variantami nodulární fasciitis měkkých tkání. U pseudosarkomatózní myofibroblastické proliferace bývá rovněž popisováno místy nápadné myxoidní stroma (obr. 4), někdy s tzv. „mukoidními jezírky“. Mitózy nebývají nápadným rysem tohoto procesu, ale v některých případech floridních lézí jsou snadno identifikovatelné. Vždy se jedná o mitózy typické. Většinou se udává 1 mitóza na 10 zorných polí (zvětšení 400x) (2,21). Léze je pozitivní při reakci s aktinem a vimentinem. Mohou být přítomné pozitivní elementy při reakci s cytokeratiny.
Obr. 4. U pseudosarkomatózní myofibroblastické proliferace bývá přítomno objemné myxoidní stroma. HE, 100x 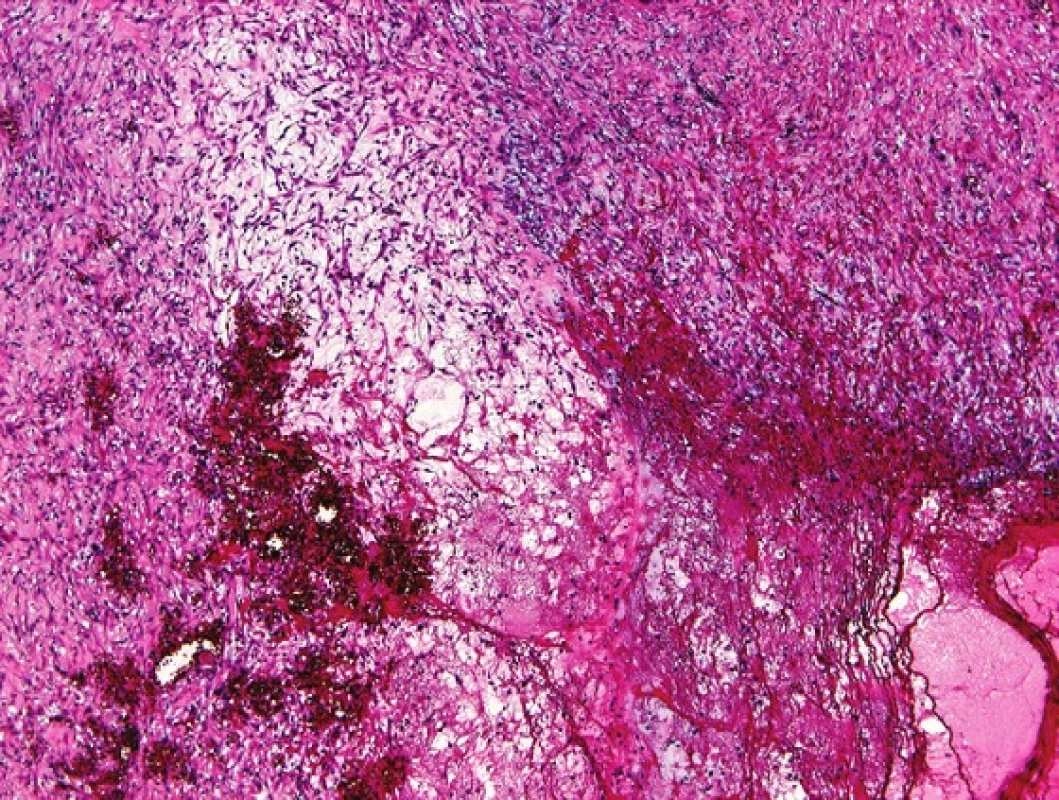
V diferenciální diagnostice je nutné vzít v úvahu skutečné vřetenobuněčné nádory , jako je leiomyosarkom, rhabdomyosarkom, maligní fibrózní histiocytom. K odlišení by měla napomáhat cytologicky klidná buněčná populace, zjevně zánětlivá infiltrace a absence atypických mitóz. Popsán byl inflamatorní liposarkom spermatického provazce, inflamatorní fibrosarkom (2,22).
POSTTRAUMATICKÉ GLANDULÁRNÍ MEZOTELIÁLNÍ INKLUZE
Posttraumatické glandulární mezoteliální inkluze se nacházejí ve varleti relativně často. Mohou vznikat z traumat rete testis, z jakékoliv struktury nadvarlete, provazce. Především traumatizované nadvarle se může prezentovat řadou pseudoneoplastických změn, jako např. dlaždicovou metaplazií, hyperplastickými či pseudoinfiltrativními změnami. Zvláštní a diagnosticky jednou z nejobtížnějších lézí je posttraumatická glandulární proliferace spermatického provazce, kde ve stromatu na pozadí pseudosarkomatózní myofibroblastické proliferace vznikají epitelové inkluze, které vypadají jako „rozsypaná“ drobná ložiska metastatického tubulárního adekarcinomu (obr. 5A,B). Též se v některých případech kolem těchto inkluzí nachází mnohojaderná reakce s cholesterolovými krystaloidy. V některých místech této posttraumatické mezoteliální proliferace se tvoří navíc i dobře formované žlázové útvary a vzhled se v těchto místech podobá dříve popsané reaktivní mezoteliální hyperplazii (23). Jindy tyto mezoteliální inkluze vytvářejí kribriformní struktury a nebo vykazují zvláštní fixační artefakt, kdy se odchlipují od stromatu a mohou připomínat růst mikropapilárního karcinomu (24). Asi v polovině případů této pseudomaligní proliferace lze zachytit zajímavé zonální uspořádání, kdy na straně nekrózy se nachází proliferace myofibroblastů, ty dále přecházejí do epiteloidních myofibroblastů a ty se pak luminizují do žlázových inkluzí a někdy i větších cyst. Lze zaznamenat přechod mezoteliálních inkluzí do adenomatoidního tumoru a je nanejvýš pravděpodobné, že adenomatoidní tumor vzniká právě přes tyto mezoteliální inkluze. Nepřímým důkazem je to, že místem v ženském genitálním traktu, kde jsou často přítomny identické mezoteliální inkluze na pozadí pseudosarkomové myofibroblastické proliferace, je Fallopiánská tuba, která je zároveň druhým nejčastějším místem vzniku adenomatoidního tumoru. U starších lézí doprovázených těmito mezoteliálními inkluzemi vytváří labyrintovité cystické prostory vystlané mezoteliemi. Zajímavé je i to, že všechny tyto struktury, včetně všech myofibroblastů, reagují imunohistochemicky pozitivně s protilátkami proti cytokeratinům AE1-AE3. Glandulární inkluze jsou samozřejmě pozitivní při barvení s calretininem. Při barvení s protilátkou 2D-40, která značí mimo endotelií i mezoteliální buňky, se znázorňuje též povrchový lem těchto metaplastických epiteliálních inkluzí, který bude nejspíše mezotelovými mikroklky. Ultrastrukturálně mají epiteloidní buňky všechny charakteristiky mezotelií včetně dlouhých mikrovilů.
Obr. 5A. Drobné mezoteliální glandulární inkluze v semenném provazci. HE, 100x 
Obr 5B. Při detailním pohledu jsou patrné poměrně blandní cytologické vlastnosti a tubulární formace jednotlivých inkluzí. HE, 400x 
Diferenciálně diagnosticky je třeba odlišit zejména metastázu adenokarcinomu. Adenokarcinom zpravidla metastazuje do varlete pod obrazem jasného a snadno diagnostikovatelného adenokarcinomu a téměř nikdy jako ojedinělé, dobře diferencované glandulární inkluze. Dále je nutné vzít v úvahu mezoteliom. U mezoteliomu nelze očekávat myofibroblastické elementy s koexpresí AE1-AE3 a hladkosvalového aktinu, zonální uspořádání a, stejně jako u metastázy adenokarcinomu, nepřítomnost mitóz.
Další lézí, která napodobuje karcinom je tzv. vasitis nodosa (protějšek salpingitis isthmica nodosa u žen). Typicky se vyskytuje v oblasti ductus deferens. Nalézá se u mladších mužů podstupujících vasektomii, eventuálně v časovém odstupu po tomto výkonu (25). Vytváří tuhé bělavé noduly, které mohou obsahovat bělavý tekutý obsah. Řada lézí je zachycena pouze mikroskopicky. Histologicky jde o drobné protáhlé tubulární mnohotné útvary vystlané obvykle plochým nebo nízce kubickým epitelem. Tubuly se mohou šířit perineurálně, čímž velmi věrně napodobují maligní tumor (26,27). Vasitis nodosa bývá někdy spojena se spermatickým granulomem (28). K odlišení od skutečného adenokarcinomu napomůže minimální polymorfie a nízká nebo nulová mitotická aktivita (29).
Okrajově je vhodné zmínit zánětlivé procesy jako granulomatózní orchiepididymitis, malakoplakii, tzv. mekoniovou periorchitis. Další léze, které je možno považovat za pseudotumor jsou ektopie kůry nadledvin, splenogonadální fúze a splenóza varlete, spermatický granulom, talkové granulomy, kongenitální testikulární lymfangiektázie, sekundární oxalóza, amyloidóza, testikulární edém, způsobený hydrokélou, klinicky napodobující nádor, Crohnova nemoc postihující varle či testikulární lipomatóza u pacientů s Cowdenovou nemocí a řada dalších zcela raritních procesů.
Adresa pro korespondenci:
Prof. MUDr. Ondřej Hes, PhD
Oddělení speciální diagnostiky ŠPAÚ
FN Plzeň, Alej Svobody 80, 304 60 Plzeň
Zdroje
1. Rosai J. Rosai and Ackerman‘s Surgical Pathology. Edinburg, London: Elsevier, Mosby, 10th ed. 2011.
2. Ulbright TM, Amin MB, Young RH. Tumors of the testis, adnexa, spermatic cord, and scrotum. Washington D.C., AFIP, 1999.
3. Halley JB. The growth of Sertoli cell tumors: a possible index of differential gonadotropin activity in the male. J Urol 1963; 90 : 220-229.
4. Barghorn A, Alioth H-R, Hailemariam S, Bannwart F, Ulbright TM. Giant Sertoli cell nodule of the testis: distinction from other Sertoli cell lesions. J Clin Pathol 2006; 59 : 1223-1225.
5. Govender D, Sing Y, Chetty R. Sertoli cell nodulus in the undescended testis: a histochemical, immunohistochemical and ultrastructural study of hyaline deposits. J Clin Pathol 2004; 57 : 802-806.
6. Johnson RE, Scheithauer B. Massive hyperplasia of testicular adrenal rests in a patient with Nelsonęs syndrome. Am J Clin Pathol 1982; 77 : 501-507
7. Krieger DT, Samojlik E, Bardin CW. Cortisol and androgen secretion in a case of Nelson’s syndrome with paratesticular tumors: response to cyprohepatadine therapy. J Clin Endocrinol Metab 1978; 47 : 837-844
8. Baranetsky NG, Zipser RD, Goebelsmann U, et al. Adrenocorticotropin-dependent virilizing paraovarian tumors in Nelson’s syndrome. J Clin Endocrinol Metab 1979; 49 : 381-386.
9. Verdonk C, Guerin C, Lufkin E, Hodgson SF. Activation of virilizing adrenal rest tissues by excessive ACTH production. An unusual presentation of Nelson’s syndrome. Am J Med 1982; 73 : 455-459.
10. Wild RA, Albert RD, Zaino RJ, Abrams CS. Virilizing paraovarian tumors: a consequence of Nelson’s syndrome? Obstet Gynecol 1988; 71 : 1053-1056.
11. Davis JM, Woodroof J, Sadasivan R, Stephens R. Case report: congenital adrenal hyperplasia and malignant Leydig cell tumor. Am J Med Sci 1995; 309 : 63-65.
12. Battaglia M, Ditonno P, Palazzo S, Bettochi C, Selvaggio O, Garofalo L, Selvaggi FP. Bilateral tumors of the testis in 21-alpha hydroxylase deficiency without adrenal hyperplasia. Urol Oncol 2005; 23 : 178 - 180.
13. Rutgers JL, Young RH, Scully RE. The testicular „tumor“ of the adrenogenital syndrome. Am J Surg Pathol 1988; 12 : 503-513.
14. Polsky EG, Ray Ch, Dubilier LD. Diffuse fibrous pseudotumor of the tunica vaginalis testis, epididymis and spermatic cord. J Urol 2004; 171 : 1625-1626.
15. Seethala RR, Tirkes AT, Weinstein S, Tomaszewski JE, Malkowitcz SB, Genega EM. Diffuse fibrous pseudotumor of the testicular tunics associated with an inflamed hydrocele. Arch Pathol Lab Med 2003; 127 : 742-744.
16. Nistal M, Paninagua R, Torres A, Hidalgo L, Regadera J. Idiopatic peritesticular fibrosis associated with retroperitoneal fibrosis. Eur Urol 1986; 12 : 64-68.
17. Vates TS, Ruemmler-Fisch Ch, Smilow PC, Fleisher MH. Benign fibrous testicular pseudotumors in children. J Urol 1993; 150 : 1886-1888.
18. Watson RA, Harper BN. Paratesticular fibrous pseudotumor in a patient with Gorlinęs syndrome: nevoid basal cell carcinoma syndrome. J Urol 1992; 148 : 1254-1255.
19. Hamilton FA, Persad RA, Webb RJ, Ball RY. Fibrous pseudotumor of the tunica vaginalis following vasectomy. J Urol Pathol 1997; 6 : 243-248.
20. Weiss SH, Goldblum JR, Folpe AL. Enzinger and Weissęs Soft Tissue Tumors, Philadelphia, Mosby, 5th ed., 2008.
21. Donnellan R, Bramdev A, Chetty R. A paratesticular pseudosarcomatous myofibroblastic proliferation. A case report. Int J Surg Pathol 1998; 6 : 235-238.
22. Kraus MD, Guillou L, Fletcher CD. Well-differentiated inflammatory liposarcoma: an uncommon and easily overlooked variant of a common sarcoma. Am J Surg Pathol 1997; 21 : 518-527.
23. Amin MB. Selected other problematic testicular and paratesticular lesions: rete testis neoplasms and pseudotumors, mesothelial lesions and secondary lesions. Mod Pathol 2005;18(Suppl 2): 131-145.
24. Michal M, Hes O, Kazakov DV. Mesothelial glandular structures within pseudosarcomatous proliferative funiculitis. A diagnostic pitfall. Report of 17 cases. Int J Surg Pathol 2008; 16 : 48-56.
25. Olson AL. Vasitis nodosa. Am J Clin Pathol 1971; 55 : 364-368.
26. Balogh K, Travis WD. The frequency of perineurial dusctules in vasitis nodosa. Am J Clin Pathol 1984; 82 : 710-713.
27. Goldman RL, Azzopardi JG. Benign neural invasion in vasitis nodosa. Histopathology 1982; 6 : 309-315.
28. Civantos F, Lubin J, Rywlin AM. Vasitis nodosa. Arch Pathol 1972; 94 : 355-361.
Štítky
Patologie Soudní lékařství Toxikologie
Článek vyšel v časopiseČesko-slovenská patologie

2012 Číslo 3-
Všechny články tohoto čísla
- Pseudotumors & MIMICKERS
- SLINNÉ ŽLÁZY VYPADAJÍ V MIKROSKOPU TAK KRÁSNĚ!
- HEMATOPATOLOGIE, UROPATOLOGIE, NEFROPATOLOGIE...
- Pseudotumors & Mimickers: Přehled vybraných pseudotumorů s uvedením nádorů, které mohou mikroskopicky imitovat
- Melanocytární pseudotumory
- Změny ve specializačním vzdělávání v patologii od roku 2012
- Diferenciální diagnostika chronické pankreatitidy a duktálního adenokarcinomu pankreatu
- Obrovskobuněčné léze kostí a jejich diferenciální diagnostika
- Pseudotumory varlete a adnexálních testikulárních struktur
- Patologie slinných žláz
- Primární dlaždicobuněčný karcinom vagíny vzniklý na podkladě skvamózní inkluzní cysty zadní stěny vagíny – popis případu
- Sarkomatoidní (metaplastický) vřetenobuněčný karcinom prsu vznikající ve fyloidním tumoru s rozsáhlou skvamózní metaplázií – kazuistika a přehled literatury
- Rozbor histopatologických pitevních nálezů u 8 pacientů s chřipkovou (H1N1) pneumonií
- Imunoexprese adiponektinového receptoru typu 1 v lidském střevě
- Historie a současnost tenkojehlové aspirační cytologie
- Česko-slovenská patologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Obrovskobuněčné léze kostí a jejich diferenciální diagnostika
- Sarkomatoidní (metaplastický) vřetenobuněčný karcinom prsu vznikající ve fyloidním tumoru s rozsáhlou skvamózní metaplázií – kazuistika a přehled literatury
- Diferenciální diagnostika chronické pankreatitidy a duktálního adenokarcinomu pankreatu
- Melanocytární pseudotumory
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



