-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Kazuistika gigantického recidivujícího angiomyolipomu podkovovité ledviny
Case report of a gigantic recurrent angiomyolipoma in a horseshoe kidney
We present a case report of gigantic recurrent angiomyolipoma of the horseshoe kidney in a young patient with suspected tuberous sclerosis syndrome. The condition was solved by repeated cytoreductive surgery in combination of systemic treatment with mTOR inhibitors.
Keywords:
angiomyolipoma – tuberous sclerosis – horseshoe kidney – mTOR inhibitor
Autoři: Markéta Hulová; Michal Staník; Daniel Macík; Jan Doležel
Působiště autorů: Oddělení urologické onkologie, Masarykův onkologický ústav, Brno
Vyšlo v časopise: Ces Urol 2020; 24(1): 69-73
Kategorie: Kazuistika
Prezentujeme kazuistiku objemného recidivujícího angiomyolipomu podkovovité ledviny u mladé pacientky s podezřením na syndrom tuberózní sklerózy. Stav byl řešen opakovanou cytoredukční operací v kombinaci se systémovou léčbou mTOR inhibitory.
Souhrn
Prezentujeme kazuistiku objemného recidivujícího angiomyolipomu podkovovité ledviny u mladé pacientky s podezřením na syndrom tuberózní sklerózy. Stav byl řešen opakovanou cytoredukční operací v kombinaci se systémovou léčbou mTOR inhibitory.
Klíčová slova:
angiomyolipom – tuberózní skleróza – podkovovitá ledvina – mTOR inhibitor
ÚVOD
Angiomyolipom (AML) je nejčastější nezhoubný mesenchymální nádor ledviny. V 80 % se jedná o sporadické onemocnění, které je nejčastěji asymptomatické, vykazuje pomalý růst a má charakteristický obraz při ultrazvukovém vyšetření a počítačové tomografii (CT) (1, 2). Historicky je doporučována operační léčba při velikosti AML nad 4cm, což byla arbitrárně stanovena hranice, při které se uvádělo vyšší riziko spontánního krvácení AML (3, 4). V současnosti je hranice 4cmzpochybňována, většinu pacientů lze bezpečně sledovat, jelikož riziko spontánního krvácení je podle studií s aktivním sledováním (AS) velmi nízké (2, 3). Pokud je indikováno odstranění nádoru, lze ho ošetřit parciální nefrektomií, radiofrekvenční ablací (RFA), kryoterapií nebo selektivní arteriální embolizací (1, 2, 5). Odlišný průběh má 20 % AML, které jsou asociovány se syndromem tuberózní sklerózy (TS). Často jsou multifokální, bilaterální a rostou rychleji (1). U této skupiny nemocných má důležité místo systémová terapie mTOR inhibitory v kombinaci s lokální léčbou (6).
KAZUISTIKA
V této kazuistice je prezentována pacientka s podkovovitou ledvinou, 43letá cizinka z Jemenu, léčená pro recidivující objemnou progredující břišní angiomyolipomatózu vycházející z ledviny. V anamnéze měla před rokem 2010 pouze exstirpaci kožních lipomů na přední straně hrudníku v Jemenu ve 23 letech, jinak nebyla nemocná. Od roku 2010 byla léčena v České republice (ČR) na několika pracovištích pro rozsáhlý tumor retroperitonea. V roce 2010 podstoupila první cytoredukční operaci (1500g), histologicky se jednalo o objemný AML. Další operace proběhla v Jemenu pro ileus v roce 2012. Při kontrole v ČR v roce 2012 byla zjištěna progrese onemocnění a pacientka byla došetřována pro podezření na tuberózní sklerózu. Nález na magnetické rezonanci mozku nepodpořil stanovení této diagnózy. Od roku 2013 do roku 2015 podstoupila pacientka imunosupresivní terapii Everolimem 3mg ve snaze o zpomalení růstu AML. Tato léčba však nepřinesla očekávaný efekt, dle kontrolních zobrazovacích vyšetření došlo k progresi onemocnění, a proto byla ukončena a doporučeno pouze sledování. V listopadu 2015 byla pacientka převzata do péče onkologie Masarykova onkologického ústavu (MOÚ) pro klinickou progresi s bolestmi břicha a zvětšením expanze v retroperitoneu. Druhým čtením byla potvrzena histologická diagnóza, imunohistochemicky byly negativní c‑kit, EGFR, ALK, PDGFR‑A. V červnu 2016 byla zahájena paliativní léčba mTOR inhibitorem sirolimem opět ve snaze zpomalit růst AML. Na uroonkologii MOÚ byla pacientka odeslána v únoru 2018 pro zhoršující se bolesti v dutině břišní. Dle CT byly AML podkovovité ledviny narostlé do gigantických objemů (Obr. 1a–b). Díky rozsáhlému defektu stěny břišní po předchozích operacích zatím nezpůsobily syndrom utlačení orgánů dutiny břišní. Pacientka byla ohrožena rizikem spontánního krvácení z nádoru a při další progresi také renálním selháním z útlaku parenchymu ledviny. Pacientce byla navržena nefrektomie na jedné straně s následnou transplantací ledviny ipsilaterálně a následná nefrektomie zbylé části podkovovité ledviny. Jako alternativa pak pokus o opětovný debulking tumoru s úpravou břišní kýly. Byla poučena o riziku komplikací obou variant a zvolila druhou možnost. V dubnu 2018 byla provedena parciální nefrektomie a debulking angiomyolipomů levé části podkovovité ledviny. Operace byla provedena bez ischemizace ledviny, četné resekční plochy byly průběžně ošetřovány suturou s klipy, což mělo za následek větší krevní ztrátu 3000 ml. Pro iatrogenní lézi levého proximálního ureteru při uvolňování tumorózní masy byla provedena laloková pyeloplastika pyeloureterální junkce se zavedením JJ stentu a navíc plastika ventrální kýly. Odstraněná masa tumoru vážila 1700 g (Obr. 2a–b). Další operace následovala po rekonvalescenci v srpnu 2018, kdy byl proveden debulking nádorové masy pravé části podkovovité ledviny s malou resekcí parenchymu, opět bez ischemizace parenchymu. Krevníztráty byly kolem 2300 ml a odstraněná masa nádoru vážila 1800 g. Patologem byl nález uzavřen jako AML (lipoma ‑ -like varianta) ledviny. Nádor vykazoval trifázický histomorfologický obraz, tvořený směsicí vyzrálé tukové tkáně, hladké svaloviny a nepravidelných silnostěnných cév, místy s hyalinizovanou vnitřní částí stěny (Obr. 3a). Imunohistochemicky byla prokázaná pozitivita SMA (Smooth Muscle Actin) v hladkosvalové komponentě a pozitivita HMB45 v perivaskulárních epiteloidních buňkách (Obr. 3b). Cytokeratiny byly negativní (CK AE1/3). S odstupem 16 měsíců je pacientka bez potíží, ledvinné funkce jsou v normě. Po operaci byla znovu nasazena terapie mTOR inhibitorem sirolimem pro klinicky suspektní syndrom tube ‑ rózní sklerózy, s cílem snížit další růst AML. Kont ‑ rolní CT břicha bylo hodnoceno jako stabilizace onemocnění, bez nových ložisek (Obr. 1c–d). U pacientky je plánováno genetické vyšetření. DISKUZE Po stanovení diagnózy AML je důležité rozlišit, jestli se jedná o sporadickou formu, nebo AML vázaný na syndrom TS (1). U menších sporadických nádorů dle nedávné systematické review Evropské urologické společnosti stačí aktivní sledování (AS), jelikož rostou většinou pomalu a ve studiích s AS bylo popsáno riziko krvácení pouze u 2 % (3). Arbitrárně stanovena veli ‑ kost AML 4 cm, kdy byla doporučena ablační léčba, je nyní zpochybňována a režim AS se zdá být bezpečný i pro větší nádory (2, 3, 7). Léčebný postup je ale nutné individuálně upravit nejenom podle velikosti nádoru, ale také s ohledem na jejich četnost, postižení jedné nebo obou ledvin, přítomnost syndromu TS, symptomy, věk pacienta a jeho komorbidity, je nutno brát v úvahu i socioekonomické prostředí pacienta, jako tomu bylo v tomto případě. U větších nádorů nebo při nejasném nálezu na zobrazovacích vyšetřeních je nutné myslet také na možnost epiteloidní varianty AML, která má agresivnější chování a metastatický potenciál (1). Z léčebných možností u sporadického AML je doporučován vždy, pokud je to technicky možné, ledvinu‑záchovný postup (1, 2). Na prvním místě je parciální nefrektomie, jako alternativy lze využít selektivní arteriální embolizaci a perkutánní nebo laparoskopickou termální ablaci (radiofrekvenční ablace nebo kryoablace) (1, 5). Vzhledem k charakteru cévního zásobení podkovovité ledviny, celkovému objemu tumorózní masy, mnohočetnosti a oboustrannosti tumoru nebylo možno uplatnit principy standardně aplikované při parciální nefrektomii. Obě fáze parciální nefrektomie byly provedeny bez ischemizace parenchymu s cílem maximálního zachování renálních funkcí. Tomu odpovídaly i pooperační krevní ztráty. Syndrom tuberózní sklerózy je autosomálně dominantní onemocnění, které je způsobeno mutací genu TSC1 nebo TSC2, s následnou zvýšenou akti ‑ vitou mTOR signální dráhy. AML u syndromu TS je často multifokální, bilaterální, s rychlejším růstem (1).U dospělých pacientů s asymptomatickým AML nad 3 cm je na prvním místě doporučována léčba mTOR inhibitorem everolimem a v druhé linii ledvinu‑záchovné postupy, jako jsou parciální nefrektomie nebo selektivní arteriální embolizace (6, 8). Ve studii EXIST-2 byl srovnáván everolimus s placebem u nemocných s AML u syndromu TS a prokázal vyšší odpověď na léčbu a delší čas do progrese. Při hodnocení dlouhodobé účinnosti popsali Bissler et al. výsledky u 102 pacientů s mediánem objemu AML 92 cm3 . Odpověď na léčbu everolimem definovanou jako redukce objemu nádoru o ≥ 50 % byla dosažena u 58 % a ≥ 30 % u více než 75 % nemocných (9). Everolimus je tedy dlouhodobě účinným a bezpečným postupem léčby. Nejčastějšími nežádoucími účinky jsou infekce (imunosupresivum), hypercholesterolemie, hypertriglyceridemie a hyperglykemie. Pro léčbu objemných AML nad 15–20 cm neexistují jasná doporučení. Pokud je to technicky možné, tak na prvním místě je cytoredukce s ledvinu‑záchovným výkonem, alternativou je nefrektomie. Efekt systémové léčby při této velikosti AML je menší než ve studiích s AML < 10 cm. Toriu et al. popsali zkušenost s léčbou everolimem u třech AML s průměrem nad 20 cm a po třech letech léčby dosáhli redukci objemu o 9–23 % (10). Kombinace systémové léčby mTOR inhibitory s konsolidační chirurgickou léčbou se jeví být optimálním postupem u této skupiny nemocných.
Obr. 1. Předoperační nález objemného angiomyolipomu (označen hvězdičkou) podkovovité ledviny s rozsáhlou ventrální hernií v sagitálním (a) a frontálním (b) řezu počítačové tomografie. Nález po cytoredukčních operacích v sagitálním (c) a frontálním (d) řezu. Hernie a podkovovitá ledvina označeny šipkou.
Fig. 1. Preoperative finding of a bulky angiomyolipoma (asterisk) of a horseshoe kidney with extensive ventral hernia in sagittal (a) and frontal (b) sections on computer tomography. Postoperative finding after cytoreductive surgery in sagittal (c) and frontal (d) sections. Hernia and kidney marked with an arrow.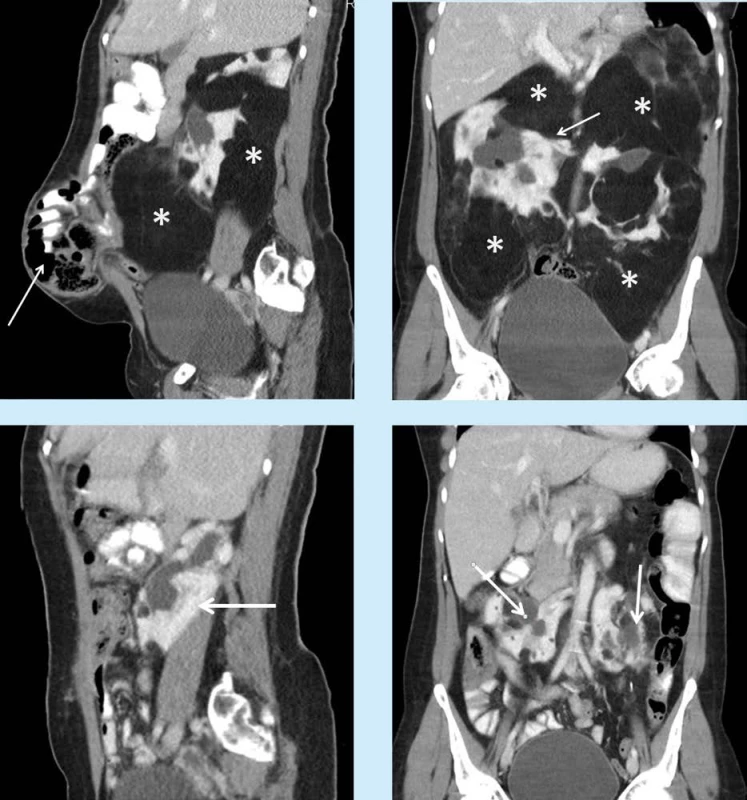
Obr. 2. Obsahem ventrální kýly byly střevní kličky, dutina břišní vyplněna tumorem (označen šipkou) (a). Odstraněný preparát angiomyolipomu při jedné z cytoredukčních operací (b).
Fig. 2. Small intestine was packed in ventral hernia as abdominal cavity was completely filled with kidney tumour (arrow) (a). Angiomyolipoma mass removed during one of cytoreductive surgeries (b)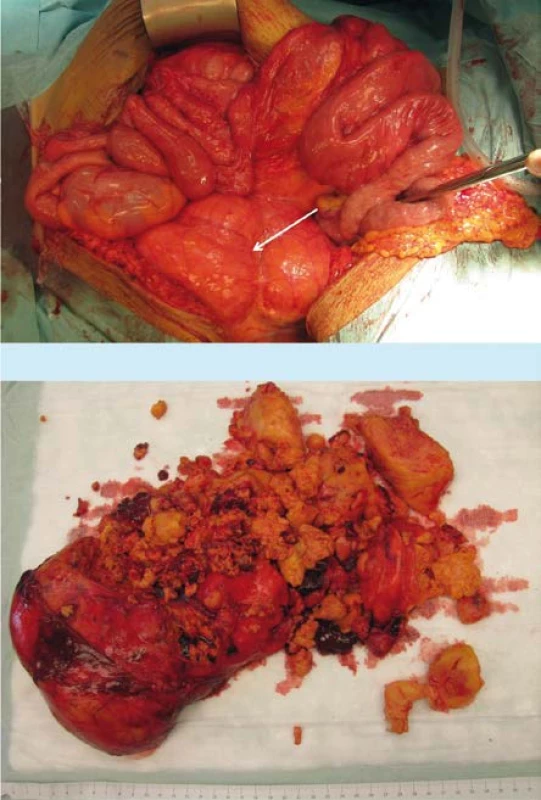
Obr. 3. Histologický nález angiomyolipom v barvení hematoxylin-eosin (a) a pozitivita HMB45 v perivaskulárních epiteloidních buňkách (b).
Fig. 3. Histological finding of angiomyolipoma in hematoxylin-eosin staining (a) and HMB45 positivity in perivascular epithelioid cells (b).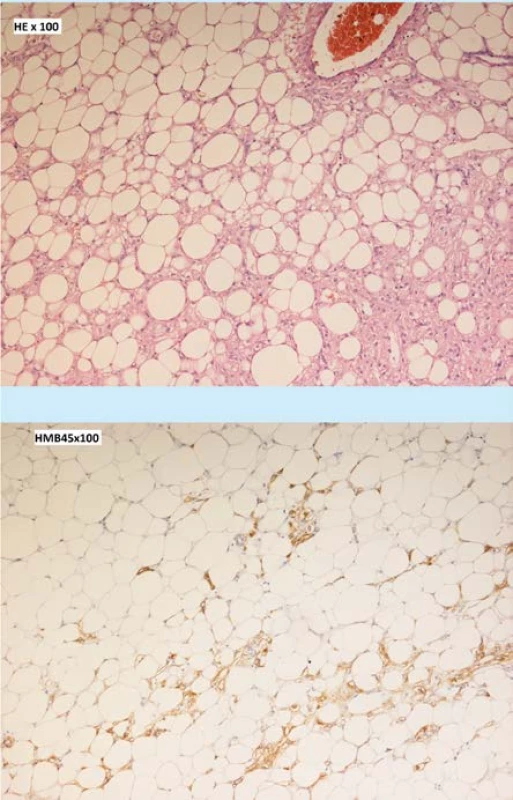
ZÁVĚR
AML má nejčastěji sporadický výskyt s pomalým růstem, u většiny pacientů s menším nádorem postačuje sledování a v případě nutnosti léčby je preferován ledvinu‑záchovný postup. V případech vazby AML na syndrom TS může mít onemocnění odlišný průběh s multifokálním výskytem a rychlou progresí. U těchto případů je kromě chirurgické léčby na zvážení kombinace se systémovou léčbou mTOR inhibitory. Podpořeno MZ ČR – RVO (MOÚ, 00209805)
Střet zájmů: Žádný.
Prohlášení o podpoře: Autoři prohlašují, že práce nevznikla s finanční podporou.
Došlo: 30. 1. 2020
Přijato: 13. 2. 2020
Kontaktní adresa:
MUDr. Markéta Hulová
Oddělení urologické onkologie,
Masarykův onkologický ústav,
Žlutý kopec 543/7,
602 00 Brno
e‑mail: marketa.hulova@mou.cz
Zdroje
1. Flum AS, Hamoui N, Said MA, et al. Update on the Diagnosis and Management of Renal Angiomyolipoma. J Urol 2016; 195 : 834–846.
2. Ürge T, Pitra T, Chudáček Z, et al. Nové trendy v léčbě renálního angiomyolipomu. Ces Urol 2015; 19(2): 106–117.
3. Fernández‑Pello S, Hora M, Kuusk T, et al. Management of sporadic renal angiomyolipomas: a systematic review of available evidence to guide recommendations from the European Association of Urology renal cell carcinoma guidelines panel. Eur Urol Oncol 2019 Jun 3. pii: S2588-9311(19)30054-9.
4. Paldus V, Šámal V, Mečl J, et al. Wunderlichův syndrom – soubor pacientů s netraumatickým spontánním krvácením do retroperitonea. Ces Urol 2019; 23 : 230–236.
5. Hušek P, Košina J, Pacovský J, et al. Roboticky asistovaná resekce objemného angiomyolipomu levé ledviny. Ces Urol 2018; 22 : 234–237.
6. Samuels JA. Treatment of renal angiomyolipoma and other hamartomas in patients with tuberous sclerosis complex. Clin J Am Soc Nephrol 2017; 12 : 1196–1202.
7. Bhatt JR, Richard PO, Kim NS, et al. Natural history of renal angiomyolipoma (AML): most patients with large AMLs >4 cm can be offered active surveillance as an initial management strategy. Eur Urol 2016; 70 : 85–90.
8. McCormack FX, Inoue Y, Moss J, et al. Efficacy and safety of sirolimus in lymphangioleiomyomatosis. N Engl J Med 2011; 364 : 1595–1606.
9. Bissler JJ, Kingswood JC, Radzikowska E, et al. Everolimus long‑term use in patients with tuberous sclerosis complex: four‑year update of the EXIST-2 study. PLoS One 2017; 12: e0180939.
10. Toriu N, Mizuno H, Sawa N, et al. Everolimus reduces the size of tuberous sclerosis complex‑related huge renal angiomyolipomas exceeding 20 cm in the longest diameter. Case Rep Oncol 2018; 11 : 258–267.
Štítky
Dětská urologie Nefrologie Urologie Onkologie
Článek Editorial
Článek vyšel v časopiseČeská urologie
Nejčtenější tento týden
2020 Číslo 1- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Kterým pacientům se SLE nasadit biologickou léčbu?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Nostiriazyn – spolehlivá 1. volba u nekomplikovaných infekcí močových cest
- Nitrofurantoin s řízeným uvolňováním: osvědčená účinnost, lepší snášenlivost a méně tablet při akutní cystitidě
-
Všechny články tohoto čísla
- Editorial
- Roboticky asistovaná okluze vezikovaginální píštěle – krok za krokem
- Multirezistentní gram‑negativní bakterie v urologii
- Hereditární renální nádorové syndromy
- Incidence karcinomu prostaty v preparátech po radikální cystoprostatektomii. Histopatologická charakteristika nádorů a posouzení vlivu histologického zpracování preparátu na incidenci nádoru
- Naše zkušenosti s využitím MRI/TRUS softwarové fúze při cílené biopsii prostaty
- Gravidita u pacientek po augmentaci měchýře střevním segmentem – naše zkušenosti
- Kazuistika gigantického recidivujícího angiomyolipomu podkovovité ledviny
- Možnost řešení obstrukce dolního segmentu ledviny u zdvojené pánvičky pomocí roboticky asistované pyelo‑pyelo anastomózy systémem da Vinci XI®
- Vzpomínka na emeritního přednostu Urologické kliniky FN Hradec Králové pana docenta MUDr. Josefa Bašeho, CSc.
- Česká urologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Naše zkušenosti s využitím MRI/TRUS softwarové fúze při cílené biopsii prostaty
- Multirezistentní gram‑negativní bakterie v urologii
- Hereditární renální nádorové syndromy
- Kazuistika gigantického recidivujícího angiomyolipomu podkovovité ledviny
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



