-
Medical journals
- Career
Laparoskopická nefrektomie při léčbě atrofické ledviny postižené vážnou infekcí
Authors: H. Yanaihara
Published in: Urol List 2013; 11(1): 23-26
Overview
Díky zdokonalování vybavení i samotných operačních technik lze v současné době laparoskopický přístup využívat prakticky v jakémkoli chirurgickém kontextu. Laparoskopická nefrektomie při léčbě atrofické ledviny postižené závažnou infekcí představuje však i nadále komplikovanou proceduru, která je vzhledem k nepředvídatelné povaze perinefrických zánětlivých změn spojena s vysokou mírou konverze k otevřené operaci a nutnosti krevní transfuze. Tento výkon je bohužel v každodenní praxi poměrně ojedinělý, a k dispozici tedy máme pouze několik studií na této téma. Standardní postup pro léčbu tohoto onemocnění navíc nebyl nikdy definován. Prvním krokem je v každém případě kontrola infekce. Nefrektomie by měla být v ideálním případě indikována až měsíc po kompletním vyléčení infekce. Osobně doporučujeme pro tento výkon transperitoneální přístup, v některých případech je však vhodné provedení i retroperitoneálního přístupu. Operační technika by měla být preciznější než při obvyklých výkonech, v některých momentech může být nezbytné učinit odvážné rozhodnutí, abychom vůbec pokročili dále. Pooperační průběh je obvykle bez komplikací. Laparoskopická nefrektomie při léčbě atrofické ledviny postižené vážnou infekcí může být obtížná. Délka výkonu je však srovnatelná s délkou laparoskopické radikální nefrektomie. Pro zkušené operatéry by tato technika měla být možností první volby a měla by být v každém případě zohledněna i méně zkušenými chirurgy.
Klíčová slova:
laparoskopická nefrektomie, atrofická ledvina, infekce
Zdokonalení laparoskopického přístupu nás přimělo vyzkoušet tuto techniku i při léčbě obtížnějších případů. Při léčbě onkologických onemocnění je standardní chirurgický postup víceméně jasně dán a k dispozici jsou spousty podobných případů. Tyto operační výkony lze tedy snadno popsat a vyhledat v běžné praxi. Nefrektomie u pacienta se závažným infekčním onemocněním představuje (vzhledem k ojedinělosti těchto případů) pro operatéra ovšem zcela odlišnou chirurgickou situaci a rovněž lze očekávat potíže při preparaci tkáně změněné zánětlivým procesem. Zejména laparoskopická nefrektomie může vzhledem k omezeným zkušenostem (na rozdíl od běžné radikální nefrektomie) představovat skutečný oříšek.
V tomto článku hodnotíme publikace zabývající se laparoskopickou nefrektomií při léčbě atrofické ledviny u pacientů se závažnou infekcí a prezentujeme vlastní zkušenosti s peroperačním průběhem.
VHODNÍ KANDIDÁTI PRO LAPAROSKOPICKOU NEFREKTOMII
Renální parenchym by měl být prakticky nefunkční nebo by měl benefit nefrektomie minimálně převážit zachování funkce ledvin. Průvodní onemocnění obvykle zahrnují urolitiázu a obstrukci ureteropelvické junkce. Xantogranulomatózní pyelonefritida je velmi vzácné onemocnění, ale tito pacienti mohou být rovněž vhodnými kandidáty. Podobně vzácnou diagnózou může být ledvina postižená tuberkulózou. Všechny informace je třeba otevřeně probrat s pacientem. Zejména může být důležité pacienta upozornit na vysokou míru krevní transfuze (7–12 %) a konverze k otevřené operaci (5–17 %), ačkoli my jsme se v našem souboru s výše uvedeným nesetkali [1–5]. Předpokládá se, že tyto komplikace souvisí zčásti s užitím bipolárního a/nebo zacelovacího zařízení, které se začaly využívat kolem roku 2006. U pacientů s nekontrolovanou infekcí nemůže být v současné době v našem centru indikována laparoskopická nefrektomie. Všechny naše případy jsou uvedeny v tab. 1.
Table 1. Předoperační a peroperační parametry. 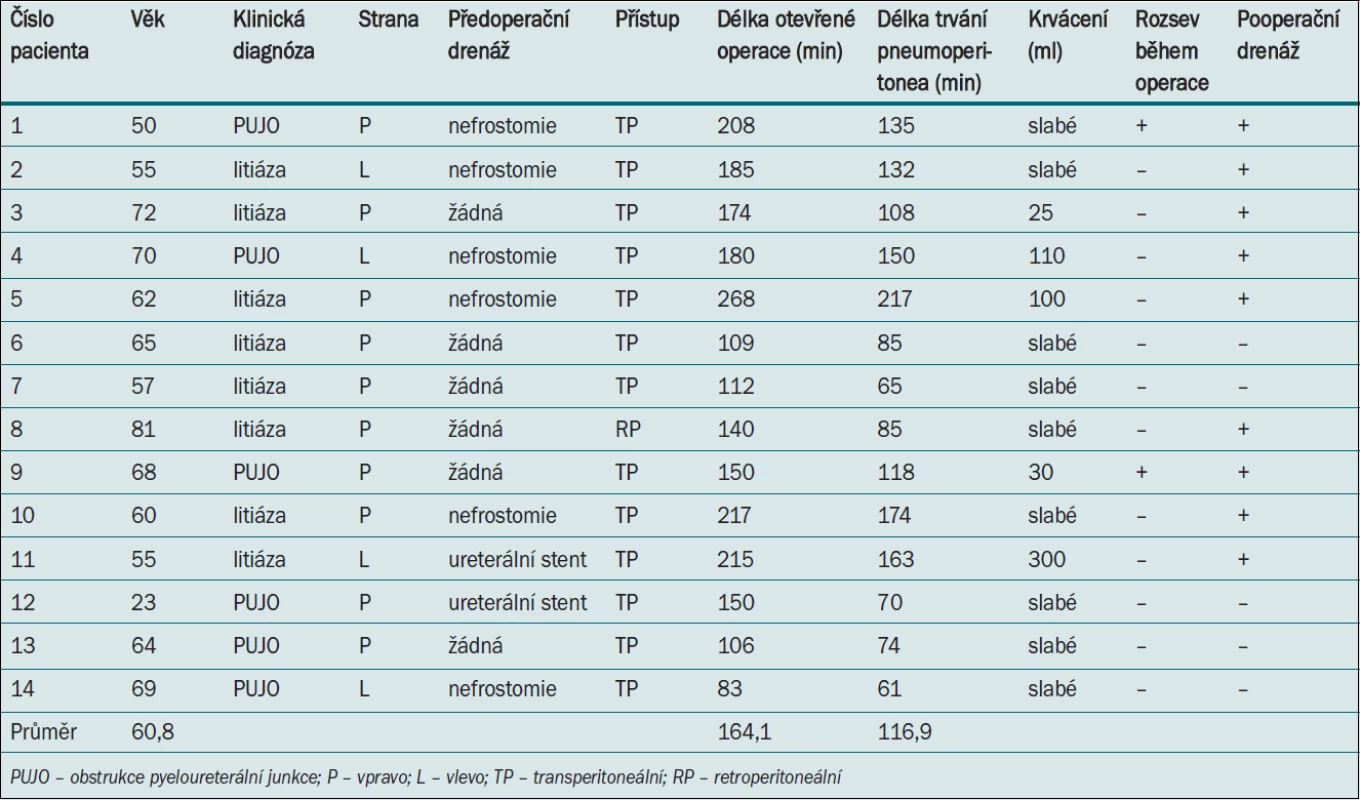
LÉČBA INFEKČNÍ LEDVINY
Bylo by skutečně žádoucí, kdyby bylo možné infekci kontrolovat pouze aplikací antibiotik. Tento postup však může způsobit pouhé zamaskování infekčního materiálu v ledvinné pánvičce, jenž může kdykoli znovu způsobit další infekci. V tomto případě obsahuje pánvička obvykle hnisavou tekutinu. Zavedení drénu, včetně nefrostomie nebo ureterálního stentu, nemá výrazný dopad na průběh samotné operace, pakliže není zavedení indikováno. Nefrostomie zavedená posteriorně přímo do ledvinné pánvičky může vyvolat zbytečné zánětlivé změny (obr. 1).
Image 1. Nefrostomie byla zavedena přímo do ledvinné pánvičky. Kolem renálního hilu je patrná závažná zánětlivá změna. 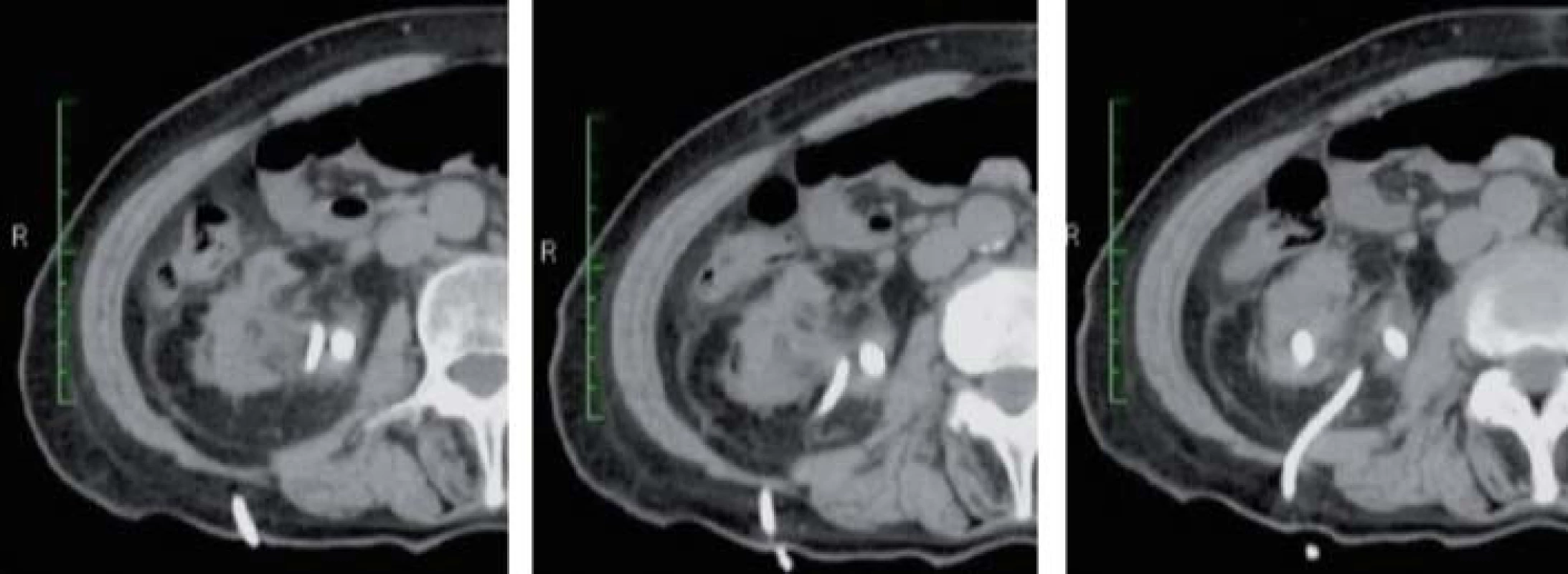
Obecně rozporuplným tématem je, zda zavádět raději nefrostomii nebo ureterální stent. V našem centru preferujeme nefrostomii, neboť obvykle umožňuje kontrolovat infekci a umožňuje přesně sledovat funkci ledviny. Z celkem 14 případů jsme nefrostomii zaváděli v šesti případech, ureterální stent ve dvou a šest případů se obešlo bez jakékoli drenáže. Katz et al popisují užití nefrostomie v 75 % případů [2].
Po zlepšení celkového stavu není aplikace antibiotik nezbytná, pakliže je zaveden drén (zejména nefrostomie). Pokud není zaveden drén, mohou antibiotika pomoci zabránit recidivě infekce, ale záleží na konkrétních okolnostech.
PŘED STANOVENÍM DATA OPERACE
Po kompletním vymizení infekce se doporučuje pacientovi minimálně měsíční klidový režim, protože u většiny pacientů trvá vyléčení infekce delší dobu, a pacienti jsou tak psychicky i fyzicky vyčerpaní. Tito pacienti navíc často trpí dalšími chorobami, jako je např. diabetes mellitus, onemocnění vyžadující léčbu steroidy nebo dialýzu, srdeční onemocnění ap. Měsíční pauza před finálním rozhodnutím je přínosná jak pro pacienta, tak pro jeho lékaře. Mezitím můžeme pacienta vyšetřit a připravit jej na pooperační péči. Než dojde ke zlepšení celkového stavu, může pacient v klidu přijmout nevyhnutelnost operačního výkonu.
Někteří pacienti si mohou stěžovat na zavedený drén, kvůli němuž může chtít lékař tuto nepříjemnou situaci co nejvíce zkrátit. V tomto ohledu nebylo dosaženo konsenzu, rozhodně se však nedoporučuje postup urychlit.
PŘEDOPERAČNÍ PÉČE
U pacientů se srdečními problémy je naprosto nezbytná přísná kontrola hladiny krevního cukru a volba antikoagulancia. Dále je nezbytné vyšetření funkce plic a srdce. Postup je téměř stejný jako před obvyklou operací.
Před operací neprovádíme přípravu střeva ani klyzma. Před elektivní kolorektální operací se nedoporučuje mechanická příprava střeva a tento postup byl převzat i urology [6,7]. Tři hodiny před výkonem je zakázán příjem tekutin. Antibiotika jsou obvykle aplikována až přímo před provedením incize.
PŘÍSTUP
V každém případě preferujeme transperitoneální přístup. Z celkem 14 pacientů byl retroperitoneální přístup indikován pouze u jedinců s ventrikulo-peritoneálním zkratem (shunt), abychom zabránili šíření mikroorganizmů do mozku. Jednou z výhod transperitoneálního přístupu je široký pracovní prostor. Hilus ledviny je často překryt tuhou tkání a je velmi obtížné ji uvolnit. Pečlivé sledování je v takto širokém prostoru užitečné pro provedení adekvátní preparace. Obvykle slýcháváme, že infekční ledvinu je nezbytné odstranit při otevřené nefrektomii z retroperitoneálního přístupu. Cílem tohoto postupu byla prevence rozšíření infekčního materiálu do sterilní dutiny břišní, což je částečně pochopitelný postup, ale pokud je operatér velmi opatrný, bude rozsev infekce minimální, a pokud nelze většímu rozšíření zabránit, zavedení drénu zajistí normální pooperační průběh.
BĚHEM OPERACE
Drén je vyjmut před zarouškováním. Tlak v pneumoperitoneu je obykle nastaven na 8 mmHg. Před odhalením hilu je nutné uvolnit adheze s okolními orgány, což ovšem bohužel nelze předvídat až do samotného zahájení výkonu. Pankreas, duodenum, kolon, slezinu a vena cava je nutné uvolnit velmi opatrně a s extrémní péčí. Skryté cévy mohou způsobit náhlé krvácení z adhezí i při užití zacelovacího zařízení. Ve většině případů však lze krvácení kontrolovat pomocí zacelovacího zařízení v prostředí vyššího tlaku (až 20 mmHg tlak pneumoperitonea).
Jakmile dosáhneme renálního hilu, může být nejhorším možným scénářem čekání na hlavního operatéra. Obvykle jsme nuceni dodržovat pravidlo „nejprve podvázat arterii renálního hilu“. Při tomto výkonu však musí být operatér připraven na základě situace flexibilně toto pravidlo změnit. Renální arterie je obvykle atrofická, kvůli čemuž je krevní zásobení ledviny značně omezené. Velikost renální žíly je často zachována, žíla je v některých případech překryta tuhou tkání. Pokud jsou arterie i žíla jasně viditelné, můžeme opatrně pokračovat v operaci. Pakliže je arterie příliš tenká, je možné ji incidovat pouze pomocí zacelovacího zařízení. V nejhorším možném případě nelze renální cévu přerušit v tuhé tkáni kolem renálního hilu. Za těchto okolností musí být operatér připraven přejít k otevřené operaci. Jednou z možností pro zkušené operatéry je přerušení celého hilu pouze pomocí zacelovacího zařízení. Může to znít trochu jako don quijotovský počin, ale pokud uvážíme omezené krevní zásobení ledviny, může se jednat o realistickou možnost, jak překonat takto změněný hilus ledviny.
Po ukončení preparace renálního hilu můžeme ledvinu vyjmout z retroperitoneální dutiny. Perinefrické adheze lze bezpečně incidovat pomocí zacelovacího zařízení s hrotem. Pokud bylo odstraněno ložisko infekce, nepředstavuje odstranění ledviny i s Gerotovou fascií problém. Jednou z možností, jak operaci dokončit, může být dokonce subkapsulární nefrektomie. Jizva po nefrostomii tuto proceduru nijak nenaruší.
Uvolněnou ledvinu vyjmeme obvyklým způsobem. Drén zavádíme pouze v případě nutnosti. Dokonce i v případě, že dojde k masivnímu rozsevu obsahu ledvinné pánvičky, může být proplach daleko důležitější než drenáž. Drén jsme zavedli v devíti ze čtrnácti případů. S ohledem na výsledný stav se domníváme, že ve většině případů nebylo zavedení drénu nutné.
Operace může trvat déle než běžná radikální nefrektomie a lze rovněž očekávat větší krevní ztrátu. Publikované série však vykazují dobré výsledky [1–5]. U námi popisovaných 14 případů činila průměrná délka operace 164 ± 52 min (83–268 min) a průměrná krevní ztráta 40 ± 83 ml (0–300 ml). V žádném případě naštěstí nebyla nutná krevní transfuze ani přechod k otevřené operaci. Domníváme se, že hlavním důvodem je skutečnost, že výkony byly prováděny až po roce 2007, odkdy jsou k dispozici bipolární a zacelovací zařízení. Nefrektomie u pacientů s xantogranulomatózní pyelonefritidou se však liší od běžných výkonů. V tomto případě se uvádí vyšší míra konverze (26–40 %) [4,8,9].
POOPERAČNÍ PÉČE
Tekutiny může pacient přijímat okamžitě po plném procitnutí z celkové anestezie. Rutinní profylaxe antibiotiky není po správně provedené operaci nutná. Můžeme pozorovat mírně zvýšenou tělesnou teplotu, obvykle až 38 °C, po několika dnech však dojde k poklesu i bez aplikace antibiotik. Druhý den po operaci je možné vyjmout drén. Již první den může pacient přijímat potravu. Tato operace nevyžaduje žádnou speciální pooperační péči. Ačkoli to nemusí být nezbytné, vždy provádíme třetí měsíc po operaci CT vyšetření pro kontrolu pooperačních změn.
ZÁVĚR
Laparoskopická nefrektomie u pacientů s infekčním onemocněním obvykle představuje komplikovanou operaci a bohužel se rozhodně nejedná o běžný výkon. Starší publikace uvádí vysokou míru krevní transfuze a konverze k otevřené operaci, a to dokonce v případě, že operaci prováděl zkušený operatér. V současné době však již lze technické obtíže díky zdokonalení instrumentária překonat. Zkušený operatér by měl volit laparoskopickou operaci za všech okolností a je to přirozený trend laparoskopických operatérů. Je třeba si však vždy uvědomovat technická omezení v jednotlivých případech a vždy mít po ruce plán B pro neočekávané situace.
Dokud benefit laparoskopické techniky převáží obtíže s ní spojené, doporučujeme volit laparoskopickou nefrektomii (po řádné přípravě) i u pacientů s infekčním onemocněním.
Adresa pro korespondenci:
Hitoshi Yanaihara, MD
Associate Professor
Saitama Medical University
Department of Urology
38 MorohongoMoroyama-Cho, Iruma
Saitama, JAPAN
yanaihara.h@gmail.com
Sources
1. Shekarriz BS, Meng MV, Lu HF et al. Laparoscopic nephrectomy for inammatory renal conditions. J Urol 2001; 166(6): 2091–2094.
2. Katz R, Pode D, Golijanin D et al. Laparoscopic nephrectomy for infected,obstructed and nonfunctioning kidneys. Surg Laparosc Percutan Tech 2004; 14(6): 340–343.
3. Manohar T, Desai M, Desai M et al. Laparoscopic nephrectomy for benign and inammatory conditions. J Endourol 2007; 21(11): 1323–1328.
4. Duarte RJ, Mitre AI, Chambô JL et al. Laparoscopic nephrectomy outside gerota fascia for management of inflammatory kidney. J Endourol 2008; 22(4): 681–686.
5. Tobias M, Lasmar MT, Batista LT et al. Laparoscopic nephrectomy in inammatory renal disease: proposal for a staged approach. Int Braz J Urol 2005; 31(1): 22–28.
6. Sugihara T, Yasunaga H, Horiguchi H et al. Does Mechanical Bowel Preparation Improve Quality of Laparoscopic Nephrectomy? Propensity Score-matched Analysis in Japanese Series. Urology 2013; 81(1): 74–79.
7. Yanaihara H, Sakamoto F, Matsushima M et al. Clinical assessment of perioperative course of patients undergoing laparoscopic nephrectomy or adrenalectomy without perioperative bowel management. Hinyokika Kiyo 2011; 57(8): 407–409.
8. Khaira HS, Shah RB, Wolf JS. Laparoscopic and open surgical nephrectomy for xanthogranulomatous pyelonephritis. J Endourol 2005; 19(7): 813–817.
9. Arvind NK, Singh O, Ali Q et al. Laparoscopic nephrectomy in xanthogranulomatous pyelonephritis: 7-year single-surgeon outcome. Urology 2011; 78(4): 797–801.
Labels
Paediatric urologist Urology
Article was published inUrological Journal

2013 Issue 1-
All articles in this issue
- Využití inhibitorů fosfodiesterázy v urologii při léčbě erektilní dysfunkce
- Tadalafil v léčbě LUTS/BPH a ED
- Léčba zanořeného penisu
- Varikokéla a smysl jejího řešení
- Laparoskopická nefrektomie při léčbě atrofické ledviny postižené vážnou infekcí
- Simultánní ipsilaterální nefrektomie a transplantace ledviny u pacientů s polycystickým onemocněním ledviny
- Retroperitoneální laparoskopická nefrektomie u pacientů léčených pomocí peritoneální dialýzy
- Předběžné výsledky transperitoneální laparoendoskopické radikální nefrektomie s užitím improvizovaného čínského zařízení s jedním portem
- Hodnocení současných trendů a kontroverzních otázek při užívání ureterálních stentů
- Vede časná ESWL po PCNL k uvíznutí konkrementů v přístupovém kanále? Mýtus nebo skutečnost
- Preference pacientů pro pokročilé urologické techniky: vodítko pro budoucí vývoj chirugické léčby?
- Bipolární plazmatická vaporizace prostaty při léčbě symptomatického zvětšení prostaty: klinické výsledky po dvou letech sledování
- Pohlavie ako faktor ovplyvňujúci klinicko-patologické ukazovatele a prognózu karcinómu obličky
- Guidelines EAU pro léčbu zakřivení penisu
- Urological Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Léčba zanořeného penisu
- Varikokéla a smysl jejího řešení
- Guidelines EAU pro léčbu zakřivení penisu
- Hodnocení současných trendů a kontroverzních otázek při užívání ureterálních stentů
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

