-
Medical journals
- Career
VYUŽITIE MULTIPLEXNEJ RT PCR V DIAGNOSTIKE MIKROBIONÁLNYCH PATOGÉNOV
Authors: Marianna Trebuňová 1,2; Ivan Vanát 1; Zuzana Vaczy 1; Ján Rosocha 1; Ladislav Bobák 1; Jozef Živčák 2
Authors‘ workplace: Združená tkanivová banka UNLP Košice, Košice, Slovensko 1; Katedra biomedicínskeho inžinierstva a merania SjF TU, Košice, Slovensko 2
Published in: Lékař a technika - Clinician and Technology No. 3, 2016, 46, 74-77
Category: Original research
Overview
Cieľom príspevku je poukázať na potenciál využitia diagnostickej súpravy AnyplexTM STI-7 (Seegene, Južná Kórea), ktorá využíva technológiu multiplexnej real time PCR. AnyplexTM STI-7 umožňuje detegovať sedem najčastejších sexuálne prenosných patogénov naraz v jednej PCR reakcii. Jedná sa o šesť mikrobiálnych patogénov (Chlamydia trachomatis, Neisseria gonorrhoeae, Mycoplasma hominis, Mycoplasma genitalium, Ureaplasma urealyticum a Ureaplasma parvum) a jeden protozoálny (Trichomonas vaginalis). Podľa údajov Európskych odporúčaní pre menežment negonokokových uretritíd z roku 2016 sú infekcie spôsobené Chlamydia trachomatis a Mycoplasma genitalium najčastejšie hlásenými sexuálne prenosnými ochoreniami. S použitím multiplexnej real time PCR AnyplexTM STI-7 sme zistili, že v našej skupine infertilných mužov bola Ureaplasma parvum najčastejšie detegovaným patogénom.
Kľúčové slová:
multiplexná real time PCR, AnyplexTM STI-7, chlamýdie, mykoplazmyÚvod
Sexuálne prenosné infekcie sú príčinou neplodnosti v 35 % prípadov. Ich príčinou je široké spektrum vírusových, bakteriálnych a protozoálnych patogénov.
Podľa údajov Svetovej zdravotníckej organizácie z roku 2012 pribudne denne vo vekovej skupine od 15 do 49 rokov 131 miliónov sexuálne prenosných ochorení zapríčinených Chlamydia trachomatis, 78 miliónov Neisseria gonorrhoeae a 142 miliónov Trichomonas vaginalis [1–4]. V Európe sú najčastejšie hlásenými sexuálne prenosnými ochoreniami infekcie spôsobené Chlamydia trachomatis a Mycoplasma genitalium („Európske odporúčania pre menežment negonokokových uretritíd“, 2016) [4–10].
Pre efektívne riešenie neplodnosti je preto potrebné zaviesť komplexné vyšetrenie pacienta na najčastejšie sexuálne prenosné ochorenia. Z hľadiska laboratórnej diagnostiky sa javí ako najefektívnejší komplexný skríning pôvodcov sexuálne prenosných ochorení. Takúto možnosť ponúka súprava AnyplexTM STI-7 (Seegene, Južná Kórea), ktorá využíva technológiu multiplexnej real time PCR. AnyplexTM STI-7 umožňuje detegovať sedem najčastejších sexuálne prenosných patogénov naraz v jednej PCR reakcii. Jedná sa o šesť mikrobiálnych patogénov (Chlamydia trachomatis, Neisseria gonorrhoeae, Mycoplasma hominis, Mycoplasma genitalium, Ureaplasma urealyticum a Ureaplasma parvum) a jeden protozoálny (Trichomonas vaginalis).
AnyplexTM STI-7 a multiplexná real time PCR
Multiplexná real time PCR je vysoko citlivá metóda, ktorá využíva technológiu multiplikácie viacerých cieľových sekvencií genetického materiálu v jednej reakčnej skúmavke. V tomto procese sa využívajú viaceré páry primerov a optimalizované reakčné podmienky. Za posledné roky zaznamenala technológia výrazný rozvoj, ktorý umožnil jej použitie aj v oblastiach, ktoré vyžadujú vysokú presnosť, spoľahlivosť a reprodukovateľnosť. Jednou z nich je aj laboratórna diagnostika infekčných ochorení. Práve v tejto oblasti si metóda multiplexnej real time PCR nachádza široké uplatnenie. Umožňuje rýchlo a spoľahlivo vyšetrovať rôzne typy biologických vzoriek a detegovať v nich mikrobiálne, vírusové a protozoálne patogény. Rýchlosť a spoľahlivosť získanej informácie je hlavným benefitom tejto metódy. Okrem kvalitatívneho hodnotenia, mnohé multiplexné testy umožňujú aj semikvantitatívne hodnotenie a následne zahájiť cielenú terapiu, sledovať priebeh a efektivitu liečby. V našom laboratóriu sme testovali možnosti využitia diagnostickej súpravy AnyplexTM STI-7(Seegene, Južná Kórea), ktorá slúži na diagnostiku hlavných patogénov sexuálne prenosných ochorení. Súprava má CE -IVD certifikát a preto je vhodná pre použitie v klinickej diagnostike. Juhokórejská firma Seegene je inovátorom v oblasti technológie multiplexnej real time PCR.
Technológia systému
Diagnostiké sety AnyplexTM sú založené na dvoch nových inovatívnych technológiách: technológii DPOTM a TOCETM [11,12].
DPOTM technológia
Technológia využíva systém DPO primerov (Dual Priming Oligonukleotide), ktoré sú štrukturálne a funkčne odlišné od bežných primerov, pričom je blokovaná tvorba nešpecifických templátov, a tým sa dosahuje trvalo vysoká špecifickosť aj za menej optimálnych reakčných podmienok.
DPO™ sa skladá z dvoch samostatných základných priming častí (5'-koniec stabilizátor a 3'-koniec určovateľ), spojených pomocou polydeoxyinozínového linkera - spojovacieho mostíka. Linker má tvar bubliny, sám o sebe nie je zapojený do primingu, ale skôr vymedzuje hranice medzi 5'-koncom a 3'-koncom.
Princíp technológie
DPO™ má dva funkčné väzobné regióny, pričom jeden je dlhší ako druhý a sú oddelené poly (I) linkerom. Tieto dva nerovnako dlhé väzobné regióny vytvárajú dvojaké väzobné reakcie, v dôsledku čoho sa tvorí cieľovo špecifický produkt.
V prvom kroku nastáva aktivácia Poly (I) linkera deoxyinozínu, ktorý má v dôsledku slabších vodíkových väzieb pomerne nízku hodnotu teploty topenia (Tm). Poly (I) linker tvorí štruktúru bubliny pri určitej teplote topenia a oddelí 5'-koniec stabilizátora od 3'-konca určovateľa na samostatný stabilizátor a určovateľ.
V druhom kroku prebehne prvá väzobná reakcia. Dlhší 5'-koniec sa prednostne viaže na templátovú DNA a iniciuje stabilné naviazanie. Pôsobí ako stabilizátor.
V treťom kroku prebehne druhá väzobná reakcia: Krátky 3'-koniec sa selektívne viaže na cieľové miesto a je základom pre cieľovo špecifické predĺženie. Pôsobí ako určovateľ.
Image 1. Princíp DPO<sup>TM</sup> technológie [13]. ![Princíp DPO<sup>TM</sup> technológie [13].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/b9622ae83254a9b1983e69f8779e51be.jpg)
TOCETM technológia
Technológia TOCE™ umožňuje multiplexnú detekciu hľadaných cieľových sekvencií DNA v jednej reakčnej skúmavke. Technológiou TOCE™ je možné realizovať kvalitatívny a zároveň aj semikvantívny test. Je to umožnené vďaka dvom použitým analýzam: Cyclic Catcher Melting Temperature Analysis a High Resolution Melting analysis. Použitie technológií DPOTM a TOCE™ v diagnostických súpravách posúva molekulárnu diagnostiku na novú, vyššiu úroveň.
Princíp technológie
Kľúčovými komponentmi TOCE™ technológie sú páry DPO™ primerov, pitchers a catchers. Pitcher je značkovací oligonukleotid, ktorý špecificky hybridizuje v cieľovej oblasti. Catcher je fluorescenčne značený templát.
Image 2. Princíp TOCE<sup>TM</sup> technológie. A: Primer a pitcher sa naviažu na cieľovú sekvenciu. B: Počas predĺženia je pitcher odstrihnutý DNA-polymerázou a označená oblasť je uvoľnená. C: Uvoľnená označená oblasť sa naviaže na catcher, ktorý má komplementárnu sekvenciu k uvoľnenej časti. D: Predĺženie označenej časti oddelí fluorescenčne značenú molekulu R od tzv. zhášacej molekuly Q, čo sa prejaví vznikom signálu [14]. ![Princíp TOCE<sup>TM</sup> technológie. A: Primer a pitcher sa naviažu na cieľovú sekvenciu. B: Počas predĺženia je pitcher odstrihnutý DNA-polymerázou a označená oblasť je uvoľnená. C: Uvoľnená označená oblasť sa naviaže na catcher, ktorý má komplementárnu sekvenciu k uvoľnenej časti. D: Predĺženie označenej časti oddelí fluorescenčne značenú molekulu R od tzv. zhášacej molekuly Q, čo sa prejaví vznikom signálu [14].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/744355a24722ebc7de00afcde686c834.jpg)
Hodnota teploty topenia catcher-a je závislá od dĺžky sekvencie. Táto vlastnosť slúži na vytváranie dostatočne odlíšiteľných templátov. Pre optimalizáciu TOCE™ môžeme hodnotu teploty topenia catcher-a ľahko upraviť, nie je obmedzená na cieľové sekvencie. Detekčné limity diagnostickej súpravy AnyplexTM STI-7 za použitia technológie TOCE™ sú porovnateľné s výsledkami testov na báze single plex real time PCR.
Technológia TOCE™ umožňuje identifikovať viac cieľových analytov súčasne v jednom kanáli. Signál je meraný v reálnom čase a analyzovaný na základe teploty topenia (Tm) catcher-a, ktorá slúži na detekciu prítomnosti cieľového analytu.
Parametrizácia a vyhodnotenie
V Laboratóriu pre diagnostiku infertility a banke spermií Združenej tkanivovej banky Univerzitnej nemocnice L. Pasteura v Košiciach sme vyšetrili v priebehu dvoch mesiacov 53 mužov (priemerný vek 31 rokov). Na izoláciu DNA boli použité dva typy vzoriek: ejakulát a moč. Odber biologického materiálu prebiehal v odberovej miestnosti za štandardných podmienok. Moč bol odoberaný v objeme 10-40 ml, vždy prvý prúd ranného moču. Skladovaný bol maximálne po dobu dvoch hodín, pri laboratórnej teplote a následne bol použitý na izoláciu DNA. Ejakulát bol odoberaný od pacientov po minimálne trojdňovej a maximálne sedemdňovej sexuálnej abstinencii do sterilnej nádoby. Následne prebiehalo jeho skvapalnenie v termostate po dobu 30 minút pri teplote 37°C. Vzorky ejakulátu boli použité na izoláciu DNA v časovom limite do 2 hodín od odberu. DNA bola izolovaná komerčnou súpravou od firmy QIAGEN: QIAamp DNA Mini kit. Izoláciu sme urobili podľa inštrukcií výrobcu s jedinou modifikáciou, keď sme predĺžili čas lýzy na 60 min [15]. Kvalita a koncentrácia izolovanej DNA bola stanovená spektrofotmetricky systémom NanoDrop. Na multiplexnú real time PCR sme použili prístroj od firmy BIO-RAD CFX 96 Real Time PCR System, verzia softwaru 2.0.5 a súpravu AnyplexTM STI-7 (Seegene, Južná Kórea). Súprava AnyplexTM STI-7 umožňuje detegovať sedem hlavných patogénov sexuálne prenosných infekcií v jednej PCR reakcii. Na obsluhu prístroja a definovanie reačných podmienok sme použili program Bio-Rad CFX Manager IVD Editor 1.6 a na kvalitatívne a semikvantitatívne vyhodnotenie výsledkov sme použili program Seegene Viewer (Obr. 3).
Image 3. Kvalitatívne a semikvantitatívne vyhodnotenie programom Seegene Viewer. UU - Ureaplasma urealyticum, UP - Ureaplasma parvum, MG - Mycoplasma genitalium, MH - Mycoplasma hominis, NG - Neisseria gonorrhoeae, CT - Chlamydia trachomatis, TV - Trichomonas vaginali, IC – interná kontrola. 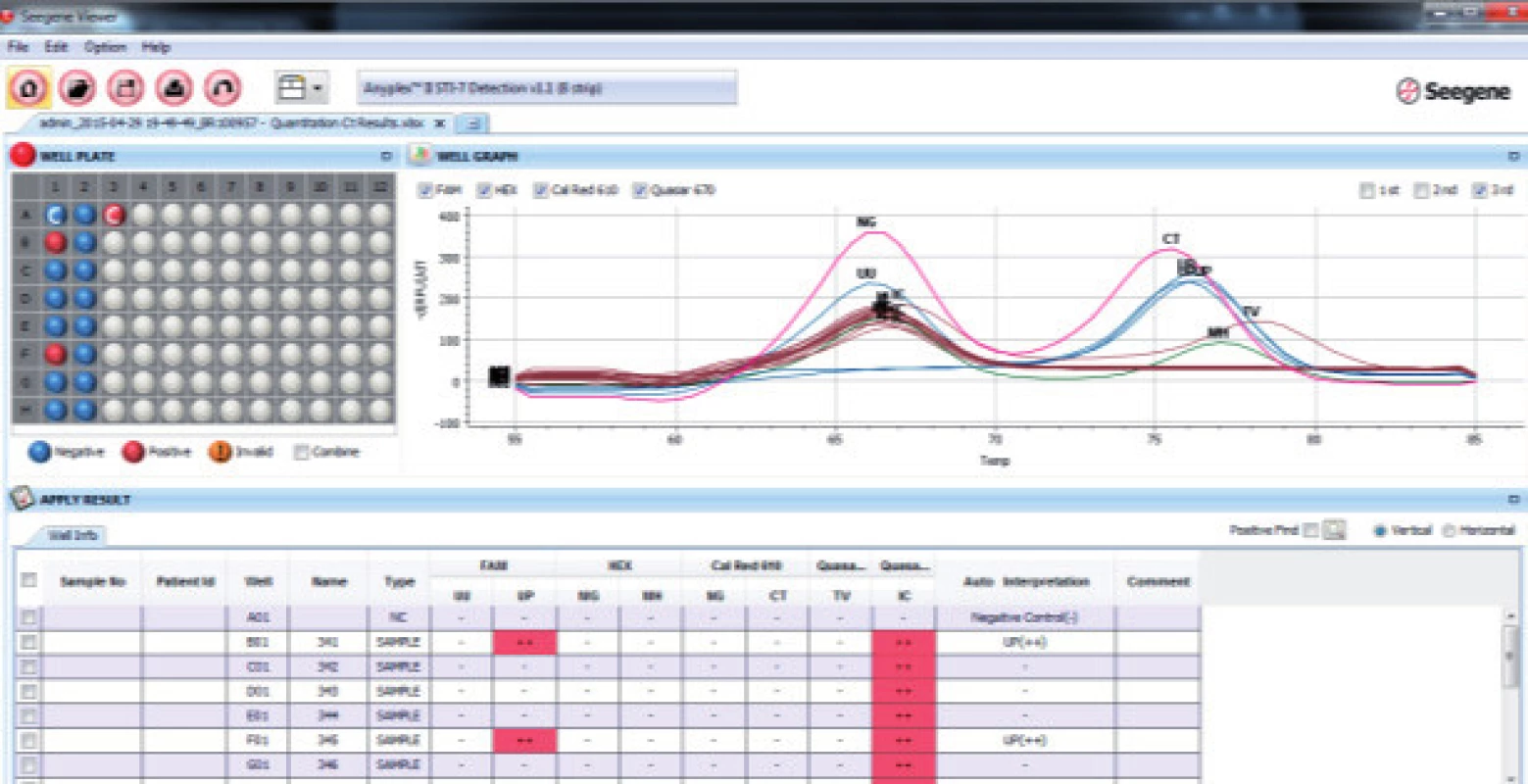
U 6-tich mužov sme vzorku DNA získali súbežne z ejakulátu a moču (100% zhoda výsledkov). U 5-tich mužov z tejto prvej vyšetrenej skupiny neboli potvrdené patogény. U jedného muža bola potvrdená kombinovaná infekcia Ureaplasma parvum (+) a Mycoplasma hominis (+). Zvyšnú skupinu tvorilo 47 mužov, kde sme vzorku DNA získali len z ejakulátu. U siedmich mužov v ejakuláte sme identifikovali Ureaplasmu parvum (++) a u jedného Ureaplasmu urealyticum (+). Vzorky ejakulátu 39 mužov z druhej vyšetrenej skupiny boli negatívne.
Diskusia a záver
Uvedenou metódou sme otestovali 53 vzoriek DNA izolovanej z moču a ejakulátu. Jedným zo zámerov testovania bolo zistiť využiteľnosť súpravy AnyplexTM STI-7 pre diagnostiku sexuálne prenosných ochorení z ejakulátu. Uvedený typ vzoriek sme testovali pre jednoduchosť prístupu k vzorkám, v Laboratóriu pre diagnostiku infertility sú vyšetrované spermiogramy infertilných mužov. Vzhľadom na odporúčania autorít vyšetrovať prvý prúd moču a/alebo výter z uretry metódami amplifikácie nukleových kyselín sme u niekoľkých pacientov porovnali výsledky vyšetrení vzoriek ejakulátu a moču.
Optimalizáciou podmienok izolácie DNA z ejakulátu sme docielili využiteľnosť súpravy AnyplexTM STI-7 aj pre dôkaz vybraných sexuálne prenosných patogénov v ejakuláte. Úspešnosť optimalizácie bola potvrdená spektrofotometrickým sledovaním výťažnosti a kvality DNA. Benefitom súpravy AnyplexTM STI-7 je interná kontrola kvality, ktorá slúži na kontrolu kvality izolácie DNA a možnosť vplyvu inhibičných látok na amplifikáciu DNA. Tým sa zároveň vylúčia falošne negatívne výsledky vyšetrenia.
Test je vhodný pre rýchlu laboratórnu diagnostiku sexuálne prenosných ochorení, umožňuje získať výsledok v deň odberu vzorky.
Môžeme konštatovať, že multiplexná real time PCR je vysoko citlivá metóda vhodná na skríning a diagnostiku sexuálne prenosných infekcií. Použitie in vitro diagnostických súprav AnyplexTM STI-7 umožňuje súčasnú detekciu siedmich patogénov sexuálne prenosných ochorení v jednej PCR reakcii, čím sa stáva diagnostika jednoduchšou a finančne efektívnejšou. V prípade potreby je možné získať finálne výsledky do siedmich hodín. Diagnostická súprava AnyplexTM STI-7 a použitý real time PCR systém CFX 96 spĺňa kritéria CE-IVD.
Poďakovanie
Práca bola podporená výzkumným grantom Vega č. 1/0515/13.
Dr.h.c. prof. Ing. Jozef Živčák, Ph.D.
Katedra biomedicínskeho inžinierstva a merania
Strojnícka fakulta
Technická univerzita v Košicach
Letná 9, SK-042 00 Košice
E-mail: jozef.zivcak@tuke.sk
Phone: +421 556 022 381
Sources
[1] Maruška, M.; Darja, K.; Jovan, M.; Mojca, M.: Clinical role of Ureaplasma parvum and Ureaplasma urealyticum presence in female lower urogenital tract: is there a place for routine screening and treatment?. Zdrav. Vestn. 2014, 83 : 629–637.
[2] WHO Sexually transmitted infections. World Health Organization 2013; Available November 15, 2013 from: http://www.who.int/mediacentre/factsheets/fs110/en/.
[3] World Health Organisation. Sixty-ninth World Health Assembly, document WHA69/2016/REC/1, GLOBAL HEALTH SECTOR STRATEGY ON SEXUALLY TRANSMITTED INFECTIONS 2016–2021, TOWARDS ENDING STIs, June 2016, 64 pp.
[4] Horner, P.J.; Blee, K.; Falk, L.; van der Meijden, W.; Moi, H.: European Guideline on the management of non-gonococcal urethritis. 2016, 26 pp.
[5] Holmes, K.K.; Stamm, W.E.; Sobel, J.D.: Lower genital tract infection syndromes in women. In: Holmes KK, Sparling PF, Stamm WE, Piot P, Wasserheit JN, Corey L, et al, eds. Sexually transmitted diseases. 4th ed. New York: McGraw-Hill; 2008. p. 987–1016.
[6] Povlsen, K.; Bjornelius, E.; Lidbrink, P.; Lind, I.: Relationship of Ureaplasma urealyticum biovar 2 to nongonococcal urethritis. Eur J Clin Microbiol Infect Dis 2002; 21 : 97–101.
[7] Deguchi, T.; Yoshida, T.; Miyazawa, T.; Yasuda, M.; Tamaki, M.; Ishiko, H., et al.: Association of Ureaplasma urealyticum (biovar 2) with nongonococcal urethritis. Sex Transm Dis 2004; 31 : 192–5.
[8] Couldwell, D.L.; Gidding, H.F.; Freedman, E.V.; McKechnie, M.L.; Biggs, K.; Sintchenko, V., et al.: Ureaplasma urealyticum is significantly associated with non-gonococcal urethritis in heterosexual Sydney men. Int J STD AIDS 2010; 21 : 337–41.
[9] Ondondo, R.O.; Whittington, W.L.; Astete, S.G.; Totten, P.A.: Differential association of ureaplasma species with non-gonococcal urethritis in heterosexual men. Sex Transm Infect 2010; 86 : 271–5.
[10] Maeda, S.; Deguchi, T.; Ishiko, H.; Matsumoto, T.; Naito, S.; Kumon, H., et al.: Detection of Mycoplasma genitalium, Mycoplasma hominis, Ureaplasma parvum (biovar 1) and Ureaplasma urealyticum (biovar 2) in patients with non-gonococcal urethritis using polymerase chain reaction-microtiter plate hybridization. Int J Urol 2004; 11 : 750–4.
[11] Chun, J. Y.: Multiplex molecular diagnostics: shifting the paradigm. In: Medical laboratory observed. 2012; Seegene bulletin, Vol.1.
[12] Choe, H. S.; Lee, D. S. et al.: Performance of AnyplexTM II multiplex RT PCR for the diagnosis of seven sexually transmitted infections: comparison with currently available methods. IJID. 17(12): 1134-1140. 2013. ISSN 1201-9712.
[13] DPO TM Technology. Novel Oligo platformo f super multiplex PCR. URL: http://seegene.com/neo/en/introduction/core_dpo.php
[14] TOCE TM Technology. The New Paradigm for High multiplex Real/time PCR. URL: http://seegene.com/neo/en/introduction/core_toce.php
[15] Kweon, O.J.; Lim, Y.K.; Oh, S.M.; Kim, T.H.; Choe, H.S.; Lee, S.J.; Cho, Y.H.; Lee, M.K.: Prevalence and Antimicrobial Susceptibility of Mycoplasma hominis, Ureaplasma urealyticum and Ureaplasma parvum in Individuals With or Without Symptoms of Genitourinary Infections. Lab Med Online. 2016 Apr;6(2):79-87. URL: https://doi.org/10.3343/lmo.2016.6.2.79.
Labels
Biomedicine
Article was published inThe Clinician and Technology Journal

2016 Issue 3
Most read in this issue- VYUŽITIE MULTIPLEXNEJ RT PCR V DIAGNOSTIKE MIKROBIONÁLNYCH PATOGÉNOV
- ANTIBACTERIAL ACTIVITY OF TITANIUM DIOXIDE AND AG-INCORPORATED DLC THIN FILMS
- RESPIRATORY ARRHYTHMIA AS AN ENCOURAGEMENT OF INAPPROPRIATE ICD THERAPY
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

