-
Medical journals
- Career
Parciální resekce jako možnost řešení pozdní infekce nativního i protetického arteriovenózního zkratu – kazuistiky
Authors: A. Svobodová 1,2; M. Slavíková 1; R. Lainková 1,2; M. Špaček 1,2; T. Grus 1,2; J. Lindner 1,2
Authors‘ workplace: II. chirurgická klinika kardiovaskulární chirurgie, 1. lékařská fakulta, Univerzita Karlova a Všeobecná fakultní nemocnice v Praze 1; 1. lékařská fakulta Univerzity Karlovy v Praze 2
Published in: Rozhl. Chir., 2022, roč. 101, č. 9, s. 460-464.
Category: Case Report
doi: https://doi.org/10.33699/PIS.2022.101.9.460–464Overview
Úvod: Infekce arteriovenózního zkratu (AV) pro hemodialýzu (HD) je spojená s rizikem život ohrožujícího krvácení, rozvojem sepse, vznikem metastatických infekčních ložisek a v neposlední řadě i zánikem zkratu. Urgence řešení infikovaného zkratu je základem úspěchu při jeho zachování.
Kazuistiky: Na dvou případech prezentujeme užití parciální resekce jako úspěšné metody řešení pozdní infekce AV. V kazuistice 1 byla resekce provedena pro infekci nativního arteriovenózního zkratu (AVF) se dvěma defekty nad aneuryzmaty odvodné žíly. V kazuistice 2 byla provedena parciální resekce a náhrada u vhojeného protetického arteriovenózního zkratu (AVG) pro infekci vpichu po HD. U obou pacientů zůstaly AV průchodné, bez dalších známek infekce v pooperačním sledování, bez nutnosti zavést dočasný HD katétr.
Závěr: Založení nové AV je u pacientů limitováno kvalitou žilního a arteriálního řečiště. Je třeba užít všech možných chirurgických, intervenčních a nechirurgických prostředků k bezpečnému zachování již založeného AV. Při dodržení požadavků včasné indikace je parciální resekce metodou volby u infekcí AV a dává možnost vyhnout se zavedení dialyzačního katétru.
Klíčová slova:
hemodialýza – infekce – arteriovenózní zkrat – parciální resekce
ÚVOD
Arteriovenózní zkrat (AV), ať už nativní (AVF), či protetický (AVG), je v dialyzační medicíně preferovaným přístupem pro dlouhodobé napojování pacienta k dialyzačnímu přístroji. Vytvoření AV vyžaduje adekvátní arteriální a venózní anatomii a také dostatečný časový interval pro vyzrání či zhojení [1]. Udržet dobře fungující AV bez nutnosti, byť jen přechodné kanylace centrálních žil, by mělo být prioritou. Péče o pacienta s AV vyžaduje multioborovou spolupráci a vysokou erudici všech členů týmu [2]. Článek se věnuje chirurgickému řešení infekce AV, kdy na dvou kazuistikách prezentuje protokol parciální resekce jako metodu zachování AV, bez nutnosti kanylace centrálních žil.
KAZUISTIKY
Prezentujeme kazuistiky popisující řešení infekce AV. V prvním případě jde o prostou parciální resekci AVF, ve druhém o parciální resekci a náhradu AVG. U obou pacientů nebyla nutná v perioperačním období kanylace centrálních žil k zajištění přístupu pro hemodialýzu (HD) a v dalším sledování u nich nebyly známky recidivy infekce AV.
KAZUISTIKA 1
58letý pacient s diabetickou nefropatií, 34 měsíců dialyzován cestou aneuryzmaticky změněné radiocefalické AVF na levém předloktí, byl odeslán do našeho centra pro defekty nad odvodnou žílou v místech kanylace (Obr. 1). Po komplexním dovyšetření (RTG srdce a plic, příjmový panel vyšetření) (Tab. 1), zhodnocení celkového stavu a defektů na AVF byl pacient indikován k akutní operaci s cílem zachování AVF. Vzhledem k absenci městnání na RTG snímku a akceptovatelné kalemii byla HD plánována pooperačně. Před výkonem byl podán 1,5 g Vankomycinu i.v. jako iniciační dávka antibiotické terapie po konzultaci s naším antibiotickým centrem. Operační výkon byl proveden v brachiálním bloku. Po zajištění žíly (Obr. 2) byly kožní defekty excidovány (Obr. 3), následně byla provedena resekce přední stěny odvodné žíly AVF. Heparin byl podán pouze lokálně. Sutura stěny žíly, podkoží a kůže byla provedena separátně. Perioperačně byla odebrána kultivace (Tab. 1). Pooperační průběh byl bez komplikací, s pravidelnou kontrolou markerů zánětu, dialyzačních parametrů a hladiny Vankomycinu (Tab. 1) s cílovou hladinou 20−25 mg/l. První pooperační den byl pacient zajištěn profylaktickou dávkou nízkomolekulárního heparinu. Od druhého dne pokračoval ve své chronické medikaci Godasal 1×100 mg/den. S výsledkem kultivace (Staphylococcus aureus) byl pacient druhý pooperační den převeden na Amoksiklav p.o. na dalších 7 dní. V rámci dokončení protokolu bylo provedeno echokardiografické vyšetření k vyloučení infekční endokarditis a zkontrolován průtok zkratem (560 ml/min.). Pacient byl hospitalizován po dobu tří dnů. Díky zachování zkratu bylo možné dialýzu provést na volný úsek odvodné žíly.
Image 1. Defekty AVF
Fig. 1: AVF defects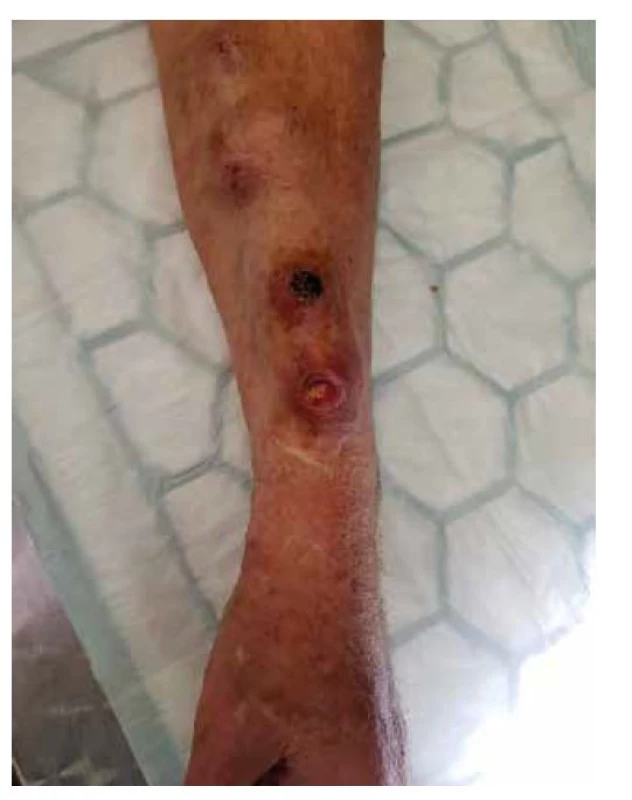
Table 1. Laboratorní výsledky (AVF)
Tab. 1: Laboratory results (AVF)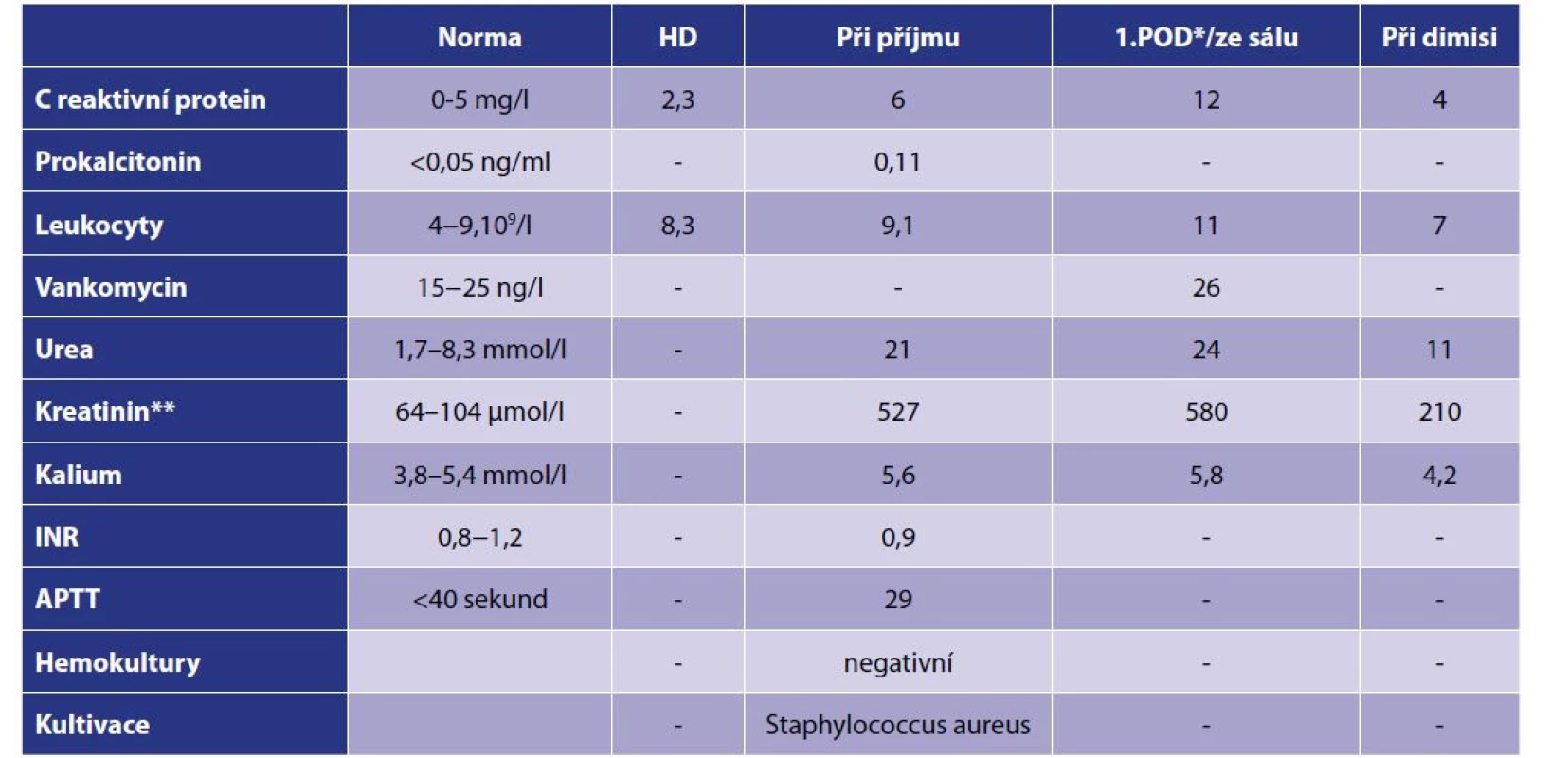
Vysvětlivky: * první pooperační den; **u muže Image 2. Zajištění žíly AVF
Fig. 2: AVF – vein isolation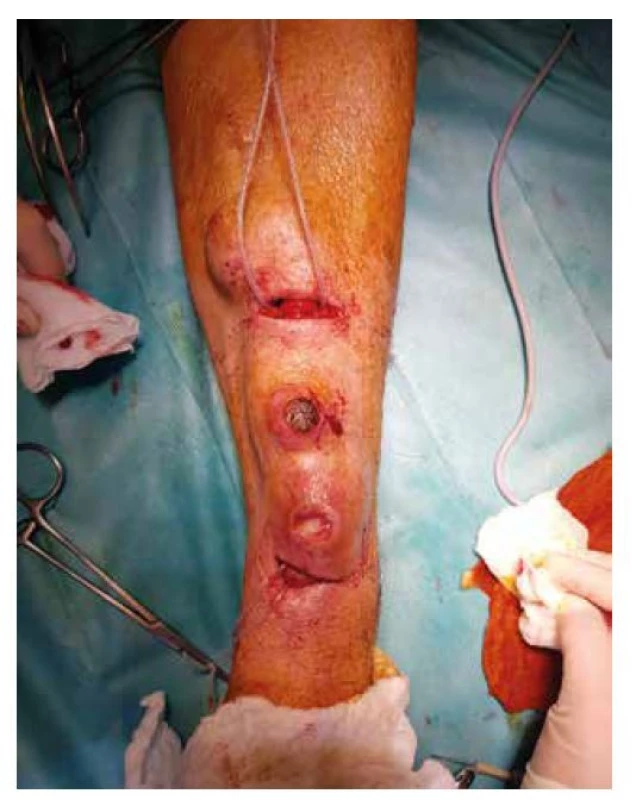
Image 3. Excize defektů AVF
Fig. 3: AVF – excision of the defects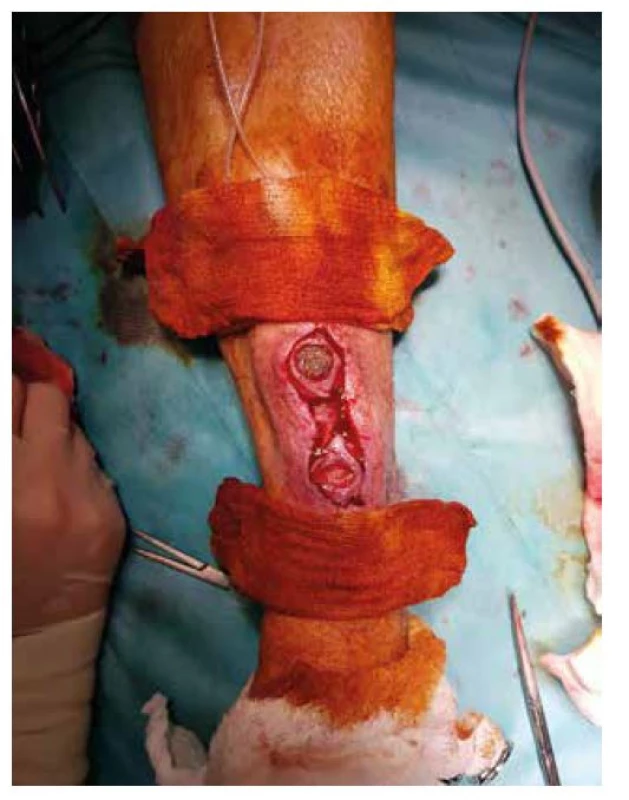
KAZUISTIKA 2
52letý pacient s diabetickou nefropatií, dialyzován 18 měsíců cestou brachiobasilického AVG na levé paži, byl odeslán do našeho centra pro krvácení z infikovaného defektu nad raménkem protézy (Obr. 4). Po komplexním dovyšetření (RTG srdce a plic, příjmový panel vyšetření) (Tab. 2), zhodnocení celkového stavu pacienta a defektu na AVG, byl pacient indikován k akutní operaci s cílem zachování AVG. Vzhledem k absenci městnání na RTG snímku a akceptovatelné kalemii byla HD naplánována pooperačně. Předoperačně byl podán 1,0 g Vankomycinu i.v. k doplnění iniciační dávky (na domácí HD již podáno 500 mg i.v.). Operační výkon byl proveden v brachiálním bloku. V prvním kroku: exkluze části protézy s defektem, tunelizace a end-to-end napojení nové protézy GORE-TEX® Stretch Vascular Graft 6 mm ve zdravém podkoží (Obr. 5). Heparin byl podán pouze lokálně a od obou anastomóz byly odebrány části původní protézy pro mikrobiologické vyšetření. Po sterilním krytí operačních ran byla v druhém kroku extirpována celá exkludovaná část protézy včetně excize kožního krytu z oblasti defektu. Materiál od defektu protézy byl odeslán na kultivaci (Tab. 2, Obr. 5). První pooperační den byl pacient zajištěn profylaktickou dávkou nízkomolekulárního heparinu. Od druhého dne pacient pokračoval ve své chronické medikaci Godasal 1×100 mg/den. S výsledkem kultivací (Staphylococcus aureus z defektu, negativní kultivace od obou nových anastomóz) byla indikována ATB terapie Vankomycinem na 3 týdny i.v., dále s převodem na p.o. terapii Dalacinem 2x300 mg/den na další 3 týdny. V rámci dokončení protokolu bylo provedeno echokardiografické vyšetření k vyloučení infekční endokarditis a zkontrolován průtok zkratem (1080 ml/min.). Pacient byl hospitalizován po dobu šesti dnů, díky parciální resekci a náhradě bylo možné provést dialýzu na zachovalý vhojený úsek protézy AVG.
Image 4. Průběh protézy AVG a defekt
Fig. 4: AVG – prothesis and defect locations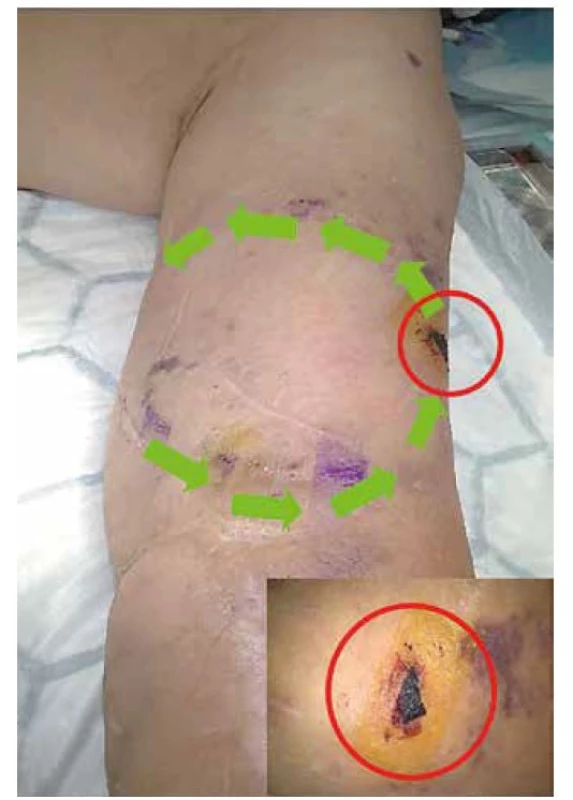
Table 2. Laboratorní výsledky (AVG)
Tab. 2: Laboratory results (AVG)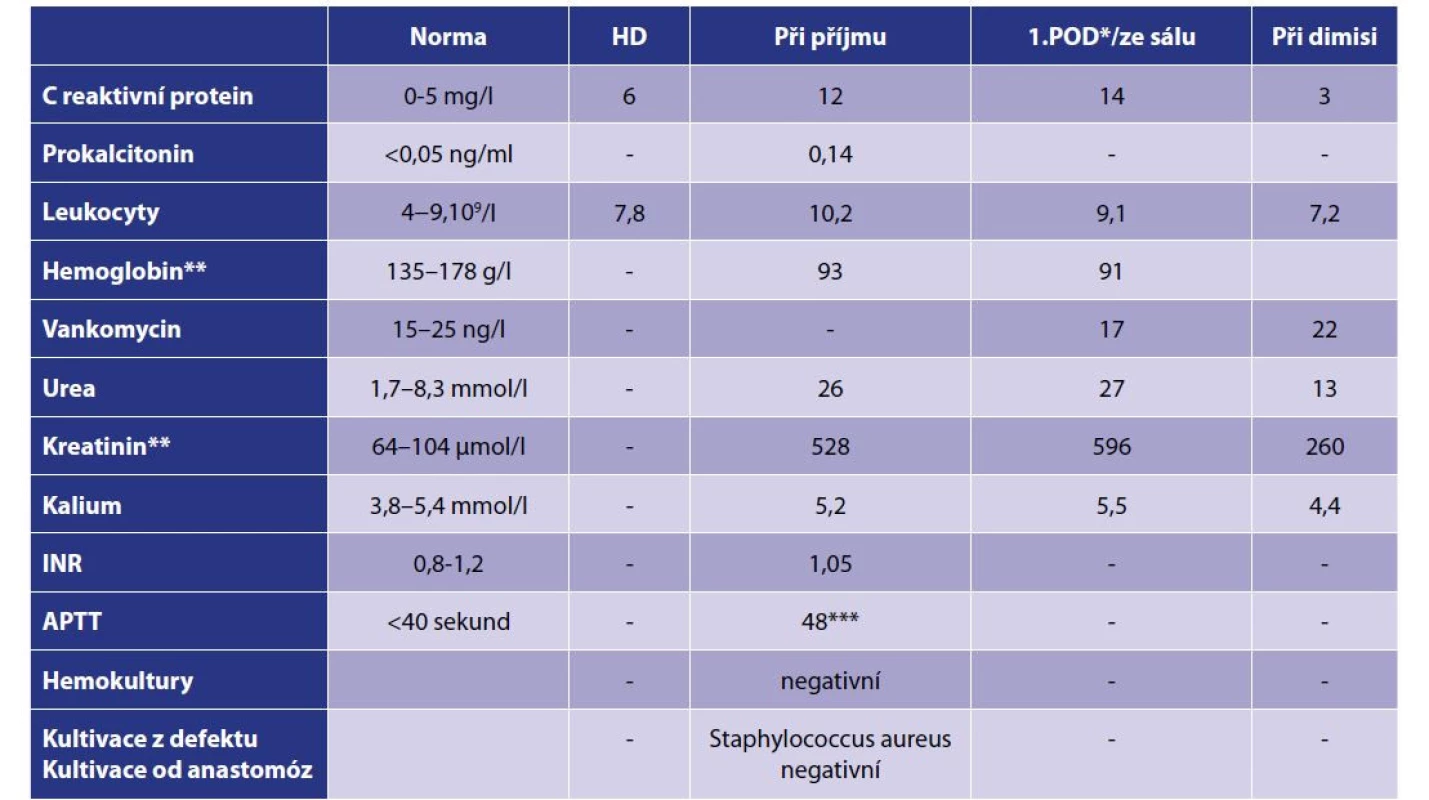
Vysvětlivky: * první pooperační den; ** u muže; *** v úvodu HD podán Heparin 1,5 tis. UI Image 5. Postup parciální resekce AVG
Fig. 5: AVG – partial resection procedure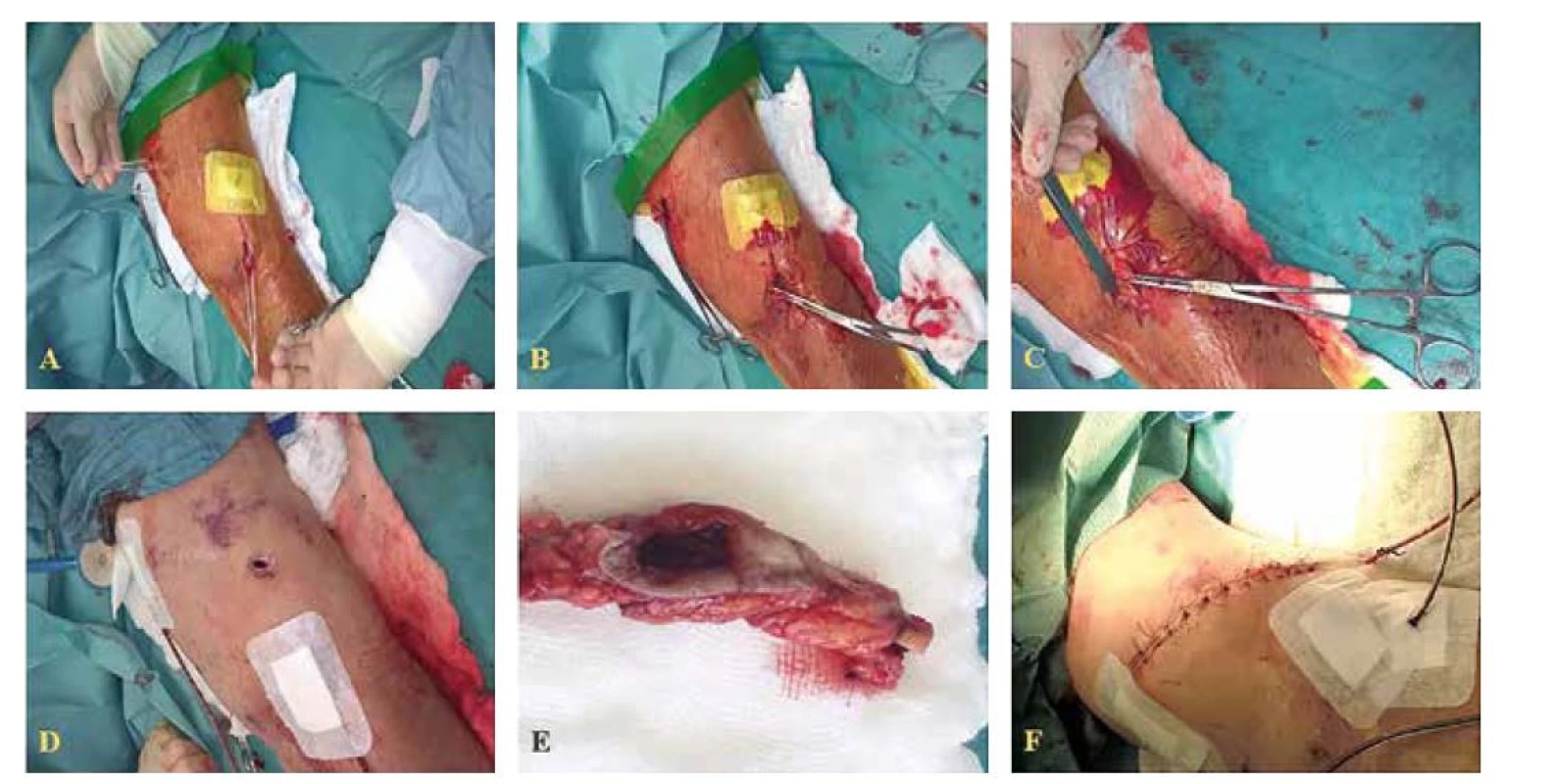
DISKUZE
V České republice je cestou cévního přístupu dialyzováno 5,5 tis. pacientů. Navzdory maximální péči dialyzačních lékařů je mortalita v této skupině vysoká, kdy infekce jsou řazeny hned na druhé místo příčin úmrtí, po kardiovaskulárních onemocněních [3].
Obecně platí, že AVF má zhruba 10× nižší riziko infekce než AVG, nicméně v praxi se setkáváme s infekčními komplikacemi obou typů AV spojek [2]. Při infekci AVF je často exponovaným místem aneuryzmatická dilatace odvodné žíly. Stává se to díky téměř vymizelému podkoží, ale také díky preferenční kanylaci (velikost aneuryzmatu láká k opakovaným punkcím) [4]. Dostatečná dilatace na druhou stranu většinou umožňuje provedení parciální resekce výdutě se zachováním zkratu. V případě pozdní infekce AVG se nejčastěji setkáváme s izolovanou infekcí v oblasti raménka. Řešením zde může být včasná parciální resekce a náhrada [4]. Podmínkou výkonu je vhojený zkrat a možnost tunelizovat nový graft zdravým podkožím. Kromě dostatečné chirurgické erudice je třeba dbát na cílenou ATB terapii po dostatečně dlouhou dobu, a to zejména v případě AVG [5]. Většina pozdních infekcí je způsobena infekcí vpichu (po HD nebo radiologickém výkonu), jako hlavní se tedy jeví důraz na aseptické podmínky, minimalizaci užití knoflíkové (buttonhole) metody a precizní kanylaci AV spojky [6,7]. Absence febrilií, negativní hemokultury a následně negativní kultivační vyšetření peroperačně odebraného materiálu od nových anastomóz AVG se jeví jako možné prediktivní faktory úspěšné parciální resekce [4].
V souboru pacientů našeho centra jsme v letech 2017 až 2021 u AVF nikdy neprovedli zrušení zkratu pro recidivu infekce po provedené parciální resekci. Ve stejném období jsme založili 343 AVG, z toho 18 % si vyžádalo chirurgické řešení infekce. Parciální resekce a náhrady byly v tomto období provedeny u 51 AVG a z této skupiny byly pouze dva zkraty následně indikovány k úplné explantaci pro recidivu infekce. 12 AVG jsme indikovali k explantaci ihned pro známky časné infekce. 8 % pacientů mělo současně nález infekční endokarditis. Důvodem úspěšných parciálních resekcí může být standardizovaný protokol našeho centra a důraz na dlouhodobou cílenou ATB terapii [8].
ZÁVĚR
Arteriovenózní zkrat vyžaduje komplexní přístup celého týmu specialistů, jeho dlouhodobě dobrá funkce je kruciální pro kvalitně prováděnou HD, a tedy i přežití pacienta. Při řešení komplikací AV je nutná dostatečná erudice chirurga, dialyzačního lékaře a v neposlední řadě i dialyzačních sester. Právě včasné odhalení zkratu s infekční komplikací a jeho rychlé předání na specializované pracoviště, jsou základem úspěšného ošetření. Prostá sutura defektu je řešením pouze provizorním v emergentní situaci, definitivním řešením je precizní odstranění infikovaného materiálu s dostatečně dlouhou cílenou ATB terapií.
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
MUDr. Alžběta Svobodová
U Nemocnice 2
128 08 Praha 2
e-mail: alzbeta.svobodova@vfn.cz
ORCID: 0000-0002-2105-6025
Sources
1. Woo K, Dillavou E, Berns J, et al. Arteriovenous fistula creation for hemodialysis and its complications. UpToDate 2021, Oct 27.
2. Lok CE, Huber TS, Lee T, et al. KDOQI clinical practice guideline for vascular access: 2019 update. Am J Kidney Dis. 2020;75:S1.
3. Rychlík I, Lopot F, Francová. Statistická ročenka dialyzační léčby v České republice v roce 2020 [2022-01-20]. Available at: www.nefrol.cz/odbornici/dialyzacni - statistika.
4. Attia MI, Atta EM, Elheneidy MA, et al. Salvage of infected autogenous arteriovenous fistulas, is it possible? The Journal of Vascular Access February 2022. doi:10.1177/11297298221080080.
5. Schmidli J, Widmer MK, Mohaupt M, et al. Vascular access: 2018 clinical practice guidelines of the European Society for Vascular Surgery. European Journal of Vascular and Endovascular Surgery 2018;6 : 757−818. doi:10.1016/j. ejvs.2018.02.001.
6. Gallieni M, Hollenbeck M, Inston N, et al. Clinical practice guideline on peri - and postoperative care of arteriovenous fistulas and grafts for haemodialysis in adults. Nephrology Dialysis Transplantation 2019;34 (Suppl 2). doi:10.1093/ndt/ gfz072.
7. Stegmayr B, Willems Ch, Growth T, et al. Arteriovenous access in hemodialysis: A multidisciplinary perspective for future solutions. Int J Artif Organs 2021 Jan;44(1):3−16. doi:10.1177/0391398820922231.
8. Hartinger JM, Šíma M, Hronová K, et al. Vancomycin pharmacokinetics in patients treated with intermittent haemodialysis based on therapeutic drug monitoring. J Chemother. 2022 May;34(3):149156. doi:1 0.1080/1120009X.2021.1979747.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2022 Issue 9-
All articles in this issue
- Sekce HPB a biliární chirurgie
- Chirurgická léčba karcinomu extrahepatálních žlučových cest – aktuální důkazy a doporučení
- Chirurgie iatrogenních poranění žlučových cest
- Zhoubné nádory mimojaterních žlučových cest
- Karcinom středního a distálního žlučovodu, retrospektivní analýza, krátkodobé a dlouhodobé výsledky chirurgické léčby
- Intrahepatický cholangiokarcinom: rizikové faktory přežití operovaných nemocných
- Allen-Mastersův syndrom jako příčina ileózního stavu – kazuistika
- Parciální resekce jako možnost řešení pozdní infekce nativního i protetického arteriovenózního zkratu – kazuistiky
- Masivní nitrohrudní krvácení jako komplikace difúzní alveolární hemoragie a antikoagulační léčby při covid 19 – 2 kazuistiky
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Chirurgie iatrogenních poranění žlučových cest
- Zhoubné nádory mimojaterních žlučových cest
- Allen-Mastersův syndrom jako příčina ileózního stavu – kazuistika
- Chirurgická léčba karcinomu extrahepatálních žlučových cest – aktuální důkazy a doporučení
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

